植物乳杆菌在预防肠道屏障损伤中的应用的制作方法
本发明属于生物
技术领域:
,具体涉及植物乳杆菌在预防肠道屏障损伤中的应用。
背景技术:
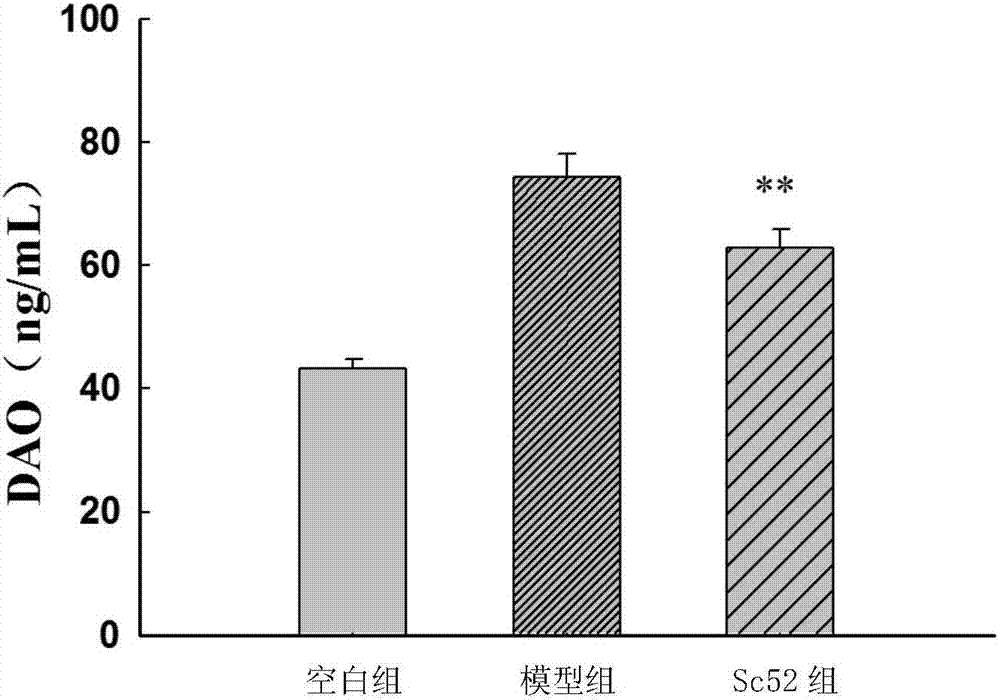
:肠道是人体最大的消化器官,完整的肠黏膜屏障能够阻止微生物及内毒素进入体循环,是对抗肠道细菌、毒素的第一道防线,对于维持上皮细胞通透性、机体内环境的稳态有重要作用,可维持肠道正常功能,保证机体健康。肠黏膜屏障功能一旦受损,肠道通透性升高,肠腔内的内毒素突破肠道屏障进入机体循环,促使大量炎性细胞因子释放,引起机体炎症,进而诱发异常的黏膜免疫反应。近年来研究发现肠黏膜屏障损伤与肠道炎症、机体免疫、肥胖、胰岛素抵抗及糖尿病等多种疾病相关,不论是哪一种肠道黏膜屏障受到损伤,都会导致机体不同程度的伤害,严重时可导致多器官功能障碍,至引起死亡。目前肠道屏障功能损伤的治疗没有特效药,一般更重视原发疾病的治疗,尽量做到早期准确诊断,早期有效治疗,尽量减少肠黏膜屏障损伤的发生机率,谷氨酰胺、重组人生长激素、中药等对肠粘膜屏障也有一定的保护作用。技术实现要素:本发明的目的是提供植物乳杆菌在预防肠道屏障损伤中的应用。本发明首先保护植物乳杆菌在制备产品中的应用;所述产品的功能为如下(a1)和/或(a2)和/或(a3)和/或(a4):(a1)保护肠道粘膜;(a2)预防和/或治疗肠道粘膜损伤;(a3)保护肠道屏障(a4)预防和/或治疗肠道屏障损伤。所述产品为菌剂、药品、保健品或食品。本发明还保护植物乳杆菌在制备产品中的应用;所述产品的功能为如下(b1)至(b15)中的至少一种:(b1)降低血清中炎症因子水平;(b2)缓解由于肠道粘膜损伤引起的血清中炎症因子水平上升;(b3)缓解由于肠道屏障损伤引起的血清中炎症因子水平上升;(b4)降低血清中肠道通透性相关指标的水平;(b5)缓解由于肠道粘膜损伤引起的肠道通透性增加;(b6)缓解由于肠道屏障损伤引起的肠道通透性增加;(b7)缓解由于肠道粘膜损伤引起的血清中肠道通透性相关指标水平上升;(b8)缓解由于肠道屏障损伤引起的血清中肠道通透性相关指标水平上升;(b9)维持肠道平衡;(b10)缓解由于肠道粘膜损伤引起的结肠内容物中短链脂肪酸含量下降;(b11)缓解由于肠道屏障损伤引起的结肠内容物中短链脂肪酸含量下降;(b12)缓解由于肠道粘膜损伤引起的回肠总蛋白中紧密连接蛋白水平下降;(b13)缓解由于肠道屏障损伤引起的回肠总蛋白中紧密连接蛋白水平下降;(b14)缓解由于肠道粘膜损伤引起的肠上皮细胞中紧密连接蛋白水平下降;(b15)缓解由于肠道屏障损伤引起的肠上皮细胞中紧密连接蛋白水平下降。所述产品为菌剂、药品、保健品或食品。本发明还保护一种产品,其活性成分为植物乳杆菌;所述产品的功能为如下(a1)和/或(a2)和/或(a3)和/或(a4):(a1)保护肠道粘膜;(a2)预防和/或治疗肠道粘膜损伤;(a3)保护肠道屏障(a4)预防和/或治疗肠道屏障损伤。所述产品为菌剂、药品、保健品或食品。本发明还保护一种产品,其活性成分为植物乳杆菌;所述产品的功能为如下(b1)至(b15)中的至少一种:(b1)降低血清中炎症因子水平;(b2)缓解由于肠道粘膜损伤引起的血清中炎症因子水平上升;(b3)缓解由于肠道屏障损伤引起的血清中炎症因子水平上升;(b4)降低血清中肠道通透性相关指标的水平;(b5)缓解由于肠道粘膜损伤引起的肠道通透性增加;(b6)缓解由于肠道屏障损伤引起的肠道通透性增加;(b7)缓解由于肠道粘膜损伤引起的血清中肠道通透性相关指标水平上升;(b8)缓解由于肠道屏障损伤引起的血清中肠道通透性相关指标水平上升;(b9)维持肠道平衡;(b10)缓解由于肠道粘膜损伤引起的结肠内容物中短链脂肪酸含量下降;(b11)缓解由于肠道屏障损伤引起的结肠内容物中短链脂肪酸含量下降;(b12)缓解由于肠道粘膜损伤引起的回肠总蛋白中紧密连接蛋白水平下降;(b13)缓解由于肠道屏障损伤引起的回肠总蛋白中紧密连接蛋白水平下降;(b14)缓解由于肠道粘膜损伤引起的肠上皮细胞中紧密连接蛋白水平下降;(b15)缓解由于肠道屏障损伤引起的肠上皮细胞中紧密连接蛋白水平下降。所述产品为菌剂、药品、保健品或食品。所述植物乳杆菌具体可为植物乳杆菌(lactobacillusplantarum)sc52。植物乳杆菌(lactobacillusplantarum)sc52,已于2015年06月29日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称cgmcc,地址为:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所),保藏登记号为cgmccno.11027。植物乳杆菌(lactobacillusplantarum)sc52cgmccno.11027,简称植物乳杆菌sc52。以上任一所述肠道屏障损伤具体可为脂多糖引起的肠道屏障损伤。以上任一所述肠道粘膜损伤具体可为脂多糖引起的肠道粘膜损伤。以上任一所述炎症因子具体可为肿瘤坏死因子-α和/或白细胞介素-6和/或白细胞介素-12和/或一氧化氮。以上任一所述肠道通透性相关指标为d-乳酸和/或二胺氧化酶。以上任一所述短链脂肪酸为乙酸和/或丙酸和/或正丁酸。以上任一所述紧密连接蛋白为紧密连接蛋白zo-1和/或紧密连接蛋白occludin和/或紧密连接蛋白claudin-1。以上任一所述食品包括但不限于:含有所述植物乳杆菌的发酵果蔬、含有所述植物乳杆菌的发酵乳、含有所述植物乳杆菌的乳酪、含有所述植物乳杆菌的含乳饮料、含有所述植物乳杆菌的乳粉或含有所述植物乳杆菌的其它食品。所述食品具体可为功能性食品,例如功能性酸奶、功能性菌剂等。以上任一所述药品可为但不限于如下剂型:胶囊、粉剂、片剂。所述药品还可包括其他药学上可以接受的赋形剂或稀释剂。制备粉剂的方法可为冷冻干燥或其它工艺。所述植物乳杆菌的建议剂量如下:每天1次,单次剂量为109-1010cfu。人类食用由乳酸菌发酵的食品已经有悠久的历史,许多乳酸菌被广泛用于乳制品、蔬菜和肉类制品的加工,因此乳酸菌被认为是一类对人类健康有益的公认安全(generallyrecognizedassafe,gras)的微生物。本发明的发明人发现,植物乳杆菌sc52有助于维持肠黏膜屏障功能的完整性,对于缓解肠道屏障损伤具有突出优良的效果。日常摄入植物乳杆菌sc52或其菌制剂,可以代替药品保护肠道屏障功能的完整性。本发明为临床干预和控制肠道屏障功能损伤相关疾病提供了新思路,具有广阔的应用前景和推广价值。附图说明图1为血清中d-lac的浓度结果。图2为血清中dao的浓度结果。图3为病理学切片(olympusbx501000×)。图4为回肠中紧密连接蛋白的水平。具体实施方式以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。清洁级icr雄性小鼠(18-22g):长春生物制品研究所。饲养环境:23±2℃,湿度50%-75%,自由摄取基础饲料和纯净水。实施例中所用的脂多糖为大肠杆菌脂多糖055:b5,sigma-aldrichcorporation,货号为l-2880。脂多糖溶液采用生理盐水作为溶剂。脂多糖可以诱导发生肠屏障损伤。用于检测血清中肿瘤坏死因子-α(tnf-α)的试剂盒:上海朗顿生物技术公司,货号bp-e20220。用于检测血清中白细胞介素-6(il-6)的试剂盒:上海朗顿生物技术公司,货号bp-e20012。用于检测血清中白细胞介素-12的试剂盒:上海朗顿生物技术公司,货号bp-e20750。用于检测血清中一氧化氮的试剂盒:上海朗顿生物技术公司,货号bp-e20293。用于检测血清中d-乳酸(d-lac)的试剂盒:上海朗顿生物技术公司,货号bp-e20072。用于检测血清中二胺氧化酶(dao)的试剂盒:上海朗顿生物技术公司,货号bp-e20139。用于提取总蛋白的ripa裂解液(货号:wb-0071)和bca蛋白定量试剂盒(货号:bca02),购自北京鼎国昌盛生物技术有限公司。植物乳杆菌(lactobacillusplantarum):北京中科质检生物技术有限公司;产品id号:128012;产品编号:cicc-6009;简称植物乳杆菌cicc-6009。实施例1、菌株的分离、鉴定和保藏一、菌株的分离样本取材:传统发酵酸菜。经bcp培养基平板反复划线培养,挑取产黄圈的单菌落接种于mrs培养基平板上继续培养,经mrs培养基平板反复划线培养纯化,得到多株纯培养菌种。纯培养的菌种接种到液体mrs培养基培养,然后加入20%甘油,-80℃冰箱保存。经革兰氏染色阳性、过氧化氢酶试验阴性、吲哚反应阴性、产硫化氢试验阴性、明胶液化试验阴性、水解淀粉试验阴性和硝酸盐还原试验阴性从纯培养的菌种中筛选出多株乳杆菌。将其中1株植物乳杆菌菌株命名为sc52。二、菌株的鉴定sc52的生理生化鉴定结果:革兰氏阳性,过氧化氢酶阴性;不运动的杆菌;在15℃和45℃能够生长;耐受6.5%nacl;不水解淀粉,不液化明胶,不产生硫化氢;发酵葡萄糖产酸不产气;联苯胺试验阴性,吲哚试验阴性,乙酰甲基甲醇试验阳性。sc52在mrs液体培养基中呈均匀浑浊生长,久置菌体呈白色沉淀。sc52的最适生长温度37~42℃,适宜ph为5.0~7.0。sc52的api50ch(法国梅里埃公司)鉴定结果:能利用核糖、半乳糖、葡萄糖、果糖、木糖、甘露糖、甘露醇、山梨醇、苦杏仁苷、熊果苷、n-乙酰-葡萄糖胺、七叶醇、柳醇、纤维二糖、菊糖、乳糖、蜜二糖、蔗糖、海藻糖、松三糖、棉籽糖、牻牛儿糖、d-阿拉伯糖醇、葡萄糖酸盐;不能利用阿东醇、阿拉伯糖、山梨糖、卫矛醇、肌醇、α-甲基-d-葡萄糖苷、α-甲基-d-甘露糖苷、淀粉、糖原、鼠李糖、木糖醇、d-松二糖、d-塔格糖、d-米苏糖、麦芽糖、葡萄糖酸盐、岩糖、l-阿拉伯糖醇、2-酮基-葡萄糖酸盐、5-酮基-葡萄糖酸盐。鉴定结果表明,菌株sc52为植物乳杆菌(lactobacillusplantarum)。三、菌株的保藏植物乳杆菌(lactobacillusplantarum)sc52,已于2015年06月29日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称cgmcc,地址为:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所),保藏登记号为cgmccno.11027。植物乳杆菌(lactobacillusplantarum)sc52cgmccno.11027,简称植物乳杆菌sc52。实施例2、植物乳杆菌sc52在提高肠道屏障中的应用一、菌悬液的制备取植物乳杆菌sc52的菌体,用无菌生理盐水悬浮,得到菌浓度为1×1010cfu/ml的菌悬液甲。取植物乳杆菌cicc-6009的菌体,用无菌生理盐水悬浮,得到菌浓度为1×1010cfu/ml的菌悬液乙。二、分组处理试验动物为清洁级icr雄性小鼠(18-22g)。取试验动物,进行连续3天的适应性饲养(即试验第1天之前的3天),然后随机分为4组,每组21只,处理如下:空白组(control):试验第1至14天,每天灌胃一次生理盐水(每只试验动物单次给予0.1ml);末次灌胃12小时后,单次腹腔注射生理盐水(每只试验动物给予0.1ml),6小时后处死试验动物;模型组(model):试验第1至14天,每天灌胃一次生理盐水(每只试验动物单次给予0.1ml);末次灌胃12小时后,单次腹腔注射脂多糖溶液(每只试验动物给予脂多糖溶液0.1ml,每只试验动物给予脂多糖的剂量为15mg/kg体重),6小时后处死试验动物;sc52组(sc52):试验第1至14天,每天灌胃一次菌悬液甲(每只试验动物单次给予0.1ml),末次灌胃12小时后,单次腹腔注射脂多糖溶液(每只试验动物给予脂多糖溶液0.1ml,每只试验动物给予脂多糖的剂量为15mg/kg),6小时后处死试验动物;cicc-6009组(cicc-6009):试验第1至14天,每天灌胃一次菌悬液乙(每只试验动物单次给予0.1ml),末次灌胃12小时后,单次腹腔注射脂多糖溶液(每只试验动物给予脂多糖溶液0.1ml,每只试验动物给予脂多糖的剂量为15mg/kg体重),6小时后处死试验动物。三、植物乳杆菌sc52降低血清中炎症因子水平步骤二中,处死试验动物的前一时刻,摘眼球取血,分离血清。取血清,分别检测其中各个炎症因子的浓度。各个炎症因子分别为:tnf-α、il-6、il-12和no。结果见表1。与空白组试验动物相比,模型组试验动物血清中的tnf-α、il-6、il-12、no水平均明显升高,说明脂多糖进入血液循环后激发机体的炎症反应,使机体炎症水平迅速升高。与模型组相比,sc52组试验动物血清中的tnf-α、il-6、il-12水平和no水平均呈不同程度降低。结果表明,植物乳杆菌sc52能明显缓解脂多糖诱导的炎症反应,降低血清中各个炎症因子的水平。表1血清中各个炎症因子的浓度组别tnf-α(ng/l)il-6(pg/ml)il-12(ng/l)no(μmol/l)空白组131.54±10.8788.39±2.60170.35±14.9048.57±8.49模型组192.79±12.63212.85±57.53236.40±1.8383.89±3.61sc52组178.10±2.97*157.85±21.36*204.49±2.18**80.48±2.83四、植物乳杆菌sc52降低血清中d-lac和dao水平步骤二中,处死试验动物的前一时刻,摘眼球取血,分离血清。取血清,检测其中d-lac的浓度,结果见图1。取血清,检测其中dao的浓度,结果见图2。腹腔注射脂多糖后,模型组试验动物血清中d-lac水平和dao的水平迅速升高,d-lac浓度为3.65μmol/ml,dao浓度为74.36ng/ml。sc52组试验动物血清中,d-lac水平浓度为3.23μmol/ml,dao浓度为62.82ng/ml,与模型组试验动物相比差异性极显著(p<0.01)。cicc-6009组试验动物血清中,d-lac水平浓度为3.41μmol/ml,dao浓度为68.37ng/ml。结果表明,脂多糖诱导试验动物肠屏障受损,肠道通透性增加,导致通透性相关的指标水平迅速升高,而植物乳杆菌sc52可以通过改善肠道通透性水平缓解脂多糖对肠道屏障造成的损伤,植物乳杆菌sc52的效果优于植物乳杆菌cicc-6009。五、植物乳杆菌sc52对小鼠回肠病理学的影响步骤二中,处死试验动物后,取1cm回肠组织(距小肠回盲部1cm处),制作石蜡切片并进行苏木素-伊红染色。空白组试验动物的病理学切片见图3的a,回肠绒毛结构完整,上皮细胞排列整齐,无明显的炎性细胞浸润及肠黏膜上皮脱落现象。模型组试验动物的病理学切片见图3的b,回肠上皮细胞排列紊乱,肠黏膜绒毛出现破损,炎细胞浸润出现血灶,这是由于脂多糖的破坏作用所引起。sc52组试验动物的病理学切片见图3的c,回肠上皮细胞排列未见明显异常,肠组织中偶见炎性细胞浸润伴有充血,但与模型组试验动物相比,症状明显减轻。与cicc-6009组试验动物相比,sc52组试验动物的肠黏膜损伤情况症状明显减轻。结果表明,植物乳杆菌sc52能够减轻脂多糖对回肠粘膜组织所造成的损伤,且效果优于植物乳杆菌cicc-6009。六、植物乳杆菌sc52对小鼠肠道短链脂肪酸的影响步骤二中,处死试验动物后,取结肠内容物0.1g,利用气相色谱测定其中的中短链脂肪酸(乙酸、丙酸和正丁酸)的含量。1、取结肠内容物0.1g,加蒸馏水5ml溶解并震荡2h,12000rpm离心10min,收集上清液。2、取2ml步骤1得到的上清液,用0.45μm滤膜过滤,然后加入0.4ml50%(质量百分含量)h2so4溶液和2.0ml乙醚,震荡30次,然后12000rpm离心5min,然后4℃静置30min,取上层乙醚相(2ml)作为待测溶液。3、将待测溶液进行气相色谱检测。gc7890a气相色谱测定条件:db-ffap色谱柱(30m×0.25mm,0.25μm)。升温程序:初温120℃,维持5min;以15℃/min速度升到250℃,保持1min;fid温度:280℃;载气:氮气,分流比为10:1,流速:2.0ml/min;待测溶液进样体积为2μl。测定采用外标法,分别用乙酸、丙酸和正丁酸作标准曲线。乙酸(货号:a116165)、丙酸(货号:p110443)、正丁酸(货号:b110439)标准品均为色谱纯,购自上海阿拉丁生化科技股份有限公司。待测溶液中的乙酸、丙酸和正丁酸的浓度见表2。与空白组试验动物相比,模型组试验动物结肠内容物中各个短链脂肪酸含量明显下降,表明模型组试验动物的肠道平衡被破坏。与模型组试验动物相比,sc52组试验动物结肠内容物中各个短链脂肪酸含量升高,具有显著差异(p<0.05)。结果表明,植物乳杆菌sc52能够升高试验动物肠道中短链脂肪酸的水平。与模型组试验动物相比,cicc-6009组试验动物结肠内容物中各个短链脂肪酸含量升高,但升高幅度低于sc52组。表2结肠内容物中各个短链脂肪酸的浓度组别乙酸(mg/ml)丙酸(mg/ml)丁酸(mg/ml)空白组2.03±0.420.31±0.160.41±0.18模型组1.35±0.380.18±0.120.20±0.13sc52组1.86±0.32*0.21±0.110.32±0.15*cicc-6009组1.68±0.270.20±0.090.27±0.13七、植物乳杆菌sc52上调回肠中紧密连接蛋白的水平步骤二中,处死试验动物后,截取回肠。取回肠,提取总蛋白,然后进行蛋白电泳和western-blot,检测紧密连接蛋白zo-1、紧密连接蛋白occludin与紧密连接蛋白claudin-1的水平。兔抗zo-1单克隆抗体:thermofisherscientific公司,货号pa5-28858。兔抗occludin单克隆抗体:英国abcam公司,货号ab167161。兔抗claudin-1单克隆抗体:英国abcam公司,货号ab180158。gapdh抗体:杭州贤至生物有限公司,货号ab-p-r-001。山羊抗兔二抗:北京中杉金桥生物技术有限公司,货号zb-5301。western-blot结果见图4的a。将图4的a进行灰度扫描后获得紧密连接蛋白zo-1、紧密连接蛋白occludin与紧密连接蛋白claudin-1的相对表达水平,结果见图4的b。脂多糖能够直接作用于肠上皮细胞,破坏紧密连接蛋白结构,使紧密连接蛋白的水平降低。与模型组试验动物相比,sc52组试验动物回肠中紧密连接蛋白occludin的相对表达水平增加了83.78%、紧密连接蛋白claudin-1的相对表达水平增加了143.24%、紧密连接蛋白zo-1的相对表达水平增加了33.33%,差异呈极显著性(p<0.01)。结果表明,植物乳杆菌sc52能够通过上调肠上皮细胞间紧密连接蛋白表达量,对脂多糖引起的肠道屏障损伤发挥保护作用。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1