利奈唑胺联合氟康唑的抗真菌产品及其应用的制作方法
本发明属于医药技术领域,具体涉及利奈唑胺联合氟康唑的抗真菌产品及其应用。
背景技术:
近年来,随着免疫力低下人群(恶性肿瘤、艾滋病、自身免疫病等患者)的增多,导管插管和器官移植等技术的开展,广谱抗生素、皮质激素和免疫抑制剂的广泛使用,真菌感染的发病率急剧上升(garcia-vidalc1,viasusd,carratalàj..pathogenesisofinvasivefungalinfections.curropininfectdis.2013jun;26(3):270-6.)。白色念珠菌是临床真菌感染中常见的分离菌,它可以造成浅表感染也可以侵入体内造成系统感染(poulaind.candidaalbicans,plasticityandpathogenesis.critrevmicrobiol.2015jun;41(2):208-17.)。
氟康唑(fluconazole,flc)作为安全、有效、价格低廉的抗真菌药物,对白色念珠菌有很好的疗效。但随着flc在临床上的广泛应用,使得白色念珠菌对唑类药物的耐药性不断增高,因此寻找新的抗真菌手段迫在眉睫。新药研究与联合用药研究均是解决真菌耐药的途径。新药研究周期长,成本高,而联合用药其前期投入少、效果显著,受到国内外的关注。联合用药研究包括两种抗真菌药联合和非抗真菌药与抗真菌药联合。由于抗真菌药物品种有限,且新的具有抗真菌作用的药物价格昂贵且副作用明显,使得非抗真菌药物与抗真菌药物的联合应用研究备受关注。
目前抗真菌的机制包括:抑制真菌细胞壁的合成;抑制真菌细胞膜主要成分麦角甾醇的合成以及直接作用于麦角甾醇的结构,作用于真菌核酸代谢等。除此之外,从其他方面寻找新的抗真菌途径也成为研究者们持续关注的热点。
利奈唑胺(linezolid,lzd)是细菌蛋白质合成抑制剂,作用于细菌核糖体的50s亚基,阻断细菌蛋白质合成,从而产生抑菌作用。主要用于治疗细菌感染,尤其是革兰氏阳性菌引起的感染。已有研究表明利奈唑胺与两性霉素b联用时具有协同抗新型隐球菌的作用(rossatol1,loreto
技术实现要素:
本发明的目的是为了克服目前真菌耐药问题,提供一种利奈唑胺联合氟康唑的抗真菌产品及其应用。
为了实现上述目的,本发明的技术方案如下:
一种利奈唑胺联合氟康唑在制备抗真菌产品中的应用。
优选的,所述真菌为白色念珠菌;
优选的,所述产品为药物;
优选的,所述利奈唑胺与氟康唑联合应用时,利奈唑胺的浓度为:32-256μg/ml,氟康唑的浓度为1-128μg/ml;
优选的,所述利奈唑胺联合氟康唑联合应用时有效浓度配比氟康唑:利奈唑胺=1:32。
所述应用时利奈唑胺的最低抑菌浓度为32μg/ml;
所述应用时氟康唑的最低抑菌浓度为1μg/ml。
一种抗真菌产品,所述产品包含利奈唑胺和氟康唑。
优选的,所述利奈唑胺和氟康唑的有效浓度配比为氟康唑:利奈唑胺=1:32;
所述利奈唑胺的最低抑菌浓度为32μg/ml;
所述氟康唑的最低抑菌浓度为1μg/ml;
试验结果表明:大于32μg/ml的利奈唑胺与大于1μg/ml的氟康唑联合应用时具有协同抗白色念珠菌的作用。
一种抗真菌产品,由利奈唑胺和氟康唑以及药学上可接受的辅料组成,在本发明提供的抗真菌产品中,药学上可接受的辅料为药物制剂中的常规辅料,如:崩解剂、润滑剂、黏合剂等;优选为甘油、丁二醇、海藻糖、甜菜碱、淀粉、羧甲基纤维素钠中的一种或多种。
本发明与现有技术相比,具有以下优点与效果:
1.本发明定量评价了临床常用的抗菌药物利奈唑胺与氟康唑的联合抗真菌作用,首次发现并分析了利奈唑胺对氟康唑的增敏效果,并进行了体外与体内的系统评价具体的,本发明采用白色念珠菌细胞进行研究,利用液体定量法,测定flc与lzd联合用药时最低有效浓度,并以fici法选择最佳药物组合浓度及评价药物联合用药的作用;同时本发明还采用大蜡螟感染模型评价药物联用在体内的抗真菌作用,需要说明的是,试验发现,lzd与flc联用对克柔念珠菌、光滑念珠菌等非白色念珠菌几乎无作用,这表明真菌耐药机制是十分复杂的,同时也说明不同药物的抗菌作用难以进行有效预期。
2.本发明为临床提供了联合用药作为治疗真菌感染的治疗方案。发明人在试验阶段发现,临床常用细菌核糖体抑制剂利奈唑胺对氟康唑具有增效作用,揭示了其协同作用机制可能与核糖体亚基及蛋白质合成有关,从而为研究抗真菌药物作用的新靶点提供思路。
具体的,本发明试验结果表明,flc与lzd联用时,可以产生协同抗真菌作用。对氟康唑耐药的白色念珠菌菌株(micflc>512μg/ml),联合用药可使其最低抑菌浓度明显降低,32μg/ml的lzd与1μg/ml的flc合用均可以杀灭80%以上的真菌,浓度再增大,效果更强。此外,发明人意外发现,对氟康唑敏感的白色念珠菌菌株(micflc<4μg/ml),联合用药也可使其最低抑菌浓度明显降低。
3.本发明试验结果表明,核糖体亚基可能是联合抗真菌作用的靶点,为新药的开发及老药新用提供可能的研究方向。
4.利奈唑胺在临床上应用广泛,其对氟康唑抗真菌的增效作用,可扩大其应用范围,并且降低flc的最低有效浓度,减少抗真菌药物的用药量,从而降低药物的不良反应的发生,从而有效克服临床真菌耐药问题,并为克服真菌耐药问题提供新的思路。
附图说明
图1为氟康唑联合利奈唑胺应用时的三维效果图;
其中:x轴代表氟康唑的浓度,y轴代表利奈唑胺的浓度,z轴代表的是各个药物组合下的δe值,高于或低于平面(δe=0)的值分别表示协同或拮抗作用,平面周围的值表示无关作用,图右侧的色彩编码条中,越靠近上端说明协同作用越强。
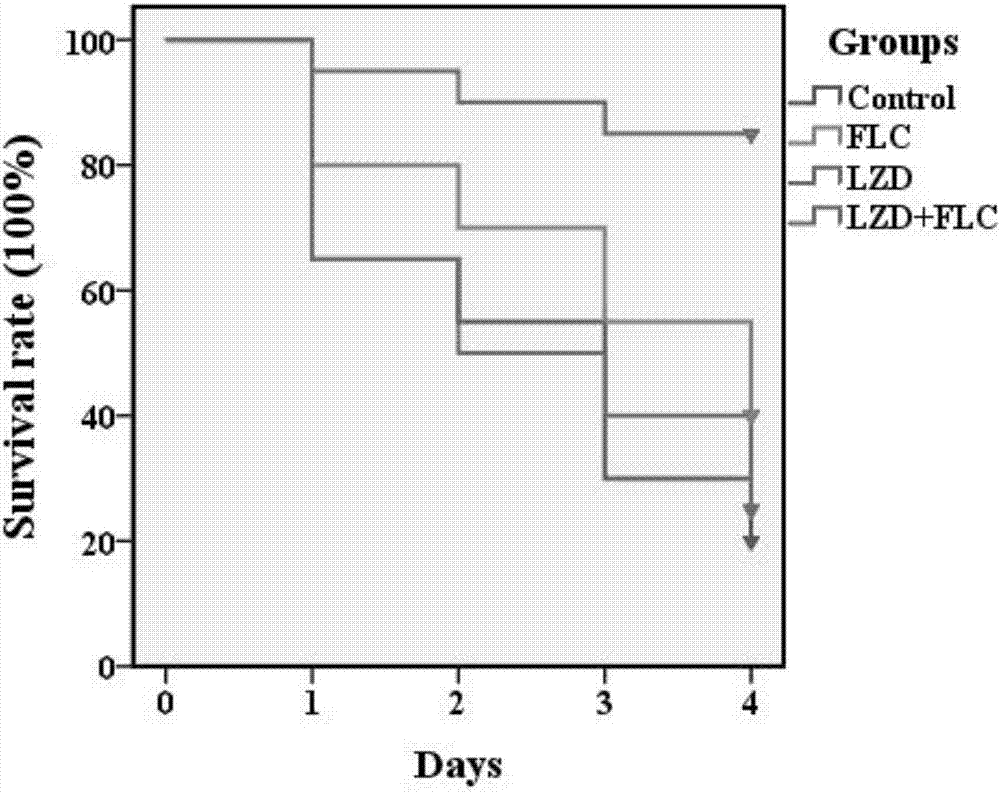
图2为氟康唑联合利奈唑胺应用时大蜡螟的生存率曲线。
具体实施方式
应该指出,以下详细说明都是例示性的,旨在对本申请提供进一步的说明。除非另有指明,本文使用的所有技术和科学术语具有与本申请所属技术领域的普通技术人员通常理解的相同含义。
需要注意的是,这里所使用的术语仅是为了描述具体实施方式,而非意图限制根据本申请的示例性实施方式。如在这里所使用的,除非上下文另外明确指出,否则单数形式也意图包括复数形式,此外,还应当理解的是,当在本说明书中使用术语“包含”或“包括”时,其指明存在特征、步骤、操作、器件、组件或它们的组合。
正如背景技术所介绍的,氟康唑(fluconazole,flc)作为安全、有效、价格低廉的抗真菌药物,对白色念珠菌有很好的疗效。但随着flc在临床上的广泛应用,使得白色念珠菌对唑类药物的耐药性不断增高,因此寻找新的抗真菌手段迫在眉睫。
有鉴于此,本发明的一种典型实施方式中,提供一种利奈唑胺联合氟康唑在制备抗真菌产品中的应用。
其中,所述真菌为白色念珠菌;
所述产品为药物;
优选的,所述利奈唑胺与氟康唑联合应用时,利奈唑胺的浓度为浓度为:32-256μg/ml,氟康唑的浓度为1-128μg/ml;
所述利奈唑胺联合氟康唑联合应用时有效浓度配比氟康唑:利奈唑胺=1:32。
所述应用时利奈唑胺的最低抑菌浓度为32μg/ml;
所述应用时氟康唑的最低抑菌浓度为1μg/ml。
本发明的又一典型实施方式中,提供一种抗真菌产品,所述产品包含利奈唑胺和氟康唑。
具体的,所述利奈唑胺和氟康唑的有效浓度配比为氟康唑:利奈唑胺=1:32;
所述利奈唑胺的最低抑菌浓度为32μg/ml;
所述氟康唑的最低抑菌浓度为1μg/ml;
试验结果表明:大于32μg/ml的利奈唑胺与大于1μg/ml的氟康唑联合应用时具有协同抗白色念珠菌的作用。
本发明的又一典型实施方式中,提供一种抗真菌产品,由利奈唑胺和氟康唑以及药学上可接受的辅料组成,在本发明提供的抗真菌产品中,药学上可接受的辅料为药物制剂中的常规辅料,如:崩解剂、润滑剂、黏合剂等;优选为甘油、丁二醇、海藻糖、甜菜碱、淀粉、羧甲基纤维素钠中的一种或多种。
下面通过具体实例对本发明进行进一步的阐述,应该说明的是,下述说明仅是为了解释本发明,并不对其内容进行限定。
实施例1flc与lzd联合抗真菌作用测定
1.材料
1.1药品与试剂
氟康唑(fluconazole,flc),山东诚创医药科技发展有限公司;
利奈唑胺(linezolid,lzd),大连美仑生物有限公司;
科玛嘉念珠菌显色培养基,郑州博赛生物工程有限公司;
ttc-沙保罗琼脂,杭州天和微生物试剂有限公司;
氢氧化钠,国营山东单县有机化工厂,批号940420;
磷酸二氢钾,上海新宝精细化工厂,批号200602132;
二甲基亚砜(dmso),天津市广成化学试剂有限公司;
rpmi1640原料药粉,美国gibco公司;
3-(n-吗啉代)丙磺酸(mops),济南朋远生物技术有限公司;
甲萘醌(menadione),美国sigma公司;
xtt(二甲氧唑黄),南京旋光科技有限公司;
乳酸林格氏液(复方氯化钠溶液),山东鲁抗辰欣药业有限公司;
丙酮,上海振兴化工一厂,批号200209510;
xtt(3,3'-[1-(苯氨酰基)-3,4-四氮唑]-二(4-甲氧基-6-硝基)苯磺酸钠)-甲萘醌溶液的配制:取xtt粉末0.0500g,溶解于100ml已灭菌的林格氏液配成0.5mg/ml的溶液,用0.22μm滤膜滤过灭菌;加入10μl的10mmol/l的甲萘醌丙酮溶液(取甲萘醌0.0860g溶解于5ml丙酮),使其终浓度为1μmol/l,摇匀,2℃~8℃避光保存。
药物溶液:氟康唑和利奈唑胺用无菌蒸馏水溶解,其他药物用二甲基亚砜溶解,分别配成2560μg/ml的储备液,过滤(0.22μm)分装。所有药液于-20℃冰箱保存,备用。
pbs(磷酸盐缓冲液):用北京鼎国昌盛生物技术有限公司的pbs磷酸盐缓冲剂(粉剂),小包装一袋溶于1l蒸馏水中,即配成0.01m,ph7.4的pbs磷酸盐缓冲液,121℃高温高压湿热灭菌20min,冷却备用。
rpmi(roswellparkmemorialinstitute)1640液体培养液:取rpmi1640(含l-谷氨酰胺,不含碳酸氢钠)粉末2.08g,加入10%葡萄糖溶液40ml(含糖终浓度2%)及mops(3-(n-吗啉基)丙磺酸)粉6.906g,加蒸馏水至200ml,混合均匀后在22℃用1mol/l的naoh溶液调ph为7.0±0.1,临用前用0.22μm混合纤维膜过滤灭菌。
1.2仪器
1.3实验菌株
质控菌株:白念珠菌atcc10231,山东大学药理教研室惠赠;
实验菌株:省立医院、千佛山医院临床分离的念珠菌;
菌株鉴定:实验用菌株在科玛嘉念珠菌显色培养基35℃下培养48小时,菌落呈绿色或翠绿色为白色念珠菌,粉红色(模糊有微毛菌落较大)为克柔念珠菌,紫色为光滑念珠菌。菌株再经山东省疾病预防控制中心微生物研究室以标准微生物学方法鉴定。
菌液制备:-20℃下保存的念珠菌室温下解冻,接种到ttc-沙保罗琼脂培养基上,35℃培养24~48h,取发育良好的单一菌落再次接种,35℃培养24h,以保证菌株处于生长期。选取若干单个较大菌落,pbs配制成菌悬液,经涡旋器振荡均匀后以中国细菌浊度标准管比浊,调整样品管与标准管浊度一致,此时念珠菌的菌浓度约为4.5×106cfu/ml,系列稀释即得到工作菌液,并以活菌计数进行浓度验证。
2.内容与方法
2.1氟康唑与利奈唑胺的联合抗真菌作用测定
2.1.1微量稀释法
根据clsim27-a3方案的棋盘法,以rpmi-1640液体培养基稀释药液使其成为4倍工作浓度,筛选lzd或flc浓度应用范围,即lzd的终浓度为4-256μg/ml,flc为0.25-128μg/ml。按浓度从低到高的顺序吸取氟康唑药液50μl,分别加入96孔平板的第2~12列,按浓度从低到高的顺序吸取利奈唑胺药液50μl,分别加入96孔平板的第g~a行,除a12外各孔再分别加100μl菌液,其余不足200μl的孔用rpmi-1640培养液补足。其中h1为生长对照,只含菌液不含药物,a12为空白对照,只含药液不含菌液。将96孔平板置35℃恒温培养箱中培养24h后,用xtt负载后以酶标仪测定并记录结果。所有实验重复三次。
2.1.2体内模型
将浓度为2560μg/ml的氟康唑和利奈唑胺药物储备液以无菌pbs稀释成所需的工作浓度。
取ttc-沙保罗琼脂培养基上传代两次的实验菌株(ca10),挑取单个较大菌落,以pbs制成菌悬液,采用中国细菌浊度标准进行比浊,当标准管与样品管浓度一致时,菌液初始浓度约为4.5×108cfu/ml,以rpmi-1640稀释至10倍工作浓度,通过活菌计数法进行浓度验证。
选取体重均为0.25±0.03g的四龄大蜡螟幼虫,排除体表发灰、有黑色斑点、触碰后无反应的个体。将大蜡螟随机分组,共4组,每组20只,放在无菌培养皿中培养。生长对照组:共1个体系,只接种白色念珠菌,注射pbs作为对照;flc单用组:注射浓度为160mg/l的flc药液;lzd单用组:注射浓度为200mg/l的lzd药液;联用组:注射flc/lzd浓度为160mg/l/200mg/l药液。注射时,选择大蜡螟最后一对腹足的左侧一只,使用微量进样针插入体腔打入10μl祸旋后的菌液。全部接种ca10后,避光需35℃培养2小时。然后,在大蜡螟最后一对腹足的右侧一只,同样使用微量进样针注射10μl药液。每只大蜡螟接受的总液体量为20μl。全部注射完成后,培养皿需35℃无光环境中培养。每24小时取出,统计死亡数。虫体发黑或用摄子触碰后无反应则视为死亡。共观察96小时,结果使用spss软件绘制生存曲线。实验重复操作3次。
2.2评价方法与结果判定
2.2.1la理论
loeweadditivity(la)理论的基本思想认为药物不可能和它本身发生相互作用,因此将药物单用或联用产生相同药效的浓度(等效位点)进行比较。其分析方法分数抑菌浓度指数法(fractionalinhibitoryconcentrationindex,fici),表述如下:
σfic=fica+ficb=ca/mica+cb/micb
mica和micb分别是药物a和b单用时的最小抑菌浓度,ca与cb为两药联用时达到相同药效时各自的浓度。fici>4为拮抗作用,fici在0.5与4之间为相加或无关作用,fici≤0.5定义为协同作用。
2.2.2生存曲线
大蜡螟幼虫经接种菌液和药物后,置35℃无光环境中培养,每24小时取出,统计死亡数。虫体发黑或用摄子触碰后无反应则视为死亡。共观察96小时,结果使用spss软件绘制生存曲线。实验重复操作3次。
3.结果
3.1氟康唑与非抗菌药物的联合抗真菌作用结果
3.1.1氟康唑与非抗菌药物联合的最低有效菌浓度
各孔中真菌生长百分数的计算方法为:
真菌生长百分数=(各孔od值-空白对照孔od值)/生长对照孔od值
按上述公式计算平板中各孔真菌生长百分数,取能够抑制真菌生长80%的最低联用药物浓度为判读终点,如果真菌生长率不恰好等于20%,取与之最接近的药物联合孔为判读终点。
flc与lzd联合抗真菌作用,对耐药株呈现强协同作用。其中耐药株ca10平板中的生长百分数实验结果如表1所示。
表1用棋盘表示flc与lzd的联合用药抗耐药白色念珠菌ca10生长百分率(以fici法换算的药物最佳作用组合用灰色标出)
3.1.2fici法评价flc/lzd的协同作用
三次重复性实验所得结果见表2。由测定结果可见,lzd与flc联合应用时,对白色念珠菌的作用fici<0.5,呈现协同作用。其中对耐药白色念珠菌的fici值更小,显示出更好的协同作用。而对耐药非白色念珠菌的fici值则在0.5和2之间,呈现无关作用。
表2以fici法评flc/lzd联合用药抗真菌作用
3.1.3体内模型评价flc/lzd联用作用
将观察得到的大蜡螟幼虫生存率结果绘制成生存曲线,可直观地看到联合用药对大蜡螟感染模型的作用效果,如图2所示:生长对照组的生存率在培养四天后为20%,药物单用组则分别为flc:40%,lzd:略大于20%。而与氟康唑单用组相比,联合用药组的生存率高出45%,达到了85%。
4.结论
面对临床应用中抗真菌药物较少且出现耐药现象的现状,研制新型的抗真菌药物是解决这一问题的途径之一,同时通过联合用药的方式来增加真菌对药物的敏感性也是一种较好的选择。lzd作为临床常用抗菌药物,其本身无明显抗真菌作用,但与flc联用抗耐药白色念珠菌却能显著的降低flc的mic值,表现协同作用。但是lzd与flc联用对非白色念珠菌几乎无作用。此外,已有文献报道,lzd与两性霉素b联用时具有抗新隐球菌的作用。lzd的抗细菌机制为与核糖体亚基结合抑制蛋白质的合成,与flc的协同作用机制是否也与核糖体亚基和蛋白质合成有关,有待进一步研究。本发明表明flc和利奈唑胺联合治疗白色念珠菌感染在临床上有一定的应用前景。
上述虽然结合附图对本发明的具体实施方式进行了描述,但并非对本发明保护范围的限制,所属领域技术人员应该明白,在本发明的技术方案的基础上,本领域技术人员不需要付出创造性劳动即可做出的各种修改或变形仍在本发明的保护范围以内。
- 还没有人留言评论。精彩留言会获得点赞!