一种超级电容器电极用含氮、氧原子的网状聚合物材料及其制备方法与流程
本发明属于材料科学领域,涉及到超级电容器电极用网状聚合物材料及其制备技术,特别涉及到一种超级电容器电极用含氮、氧原子的网状聚合物材料及其制备方法。
背景技术:
超级电容器作为一种独特的能量存储装置,兼具传统介电电容和电池的特性,其具有功率密度高、快速充放电、使用寿命长、温度特性好、免维护、环境友好等特点,因此被视为本世纪最有希望的新型绿色能源。
超级电容器已成为材料、电力、电子、物理、化学等多学科交叉领域研究的热点之一。主要研究目标是制备高能量密度和高功率密度的低成本电极材料,而影响能量密度的重要参数是电极材料的比电容。目前,超级电容器的比电容较低,进而限制了其广泛应用,而超级电容器中电极材料的化学组成和微观结构是影响超级电容器的比电容的决定性因素,所以需要设计新型大容量的、具有优异循环稳定性的超级电容器电极材料。
近年来,已有研究表明向超级电容器电极材料中引入杂原子可使电极材料内部发生快速氧化还原反应,从而提高超级电容器的比电容,其中应用最广泛的杂原子是氮原子及氧原子。例如,Liang等(N-doped mesoporous carbon as a bifunctional material for oxygen reduction reaction and supercapacitors,Chinese Journal of Catalysis,2014,35:1078-1083.)制备得到一种氮掺杂的微孔炭材料,其比电容可达252F/g;Li等(Preparation and Supercapacitor Performance of Nitrogen-Doped Carbon Nanotubes from Polyaniline Modification,Acta Physico-Chimica Sinica,Volume 29 2013,29:111-116(6).)将碳纳米管通过聚苯胺修饰得到超级电容电极材料,其比电容可达205F/g;Lee等(Theoretical approach to ion penetration into pores with pore fractal characteristics during double-layer charging/discharging on a porous carbon electrode,Langmuir,2006,22:10659-10665.)的研究结果表明合理的杂原子含量及孔结构会具有更好的倍率性能。但是,上述方法多为单一引入某一种杂原子,这会导致材料的有效活性位点较少,且易发生分布不均匀的情况。如何保证超级电容器用电极材料上活性位点较多且分布均匀,目前仍是一个挑战。
技术实现要素:
本发明涉及一种超级电容器电极用含氮、氧原子的网状聚合物材料及其制备方法,具体是制备一种含二氮杂萘酮及均三嗪结构的聚合物,其制备方法简单、产率高。以该网状聚合物材料为电极的超级电容器具有高的比电容,且循环稳定性优异等特点,该材料是超级电容器的一种新型高效电极材料。本发明的聚合物是含二氮杂萘酮及均三嗪结构的有机网状聚合物,是含氰基官能团的杂环芳烃通过氰基三聚反应形成的三维网状结构聚合物,具有高比表面积、丰富的孔结构,通过调控聚合反应条件可调控聚合物的分子结构和杂原子掺杂(包括杂原子种类及含量均可控)。
为实现上述目的,本发明采用以下技术方案:
一种超级电容器电极用含氮、氧原子的网状聚合物材料,所述含氮、氧原子的网状聚合物材料由式Ⅱ所示的二腈单体聚合而成,一个所述二腈单体中的某一氰基与另外两个所述二腈单体中的某一氰基随机三环化以形成均三嗪结构,所述网状聚合物材料是含二氮杂萘酮及均三嗪结构的网状聚合物,所述网状聚合物材料中具有式Ⅰ所示的重复单元结构:
其中:为
为
为
相同或不同;
R1、R2、R3、R4独立为H、F、Cl、Br、I、COOH、烷氧基中的一种;
R1、R2、R3、R4相同或不同。
本发明中所述网状聚合物材料统一命名为:multiple heteroatoms carbon framework,简写是MHCF;中文名称为:多种杂原子的碳网络材料。不同温度下聚合而成的网状聚合物材料命名为MHCF@聚合温度,比如在600℃下聚合,即写成MHCF@600。
一种上述超级电容器电极用含氮、氧原子的网状聚合物材料的制备方法,包括以下步骤:
步骤一:以式Ⅲ所示的含二氮杂萘酮结构的卤代物和氰化试剂为原料,进行偶联反应,反应液经后处理得到式Ⅱ所示的二腈单体;
步骤二:以所述二腈单体为原料,进行聚合反应,反应产物经后处理得到所述网状聚合物材料。
所述X为F、Cl、Br、I中的一种;R1、R2、R3、R4独立为H、F、Cl、Br、I、COOH、烷氧基中的一种;R1、R2、R3、R4相同或不同。
在上述制备方法中,作为一种优选实施方式,在所述步骤一中,所述偶联反应具体如下:在非质子极性溶剂中,在碳酸盐、催化剂存在下,所述含二氮杂萘酮结构的卤代物与所述氰化试剂进行反应,反应温度为50~200℃(比如55℃、60℃、80℃、100℃、120℃、140℃、160℃、180℃、195℃),反应时间为2~10h(比如2.5h、3h、4h、5h、6h、7h、8h、9h、9.5h);
更优选地,所述非质子极性溶剂为N,N-二甲基甲酰胺(DMF)、N,N-二甲基乙酰胺(DMAc)、二甲基亚砜(DMSO)、N-甲基吡咯烷酮(NMP)中的一种或几种的混合溶剂;所述碳酸盐为Li2CO3,Na2CO3,K2CO3,Rb2CO3,Cs2CO3中的一种;所述氰化试剂为亚铁氰化钾(即K4[Fe(CN)6]);所述催化剂为醋酸镍、醋酸钯或醋酸铂。
在上述制备方法中,作为一种优选实施方式,所述偶联反应中,以非质子极性溶剂的用量为100mL计,所述含二氮杂萘酮结构的卤代物的用量为5-15g(比如5.5g、6g、7g、8g、9g、10g、11g、12g、13g、14g、14.5g),所述氰化试剂的用量为2-7g(比如2.5g、3g、3.5g、4g、4.5g、5g、5.5g、6g、6.5g),所述碳酸盐的用量为2-7g(比如2.5g、3g、3.5g、4g、4.5g、5g、5.5g、6g、6.5g),所述催化剂的用量为0.02-0.6g(比如0.021g、0.03g、0.05g、0.1g、0.15g、0.2g、0.25g、0.3g、0.35g、0.4g、0.45g、0.5g、0.55g、0.59g)。
在上述制备方法中,作为一种优选实施方式,在所述步骤一中,所述后处理具体如下:将所述反应液倒入沉淀剂中,经静置、抽滤后收集固体,收集到的固体经提纯、烘干得到白色粉末状二腈单体。
更优选地,所述静置的时间为10~30h(比如11h、12h、14h、16h、18h、20h、22h、24h、26h、28h、29h);
更优选地,所述沉淀剂为醇类或/和水;进一步地,所述醇类为乙醇;
更优选地,所述提纯是将所述固体在N-甲基吡咯烷酮(NMP)中进行重结晶;进一步地,所述重结晶的方法如下:按照所述固体质量:N-甲基吡咯烷酮质量=1:2~4(比如1:2.1、1:2.2、1:2.4、1:2.6、1:2.8、1:3.0、1:3.2、1:3.4、1:3.6、1:3.8、1:3.9)将所述固体和N-甲基吡咯烷酮混合,然后回流0.5~1.5h(比如0.6h、0.8h、1.0h、1.2h、1.4h),之后趁热过滤,弃滤饼留滤液,再将滤液静置10-30h(比如11h、12h、14h、16h、18h、20h、22h、24h、26h、28h、29h),析出白色固体后抽滤,留滤饼,再用乙醇冲洗所述滤饼3-5次(比如3次、4次、5次);
更优选地,所述烘干是在相对真空度为-0.1MPa的条件下,于100~150℃(比如101℃、105℃、110℃、120℃、130℃、140℃、145℃)烘干20-30h(比如21h、22h、24h、26h、28h、29h)。
在上述制备方法中,作为一种优选实施方式,在所述步骤二中,所述聚合反应具体如下:在路易斯酸催化剂和真空条件下,所述二腈单体在600~700℃(比如601℃、610℃、620℃、630℃、640℃、660℃、680℃、695℃)聚合20~40h(比如21h、25h、30h、35h、39h);
更优选地,在路易斯酸催化剂和真空条件下,采用程序升温,先以3~5℃/min(比如3.1℃/min、3.5℃/min、4℃/min、4.5℃/min、4.9℃/min)的升温速度将所述二腈单体升温至300~400℃(比如301℃、310℃、320℃、330℃、340℃、360℃、380℃、395℃)并保温10~30h(比如11h、12h、14h、16h、18h、20h、22h、24h、26h、28h、29h),然后再以3~5℃/min(比如3.1℃/min、3.5℃/min、4℃/min、4.5℃/min、4.9℃/min)升温至600℃~700℃(比如601℃、610℃、620℃、630℃、640℃、660℃、680℃、695℃)并保温聚合20~40h(比如21h、25h、30h、35h、39h)。
在聚合步骤采用程序升温,可使得二腈单体聚合更加充分。
更优选地,所述路易斯酸催化剂为三氯化铝、三氯化铁、四氯化钛、氯化锌、三氟化硼中的一种或几种混合物;所述真空条件的相对真空度为-0.07MPa~-0.1MPa(比如-0.075MPa、-0.08MPa、-0.09MPa、-0.095MPa)。
在上述制备方法中,作为一种优选实施方式,在所述聚合反应中,所述二腈单体与所述路易斯酸催化剂的摩尔比为1:5~10(比如1:5.1、1:5.5、1:6、1:6.5、1:7、1:7.5、1:8、1:8.5、1:9、1:9.5、1:9.9)。
在上述制备方法中,作为一种优选实施方式,在所述步骤二中,所述后处理具体如下:将反应产物依次进行酸洗、水洗、过滤并收集固体、干燥,从而得到所述网状聚合物材料。
更优选地,所述酸洗是将所述反应产物分散在浓度为0.5~1.5M(比如0.6M、0.7M、0.8M、0.9M、1.0M、1.1M、1.2M、1.3M、1.4M)的酸液中,采用机械搅拌或超声分散洗涤10~20h(比如11h、12h、13h、14h、15h、16h、17h、18h、19h)后进行过滤或离心分离,收集得到的固体;进一步地,所述酸液为稀盐酸、稀硫酸、稀硝酸;所述反应产物在所述酸液中的质量浓度为0.03~0.15g/mL(比如0.04g/mL、0.06g/mL、0.08g/mL、0.10g/mL、0.12g/mL、0.14g/mL);
酸洗的目的是洗去残留在网状聚合物中的路易斯酸催化剂;
更优选地,所述水洗是用去离子水洗10~20h(比如11h、12h、13h、14h、15h、16h、17h、18h、19h)至中性;
更优选地,所述干燥是在100~120℃(比如101℃、105℃、110℃、115℃、119℃)条件下,干燥20~30h(比如21h、22h、24h、26h、28h、29h)。
为了进一步考证本发明提供的含二氮杂萘酮及均三嗪结构的网状聚合物的电性能,将本发明的网状聚合物与导电炭黑和6wt%的聚四氟乙烯的去离子水溶液,按质量比80:10:10的比例,加到无水乙醇中混合制成浆料,反复碾压浆料,得到薄片状电极材料。将所述电极材料放在相应大小的钛网集流体上,3兆帕冷压20s,然后120℃下烘干10~30h(比如11h、12h、14h、16h、18h、20h、22h、24h、26h、28h、29h),之后将干燥好的薄膜用压片机压成12mm直径的圆片,将其压到400目钛网上(15mm*30mm*0.03mm)作为电极,并组装成对称超级电容器,然后将其放入1M的H2SO4溶液中测试其电性能。使用Ag/AgCl和铂电极分别作为参比电极和对电极。经采用循环伏安法、恒流充放电法、交流阻抗法、CHI660D电化学工作站进行全面的测试表征。以下实施例制备的聚合物均采用该种方法进行电化学性能的测试。
本发明的有益效果:本发明的含有氮、氧原子的网状聚合物制备的电极材料所组装的三电极体系超级电容器具有优异的电化学特性,即具有高的比电容,在电解液为水系的条件下,电流密度0.1A.g-1时比电容可达到308F.g-1;良好的循环稳定性,特别是高倍率下的充放电,其电容衰减不明显(经30000次充放电后其比电容无衰减)。可见本发明提供的含有氮、氧原子的网状聚合物材料可以作为制备超级电容器的电极材料。
另外,本发明中含氮、氧原子的网状聚合物的制备方法简单、收率高,易于控制,有利于工程化技术的实现。本发明制备的含氮、氧原子的网状聚合物中,氮、氧杂原子分布均匀,且具有较大的比表面积和合理的孔径分布(微孔孔径范围:<2nm,中孔孔径范围:2~5nm)。本发明方法的聚合物收率为60-80%。
附图说明
图1为PDBN的1H NMR谱图。
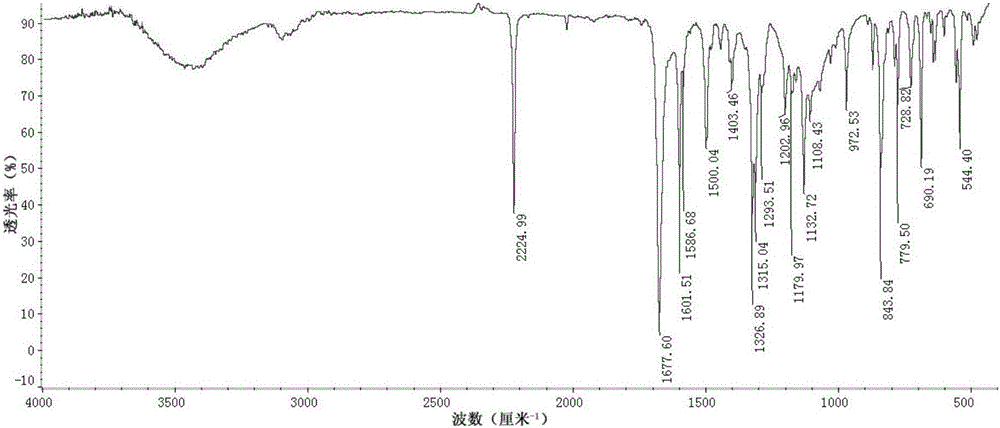
图2为PDBN的红外谱图。
图3为PDBN的DSC谱图。
图4为PDBN的TGA谱图。
图5为MHCF@600的红外光谱图。
图6是不同温度焙烧制备的MHCF的氮气吸脱附曲线图和孔径分布图,其中:(a)为不同温度焙烧制备的MHCF的氮气吸脱附曲线图;(b)为不同温度焙烧制备的MHCF的孔径分布。
图7是MHCF@600的高分辨率TEM谱图,其中:(a)为MHCF@600的高分辨率TEM谱图;(b)为MHCF@600的高分辨率TEM局部放大图;(c)为MHCF@600的碳原子分布标记图;(d)为MHCF@600的氮原子分布标记图;(e)为MHCF@600的氧原子分布标记图。
图8是不同聚合温度下制备的MHCF的C-V循环曲线图(5mV/s)。
图9是不同聚合温度下制备的MHCF的恒流充放电曲线图(3A/g)。
图10是不同聚合温度下制备的MHCF所得的电极材料的比容量随电流密度的变化情况。
图11是不同聚合温度下制备的MHCF所得的电极材料的交流阻抗图谱。
图12是MHCF@600所得的电极材料循环稳定性测试图。
具体实施方式
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于本发明而不用于限制本发明的范围。对外应理解,在阅读了本发明的内容之后,本领域技术人员对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1
本实施例通过偶联反应、聚合反应制备MHCF@600。
MHCF@600由式Ⅱ所示的二腈单体聚合而成,每个二腈单体中均含有两个氰基,每个氰基都可以和另外两个二腈单体中的某一氰基随机三环化以形成均三嗪结构,多个二腈单体之间的氰基发生三环化反应,从而连接成含有均三嗪结构的网状聚合物,具有如下式Ⅰ所示的重复结构单元:
其中:为
为
为
相同或不同;
R1、R2、R3、R4独立为H、F、Cl、Br、I、COOH、烷氧基中的一种;
R1、R2、R3、R4相同或不同;
下面列举网状聚合物中所含的其中一种典型结构,如下所示:
在本实施例中,R1、R2、R3、R4都为H。
具体制备方法如下:
(1)PDBN的制备
向三口瓶中加入11g含二氮杂萘酮结构的溴代物(结构式如下式i所示)、3g亚铁氰化钾、3.5g碳酸钠、0.1g醋酸钯,再向三口瓶中加入100ml的N-甲基吡咯烷酮NMP,搅拌并在搅拌下抽真空然后充入氮气,升温至120℃反应12h;将得到反应液倒入到500mL乙醇中,静置25h后抽滤并收集固体,然后按照固体质量:N-甲基吡咯烷酮质量=1:3将固体和N-甲基吡咯烷酮混合,然后回流1h,之后趁热过滤,弃滤饼留滤液;再将滤液静置20h,析出白色固体后抽滤,留滤饼,再用乙醇冲洗滤饼4次,过滤收集固体,固体在相对真空度为-0.1MPa(真空表上的读数)的条件下,于130℃烘干25h,得到白色粉末状固体即为PDBN(结构式如下式ii所示)。整个反应式如下:
其中,上式中所示的化合物ii英文名称为4,4'-(4-oxophthalazine-1,3(4H)-diyl)dibenzonitrile,简写是PDBN,中文名称为4,4’-二氮杂萘酮基二苯腈。
得到的PDBN为6.5g,纯度为98%,收率为68%。
对得到的白色粉末状固体产物进行表征,如图1~图4所示。
图1为PDBN的1H NMR谱图,测试PDBN氢谱所用溶剂为d6-二甲基亚砜,所用仪器为500MHz核磁共振仪,图中所显示的氢的个数、化学位移、峰型与式ii所示的化合物相符;具体地,PDBN单体的1H-NMR谱的质子化学位移归属如下:δ7.70~δ7.72峰面积积分为1,是杂萘环的He;δ7.9处有二重峰,峰面积积分为2,是苯环上的Hd;δ8.0处峰面积积分为6,是苯环上的Hc,由于苯环是一个对称结构,且在其两个取代位点上所接的基团的吸电子强度接近,使得苯环上的Hc的化学环境相同,在同一场强下出峰;δ8.1有二重峰,峰面积积分为2,是苯环上的Hb;δ8.5峰面积积分为1,是杂萘环上的迫位氢Ha,由于Ha周围连接有碳基,碳基有很强吸电子能力,使得Ha的电子密度低,化学位移高,在低场位置出峰。所以由分析可得,目标产物被成功制得。
图2为PDBN的红外谱图;具体地,2224.99cm-1为氰基的伸缩振动峰,1677.60cm-1为羰基的伸缩振动峰,1601.51cm-1、1586.68cm-1、1500.04cm-1为苯环的伸缩振动峰;
图3为PDBN的DSC谱图,由图可知,DSC谱图上有一吸热峰,是熔点峰,峰面积较小,所以PDBN单体的纯度较高且结构排列较为规整,熔限较窄;
图4为PDBN的TGA-DTG谱图,由TGA图和DTG图可知,失重5%、10%和最大失重时的温度Td,5%、Td,10%、Td,max分别为378.2℃、400.5℃、468.1℃。这说明二腈单体在378℃前结构比较稳定,只有少量单体被分解,这是由于单体结构皆是芳环结构,不存在热不稳定化学键,所以耐热性好,在较低温度下不分解。温度达到468.1℃时,热失重达到最大值,此时所有的单体全部分解,直至全部分解完全。
(2)MHCF@600的制备
将0.5gPDBN(结构式如式ii所示)、0.2g无水氯化锌装入石英管中,抽真空至相对真空度为-0.05MPa,封管,以5℃/min升至400℃,保温20h,再以5℃/min升至600℃保温30h,石英管随炉降温至室温,取出石英管,将石英管中的产物倒入到1.5M的稀盐酸中超声1.5h,离心后用去离子水洗至中性、再经过滤收集固体,然后将固体在100℃干燥12h,即得到MHCF@600。聚合物的产量为350mg,收率为70%。
本发明聚合物是一种交联结构,不溶不融,是一种黑色固体粉末,其分子量无法测定,可通过控制聚合反应条件来控制聚合产物。
图5为MHCF@600的红外谱图;图中,1100~1200cm-1,1436cm-1,1550cm-1为均三嗪环伸缩振动吸收峰。
图6中,(a)为不同聚合温度下制备的MHCF的氮气吸脱附曲线图;P/P0<0.01时,聚合物吸附速度迅速增加,说明聚合物相对比表面积比较大,进而说明微孔存在;当存在滞后回线(磁滞回线),证明中孔存在。
(b)为不同聚合温度下制备的MHCF的孔径分布图;由孔径分布曲线得知,微孔孔径范围:<2nm;中孔孔径范围:2~5nm;随着温度的升高,材料的中孔结构呈现上升趋势。
图7中,图(a)是MHCF@600的投射扫描电镜照片;图(b)是图(a)的局部放大照片;图(c)是图(b)的碳原子标记图;图(d)是图(b)的氮原子标记图;图(e)是图(b)的氧原子标记图。
为了进一步考证其电性能,进行电化学性能测试。
称取30mg干燥的MHCF@600(活性物质)、3.75mg导电炭黑和3.75mg6wt%的聚四氟乙烯的去离子水溶液,加无水8mL乙醇混合制成浆料,反复碾压浆料得到的薄片状电极材料,将所述电极材料放在相应大小的集流体上,3兆帕冷压20s,然后120℃下烘干,之后将干燥好的薄膜用压片机压成直径为12mm、厚度为0.08mm的圆片,将其压到400目钛网上(15mm*30mm*0.03mm)作为电极,然后将其放入1M的H2SO4溶液中测试其电性能。使用Ag/AgCl和铂电极分别作为参比电极和对电极。
图8为由不同聚合温度下制备的MHCF所得的电极材料C-V循环曲线图(5mV/s);由图可知C-V循环曲线有两处突出的部分,这是由于体系中掺杂了氮、氧杂原子,因而材料中存在赝电容机制,并且随着温度的升高,C-V曲线所围成的内部面积逐渐增大,即材料的比电容呈现上升的趋势。
图9为由不同聚合温度下制备的MHCF所得的电极材料恒流充放电曲线图(3A/g);由图可知,恒流充放电曲线近乎为等腰三角形,仅有很小的IR降,表明其电化学稳定性和可逆性较好。
图10为由不同聚合温度下制备的MHCF所得的电极材料的比容量随电流密度的变化情况;600℃:在电流密度为0.1A·g-1时,测得比电容为278F·g-1,当电流密度为3A·g-1,比电容下降到220F·g-1,当电流密度大于3A·g-1时,随着电流密度的增加,比电容下降缓慢;650℃:在电流密度为0.1A·g-1时,测得比电容为295F·g-1,当电流密度为3A·g-1,比电容下降到239F·g-1,当电流密度大于3A·g-1时,随着电流密度的增加,比电容下降缓慢;700℃:在电流密度为0.1A·g-1时,测得比电容为302F·g-1,当电流密度为3A·g-1,比电容下降到248F·g-1,当电流密度大于3A·g-1时,随着电流密度的增加,比电容下降缓慢。从图10中看出,700℃时,比电容最大且该体系三种材料的比电容保持率也较好;
在对以上聚合温度得到的聚合物的性能进行测试的同时,设定了550℃得到的聚合物做了对比例,550℃条件下得到的聚合物基本无电性能。
图11为由不同聚合温度下制备的MHCF所得的电极材料的交流阻抗图谱;在高频区交流阻抗曲线与实轴的交点对应的是包括电解液、材料内阻、接触内阻等在内的等效串联电阻,曲线与横轴的交点为0.2~0.5,所以等效串联电阻较小;曲线的半圆环直径对应着电荷的传递电阻,图中半圆环直径也较小,所以电荷的传递电阻也相应较小;而在低频区的曲线斜线与离子扩散和电容特性相关,即曲线斜率越大,离子扩散速率越快。由图可知,随着温度的升高,材料的电阻呈现降低的趋势,在700℃制得的材料其电阻最小。
图12为MHCF@600所得的电极材料循环稳定性测试图,经30000次充放电后,其比电容无衰减,仍能保持在112%。
实施例2
本实施例通过偶联反应、聚合反应制备MHCF@650。
(1)PDBN的制备
如实施例1所述。
(2)MHCF@650的制备
除将实施例1步骤(2)中的聚合温度600℃改为650℃以外,其他工艺和参数与实施例1相同。得到的聚合物MHCF@650的产量为320mg,收率为64%。
MHCF@650的氮气吸脱附曲线图和孔径分布图见图6。
为了进一步考证其电性能,进行电化学性能测试。测试方法如实施例1所述。
由MHCF@650的制得的电极材料循环伏安曲线图、恒流充放电曲线图、比容量随电流密度的变化情况及交流阻抗图谱参见图8-11。
650℃聚合得到的电极材料经30000次充放电后,其比电容无衰减,仍能保持在108%。
实施例3
本实施例通过偶联反应、聚合反应制备MHCF@700。
(1)PDBN的制备
如实施例1所述。
(2)MHCF@700的制备
除将实施例1步骤(2)中的聚合温度600℃改为700℃以外,其他工艺和参数与实施例1相同。得到的聚合物MHCF@650的产量为360mg,收率为72%。
MHCF@700的氮气吸脱附曲线及孔径分布参见图6。
为了进一步考证其电性能,进行电化学性能测试。测试方法如实施例1所述。
由MHCF@700的制得的电极材料循环伏安曲线图、恒流充放电曲线图、比容量随电流密度的变化情况及交流阻抗图谱参见附图8-11。
650℃聚合得到的电极材料经30000次充放电后,其比电容无衰减,仍能保持在105%。
实施例4
本实施例通过偶联反应、聚合反应制备MHCF-20h@600。
(1)PDBN的制备
如实施例1所述。
(2)MHCF-20h@600的制备
除将实施例1步骤(2)中的600℃保温30h改为20h以外,其他工艺和参数与实施例1相同。得到的聚合物MHCF-20h@600的产量为360mg,收率为72%。
为了进一步考证其电性能,进行电化学性能测试。测试方法如实施例1所述。
在电流密度为0.1A·g-1时,测得比电容为252F·g-1,当电流密度为3A·g-1,比电容下降到221F·g-1,当电流密度大于3A·g-1时,随着电流密度的增加,比电容下降缓慢;
600℃保温20h聚合得到的电极材料经30000次充放电后,其比电容无衰减,仍能保持在108%。
实施例5
本实施例通过偶联反应、聚合反应制备MHCF-F@600。
(1)下式中化合物iv的制备
除将实施例1步骤(1)中的含二氮杂萘酮结构的溴代物结构改为如下式iii所示,用量由11g改为13g,其他工艺和参数与实施例1相同。得到结构式如下式iv所示化合物的产量为7.75g,收率为68%。
(2)MHCF-F@600的制备
与实施例1相同。得到的聚合物MHCF-F@600的产量为400mg,收率为80%。
为了进一步考证其电性能,进行电化学性能测试。测试方法如实施例1所述。
在电流密度为0.1A·g-1时,测得比电容为272F·g-1,当电流密度为3A·g-1,比电容下降到258F·g-1,当电流密度大于3A·g-1时,随着电流密度的增加,比电容下降缓慢;
电极材料MHCF-F@600经30000次充放电后,其比电容无衰减,仍能保持在110%。
- 还没有人留言评论。精彩留言会获得点赞!