BMP3基因甲基化检测用试剂体系和试剂盒及其应用的制作方法
本发明涉及医学检验
技术领域:
,具体涉及一种BMP3基因甲基化检测用试剂体系和试剂盒及其应用。
背景技术:
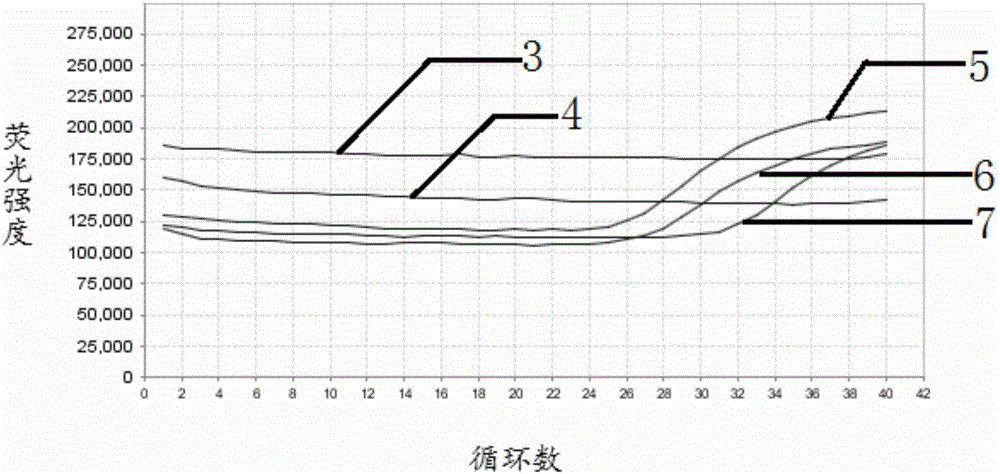
:结直肠癌是目前发病率较高的恶性肿瘤,在欧美发达国家,其发病率居恶性肿瘤第2位,仅次于肺癌,也是最常见的胃肠道恶性肿瘤。近年来,我国结直肠癌发病率和死亡率呈不断上升趋势,死亡率为恶性肿瘤第5位。早期结直肠癌患者经治疗后5年生存率可达90%以上,但往往早期结直肠癌患者很少有临床症状,不易被发现。而晚期结直肠癌患者的5年生存率不足10%。因此,寻找一个有效的易于筛查及早期诊断结直肠癌的试验方法,对结直肠癌的治疗甚至治愈有很重要的意义。目前常用的结直肠癌筛查、诊断方法,如粪便隐血试验及结直肠镜检查等存在特异性、敏感性或患者依从性的不足,限制了其在结直肠癌筛查及早期诊断中的广泛应用。在肿瘤研究中许多肿瘤的产生都伴随有基因的甲基化,癌基因的去甲基化和抑癌基因的甲基化状态,可导致癌基因的激活、抑癌基因的失活。癌基因的低甲基化和抑癌基因的高甲基化改变是肿瘤细胞的一个重要特征。因此本发明选择了与结直肠癌发生相关的BMP3基因甲基化状态来确定结直肠癌的发生。经过大量临床试验确定了BMP3基因的甲基化会导致结直肠癌的发生,通过检测病人肠道内大量脱落癌细胞中的BMP3基因甲基化状态,从而诊断结直肠癌的发生。本发明采用先进的分子诊断方法,采用荧光PCR法早期、快速、简便、敏感、特异检测结直肠癌。荧光PCR技术在1995年由美国PE公司率先研制成功,它兼有PCR的高灵敏性、DNA杂交的特异性和光谱技术精确定量的优点,结果直观,能直接检测PCR过程中的变化。与普通PCR相比,其结果可实时观察,产物不需要凝胶电泳检测,完全闭管操作,有效地降低了污染。技术实现要素:本发明需要解决的现有技术问题是:结直肠癌早期诊断困难,现有技术的诊断方法敏感性低、阳性率低并且不方便,尚未有能够快速、简便地检测BMP3基因甲基化状态的试剂。为了解决上述问题,本发明提供了一种BMP3基因甲基化检测用试剂体系和试剂盒及其应用,用来解决现有的结直肠癌诊断困难,敏感性低、阳性率低和不方便的问题。具体而言,针对现有技术的不足,本发明提供了如下技术方案:一方面,本发明提供了一种BMP3基因甲基化检测用试剂体系,所述试剂体系包括特异性引物和特异性探针,所述特异性引物如SEQIDNO.1和SEQIDNO.2所示,所述特异性探针如SEQIDNO.3所示。优选的,所述特异性探针上连接有荧光基团和淬灭基团,其中,所述的荧光基团选自6-羧基荧光素、六氯-6-甲基荧光素、四氯-6-羧基荧光素、2,7-二甲基-4,5-二氯-6-羧基荧光素、异硫氰酸荧光素、TexasRed、Cy3、Cy5或VIC中的一种;所述的淬灭基团选自BHQ、4-(4-恶氨基苯偶氮)苯甲酸)或羧基四甲基罗丹明。优选的,所述试剂体系还包括阳性标准品,所述阳性标准品中含有插入了BMP3基因甲基化特异性序列SEQIDNO.4的重组质粒。优选的,试剂体系还包括阴性标准品,所述的阴性标准品中含有未插入BMP3基因甲基化特异性序列的质粒。优选的,所述重组质粒的浓度为1.0×103-1.0×104copies/μL,所述阴性标准品中质粒浓度为1.0×103-1.0×104copies/μL。优选的,所述的质粒或重组质粒相同,选自pETs、pUCs、pGM-T、pBR322或pMD-T中的一种,优选为pGM-T或pBR322。优选的,所述阳性标准品中的重组质粒和所述阴性标准品中的质粒的制备方法如下:(1)以序列SEQIDNO.4为模板,利用引物序列SEQIDNO.5和SEQIDNO.6进行扩增,得到目的基因;(2)将目的基因连接到质粒载体上,得到连接产物;(3)将连接产物转化到宿主细胞内;(4)筛选含有构建好的重组质粒作为阳性标准品;不含目的基因的重组质粒作为阴性标准品。优选的,所述的试剂体系还包括缓冲液和dNTPs,所述的缓冲液包括三羟甲基氨基甲烷、氯化钾和氯化镁。优选的,所述的三羟甲基氨基甲烷的浓度为50~200mM;氯化钾的浓度为300~800mM;氯化镁的浓度为20~50mM。优选的,所述的三羟甲基氨基甲烷的浓度为100~150mM;氯化钾的浓度为400~600mM;氯化镁的浓度为30~40mM。优选的,所述的试剂体系还包括DNA聚合酶。优选的,所述的DNA聚合酶为TaqDNA聚合酶。第二方面,本发明提供了一种BMP3基因甲基化检测用试剂盒,其包含以上任一项所述的试剂体系。第三方面,本发明提供了特异性引物SEQIDNO.1和SEQIDNO.2以及特异性探针SEQIDNO.3在制备BMP3基因甲基化检测试剂或者试剂盒中的应用。优选的,本发明提供了特异性引物SEQIDNO.1和SEQIDNO.2以及特异性探针SEQIDNO.3在制备BMP3基因甲基化结直肠癌检测试剂或者试剂盒中的应用。优选的,以上应用中,所述的BMP3基因甲基化检测试剂或试剂盒的使用方法包括如下步骤:(1)对样本DNA进行甲基化处理;(2)利用特异性引物SEQIDNO.1和SEQIDNO.2以及特异性探针SEQIDNO.3,对步骤(1)得到的甲基化处理的样本DNA进行荧光定量PCR反应,检测样本DNA的甲基化水平。优选的,以上应用中,所述使用方法还包括:将含有插入了BMP3基因甲基化特异性序列SEQIDNO.4的重组质粒作为阳性标准品,进行荧光定量PCR反应;将含有未插入BMP3基因甲基化特异性序列SEQIDNO.4的质粒作为阴性标准品,进行荧光定量PCR反应。优选的,以上应用中,所述将甲基化处理的样本DNA的制备方法包括如下步骤:(1)从粪便样本中提取基因组DNA;(2)利用亚硫酸氢盐处理基因组DNA,得到甲基化处理的样本DNA。优选的,以上应用中,所述的荧光定量PCR反应条件为:94~95℃预变性2~5min,1个循环;94~95℃15~20s、53~55℃30~50s、58~60℃30~50s,40~50个循环本发明的有益效果为:(1)本发明试剂盒定量准确,兼有PCR的高灵敏性、DNA杂交的特异性和光谱技术精确定量的优点,结果直观,能直接检测PCR过程中的变化,与普通PCR相比,其结果可实时观察,产物不需要凝胶电泳检测,完全闭管操作,有效地降低了污染。(2)本发明试剂盒检测灵敏度和特异性高,由于采取特异性引物和探针的双保险设计,灵敏度和特异性均有很大提高,能在临床症状出现之前检测结直肠癌。(3)本发明试剂盒检测速度快,总共仅需2个小时,步骤简单,可同时进行高通量样本检测。下面结合附图和各个具体实施方式,对本发明及其有益技术效果进行详细说明,其中:附图说明图1为本发明实施例一提供的结直肠癌阳性标准品的荧光PCR扩增曲线和阴性标准品的荧光PCR扩增曲线。其中编号1为阳性标准品,编号2为阴性标准品。图2为本发明实施例二提供的志愿者样本的荧光PCR扩增曲线。其中,编号为5,6,7的样本检测结果为结直肠癌样本,编号为3,4的样本检测结果为非结直肠癌样本。具体实施方式如上所述,本发明提供了一种BMP3基因甲基化检测用试剂体系和试剂盒,其目的是为了提高被测人群结直肠癌诊断的灵敏度和特异性,提供早期诊断的可靠性。具体而言,本发明提供了一种BMP3基因甲基化结直肠癌检测用试剂体系,所述的试剂盒包括用于结直肠癌检测的特异性引物SEQIDNO.1和SEQIDNO.2和特异性探针SEQIDNO.3。具体而言,本发明提供了一种BMP3基因甲基化检测用的试剂体系和试剂盒,所述试剂体系中含有反应液和DNA聚合酶。反应液中含有特异性引物SEQIDNO.1和SEQIDNO.2,以及特异性探针SEQIDNO.3;特异性探针的5’和3’端分别连接有荧光基团和荧光淬灭基团。所述荧光基团和荧光淬灭基团为本领域技术人员常用的基团。当探针上同时含有荧光报告基团和荧光淬灭基团时,不发出荧光;当特异性探针被DNA聚合酶降解时,荧光报告基团和荧光淬灭基团分开,发出荧光。反应液中还含有聚合酶链式反应需要的基本组分,比如缓冲液和dNTPs。在其中一优选实施方式中,反应液中的缓冲液组成为50~200mM三羟甲基氨基甲烷,300~800mM氯化钾和10~30mM氯化镁。试剂体系中的DNA聚合酶为TaqDNA聚合酶。在另一优选实施方式中,本发明提供了一种含有BMP3基因甲基化序列的重组质粒,所述BMP3基因甲基化序列如SEQIDNO.4所示,所述质粒选自pETs、pUCs、pGM-T、pBR322和pMD-T中的一种。在重组质粒筛选过程中,转化成功的含有BMP3基因甲基化序列的重组质粒装入阳性标准品管内,作为阳性对照;没有转化成功的空白质粒装入阴性标准品管内,作为阴性对照。在又一优选实施方式中,本发明提供了一种BMP3基因甲基化检测用试剂盒,所述试剂盒包含作为阳性对照的阳性标准品,作为阴性对照的阴性标准品,反应液以及DNA聚合酶。反应液与前述BMP3基因甲基化检测用的试剂体系中的反应液相同,同样含有特异性引物SEQIDNO.1和SEQIDNO.2,以及特异性探针SEQIDNO.3,反应液的组成为:每16μL反应液中含有的SEQIDNO.1、SEQIDNO.2、SEQIDNO.3和dNTP的量依次为10-15μM,10-15μM,10-15μM和2.5-3.0mM。试剂盒中的样品管内装有从粪便中提取、并经甲基化处理后的DNA样本。作为阳性标准品的重组质粒和作为阴性标准品的质粒筛选方法包括以下步骤:(1)以序列SEQIDNO.4为模板,利用引物进行PCR扩增,所述引物序列如SEQIDNO.5和SEQIDNO.6所示;(2)将PCR扩增产物连接到质粒上;(3)转化到大肠杆菌内;(4)筛选含有构建好的重组质粒装入阳性标准品管内,不含重组质粒的装入阴性对照品管内。采用本发明所述试剂盒检测BMP3基因甲基化的情况,检测方法包括以下步骤:样品预处理,将处理后的样品加入样品管内。制备待测溶液,即往阳性标准品管、阴性标准品管和样品管中分别加入反应液和DNA聚合酶,混匀;各组待测溶液中的样品量或阳性标准品含量或者阴性标准品含量相同,且反应液和DNA聚合酶的含量也相同;通常,待测溶液中阳性标准品、阴性标准品或者样品与反应液、DNA聚合酶的比为:(1-2)μL:(18-20)μL:(5-20)U。将待测溶液放入荧光定量PCR仪中进行测定,PCR测定的条件为:94~95℃预变性2~5min,1个循环;94~95℃15~20s,53~55℃30~50s,58~60℃30~50s,共40~50个循环;最后分析荧光定量PCR测定结果,判断样品提供者是否患有结直肠癌。检测前的样品处理方法包括,先利用基因组DNA提取试剂盒从粪便样本中提取DNA,再利用基因组DNA甲基化处理试剂盒处理提取得到的DNA。甲基化处理试剂盒的原理为亚硫酸氢盐法甲基化处理,经甲基化处理试剂盒处理后的DNA作为样品。本发明中的样本DNA来源于人的粪便DNA经过亚硫酸氢盐法甲基化的处理。样本基因组DNA经甲基化处理试剂盒处理后,若样本基因组中的BMP3基因序列中的胞嘧啶(C)已经被甲基化,则经甲基化处理试剂盒处理之后的BMP3基因序列不变,如SEQIDNO.4所示,特异性引物SEQIDNO.1和SEQIDNO.2以及特异性探针SEQIDNO.3能与SEQIDNO.4结合,荧光PCR反应过程中,在DNA聚合酶的作用下探针SEQIDNO.3上的5’荧光基团与3’淬灭基团分离,发出荧光;若样本基因组中的BMP3基因序列中的胞嘧啶(C)没有被甲基化,则经甲基化处理试剂盒处理后,BMP3基因序列中的C变成U,即甲基化处理后的BMP3基因序列与SEQIDNO.4不同,特异性引物SEQIDNO.1和SEQIDNO.2以及特异性探针SEQIDNO.3无法与处理后的样本DNA结合,荧光PCR反应过程中,探针SEQIDNO.3保持完整,由于同时连接有5’荧光基团与3’淬灭基团,荧光PCR反应过程中不发出荧光;即经甲基化处理试剂盒后,甲基化的BMP3基因在荧光定量PCR检测过程中会发出荧光,而没有甲基化的BMP3基因不发荧光。因此,本发明所述的试剂体系和试剂盒与荧光定量PCR检测相结合后,可以用于检测BMP3基因的甲基化状态。BMP3基因高度甲基化是结直肠癌的重要分子标志,故本发明所述的试剂体系和试剂盒及其使用在结直肠癌诊断中具有重要意义。采用本发明所述试剂盒检测BMP3基因甲基化状态的方法简单,灵敏度高,特异性强;通过检测BMP3基因甲基化能有效判断样本供体是否为结直肠癌患者。应当说明的是,实施例中未说明的常规条件和方法,通常按照所属领域实验人员常规的方法,具体可参照萨姆布鲁克和拉塞尔主编的《分子克隆实验指南》第三版,或按照制造厂商所建议的步骤和条件。下面结合附图和具体的实施例对本发明做进一步详细的说明,其中实施例中所用的试剂和仪器的厂家如下:荧光定量PCR仪,厂家:美国ABI实时荧光定量PCR仪7500,美国;dNTPs,厂家:TAKARA,日本;TaqDNA聚合酶,厂家:TAKARA,日本;SAP酶EF0511,厂家:赛默飞世尔科技有限公司;ExoI酶,厂家:TAKARA,日本;基因组DNA提取试剂盒,购自天根公司;基因组DNA甲基化处理试剂盒,购自QIAGEN公司;pGM-T质粒载体,pUC18质粒载体,pMD18-T质粒载体,均购自天根生化科技(北京)有限公司;本发明中用到的特异性引物,以及特异性探针序列均由上海英骏生物技术有限公司合成,其中,特异性探针上连接的荧光基团和淬灭基团一并由上海英俊生物技术有限公司合成。实施例一试剂盒的准备(一)阳性标准品和阴性标准品的制备通过对大量临床结直肠癌患者以及正常人群的DNA序列进行比对分析,设计得到一条和结直肠癌疾病有关的序列,BMP3基因甲基化序列SEQIDNO.4,SEQIDNO.4序列如下:TTATTTCGTTGTATTCGGTCGCGTTTCGGGTTTCGTGCGTTTTCGTTTTAGTTGGTTTGG60AGTTTAATTTTCGGTTTCGTCGTCGGTTTTTTGCGTTTTCGGAGTGTTTCGTAGCGACGT120CGGGAGTCGACGCGTCGCGCGGGTATTTAGTTATGGTT158人工合成SEQIDNO.4序列,然后以SEQIDNO.4序列为模板,采用常规PCR技术,以结直肠癌细胞基因组甲基化处理后的DNA(SEQIDNO.4序列)为模板,扩增BMP3基因靶序列,PCR反应体系见表1。其中引物序列SEQIDNO.5为:5’-TTATTTCGTTGTATTCGGTCGCG-3’;引物序列SEQIDNO.6为:5’-AACCATAACTAAATACCCGCGCGA-3’,表1PCR反应体系表1中的缓冲液为pH8.0的Tris-HCl缓冲液。扩增结束后,将经过纯化的PCR产物连接到pGM-T质粒载体上,得到连接有目的基因的质粒;所述PCR产物的纯化体系如表2所示:表2PCR产物纯化体系组分体积(μL)PCR产物20SAP酶0.85(1U/μL)ExoI酶0.375(10U/μL)ddH2O3.775总体积25将PCR产物纯化体系放置于PCR扩增仪内进行反应,反应条件为37℃、20min,73℃、20min。然后将产物转化大肠杆菌TOP10感受态细胞,将构建的重组质粒经双向DNA测序鉴定,目的基因与质粒连接成功的重组质粒作为阳性标准品,提取质粒,紫外分光光度计定量,并将阳性标准品稀释到103拷贝每微升的浓度,保存于-20℃。将没有发生重组的pGM-T质粒稀释到103拷贝每微升的浓度作为阴性标准品。(二)反应液的制备根据BMP3基因的高甲基化序列SEQIDNO.4,设计特异性引物SEQIDNO.1和SEQIDNO.2和特异性探针SEQIDNO.3,其中,正向引物SEQIDNO.1为5’-GTTTAATTTTCGGTTTCGTCGTC-3’;反向引物SEQIDNO.2为5’-CTCCCGACGTCGCTACG-3’;特异性探针SEQIDNO.3为5’-TTTTTTGCGTTTTCGGAGTGTTTCG-3’,特异性探针上含有荧光报告基团FAM和荧光淬灭基团BHQ,FAM和BHQ分别连接在特异性探针序列SEQIDNO.3的5’和3’端。按照表3所示的配方,制备反应液,备用。表3反应液的配方反应液成分体积(μL)10*buffer2引物SEQIDNO.1(10μM)0.4引物SEQIDNO.2(10μM)0.4特异性探针SEQIDNO.3(10μM)0.4dNTPs(2.5mM)0.8水14总体积18其中,缓冲液(buffer)溶液的配方如下:Tris-HCl100mM、KCl500mM、MgCl225mM,其中Tris-HCl的pH值为8.5。(三)试剂盒的组成将以上制备得到的阳性标准品、阴性标准品、反应液和DNA聚合酶分别装在不同的ep管中,制备得到本实施例所述的试剂盒,其中,所述反应液中含有用于结直肠癌检测的特异性引物SEQIDNO.1和SEQIDNO.2以及特异性探针SEQIDNO.3。阳性标准品管和阴性标准品管的容量均为200μL,分别装有浓度为103copies/μL的阳性标准品和阴性标准品。反应液管的容积为500μL,管内的反应液总体积为380μL。DNA聚合酶管的容积为0.65mL,其装有TaqDNA聚合酶22μL,其浓度为0.5U/μL。实施例二试剂盒的使用利用实施例一制备得到的试剂盒检测样品的BMP3基因甲基化水平。(1)样本预处理从天津总医院获得临床结直肠癌患者或者潜在患者的粪便样本。将粪便样本(样本编号分别为样本3,样本4,样本5,样本6和样本7)按照粪便基因组DNA提取试剂盒(购自QIAGEN公司)上的操作说明提取粪便中的结直肠癌的DNA。然后再用QIAGEN的甲基化处理试剂盒(购自QIAGEN公司)处理上述提取到的基因组DNA,待用。(2)样本检测取新的反应管,分别命名为样品检测组、阳性对照组和阴性对照组,分别按照表4各实验组配方配制溶液,用移液枪吹打均匀,然后置于荧光定量PCR仪中进行测定。表4各实验组配方检测组样品检测组阳性对照组阴性对照组反应液18μL18μL18μL模板DNA1μL——阳性标准品—1μL—阴性标准品——1μLDNA聚合酶(0.5U/μL)1μL1μL1μL(3)反应程序探针SEQIDNO.3上的荧光报告基团FAM发出绿色荧光,当探针中的序列无法与待测溶液中的DNA模板配对时,探针保持完整,即同时含有荧光报告基团FAM和荧光淬灭基团BHQ,PCR扩增后无法检测到荧光;而当探针能够与待测溶液中的DNA发生碱基互补配对时,探针被TaqDNA聚合酶降解,探针5’的报告基团与3’的淬灭基团分离,PCR扩增过程中能够检测到荧光。探针序列SEQIDNO.3是以BMP3基因高甲基化后的DNA序列为模板设计的,若PCR扩增过程能检测到荧光则说明体系中存在BMP3基因高甲基化后的序列,结直肠癌检测结果很可能为阳性;若PCR扩增过程中无法检测到荧光,则结直肠检测结果可能为阴性;具体的结直肠癌检测结果判断还需要结合PCR扩增后的定量分析。打开参数窗口,设置程序为:95℃5分钟,1个循环;95℃15秒,53℃40秒,58℃40秒,共40个循环。设置完成后,保存文件,运行程序。(4)反应结果判断采用软件对荧光定量PCR结果进行分析,根据分析后图像调节基线参数的起始值、停止值以及阈值(用户可根据实际情况自行调整,起始值可以在1~10、停止值可以在5~20范围选择),使标准曲线窗口下的标准曲线图达到最佳。在定量分析菜单下分析结果,根据标本点在标准曲线的位置确定标本浓度。其中,如果增长曲线不呈S型曲线或Ct值>=36,则判断样品为阴性或样品的总含量小于检测极限。如果增长曲线呈S型曲线且Ct值<36,则样品的诊断结果为阳性。当荧光PCR仪程序运行完成后,在软件中选中阳性标准品和阴性标准品时其荧光曲线图应为图1所示。本次实验的临床样本荧光曲线图如图2所示。从图1可以看出,阴性标准品(编号2)为一条CT值为40的水平直线,阳性标准品为CT值小于36的S型曲线。图1所示结果同时表明,本发明的试剂盒工作正常。图2为临床样本的检测结果,从图2的检测结果可以看出,样品编号为5,6和7的样本,患了结直肠癌,样品编号为3和4的样本为阴性,没有患结直肠癌。以上所述仅为本发明较佳实施例,并不用于局限本发明,凡在本发明的精神和原则之内所做的修改、等同替换和改进等,均需要包含在发明的保护范围之内。SEQUENCELISTING<110>天津脉络生物科技有限公司<120>BMP3基因甲基化检测用试剂体系和试剂盒及其应用<130>OICN160091<160>6<170>PatentInversion3.3<210>1<211>23<212>DNA<213>人工序列<400>1gtttaattttcggtttcgtcgtc23<210>2<211>17<212>DNA<213>人工序列<400>2ctcccgacgtcgctacg17<210>3<211>25<212>DNA<213>人工序列<400>3ttttttgcgttttcggagtgtttcg25<210>4<211>158<212>DNA<213>人工序列<400>4ttatttcgttgtattcggtcgcgtttcgggtttcgtgcgttttcgttttagttggtttgg60agtttaattttcggtttcgtcgtcggttttttgcgttttcggagtgtttcgtagcgacgt120cgggagtcgacgcgtcgcgcgggtatttagttatggtt158<210>5<211>23<212>DNA<213>人工序列<400>5ttatttcgttgtattcggtcgcg23<210>6<211>24<212>DNA<213>人工序列<400>6aaccataactaaatacccgcgcga24当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1