基因表现图谱以及将其应用于乳癌医疗之方法与流程
本发明大体而言关于基因表现图谱以及将其应用于乳癌医疗之方法,尤其、但不仅限关于在乳房切除手术(mastectomy)和/或乳房保留手术(breast-conservingsurgery)后,根据一乳癌患者的基因表现图谱,来为该患者预估乳癌局部区域复发率(loco-regionalrecurrence)的一种方法。本发明尤其、但不限于提供一种方法,其有关在乳房切除手术和/或乳房保留手术后,测量至少一种与乳癌相关之基因的表现程度(expressionlevel),以及根据一预设模型演算得出一分数,来为一乳癌患者预估乳癌局部区域复发率和/或远端转移风险(distantmetastasisrisks)。该方法可于乳房切除手术和/或乳房保留手术后,帮助医疗人员决定乳癌患者所需之治疗类型。
背景技术:
:以下关于本发明背景的讨论,用意在于使本发明清楚易懂。然而,此处的讨论并未认可或承认任何其中所提资料在本申请案的优先日期时,在任何专利辖区范围内已出版、已为公知或已属一般常见知识的一部分。应用演算乳癌局部区域复发风险以判断患者是否需要接受放射性治疗(radiotherapy)的一种公知方法,根据的是已被发现与局部区域复发率息息相关的临床风险因子,例如肿瘤大小、腋下淋巴结的波及程度(involvementofaxillarylymphnodes)、雌激素受体(estrogenreceptor)、初诊年龄、淋巴血管侵犯(lymphovascularinvasion)等(参考文献1到2)。虽然某些研究报告已指出有个别基因与局部区域复发率相关,但截至目前为止,仍未有可靠的生物标记(biologicalmarkers)可用来预估乳癌的局部区域复发率(参考文献3到4)。在临床实践中,降低乳癌局部区域复发率的对策是为患者进行术后放射性治疗,而减少远端转移的对策则是为患者进行全身性的辅助性化学治疗(systemicadjuvantchemotherapy)和/或荷尔蒙治疗(hormonaltherapy)。一般认为,有4颗及4颗以上腋下淋巴结被波及的乳癌患者,应该接受乳房切除术后放射性治疗(post-mastectomyradiotherapy)(参考文献5)。至于有1到3颗阳性腋下淋巴结的患者,乳房切除术后放射性治疗在他们身上的效果,已经由三个大型随机对照实验的结果所证实,因此美国国家癌症资讯网(nccn)的指南,建议咨询医师「强力考虑」为这样的患者进行乳房切除术后放射性治疗(参考文献6到8)。然而,同样也有报告指出,淋巴结阴性患者的十年局部区域复发率小于5%,而患者有1到3颗阳性淋巴结的复发率大约20%,患者有4颗或4颗以上阳性淋巴结的复发率则为32%(参考文献9)。因此,根据临床参数,大约有70%到80%的淋巴结阳性患者有可能完全无术后局部区域复发之虞,也因此不会需要乳房切除术后放射性治疗,而有复发风险的患者,则有可能会得益于乳房切除术后放射性治疗。近来,将基因体分析(genomicanalysis)作为肿瘤生物学之有效评估工具的研究,有了进一步的发展,而这样的发展为风险分级技术(riskstratification)的改良开启了可能性,使医疗人员能为有1到3颗阳性淋巴结的乳癌患者做出更针对个别患者的预估(参考文献10)。例如,cheng,sh等人尝试应用无监督式分群(unsupervisedclustering)以及贝叶斯树模型(bayesiantreemodel)发展出不同的基因组,而且应用该些基因组来将n0与n1的乳癌患者区分成局部区域复发的高风险群以及低风险群,以演算出该些患者的三年局部区域可能复发率(参考文献11)。在另一方面,solin,lj等人报告了一种12基因表现检验法(12-geneexpressionassay),其可在广泛性局部切除手术(widelocalexcision)后,为乳腺管原位癌(ductalcarcinomainsitu,一种非侵袭性乳癌)患者预估局部区域复发率(参考文献12)。美国专利第8741605b2号发明案揭示了一种应用乳癌患者的基因表现标记(geneexpressionmarkers)进行评估的方法。该方法应用一基因序列(genesequence)做为序列辨识码编号162(seqidno.162)的前导体(precursor),将乳癌患者之cd68的rna转译程度与一乳癌样本之cd68的rna转译程度作定量比较(quantitativecomparisons),以供评估或预估该乳癌患者是否能在无远端复发(distalrecurrence)风险下长时间存活。此评估方法应用一cd68基因体预后诊断套组(genomicprognostickit)且参考患者基因的统计数据,以评估该患者的存活率。惟此方法赖以为据的基因过于多元,且由于因此取得的统计值大于1.01,所以其参数也过于多元。已公开之世界专利第2014/085653a1号发明案,揭露了一种应用复数基因来评估是否需以辅助性化学治疗介入治疗患者的方法。揭露之该评估方法应用一14基因组,其可帮助医疗人员判断一乳癌患者是否需要进一步的辅助性化学治疗,或是评估一乳癌患者是否有远端转移的风险。然而,该方法只针对已停经之乳癌女患者此一特定族群。在乳房切除手术和/或乳房保留手术后,很重要的是能辨识出患者是否有局部区域复发和/或远端转移的风险,因为此类风险的精准评估会立即影响到是否进行辅助性治疗的决定。风险分级技术的改良能为个别患者做出更精准的风险预估,辨识出不需要乳房切除术后放射性治疗、区域性淋巴放射治疗(regionalnodeirradiation)、化学治疗以及荷尔蒙治疗等复发和/或远端转移风险低的患者,有助于减少或避免过重或过度的治疗。避免初期乳癌过度治疗以及为个别患者安排适当治疗的关键,在于应用分子诊断技术(moleculardiagnostics)来判断癌细胞有无侵袭性(参考文献13与14)。虽然公知已有某些基因检测组合(genepanels)可如上所述般为乳癌患者预估局部区域复发率和/或远端转移率,但这些基因检测组合仅限用于特定的患者族群,也仅限用于特定的乳癌亚型。至于能为各种不同乳癌亚型、分期或治疗方案之乳癌患者评估局部区域复发和/或远端转移可能性的方法,目前则仍阙如。此外,应用公知基因体检测组合(genomicpanel)为非管状型(non-luminal)乳癌做风险分级的技术,至今也仍相当有限(参考文献15)。因此,目前仍须发展可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移风险的方法,以求至少在某种程度上克服前述的一些缺点。技术实现要素:除非特别点出,否则本说明书中例如「包括」、「由……组成」等用语,需被理解为非全面性,又或者为「包括、但不限于」。本发明的一第一面向,在于提供一种可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的方法,包括:i.从该乳癌患者取出一样本,测量其中至少一基因的表现程度;以及ii.根据测量所得之该至少一基因的表现程度,演算得出一分数;其中该至少一基因选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分(fragment)、一同源基因(homologue)、一变异基因(variant)或一衍生基因(derivative);以及其中演算得出之分数显示该乳癌患者局部区域复发和/或远端转移的可能性。在一较佳实施例中,根据测量所得之该至少一基因的表现程度,演算得出一分数的步骤,应用一预测性的分类模型来进行。在一较佳实施例中,该预测性分类模型包括至少一得分算式(scoringalgorithm)。在一较佳实施例中,该方法包括在演算得出的分数低于一第一预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移之一低风险群的一步骤。在一较佳实施例中,该方法包括在演算得出的分数等于或高于该第一预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移之一高风险群的一步骤。在一较佳实施例中,该方法包括在演算得出的分数低于一第二预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移之一低风险群的一步骤。在一较佳实施例中,该方法包括在演算得出的分数等于或高于一第三预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移之一高风险群的一步骤。在一较佳实施例中,该方法包括在演算得出的分数介于该第二预设参照值(含)以及该第三预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移之一中度风险群的一步骤。在一较佳实施例中,该至少一得分算式选自一组算式,该组算式包括:i.分数=trpv6+ddx39+bub1b+ccr1+stil+blm+c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+nfatc2ip+obsl1+mmp15;其中当风险比值(hazardratio)<1时,每一基因以1分计算,总分数为18分;ii.分数=trpv6+ddx39+bub1b+ccr1+stil+blm+2×c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+2×nfatc2ip+obsl1+2×mmp15;其中当风险比值<1时,若以单变量分析(univariateanalysis)验证该些基因,则每一基因以1分计算,若以多变量分析(multivariateanalysis)验证该些基因,则每一基因以2分计算,所以总分数为21分;iii.分数=3×trpv6+5×ddx39+18×bub1b+4×ccr1+4×stil+7×blm+7×c16orf7+4×pim1+9×tpx2+8×pti1+3×tcf3+7×ccnb1+2×dtx2+2×ensa+5×rchy1+6×nfatc2ip+2×obsl1+6×mmp15;其中该些基因以单变量分析验证,而每一基因的分数根据其加权值(weighting)重新调整(re-scale),所以总分数为102分;iv.分数=2×trpv6+2×ddx39+2×bub1b+ccr1+stil+2×blm+5×c16orf7+3×pim1+3×tpx2+5×pti1+tcf3+ccnb1+dtx2+2×ensa+3×rchy1+4×nfatc2ip+obsl1+mmp15;其中该些基因以多变量分析验证,而每一基因的胜算比(oddsratio)重新调整为一介于1到5之间的分数,当胜算比<1时,每一基因以1分计算,所以总分数为40分;以及v.分数=4×trpv6+3×ddx39+8×bub1b+ccr1+stil+3×blm+11×c16orf7+4×pim1+tpx2+2×pti1+2×tcf3+ccnb1+dtx2+2×ensa+5×rchy1+4×nfatc2ip+obsl1+2mmp15;其中该些基因以多变量分析验证,而每一基因的胜算比重新调整为一介于1到11之间的分数,当胜算比<1时,每一基因以1分计算,所以总分数为56分。在一较佳实施例中,测量该至少一基因之表现程度的步骤,包括使该至少一基因与至少一基因探针(geneprobe)杂交,且测量该至少一基因的表现程度。在一较佳实施例中,该至少一基因探针包括选自一组基因的至少一基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因。在一较佳实施例中,该至少一基因探针固定在一微阵列晶片(microarraychip)上。在一较佳实施例中,应用一微阵列或定量逆转录聚合酶连锁反应(quantitativereversetranscriptionpolymerasechainreaction)来测量基因的表现程度。在一较佳实施例中,该第一预设参照值为31分。在一较佳实施例中,该第二预设参照值为21分。在一较佳实施例中,该第三预设参照值为44分。在一较佳实施例中,该患者有下列情形之一:无阳性淋巴结、1到3颗阳性淋巴结、以及3颗以上阳性淋巴结。本发明的一第二面向,在于提供可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的一套组,包括:i.可特别与患者身上取得之一样本中的至少一基因结合的至少一试剂(reagent),用以定量该至少一基因的表现程度;以及ii.一预测性的分类模型,其包括至少一得分算式,用以根据该至少一基因的表现程度演算得出一分数;其中该至少一基因选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因;以及其中演算得出之分数显示该乳癌患者局部区域复发和/或远端转移的可能性。在一较佳实施例中,当演算得出的分数低于一第一预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一低风险群。在一较佳实施例中,当演算得出的分数等于或高于该第一预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一高风险群。在一较佳实施例中,当演算得出的分数低于一第二预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一低风险群。在一较佳实施例中,当演算得出的分数等于或高于一第三预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一高风险群。在一较佳实施例中,当演算得出的分数介于该第二预设参照值(含)以及该第三预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一中度风险群。在一较佳实施例中,该至少一得分算式选自一组算式,该组算式包括:i.分数=trpv6+ddx39+bub1b+ccr1+stil+blm+c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+nfatc2ip+obsl1+mmp15;其中当风险比值<1时,每一基因以1分计算,总分数为18分;ii.分数=trpv6+ddx39+bub1b+ccr1+stil+blm+2×c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+2×nfatc2ip+obsl1+2×mmp15;其中当风险比值<1时,若以单变量分析验证该些基因,则每一基因以1分计算,若以多变量分析验证该些基因,则每一基因以2分计算,所以总分数为21分;iii.分数=3×trpv6+5×ddx39+18×bub1b+4×ccr1+4×stil+7×blm+7×c16orf7+4×pim1+9×tpx2+8×pti1+3×tcf3+7×ccnb1+2×dtx2+2×ensa+5×rchy1+6×nfatc2ip+2×obsl1+6×mmp15;其中该些基因以单变量分析验证,而每一基因的分数根据其加权值重新调整,所以总分数为102分;iv.分数=2×trpv6+2×ddx39+2×bub1b+ccr1+stil+2×blm+5×c16orf7+3×pim1+3×tpx2+5×pti1+tcf3+ccnb1+dtx2+2×ensa+3×rchy1+4×nfatc2ip+obsl1+mmp15;其中该些基因以多变量分析验证,而每一基因的胜算比重新调整为一介于1到5之间的分数,当胜算比<1时,每一基因以1分计算,所以总分数为40分;以及v.分数=4×trpv6+3×ddx39+8×bub1b+ccr1+stil+3×blm+11×c16orf7+4×pim1+tpx2+2×pti1+2×tcf3+ccnb1+dtx2+2×ensa+5×rchy1+4×nfatc2ip+obsl1+2mmp15;其中该些基因以多变量分析验证,而每一基因的胜算比重新调整为一介于1到11之间的分数,当胜算比<1时,每一基因以1分计算,所以总分数为56分。在一较佳实施例中,该第一预设参照值为31分。在一较佳实施例中,该第二预设参照值为21分。在一较佳实施例中,该第三预设参照值为44分。在一较佳实施例中,该患者有下列情形之一:无阳性淋巴结、1到3颗阳性淋巴结、以及3颗以上阳性淋巴结。本发明的一第三面向,在于提供可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的一微阵列,包括至少一基因探针,用来测量选自一组基因之至少一基因的表现程度,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因。在一较佳实施例中,估算出的局部区域复发和/或远端转移可能性,于乳房切除手术和/或乳房保留手术后,用来依照本发明之第一面向为患者预估或决定辅助性治疗的方案。在一较佳实施例中,估算出的局部区域复发和/或远端转移可能性,于乳房切除手术和/或乳房保留手术后,用来依照本发明之第二面向为患者预估或决定辅助性治疗的方案。在一较佳实施例中,估算出的局部区域复发和/或远端转移可能性,于乳房切除手术和/或乳房保留手术后,用来依照本发明之第三面向为患者预估或决定辅助性治疗的方案。本发明的一第四面向,在于提供可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的一方法,包括:i.从该乳癌患者取出一样本,测量其中复数基因的表现程度;以及ii.根据测量所得之该些复数基因的表现程度,演算得出一分数;其中该些复数基因选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因;以及其中演算得出之分数显示该乳癌患者局部区域复发和/或远端转移的可能性。本发明的一第五面向,在于提供可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的一套组,包括:i.可特别与患者身上取得之一样本中的复数基因结合的至少一试剂,用以定量该些复数基因的表现程度;以及ii.一预测性的分类模型,其包括至少一得分算式,用以根据该些复数基因的表现程度演算得出一分数;其中该些复数基因选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因;以及其中演算得出之分数显示该乳癌患者局部区域复发和/或远端转移的可能性。本发明的其他面向如下:本发明的另一面向,有关在乳房切除手术和/或乳房保留手术后,利用检测包含以下基因之一基因组的表现程度,以预估乳癌患者的局部区域复发率及其对放射性治疗之反应的一种方法,该基因组包括的基因如下:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15。该方法包括:(1)在乳房切除手术和/或乳房保留手术后,从取自患者之一检体中萃取基因(mrna);(2)使萃取所得之基因与基因探针中的基因杂交;(3)该些基因的每一个基因探针选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15;(4)测量从检体萃取所得之基因的表现程度;以及(5)应用一18基因分类法(18-geneclassifier)(预测性的分类模式)以及计算比例风险(proportionalhazards)的分析算式(analysisalgorithms),进行乳癌局部区域复发率的评估。在某些实施例中,本发明的方法包括:在乳房切除手术及/或乳房保留手术后,从患者身上取得一肿瘤组织样本;从该样本中萃取总rna;使该总rna与一基因微阵列接触,该基因微阵列由trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15所组成的一基因组;测量该基因组中一或所有基因的表现程度;并应用18基因分数计算风险比值。在某些实施例中,当18基因分类法应用一算式得出的分数≧31时,即将该患者归类于乳癌局部区域复发的高风险群。当该分数<31时,则将该患者归类于乳癌局部区域复发的低风险群。本发明进一步提供在乳房切除手术和/或乳房保留手术后,用来评估乳癌患者的局部区域复发风险及其对放射性治疗之反应的一种预估或判断方法,该方法包括:(1)在乳房切除手术和/或乳房保留手术后,从取自患者之一检体中萃取基因(mrna);(2)使萃取所得之基因与基因探针中的基因杂交;(3)该些基因的每一个基因探针选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15;(4)测量从该检体萃取所得之基因的表现程度;以及(5)应用一18基因分类法以及计算比例风险的分析算式,进行乳癌局部区域复发率的评估。该方法进一步包括在患者被归类于乳癌局部区域复发的高风险群时,帮助医疗人员评估是否该以放射性治疗介入治疗该患者,以此来避免乳癌的局部区域复发。本发明提供包括18个基因的一基因晶片。当该等18基因中4个(rchy1、pti1、ensa及obsl1)之任何一个的表现程度提高时,局部区域复发风险降低。当该等18基因中另外14个(blm、tcf3、pim1、ddx39、bub1b、stil、tpx2、ccnb1、mmp15、ccr1、nfatc2ip、trpv6、c16orf7及dtx2)之任何一个的表现程度提高时,则局部区域复发风险增加。本发明的另一目的在于将患者分类,其中当该分类法应用一算式得出的分数≧31时,即将该患者归类于乳癌局部区域复发的高风险群,而当该分数<31时,则将该患者归类于乳癌局部区域复发的低风险群。本发明的另一目的在于将患者分类,其中当该分类法应用一算式得出的分数≧31时,即将该患者归类于乳癌局部区域复发以及远端转移的高风险群。本发明的另一目的在于,当患者被归类于乳癌局部区域复发的高风险群时,帮助医疗人员评估是否该以放射性治疗介入治疗该患者,以此来避免乳癌的局部区域复发。本发明的另一目的在于提供固定在一微阵列晶片上的基因探针。在本发明的评估方法中,基因表现程度的测量包括以定量的聚合酶连锁反应(qpcr)或称逆转录聚合酶连锁反应(rt‐pcr)来测量。本发明的评估方法,应用18基因分类法以及计算比例风险的分析算式分析基因表现程度,以评估乳癌的局部区域复发率,其中该计算比例风险的分析算式包括分析用的算式。本发明有关用来评估乳癌局部区域复发率的医疗用品,其运用一方法以及读数器材来评估乳癌局部区域复发率。本发明进一步提供用来评估乳癌局部区域复发率的一基因探针组,包括:(1)选自一组基因的任何一基因,该组基因包括trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15;(2)使该等基因与萃取自乳癌患者的基因杂交,以测量患者基因的表现程度。该乳癌患者的基因应用一18基因分类法以及计算比例风险的分析算式进行分析,以评估该患者的乳癌局部区域复发率。本发明也提供一种应用前述基因探针组,来预估乳癌患者的局部区域复发及其对放射性治疗之反应的一种方法,用以评估癌症的局部区域复发率。本发明进一步提供一种应用前述基因探针组,来评估癌症局部区域复发率的评估方法,其中当18基因分类法应用一算式得出的分数≧31时,即将该患者归类于乳癌局部区域复发的高风险群。借此可提供精准的评估讯息给相关医疗人员,减少医疗费用、健保给付或保险资源的负担与浪费。本发明进一步提供一种应用前述基因探针组,以及18基因分类法应用的一算式,来精准预测癌症患者器官或淋巴组织远端转移风险的方法。在一较佳实施例中,该样本检体为取自一乳癌肿瘤的一肿瘤组织,且最好是一乳癌肿瘤主要组织。该组织以本
技术领域:
之一公知方法进行分析。本发明的另一面向,是在乳房切除手术后,应用判断一患者组织(例如乳房肿瘤、其他乳房组织、淋巴结肿瘤和/或组织及血液)中一基因组的表现程度,并调整该患者组织与乳癌局部区域复发率的相关性,以评估乳癌患者的局部区域复发风险。研究发现,与乳癌局部区域复发率高度相关的基因组包括trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15。基因表现程度可应用任何本
技术领域:
公知之方法进行测量(例如定量聚合酶链锁反应,或称逆转录聚合酶链锁反应),或应用未来可能设计出的、可提供关于基因表现之定量资讯的一定量方法。在某些实施例中,基因表现图谱藉由基因表现的产物来进行定量测定,例如蛋白质、多胜肽或核酸(nucleicacid)分子(如mrna、trna、rrna)。核酸可应用核酸直接定量或藉由规则的基因序列定量。此外,基因片段或多型性基因片段也可被定量。在一较佳实施例中,从一乳癌患者取得一检体或样本,测量其中的基因表现程度,以完成定量。此定量测定可应用本
技术领域:
之一公知方法来执行。在另一实施例中,检体样本中mrna的杂交程度,由固定在一基因组微阵列上的基因探针进行测量,该基因组微阵列具有一特定适当的核酸。制造寡核苷酸微阵列的方法已揭露于世界专利第95/11995号发明案。也可应用其他本
技术领域:
之公知方法。基因表现图谱可应用任何便捷的方法从检体中的原始核酸样本产生。亦即,基因表现图谱可应用任何公知方法取得,例如已应用于本
技术领域:
的差异性基因表现(differentialgeneexpression)分析法。一具代表性且便捷的基因表现图谱应用微阵列来产生。本发明的评估方法于乳房保留手术后,应用一基因微阵列来评估取自患者、与乳癌局部区域复发率相关的基因,该等基因包括有下列基因组成的一基因组:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15。根据一序列的一讯号产生系统,将一初始备制之检体中的标靶核酸予以标记。在备妥该检体样本的标靶核酸后,使该标靶核酸的样本与一基因阵列杂交。已标记之核酸的杂交复合物(hybridizedcomplex),其具有的基因序列,与探针阵列表面上之基因的基因序列互补。该杂交复合物以定性或定量方法检测。基因表现程度应用一装置进行数值化评估(numericallyassessed)或测量。该等数值是由该装置取得的原始数值(rawvalues),必要时可加以调整、筛选和/或标准化(normalized)该等数值。该等资料取自例如一基因晶片、rtm、探针阵列或微阵列(昂飞公司﹝affymetrix﹞取得的美国专利第5,631,734、5,874,219、5,861,242、5,858,659、5,856,174、5,843,655、5,837,832、5,834,758、5,770,722、5,770,456、5,733,729以及5,556,752号,这些专利的整体技术在此全部并入本发明作为参考)。基因体表现程度应用软体计算(如昂飞公司的基因晶片软体)。在严格条件下,使取自一检体的核酸(如mrna)与一特定微阵列(一般也称为dna晶片或生物晶片)的一探针杂交。在某些实施例中,探针套组固定在一微阵列上。在一较佳实施例中,该微阵列为u133plus2.0阵列。进一步检验取自该检体的基因表现程度原始资料,且应用该比例风险模型计算18基因分数。在本发明的一实施例中,该18基因分数应用有下列方程式的算式计算:分数=trpv6+ddx39+bub1b+ccr1+stil+blm+c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+nfatc2ip+obsl1+mmp15;其中当风险比值<1时,每一基因以1分计算,总分数为18分。在另一实施例中,该18基因分数应用有下列方程式的算式计算:分数=trpv6+ddx39+bub1b+ccr1+stil+blm+2×c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+2×nfatc2ip+obsl1+2×mmp15;其中当风险比值<1时,若以单变量分析验证该些基因,则每一基因以1分计算,若以多变量分析验证该些基因,则每一基因以2分计算,所以总分数为21分。在另一实施例中,该18基因分数于一单变量cox回归分析模型(univariatecoxregressionmodel)中,应用有下列方程式的算式计算:分数=3×trpv6+5×ddx39+18×bub1b+4×ccr1+4×stil+7×blm+7×c16orf7+4×pim1+9×tpx2+8×pti1+3×tcf3+7×ccnb1+2×dtx2+2×ensa+5×rchy1+6×nfatc2ip+2×obsl1+6×mmp15;其中每一基因的分数根据其加权值重新调整,所以总分数为102分。在另一实施例中,该18基因分数于一多变量cox回归分析模型中,应用有下列方程式的算式计算:分数=2×trpv6+2×ddx39+2×bub1b+ccr1+stil+2×blm+5×c16orf7+3×pim1+3×tpx2+5×pti1+tcf3+ccnb1+dtx2+2×ensa+3×rchy1+4×nfatc2ip+obsl1+mmp15;其中每一基因的胜算比重新调整为一介于1到5之间的分数,当胜算比<1时,每一基因以1分计算,所以总分数为40分。在另一实施例中,该18基因分数于一多变量cox回归分析模型中,应用有下列方程式的算式计算:分数=4×trpv6+3×ddx39+8×bub1b+ccr1+stil+3×blm+11×c16orf7+4×pim1+tpx2+2×pti1+2×tcf3+ccnb1+dtx2+2×ensa+5×rchy1+4×nfatc2ip+obsl1+2mmp15;其中每一基因的胜算比重新调整为一介于1到11之间的分数,当胜算比<1时,每一基因以1分计算,所以总分数为56分。本发明的另一面向,是提供在乳房切除手术后,用以评估乳癌局部区域复发率的一微阵列,该基因组包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15。本发明的另一面向,是提供在乳房切除手术和/或乳房保留手术后,用以评估乳癌局部区域复发率的一微阵列,该基因组包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15。本发明的另一面向,是提供用于上述评估方法的一基因组。在某些实施例中,该基因组包括一试剂,用以于乳房切除手术和/或乳房保留手术后,检测取自乳癌患者之一检体的基因表现,其中该试剂具有一基因组中的任一或多个基因,该基因组包括下列被检测的特定基因:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1以及mmp15。接着参照下列关于本发明之各个实施例的图示进一步详细说明。在阅读下列说明后,本
技术领域:
之一般技艺者将清楚明白本发明的其他面向与优点。附图说明以下将仅就示范性的实施例,并参照下列附图,进一步说明本发明:图1a显示根据本发明的一实施例,用来评估乳癌局部区域复发率以及远端转移风险之一评估方法的一流程图。图1b显示18基因分数<31以及≧31之患者的五年局部区域复发控制机率。图2显示根据本发明的一实施例,一18基因分类法模型的一接收者操作特征(receiveroperatingcharacteristic)曲线。图3显示乳癌保留手术后,患者的五年局部区域复发控制机率(其中有94%的患者有接受辅助性的放射性治疗)。图4显示病人筛选与外在效度(externalvalidation)的一流程图。图5显示经由18基因分类法分类之低、中度、与高风险患者的无远端转移机率(distantmetastasis-freeprobability):(a)所有患者(n=818),(b)第一期患者(n=218),(c)第二期患者(n=411),(d)第三期患者(n=184),(e)次族群分析,(f)不同乳癌亚型(la:管状a型﹝luminalalike﹞;lb:管状b型﹝luminalblike﹞;lh:管状her2型﹝luminalher2﹞;tnbc:三重阴性乳癌﹝triplenegativebreastcancer﹞)之低(分数<21)、中度(分数介于21到43之间)、与高风险(分数≧44)患者的比例。图6显示每一乳癌亚型的风险比值森林图,以18基因分数(作为连续变项)预测(a):远端复发率,(b)死亡率,(c)局部/区域复发率,(d)任何复发率。图7(a)显示未接受乳房切除术后放射性治疗之n0到n1患者(n=114),五年内局部区域复发的累积发生率。分数为31分的患者,估算的局部区域复发率是5.3%。图7(b)显示最佳临界点是31分,乳房切除术后放射性治疗将局部区域复发率从14.9%降到1.6%(p=0.099),将任何复发率从34.7%降到8.4%(p=0.015)。图8显示根据18基因分数所揭示的、复发及无复发病人的不同基因表现图谱,在135名患者身上进行的一18基因无监督式分群分析,以及监督式分群。有局部区域复发的患者以蓝色表示,有局部区域复发以及远端转移的患者以紫色表示,有远端转移的患者以红色表示,而无任何疾病的患者则以黄色表示。具体实施方式本发明的其他特征与优点将在以下实施例中进一步说明与叙述。此说明书所叙述的实施例仅用于说明本发明,而非限制本发明。除非另行定义,否则此处所用的技术与科学用语,意义与本
技术领域:
之一般技艺人士普遍所理解的相同。此外,除非另行定义,否则单数用语也包含复数意义,而复数用语也包含单数意义。大体而言,在此说明书中使用的、与分子生物学、蛋白质、寡核苷酸或多核苷酸化学与杂交技术相关等学术用语,皆为本领域公知与普遍应用的术语。本发明不限于所述之特定检测方法、检测试剂和检测装置,因为这些检测方法和试剂可在适度修改或变更后达到相同结果与目的。此处所使用的科学术语仅用来做具体描述,而不是要限制本发明的范围或领域。此外,除非上下文中有所限定,否则单数用语也包含复数意义,而复数用语也包含单数意义。除非特别点出,否则本说明书使用的下列术语,应理解为有下列意义:本说明书使用的「和/或」一词,需理解为特定揭露该两个特定特征或元件之中的每一个,无论同时有或没有另一个。例如,「a和/或b」需理解为特定揭露(1)a、(2)b、以及(3)a与b这三者之中的每一个,正如同好像这三者之中的每一个都在此处个别说明一样。本说明书使用的「侵袭性乳癌」一词,指称一种从乳小叶膜或乳腺管膜(membraneofthelobuleorduct)扩散到乳房组织中的癌症,之后癌细胞可能继续扩散进入到腋下或其他部位的淋巴结。当身体其他部位发现乳癌细胞时,称为「转移性乳癌」。本说明书使用的「局部区域复发」一词与乳癌相关时,指称患者于乳房切除手术和/或乳房保留手术治疗后,该疾病在患者乳房的局部和/或区域复发,这些乳房的局部和/或区域包括乳房、胸壁、腋窝、锁骨、锁骨上或胸骨旁淋巴结区域。本说明书使用的「远端转移」一词,指称在乳房切除手术和/或乳房保留手术后,已经从原发性肿瘤扩散到身体的一或多个部位、器官、或远端淋巴结(未被包括在前段所述之「局部区域复发」一词中的淋巴结)的乳癌。「多变量统计学」一词指称一种统计学类型,包含同时观察及分析一个以上的结果变项(outcomevariable)。多变量统计学的应用称为「多变量分析」。本说明书使用的「比例风险模型」一词,指称统计学中的一种存活模型,其中当存活资料进一步包括共变数(covariates)与风险因子时,这些资料可用来推估这些共变数对存活时间的影响,也可用来预测在一段特定时间内的存活机会。cox比例风险模型由考克斯(davidcox)爵士于1972年提出,是存活分析中最常用的一种回归分析模型。此方法常被称为cox模型或是比例风险模型。本说明书使用的核酸「杂交」一词,指称将核酸两互补股(如rna、dna或寡核苷酸)结合的一过程。在某些实施例中,核酸分子与所对应的基因感应股(sensestrands),同时或依序被验证,又或者核酸分子与所对应的感应股互补。典型来说,核酸分子是在严格条件下与该等感应股杂交,呈现其对应程度。本说明书使用的「微阵列」一词,指称一大群聚集与固定在一坚固表面上的微小dna点。每一个dna点都包含一微微克(picomole)的一特定dna序列,称为一探针。这些探针可以是在高严格条件下与检体(称为标靶)样本中一cdna或crna(亦称为反义rna)杂交之一基因或一dna的一短小片段。本说明书使用的「严格」一词,指称序列错配(mismatchedsequence)的核酸分子之间可能产生杂交的程度。高严格条件要求该等分子间有绝对的互补性,而低严格条件则是在有某些错配碱基(mismatchedbases)时仍允许杂交。典型而言,高严格条件的达成藉由降低氯化钠(nacl)的浓度,抑或将温度提高到接近参与分子的熔点温度(tm)。一个高严格条件的例子,是在50℃或更高的温度(如55℃),以及0.1ssc(0.15m的氯化钠以及0.015m的柠檬酸钠﹝sodiumcitrate﹞)的浓度下进行杂交。本说明书使用的「复数基因」一词,指称两个或两个以上的基因。本说明书使用的「dmfp」缩写字,指称无远端转移的机率(probabilityoffreedomfromdistantmetastasis)。在本说明书中,远端转移的定义是经由切片检查证实或临床诊断为复发的侵袭性乳癌。本说明书使用的「her2」缩写字,指称人类表皮生长因子受体第二型(humanepidermalgrowthfactorreceptortype2)。本说明书使用的「lrcp」缩写字,指称局部/区域控制机率(local/regionalcontrolprobability),无局部区域复发的机率。本说明书使用的「lvi」缩写字,指称淋巴血管侵犯。本说明书使用的「os」缩写字,指称总存活率(overallsurvival),其包含任何原因的死亡,包括乳癌、非乳癌、或不明原因。本说明书使用的「pmrt」缩写字,指称乳房切除术后放射性治疗(post-mastectomyradiotherapy)。本说明书使用的「rfp」缩写字,指称无复发的机率(relapse-freeprobability)。在本说明书中,复发的定义是任何局部区域复发以及/或远端转移。当一核酸或核酸片段与另一核酸(或其互补股)理想匹配(藉由适当的核酸插入或删除)时,如果在至少大约60%、通常是至少大约70%、更通常是至少大约80%、最好是至少大约90%的核苷酸碱基中,存在相同的核苷酸序列时,则该核酸或核酸片段与另一核酸或核酸片段「基本上同源」(「或基本上相似」)。又或者,当一核酸或核酸片段在选择性的杂交条件下,会与另一核酸(或该核酸的一互补股)的一股、或其互补股杂交时,即存在基本上同源或(相同)。当出现比完全欠缺明确性(totallackofspecificity)还要显著更具选择性的杂交时,则存在杂交的选择性(selectivity)。典型而言,当一片至少大约14个核苷酸有至少大约55%、较好是有至少大约65%、更好是有至少大约75%、且最好是有至少大约90%的相同性时,会发生选择性杂交。如上所述,同源比较(homologycomparison)可在更长的片段中进行,且在某些实施例中,通常会是至少大约9个核苷酸、通常是至少大约20个核苷酸、更常是至少大约24个核苷酸、典型是至少大约28个核苷酸、更典型是至少大约32个核苷酸、且更好是至少大约36个或更多核苷酸的片段。因此,本发明的多核苷酸与下文列表1或序列列表中所示的序列之间,较好是有至少75%、更好是有至少85%、再更好是有至少90%的同源性。更好是有至少95%、再更好是有至少98%的同源性。可依下列所述,对多胜肽进行核苷酸同源比较。一较佳序列比较程式,是下列所述的gcg威斯康辛最佳匹配程式(gcgwisconsinbestfitprogram)。在预设的得分矩阵(scoringmatrix)中,每一个相同的核苷酸有10分的匹配值(matchvalue),而每一个错配的核苷酸则有-9分的匹配值。就每一个核苷酸而言,创造空位(gapcreation)的预设罚分是-50分,而延伸空位断裂(gapextension)的预设罚分则是-3分。在本发明的脉络中,一同源物或同源序列包括的一核苷酸序列,与下文序列列表或列表1中所示的核苷酸序列之间,在至少20、50、100、200、300、500或1000个核苷酸中,至少有60%、70%、80%或90%、更好是至少有95%或98%,在氨基酸层(attheaminoacidlevel)是相同的。特别是,在该序列中与同源比较相关的区域,典型应该是那些编码已知是蛋白质功能所不可或缺之相邻氨基酸序列、而不是非必要之相邻序列的区域。本发明之多胜肽所包括的一较佳相邻序列,与该等序列中所示之一或多个核苷酸序列,有高于50%、60%或70%的同源性、一更佳相邻序列则有高于80%、90%或97%的同源性。较佳多核苷酸可选择改为或可进一步包括的一相邻序列,与下文序列列表或列表1中所示、编码含对应氨基酸序列之多胜肽的序列之间,有高于80%、95%或97%的同源性。其他较佳多核苷酸包括的一相邻序列,与所示的、编码含对应氨基酸序列之多胜肽的序列,有高于40%、50%、60%或70%的同源性,一更佳相邻序列则有高于80%、90%、95%或97%的同源性。核苷酸序列的长度,较好是至少15个核苷酸,更好是至少20、30、40、50、100或200个核苷酸。一般而言,多核苷酸的长度越短,达到选择性杂交所需的同源性就越高。因此,当本发明的多核苷酸由少于大约30个核苷酸组成时,与下文序列列表或列表1中所示的核苷酸序列比较后,较好有高于75%、更好有高于90%或95%的相同性。反之,当本发明的多核苷酸由例如多于50或100个核苷酸组成时,与下文序列列表或列表1中所示的核苷酸序列比较后,可以有较低的相同比例,例如高于50%、更佳的是高于60%或75%。本发明之「多核苷酸」的组成,如本领域之一般技艺人士会立即理解的,包括rna、cdna、基因体dna、合成形式(syntheticforms)、以及混和聚合物(mixedpolymers)、感应股与反义股(antisensestrand)、也可以是化学或生物化学改造过、或可包含非天然或衍生的核苷酸碱基。这些改造包括例如标记、甲基化(methylation)、将一或多个天然产生的核苷酸替换成一类似物(analog)、核苷酸间改造(internucleotidemodifications)例如不带电荷的链结(unchargedlinkages)(例如methylphosphonates、phosphotriesters、phosphoamidates、carbamates等)以及带电荷的链结(例如phosphorothioates、phosphorodithioates等)、悬垂成分(pendentmoieties)(例如多胜肽)、嵌入(例如acridine、psoralen等)、钳合(chelators)、烷化(alkylators)、以及改造链结(例如alphaanomericnucleicacids等)。同样也包括在内的,还有模拟多核苷酸透过氢键(hydrogenbonding)及其他化学反应与一指定序列结合之能力的合成分子(syntheticmolecule)。这些分子为本领域已公知,包括例如那些在其分子骨架中由多肽链结(peptidelinkages)替换磷酸链结(phosphatelinkages)的分子。「多胜肽」一词指称一氨基酸聚合物,以及其相等物,并非指称该产物的一特定长度。因此,多肽、寡肽(oligopeptides)以及蛋白质都包含在多胜肽的定义中。此一用词也非指称、或排除多胜肽的改造物,例如糖基化物(glycosylations)、乙醯化物(acetylations)、磷酸化物(phosphorylations)等。包含在此定义中的,有例如包含一或多个氨基酸类似物的多胜肽(包括例如天然氨基酸等)、有替换链结的多胜肽、以及其他本领域公知的改造物,无论是天然或非天然产生的。在本发明的脉络中,一同源序列包括的一氨基酸序列,与下文序列列表或列表1中所示、编码含对应氨基酸序列之多胜肽的序列之间,在至少20、50、100、200、300或400个氨基酸中,至少有60%、70%、80%或90%、较好是至少有95%或98%,在氨基酸层是相同的。特别是,与同源性比较相关的,典型应该是那些已知是蛋白质功能所不可或缺之序列的区域,而不是非必要的相邻序列。本发明的多胜肽包括的一较佳相邻序列,与一或多个对应氨基酸,有高于50%、60%或70%的同源性、一更佳相邻序列则有高于80%或90%的同源性。其他较佳多胜肽包括的一相邻序列,与下文序列列表或列表1中所示、编码含对应氨基酸序列之多胜肽的序列之间,具有高于40%、50%、60%或70%的同源性。虽然同源性也可从相似度来考量(例如有类似化学特性/功能的氨基酸残基﹝residue﹞),在本发明的脉络中,较好是以序列相同性来表示同源性。当指称多胜肽时,「基本上同源」或「基本上相同」两用语,表示的是谈论中的多胜肽或蛋白质,展现与一整个天然产生或其一部分的蛋白质之间,有至少大约70%、通常至少大约80%、及较好至少大约90%或95%的相同性。同源比较可以肉眼进行,或更通常的是应用容易取得的序列比较程式进行。这些市场上可取得的电脑程式可计算两个或更多序列之间的同源性。同源性比例的计算可横跨相邻序列,亦即,将一序列与另一序列匹配(align),然后直接将一序列的每一氨基酸与另一序列的对应氨基酸进行比较,一次只进行一残基的比较,称为一「无空位」比对(“ungapped”alignment)。典型而言,这样的无空位比对只横跨相对数量较少的残基(例如少于50个相邻氨基酸)。虽然这是一个非常简单且一致的方法,但其并未考量到的是,例如在其他方面相同的一组序列中,一个插入或删除都会导致接下来的氨基酸残基失去匹配度,因此,在进行全局比对(globalalignment)时,该方法有可能大幅降低同源性比例。因此,大部分序列比较方法的设计,都希望达到最佳比对,能既考虑到可能的插入或删除,又同时不过度低估整体的同源性分数。而此一目标的达成,可透过在序列比对中插入「空位」的方式,以尝试将局部同源性最大化。然而,这些较复杂的方法会指定「空位罚分」给每一个在比对中产生的空位,使得在同样数量的相同氨基酸下,空位极少化的一序列比对(反映两相比序列之间有较高的相关性),会比空位很多的一序列比对取得较高分数。典型应用的是「空位延伸罚分模型」(affinegapcosts),给予一空位的存在相对较高的罚分,而给予空位后的每一个残基较低罚分。这是最常被应用的空位罚分系统。高的空位罚分当然会产生有较少空位的最佳化比对。大部分的比对程式允许修改空位罚分。然而,在应用这样的软体来做序列比较时,较好是使用预设值。例如当应用gcg威斯康辛最佳匹配程式(参见下方说明)时,氨基酸序列的预设空位罚分是每一空位-12分,每一空位延伸-4分。最高同源性比例的计算因此首先需要产生一最佳化比对,并将空位罚分考虑进去。执行这种比对的一适当电脑程式是gcg威斯康辛最佳匹配程式(美国威斯康辛大学;devereux等人,1984,核酸研究,第12期,第387页)。其他可执行序列比较之软体的例子包括、但不限于blast套装软体(参见ausubel等人,1999,出处同上,第18章)、fasta(atschul等人,1990,分子生物学期刊,第403到410页)、以及geneworks比较工具套组。blast与fasta都可离线及线上搜寻(参见ausubel等人,1999,出处同上,第7~58到7~60)。不过,较好还是应用gcg威斯康辛最佳匹配程式。虽然最后的同源性比例可根据相同性来测量,但比对过程本身典型并非根据非全有即全无式的配对比较。相反的,通常会应用的是一种有比例的相似性得分矩阵(scaledsimilarityscorematrix),根据化学相似性或演化距离(evolutionarydistances),给予每一个配对比较分数。这类矩阵被普遍应用的一个例子是blosum62矩阵——blast套装程式的预设矩阵。gcg威斯康辛程式通常应用公用预设值,或是一客制化的符号比较表,如果有提供的话(进一步细节请参见使用者手册)。较好是使用blast套装软体的公用预设值,或是若应用其他软体时,则较好是使用预设矩阵,例如blosum62。当软体产生了一最佳化比对后,便可能计算出同源性比例,较好是序列相同性比例。软体计算典型是将其做为序列比较的一部分来进行,并产生一数值结果。一多胜肽「片段」、「部分」、或「区段」是指一片至少大约5到7个、通常至少大约7到9个、典型至少大约9到13个、最好至少大约20到30个或更多相邻氨基酸的氨基酸残基。本发明的较佳多胜肽与下文序列列表或表1中所示的序列,有基本上类似的功能。本发明之较佳多核苷酸编码的多胜肽,与下文序列列表或表1中所示的序列有基本上类似的功能。「基本上类似的功能」指一核酸的功能,或与下文序列列表或表1中所示、编码含对应氨基酸序列之序列的多胜肽类似物、变异物、衍生物、或片段之功能。如本
技术领域:
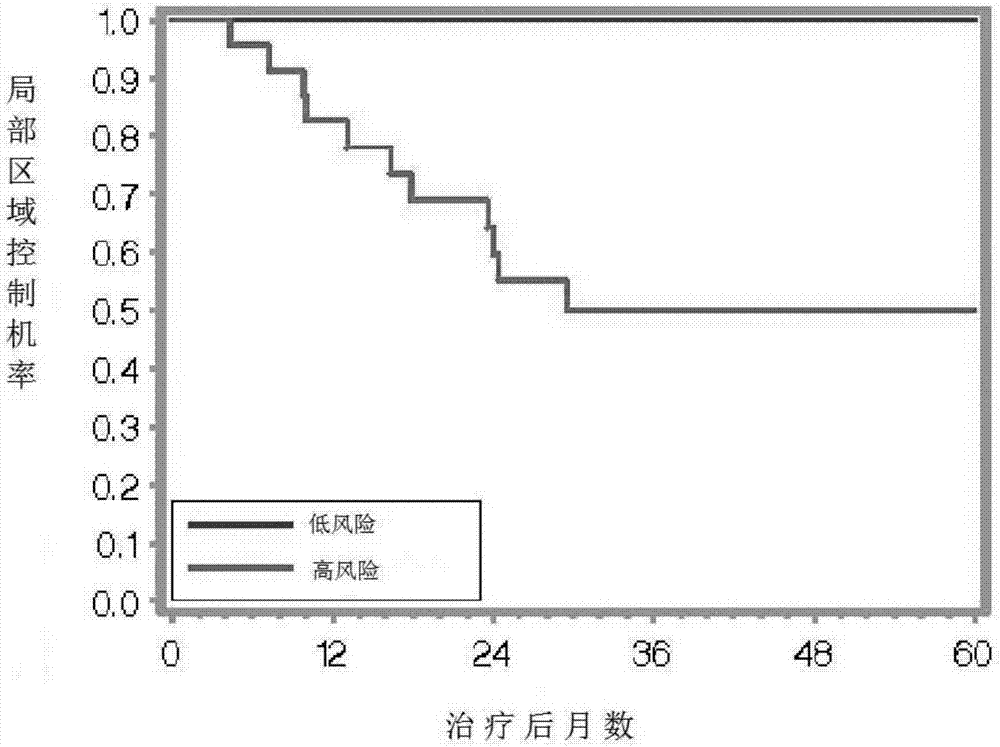
一般技艺人士会立即理解的,除了盐基组成、互补股长度、以及杂交核酸之间核苷酸碱基错配的数量之外,盐浓度、温度、或有机溶剂等条件也会影响核酸杂交。严格的温度条件典型一般会超过30℃、典型是超过37℃、较好是超过45℃的温度。严格的盐条件通常会低于1000mm、典型是低于500mm、较好是低于200mm。然而,参数的组合比任何单一参数的测量要更加重要。严格杂交条件的一个例子是65℃及0.1×ssc(1×ssc=0.15m氯化钠,0.015m柠檬酸钠,ph7.0)。本发明的其他特征与优点将在以下的实施例中进一步说明与叙述。此说明书所叙述的实施例仅用于说明本发明,而非限制本发明。图1a显示根据本发明的一实施例,用来评估乳癌局部区域复发率以及远端转移风险之一评估方法的一流程图。本发明的一实施例,描述一种可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的方法,包括:从该乳癌患者取出一样本,测量其中至少一基因的表现程度;以及根据测量所得之该至少一基因的表现程度,演算得出一分数;其中该至少一基因选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因;以及其中演算得出之分数显示该乳癌患者局部区域复发和/或远端转移的可能性。选自上述18基因组的该至少一基因包括(1)一多核苷酸,其包含以下所示之任一序列中的一核苷酸序列:序列辨识码编号1、序列辨识码编号2、序列辨识码编号3、序列辨识码编号4、序列辨识码编号5、序列辨识码编号6、序列辨识码编号7、序列辨识码编号8、序列辨识码编号9、序列辨识码编号10、序列辨识码编号11、序列辨识码编号12、序列辨识码编号13、序列辨识码编号14、序列辨识码编号15、序列辨识码编号16、序列辨识码编号17、序列辨识码编号18、或前述序列的一片段、同源物、变异物或衍生物;(2)一多核苷酸,其包含(1)中所示之任一序列中、编码含对应氨基酸序列之多胜肽的一核苷酸序列;或(3)一多核苷酸,其包含可与(1)及(2)中之任一序列、或其中任一序列之互补物,进行选择性杂交的一核苷酸序列。包括至少一得分演算法的一预测性分类模型,其用来执行的步骤是,根据测量所得之该至少一基因的表现程度,演算得出一分数。在演算得出的分数低于一第一预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一低风险群。在演算得出的分数等于或高于该第一预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一高风险群。在演算得出的分数低于一第二预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一低风险群。在演算得出的分数等于或高于一第三预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一高风险群。在演算得出的分数介于该第二预设参照值(含)以及该第三预设参照值时,将该乳癌患者归类于局部区域复发和/或远端转移的一中度风险群。在一较佳实施例中,该第一预设参照值为31分,该第二预设参照值为21分,该第三预设参照值为44分。本发明的另一实施例,描述可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的一套组,包括可特别与患者身上取得之一样本中的至少一基因结合的至少一试剂,用以定量该至少一基因的表现程度;以及一预测性的分类模型,其包括至少一得分算式,用以根据该至少一基因的表现程度演算得出一分数,其中该至少一基因选自一组基因,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因;以及其中演算得出之分数显示该乳癌患者局部区域复发和/或远端转移的可能性。选自上述18基因组的该至少一基因包括(1)一多核苷酸,其包含以下所示之任一序列中的一核苷酸序列:序列辨识码编号1、序列辨识码编号2、序列辨识码编号3、序列辨识码编号4、序列辨识码编号5、序列辨识码编号6、序列辨识码编号7、序列辨识码编号8、序列辨识码编号9、序列辨识码编号10、序列辨识码编号11、序列辨识码编号12、序列辨识码编号13、序列辨识码编号14、序列辨识码编号15、序列辨识码编号16、序列辨识码编号17、序列辨识码编号18、或前述序列的一片段、同源物、变异物或衍生物;(2)一多核苷酸,其包含(1)中所示之任一序列中、编码含对应氨基酸序列之多胜肽的一核苷酸序列;或(3)一多核苷酸,其包含可与(1)及(2)中之任一序列、或其中任一序列之互补物,进行选择性杂交的一核苷酸序列。本发明的另一实施例,描述可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估局部区域复发和/或远端转移可能性的一微阵列,包括至少一基因探针,用来测量选自一组基因之至少一基因的表现程度,该组基因包括:trpv6、ddx39、bub1b、ccr1、stil、blm、c16orf7、tpx2、pti1、tcf3、ccnb1、dtx2、pim1、ensa、rchy1、nfatc2ip、obsl1、mmp15、以及上述基因的一部分、一同源基因、一变异基因或一衍生基因。选自上述18基因组的该至少一基因包括(1)一多核苷酸,其包含以下所示之任一序列中的一核苷酸序列:序列辨识码编号1、序列辨识码编号2、序列辨识码编号3、序列辨识码编号4、序列辨识码编号5、序列辨识码编号6、序列辨识码编号7、序列辨识码编号8、序列辨识码编号9、序列辨识码编号10、序列辨识码编号11、序列辨识码编号12、序列辨识码编号13、序列辨识码编号14、序列辨识码编号15、序列辨识码编号16、序列辨识码编号17、序列辨识码编号18、或前述序列的一片段、同源物、变异物或衍生物;(2)一多核苷酸,其包含(1)中所示之任一序列中、编码含对应氨基酸序列之多胜肽的一核苷酸序列;或(3)一多核苷酸,其包含可与(1)及(2)中之任一序列、或其中任一序列之互补物,进行选择性杂交的一核苷酸序列。一个令人意外的优点是,在乳房切除手术和/或乳房保留手术后,可应用任何数量之上述实施例中所提的18基因,且以任何组合方式,来为乳癌患者预估局部区域复发和/或远端转移可能性。还有另一个优点的则是,预估的局部区域复发和/或远端转移可能性,可在乳房切除手术和/或乳房保留手术后,用来为乳癌患者预估或决定辅助性治疗的类型。实施例实施例1基因微阵列分析,用以在乳房切除手术与乳房保留手术后,验证与术后局部区域复发率相关的基因表现图谱:在一项肿瘤基因医学研究里,最终挑选了侵袭性乳癌的患者,以发展新的乳癌分类法。该项研究挑选了总计217位侵袭性乳癌的患者,他们分别在2005年与2012年之间接受过乳房切除手术或乳房保留手术,而且有组织检体可供制作dna(或基因)微阵列。在217名患者中,有130名患者接受过乳房切除手术,87名患者接受过乳房保留手术。所有217名患者皆同意让其原发肿瘤组织接受dna(或基因)微阵列的研究。符合本研究资格的患者在至少两年追踪期内,不可接受乳房切除术后放射性治疗(n=130)。接受过乳房保留手术(n=87)的患者另外单独分析,以检视基因表现图谱在预测局部区域复发率的成效表现。参与本研究的患者,于乳房切除手术或乳房保留手术后的临床特征,显示于下方表1中。根据这些临床特征,大多数患者属于t2或以上分期(56%,73/130),且有93%(121/130)的患者有n0与n1的乳癌。所有患者于乳房切除手术或乳房保留手术后,皆未接受放射性治疗。表1:乳房切除手术与乳房保留手术患者的术后临床特征此217名患者的冷冻组织样本,于治疗之前(乳房切除手术或乳房保留手术之前)取自从患者身上取得之原发肿瘤的外科检体(surgicalspecimens)。总rna以抽提试剂trizol(加州卡尔斯巴市的莱富生命科技制造﹝invitrogen,carlsbad,ca﹞)自肿瘤组织萃取而得,以总rna纯化试药组(rneasyminikit)(加州瓦伦西亚市的凯杰公司﹝qiagen,valencia,ca﹞)纯化,并以一安捷伦2100生物分析仪器(agilent2100bioanalyzer)进行定性评估。杂交标靶根据昂飞协定(affymetrixprotocol),从总rna制备,并与u133plus2.0阵列杂交。经过cox比例风险模型的单变量分析后,发现在130名乳房切除手术患者中,有18个基因与局部区域复发率显著相关。与这18基因之功能相关的基因,是参与致癌过程(oncogenicprocess)、细胞增生(proliferation)、侵袭、发炎、细胞间交互作用(cell-cellinteraction)、细胞凋亡(apoptosis)和代谢的基因。在这些与局部区域复发率显著相关的基因当中,blm、tcf3、pim1、rchy1和pti1涉及致癌过程;ddx39、bub1b、stil、tpx2和ccnb1涉及细胞增生;mmp15与侵袭有关;ccr1和nfatc21p涉及发炎;trpv6和dtx2与细胞凋亡有关;而ensa则与代谢相关(参见下方表2)。请同时参考列出一22探针组中之18基因的表3。表2:与局部区域复发率相关之18基因个别涉及的过程或途径表3:一22探針組中的18個基因——其最佳臨界點实施例2经统计分析验证之局部区域复发率基因表现图谱本发明之新平台(platform)中的34个基因,分布在一84基因探针组中,其中有4个功能未明的基因无法辨识。经由单变量分析发现,剩下之30个基因中的18个,可根据局部区域复发率,将乳房切除手术患者归类于一低风险群与一高风险群。经由多变量分析发现,可将患者归类于一低风险群与一高风险群。该18基因被用来将乳房保留手术患者归类于一低风险群与一高风险群。18基因分数≧31的患者被定义为高风险,而分数<31的患者则被定义为低风险。根据该18基因(18基因检测组合或分类法)演算得分的算式表4显示应用该比例风险模型,来根据该18基因的每一个,演算得出或计算出分数的单变量分析与多变量分析。当风险比值<1时,每一个基因在多变量分析中以1分计算。表4:应用比例风险模型的单变量分析与多变量分析参数单风险比值多风险比值pr>卡方trpv62.7692.480.1604ddx395.4012.1230.3525bub1b17.7833.2910.4061ccr13.5850.9410.9378stil3.9651.2150.8093blm7.1601.9990.4305c16orf77.0274.8910.0494tpx28.5803.1410.5113pti18.3493.7450.0853tcf33.1251.3840.5892ccnb16.6590.3230.5195dtx22.2330.8850.8258pim15.6650.6140.5861ensa1.9001.9240.254rchy15.2393.480.0406nfatc2ip5.4923.5060.0797obsl12.3001.4030.5516mmp156.0721.3770.6519以下是根据该18基因检测组合演算分数的四个范例算式:算式1:每个基因以1分计算,总共有18个基因,总分为18分。分数=trpv6+ddx39+bub1b+ccr1+stil+blm+c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+nfatc2ip+obsl1+mmp15算式2:当风险比值<1时,若以单变量分析验证该些基因,则每一基因以1分计算,若以多变量分析验证该些基因,则每一基因以2分计算,所以总分数为21分。分数=trpv6+ddx39+bub1b+ccr1+stil+blm+2×c16orf7+tpx2+pti1+tcf3+ccnb1+dtx2+pim1+ensa+rchy1+2×nfatc2ip+obsl1+2×mmp15算式3:根据单变量分析的单变量胜算比计算出18基因分数。每一基因的分数根据其加权值重新调整,所以总分数为102分。分数=3×trpv6+5×ddx39+18×bub1b+4×ccr1+4×stil+7×blm+7×c16orf7+4×pim1+9×tpx2+8×pti1+3×tcf3+7×ccnb1+2×dtx2+2×ensa+5×rchy1+6×nfatc2ip+2×obsl1+6×mmp15算式4:根据多变量分析的胜算比计算出18基因分数。根据胜算比,将每一基因的分数重新调整为一介于1到5之间的分数;当胜算比<1时,每一基因以1分计算,所以总分数为40分。分数=2×trpv6+2×ddx39+2×bub1b+ccr1+stil+2×blm+5×c16orf7+3×pim1+3×tpx2+5×pti1+tcf3+ccnb1+dtx2+2×ensa+3×rchy1+4×nfatc2ip+obsl1+mmp15结果由于临床决策需要冷静保守,因而可能倾向于过度治疗患者。以之为基准,则接收者操作特征曲线上的最佳临界点(或预设参照值)是31分。这些预测的总体准确度是87%,估计灵敏度(真阳性率)为91%,特异度(specificity,真阴性率)为87%。18基因分数≧31与<31的患者,其五年局部区域复发控制机率分别是50%与100%(p<0.0001)(参见图1b)。在总体诊断中,淋巴结状态是非常重要的一个因素,其可用来判断一原发性肿瘤是否已经以「远端转移」的方式扩散。其可藉由计算用来做评估,且可为后续处理提供参考。根据淋巴结状态,在n0与n1分期的患者中,18基因分数≧31与<31的患者,其五年局部区域复发控制机率在统计数字上不同(50%对比100%,p<0.0001)。n2患者的数量太少不足以下定论,但是该18基因检测组合的预测能力与n0~n1患者类似。经由18基因分类法(或预测性分类模型)定义为高风险的患者,不论有无淋巴结转移,其五年无转移的存活率和总存活率极低。进一步的细节与资料提供于上方表4。表5:根据乳房切除手术患者的淋巴结状态,应用该18基因检测组合,将之归类于不同风险程度的次族群如表5所示,根据该18基因检测组合制作的图谱,主要针对n0和n1的乳房切除手术患者。在本研究中,n0患者的局部区域复发率大约为5%;我们的基因分类法(18基因检测组合)证实,有9%的n0患者具有高风险,而这些患者当中有50%会有癌症复发。相对的,n1患者的局部区域复发率大约为20%;我们的基因分类法(18基因检测组合)证实,约有38%的n1患者具有高风险,而这些患者当中有50%会有癌症复发。至于n2患者,由于我们的样本数过少,不足以下定论,然而,其预测精确度也相类似;有55%的n2患者会被归类于高风险群。在乳房切除手术与乳房保留手术的患者中,18基因分类法的成效表现皆有相当确定的一致性。这强而有力的表示,18基因分类法可预估乳癌患者是否有局部区域复发的风险。实施例3乳房切除手术患者的cox比例风险模型根据现行的临床实务,用来评估n1乳癌患者是否需要辅助性放射性治疗的方法,会替其中的80%安排辅助性放射性治疗。然而,放射性治疗可为这些患者降低局部区域复发率,并可改善总存活率。cox比例风险模型已被广泛用来描述存活率与相关变项。因此,本研究检视的是,该(18基因检测组合)分类法是否为一独立的预后因子。传统的比例风险分析已确立了与比例风险及定量评估相关的临床参数,包括与局部区域复发率相关的淋巴结转移程度与雌激素受体状态。我们应用了临床参数与该分类法的分类系统,充分分析取自130名(乳房切除手术)患者之检体的比例风险。本研究证实,这些传统临床变项与该(18基因检测组合)分类法的结合,可以是预估局部区域复发率的一个重要独立因子。该(18基因检测组合)分类法与比例风险分析的应用,显示当一患者的18基因分数≧31(参见表6)时,其局部区域复发率的风险比值为67.8(95%信赖区间,8.3~552.5)。本研究再次肯定,应用一新颖的基因表现图谱及评估模式,可以将n0和n1患者归类于更加具同质性的次族群。表6:所有乳房切除手术患者的cox比例风险模型实施例4应用该(18基因检测组合)分类法,为乳房保留手术患者评估局部区域复发率应用微阵列资讯为87名乳房保留手术患者做分析;其中有94%的患者(82/87)已被安排术后放射线治疗(参见表1)。这些患者的临床特征,略微不同于已接受辅助性治疗的t1乳房切除手术患者。单变量与多变量分析证实,该(18基因检测组合)分类法可在乳房保留手术的术后辅助性化学治疗后,验证患者是否有局部区域复发的高风险。该(18基因检测组合)分类法为没接受辅助性化学治疗的患者,改良了预后风险评估的成效表现。多变量分析显示,18基因分数≧31以及显著的淋巴血管侵犯,是局部区域复发率的独立风险因子。未接受辅助性化学治疗的乳房保留手术患者,有40%的局部区域复发率风险,而经由(18基因检测组合)分类法验证归类于一低风险群的患者,则只有3%的局部区域复发率(参见表7与图3)。若经由(18基因检测组合)分类法验证归类于一低风险群时,未接受辅助性化学治疗的患者,不会有局部区域复发。表7:使乳房保留手术患者与局部区域复发率产生关系的因子最后,在本发明中应用的(18基因检测组合)分类法,可验证具有局部区域复发高风险的乳房切除手术与乳房保留手术患者。在本发明中,该(18基因检测组合)分类法可在乳房切除手术与乳房保留手术后,验证高风险患者是否需要放射性治疗的介入。实施例5为不同亚型、分期或治疗方案的患者预估远端转移可能性资料与方法本研究挑选了总共818名乳癌患者,他们的乳癌可开刀治疗,且他们已接受过主要手术,其原发肿瘤组织有应用微阵列制作的基因表现图谱。这些患者是临床i到iii期的乳癌患者,他们分别在2005年到2012年之间,于和信治癌中心医院(koofoundationsunyat-sencancercenter)接受主要手术。患者筛选的流程显示于图4。本研究中的合适患者必须符合下列的纳入标准(inclusioncriteria):(1)有侵袭性乳癌恶性肿瘤的妇女;(2)治疗前属临床i到iii期;(3)接受过改良型乳房切除手术(modifiedmastectomy)或全乳房切除手术(totalmastectomy),并做过前哨淋巴结切片(sentinellymphnodebiopsy);(4)有冷冻的新鲜组织;以及(5)签署过知情同意书。应用u133plus2.0阵列的微阵列研究在2005年到2014年间,于任何系统性治疗之前,从患者身上取得原发性肿瘤的外科检体,总数共有818份的冷冻组织样本。杂交标靶从总rna制备,且根据昂飞协定,与u133plus2.0阵列杂交。18基因与得分算式该18基因检测组合或分类法包括下列基因:blm、tcf3、pim1、rchy1、pti1、ddx39、bub1b、stil、tpx2、ccnb1、mmp15、ccr1、nfatc2ip、trpv6、obsl1、c16orf7、dtx2(notch)以及ensa。18基因分数的计算根据多变量分析的胜算比。每一基因的分数根据该胜算比重新调整为介于1与11之间的一个分数;当胜算比<1时,每一基因以1分计算,所以总分数为56分。其得分算式如下:18基因分数=4×trpv6+3×ddx39+8×bub1b+ccr1+stil+3×blm+11×c16orf7+4×pim1+tpx2+2×pti1+2×tcf3+ccnb1+dtx2+2×ensa+5×rchy1+4×nfatc2ip+obsl1+2mmp15;总分数为56分。18基因分数<21的患者,被定义为远端转移的低风险患者,分数介于21与43之间的患者,被定义为远端转移的中度风险患者,而分数≧44的患者,则被定义为远端转移的高风险患者。统计方法cox比例风险回归分析模型用来评估下列风险因子的预后重要性:初诊年龄、原发性肿瘤大小、腋下淋巴结被波及的数量、组织学分级(histologicalgrade)、细胞核分化程度、淋巴血管侵犯、雌激素受体/黄体激素受体状态、her2过度表现以及18基因分数。局部区域控制的期间,从治疗的第一天开始计算,直到胸壁或区域腋下淋巴结复发(nodalrecurrence),或最后一次追踪为止。局部/区域控制机率依照kaplan-meier方法计算。应用对数等级检定(log-ranktest)来评估患者次族群之间,在局部/区域控制机率、无复发机率、无远端转移机率以及总存活率等方面之差异的统计显著性(statisticalsignificance)。结果患者所有818名患者的基线特征(baselinecharacteristics)都可见于下方表8。无转移患者的追踪间隔中位数(medianfollow-upinterval)是56.4(0~159.4)个月。有转移患者(仅含存活患者)的追踪间隔是61.4(18.0~168.2)个月。最普遍的年龄是介于40到60岁之间。原发性肿瘤通常大于2cm(n=484,59.2%)。n0乳癌最为普遍(n=392,47.9%),n1乳癌(n=248,30.3%)次之。大部分患者是雌激素受体阳性或黄体激素受体阳性(n=537,65.6%)以及her2阴性(n=512,62.6%)。显著淋巴血管侵犯出现在24.3%的患者中(n=199)。肿瘤等级iii(n=461,56.4%)最为普遍,等级ii(n=267,32.6%)次之。关于乳癌亚型(参见图6),有32.5%(n=266)的患者属管状a亚型,12.6%(n=103)的患者属管状b亚型,20.5%(n=168)的患者属管状her2亚型,16.9%(n=138)的患者属her2亚型,而17.5%(n=143)的患者则属三重阴性亚型。接受辅助性化学治疗的有87.7%(n=717)的患者,接受辅助性荷尔蒙治疗的有62.1%(n=508),而接受辅助性放射性治疗的则有69.1%(n=565)。如下方表1所示,与远端转移显著相关的风险因子包括较高的肿瘤分期、较晚的淋巴分期、荷尔蒙受体阴性以及显著的淋巴血管侵犯。18基因分类法根据18基因得分算式,21.9%(n=179)的患者被归类于低风险群(分数<21),57.5%(n=470)被归类于中度风险群(分数介于21到43之间),而20.7%(n=169)则被归类于高风险群(分数≧44)。低风险群、中度风险群以及高风险群的远端转移率,分别是2.2%、14.3%以及32%(p<0.0001,参见表1)。应用cox比例风险回归模型,针对远端转移相关因子进行的单变量与多变量分析,可见于下方表9。应用cox比例风险回归模型进行的远端转移单变量分析,显示基因分数≧21的患者,有8.9的风险比值(3.3~24.2)(参见表9)。在多变量分析中,该风险比值为5.7(2.0~15.9)。其他独立的远端转移相关因子包括t分期(t3vs.t1,hr3.8,95%信赖区间,1.8~8.1)以及n分期(n3vs.n0,hr5.9,95%信赖区间,3.3~10.7)。没有任一种辅助性治疗(荷尔蒙治疗、放射性治疗以及化学治疗)增加了远端转移的风险,荷尔蒙治疗的风险比值是2.3(1.1,4.9),化学治疗的风险比值是2.1(1.1,3.9),放射性治疗的风险比值则是1.8(1.1,3.0)(参见表9)。18基因分类法在不同分期、亚型以及次族群中的成效表现依图5a显示,低风险群、中度风险群以及高风险群的五年无远端转移机率分别是96.6%、85.0%以及59.6%。经由18基因分类法分析为低风险群的比例,在分期i、ii以及iii中分别是36.2%(79/218)、19.9%(82/411)以及9.7%(18/184)(图5)。在分数<21的患者(低风险群)中,分期i、ii以及iii的五年无远端转移机率分别是100%、94.5%以及90.9%。在高风险群(分数≧44)中,对应的五年无远端转移机率分别是79.3%、68.0%以及40.6%。依图5e显示,在管状a型、管状b型、管状her2型、her2型以及三重阴性亚型中,低风险患者的比例分别是43.2%(115/266)、8.7%(9/103)、15.5%(26/168)、9.4%(13/138)以及11.2%(16/143)。如图5e所示,在管状a型、管状b型、管状her2型、her2型以及三重阴性亚型中,低风险群的五年无远端转移机率分别是97.5%、100%、90%、92.3%以及100%。对应的五年无复发机率分别为98.8%、100%、100%、100%以及90%。在高风险群中,对应的五年无远端转移机率分别是54.5%、54.2%、68.1%、47.9%以及69.2%。管状亚型的平均18基因分数(26.8)低于her2亚型(35.6)与三重阴性亚型(36.7)的平均18基因分数。图7以18基因分数做为一连续变项,说明18基因分类法是与远端复发、局部区域复发、任何复发以及总存活率相关的一独立预后因子。此一观察所得全面性见于不同的年龄族群(<40、40~60以及>60)、分期(t3与t4除外)、亚型(雌激素受体、黄体激素受体以及her2状态)以及治疗方案(化学治疗、放射性治疗以及荷尔蒙治疗)。风险比值大约是1.06到1.14。分数每增加一分,则复发风险增加1.06到1.14。在本发明的另一实施例中,有与没有局部区域复发和/或远端转移之患者的基因表现图谱,以一树状图来表示(参见图8)。以一无监督式分群分析18基因,以及根据该18基因分数进行135名患者的监督式分群后,揭露了有与没有复发之患者的明显差异基因表现图谱。有局部区域复发的患者以蓝色表示,有局部区域复发以及远端转移的患者以紫色表示,有远端转移的患者以红色表示,而无任何疾病的患者则以黄色表示,如图8热图(heatmap)最下方所示。讨论18基因分类法为一多功能的基因检测组合,其可为无论任何癌症亚型、分期、外科手术类型或辅助性治疗,做远端转移的预估。低风险群、中度风险群以及高风险群的五年无远端转移机率分别是96.6%、85.0%以及59.6%。经过其他临床与病理学变项调整的18基因分类法,是远端转移的一独立预后因子,其风险比值为5.7(95%信赖区间,2.0~15.9)(参见表9)。树状图证实,18基因分类法与不同次族群中的局部区域复发、远处转移、任何复发与死亡率之间显著相关(图5a到5d)。以18基因分数做为一连续变项,每增加1分,则远端转移的风险比值是1.08(95%信赖区间,1.06~1.1)、局部复发的风险比值是1.09(1.06~1.13)、任何复发的风险比值是1.08(1.06~1.09)、而死亡率的风险比值则是1.09(1.06~1.13)。18基因分类法有能力同时做为远处转移及局部区域复发的一预后生物标记。本研究族群的818名患者,筛选自含有8,155名患者的一原始群组,这表示他们是从一独立癌症中心随机筛选的一乳癌患者族群,且该癌症中心治疗了台湾大约十分之一的乳癌患者(参考文献16及17)。不同于其他针对一特定亚型及乳癌分期的多基因检测组合试验,本研究指出,18基因分类法可以是一种通用的多基因检测组合,可为全体乳癌患者提供关于远端转移的好坏预后价值。本研究族群中的远端转移率高于一原始族群,这是因为有死亡率或复发的患者会最先被加入到研究中(图4)。然而,此一族群的研究结果,与下列几项普遍共识一致:(1)较高的t与n分期增加远端转移的可能性;(2)辅助性治疗减少远端转移的可能性;(3)相较于管状型乳癌,三重阴性亚型有较高的18基因分数以及复发率,比较有侵犯性。18基因分类法可揭露总共22%、五年远端转移率低于4%的低风险乳癌患者。18基因分类法有三个独特特征。首先,它是第一个以亚洲为本、在大数量的一般乳癌患者中获得证实的基因体检测组合。其次,它似乎可为非管状型乳癌进行复发风险分级。其三,它可同时预估局部区域复发以及远端转移的可能性。过去15年来的一个共识是,初期乳癌是有不同分子亚型及预后的一种异质性疾病(参考文献13、18及19)。正如上述关于背景的段落所言,截至目前为止已为初期乳癌发展出好几个多基因检测组合(参考文献15)。据宣称,对于晚期远端转移的预估,后续发展的多基因检测组合(安欣娜﹝prosigna﹞、endopredict以及乳癌指数﹝breastcancerindex﹞)比前期发展的多基因检测组合(安可待﹝oncotypedx﹞、欣扶妳﹝mammaprint﹞以及基因体分级指标﹝genomicgradeindex﹞)成效表现较好(参考文献20及21)。这几个多基因检测组合主要聚焦在管状型(雌激素受体阳性/her阴性)以及淋巴结阳性的乳癌,因此可能导致医疗人员忽略为亚型中的低风险群安排化学治疗。然而,以现有的检测组合仍无法为非管状型乳癌患者做复发风险分级。例如,70与76基因检测组合对雌激素受体阳性患者的预后风险评估极具鉴别度,但只有低于5%的雌激素受体阴性患者被归类于低风险群(参考文献13及14)。此外也有报告指出,21基因检测组合对于her2亚型患者的评估,有相对高(>50%)的伪阴性率(参考文献22)。这可能是因为第一代基因体检测组合主要凭借细胞增生相关基因的量化,来判断雌激素受体阳性疾病的预后(参考文献23)。因此,这些研究使多基因检测组合的临床效用局限在其他乳癌亚型的评估上。好几项研究已显示,与免疫反应(immuneresponse)及基质侵犯(stromalinvasion)相关的基因表现图谱,对于雌激素受体阴性与高增生的雌激素受体阳性乳癌,有预后价值(参考文献24到27)。然而,被第二代基因体检测组合归类为低风险群的患者,仍有高达20%的五年复发率。本18基因分类法的18个基因,与细胞增生、致癌过程、侵袭、发炎、细胞间交互作用、细胞凋亡和代谢相关的基因。在本研究中,18基因分类法将12.7%的her2阳性与11.2%的三重阴性乳癌患者,分别归类于五年远端转移率8%及0%的低风险群。此一出人意表的结果提供了为非管状型乳癌做复发风险分级的可能性。若果真如此,则将可能为此疾病亚型减少或免除化学治疗的剂量。其他已知资讯是,18基因分类法归类为高风险群的患者,无论接受何种治疗、何种剂量密集(dose-dense)的化学治疗或何种新的临床试验,他们的五年无远端转移机率都只有40%到60%。此外,乳癌的种族差异性是另一个议题(参考文献28)。相较于非西语白种人及非裔美人,亚洲女性在某些方面有较高存活率,这可能导致西方基因体检测组合高估亚洲族裔的风险(参考文献29)。本发明的18基因分类法也能在高风险群患者中,辨识出那些能得益于剂量密集化学治疗以及高剂量放射性治疗的患者。低风险群患者的五年远端转移率只有2.2%(4/179)。从先前研究可知,辅助性化学治疗可降低30%到50%的复发风险。假定可能性为最高,例如50%,则低风险群患者不接受化学治疗的原始远端转移率可在大约4.4%。增加不到3%,因此可将剩余其他95%的低风险群患者排除在化学治疗的毒性作用外。综合考量下,18基因分类法是一种可同时预估局部区域复发以及远端转移的通用检测组合。表8:所有818名患者的基线特征*应用双样本平均数差异t检定(two-samplet-test)来检定该两群组的平均追踪期**有6名患者的her2状态根据分子表现程度重新分类。表9:应用cox比例风险回归模型,进行远端转移相关因子的单变量与多变量分析列表1:18基因分类法的18个基因中,每一个基因的基因编码序列1.trpv6:瞬态感受器电位阳离子通道(transientreceptorpotentialcationchannel)子类v成员6﹝人类﹞,国家生物技术资讯中心参考序列:nm_014274.3(序列辨识码编号1)2.ddx39:死亡盒螺旋酶39a(dead-boxhelicase39a)﹝人类﹞(序列辨识码编号2)3.bub1b:bub1丝分裂关卡丝胺酸/羟丁氨酸激酶b(bub1mitoticcheckpointserine/threoninekinaseb)﹝人类﹞(序列辨识码编号3)4.ccr1:cc主题趋化因子受体1(c-cmotifchemokinereceptor1)﹝人类﹞国家生物技术资讯中心参考序列:nm_001295.2(序列辨识码编号4)5.stil:scl/tal1阻断基因座(interruptinglocus)﹝人类﹞国家生物技术资讯中心参考序列:nm_003035.2(序列辨识码编号5)6.blm:布卢姆综合症类recq螺旋酶(bloomsyndromerecqlikehelicase)﹝人类﹞国家生物技术资讯中心参考序列:nm_000057.3(序列辨识码编号6)7.c16orf7(旧名):vps9结构域包含1(vps9domaincontaining1)﹝人类﹞国家生物技术资讯中心参考序列:nm_004913.2(序列辨识码编号7)8.tpx2:tpx2,微管核因子(microtubulenucleationfactor)﹝人类﹞国家生物技术资讯中心参考序列:nm_012112.4(序列辨识码编号8)9.pti1(又名eef1a1):真核翻译延伸因子1阿尔法1(eukaryotictranslationelongationfactor1alpha1)﹝人类﹞国家生物技术资讯中心参考序列:nm_001402.5(序列辨识码编号9)10.tcf3:转录因子3(transcriptionfactor3)﹝人类﹞国家生物技术资讯中心参考序列:nm_003200.3(序列辨识码编号10)11.ccnb1:周期素b1(cyclinb1)﹝人类﹞国家生物技术资讯中心参考序列:nm_031966.3(序列辨识码编号11)12.dtx2:deltex2,e3泛素化连接酶(ubiquitinligase)﹝人类﹞国家生物技术资讯中心参考序列:nm_020892.2(序列辨识码编号12)13.pim1:pim-1原致癌基因(proto-oncogene),丝胺酸/羟丁氨酸激酶﹝人类﹞国家生物技术资讯中心参考序列:nm_002648.3(序列辨识码编号13)14.ensa:内磺肽阿尔法(endosulfinealpha)﹝人类﹞国家生物技术资讯中心参考序列:nm_207042.1(序列辨识码编号14)15.rchy1:环指与chy锌指结构域包含1(ringfingerandchyzincfingerdomaincontaining1)﹝人类﹞国家生物技术资讯中心参考序列:nm_015436.3(序列辨识码编号15)16.nfatc2ip:活化t细胞核因子交互作用蛋白(nuclearfactorofactivatedt-cells2interactingprotein)﹝人类﹞国家生物技术资讯中心参考序列:nm_032815.3(序列辨识码编号16)17.obsl1:类obscurin1(obscurin-like1)﹝人类﹞国家生物技术资讯中心参考序列:nm_015311.2(序列辨识码编号17)18.mmp15:基质金属蛋白酶15(matrixmetallopeptidase15)﹝人类﹞国家生物技术资讯中心参考序列:nm_002428.3(序列辨识码编号18)本发明的优点乳房切除术后放射性治疗以每天一次、每周五次的频率为患者进行。每个疗程通常持续4到6周。这样的治疗方式不但对患者本人来说是沉重的负担,也同样给患者家属及社会带来极大压力,包括每天为了治疗通勤、向职场请假、因为员工请假而必须重新安排人力配置、额外的财务支出等。本发明的预后检测与套组可提供更精准正确的评估,藉由辨识出复发和/或远端转移风险低、不需要辅助性治疗(例如乳房切除术后放射性治疗、化学治疗以及荷尔蒙治疗)的患者,进而影响辅助性治疗的决定,减少或避免过重或过度的治疗。而减少或避免过重或过度的治疗将可减少或避免不必要、与术后治疗相关的副作用。加诸在患者、患者家属以及社会上的相关负担,可因此得到缓解。虽然本发明所应用的(18基因检测组合)分类法,与图2所示的34基因组预测模型有一些共同的基本概念,但本发明提供的评估套组,具有高度准确性、灵敏性(真阳性率)与特异性(真阴性率),可准确进行评估与验证。在临床上,本(18基因检测组合)分类法为患者局部区域复发潜在风险的预估,提供一有效的辅助评估工具。此外,本(18基因检测组合)分类法也可预估乳癌患者的远端转移可能性。根据得分算式,18基因分数<21的患者被定义为远端转移的低风险群,18基因分数介于21与43之间的患者被定义为远端转移的中度风险群,而18基因分数≧44的患者则被定义为远端转移的高风险群。其优点是,主要治疗结果为五年无远端转移机率。追踪期中位数为56.7(0到168.2)个月,低风险群(n=179/818,21.9%)、中度风险群(n=470/818,57.5%)以及高风险群(n=169/818,20.7%)患者的五年无远端转移机率,分别是96.6%、85%以及59.6%。第1期低风险群患者(n=79/218,36.2%)的五年无远端转移机率为100%,第2期低风险群患者(n=82/411,19.9%)的五年无远端转移机率为94.5%,第3期低风险群患者(n=18/184,9.7%)的五年无远端转移机率则为90.9%。多变量分析揭露,无论患者年龄、癌症亚型、肿瘤等级、淋巴结状态或辅助性治疗类型,本18基因分类法为一独立预后因子,在分数≧21的风险比值调整为5.7(95%信赖区间,2.0到15.9;9=0.0009)时,影响远端转移。业界典型认为,任何种类的风险预估一般都以5%的风险为基础(或是95%的信赖水准)。在本发明中,在乳房切除手术以及/或乳房保留手术后,为乳癌患者预估局部区域复发以及/远端转移可能性时,区域复发以及/远端转移风险分级的建议临界值,即以5%的风险为基础(或是95%的信赖水准)。然而,本领域技术人员可知,若有偏好或有要求比较保守或比较不保守时,临界值可随之改变。例如,在上述一或多个实施例中,根据得分算式将患者归类于局部区域复发的一低风险群或高风险群时,最佳临界值是31分。其中<31的分数被定义为局部区域复发的低风险群,而≧31分的分数则被定义为局部区域复发的高风险群。又例如,在上述一或多个实施例中,根据得分算式,分数<21的患者被定义为远端转移的低风险群,分数介于21与43之间的患者被定义为远端转移的中度风险群,而分数≧44的患者则被定义为远端转移的高风险群。上述所提之参照分数31(或第一预设参照值),也可用来将患者归类于远端转移的一低风险群或一高风险群。然而,若将这样的分数应用在远端转移的风险分级,则整体准确度、灵敏度与特异度都会受到影响(例如,增加或减少)。同样地,上述所提之<21的分数(或第二预设参照值)、介于21与43之间的分数以及≧44的分数(或第三预设参照值),也可用来将患者归类于局部区域复发的一低风险群或一高风险群。然而,若将这样的分数应用在局部区域复发的风险分级,则整体准确度、灵敏度与特异度都会受到影响(例如,增加或减少)。综合考量下,虽然本说明书描述了局部区域复发以及远端转移风险分级的较佳或最佳分数,但仍可依照偏好或要求的保守程度或风险嗜好改变最佳参照值。本18基因分类法的优点是,它为一通用的乳癌预后生物标记,可用来为乳癌患者预估或评估局部区域复发和/或远端转移风险。现行的医疗实务是根据静态的平均数(staticaverage)安排治疗。虽然某些治疗的确能提供帮助,但某些治疗却不然。这导致医疗资源的大浪费。相较之下,本发明的优点是提供一精准有效的评估方法、系统与套组,使医疗与保险资源的运用更加准确有效。其他实施例根据本发明之一面向的一套组可包括抗体(antibodies)、适体(aptamer)、放大系统(amplificationsystem)、检测试剂(色原﹝chromogen﹞以及萤光团﹝fluorophore﹞等)、稀释用缓冲溶剂(dilutionbuffer)、洗涤液(washingsolution)、对比染色(counterstain)或前述的任何组合。可将套组组件予以包装,方便手动或部分或全自动执行上述方法。在其他应用套组的实施例中,本发明提供的一套组包括本发明的构成组件,并可选择包括这些构成组件的用法说明。这样的套组可有各种不同用途,包括例如将患者族群分级、诊断、预后、导引治疗处置的决定以及其他应用。在本说明书、或并入本说明书做为参考之任何文件中,所提及之任何产品的任何制造者用法说明、描述、产品说明书以及产品单,都在此并入本说明书做为参考,且可应用在本发明的实施中。本说明书揭露的所有特征都可以任何组合形式结合。在本发明书中揭露的每一个特征都可以一替代特征取代,达到相同、相等或类似目的。因此,除非特别另行声明,否则本说明书所揭露的每一个特征都只是一系列相等或类似特征的其中一个范例。综上所述,需了解上述实施例仅只做为本发明的范例说明,本
技术领域:
之一般技艺人士很容易可确定本发明的基本特征,且可在不偏离本发明的精神与范畴之下,为本发明做各种更改与变化,以使之适合各种用法与条件。因此,其他实施例也涵盖在本发明专利申请范围之内。参考文献1.taghiana、jeongjh、mamounase等人。在接受乳房切除手术,以及有或无抗雌激素(tamoxifen)的辅助性化学治疗,但未受放射性治疗下,可开刀治疗之乳癌患者的局部区域失败模式:国家外科辅助乳房及胃肠计画(nationalsurgicaladjuvantbreastandbowelproject)五项随机临床试验的结果。临床肿瘤学期刊(jclinoncol),2004年,第22期,第4247到4254页。2.chengsh、horngcf、clarkejl等人。乳房切除手术后,乳癌患者局部区域复发的预后指数分数以及临床预测模型。放射肿瘤学、生物学、物理学国际期刊(intjradiaoncolbiolphys),2006年,第64期,第1401到1409页。3.zellarsrc、hilsenbecksg、clarkbm等人。乳房切除手术后,p53应用于乳癌患者局部失败的预后价值。临床肿瘤学期刊,2000年,第18期,第1906到1913页。4.vanderhageja、vandenbroeklj、legrandc等人。p70s6激酶蛋白的过度表现,与淋巴结阴性、停经前期(premenopausal)之初期乳癌患者局部区域复发风险增加的相关性。英国癌症期刊(brjcancer),2004年,第90期,第1543到1550页。5.rechta、edgesb、solinlj等人。乳房切除术后放射性治疗:美国临床肿瘤学学会(americansocietyofclinicaloncology)的临床实务指导方针。临床肿瘤学期刊,2001年,第19期,第1539到1569页。6.overgaardm、hansenps、overgaardj等人。接受辅助性化学治疗、停经前期之高风险乳癌患者的术后放射性治疗。丹麦乳癌合作组织(danishbreastcancercooperativegroup)第82b号试验。国家英语医学期刊(nengljmed),1997年,第337期,第949到955页。7.overgaardm、jensenmb、overgaardj等人。接受辅助性抗雌激素、停经前期之高风险乳癌患者的术后放射性治疗。丹麦乳癌合作组织第82c号随机试验。刺胳针(lancet),1999年,第353期,第1641到1648页。8.ragazj、jacksonsm、len等人。淋巴结阳性、停经前期乳癌患者的辅助性放射性治疗以及化学治疗。国家英语医学期刊,1997年,第337期,第956到962页。9.ebctcg、mcgalep、taylorc等人。乳房切除手术以及腋下手术(axillarysurgery)后,放射性治疗对于十年复发以及二十年乳癌死亡率的影响:22个随机试验中8135名妇女的个别病人资料综合分析(meta-analysis)。刺胳针,2014年,第383期,第2127到2135页。10.paiks、shaks、tangg等人。抗雌激素治疗后,用来预估淋巴结阴性乳癌复发的一多基因检验法。国家英语医学期刊,2004年,第351期,第2817到2826页。11.chengsh、horngcf、westm等人。乳房切除术后乳癌局部区域复发的基因体预估。临床肿瘤学期刊,2006年,第24期,第4594到4602页。12.solinlj、grayr、baehnerfl等人。用来预估胸部乳腺管原位癌局部复发风险的一多基因表现检验法。国家癌症协会期刊(jnatlcancerinst),2013年,第105期,第701到710页。13.van’tveerlj、daih、vandevijvermj等人。以基因表现图谱预估乳癌的临床治疗结果。自然(nature),2002年,第415期,第530到536页。14.wangy、klijnjg、zhangy等人。用来预估淋巴结阴性原生乳癌之远端转移的基因表现图谱。刺胳针,2005年,第365期,第671到679页。15.harrisln、ismailan、mcshanelm等人。应用生物标记为初期侵袭性乳癌妇女决定辅助性系统性治疗类型:美国临床肿瘤学学会的临床实务指导方针。临床肿瘤学期刊,2016年。16.台湾癌症登记年报(cancerregistryannualreport),2012台湾。台湾hpamohaw主编。台北,2015年,第68到69页。17.porterme、baronjf、wangcj。和信治癌中心医院:乳癌治疗在台湾。哈佛商业评论(harvardbusinessschoolreview),2010年。18.sorliet、peroucm、tibshiranir等人。以乳癌的基因表现模式辨别肿瘤子型(tumorsubclass)的临床意义。美国国家科学院院刊(procnatlacadsciusa),2001年,第98期,第10869到10874页。19.peroucm、sorliet、eisenmb等人。人类乳房肿瘤的分子图像(molecularportraits)。自然,2000年,第406期,第747到752页。20.mooks、schmidtmk、vialeg等人。在一独立的验证研究中,以70基因预后标志(prognosis-signature),为1到3颗阳性淋巴结的乳癌患者预估疾病治疗结果。乳癌研究与治疗(breastcancerrestreat),2009年,第116期,第295到302页。21.dubskyp、brasejc、jakeszr等人。以endopredict分数,为雌激素受体阳性/her2阴性的乳癌患者,提供关于晚期远端转移的预后资讯。英国癌症期刊,2013年,第109期,第2959到2964页。22.dabbsdj、kleinme、mohsinsk、tubbsrr、shuaiy、bhargavar。安可待检测中her2定量逆转录聚合酶连锁反应的高伪阴性率:一独立的品质保证(qualityassurance)研究。临床肿瘤学期刊,2011年,第29期,第4279到4285页。23.reis-filhojs、pusztail。乳癌的基因表现图谱:分类、预后以及预估。刺胳针,2011年,第378期,第1812到1823页。24.reyalf、vanvlietmh、armstrongnj等人。一全面性的预后标志分析揭露,乳癌中细胞增生、免疫反应以及rna剪接模组(splicingmodules)具有高度预估能力。乳癌研究,2008年,第10期,r93。25.teschendorffae、caldasc。有高度预估价值、能在雌激素受体阴性乳癌中辨识出预后良好患者的一稳健分类法。乳癌研究,2008年,第10期,r73。26.bianchinig、qiy、alvarezrh等人。乳癌基质(stroma)的分子解剖(molecularanatomy),以及将其应用在雌激素受体阳性与阴性癌症中的预后价值。临床肿瘤学期刊,2010年,第28期,第4316到4323页。27.finakg、bertosn、pepinf等人。以基质基因表现预测乳癌的临床治疗结果。自然医学(natmed),2008年,第14期,第518到527页。28.albainks、ungerjm、crowleyjj、coltmanca、hershmandl。西南肿瘤小组(southwestoncologygroup)随机临床试验患者之癌症存活率的种族差异性。国家癌症机构期刊(journalofthenationalcancerinstitute),2009年。29.careyla、peroucm、livasyca等人。卡罗莱纳州乳癌研究中的种族、乳癌亚型以及存活率。美国医学会杂志(jama),2006年,第295期,第2492到2502页。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种基于片状锶铁氧体双重放大的乳腺癌易感基因免疫传感器的制备方法
- 基于pcr引物3’末端核苷酸双脱氧修饰的乳腺癌易感基因snp快速、灵敏检测方法
- 用于乳腺癌易感基因BRCA1和BRCA2的Long-range PCR检测的引物组、方法及试剂盒的制作方法
- 一种基于纳米银及纳米铜联合构建的双通道乳腺癌易感基因传感器的制备方法及应用
- 预测乳腺癌结果的nano46基因和方法
- Brca基因易感snp位点检测组合物的制作方法
- 3d热乳癌检测的制作方法
- 基于微流控芯片的基因治疗乳腺癌的药物的制备方法
- 一种检测原发性肝细胞癌的易感基因的荧光定量pcr基因分型方法及其试剂盒的制作方法
- Akr1b10基因蛋白作为乳腺癌诊断标志物和药物靶标的制作方法