一种智能聚合物、制备方法及应用与流程
本发明涉及聚合物的制备技术领域,特别涉及一种智能聚合物、制备方法及应用。
背景技术:
众所周知的,在生物界中,糖、核酸以及蛋白质是构成生命体的三类最基本的物质。
多年来,人们对于糖的认识还仅局限于其作为生命活动的能源与结构物质。然而,随着科学技术的发展,特别是分子生物学和细胞生物学的迅猛发展,糖类又以一种全新的角色呈现在世人面前——信息传递者。例如,在生命体中引导糖蛋白的折叠或细胞间信息的传输,并且多以一种糖复合物或者糖缀合物的形式存在。
然而由于糖蛋白的种类繁多,在当前的生命科学的研究中,如何有效地识别并检测生物体中各种糖的类型早已成为生命科学中的重要研究内容,因此开发高灵敏度和高选择性的糖识别方法在生命科学领域中有着重要意义。
技术实现要素:
基于此,本发明的目的在于提出一种可以有效识别并检测糖类物质类型的智能聚合物,以在实际生物研究与应用中更加高效地确定糖类物质的类型,满足实际的检测需要。
本发明提出一种智能聚合物,其中,该智能聚合物的通式为:(sa)x(pt)y(nipaam)1-x-y,其中,sa、pt以及nipaam分别为识别单元、介导单元以及功能转换单元,x、y为单体摩尔比;
所述识别单元为糖基单体,所述介导单元为n-丙烯酰基-n’-4-(三氟甲基)-苯基硫脲单体,所述功能转换单元为n-异丙基丙烯酰胺单体。
所述智能聚合物,其中,所述糖基单体由葡萄糖胺或半乳糖胺分别与丙烯酰氯反应制得。
所述智能聚合物,其中,所述糖基单体由葡萄糖、半乳糖、甘露糖、木糖、麦芽糖、乳糖、蔗糖、麦芽糖或棉籽糖中的至少一种经氨基化处理后再与丙烯酰氯反应制得。
本发明还提出一种智能聚合物的制备方法,其中,所述方法包括如下步骤:
分别量取1-5ml超纯水、1-5ml甲醇以及1-10mln,n-二甲基甲酰胺并依次加入一反应茄瓶中,进行搅拌至混合均匀;
分别称量0.1-1g的n-异丙基丙烯酰胺单体、0.1-1g的n-丙烯酰基-n’-4-三氟甲基-苯基硫脲单体以及0.1-1g糖基单体并加入到所述反应茄瓶中进行搅拌溶解,超声1-30min;
将所述反应茄瓶在液氮中冷冻2-10min后进行抽气作业,并同时将所述反应茄瓶置于20-50℃的液态水中以加速溶解除气直至所述反应茄瓶中的溶液完全溶解;
在所述反应茄瓶中依次加入0.01-0.1g溴化亚铜粉末以及20-200μln,n,n’,n’,n”-五甲基二亚乙基三胺,完全溶解以得到中间产物溶液;
抽取所述中间产物溶液并加入到一预先充满氮气且装有氨基化基质材料的锥形瓶中,在30-70℃的环境中油浴1-6h得到预产物,将所述预产物经甲醇、水洗后并烘干得到所述智能聚合物。
所述智能聚合物的制备方法,其中,所述糖基单体的制备包括如下步骤:
配制2mol·l-1的k2co3溶液,称取1-20gd-(+)-氨基葡萄糖盐酸盐溶于所述k2co3溶液中,并在冰浴条件下进行搅拌溶解;
逐滴滴加1-10ml丙烯酰氯,在冰浴条件下继续搅拌1-6h,之后在室温条件下搅拌12h得到第一混合溶液;
对上述第一混合溶液进行过滤处理,将滤液经乙醚洗涤后用10wt%的盐酸调节ph为2,乙醚重复洗涤3次后再用1mol·l-1的naoh溶液调节ph至7得第二混合溶液;
将上述第二混合溶液进行过滤后取滤液旋转蒸发重结晶以得到所述糖基单体。
所述智能聚合物的制备方法,其中,所述n-丙烯酰基-n’-4-三氟甲基-苯基硫脲单体的制备包括如下步骤:
称取0.1-2gkscn固体加入到烧瓶中,然后继续加入3-40ml无水丙酮,室温条件下进行磁力搅拌直至完全溶解;
量取0.2-2ml丙烯酰氯,逐滴滴加到上述溶液中并持续搅拌反应1-18h后进行离心并保留上清液;
将0.3-2ml的4-三氟甲基苯胺溶解于3-40ml二氯甲烷溶液中,室温条件下搅拌均匀后逐滴加入所述上清液继续搅拌反应2-12h后加入无水硫酸钠搅拌均匀;
对上述溶液进行过滤并旋转蒸发重结晶以得到所述n-丙烯酰基-n’-4-三氟甲基-苯基硫脲单体。
本发明还提出一种智能聚合物的应用,其中,将所述智能聚合物在不同种类的糖溶液中进行浸泡处理,根据所述智能聚合物的表面形貌、浸润性以及表面硬度的变化来识别检测所述糖溶液的类型。
所述智能聚合物的应用,其中,所述智能聚合物还用于基于所述智能聚合物与糖蛋白酶解物之间的相互作用进行糖肽富集与分离。
所述智能聚合物的应用,其中,所述糖肽富集与分离的操作在固相萃取模式或分散固相萃取模式下进行。
所述智能聚合物的应用,其中,所述糖肽富集与分离的操作中所述糖蛋白酶解物与待处理物之间的质量比为1:5-200,进行富集与分离时的温度为10-60℃。
本发明提出的智能聚合物中的识别单元(也即糖基单元)对不同的糖呈现出不同的结合能力,根据该结合能力的差异以区分出不同类型的糖,从而便于实际应用研究中对糖类物质的检测,满足了实际应用需求。
本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
附图说明
图1为本发明第一实施例中智能聚合物的初始接触角与分别经过甘露糖、半乳糖、n-乙酰葡萄糖胺、葡萄糖、n-乙酰半乳糖胺、岩藻糖、及唾液酸溶液浸泡处理后的表面接触角值;
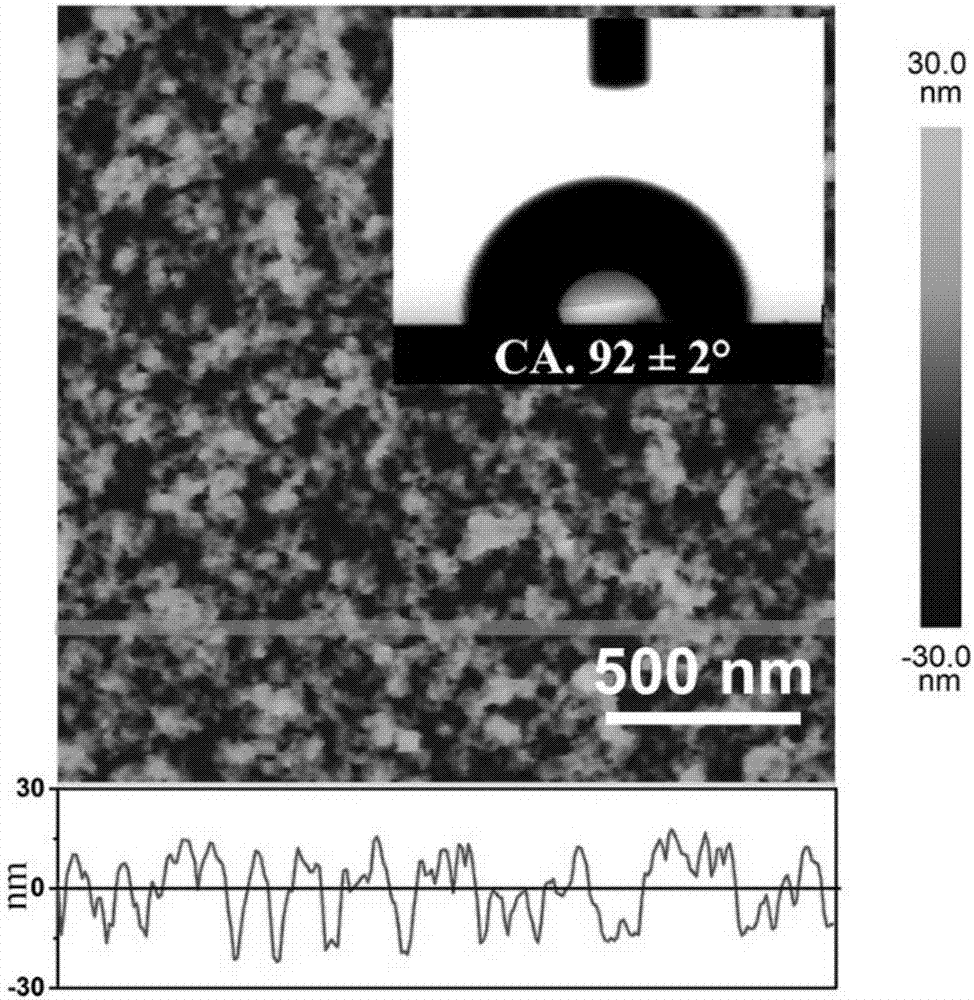
图2为本发明第一实施例中智能聚合物的初始表面接触角以及表面形貌;
图3为本发明第一实施例中智能聚合物经半乳糖溶液浸泡处理后的表面接触角和表面形貌;
图4为本发明第一实施例中智能聚合物经岩藻糖溶液浸泡处理后的表面接触角和表面形貌;
图5为本发明第一实施例中智能聚合物经唾液酸溶液浸泡处理后的表面接触角和表面形貌;
图6为本发明第一实施例中智能聚合物的初始表面杨氏模量与经半乳糖、岩藻糖和唾液酸溶液处理后的表面杨氏模量;
图7为本发明第二实施例中智能聚合物在固相萃取模式下对胎球蛋白和牛血清蛋白(质量比为1:50)混合物的酶解产物进行富集后的maldi-tof质谱图;
图8为本发明第二实施例中智能聚合物在固相萃取模式下对胎球蛋白和牛血清蛋白(质量比为1:100)混合物的酶解产物进行富集后的maldi-tof质谱图。
具体实施方式
为了便于理解本发明,下面将参照相关附图对本发明进行更全面的描述。附图中给出了本发明的首选实施例。但是,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施例。相反地,提供这些实施例的目的是使对本发明的公开内容更加透彻全面。
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。本文所使用的术语“及/或”包括一个或多个相关的所列项目的任意的和所有的组合。
实施例1
本发明提出一种智能聚合物,其中,该智能聚合物的通式为:(sa)x(pt)y(nipaam)1-x-y,sa、pt以及nipaam分别为识别单元、介导单元以及功能转换单元,x、y为单体摩尔比,所述识别单元为糖基单体,所述介导单元为n-丙烯酰基-n’-4-(三氟甲基)-苯基硫脲单体,所述功能转换单元为n-异丙基丙烯酰胺单体。
在此需要说明的是,对所述糖基单体而言,其可以由葡萄糖胺或半乳糖胺分别与丙烯酰氯反应制得,也可以由葡萄糖、半乳糖、甘露糖、木糖、麦芽糖、乳糖、蔗糖、麦芽糖或棉籽糖中的至少一种经氨基化处理后再与丙烯酰氯反应制得。
在本实施例中,所述糖基单体为葡萄糖单体(glc),该葡萄糖单体由葡萄糖胺与丙烯酰氯反应制得,此时该智能聚合物对应的通式可以记为:(nipaam-co-pt-co-glc),对应的具体结构式为:
在此需要说明的是,对该智能聚合物(nipaam-co-pt-co-glc)而言,其化学形态根据与其进行接枝反应的基质材料的形态直接相关。具体的,若将该智能聚合物接枝到二维平面无机基质材料的表面,那么此时该智能聚合物便以薄膜的形态呈现,也即智能聚合物薄膜;若将该智能聚合物接枝到球状多孔无机基质材料上,则该智能聚合物便以多孔球状聚合物的形态呈现,且常用作柱色谱分离材料。一般的,该二维平面无机基质材料包括半导体si、sio2,金属au、ag、cu、al或pt、金属氧化物cuo、al2o3、fe3o4或tio2中的至少一种,制得的是智能聚合物薄膜材料。在本实施例中所制得的也为二维的智能聚合物薄膜材料。
对于本实施例中的智能聚合物而言,对应的识别单元为葡萄糖单体。该葡萄糖单体的制备过程具体如下:
首先配制2mol·l-1的k2co3溶液,然后称取1-20gd-(+)-氨基葡萄糖盐酸盐溶于50~60ml的配置好的k2co3溶液中,并在冰浴条件下进行搅拌溶解。然后往溶液中用注射器逐滴滴加丙烯酰氯2.5ml,在冰浴条件下继续搅拌2h,之后转移到室温条件下搅拌过夜。
反应完成后的水溶液用10wt%的盐酸调节ph为2左右,然后再次于分液漏斗中用乙醚洗涤3次,收集到的水溶液继续用1mol·l-1的naoh溶液调节水溶液ph到7左右。之后,水溶液经冷冻干燥除去全部水分后,残余的固体捣碎后用甲醇进行溶解,磁力搅拌2h,然后用装有一半容积硅藻土的布氏漏斗进行过滤,收取滤液并旋转蒸发除去60%的溶剂。然后再用新装的硅藻土进行过滤,取滤液并旋转蒸发大部分溶剂,少量较浓的溶液等待上柱、分离。
然后采用湿法进行填装硅胶柱进行上样,以固定比例(甲醇/乙酸乙酯,体积比为1/4)的淋洗液进行冲洗,点板后用干净的锥形瓶收集洗脱液,此时目标产物在4℃温度下以自发结晶的形式于甲醇和乙酸乙酯(体积比为1/4)的混合溶液中析出,过滤后真空干燥得到白色粉末,然后再次于甲醇和乙酸乙酯(体积比为1/4)的混合溶液重结晶,得到白色目标产物1.62g,产量约为31%,熔点为130~135℃。
在制备得到了葡萄糖单体之后,对制得的葡萄糖单体进行了具体表征。其中,该葡萄糖单体(glc)的核磁氢谱为:1hnmr(500mhz,d2o):δ(ppm)6.46-6.17(m,co-ch,ch=ch,anti),5.98-5.71(ch=ch,syn),5.28(d,j=3.5hz,ch),4.13-3.43(ch×5);1hnmr(500mhz,dmso-d6):δ(ppm)7.93(d,j=8.1hz,1h,co-nh),6.45(d,j=3.5hz,1h,c-oh),6.39(d,d,j1=j2=10hz,1h,c=ch),6.07(d,d,j1=j2=2.5hz,1h,c=ch),5.55(d,d,j1=2hz,j2=2.5hz,1h,c=ch),4.98(m,2h,c-ch),4.78(d,j=5.5hz,1h,c-ch),4.45(t,j1=j2=5.8hz,1h,c-ch),3.68-3.46(m,5h,c-ch,c-coh),3.19-3.10(m,2h,c-coh)。该葡萄糖单体的(glc)的核磁碳谱为:13cnmr(126mhz,dmso-d6):δ(ppm):165.12,132.59,125.25,90.94,72.53,71.55,70.78,61.54,54.97。
对该葡萄糖单体(glc)的红外特性(ft-ir)也进行了表征,具体为:3423,3325,3275,2924,1652,1626,1609,1550,1442,1410,1351,1330,1285,1266,1238,1144,1119,1101,1054,1037,1018,990,955,863,846,806,785,740cm-1。其中,1652cm-1和1626cm-1两个强峰为酰胺ⅰ带和酰胺ⅱ带的特征峰。
与此同时,该葡萄糖单体(glc)的质谱数据为:calcd.for(理论值):c9h15no6:233.09;found(实验值):256.03[m+na]+。该葡萄糖单体(glc)的元素分析数据为:calcd.for(理论值):c9h15no6(%):c,46.35;h,6.48;n,6.01;found(实验值):c,45.86;h,6.93;n,5.89。
在制备了上述葡萄糖单体之后,还需要制备合成介导单元n-丙烯酰基-n’-4-(三氟甲基)-苯基硫脲单体。该介导单元的合成步骤如下:
首先称取1.45g的kscn固体,将其加入到100ml的烧瓶中,然后继续加入30ml无水丙酮,在室温条件下进行磁力搅拌直至溶解。然后用注射剂吸取1.21ml的丙烯酰氯溶液,逐滴缓慢地滴加到反应物溶液中并持续搅拌反应12h。反应结束后,将产生的固体溶液混合物进行离心分离,取黄色上清液待用。
然后量取1.88ml的4-三氟甲基苯胺并将其溶解混合于30ml的二氯甲烷溶液中,在室温条件下进行搅拌,再用恒压滴定漏斗逐滴滴加上一步所收集的黄色上清液,滴加完成后在室温条件下继续搅拌反应12h,待反应结束后加入适量无水硫酸钠干燥过夜。随后,对水溶液进行过滤并收集滤液,然后用旋转蒸发仪蒸发大部分溶剂以得到较浓的溶液,放置于低温冰箱中(4℃)结晶干燥得到淡黄色针状晶体,然后再次溶解于二氯甲烷中重结晶,最终得到淡黄色的针状晶体1.4g,产率约为35%,熔点为125~130℃。
在制备得到了该介导单体之后,对该介导单体的性质进行了表征。具体的,该介导单体的核磁氢谱为:1hnmr(500mhz,dmso-d6):δ(ppm)12.72(s,1h,co-nh),11.74(s,1h,co-nh),7.91(d,j=8.4hz,2h,ph-h),7.74(d,j=8.5hz,2h,ph-h),6.61(d,d,j1=j2=10.2hz,1h,c=ch),6.44(d,d,j1=j2=17.1hz,1h,c=ch),6.00(d,d,j1=j2=9.9hz,1h,c=ch)。该介导单体的核磁碳谱为:13cnmr(126mhz,dmso-d6):δ(ppm)179.72,166.10,141.91,132.51,130.21,126.29,126.26,124.94cm-1。
此外,对该介导单体的红外特性(ft-ir)也进行了表征,具体为:3148,3023,1940,1690,1630,1613,1594,1527,1405,1314,1246,1168,1109,1062,1016,977,894,851,799,741,727,682cm-1,其中1690cm-1和1630cm-1两个强峰为酰胺i带和酰胺ⅱ带的特征峰,1109cm-1的强峰归属于硫脲基团中c=s的振动,851cm-1的强峰归属于对位取代苯环。
与此同时,该介导单体的质谱数据为:calcd.for(理论值)c11h9f3n2os:274.04;found(实验值):275.07[m+h]+。pt单体的元素分析数据为:calcd.for(理论值):c11h9f3n2os(%):c,48.17;h,3.31;n,10.21;s,11.69;found(实验值):c,48.01;h,3.25;n,10.23;s,11.79。
在制备了上述葡萄糖单体以及介导单元n-丙烯酰基-n’-4-(三氟甲基)-苯基硫脲单体之后,进行二维接枝处理。在本实施例中,二维平面无机材料选用单晶硅片。具体的,首先将单晶硅片切成约1cm×1cm大小,取数片置于称量瓶中,依次用乙醇、异丙醇、丙酮以及超纯水分别超声清洗10min,然后用大量的超纯水冲洗硅片,再用氮气气流进行吹干后置于铬酸洗液中浸泡2h。取出该单晶硅片,用大量超纯水清洗并吹干。将洗净的硅片浸入浓硫酸/双氧水(体积比为7/3)的溶液中在100℃的环境下加热20min后取出硅片,然后浸泡在超纯水中,并用大量超纯水冲洗硅片,在氮气气流下吹干并在60℃下干燥2h。
然后量取10ml无水甲苯加入到100ml的锥形瓶中,同时用移液枪量取0.5ml的3-氨基丙基三甲氧基硅烷(atms)加入到锥形瓶中,充分摇晃溶液至完全混合。将上述干燥后的单晶硅片转移到锥形瓶中,置于油浴中,连接上冷凝回流管以及自来水管路进行冷凝回流6h后取出硅片置于称量瓶中,分别用甲苯以及二氯甲烷浸泡清洗三次,氮气气流吹干待用。
将接枝有氨基的硅片表面用二氯甲烷溶液清洗2次,并在溶液中超声数秒以除去表面团聚或残留的atms,氮气流吹干后用镊子转移到装有10ml由无水二氯甲烷以及0.2ml无水吡啶所组成的混合溶液的锥形瓶中,保证溶液完全覆盖硅片。然后将锥形瓶放入含少量冰的水浴条件下放置15min,用移液枪量取200μl引发剂α-溴异丁酰溴(bibb),逐滴加入到锥形瓶中,小心摇晃均匀。继续保持在冰浴条件下避光放置1h,随后转移到室温条件且避光放置过夜(约10h)。反应完成后取出硅片,用二氯甲烷清洗3次,然后浸泡在二氯甲烷中避光,留待下一步骤使用。
在制备了带有溴基团的基质材料(单晶硅片)之后,再分别量取2.5ml的超纯水、2.5ml的纯制甲醇、5ml的n,n-二甲基甲酰胺(dmf)于25ml的具有节门高真空阀门的反应茄瓶中进行混合。然后称量0.79g的n-异丙基丙烯酰胺单体(nipaam)、0.41g的三氟甲基苯基硫脲介导单体(pt)以及0.35g的葡萄糖单体(glc)加入到反应茄瓶中进行溶解,超声20min。随后塞上翻口橡胶塞并旋紧高真空阀门,将反应茄瓶置于液氮中冷冻5min,然后打开油泵电源,连接好抽气管路,旋开阀门抽气,同时用40℃的水加速溶解除气。当反应茄瓶中的溶液完全融化后,旋紧阀门,拔出油泵管路,关闭油泵电源,此为一次完整的冷冻-溶解除氧循环,重复循环3次。此外,上述反应茄瓶中的溶液在最后一次冷冻后通氮气至橡胶塞膨胀后打开橡胶塞,快速加入称量好的溴化亚铜粉末以及160μl的配体n,n,n′,n′,n”-五甲基二亚乙基三胺(pmdeta),塞上橡胶塞再次进行冷冻溶解除氧一次,溶解后通入适量氮气(用手感知橡胶塞轻微鼓起),超声30s,再重复冷冻溶解除气两次。最后溶解后,通氮气至反应瓶充满,用10ml注射器连接7#不锈钢长针头抽出溶液,经过针头过滤器过滤后注入预先充满氮气的含有硅片的100ml锥形瓶中,然后用锡箔纸包裹住整个锥形瓶进行避光,放入55℃油浴中反应6h。反应完成后取出硅片,依次用dmf、甲醇以及超纯水进行清洗,然后氮气气流吹干,最终得到上述二维的智能聚合物薄膜材料poly(nipaam-co-pt-co-glc)。
对于本实施例中所制备得到的二维的智能聚合物薄膜材料而言,由于该智能聚合物(薄膜)中的糖基单体(此时为葡萄糖单体)对不同的糖类物质具有不同的结合能力,在本实施例中,设置了一组对照试验用于比较其对不同糖类物质的结合性质,在本实施例中,采用了荧光滴定的方法测定了葡萄糖单体(glc)作为识别单元的智能聚合物(nipaam-co-pt-co-glc)分别与唾液酸、海藻糖、n-乙酰-d-半乳糖胺、葡萄糖、n-乙酰葡萄糖胺、半乳糖以及甘露糖之间的结合能力的大小,所得到的结合常数如表一所示:
表一
从表一可以很明显地看出:该智能聚合物(nipaam-co-pt-co-glc)中的葡萄糖单体与各种单糖的结合能力大小依次为:唾液酸>海藻糖>n-乙酰-d-半乳糖胺>葡萄糖>n-乙酰葡萄糖胺>半乳糖>甘露糖。在实际检测应用中,由于不同的单糖与该智能聚合物(nipaam-co-pt-co-glc)之间的结合能力均对应一个较为具体的结合常数,且不同的单糖与该智能聚合物之间的结合常数差异较大,因此可以根据所检测到的结合常数的大小作为判定与该智能聚合物进行结合作用的单糖类型的一个重要参考因素。
除此之外,请参阅图1,该智能聚合物(nipaam-co-pt-co-glc)在与不同的单糖进行相互作用之后,其初始接触角会发生一定的变化。在本实施例中,该智能聚合物(nipaam-co-pt-co-glc)分别在甘露糖、半乳糖、n-乙酰葡萄糖胺、葡萄糖、n-乙酰半乳糖胺、岩藻糖、及唾液酸溶液中浸泡之后,通过接触角仪和原子力显微镜及观察浸泡不同种糖溶液前后该智能聚合物表面的接触角的变化。从图1可以看出,对于该智能聚合物而言,其初始接触角为92°,在经唾液酸溶液浸泡之后,其初始接触角的变化值最大,由原来的初始接触角92°直接变为49°,而经甘露糖溶液浸泡之后,其初始接触角变化最小,接触角变为91°。经半乳糖溶液浸泡之后接触角变为90°,经岩藻糖溶液浸泡后接触角变为75°。
在观察浸泡前后接触角变化的同时,对该智能聚合物的表面形貌的变化也进行了观察。请参阅图2至图5,分别为该智能聚合物(nipaam-co-pt-co-glc)的初始表面形貌以及经半乳糖溶液、岩藻糖溶液以及唾液酸溶液浸泡之后的表面形貌的变化。从图中可以看出,该智能聚合物(nipaam-co-pt-co-glc)经半乳糖溶液以及岩藻糖溶液浸泡之后其表面形貌几乎没有发生任何变化,而经过唾液酸溶液浸泡之后其表面形貌发生了较大变化,具体的,智能聚合物的初始状态所呈现出的凸起以及凹陷均被抹平,显示出较为平滑的表面形貌。
进一步的,对于该智能聚合物而言,在经不同的糖溶液浸泡之后,除了比较其结合常数、接触角以及表面形貌的变化之外,通过原子力显微镜的力学模式进行观察,进一步发现智能聚合物(薄膜)的软硬程度也会发生一定的变化,而该智能聚合物的软硬程度对应表面杨氏模量的大小。具体的,如图6所示,没有经过糖溶液浸泡的智能聚合物的杨氏模量经测量为99.78±32.98mpa,而经过半乳糖溶液浸泡之后的智能聚合物的杨氏模量为93.23±33.23mpa,相比并无明显变化;经岩藻糖溶液浸泡处理之后的智能聚合物的杨氏模量变为75.04±14.79mpa,相比仅发生了较小的变化;而经唾液酸溶液浸泡处理之后的智能聚合物的杨氏模量发生了巨大的变化,直接变为45.71±8.05mpa,这也充分印证了之前的该智能聚合物(薄膜)与唾液酸溶液之间的结合常数最大的结论。
综上所述可以得知,对于该智能聚合物而言,在经不同的糖溶液浸泡处理之后,其接触角、表面形貌以及表面杨氏模量的变化程度均与结合常数成正比,也即结合常数越大,其所对应的接触角、表面形貌以及表面杨氏模量的变化量也就越大。在进行实际糖类的检测时,可以综合根据该智能聚合物的接触角、表面形貌、表面杨氏模量以及结合常数来对糖溶液的类型进行综合判别。
实施例2
如上所述,当与所述智能聚合物进行接枝反应的为二维平面无机基质材料时,所制得的为二维的智能聚合物薄膜材料。而当与所述智能聚合物进行接枝反应的为球状多孔无机基质材料时,此时所得到的智能聚合物便为多孔球状聚合物。在本实施例中,进行接枝反应的为球状多孔无机基质材料。一般的,该球状无机基质材料包括半导体si、sio2,金属au、ag、cu、al或pt、金属氧化物cuo、al2o3、fe3o4或tio2中的至少一种,所制得的智能聚合物为多孔球状聚合物。
具体的,其制备过程如下:
首先称取6g硅球加入到2mol·l-1的盐酸溶液中,在室温条件下磁力搅拌48h以活化硅球,随后用离心的方法去除溶液,超纯水离心清洗5次后用乙醇离心清洗5次,再进行离心分离,在80℃的温度下进行真空干燥24h,取出后置于干燥器中待用。
然后称取3g活化后的硅球,量取60ml的无水甲苯以及12ml的atms加入到一100ml的圆底烧瓶中,连接上冷凝回流管以及自来水管路,然后置于油浴中在115℃温度下加热并冷凝回流24h。随后,待反应溶液冷却至室温后进行离心,依次用甲苯和丙酮超声离心清洗分离5次,再用乙醇离心清洗2次后在室温条件下进行真空干燥24h。
再称取1g经氨基化后的硅球,量取20ml的无水甲苯以及8ml的无水三乙胺置于50ml的圆底烧瓶中,在冰浴环境下磁力搅拌。然后量取4ml的α-溴异丁酰溴与以及8ml的无水甲苯进行混匀,用恒压滴定漏斗缓慢逐滴地将其滴加到上述硅球溶液中,在冰浴环境下反应2h后移除冰浴,在室温条件下反应24h。待反应结束后,依次用甲苯以及丙酮超声离心清洗分离5次,再用乙醇离心清洗2次,离心后去除上层乙醇溶液,在室温条件下真空干燥24h最终得到目标产物。该三维的多孔球状聚合物常被用作柱色谱分离材料,进行糖肽/糖蛋白富集以及分离。
一般的,该多孔球状聚合物常用作柱色谱分离。在本实施例中,将对该多孔球状聚合物作为柱色谱分离材料进行色谱分离操作展开较为详细的描述。
首先,在进行柱色谱分离时,先将1mg由该多孔智能聚合物poly(nipaam-co-pt-co-glc)制备的柱色谱分离材料装入移液枪头中制备成微型柱,然后用1μl(40pmol)的胎球蛋白与牛血清蛋白混合样品的蛋白酶解液上样后,再分别用30μl的体积浓度为85%乙腈/0.1%甲酸(ph=3)洗脱两次,随后用30μl含有80%乙腈/水溶液洗脱两次,最后用20μl50%乙腈/水溶液洗脱,将洗脱所得到的洗脱液直接在质谱上进行分析。
具体的,在进行糖肽/糖蛋白富集以及分离时,一般分为固相萃取模式以及分散固相萃取模式下进行。在固相萃取(spe)模式时,采用该三维的多孔聚合物材料富集分离糖肽,将糖蛋白酶解物上载到该三维的多孔聚合物材料填装的spe柱上,然后采用淋洗液冲洗,除去非糖肽,采用洗脱液淋洗分离出糖肽。在分散固相萃取模式时,采用该三维的多孔聚合物材料富集糖肽时,将糖蛋白酶解物上直接与富集材料混合,采用洗脱溶剂,使用离心方式、台阶梯度洗脱条件,富集出糖肽。其中,糖蛋白酶解物与待处理材料的质量比例为1:5-200,进行富集与分离时的温度为10-60℃。对所述淋洗液而言,其溶剂组成如下所示:a相为水,b相为乙腈,体积比a/b:10/90-40/60,或者a相为水,b相为甲醇,体积比a/b:10/90-40/60;对所述洗脱液而言,其溶剂组成如下所示:a相为水,b相为乙腈,体积比a/b:40/60-100/0;或者a相为水,b相为甲醇,体积比a/b:40/60-100/0。
如图7与图8所示,糖肽可以被从智能聚合物材料上洗脱下来,当胎球蛋白与牛血清蛋白的质量比为1:50时,采用多孔智能聚合物poly(nipaam-co-pt-co-glc)制成的柱色谱分离材料可以富集出32个糖肽;当胎球蛋白和牛血清蛋白的质量比为1:100时,采用该多孔智能聚合物poly(nipaam-co-pt-co-glc)制成的柱色谱分离材料仍然可以富集出24个糖肽,并且其中大部分都是唾液酸糖肽,由此说明多孔智能聚合物poly(nipaam-co-pt-co-glc)制成的柱色谱分离材料能特异性地富集唾液酸类糖肽。
本发明提出的智能聚合物中的识别单元(也即糖基单元)对不同的糖呈现出不同的结合能力,在不同种糖溶液进行浸泡之后,智能聚合物的接触角、表面形貌以及表面硬度均会产生特定的差异,根据上述差异以区分出不同类型的糖,从而便于实际应用研究中对糖类物质的检测,满足了实际应用需求。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!