一种母血浆游离DNA文库的构建方法以及父源等位基因的分型方法与流程
本发明属于生物学
技术领域:
。更具体地,涉及一种母血浆游离dna文库构建方法和父源等位基因的分型方法,包括设计母血浆游离dna的文库构建和高通量测序方法和试剂,以及游离dna中父源等位基因的确定方法。
背景技术:
:以往产前的胎儿遗传诊断主要基于有创取样,包括绒毛膜绒毛取样(chorionicvillussampling,cvs)和羊水穿刺(amniocentesis),这些诊断方法虽然准确率高,但其操作有创伤性,可导致宫内感染、流产和死胎等多种妊娠不良反应,且其取样时间均不可早于10周。1997年在孕妇血浆中游离胎儿dna(fetalcell-freedna,cffdna)的发现,使无创产前检测成为可能,对避免有创取样带来的风险,有效保障母胎健康有重要的意义。进一步研究表明,cffdna片段能够携带胎儿整个染色体组的遗传信息,从怀孕第4周开始在孕妇血浆中出现,孕7周后cffdna可以一定的比例稳定地存在于母体外周血中,其含量随着孕龄的增加逐渐增高,直至分娩前迅速增加,并能够在胎儿娩出后48小时内迅速从产妇体内代谢排出,不受既往妊娠的干扰。因此,孕妇血浆中的cffdna被认为是目前最理想的无创性胎儿检材。目前,cffdna在胎儿性别诊断、单基因遗传性疾病、胎儿三体综合征等多种临床产前诊断中有广泛的应用。在法医遗传学研究中,研究者一直致力于利用孕妇血浆cffdna进行遗传标记的检测和父源等位基因的分析,以实现无创父权鉴定。基于一代毛细管电泳(ce)的str分型系统是目前在法医遗传学研究中应用最广泛、最成熟的方法技术。然而,cffdna浓度在母血浆总游离dna(cell-freedna,cfdna)中含量较低,一般认为小于20%,在孕早期中一般小于5%,且呈高度片段化,其大小主要集中在150~200bp范围;而常规的str扩增子长度在100~350bp范围内且大小不均一,导致大片段父源str等位基因得不到有效扩增而被强大的母体dna背景掩盖此外,str分型中容易出现的影子带(stutterband)等非特异产物,增加分析的难度,影响分型的准确性。与str相比,单个snp位点因其分布广泛、突变率低、扩增片段短等特点使其具有较好的法医学应用前景,被认为是第三代dna遗传标记。随着snp数据库的不断完善以及相关检测技术的长足发展,越来越多的研究者开始采用snp分型技术对母血浆游离dna进行法医遗传学分析。按照snp分型通量的大小可以分为:低通量的snp分型方法有sanger测序法,等位基因特异性杂交电泳法等;中通量的snp分型方法有质谱法、snapshot法、高分辨溶解曲线分析法;高通量的snp分型方法包括snp基因芯片分型和基于新一代测序(nextgenerationsequecing,ngs)平台的snp分型。目前,越来越多的研究使用ngs技术对母血浆游离dna进行目标snp区域的父源等位基因检测和分析。基于ngs技术的游离dna检测其关键环节在于测序文库的构建。但是,现阶段主要采用芯片杂交捕获法(on-arrayhybrid-capture)进行高通量测序的文库制备,此法需要的模板dna量较大,且需定制大量的区域特异性探针,通过杂交技术捕获目标snp区域,成本高,实验周期长,技术流程繁琐,因此在大样本分析、技术转化和推广应用等方面均面临着巨大的挑战。技术实现要素:本发明要解决的技术问题是克服上述现有技术的缺陷和不足,提供一种游离dna的高通量测序文库及其构建方法,它适用于片段化的母血浆游离dna样品的高通量测序文库制备,并对父源等位基因进行分型。本发明解决了母血浆游离dna父源等位基因的准确分型鉴定问题,发挥了新一代测序技术在处理混合、降解(片段化)、微量检材中分型结果精确、高通量操作的优点,在无创性父权鉴定、多态性检测、基因频率调查等法医遗传学领域相关中有非常良好的应用前景。本发明的目的是提供一种母血浆游离dna文库的构建方法。本发明另一目的是提供一种父源等位基因分型方法。本发明上述目的通过以下技术方案实现:一组扩增母血浆游离dna中snp的特异性引物组,其特征在于,包括720对引物,上下游引物序列依次如seqidno.1~1440所示。其中,所述snp有720个,如实施例中表1所示。一种母血浆游离dna文库的构建方法,包括如下步骤:(1)制备待测样本dna,其中包括基因组dna和血浆游离dna;(2)利用权利要求1所述的720对引物进行超多重pcr复合扩增;(3)在扩增得到的720条片段两端分别连接标签序列(barcode)的接头和公用接头。其中,步骤(1)所述样品dna为孕妇外周血dna,包括基因组dna和血浆游离dna。优选地,步骤(2)所述超多重pcr复合扩增的反应体系为:5×ionampliseqtmhifimix4.0μl、引物组10.0μl、模板(gdna或cfdna)6.0μl。优选地,步骤(2)所述超多重pcr复合扩增的反应程序为:酶激活99℃2min;99℃15s,60℃4min,19个循环(cfdna)或18个循环(gdna);冷却到10℃保存。优选地,步骤(3)是采用ionxpresstmbarcodeadapters1-96试剂盒(thermofisherscientific),在片段两端分别连接有标签序列(barcode)的接头和公用接头。优选地,在步骤(3)之前,还需先消化步骤(2)扩增产物中多余的引物。具体优选地,是利用fupareagent(thermofisherscientific)消化步骤(2)扩增产物中多余的引物的具体方法为:在pcr扩增产物中加入2μlfupareagent,总体积达22μl;用pcr仪(abi9700)分别按以下程序进行反应:50℃10min,55℃10min,60℃20min,冷却到10℃保存。另外,上述方法构建得到的母血浆游离dna文库,也在本发明的保护范围之内。一种游离dna中父源等位基因的分型方法,包括如下步骤:s1.在上述构建文库的基础上,采用磁珠法将文库纯化;s2.将纯化后的文库进行qpcr定量;s3.选择合适的文库数目,进行测序模板的制备和测序;s4.数据分析,确定父源等位基因的分型。具体的详细操作方法见实施例。实际应用时,以该方法分析出的父源等位基因的分型与被控父的等位基因分型进行比对,可实现父权分析。另外,本发明还提供一种游离dna中父源等位基因的分型试剂盒,包括上述的720对引物。优选地,还包括上述构建文库所需的试剂。优选地,还包括上述游离dna中父源等位基因的分型方法中所需的试剂。本发明根据人类22条常染色体和y染色体的基因序列,针对720个均匀分布于基因组中的snp位点分别设计特异扩增引物,扩增子长度不超过140bp;采集9-20周孕妇外周血用于血浆游离dna提取,并应用多重复合pcr扩增技术对进行游离dna的文库构建;文库经纯化、定量后,在iontorrenttm平台上机测序。使用同样的方法对相应的母血细胞和胎儿组织基因组dna进行文库制备和测序。根据测序结果,选择母血细胞为纯合子的snp位点,分析母血浆中游离dna在相应位点上非母等位基因的百分比浓度,达到确定游离dna中父源等位基因的目的。本发明的方案中,目标snp的引物设计是文库构建的关键,采用在线工具ionampliseqdesigner(https://www.ampliseq.com/)进行引物设计及体系优化,保证目标区域的覆盖度在99%以上;由于血浆游离dna呈高度片段化(片段长度为150~200bp),因此将扩增子片段长度设置为140bp以下,以提高建库的成功率。父源等位基因的分型是本发明中另一个关键。对于常染色体snp,本发明选择母血细胞分型为纯合子的snp位点,分析母血浆游离dna在相应位点中的测序数据,计算非母等位基因的百分比浓度,将浓度超过2.0%的非母等位基因定义为父源等位基因;对于y染色体,由于母体基因组中并没有y染色体,因此胎儿的y染色体snp序列可直接获取。本发明具有以下有益效果:本发明根据人类22条常染色体和y染色体的基因序列,针对720个均匀分布于基因组中的snp位点分别设计特异扩增引物,适用范围广,且扩增子长度不超过140bp,对建库成功率的提高具有重要的意义。本发明所建立的超多重pcr反应构建文库,适用于对微量、短片段的血浆cfdna进行高通量测序,并有效的降低了实验的成本和周期;根据测序结果,精确的对父源等位基因进行分型,方法简单、直观、准确。随着新一代测序技术的普及,高通量获得的父源等位基因精确信息在无创性父权鉴定、多态性检测、基因频率调查等法医遗传学领域相关应用中受到高度重视。本发明所提供的试剂盒可作为一种独立、有效的分析方法,解决了母血浆游离dna父源等位基因的准确分型鉴定问题,发挥了新一代测序技术在处理混合、降解(片段化)、微量检材中分型结果精确、高通量操作的优点,对避免有创取样带来的风险,有效保障母胎健康有重要的意义。附图说明图1为本发明中检测标本的720个目标snp在个染色体上的分布以及snp扩增子的长度分布;其中,图a为常染色体snp在各染色体上的分布,图b为720个扩增子的长度分布。图2为本发明中检测母血浆游离dna标本所在ion318tm芯片的测序结果总结(每张318芯片检测4个血浆cfdna样品)。具体实施方式以下结合说明书附图和具体实施例来进一步说明本发明,但实施例并不对本发明做任何形式的限定。除非特别说明,本发明采用的试剂、方法和设备为本
技术领域:
常规试剂、方法和设备。除非特别说明,以下实施例所用试剂和材料均为市购。实施例1根据人类22条常染色体和y染色体的基因序列,针对720个均匀分布于基因组中的snp位点分别设计特异扩增引物(如表1所示,序列依次如seqidno.1~1440所示),适用范围广,且扩增子长度不超过140bp。该引物组检测的720个目标snp在个染色体上的分布(a)以及snp扩增子的长度分布(b)如图1所示。选择位于22条常染色体上的697个snp位点(a-snps)和y染色体上的23个snp位点(y-snps)并设计特异性引物。720个扩增子的长度非常集中,超过80%的长度为136-139bp,平均值为137bp,其中最短为124bp,最长为139bp。表1实施例2本实施具体以一孕12+5周孕妇进行血浆游离dna建库、测序以及父源snp等位基因的检测为例对本
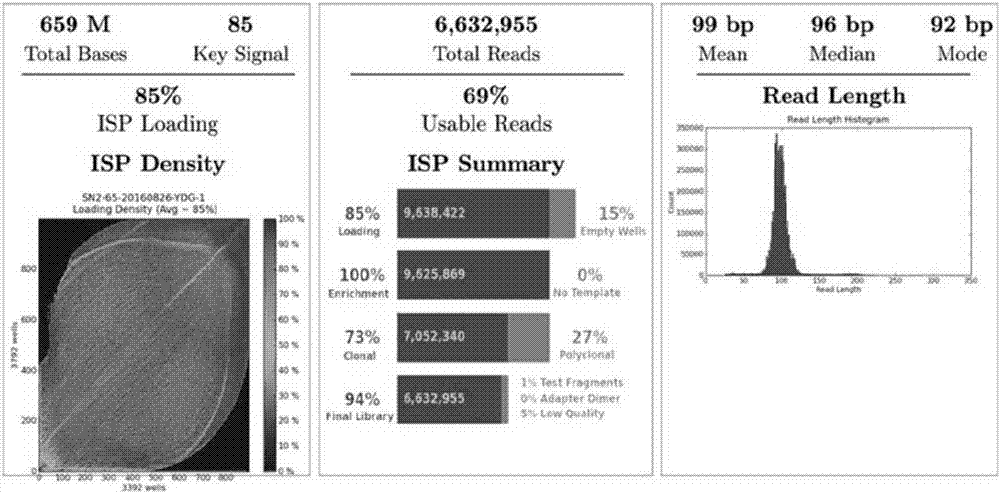
发明内容作详细说明,本发明所采用的基于高通量测序平台的游离dna建库、测序以及父源snp等位基因的检测方法包括以下步骤:1、样品的采集、处理和dna提取,为后续步骤的文库制备提供模板遵循“知情同意”原则在穿刺前抽取孕妇外周血5ml,存放于edta抗凝管内,8h内在4℃条件下,以1600g离心10min后,上清部分再以16000g离心10min收获血浆;沉淀血细胞部分10000g离心5min,吸弃残余上清部分。在无菌条件下通过b超介导收集胎儿绒毛组织,用磷酸盐缓冲液彻底冲洗,以除去母体血细胞。以上样本存放于-80℃保存。母血细胞使用qiaampdnabloodminikit(qiagen)提取;胎儿绒毛组织基因组dna使用qiaampdnaminikit(qiagen)提取。血浆游离dna提取使用采用mapurecirculatingdnaisolationkit(magen)。采用qubit2.0定量平台测定提取dna的浓度;采用安捷伦2100生物分析仪检测提取的游离dna片段长度分布情况。2、文库构建(1)采用ionampliseqtmlibrary2.0试剂盒(thermofisherscientific)和定制的720对snp引物进行超多重pcr复合扩增。体系如表2:表2试剂体积(μl)5×ionampliseqtmhifimix4.02×定制引物池10.0模板(gdna或cfdna)6.0总体积20.0(2)用pcr仪(abi9700)分别按以下程序扩增:扩增条件:酶激活99℃2min;99℃15s,60℃4min,19个循环(cfdna)或18个循环(gdna);冷却到10℃保存。(3)fupa酶消化多余的引物。在上一步pcr扩增产物中加入2μlfupa酶,总体积达22μl。用pcr仪(abi9700)分别按以下程序进行反应:反应条件:50℃10min,55℃10min,60℃20min,冷却到10℃保存。(4)采用ionxpresstmbarcodeadapters1-96试剂盒(thermofisherscientific),在片段两端分别连接有标签序列(barcode)的接头和公用接头。1)稀释barcode(1:4稀释),如表3:表3试剂体积ionp1adapter2μlionxpresstmbarcodex2μlnuclease-freewater4μl总体积8μl2)配置反应体系,如表4:表4试剂体积switchsolution4μl稀释好的barcode2μl步骤2.4.2的消化后产物22μl总体积28μl3)在上步反应体系中加入2μldnaligase,用pcr仪(abi9700)按以下程序进行反应:反应条件:22℃30min,72℃10min,冷却到10℃保存。3、纯化文库使用xp试剂盒(thermofisherscientific))对以上构建的文库进行纯化。4、文库定量采用ionlibraryquantitationkit试剂盒在7500实时定量pcr仪器上进行qpcr定量。1)稀释文库(1:1000稀释)。两步稀释法,先稀释10倍再稀释100倍。2)在冰盒里融化e.colidh10bioncontrollibrary和reagents,轻柔涡旋,短离心。3)稀释e.colidh10bioncontrollibrary,如表5:表5standardcontrollibrary体积水浓度(pmol)15μl(未稀释)45μl6.825μl(standard1)45μl0.6835μl(standard2)45μl0.0684)配置混合物(标准品+样品+空白对照),如表6:表65)在八联管中加入11μl步骤4配置的反应混合物。6)加入9μl的标准品或稀释的文库或水。7)短离心,去掉大的气泡。8)用7500实时定量pcr仪器按以下程序扩增:扩增条件:50℃2min;95℃20s;95℃3s,60℃32s,40个循环。5、模板制备和测序(1)模板制备1)稀释待测的文库。按照100pmol的浓度,将4μl文库与46μl去核酸酶水混合于同一1.5ml离心管,涡旋振荡5s,离心机轻甩2s。将稀释的文库置于冰上。2)配置反应体系,如表7。在室温下,取一个1.5ml离心管,按照下列剂量添加试剂。用移液器上下吹打混匀。表7试剂体积nuclease-freewater25μlionpgmtmtemplateot2200reagentmix500μlionpgmtmtemplateot2200pcrreagentb300μlionpgmtmtemplateot2200enzymemix50μl稀释的文库25μl合计900μl3)涡旋振荡上一步骤混合物5s,离心机轻甩2s。4)以最大速涡旋振荡ionpgmtmtemplateot2200ionspheretmparticles1min,使微珠重悬。离心机轻甩2s后用移液枪上下吹打,吸取100μl加入扩增反应液。5)涡旋振荡步骤4中配制的扩增反应溶液5s,必须在配好该溶液15min内进行iononetouch2仪进行微珠的扩增反应。6)充填ionpgmtmonetouchplus反应过滤器。并向反应滤器中加注onetouchtmreactionoil1.5ml,避免产生气泡。7)在iononetouch2仪器上安装充填好的ionpgmtmonetouchplus反应过滤器。上机运行任务,余按仪器提示要求操作。8)收集模板阳性的ionpgmtmtemplateot2200ionspheretm微珠。(2)富集模板阳性的isp微珠1)准备melt-off溶液,如表8:表82)清洗和重悬myonetmstreptavidinc1磁珠。涡旋震荡装有myonetmstreptavidinc1beads的试管30s,瞬时离心2s。吸取13μlmyonetmstreptavidinc1磁珠到一个新的1.5ml离心管中,放入dynamagtm-2磁力架上2min,小心移弃上清后加入130μlmyonetmbeadswashsolution,涡旋振荡30s,离心机轻甩2s备用。3)取出es八孔条(左方右圆放置),加样。如表9:表9孔号对应的试剂1模板阳性的isp微珠(100μl)2130μl重悬好的磁珠3300μliononetouchtm洗液4300μliononetouchtm洗液5300μliononetouchtm洗液6空白7300μl新鲜配置的melt-off溶液8空白4)按加样时的摆放位置将加样条靠右装到托盘槽中。5)更换新的加样枪头到加样臂上。6)取一个新的0.2mlpcr管,加入10μl中性溶液,插入加样枪头下方基座上,pcr管盖保持打开。7)运行iononetouchtmes仪器。(3)ionpgmtm测序采用ionpgmtmhi-qisequencing试剂盒(thermofisherscientific)在iontorrentpgmtm平台上测序。本实验采用ion316tm芯片(基因组dna样品)和ion318tm芯片(血浆游离dna样品)。6、数据分析测序数据使用iontorrentsuitetm4.6版本服务器(thermofisherscientific)进行分析,使用的参考基因为hg19,使用目标区域bed文件(custom-madeprimerpanel.designed.bed)定位感兴趣的目标区域,使用hotspotsbed文件(custom-madeprimerpanel.hotspot.bed)识别具体位点的突变。使用的分析插件有coverageanalysis插件v4.4.0.12和torrentvariantcaller4.6。7、实施案例分析结果通过以上步骤,获得母血细胞基因组dna、血浆游离dna以及相应胎儿基因组dna(试验参照)在目标snp位点中的测序数据。如图2所示,母血浆游离dna标本所在ion318tm芯片(每张318芯片检测4个血浆cfdna样品)测得总碱基数是659m,芯片loading率是85%,可用reads数是69%,有活性的微珠比例为100%,其中73%是单克隆模板,平均序列读长是99bp,结果提示游离dna建库成功。对于常染色体,选择最小覆盖度分别为100×(基因组dna样品)和1000×(血浆游离dna样品)的位点做进一步的分析;然后选择母血细胞分型为纯合子的snp位点,分析母血浆游离dna在相应位点中的测序数据,计算非母等位基因的百分比浓度(非母等位基因分型读数/该位点的测序总读数);以2%作为阈值,将浓度超过2%的非母等位基因定义为父源等位基因。结果显示,在实施例的游离dna中共有92个常染色体snp位点上的非母等位基因被定义为父源等位基因,从而推断出胎儿的91个常染色体snp分型。对于y染色体,由于母体dna中并没有y染色体,因此胎儿的y-snp序列可直接获取。最后,通过与相应胎儿基因组dna的分型结果的一致性比较,显示了通过母血浆对胎儿父源等位基因推断的准确性。具体地,该案例各样品测序结果如下表10所示,表中只展示了能体现父源等位基因的阳性位点。表10综上所述,本发明所提供的试剂盒可作为一种独立、有效的分析方法,解决了母血浆游离dna父源等位基因的准确分型鉴定问题,发挥了新一代测序技术在处理混合、降解(片段化)、微量检材中分型结果精确、高通量操作的优点,在无创性父权鉴定、多态性检测、基因频率调查等法医遗传学领域相关应用中受到高度重视。上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1