一种双喹啉二聚体盐衍生物及其制备方法和应用与流程
本发明涉及有机化合物,具体涉及双喹啉二聚体盐衍生物,以及所述化合物在以多倍体G-四链体为靶点的抗肿瘤药物中的应用。
背景技术:
G-四链体(G-qμadrμplex)是一种特殊的DNA二级结构。人类基因组中很多富含鸟嘌呤(G)区域具有形成这一结构的能力,包括端粒末端鸟嘌呤重复序列,以及多种基因的启动子区域,如c-kit、c-myc、c-myb、bcl-2、PDGF、kRAS、VEGF、Rb和胰岛素基因等。G-四链体结构的形成对于体内的一系列生理过程都存在调控作用。有研究表明,某些启动子区域的G-四链体结构会显著影响基因的转录和翻译水平,因此G-四链体结构被认为是起到分子开关的功能,其形成和拆散可能涉及到信号传导、细胞凋亡和细胞增殖等一系列体内重要的生理过程。所以在体内或者体外试验中,能够特异性地结合G-四链体结构或诱导G-四链体结构的形成,对于开发以G-四链体结构为靶点的抗癌药物具有非常重要的作用。
人端粒DNA是染色体末端由DNA重复序列TTAGGG组成的双螺旋区,其末端是含有100-200nt(核苷酸)的富G碱基的单链悬突,虽然它们大多数是趋向于形成单倍体G-四链体,但是仍有少数趋向于形成更复杂的由TTA碱基序列连接的双倍体或多倍体G-四链体结构。而且多倍体G-四链体的形成,仅出现在人端粒DNA和与渐冻人症(ALS)相关的r(GGGGCC)n的RNA重复序列中。近些年来,大部分研究集中于对不同构象的单倍体G-四链体的选择性结合和识别研究,而对双倍体或多倍体G-四链体结合剂的研究较少。因此设计一些小分子化合物,用于靶向识别不同生物功能中的G-四链体结构中的多倍体G-四链体,对于获得毒副作用更少的抗肿瘤药物具有更大的意义。
双喹啉是一类选择性结合单倍体G-四链体的配体。目前已报道了一系列的双喹啉衍生物,最早以360A为先导化合物,相继报道了3AQN、6AQN、PDS、PDF等8种双喹啉衍生物(J.Am.Chem.Soc.2007,129,1856-1857;J.Org.Chem.2012,77,229-242;Angew.Chem.Int.Ed.2014,53,999-1002;Bioorg.Med.Chem.Lett.2016,26,1660-1663;CN103204808A)。虽然该类双喹啉化合物均显示了优良的选择性结合单倍体G-四链体的作用,但选择性结合多倍体G-四链体的物质未见报道。
技术实现要素:
本发明所要解决的技术问题是提供一种双喹啉二聚体盐衍生物,该化合物与双倍体G-四链体平面的π-π堆积作用强,具有选择性结合和稳定双倍体G-四链体DNA的优良活性。
本发明的目的之一在于提供一种双喹啉二聚体盐衍生物。
本发明的另一目的在于提供上述双喹啉二聚体盐衍生物的制备方法。
本发明的再一目的在于提供上述双喹啉二聚体盐衍生物的应用。
本发明所采取的技术方案是:
一种双喹啉二聚体盐衍生物,该化合物的化学结构如下所示:
其中n为1、2或3,X为负一价阴离子。
进一步的,所述X选自F-、I-、Br-、Cl-或NO3-。
一种制备上述所述的双喹啉二聚体盐衍生物的方法,其特征在于,包括以下步骤:
1)化合物1的合成:将4-羟基吡啶-2,6-二甲酸、1-羟基苯并三氮唑、二环己基碳二酰亚胺在溶剂中混合反应完全,将产物过滤,取滤液,加入3-氨基喹啉,在催化剂作用下进行酰化反应,纯化产物,得化合物1:
2)化合物2的合成:将化合物1、化合物3在溶剂中混匀、反应完全,将反应产物纯化得化合物2:其中n为1、2或3;
所述化合物3为其中n为1、2或3,其中Ts表示对甲苯磺酰基;
3)双喹啉二聚体盐衍生物的合成:取化合物2进行甲基化反应,将甲基化反应产物分离纯化得上述任一项所述双喹啉二聚体盐衍生物。
进一步的,步骤1)中,所述4-羟基吡啶-2,6-二甲酸、1-羟基苯并三氮唑、二环己基碳二酰亚胺、3-氨基喹啉的摩尔用量比为1:2~6:4~6:1.5~2.5。
进一步的,步骤2)中,所述化合物1和化合物3的摩尔用量比为1:0.3~0.7。
进一步的,步骤1)中,所述纯化的具体操作为:将酰化反应产物加入水中,过滤,取滤渣,将滤渣用甲醇:氯仿体积比为(0:60)~(1.2:60)的洗脱液进行梯度洗脱,收集体积比为0.8~1.2:60的甲醇:氯仿洗脱液,将所得洗脱液除去甲醇和氯仿得到N,N’-双喹啉-2,6-二酰胺-4-羟基吡啶;
步骤2)中,所述纯化的具体操作为:将反应产物加入水中,过滤,取滤渣,将滤渣用体积比为(0:55)~(1:55)的甲醇:氯仿洗脱液进行梯度洗脱,收集体积比为0.8~1.2:55的甲醇:氯仿洗脱液,将所得洗脱液除去甲醇和氯仿得到化合物2;
步骤3)中,所述分离纯化的具体操作为:将反应产物中加入乙醚,减压抽滤得固体,洗涤、干燥,得到双喹啉二聚体盐衍生物。
进一步的,步骤3)中,所述甲基化反应用到的试剂为CH3I。
进一步的,步骤3)中,甲基化反应产物通过阴离子交换树脂得到含相应阴离子的双喹啉二聚体盐衍生物,所述阴离子为F-、Br-、Cl-或NO3-。
上述所述的双喹啉二聚体盐衍生物在特异性结合或/和稳定双倍体G-四链体结构中的应用。
上述所述的双喹啉二聚体盐衍生物在制备抗肿瘤药物中的应用。
本发明的有益效果是:
本发明所述的双喹啉二聚体盐衍生物中,本发明化合物π-π堆积G-四链体平面,相较于单倍体G-四链体DNA和双链DNA,本发明化合物具有优良的选择性结合和热力学稳定双倍体G-四链体DNA的能力。本发明所述的双喹啉二聚体盐衍生物还具有抗肿瘤作用。
附图说明
图1为未褪火的双倍体G-四链体DNA溶液(2.5μM)中含不同浓度的的双喹啉二聚体盐衍生物时的圆二色谱曲线图,图中,曲线依次表示所述双喹啉二聚体盐衍生物浓度为0、2.5μM、5.0μM、7.5μM和10.0μM的圆二色谱曲线,其中(a)为双喹啉二聚体盐衍生物I;(b)双喹啉二聚体盐衍生物II;(c)双喹啉二聚体盐衍生物III。
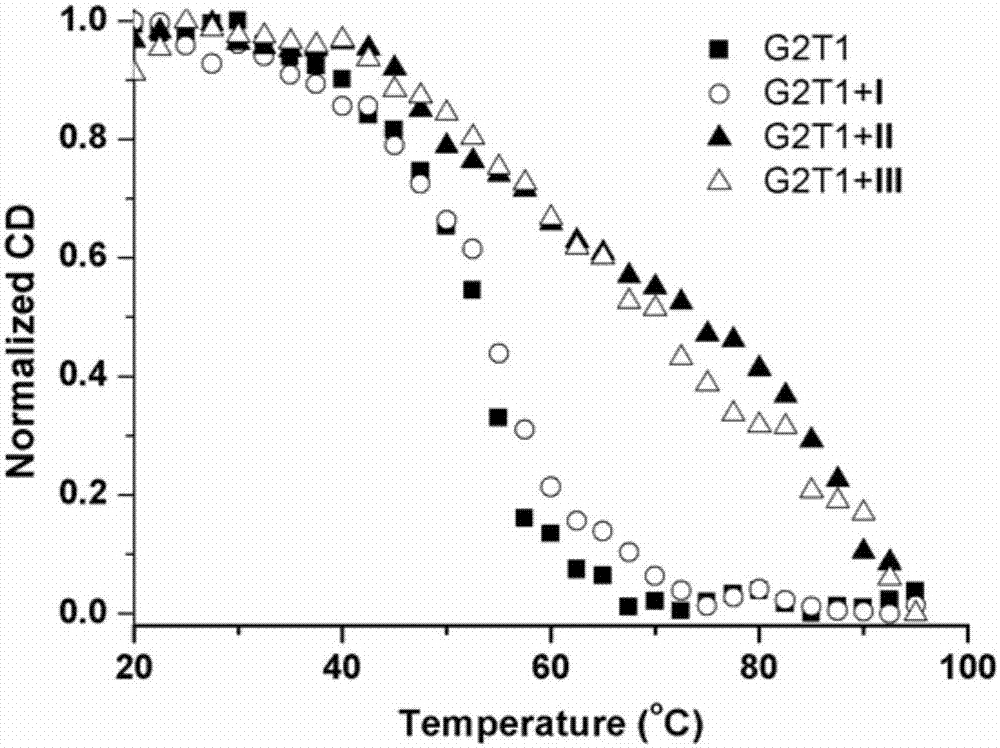
图2为反平行双倍体G-四链体DNA溶液(2.5μM)中含浓度为0和7.5μM的所述双喹啉二聚体盐衍生物时的圆二色谱与解链温度关系的曲线图,图中,图例■、○、▲和△所示曲线分别表示不含和含所述双喹啉二聚体盐衍生物I~III的圆二色谱与解链温度关系曲线。
图3为反平行单倍体G-四链体DNA溶液(5.0μM)中含浓度为0和7.5μM的所述双喹啉二聚体盐衍生物的圆二色谱与解链温度关系的曲线图,图中,图例■、○、▲和△所示曲线分别表示含和不含所述双喹啉二聚体盐衍生物I~III的圆二色谱与解链温度关系曲线。
图4为双链ds DNA溶液(5.0μM)中含浓度为0和15μM的所述双喹啉二聚体盐衍生物的圆二色谱与解链温度关系的曲线图,图中,图例■、○、▲和△所示曲线分别表示不含和含所述双喹啉二聚体盐衍生物I~III的圆二色谱与解链温度关系曲线。
图5为本发明所述双喹啉二聚体盐衍生物II与双倍体G-四链体DNA结合的紫外光谱图。
图6为本发明所述双喹啉二聚体盐衍生物II与单倍体G-四链体DNA结合的紫外光谱图。
图7为本发明所述双喹啉二聚体盐衍生物II与双链CT DNA结合的紫外光谱图。
图8为单倍体G-四链体DNA(G1)和双倍体G-四链体DNA(G2T1)的非变性聚丙烯酰胺凝胶电泳图,图中,泳道1~10依次分别为G1(16μM)、本发明所述双喹啉二聚体盐衍生物(24μM)+G1(16μM)、G2T1(8μM)、本发明所述双喹啉二聚体盐衍生物(24μM)+G2T1(8μM)、G1(16μM)+G2T1(8μM)、G1(16μM)+G2T1(8μM)+8μM本发明所述双喹啉二聚体盐衍生物、G1(16μM)+G2T1(8μM)+16μM本发明所述双喹啉二聚体盐衍生物、G1(16μM)+G2T1(8μM)+24μM本发明所述双喹啉二聚体盐衍生物、G1(16μM)+G2T1(8μM)+32μM本发明所述双喹啉二聚体盐衍生物、DNAmaker的电泳条带;图中G2T1+II表示双喹啉二聚体盐衍生物与双倍体G-四链体的结合体。
具体实施方式
一种双喹啉二聚体盐衍生物,该化合物的化学结构如下所示:
其中n为1、2或3,X为负一价阴离子。
优选的,所述X选自F-、I-、Br-、Cl-或NO3-。
一种制备上述所述的双喹啉二聚体盐衍生物的方法,包括以下步骤:
1)化合物1的合成:将4-羟基吡啶-2,6-二甲酸、1-羟基苯并三氮唑、二环己基碳二酰亚胺在溶剂中混合反应完全,将产物过滤,取滤液,加入3-氨基喹啉,在催化剂作用下进行酰化反应,纯化产物,得化合物1:
2)化合物2的合成:将化合物1、化合物3在溶剂中混匀、反应完全,将反应产物纯化得化合物2:其中n为1、2或3;
所述化合物3为其中n为1、2或3,其中Ts表示对甲苯磺酰基;
3)双喹啉二聚体盐衍生物的合成:取化合物2进行甲基化反应,将甲基化反应产物分离纯化得上述任一项所述双喹啉二聚体盐衍生物。
优选的,步骤1)中,所述4-羟基吡啶-2,6-二甲酸、1-羟基苯并三氮唑、二环己基碳二酰亚胺、3-氨基喹啉的摩尔用量比为1:2~6:4~6:1.5~2.5。
优选的,步骤1)中,所述溶剂选自N,N-二甲基甲酰胺、四氢呋喃和二甲基亚砜中的至少一种。
优选的,步骤1)中,所述催化剂选自4-二甲氨基吡啶、三乙胺和吡啶中的至少一种。
优选的,步骤1)中,所述纯化的具体操作为:将酰化反应产物加入水中,过滤,取滤渣,将滤渣用甲醇:氯仿体积比为(0:60)~(1.2:60)的洗脱液进行梯度洗脱,收集体积比为0.8~1.2:60的甲醇:氯仿洗脱液,将所得洗脱液除去甲醇和氯仿得到N,N’-双喹啉-2,6-二酰胺-4-羟基吡啶。
优选的,步骤2)中,所述化合物1和化合物3的摩尔用量比为1:0.3~0.7。
优选的,步骤2)中,反应温度为85~95℃,反应时间8~12h。
优选的,步骤2)中,所述溶剂选自N,N-二甲基甲酰胺、无水乙醇、丙酮和二甲基亚砜中的至少一种。
优选的,步骤2)中,反应体系中还含有碱,所述碱的摩尔用量为化合物1的0.8~1.2倍。
优选的,所述碱选自碳酸钾、碳酸钠、碳酸氢钠、氢氧化钠、氢氧化钾中的至少一种。
优选的,步骤2)中,所述纯化的具体操作为:将反应产物加入水中,过滤,取滤渣,将滤渣用积比为(0:55)~(1:55)的甲醇:氯仿洗脱液进行梯度洗脱,收集体积比为0.8~1.2:55的甲醇:氯仿洗脱液,将所得洗脱液除去甲醇和氯仿得到化合物2。
优选的,步骤3)中,所述甲基化反应用到的试剂为CH3I。
优选的,步骤3)中,甲基化反应产物通过阴离子交换树脂得到含相应阴离子的双喹啉二聚体盐衍生物,所述阴离子为F-、Br-、Cl-或NO3-。
优选的,步骤3)中,反应温度为35~45℃,反应时间20~28h。
优选的,步骤3)中,反应体系中还含有溶剂,所述溶剂选自N,N-二甲基甲酰胺和二甲基亚砜中的至少一种。
优选的,步骤3)中,所述分离纯化的具体操作为:将反应产物中加入乙醚,减压抽滤得固体,洗涤、干燥,得到双喹啉二聚体盐衍生物。
上述所述的双喹啉二聚体盐衍生物在特异性结合或/和稳定G-四链体结构中的应用。
优选的,所述的G-四链体DNA结构为双倍体G-四链体结构。
优选的,所述双倍体G-四链体结构为5’-A(GGGT TA)7G3-3’序列构成的双倍体G-四链体结构。
上述所述的双喹啉二聚体盐衍生物在制备抗肿瘤药物中的应用。
优选的,所述肿瘤包括宫颈癌细胞、肝癌、肺癌和乳腺癌。
下面结合实施例对本发明作进一步说明。
实施例1双喹啉二聚体盐衍生物I的合成
(1)化合物1的合成
取5mmol的4-羟基吡啶-2,6-二甲酸和20mmol的1-羟基苯并三氮唑,加入12mL的N,N-二甲基甲酰胺溶解,再加入30mmol的二环己基碳二酰亚胺,常温3h,过滤除去白色固体,得到棕色澄清滤液;取10mmol的3-氨基喹啉溶于3mL的N,N-二甲基甲酰胺和15mmol的4-二甲氨基吡啶(DMAP),然后加入到上述滤液中,常温下搅拌24h,将反应液滴加到150mL蒸馏水中析出沉淀,过滤,并将收集的固体物质装硅胶柱,以甲醇:氯仿为0:60~1:60体积比的洗脱液梯度洗脱,收集甲醇:氯仿为1:60体积比的洗脱液,除去溶剂得到696mg白色固体化合物,经鉴定该物质为化合物1:
上述化合物1的具体鉴定数据如下:
1H NMR(400MHz,DMSO-d6):δ=11.88(bs,1H),11.372(s,2H),9.37(d,J=1.2Hz,2H),8.99(d,J=1.2Hz,2H),8.07(s,2H),8.04(s,2H),7.81(s,2H),7.73(t,J=7.6Hz,2H),7.65(t,J=7.6Hz,2H).13C NMR(100MHz,DMSO-d6):δ=167.6,162.8,150.8,146.4,145.1,132.2,129.1,128.8,128.1,127.6,124.7,113.1.ESI-MS:m/z 434.58([M-H]+)and HR-MS for C54H40N10O7([M-H]+)Calcd:434.1248,found:434.1263.
(2)化合物2的合成
取0.5mmol化合物1,0.25mmol的化合物3其中n为1,0.5mmol无水碳酸钾,加入5mL的N,N-二甲基甲酰胺溶解,90℃搅拌反应10h,除溶剂,并将收集的固体物质装硅胶柱,以甲醇:氯仿=0:55~1:55体积比的洗脱液梯度洗脱,收集甲醇:氯仿为1:55体积比的洗脱液,除去溶剂得到126mg白色固体化合物,经鉴定该物质为化合物2:其中n为1。
上述化合物2的具体鉴定数据如下:
1H NMR(600MHz,CDCl3/CD3OD=2:1):δ=9.08(s,4H),8.86(s,4H),8.02(s,4H),7.95(d,J=8.4Hz,4H),7.78(d,J=8.4Hz,4H),7.64(t,J=8.4Hz,4H),7.65(t,J=8.4Hz,4H),4.38(s,4H),4.08(s,4H).13C NMR(150MHz,CDCl3/CD3OD=2:1):δ=172.0,166.8,154.5,148.6,148.4,135.5,132.8,132.1,131.8,131.3,129.9,129.9,116.4,73.7,72.3.ESI-MS:m/z 941.47([M-H]+)and HR-MS for C54H40N10O7([M-H]+)Calcd:941.3154,found:941.3151.
(3)双喹啉二聚体盐衍生物的合成
取0.05mmol的化合物2,加入1.0mL的N,N-二甲基甲酰胺,40℃搅拌溶解,再加入1.0mL碘甲烷,40℃搅拌反应24h,在反应液中加入8mL乙醚,减压抽滤得到黄色固体,乙醚洗涤3次后,将黄色固体再用20mL丙酮洗涤,干燥得到64mg淡黄色固体,经鉴定该物质为双喹啉二聚体盐衍生物I:其中n为1,X为I-。
上述化合物双喹啉二聚体盐衍生物I的具体鉴定数据如下:
1H NMR(400MHz,DMSO-d6):δ=11.59(s,4H),10.36(s,4H),9.42(s,4H),8.45(d,J=8.0Hz,4H),8.20(d,J=8.0Hz,4H),7.86(t,J=7.6Hz,4H),7.79(s,4H),7.77(t,J=7.6Hz,4H),4.73(s,12H),4.55(s,4H),4.01(s,4H).13C NMR(100MHz,DMSO-d6):δ=168.4,162.2,149.0,144.1,135.1,134.0,132.3,132.2,130.0,129.6,129.0,118.8,112.7,70.3,69.3,46.5.ESI-MS:m/z250.71([M]4+),376.33([M+I-]3+),627.51([M+2I-]2+)and HR-MS for C58H52I4N10O7([M+I-]3+)Calcd:375.7688,found:375.7684;([M+2I-]2+)Calcd:627.1055,found:627.1065.
实施例2双喹啉二聚体盐衍生物II的合成
方法同实施例1中合成双喹啉二聚体盐衍生物I的方法,本实施例中所用的化合物3为其中n为2,其他均与实施例1相同。得产物淡黄色固体,即为双喹啉二聚体盐衍生物II:其中n为2,X为I-。
上述双喹啉二聚体盐衍生物II的具体鉴定数据如下:
1H NMR(400MHz,DMSO-d6):δ=11.61(s,4H),10.34(s,4H),9.45(s,4H),8.45(d,J=8.0Hz,4H),8.22(d,J=8.0Hz,4H),7.89(t,J=8.0Hz,4H),7.80(t,J=8.0Hz,4H),7.75(s,4H),4.74(s,12H),4.46(s,4H),3.95(s,4H),3.78(s,4H)。13C NMR(100MHz,DMSO-d6):δ=168.1,162.1,149.3,144.2,135.2,134.0,132.6,132.2,130.1,129.7,129.0,118.8,112.2,70.8,69.3,68.8,46.5.ESI-MS:m/z 261.68([M]4+),m/z 391.02([M+I-]3+),m/z 649.51([M+2I-]2+);HR-MS for C60H56I4N10O8Calcd:390.4442([M+I-]3+),649.1186([M+2I-]2+),found:390.4438([M+I-]3+),649.1205([M+2I-]2+).
实施例3双喹啉二聚体盐衍生物III的合成
方法同实施例1中合成双喹啉二聚体盐衍生物I的方法,本实施例中所用的化合物3为其中n为3,其他均与实施例1相同。得产物淡黄色固体,即为双喹啉二聚体盐衍生物III:其中n为3,X为I-。
上述双喹啉二聚体盐衍生物III的具体鉴定数据如下:
1H NMR(400MHz,DMSO-d6)δ=11.61(s,4H),10.29(s,4H),9.48(s,4H),8.46(d,J=8.4Hz,4H),8.27(d,J=8.4Hz,4H),7.93(t,J=8.0Hz,4H),7.83(t,J=8.0Hz,4H),7.76(s,4H),4.74(s,12H),4.46(s,4H),3.98(s,4H),3.73(d,J=4.8Hz,4H),3.70(d,J=4.8Hz,4H).13C NMR(100MHz,DMSO-d6):δ=168.1,162.2,149.4,144.2,135.4,134.1,132.9,132.2,130.2,129.8,129.1,118.9,112.3,70.4,70.3,69.4,68.9,46.5.ESI-MS:m/z 272.71([M]4+),405.71([M+I-]3+),671.52([M+2I-]2+)and HR-MS for C62H60I4N10O9([M+I-]3+)Calcd:405.1196,found:405.1192;([M+2I-]2+)Calcd:671.1317,found:671.1320.
实施例4双喹啉二聚体盐衍生物的合成
将实施例1~3所得双喹啉二聚体盐衍生物I~III分别用阴离子交换树脂对其中的I-进行离子交换,从而制得被F-、Br-、Cl-或NO3-取代I-的双喹啉二聚体盐衍生物。
实施例5本发明双喹啉二聚体盐衍生物的活性检测
1、样品制备
DNA样品:DNA样品购自上海生物生工技术有限公司,将适量DNA溶于相应的缓冲溶液,95℃加热10min后缓慢降至室温,4℃孵育过夜,最后在SMA1000上测量260nm处的吸光度,根据朗伯比尔定律计算DNA的浓度。
DNA样品包括:
CT DNA:小牛胸腺DNA,为双链线性DNA;
ds DNA:5’-CAATCGGATCGAATTCGATCCGATTG-3’;
G1(单倍体G-四链体):5’-AGGG(TTAGGG)3-3’;
G2T1(双倍体G-四链体):5’-AGGG(TTAGGG)7-3’。
本发明双喹啉二聚体盐衍生物溶液的制备:
将实施例1~3所制备的双喹啉二聚体盐衍生物溶解在DMSO中得到母液,该母液中双喹啉二聚体盐衍生物的浓度为1.0mM,用DMSO溶液溶解,得到双喹啉二聚体盐衍生物溶液。
2、用CD光谱检测本发明所述双喹啉二聚体盐衍生物可否诱导形成双倍体G-四链体结构
将人端粒寡聚核苷酸G2T1溶于10mM Tris-HCl,pH 7.0缓冲溶液中,得到2.5μM的未褪火的G2T1溶液,在CD光谱仪上检测G2T1的CD光谱的变化,比色皿宽4mm,反应液为700μL,扫描范围为200-500nm;向含有2.5μM G2T1溶液中,分别不加和加入1.5μL、3.0μL、6.0μL和12.0μL的1mM双喹啉二聚体盐衍生物溶液,使双喹啉二聚体盐衍生物浓度分别为0、2.5μM、5.0μM、10.0μM和20.0μM,测定五种混合溶液的CD光谱,最后上述五种溶液的CD光谱图用Origin 8.0软件处理,实验结果如图1中的所示,其中(a)、(b)、(c)图分别为双喹啉二聚体盐衍生物I、II、III的检测结果。
由图1可以看出,随着双喹啉二聚体盐衍生物(I~III)浓度的不断增大,250nm单链DNA的CD信号峰逐渐降低,反平行双倍体G-四链体的特征CD信号峰(295nm处的正峰和265nm处的负峰)出现,说明双喹啉二聚体盐衍生物可诱导形成反平行双倍体G-四链体结构。
3、用CD-melting实验检验本发明双喹啉二聚体盐衍生物对双倍体G-四链体DNA的热稳定性
将寡聚核苷酸G2T1用10mM Tris-HCl和100mM NaCl(pH 7.0)的缓冲溶液稀释到100μM,95℃加热10min后缓慢降至室温,4℃孵育过夜。CD-melting实验中,缓冲液中含有300μL 2.5μM G2T1,采集20℃~95℃温度范围内295nm处的CD值,Origin8.0软件处理数据,求出G2T1DNA本身的熔点TDNA;向上述浓度的DNA溶液中加入22.5μL的100μM的双喹啉二聚体盐衍生物溶液,配制双喹啉二聚体盐衍生物浓度为7.5μM的G2T1混合溶液,采集溶液在20℃~95℃温度范围内295nm处的CD值,Origin 8.0软件处理数据,求出加入双喹啉二聚体盐衍生物后DNA的熔点Tm;根据TDNA和Tm的值,计算DNA熔解温度的变化值ΔTm=Tm-TDNA。
其实验结果如图2,双喹啉二聚体盐衍生物的加入,特别是双喹啉二聚体盐衍生物II和III的加入,ΔTm(Tm-TDNA)分别达到了20.5℃和17.1℃,可以判断本发明双喹啉二聚体盐衍生物对双倍体G-四链体DNA具优良的热稳定性。
4、用CD-melting实验检验本发明双喹啉二聚体盐衍生物对单倍体G-四链体DNA的热稳定性
将寡聚核苷酸G1溶于10mM Tris-HCl和100mM NaCl(pH 7.0)的缓冲溶液稀释到100μM,95℃加热10min后缓慢降至室温,4℃孵育过夜。CD-melting实验中,缓冲液中含有300μL 5.0μM的G1,采集20℃~95℃温度范围内295nm处的CD值,Origin8.0软件处理数据,求出G1-DNA本身的熔点TDNA;向上述浓度的DNA溶液中加入22.5μL的100μM的双喹啉二聚体盐衍生物溶液,配制含双喹啉二聚体盐衍生物浓度为7.5μM的G1混合溶液,采集溶液在20℃~95℃温度范围内295nm处的CD值,Origin 8.0软件处理数据,求出加入双喹啉二聚体盐衍生物后DNA的熔点Tm;根据TDNA和Tm的值,计算DNA熔解温度的变化值ΔTm=Tm-TDNA。
其实验结果如图3,双喹啉二聚体盐衍生物I~III加至G1溶液中,其ΔTm(Tm-TDNA)为-1.0℃、2.7℃和13.4℃。由ΔTm的大小,可以判断双喹啉二聚体盐衍生物对双倍体G-四链体DNA的热稳定性明显强于单倍体G-四链体DNA。
5、用CD-melting实验检验本发明双喹啉二聚体盐衍生物对双链DNA的热稳定性
将两条单链DNA溶于10mM Tris-HCl(pH 7.6)、50mM NaCl和1mM EDTA缓冲溶液中稀释至100μM,95℃加热10min后缓慢降至室温,4℃孵育过夜。CD-melting实验中,缓冲液中含有300μL 5.0μM的ds DNA,采集20℃~95℃温度范围内295nm处的CD值,Origin8.0软件处理数据,求出ds DNA本身的熔点TDNA;向上述浓度的DNA溶液中加入45μL的100μM的双喹啉二聚体盐衍生物溶液,配制含双喹啉二聚体盐衍生物浓度为15.0μM的ds DNA混合溶液,采集溶液在20℃~95℃温度范围内275nm处的CD值,Origin 8.0软件处理数据,求出加入双喹啉二聚体盐衍生物后DNA的熔点Tm;根据TDNA和Tm的值,计算DNA熔解温度的变化值ΔTm=Tm-TDNA。
其实验结果如图4,双喹啉二聚体盐衍生物I~III加至ds DNA溶液中,其ΔTm(Tm-TDNA)分别为2.1℃、0.3℃和0.3℃,该实验结果说明双喹啉二聚体盐衍生物对双链DNA无明显的热力学稳定性。结合图2~4的结果说明:双喹啉二聚体盐衍生物对双倍体G2T1的热稳定性明显强于单倍体G1和双链DNA。
6、紫外滴定法考察本发明双喹啉二聚体盐衍生物与双倍体G-四链体的结合能力
紫外滴定法测试使用了如下三种DNA序列:CT DNA,双链线性DNA;G1,单倍体G-四链体;G2T1,双倍体G-四链体。将人端粒寡聚核苷酸G1和G2T1溶于10mM Tris-HCl,pH 7.0和100mM NaCl缓冲溶液中,得到500μM的DNA溶液,95℃加热10min后缓慢降至室温,4℃孵育过夜。按需要配制500μM DNA溶液,该溶液作为滴定液。CT DNA溶液直接用10mM Tris-HCl,pH 7.0和100mM NaCl缓冲溶液配制成500μM。用对应的缓冲溶液配制30μM双喹啉二聚体盐衍生物溶液,此溶液作为紫外滴定法的测定溶液,固定化合物的浓度,不断加入500μM DNA的溶液,测试300-700nm范围内的吸收光谱,双喹啉二聚体盐衍生物与DNA的表观结合常数Ka根据公式(1)计算,
[DNA]/Δεap=[DNA]/Δε+1/(Δε×K) (1)
公式(1)中εa=Aobserved/[Complex],Δεap=[εa–εf],Δε=[εb–εf],εb是双喹啉二聚体盐衍生物结合DNA后的吸光系数,εf是化合物的吸光系数。以双喹啉二聚体盐衍生物II为例,说明DNA滴定化合物的紫外滴定情况,其结果如图5~7。
图5显示了在10mM Tris-HCl,pH 7.0和100mM NaCl缓冲溶液中,终浓度为0~10μM的双倍体G2T1对30μM双喹啉二聚体盐衍生物的紫外光谱的影响;图6显示了在10mM Tris-HCl,pH 7.0和100mM NaCl缓冲溶液中,终浓度为0~10μM的单倍体G1对30μM双喹啉二聚体盐衍生物溶液的紫外光谱的影响。图5和6分别显示双倍体G2T1和单倍体G1均使双喹啉二聚体盐衍生物在352nm处的吸收峰发生了明显的减色效应和6nm的红移,说明双喹啉二聚体盐衍生物与双倍体G2T1和单倍体G1发生了较强的π-π堆积作用。图7显示了在10mM Tris-HCl,pH 7.0和100mM NaCl缓冲溶液中,终浓度为0~10μM的CT DNA对30μM双喹啉二聚体盐衍生物溶液的紫外光谱的影响,CT DNA的加入使双喹啉二聚体盐衍生物在352nm处的吸收峰发生了明显的减色效应,但是没有发生峰的红移,说明所述的双喹啉二聚体盐衍生物与双链DNA主要是沟槽结合模式。双喹啉二聚体盐衍生物I和III对DNA的紫外滴定光谱,与双喹啉二聚体盐衍生物II相类似。
根据紫外光谱数据分析得到表观结合常数,其结果如下表1所示。对比研究发现:相对于单倍体G1和双链DNA,双喹啉二聚体盐衍生物,特别是双喹啉二聚体盐衍生物II~III对双倍体G-四链体DNA显示了更高的结合亲和力和选择性。
表1本发明双喹啉二聚体盐衍生物与DNA的键合常数Ka。
7、电泳法检测本发明双喹啉二聚体盐衍生物与双倍体G-四链体的特异性结合
以双喹啉二聚体盐衍生物II为例说明。将寡聚核苷酸G1和G2T1分别溶于10mM Tris-HCl和100mM NaCl(pH 7.0)的缓冲溶液稀释到60μM,95℃加热10min后缓慢降至室温,4℃孵育过夜;将1mM双喹啉二聚体盐衍生物溶液用上述缓冲溶液稀释到120μM。取一定量的60μM G1或G2T1溶液、120μM的双喹啉二聚体盐衍生物溶液及上述缓冲溶液混合,制备如下体积均为10μL的九种混合溶液:1号溶液,16μM G1;2号溶液,16μM G1和24μM双喹啉二聚体盐衍生物混合液;3号溶液,8μM G2T1;4号溶液,8μM G2T1和24μM双喹啉二聚体盐衍生物混合液;5号溶液,16μM G1和8μM G2T1混合液;6号溶液,16μM G1、8μM G2T1和8μM双喹啉二聚体盐衍生物混合液;7号溶液,16μM G1、8μM G2T1和16μM双喹啉二聚体盐衍生物混合液;8号溶液,16μM G1、8μM G2T1和24μM双喹啉二聚体盐衍生物混合液;9号溶液,16μM G1、8μM G2T1和32μM双喹啉二聚体盐衍生物混合液。然后将上述九种溶液在4℃反应3h,然后在15%非变性聚丙烯酰胺凝胶上,1×TBE缓冲液(pH 8.3)中电泳,最后用EB染色,拍照,其结果如图8。
如图8所示,对比条带1和2,双喹啉二聚体盐衍生物与单倍体G1混合后,并没有出现新的DNA条带,说明双喹啉二聚体盐衍生物与DNA没有形成稳定的化合物;对比条带3和4,双喹啉二聚体盐衍生物和双倍体G2T1混合后,在条带4中出现了一个泳动速度更快的新的条带,说明双喹啉二聚体盐衍生物与双倍体G2T1结合后,形成了结构更加紧密的新的化合物;条带5~9为不断增大双喹啉二聚体盐衍生物的浓度,单倍体G1和双倍体G2T1混合DNA溶液的条带的变化,由图说明即使单倍体和双倍体G-四链体DNA混合在一起,双喹啉二聚体盐衍生物也只是和双倍体G-四链体DNA结合,并且存在一定的浓度依赖关系,随着双喹啉二聚体盐衍生物浓度的增加,与双倍体G-四链体DNA的结合体G2T1+II的结合量越大。这些结果说明:双喹啉二聚体盐衍生物对双倍体G-四链体DNA具有特异性结合能力。
8、抗肿瘤活性
选择实施例1~3制备的化合物,采用MTT法(见文献C.-Q.Zhou,Y.-L.Lin,J.-W.Yang,J.-X.Chen,W.-H.Chen,Synthesis,DNA-cleaving and cytotoxicities of C2-symmetrical dipyrrole-polyamide dimer-based Cu(II)complexes:A comparative study,Eur.J.Med.Chem.2013,66:508-515),对四种肿瘤细胞Hela(宫颈癌细胞)、HepG2(肝癌)、A549(肺癌)和MCF7(乳腺癌)进行了抗肿瘤活性测试,其IC50值如表2所示。实验结果显示:实施例1~3制备的化合物具有抗肿瘤活性,对宫颈癌细胞、肝癌、肺癌和乳腺癌具有一定的治疗作用。
表2 双喹啉二聚体盐衍生物抗肿瘤活性的IC50值(48h)。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!