一类金属钴络合的聚合物催化剂及制备方法和应用与流程
本发明合成了金属钴络合高分子聚合物Co-Poly-O-(CH2)y-N+Bu3Br-,并以其作为催化剂在不需要加入任何溶剂和助催化剂的条件下实现了催化CO2与环氧烷烃反应合成相应的环状碳酸酯,且该高分子催化剂的可以多次重复使用。
背景技术:
CO2作为地球上最丰富的C1资源,具有储量丰富、安全无毒、廉价易得等诸多优点,同时,CO2也是最主要的温室气体之一,近年来,随着大气中CO2浓度的不断上升,全球温室效应不断增强,进而导致全球气候变暖,同时灾害性天气越发频繁,因此,如何较方便的处理和利用这些CO2已经变的尤为重要。
截止目前,对于CO2的处理手段,主要是吸附捕获和催化转化。也就是将其固定或者采用化学催化转化的方法转变成有机物,这些过程的高效实施,对我们人类社会的健康发展具有重大的意义。在化学催化转化领域,利用CO2与环状烷烃经过环加成反应合成环状碳酸酯是最主要的途径之一,通过这一途径将CO2转化为具有更高商业利用价值的有机化学品,但是此类反应过程中所使用的催化剂催化转化CO2的条件较为苛刻,其催化活性受到高温(>150℃)高压条件(>5.0MPa)以及需要加入共催化剂或者溶剂的限制,因此,寻找一类能在相对温和的条件下实现CO2的催化转化的高效催化剂是目前急待解决的问题。
技术实现要素:
为了实现在较温和的条件下,同时不需要加入任何共催化剂时催化转化CO2的愿望,本发明在之前研究的基础上,设计合成了一类金属钴络合的高分子聚合物催化剂,利用此催化剂在不需任何共催化剂的条件下,能够将CO2和环状烷烃催化转化为相应的环状碳酸酯;且利用此聚合物催化剂在高温高压条件下,可以较大的缩短生成环状碳酸酯的时间。
一、本发明钴络合聚合物催化剂的合成方法如下:
1.合成Salen:见专利一:201210135309.2和专利二:20121272056.3;
2.合成Salen-Co:见专利一:201210135309.2和专利二:201201272056.3;
3.合成Salen-Co-R1:见专利一:2012010135309.2和专利二:20121272056.3;
4.合成1,3,5-三溴-2-[(4-溴丁基)氧基]苯:
称取一定量的2,4,6-三溴苯酚和一定量的无水碳酸钾(2,4,6-三溴苯酚与碳酸钾的物质的量比为5:1)置于三颈烧瓶内,通惰性气体保护,用注射器加入干燥丙酮,搅拌5~10min,加入相应量的1,4-二溴丁烷(2,4,6-三溴苯酚与1,4-二溴丁烷的物质的量比为1:3),60℃搅拌3~4天,后处理得到目标化合物1,3,5-三溴-2-[(4-溴丁基)氧基]苯。
注:1,3,5-三溴-2-[(6-溴己基)氧基]苯和1,3,5-三溴-2-[(8-溴辛基)氧基]苯的合成方法与1,3,5-三溴-2-[(4-溴丁基)氧基]苯的合成方法一致。
5.合成2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯:
称取一定量的1,3,5-三溴-2-[(4-溴丁基)氧基]苯置于三颈烧瓶内,同时加入双(三苯基膦)二氯化钯和碘化亚铜做为催化剂,通惰性气体保护,用注射器加入干燥的三乙胺做溶剂,搅拌20~30min,加入相应量的三甲基硅乙炔(1,3,5-三溴-2-[(4-溴丁基)氧基]苯与三甲基硅乙炔的物质的量比为1:3~4),70~80℃回流24-36h,后处理之后得到中间产物[(2-(4-bromobut oxy)benzene-1,3,5-triyl)tris(ethyne-2,1-diyl)]tris(trimethylsilane),该中间产物用无水乙醇做溶剂,加入无水碳酸钾搅拌24h脱去硅炔基即可得到目标化合物2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯。
注:{2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯和2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯)的合成方法与2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯的合成方法一致。}
6.合成N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物:
称取一定量的2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯置于三颈烧瓶内,氯仿和乙腈作为溶剂(体积比为1:1),通惰性气体保护,用注射器加入相应量的三正丁胺(2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯与三正丁胺的物质的量比为1:1.5~2),70~80℃避光搅拌回流3~4天,后处理即可得到目标化合物N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物。
注:N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物和N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物)的合成方法与N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物的合成方法一致。
7.合成聚合物催化剂Co-CMP-O-(CH2)4-N+Bu3Br-:(以y=4为例)
称取一定量的Salen-Co-R1,然后加入相应量的1,3,5-三乙炔基苯(Salen-Co-R1与1,3,5-三乙炔基苯的物质的量比约为1:2~4),用CuI、四(三苯基磷钯)做催化剂,以上原料按量置于反应瓶内,通氩气保护,用注射器加入甲苯和三乙胺(甲苯与三乙胺 体积比约为3:1),先40℃搅拌40min~1h,然后升温至80~90℃,回流72~96h,反应完成后,冷却至室温,抽滤,依次用CH2Cl2,CH3OH,H2O,丙酮洗涤固体,索氏提取24~36h(提取液为CH2Cl2与CH3OH体积比为1:1的混合液),70℃真空干燥过夜即可得到聚合物催化剂Co-CMP-O-(CH2)4-N+Bu3Br-。
注:催化剂Co-CMP-O-(CH2)6-N+Bu3Br-和Co-CMP-O-(CH2)8-N+Bu3Br-的合成过程与Co-CMP-O-(CH2)4-N+Bu3Br-的合成过程一致。
二、经过以上七步所得到的聚合物催化剂Co-CMP-O-(CH2)y-N+Bu3Br-的结构如下:
X=乙二胺时,Co-Poly-O-(CH2)y-N+Bu3Br-:
X=1,2-环己二胺时,Co-Poly-O-(CH2)y-N+Bu3Br-:
X=联苯二胺时,Co-Poly-O-(CH2)y-N+Bu3Br-:
结构式中:R1=-OAc、-Cl、-Br或-I;R2=-H、-tBu、-iBu、-NO2,-Cl,-CH2NEt2或-CH2N(Bn)Et2Br;y=2~8。
本发明制备过程中的反应方程式如下:
反应方程式中:R1=-OAc、-Cl、-Br或-I;R2=-H、-tBu、-iBu、-NO2,-Cl,-CH2NEt2或-CH2N(Bn)Et2Br。
三、用所得高分子聚合物[Co-Poly-O-(CH2)y-N+Bu3Br-]催化环氧烷烃与CO2的反应:
上式中的反应过程不需要加入任何的溶剂或者助催化剂;环氧烷烃、Co-Poly-O-(CH2)y-N+Bu3Br-的物质的量比约为100~2000:1;式中R3=-H、-CH3、-CH2CH3、-CH2CH2Cl、-CH2CH2CH2CH3、-Ph或-CH2Ph等等;y=2~8。
本发明与现有技术相比的优点在于:本发明在25~120℃,0.1~6.0MPa以及无溶剂和无助催化剂条件下催化CO2与环状烷烃反应生成环状碳酸酯的聚合物催化剂以及该催化剂的制备方法,催化反应进行1~48h,得到的环状碳酸酯的产率为25~95%,且催化剂可以多次重复使用。
附图说明
图1. 1,3,5-三溴-2-[(4-溴丁基)氧基]苯的1H NMR;
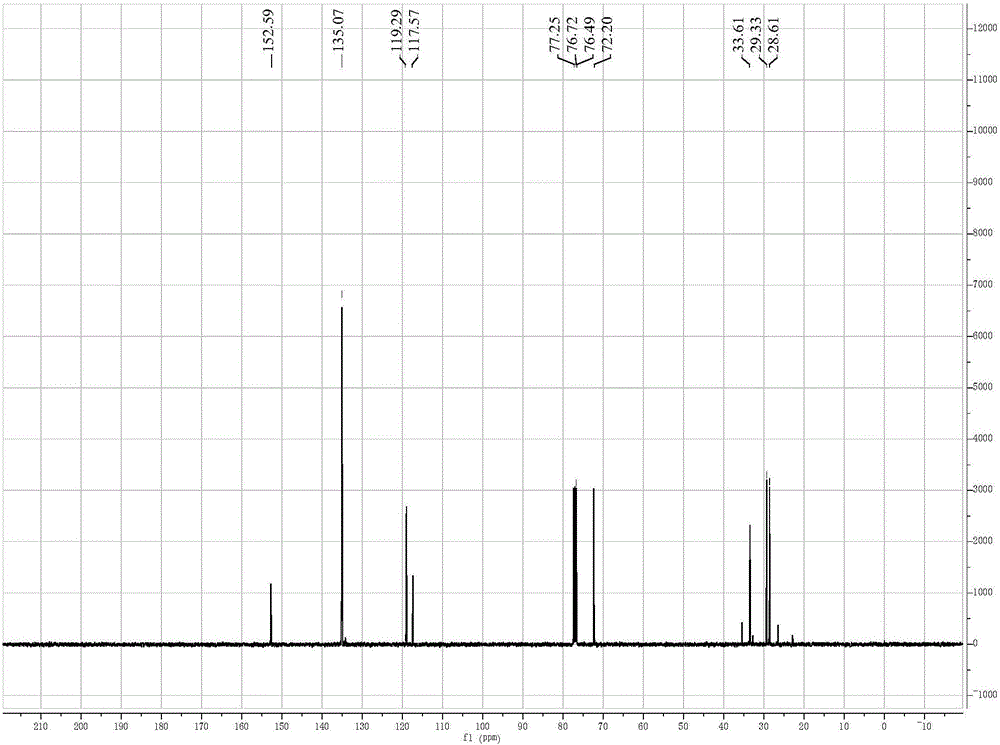
图2. 1,3,5-三溴-2-[(4-溴丁基)氧基]苯的13C NMR;
图3. 2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯的1H NMR;
图4. 2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯的13C NMR;
图5. N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物的1H NMR;
图6. N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物的13C NMR;
图7. Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)的FT-IR;
图8. 1,3,5-三溴-2-[(6-溴己基)氧基]苯的1H NMR;
图9. 1,3,5-三溴-2-[(6-溴己基)氧基]苯的13C NMR;
图10. 2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯的1H NMR;
图11. 2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯的13CNMR;
图12. N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物的1H NMR;
图13. N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物的13C NMR;
图14. Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)的FT-IR;
图15. Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和乙二胺所得,R2为H)的FT-IR;
图16. 1,3,5-三溴-2-[(8-溴辛基)氧基]苯的1H NMR;
图17. 1,3,5-三溴-2-[(8-溴辛基)氧基]苯的13C NMR;
图18. 2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯的1H NMR;
图19. 2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯的13C NMR;
图20. N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物的1H NMR;
图21. N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物的13C NMR;
图22. Co-poly-O-(CH2)8-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)的FT-IR。
具体实施方式
本发明技术方案不局限于以下所列举的具体实施方式,其中包括各具体实施方案间的任意组合。
实施例1:
1)、Salen的合成方法:将4.0mmol环己二胺(或乙二胺或苯二胺)溶于60mL无水乙醇中,用注射器加入苯环上具有R2取代基的水杨醛溶液(8.0mmol R2取代的水杨醛溶于10mL四氢呋喃),在氩气保护下,温度在70℃的条件下回流5h,制得所需的Salen化合物;
2)、Salen-Co的合成方法:将0.75mmol Salen溶于10mL干燥的无水甲苯中,用注射器加入醋酸钴的甲醇溶液(1mmol Co(OAc)2溶于10mL甲醇中),80℃回流5h,得到所需Salen-Co化合物;
3)、Salen-Co-R1的合成方法:将0.65mmol Salen-Co溶于6mL甲苯和18mL CH2Cl2的混合溶剂中,注射器加入6.5mmol的CH3COOH(或HCl或HBr或HI),氩气保护下,25℃搅拌5h,得到所需Salen-Co-R1化合物;
4)、1,3,5-三溴-2-[(4-溴丁基)氧基]苯的合成方法:将6.0mmol 2,4,6-三溴苯酚和30mmol K2CO3溶于30mL干燥丙酮,用注射器加入1,4-二溴丁烷溶液(18.0mmol 1,4-二溴丁烷溶于10.0mL干燥丙酮),氩气保护下,60℃搅拌48h,得到所需的1,3,5-三溴-2-[(4-溴丁基)氧基]苯化合物;1,3,5-三溴-2-[(4-溴丁基)氧基]苯的1H 13C NMR如图1、2所示;
5)、2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯的合成方法:将3.0mmol 1,3,5-三溴-2-[(4-溴丁基)氧基]苯,100mg Pd(PPh3)2Cl2和50mg CuI溶于90mL干燥的三乙胺,用注射器加入12.0mmol三甲基硅基乙炔,氩气保护下,70℃搅拌24h后,冷却至室温,后处理得中间产物,将该中间产物溶于20.0mL乙醇,加入碳酸钾溶液(130mg K2CO3溶于6.0mL蒸馏水),室温下搅拌24h,得到所需的2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯化合物;2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯的1H 13C NMR如图3、4所示;
6)、N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物的合成方法:将2.0mmol 2-[(4-溴丁基)氧基]-1,3,5-三乙炔基苯溶于5.0mL干燥的氯仿和5.0mL干燥的二氯甲烷,用注射器加入3.0mmol三正丁胺,氩气保护下,70℃避光搅拌72h,得到所需的N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物;N,N,N-三丁基-4-(2,4,6-三乙炔 基苯氧基)丁烷-1-铵溴化物的1H 13C NMR如图5、6所示;
7)、高分子聚合物Co-poly-O-(CH2)4-N+Bu3Br-的合成方法:0.28mmol的Salen-Co-R1,0.83mmol N,N,N-三丁基-4-(2,4,6-三乙炔基苯氧基)丁烷-1-铵溴化物,40mg CuI,100mg四(三苯基磷钯),用15mL甲苯和5mL三乙胺做溶剂,80℃回流72h,得到所需的Co-poly-O-(CH2)4-N+Bu3Br-化合物;Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)的FT-IR如图7、8所示;
8)、用Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为46.5%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为87.5%。
9)、用Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和乙二胺所得,R2为H)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为47.1%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为89.1%。
10)、用Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和邻苯二胺所得,R2为H)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为42.2%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为83.6%。
实施例2:
1)、Salen的合成方法:将3.0mmol环己二胺(或乙二胺或苯二胺)溶于50mL无水乙醇中,用注射器加入苯环上具有R2取代基的水杨醛溶液(6.0mmol R2取代的水杨醛溶于8mL四氢呋喃),在氩气保护下,温度在70℃的条件下回流5h,制得所需的Salen化合物;
2)、Salen-Co的合成方法:将0.8mmol Salen溶于10mL干燥的无水甲苯中,用注射器加入醋酸钴的甲醇溶液(1mmol Co(OAc)2溶于10mL甲醇中),80℃回流5h, 得到所需Salen-Co化合物;
3)、Salen-Co-R1的合成方法:将0.6mmol Salen-Co溶于6mL甲苯和18mL CH2Cl2的混合溶剂中,注射器加入6.0mmol的CH3COOH(或HCl或HBr或HI),氩气保护下,25℃搅拌5h,得到所需Salen-Co-R1化合物;
4)、1,3,5-三溴-2-[(6-溴己基)氧基]苯的合成方法:将6.0mmol 2,4,6-三溴苯酚和30mmol K2CO3溶于30mL干燥丙酮,用注射器加入1,6-二溴己烷溶液(18.0mmol 1,6-二溴己烷溶于10.0mL干燥丙酮),氩气保护下,60℃搅拌48h,得到所需的1,3,5-三溴-2-[(6-溴己基)氧基]苯化合物;1,3,5-三溴-2-[(6-溴己基)氧基]苯的1H 13C NMR如图9、10所示;
5)、2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯的合成方法:将3.0mmol 1,3,5-三溴-2-[(6-溴己基)氧基]苯,100mg Pd(PPh3)2Cl2和50mg CuI溶于90mL干燥的三乙胺,用注射器加入12.0mmol三甲基硅基乙炔,氩气保护下,70℃搅拌24h后,冷却至室温,后处理得中间产物,将该中间产物溶于20.0mL乙醇,加入碳酸钾溶液(130mg K2CO3溶于6.0mL蒸馏水),室温下搅拌24h,得到所需的2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯化合物;2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯的1H 13C NMR如图11、12所示;
6)、N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物的合成方法:将2.0mmol 2-[(6-溴己基)氧基]-1,3,5-三乙炔基苯溶于5.0mL干燥的氯仿和5.0mL干燥的二氯甲烷,用注射器加入3.0mmol三正丁胺,氩气保护下,70℃避光搅拌72h,得到所需的N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物;N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物的1H 13C NMR如图13、14所示;
7)、高分子聚合物Co-poly-O-(CH2)6-N+Bu3Br-的合成方法:0.3mmol的Salen-Co-R1,0.9mmol N,N,N-三丁基-6-(2,4,6-三乙炔基苯氧基)己烷-1-铵溴化物,50mg CuI,100mg四(三苯基磷钯),用15mL甲苯和5mL三乙胺做溶剂,80℃回流96h,得到所需的Co-poly-O-(CH2)6-N+Bu3Br-化合物;Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)的FT-IR如图8所示;Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和乙二胺所得,R2为H)的FT-IR如图15所示;
8)、用Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为44.6%;
②、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0 MPa,100℃下反应3h,得到碳酸丙烯酯的产率为88.7%。
9)、用Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和乙二胺所得,R2为H)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为58.5%;
②、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为97.1%;
③、184mg Co-poly-O-(CH2)6-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为62.8%;
④、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.57mL环氧氯丙烷,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为57.4%;
⑤、150mg Co-poly-O-(CH2)6-N+Bu3Br-,2.15mL1,2-环氧丁烷,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为54.1%;
⑥、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.51mL1,2-环氧己烷,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为46.2%;
⑦、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.41mL1,2-环氧-5-己烯,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为41.8%;
⑧、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.35mL缩水甘油基丙炔基醚,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为41.2%;
⑨、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.425mL苯基环氧乙烷,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为41.5%;
⑩、150mg Co-poly-O-(CH2)6-N+Bu3Br-,1.82mL1,2,7,8-环氧辛烷,CO2常压、常温反应48h,得到相应环状碳酸酯的产率为51.7%。
10)、用Co-poly-O-(CH2)6-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和邻苯二胺所得,R2为H)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为41.3%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为82.1%。
实施例3:
1)、Salen的合成方法:将4.5mmol环己二胺(或乙二胺或苯二胺)溶于70mL 无水乙醇中,用注射器加入苯环上具有R2取代基的水杨醛溶液(9.0mmol R2取代的水杨醛溶于15mL四氢呋喃),在氩气保护下,温度在70℃的条件下回流5h,制得所需的Salen化合物;
2)、Salen-Co的合成方法:将0.8mmol Salen溶于10mL干燥的无水甲苯中,用注射器加入醋酸钴的甲醇溶液(1mmol Co(OAc)2溶于10mL甲醇中),80℃回流5h,得到所需Salen-Co化合物;
3)、Salen-Co-R1的合成方法:将0.8mmol Salen-Co溶于6mL甲苯和18mL CH2Cl2的混合溶剂中,注射器加入8.0mmol的CH3COOH(或HCl或HBr或HI),氩气保护下,25℃搅拌5h,得到所需Salen-Co-R1化合物;
4)、1,3,5-三溴-2-[(8-溴辛基)氧基]苯的合成方法:将5.0mmol 2,4,6-三溴苯酚和25mmol K2CO3溶于30mL干燥丙酮,用注射器加入1,8-二溴辛烷溶液(18.0mmol 1,8-二溴辛烷溶于10.0mL干燥丙酮),氩气保护下,60℃搅拌60h,得到所需的1,3,5-三溴-2-[(8-溴辛基)氧基]苯化合物;1,3,5-三溴-2-[(8-溴辛基)氧基]苯的1H 13C NMR如图16、17所示;
5)、2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯的合成方法:将3.0mmol 1,3,5-三溴-2-[(8-溴辛基)氧基]苯,100mg Pd(PPh3)2Cl2和50mg CuI溶于90mL干燥的三乙胺,用注射器加入12.0mmol三甲基硅基乙炔,氩气保护下,70℃搅拌30h后,冷却至室温,后处理得中间产物,将该中间产物溶于20.0mL乙醇,加入碳酸钾溶液(145mg K2CO3溶于6.0mL蒸馏水),室温下搅拌24h,得到所需的2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯化合物;2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯的1H 13C NMR如图18、19所示;
6)、N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物的合成方法:将2.0mmol 2-[(8-溴辛基)氧基]-1,3,5-三乙炔基苯溶于5.0mL干燥的氯仿和5.0mL干燥的二氯甲烷,用注射器加入3.0mmol三正丁胺,氩气保护下,70℃避光搅拌96h,得到所需的N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物;N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物的1H 13C NMR如图20、21所示;
7)、高分子聚合物Co-poly-O-(CH2)8-N+Bu3Br-的合成方法:0.4mmol的Salen-Co-R1,1.2mmol N,N,N-三丁基-8-(2,4,6-三乙炔基苯氧基)辛烷-1-铵溴化物,50mg CuI,110mg四(三苯基磷钯),用18mL甲苯和6mL三乙胺做溶剂,80℃回流96h,得到所需的Co-poly-O-(CH2)8-N+Bu3Br-化合物;Co-poly-O-(CH2)8-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二胺所得,R2为叔丁基)的FT-IR如图22所示;
8)、用Co-poly-O-(CH2)8-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和环己二 胺所得,R2为叔丁基)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)8-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为38.5%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为80.6%。
9)、用Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和乙二胺所得,R2为H)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为43.1%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为84.6%。
10)、用Co-poly-O-(CH2)4-N+Bu3Br-(结构中Salen部分由R2取代水杨醛和邻苯二胺所得,R2为H)催化CO2与环氧烷烃反应:
①、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,CO2常压、常温反应48h,得到碳酸丙烯酯的产率为39.2%;
②、150mg Co-poly-O-(CH2)4-N+Bu3Br-,1.75mL环氧丙烷,二氧化碳压力为3.0MPa,100℃下反应3h,得到碳酸丙烯酯的产率为80.9%。
提供以上实施例仅仅是为了描述本发明的目的,而并非要限制本发明的范围。本发明的范围由所附权利要求限定。不脱离本发明的精神和原理而做出的各种等同替换和修改,均应涵盖在本发明的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!