一种杂多酸/氧化石墨烯复合物及其制备方法和应用与流程
本发明涉及环保材料技术领域,具体是一种杂多酸/氧化石墨烯复合物及其制备方法和应用。
背景技术:
印染废水对我们的饮用水和生态环境造成极大的危害,甚至人们的正常生活和生存环境也受到威胁,处理印染废水造成的污染成为人类的一大难题。目前染料的种类丰富多样,可大致分为三类:阳离子染料、阴离子染料、非离子染料。传统方法处理染料废水的效果并不理想,光催化法作为一种绿色、新兴、低能的处理废水的新方法,在过去数十年里越来越引起人们的关注。
多金属氧酸盐简称多酸,已有百余年的发展史,多年来,多酸化合物由于其活性高、反应条件温和、对设备腐蚀性小等优点作为无机化学中重要的研究课题得到了社会各界的广泛关注。1864年C. Marignac等人合成硅钨酸,1872年C.Scheibler等人合成了12-钨磷酸,为多金属氧酸盐开拓出了新的时代。多酸由于结构丰富、种类众多并具有氧化还原性和表面性质,是多功能环境友好型催化剂,具有很好的应用前景。多酸在催化研究方面已取得了巨大的研究成果。杂多酸催化剂在应用过程中,许多研究人员发现多金属氧酸盐存在比表面积小、溶解性好不利于回收等问题,以至于不利于其在应用方面的发展。在2004年,Geim教授发现了石墨烯的存在,并进一步证明二维晶体是可以稳定存在的,石墨烯具有比表面积大的特点,且在水溶液中的溶解度极低,便于将石墨烯与水溶液分离开。研究表明,石墨烯的物理和化学性能都非常不错,这使得它非常适合负载各种催化剂,现已制出多种石墨烯复合材料。所以,许多科研学者就尝试将具有良好化学性能的石墨烯与其掺杂,形成一种杂多酸盐与石墨烯掺杂的新型催化材料,在增大杂多酸催化剂比表面积的同时也提高了催化剂的循环利用效率。
相对于单一材料,二元复合材料能够集组分的优点使性能更加优越。因此,基于氧化石墨烯的大比表面积和杂多酸、聚苯胺独特的光电特性,设计合成的二元复合物材料用于光催化降解,是一种新的研究思路。作为新的研究课题,该复合材料在催化、电学材料和光学材料等方面潜力巨大,有待进一步研究,以开拓其应用。
技术实现要素:
本发明的目的在于提供一种杂多酸/氧化石墨烯复合物及其制备方法和应用,以解决上述背景技术中提出的问题。
为实现上述目的,本发明提供如下技术方案:
一种杂多酸/氧化石墨烯复合物的制备方法,包括以下步骤:
一、制备杂多酸:称取偏硅酸钠置入蒸馏水中制得混合液A,偏硅酸钠与蒸馏水的固液比为 8-15g:200mL;将钨酸钠与沸水混合,在搅拌条件下向沸腾溶液中缓慢滴加3-5mol/L的HCl 溶液,剧烈搅拌下使局部产生的钨酸沉淀溶解,然后迅速加入混合液A,向溶液中滴加5-7mol/L的HCl溶液;并保持pH值在5~6之间,加热沸腾0.8-1.2h,冷却至室温,再加入固体KCl,搅拌反应15-30min后抽滤,洗涤,制得杂多酸;其中,钨酸钠与沸水的固液比为2g:3mL;钨酸钠与3-5 mol/L的HCl溶液固液比为25g:15-25mL;钨酸钠与5-7mol/L的HCl溶液固液比为25g:2-6mL;钨酸钠与固体KCl的质量比为2-6:1;
二、将杂多酸溶解到蒸馏水中制得溶液A,将氧化石墨烯溶解到去离子水中制得质量体积浓度为1-3g/L的溶液B,将溶液A和溶液B分别超声0.3-0.8 h后混合并搅拌18-24h,干燥后即得杂多酸/氧化石墨烯复合物;其中杂多酸与氧化石墨烯的质量比为10-90:1。
作为本发明进一步的方案:步骤一中,偏硅酸钠与蒸馏水的固液比为11g:200mL。
作为本发明进一步的方案:钨酸钠与3-5 mol/L的HCl溶液固液比为25g:21mL;钨酸钠与5-7mol/L的HCl溶液固液比为25g:4mL;钨酸钠与固体KCl的质量比为4:1。
作为本发明进一步的方案:杂多酸与氧化石墨烯的质量比为50:1。
作为本发明进一步的方案:氧化石墨烯的制备步骤包括:
1)低温部分:取浓H2SO4与天然鳞片石墨混合,并在冰浴冷却的条件下搅拌5 min;之后缓慢地加入NaNO3,搅拌2 h,再慢慢地加入KMnO4并继续搅拌2 h,制得混合物料A;天然鳞片石墨与浓H2SO4的固液比为1g:20-30mL;天然鳞片石墨、NaNO3、KMnO4的质量比为1-3:1:4-8;
2)中温部分:将混合物料A在35℃的水浴中反应30 min;
3)高温部分:向混合物料A中缓慢加入去离子水,将水浴温度升高至95-100℃,再继续反应0.5 h;在不断搅拌中加入45-70℃的温水至溶液总体积达到体积的6-7倍,然后冷却至室温,之后再加入质量百分含量30%的H2O2,静置过夜;过滤取沉淀,将沉淀进行反复洗涤,直到上澄清液呈中性,离心,干燥得到氧化石墨烯;去离子水、浓H2SO4、H2O2的体积比为36-60:20-30:1。
作为本发明进一步的方案:天然鳞片石墨与浓H2SO4的固液比为1g:24mL;天然鳞片石墨、NaNO3、KMnO4的质量比为2:1:6。
作为本发明进一步的方案:去离子水、浓H2SO4、H2O2的体积比为36-60:24:1。
本发明另一目的是提供所述方法制得的杂多酸/氧化石墨烯复合物。
本发明另一目的是提供所述杂多酸/氧化石墨烯复合物在工业染料废水处理中的应用。
作为本发明进一步的方案:所述杂多酸/氧化石墨烯复合物用量为7.5mg/L。
与现有技术相比,本发明的有益效果是:
本发明以氧化石墨烯为载体,制备了β2-SiW11/GO,是将杂多化合物负载在载体上,不仅可以使比表面积大大提高、催化性能变好,还能提高其在应用中的可重复性、可回收性等。以甲基紫染料模拟工业废水来考察复合材料的性能。结果表明,本发明杂多酸/氧化石墨烯复合物的用量、染料溶液的初始浓度以及染料溶液的初始pH值对其降解率均有影响。本发明可以用于工业染料废水处理。
附图说明
图1是不同样品的红外光谱图;
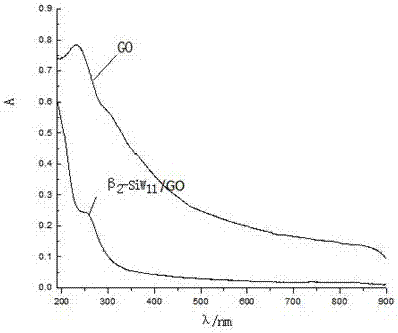
图2是不同样品的紫外漫反射光谱图;
图3是不同样品的X-射线衍射图;
图4是β2- SiW11/GO的TG-DTG曲线图;
图5是β2-SiW11/GO的扫描电镜图;
图6是β2-SiW11/GO的透射电镜谱图;
图7是甲基紫的紫外可见吸收光谱图;
图8是β2SiW11/GO的吸附-脱附结果图;
图9是20℃杂多酸/氧化石墨烯复合物对甲基紫的吸附等温曲线图;
图10是β2SiW11/GO用量对甲基紫的脱色率的影响结果图;
图11是pH对杂多酸/氧化石墨烯复合物降解效果的影响结果图。
具体实施方式
下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
一、杂多酸(β2-K8SiW11O39·nH2O,简记为β2SiW11)的合成
称取2.75 g Na2SiO3·nH2O,室温下置于 50 mL 蒸馏水中,制得混合液A,向 1 L 烧杯中加入50 g Na2WO4·2H2O,用 75 mL 沸水溶解,在磁力搅拌下向沸腾溶液中缓慢滴加 4 mol/L HCl 42 mL,剧烈搅拌下使局部产生的钨酸沉淀溶解,然后迅速加入混合液A,向溶液中滴加 8 mL 6 mol/L HCl溶液。并保持pH值在5~6之间,沸腾 1 h,冷却至室温。若溶液浑浊则需滤出不溶物,向滤液中加入 12.5 g 固体KCl,保持磁力搅拌,反应 20 min后抽滤,用 25 mL 1 mol/L KCl溶液洗涤两次,再用冷水洗涤,得到白色粉未,即得杂多酸,为β2-K8SiW11O39·nH2O,简记为β2SiW11。
二、氧化石墨烯的制备(简记为GO)
采用改进的Hummer法用天然鳞片石墨为原料制备氧化石墨烯,在制备过程中可分为三部分进行:首先低温部分,量取120 mL浓H2SO4倒进1000 mL的大烧杯中,再称取5 g天然鳞片石墨倒入大烧杯中,并在冰浴冷却的条件下电动搅拌5 min。之后缓慢地向体系中加入2.5 g的NaNO3,接着搅拌2 h,再向烧杯中慢慢地加入15.0 g的KMnO4并继续搅拌2 h,2 h后所得的溶液呈紫绿色。其次是中温部分,将烧杯转移到35℃的水浴中,在水浴中反应30 min。最后高温部分,在反应结束后,向大烧杯中缓慢加入230 mL的去离子水,将水浴温度升高至98℃左右,再继续反应0.5 h。反应结束后取出烧杯,进行电动搅拌,在不断搅拌中加入温水至800 mL刻度线,冷却至室温,之后再量取5 mL30%的H2O2加入到烧杯中,溶液呈土黄色,静置过夜。溶液中出现沉淀,将沉淀进行反复洗涤,直到上澄清液呈中性,之后经多次离心,干燥得到氧化石墨烯。
三、杂多酸/氧化石墨烯复合物(β2SiW11/GO)的合成
采用溶液共混法制备β2SiW11/GO:称取一定质量的β2SiW11溶解到150 mL的蒸馏水中制得溶液A,称取0.1 g的氧化石墨烯溶解到50 mL的去离子水中制得溶液B,将溶液A和溶液B分别超声0.5 h后混合,并搅拌20 h,干燥后即可得到成品β2SiW11/GO。分别称取质量为1.0 g、3.0 g、5.0 g、7.0 g、9.0 g的β2SiW11与0.1 g的氧化石墨烯进行上述步骤,即可制取配比为1:0.1、3:0.1、5:0.1、7:0.1、9:0.1的β2SiW11/GO纳米复合材料。
通过红外光谱、紫外光谱、X-射线衍射等手段对制备的杂多酸(β2SiW11)、氧化石墨烯(GO)、杂多酸/氧化石墨烯复合物(β2SiW11/GO)进行表征。结果如下所述。
1.红外光谱分析
图1为GO、β2SiW11/GO的红外光谱图,从GO的红外光谱图可知,在3000~3700 cm-1处出现归属于OH-的伸缩振动峰,其吸收峰较宽、较强;1634.83 cm-1处是OH-基团的振动吸收峰,说明有水分子存在,这与氧化石墨不能被完全干燥吻合。
β2SiW11/GO中β2-SiW11位于994,950,888,798,735 cm-1的吸收峰分别对应于Si-Oa,W=Od,W-Ob-W和W-Oc-W的振动,表明Keggin结构的存在。与纯β2-SiW11相比,杂多酸/氧化石墨烯复合物中W=Od键发生红移,而两种W-O-W键均发生蓝移,这与W=Od和GO片层(W=Od…C=C)之间的共轭作用有关,从而说明GO和β2-SiW11之间不是简单地混合,而是存在相互作用。
2、紫外-可见吸收光谱
图2是GO、β2SiW11/GO的紫外-可见光谱曲线,杂多酸/氧化石墨烯复合物结构可通过紫外光谱进行分析。谱图中GO结构的C-C共轭特征吸收峰出现于232 nm。β2SiW11/GO中由Od→W以及Ob/Oc→W荷移跃迁产生的杂多酸特征峰分别出现在192 nm和255 nm,因此杂多酸和氧化石墨烯负载成功。
3、X-射线衍射分析
从图3中可以看出,GO单体的衍射峰强且分布较窄。GO的特征峰位于2θ=11.1 °,根据布拉格方程2dsinθ=nλ计算得知,GO的层间距约为7.5 Å。β2SiW11/GO的衍射峰位于2θ=13.4 o,层间距=6.5 Å,缩小1 Å,说明GO和β2-SiW11负载成功,产生键能导致其层间距缩小。从该谱图中可以观察到β2-SiW11的特征峰,进而说明β2-SiW11粒子已经很好的掺杂在GO片层中。
4、热稳定性能分析
本实验使用SII 型的Pryis Diamond热分析仪(美国PE公司的),升温速率为10 ℃/min,在氮气的保护下对复合材料进行TG-DTA分析,结果如图4。
由图4可知,β2-SiW11/GO在20~1000 ℃范围内的失重分为三个部分。20~120 ℃为第一步失重,此时较快失去的是少量吸附水和结晶水,失重率约为8.33 %。在120~140 ℃之间出现平台,此时样品质量基本保持不变;第二阶段失重范围在160~650 ℃之间,此阶段在失去质子化水的同时,氧化石墨烯开始分解,失重约30.83 %,DTA曲线在187 ℃有一分解放热峰;第三阶段失重的温度范围在850~1000 ℃之间,失重约12.40 %,950 ℃分解放热峰碳骨架杂多酸完全分解。
5、SEM-TEM分析
图5为氧化石墨烯掺杂材料的SEM图片。可以看到,在许多层状材料的表面有微小颗粒均匀的分布。推测这种小颗粒为β2-SiW11,而氧化石墨烯则呈现的是片层结构,β2-SiW11均匀分散在GO各片层之间,其与GO间的相互作用阻止了GO的各片层的聚集。
图6中可以看到多酸粒子均匀地分散在氧化石墨烯片层中间,没有团聚现象发生,并且氧化石墨烯依然保存着层状结构。
6、β2SiW11/GO吸附甲基紫
(1)甲基紫的最大吸收波长
配制一定浓度的甲基紫溶液,用分光光度计在190 nm-900 nm内进行扫描,如图7。由图7可知,在595 nm处出现最高吸收峰,所以下面实验均在此处测定。
(2)复合材料对甲基紫的吸附平衡时间测定
50 mL 75 mg/L该溶液于烧杯中,称5.0 mg配比为5:0.1的β2SiW11/GO加入到染料溶液中,超声3~5 min后开始避光,每隔10 min测定吸光度,绘制β2SiW11/GO的吸附量-时间曲线(如图8)。
由图8可知,一开始随着反应时间的增加,吸附率增加,而到30 min时吸附率达到最大,而后随着时间的增加,吸附率不再增大。因此,下面的实验均先避光30 min再进行其他的操作步骤。
(3) β2SiW11/GO对甲基紫的吸附等温线
配制浓度为25 mg/L的甲基紫溶液,测量初始吸光度A0,取5份50 ml该溶液,并编号1、2、3、4、5,分别称取5.0 mg配比为1:0.1、3:0.1、5:0.1、7:0.1和9:0.1的β2SiW11/GO于盛有染料的烧杯中,超声3~5 min后避光30 min,测定吸光度。分别配制50、75、100、125和150 mg/L的甲基紫溶液,重复上述步骤,制作吸附等温曲线(见图9)。
由图9中可知,当甲基紫溶液浓度为75 mg/L,β2SiW11/GO的配比为5:0.1时,复合材料的吸附率最高为97.63 %,吸附量可达732.23 mg/g,染料溶液的脱色率达到90.98 %。因此,选择该条件进行下面的吸附试验。
(4)β2SiW11/GO的用量对甲基紫吸附量的影响
50 mL 75 mg/L该溶液测定初始吸光度。分别投加2.5、5.0、7.5、10.0、12.5 和15.0 mg的β2SiW11/GO,避光30 min后离心,测吸光度,记录数据。处理后得出吸附活性曲线,如图10所示。
从图10可以看出,β2SiW11/GO的用量为2.5 mg~5.0 mg时,脱色率持续增加,这是由于用量的增加使杂多酸/氧化石墨烯复合物氧化反应的活化位也增加;当β2SiW11/GO的用量大于5.0 mg时,脱色率开始降低,与杂多酸/氧化石墨烯复合物本身有颜色,过多的用量影响到吸光度的测定有关。当β2SiW11/GO的用量为5.0 mg时,吸附率达到最高值,为94.76 %,脱色率可达到79.41 %,此时的吸附量也是最高的,可达710.73 mg/g。所以选择该条件进行下面的试验。
(5)溶液酸度对β2SiW11/GO吸附甲基紫的影响
配制浓度75 mg/l的甲基紫溶液,量取6份50 mL该溶液,用HCl和NaOH溶液调节pH值,分别为1、3、5、7、9、11,并编号,测定吸光度。分别加入5.0 mg配比为5:0.1的β2SiW11/GO,闭光30 min后离心,测吸光度。绘制吸附曲线(图11)。
由图11可以看出,在pH=5左右的条件下,配比为5:0.1的β2SiW11/GO吸附效果最好,吸附率最高为97.68 %,吸附量达到731.53 mg/g,且此时的酸度最接近原始染料溶液的pH,有较好的价值,因此在后续的实验中,都将染料溶液调到pH=5。
(6)正交实验
根据考察单因素吸附实验的信息,采用L9 (33) 正交实验表优化吸附反应条件。实验水平和因素见表1。该吸附实验在常温条件下进行,结果见表3.8。从极差R的数据可以看出,杂多酸/氧化石墨烯复合物用量对β2SiW11/GO吸附甲基紫的吸附率影响最大,其大小顺序依次为:杂多酸/氧化石墨烯复合物用量>溶液的pH值>染料的浓度。从表2均值K的数据可以分析出优化的吸附反应条件为:杂多酸/氧化石墨烯复合物用量为7.5 mg,溶液的pH值为5,染料的浓度为100 mg/L。
表1 实验水平和因素表
表2 正交实验表
对于本领域技术人员而言,显然本发明不限于上述示范性实施例的细节,而且在不背离本发明的精神或基本特征的情况下,能够以其他的具体形式实现本发明。因此,无论从哪一点来看,均应将实施例看作是示范性的,而且是非限制性的,本发明的范围由所附权利要求而不是上述说明限定,因此旨在将落在权利要求的等同要件的含义和范围内的所有变化囊括在本发明内。
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种纳米银/氧化石墨烯复合材料分散液及其制备方法和应用与制造工艺
- 四氧化三钴/石墨烯复合材料(Co3O4/N‑RGO)的制备方法及应用与制造工艺
- 一种添加纳米氧铁体石墨烯复合材料的氯磺化聚乙烯防腐涂料的制造方法与工艺
- 磁性四氧化三铁/石墨烯复合材料的制备及其在制备磁性油漆中的应用的制造方法与工艺
- 一种利用掺氮氧化石墨烯/TiO2复合颗粒增强抗污染性的超滤膜的制备方法与制造工艺
- 一种制备聚合物/还原氧化石墨烯复合材料的方法与制造工艺
- 一种氧化石墨烯‑喹诺酮复合材料的制造方法与工艺
- 基于微波还原剥离氧化石墨烯或其复合物的高效催化宏量制备方法与制造工艺
- 一种聚丙烯接枝氧化石墨烯复合材料的制备方法
- 一种氧化石墨烯改性热塑性淀粉复合材料及其制备方法