一种用于癫痫预测的生物标志物的制作方法
本发明涉及疾病诊断及预测的生物标志物领域。特别地,本发明涉及以Hemoglobinsubunitalpha蛋白及其生物降解产物作为生物标志物在癫痫预测、诊断、治疗及预后评估中的用途和蛋白组学筛选及检测方法。还涉及Hemoglobinsubunitalpha蛋白或其生物降解产物在制作癫痫检测试剂盒中的应用。
背景技术:
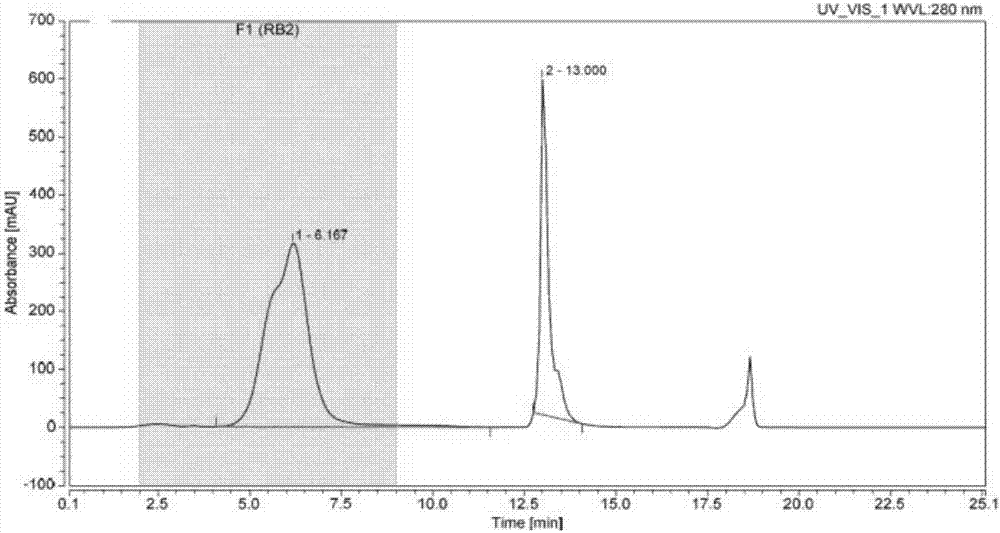
:癫痫是急性脑功能失常的综合征,是由大脑神经元异常同步化的放电导致的。据流行病学统计,目前,癫痫影响全球约1%的人口,发病率仅次于神经血管性疾病的病种。根据我国最新流行病学显示,我国的癫痫发病率为7‰-1%。癫痫对患者的神经功能影响极其严重,对于生长发育早期的婴幼儿甚至是灾难性的。在人出生后的3年里是人类神经系统发育的黄金时期,在这个时期里,神经系统要逐步形成正常的神经网络以逐步实现例如:运动、言语、记忆、理解力等功能,而由于癫痫的反复发作,导致患儿的神经系统无法建立正常的联系,继而出现神经运动功能发育迟滞,严重影响患儿的预后,及未来的生活。而对于成年人,癫痫对神经功能的影响也是不可小视的,由于反复的癫痫发作,导致患者出现记忆力下降,认知能力下降,精神障碍等,患者无法正常工作、生活、学习,给患者造成了非常严重的精神负担。因此,无论对于患者,还是对于家人来说,癫痫均已成为一种严重的经济及社会负担。能够在癫痫形成的早期进行诊断,并尽早干预,对于患者神经功能改善以及预后均有较大帮助。目前,癫痫的治疗主要有三种方式,药物,手术以及神经调控治疗三种,70%的患者仍以药物治疗为主,但是仍有约1/3的患者对药物治疗无效,这类对药物治疗无效的癫痫被称为药物难治性癫痫。依据比较流行的诊断标准,药物难治性癫痫的诊断依据主要是,口服2种或2种以上适宜的抗癫痫药物治疗二年,平均每个月的癫痫发作日大于或等于一天。临床上,较为常见的药物难治性癫痫包括:颞叶癫痫,外伤、肿瘤、出血等因素继发的癫痫等,而颞叶癫痫在药物难治性癫痫中占的比例约50%,药物难治性癫痫在治疗上可以选择包括切除性手术、姑息性手术、神经调控手术等治疗方法。在临床上,对于不同的难治性癫痫患者,需要依据脑电图、影像学、发作期症状学、脑功能损伤情况等综合判断选择何种手术治疗的方式,但治疗预后却有很大差异。有时,同为一类型的癫痫,比如:颞叶内侧型癫痫,采取同样的手术方法(海马杏仁核颞叶切除),一部分患者治疗效果满意,但仍有一部分患者术后仍然会出现癫痫发作症状。且切除性手术本身由于在切除病灶的过程中需要切除部分正常脑组织,故在术后难免会出现神经功能缺损。更重要的是手术的机会可能只有一次。因此,寻找决定治疗效果差异的因素是必要以及迫切的,以便以差异因素为依据选择最佳手术方案,并预测手术治疗的效果,从而避免难以恢复的神经功能损伤。目前,临床上对于癫痫的治疗,仍然没有有效的预测手段和方法。此外,药物难治性癫痫手术治疗以后,一般情况下,需要继续口服抗癫痫药物治疗至少2年,之后依据患者的预后情况,以及发作情况综合判断是否能够减停药物。但是在临床上,长期口服抗癫痫药物所带来的副作用,如:肥胖、精神症状、肝肾功能损伤等情况以及经济因素是临床医生公认的事实,因此,手术后尽量缩短抗癫痫药物的服用期,对于减轻上述副作用的影响非常重要。目前,临床上仍然没有一种针对上述问题的血清或脑脊液的预测、诊断、治疗以及预后评估的方法和试剂盒产品。本发明依据蛋白质组学的技术,通过对药物难治性癫痫患者血清的研究,研究发现了较为稳定的可以作为癫痫疾病生物标志物的蛋白或其生物降解产物,在临床上具有较为广阔的应用前景。技术实现要素:本发明采用蛋白质组学的方法,以药物难治性癫痫患者的血清为研究对象,发现了较为稳定的生物标志物,其为Hemoglobinsubunitalpha蛋白或其生物降解产物,编码基因为HBA1。该生物标志物在药物难治性癫痫患者,尤其是颞叶癫痫患者术前血清中有稳定的高表达,但是在手术后不同时间节点随访时采集的血清中表达量明显下降,这一结果提供了一种新的癫痫预测、诊断、治疗以及预后评估的思路和方法。因此,本发明涉及一种用于癫痫预测、诊断、治疗以及预后评估的生物标志物,其为编码基因HBA1的Hemoglobinsubunitalpha蛋白或其生物降解产物。其氨基酸序列如序列表SEQIDNo.1所示。第一方面,本发明提供了所述生物标志物的筛选和检测方法,其包括在生物样本中,应用蛋白质组学的技术进行筛选和检测。进一步地,所述生物样本为体液或组织,优选来自血清或脑脊液的样本。进一步地,其中所述蛋白质组学的技术包括:样本制备,高效液相色谱(HPLC)去除高丰度蛋白,样本的酶切、脱盐、标记,高效液相色谱(HPLC)肽段分离,质谱(MS)检测、分析等。在第二方面,所述蛋白或其生物降解产物在制备用于癫痫预测、诊断、治疗以及预后评估的生物标志物中的用途。进一步地,本发明涉及的生物标志物,Hemoglobinsubunitalpha蛋白或其生物降解产物,可作为癫痫神经元兴奋性的指标。进一步地,本发明涉及的生物标志物,Hemoglobinsubunitalpha蛋白或其生物降解产物,其可用于药物难治性癫痫的预测及分型诊断,如区分颞叶癫痫与额叶癫痫等。进一步地,本发明涉及的生物标志物,Hemoglobinsubunitalpha蛋白或其生物降解产物,可用于药物难治性癫痫术后的预后评估,以及减少药量或停药(减停药物)的指标。在第三方面,本发明涉及一种Hemoglobinsubunitalpha蛋白或其生物降解产物的筛查和检测系统,其包括检测受试者的体液或组织中Hemoglobinsubunitalpha蛋白或其生物降解产物的表达,所述体液或组织优选来自血清或脑脊液的样本。进一步地,所述的筛查和检测系统,包括本专利所述的蛋白或其生物降解产物单独应用或与其它生物标志物在癫痫疾病筛查检测中的联合应用。在第四方面,所述生物标志物在制备用于癫痫预测、诊断、治疗以及预后评估的试剂盒中的应用。进一步地,所述的试剂盒包括编码基因为HBA1的Hemoglobinsubunitalpha蛋白或其生物降解产物的抗体。本发明所检测到的Hemoglobinsubunitalpha蛋白或其生物降解产物是通过蛋白质组学的方法,在药物难治性癫痫患者血清中发现的,其在所检测的不同患者样本手术前后的变化具有高度的一致性和稳定性,可以作为一种药物难治性癫痫的生物标志物,可用于包括评估癫痫疾病状态,即癫痫神经元兴奋性,药物难治性癫痫的分型诊断,药物难治性癫痫术后减停药物依据等方面。然而,本发明的方法及生物标志物用途不仅仅限于上述的几个方面。关于本发明中术语的描述,若与本领域公知的描述不同,应以本申请中的描述为准。附图说明图1本发明的蛋白质组学技术实验流程图;图2高效液相色谱(HPLC)分离高丰度蛋白的液相图;图3高效液相色谱(HPLC)肽段分离的液相图;图4HBA1肽段的质谱(MS)定量图;图5筛选实验高效液相色谱(HPLC)去除高丰度蛋白峰面积;图6验证实验9组样本高效液相色谱(HPLC)去除高丰度蛋白峰面积平均值;图7HBA1标准肽段定量标准曲线。具体实施方式下面结合具体实施方式对本发明做进一步说明,所述的实施方式是对本发明的解释而不是限定。实施方式11.样本采集临床上诊断为药物难治性癫痫患者共6例,以及非癫痫患者空白对照1例(表1),难治性癫痫患者均为颞叶癫痫,均进行同样的外科治疗:前颞叶加海马杏仁核切除术。术后进行随访。随访期间,通过脑电图及临床发作情况的验证,这6例患者均符合临床治愈的标准。按照不同的时间节点采集患者的外周静脉血或动脉血,时间点分别为:术前、术后随访半年、术后随访一年。每次抽取外周血5ml,以4000rpm/min离心20分钟,之后取上清(血清),-80℃保存。表1.临床样本基本情况I号病例为筛选实验样本,II-VI号病例为验证实验及定量实验样本,VII号血清为非癫痫患者空白对照组,用于配制梯度浓度标准肽,制作定量标准曲线。2.实验技术流程(图1)-筛选实验2.1.样本制备(1)将I号病例的术前血清“I-PRE”,和术后半年血清“I-POST-HALF”,取出后室温解冻,各抽取血清20μl,分别加入“BufferA”试剂(美国Agilent公司)60μl,混匀。(2)配比完成后,2组样本(各80μl)以16000g离心15min(20℃)。2.2.高效液相色谱(HPLC)去除高丰度蛋白实验(图2)(1)将上述制备完成的2组样本转移至高效液相色谱仪(美国Thermo-Ultimate3000)的自动加样器的底盘中。(2)选择美国AgilentMARC液相色谱柱,并设置分离程序(LCmethod)。(3)2组样本去高丰度蛋白后回收。2.3.样本的酶切(1)上述2组样本分别加入二硫苏糖醇(DTT),反应30分钟。(2)反应后每组样本各加入碘乙酰氨(IAA),避光反应30分钟。(3)按照1:20-1:100(m/m)的比例向每组样本中加入Trypsin酶切,37℃摇床过夜。2.4.样本的脱盐、标记、抽干(1)取2枚SPE脱盐柱(WatersHLBCartridge),分别用1mlACN润湿。(2)ddH2O各1ml分别平衡2枚脱盐柱。(3)将2组样本分别加入2枚脱盐柱中。(4)ddH2O各1ml分别洗涤载有样本的2枚脱盐柱。(5)PBS各1ml分别洗涤载有样本的2枚脱盐柱。(6)2枚脱盐柱分别用各1ml的重标试剂(CD2O)和轻标试剂(CH2O)洗涤,并各洗5次。“I-PRE”为重标标记,“I-POST-HALF”为轻标标记。(7)ddH2O各1ml分别洗涤载有标记过的样本的2枚脱盐柱。(8)应用TFA各500μl洗脱2组样本,洗脱后将标记过的“I-PRE”和“I-POST-HALF”样本合并,合并后的样本编号:1。(9)合并后的样本应用美国Thermo真空抽干机抽干。2.5.高效液相色谱(HPLC)肽段分离实验(1)抽干后的样本加入A相(水相)50μl溶解,离心机16000g,20℃,离心15min。(2)将上述样本转移至高效液相色谱仪(美国Thermo-Ultimate3000)的自动加样器的底盘中。(3)选择美国WatersBEHC18液相色谱柱,并设置分离程序(LCmethod)。(4)样本肽段分离后(图3)回收至24枚回收瓶中。(5)回收的样本按照“第1瓶+第13瓶,第2瓶+第14瓶...”的原则,合并为12瓶样本。(6)合并后的样本应用美国Thermo真空抽干机抽干。2.6.质谱检测、分析实验(1)抽干后的12个样本分别加入1%乙酸(AA)10μl溶解,混匀。(2)12个样本(各10μl)离心机16000g,20度,15min离心。(3)将上述样本转移至液相质谱仪(美国Thermo-LTQOrbitrapElite)的液相部分。(4)设置质谱程序,采集数据,数据库检索,分析(图4)。3.结果分析经过上述实验过程,得出如下结论:3.1.在进行步骤2.2时得到的血清中总体待测蛋白峰面积,样本“I-PRE”与样本“I-POST-HALF”存在很大差异(图5)。这说明术后样本与术前样本相比,血清中待测蛋白总体水平显著下降。3.2.Hemoglobinsubunitalpha蛋白或其生物降解产物,编码基因为HBA1,其在I号病例的手术前后差异明显,手术前后比为“PRE/POST-HALF,H/L=199.33”(表2),即术前该蛋白和其生物降解产物在血清中的含量是术后的199.33倍。表2.筛选实验结果实施方式2基于上述结果扩大样本的验证实验实验技术流程同筛选实验技术流程(图1)验证实验样本的病例编号为II-VI,同筛选实验病例I一样同为颞叶癫痫手术后治愈病例。验证实验所应用的试剂、配比、反应时间、轻-重标记等方法均同于筛选实验。表3.验证实验的样本分组及标记方法标记后的样本编号重标(H)轻标(L)2II-PREII-POST-HALF3III-PREIII-POST-HALF4IV-PREIV-POST-HALF5IV-PREIV-POST-ONE6V-PREV-POST-HALF7V-PREV-POST-ONE8VI-PREVI-POST-HALF9VI-PREVI-POST-ONE结果分析经过上述验证实验过程,得出:1.在进行步骤“高效液相色谱(HPLC)去除高丰度蛋白实验”后得到的血清中待测蛋白总体峰面积“POST”样本(n=8)与“PRE”样本(n=8)相比均有显著下降(图6)。这说明,待测蛋白总的表达水平,术后相较术前有显著的下降。2.Hemoglobinsubunitalpha蛋白或其生物降解产物,编码基因为HBA1,其在另外8组样本中的变化仍然非常明显。结合筛选实验共9组结果,进行综合T-test统计结果显示,Hemoglobinsubunitalpha蛋白或其生物降解产物在手术前后的变化具有显著差异,统计结果有统计学意义(P<=0.01=(表4)。表4.实验结果及统计分析实施方式3对患者样本中的Hemoglobinsubunitalpha蛋白或其生物降解产物进行定量检测。2.定量实验2.1.标准肽的制备(1)制备蛋白HBA1中“VGAHAGEYGAEALER”肽段的标准肽(由吉尔生化(上海)有限公司合成),用0.5%乙酸溶解,并配制成浓度为1nmol/μl的溶液。2.2.样本制备(1)将I-III号以及VII号病例的术前血清“I-PRE”、“II-PRE”、“III-PRE”,和术后一年血清“I-POST-ONE”、“II-POST-ONE”、“III-POST-ONE”以及VII-BLANK取出后室温解冻,各抽取血清20μl,分别加入“BufferA”试剂(美国Agilent公司)60μl,混匀。(2)配比完成后,7组样本(各80μl)以16000g离心15min(20℃)。2.3.高效液相色谱(HPLC)去除高丰度蛋白实验(1)将上述制备完成的7组样本转移至高效液相色谱仪(美国Thermo-Ultimate3000)的自动加样器的底盘中。(2)选择美国AgilentMARC液相色谱柱,并设置分离程序(LCmethod)。(3)7组样本去高丰度蛋白后回收。2.4.样本的酶切按照1:20-1:100(m/m)的比例向每组样本中加入Trypsin酶切,37℃摇床过夜。2.5.样本的脱盐、抽干(1)取7枚SPE脱盐柱(WatersHLBCartridge),分别用1mlACN润湿。(2)ddH2O各1ml分别平衡7枚脱盐柱。(3)将7组样本分别加入7枚脱盐柱中。(4)ddH2O各1ml分别洗涤载有样本的7枚脱盐柱。(5)应用TFA各500μl洗脱7组样本,洗脱后用真空抽干机抽干。2.6.标准肽梯度溶液的制备抽干后的7个样本分别加入1%乙酸(AA)100μl溶解。在“VII-BLANK”溶解后,用“VII-BLANK”将之前配好的1nmol/μl标准肽溶液梯度稀释成以六个下浓度:100pmol/μl、10pmol/μl、1pmol/μl、100fmol/μl、10fmol/μl、1fmol/μl,混匀。质谱检测、分析实验(1)7个样本,以及浓度梯度溶液(6个)离心机16000g,20度,15min离心。(3)将上述样本各取10μl转移至液相质谱仪(美国Thermo-QExactive)的液相部分。(4)设置质谱程序,采集数据,数据库检索,分析。3.结果分析3.1.标准曲线的绘制通过上述实验步骤分别测得6个浓度梯度溶液中标准肽信号强度的峰面积,排除“VII-BLANK”中“VGAHAGEYGAEALER”肽段信号的干扰,通过6个标准肽溶液的浓度和信号强度峰面积(表5)绘制信号强度-肽量标准曲线(图7)(LC-MS进样量4μl)。表5.标准肽梯度溶液的信号强度峰面积与浓度标准肽样本浓度标准肽绝对量信号强度峰面积VII-BLANK-7133001fmol/μl4fmol78390010fmol/μl40fmol2110000100fmol/μl400fmol103800001pmol/μl4pmol7963000010pmol/μl40pmol1077000000100pmol/μl400pmol66690000003.2.“I-PRE”、“II-PRE”、“III-PRE”、“I-POST-ONE”、“II-POST-ONE”、“III-POST-ONE”号样本绝对浓度的定量测定。通过上述实验步骤分别测得“I-PRE”、“II-PRE”、“III-PRE”,“I-POST-ONE”、“II-POST-ONE”、“III-POST-ONE”6个样本的信号强度峰面积,将其代入3.1绘制的标准曲线中,算得绝对浓度(表6)。通过定量结果,可以看出,三个患者术后内源性HBA1蛋白“VGAHAGEYGAEALER”肽段在血液中的含量,相较术前均有显著的下降。但是三个患者之间的个体差异相对较大,如需得出较为准确的该肽段血液浓度分布区间,还需扩大定量实验的样本量。表6.峰面积与定量结果样本编号信号强度峰面积肽段浓度(fmol/μl)VII-BLANK713300-I-PRE2624700282.7253954I-POST-ONE39870042.00237712II-PRE18888670021399.34912II-POST-ONE1905700204.5027659III-PRE633167007081.352216III-POST-ONE2010700215.9070306实施方式4试剂盒:检测血清或脑脊液等体液或组织中Hemoglobinsubunitalpha蛋白或其生物降解产物的试剂盒,其包含抗Hemoglobinsubunitalpha蛋白或其生物降解产物的抗体。利用上述试剂盒检测患者血清中Hemoglobinsubunitalpha蛋白或其生物降解产物的步骤:按照实施方式1的方式采集患者的血清,与Hemoglobinsubunitalpha蛋白或其生物降解产物的抗体进行反应,有效的检测本发明的生物标志物的表达水平,从而能够有效地检测待检测者是否存在癫痫的疾病状态,辅助药物难治性癫痫的分型诊断,以及药物难治性癫痫术后是否可以减停药物的判断等。如上所述的实施方式的目的在于对本发明的具体实施方式作进一步的说明,并非对本发明作任何限制,凡是根据本发明技术方案所作的任何简单修改、变更及等效变化,均仍落入本发明技术方案的保护范围内。SEQUENCELISTING<110>北京大学<120>一种用于癫痫预测的生物标志物<160>1<210>1<211>142<212>PRT<213>Homosapiens<400>1MetValLeuSerProAlaAspLysThrAsnValLysAlaAlaTrpGly151015LysValGlyAlaHisAlaGlyGluTyrGlyAlaGluAlaLeuGluArg202530MetPheLeuSerPheProThrThrLysThrTyrPheProHisPheAsp354045LeuSerHisGlySerAlaGlnValLysGlyHisGlyLysLysValAla505560AspAlaLeuThrAsnAlaValAlaHisValAspAspMetProAsnAla65707580LeuSerAlaLeuSerAspLeuHisAlaHisLysLeuArgValAspPro859095ValAsnPheLysLeuLeuSerHisCysLeuLeuValThrLeuAlaAla100105110HisLeuProAlaGluPheThrProAlaValHisAlaSerLeuAspLys115120125PheLeuAlaSerValSerThrValLeuThrSerLysTyrArg130135140当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1