一种寨卡病毒E抗原及其在检测抗寨卡病毒抗体中的应用的制作方法
本发明属于抗寨卡病毒抗体的免疫检测领域,具体涉及一种寨卡病毒E抗原及其在检测抗寨卡病毒抗体中的应用。
背景技术:
Zika病毒(Zika virus,ZIKV)是伊蚊传播的虫媒病毒,于1947年首次分离自乌干达Zika森林中的恒河猴。2005年以前在非洲和东南亚区域有散发的Zika病毒人感染病例。2007年在西太平洋密克罗尼西亚联邦雅浦岛(Yap Island)首次暴发人感染Zika病毒疫情,随着Zika病毒在世界范围内的传播扩散及疫情加重,世界卫生组织(World Health Organization,WHO)和各国均发布了Zika病毒病预防控制方案,我国也及时发布了2016年Zika病毒病诊疗方案,指导临床病例的诊断和治疗。Zika病毒感染者中有1/4-1/5的感染者会发病,且患者临床症状轻微,多为流感样表现,持续数天到一周则会痊愈,但是也有部分患者出现格林-巴利综合征(Guillain-Barre syndrome),孕妇感染Zika病毒与新生儿小头畸形存在关联,并可通过性途径传播。因此,Zika病毒病的防控不容忽视。
Zika病毒属于黄病毒科黄病毒属,为单股正链RNA病毒,基因组长度为10 794bp,由5’端非编码区(non-coding region,NCR)、单个开放读码框架(open reading frame,ORF)和3’端非编码区组成。编译的病毒多肽经蛋白酶水解后形成3个病毒结构蛋白:衣壳(capsid,C)、前膜(pre-membrane,preM)和包膜(envelope,E)和7个非结构蛋白(NS1、NS2A、NS2B、NS3、NS4A、NS4B和NS5)。E蛋白(约53kDa)是病毒粒子主要的表面蛋白,参与病毒的生活周期,介导病毒的连接和膜融合。
对于寨卡病毒感染,现阶段尚缺乏有效的治疗方法和预防性疫苗,这给疫情防控带来了不小的阻碍。同时,寨卡病毒的感染症状轻微,甚至约80%的寨卡病毒感染者不会出现任何症状,也给临床诊断造成很大干扰。Zika病毒感染的实验室诊断方法包括血清或血浆分离病毒、检测病毒核酸或病毒特异性IgM抗体及中和抗体。
病毒学检测方法能够检测样本中的寨卡病毒RNA,从而确定患者是否被感染。然而,感染者体内寨卡病毒载量的动态发展情况尚不清楚。目前的研究表明,寨卡病毒的潜伏期可能为3~12d,在感染症状出现前2d和出现后11d内均可在感染者血清中检测出病毒,病毒载量可达每毫升血清中存在8.1×106个病毒核酸拷贝数。然而大多数研究表明,在病毒感染症状出现后1周左右的时间里才能在感染者血清中稳定地检测出较高水平的病毒。
一直以来,传统的血清学检测方法都是寨卡病毒检测的主要方法。研究表明,在感染症状出现约3d后的感染者血清中即可检测出寨卡病毒特异性免疫球蛋白M(immunoglobulin M,IgM)以及中和抗体,而恢复期的感染者血清样本中可以检测到特异性IgM、免疫球蛋白G(immunoglobulinG,IgG)以及中和抗体。根据WHO和美国CDC的诊断建议,应选择感染症状出现4d以及2周后的血清样本,应用酶联免疫吸附测定法(enzyme-linked immuno sorbent assay,ELISA)检测寨卡病毒特异性IgM抗体和中和抗体。
我国疾病控制预防中心以及一些企业已经研制出了寨卡病毒核酸类诊断试剂,尚缺乏免疫检测试剂。
技术实现要素:
本发明的目的是提出一种寨卡病毒E抗原及在检测抗寨卡病毒抗体中的应用,具体技术方案如下:
一种寨卡病毒E抗原的氨基酸序列为以下任一种:
1)序列表中SEQ ID No.1所示的氨基酸序列;
2)与SEQ ID No.1所示的氨基酸序列具有80%以上相似性的序列。
所述与SEQ ID No.1所示的氨基酸序列具有80%以上相似性的序列是SEQ ID No.1所示的氨基酸序列通过氨基酸替换、缺失或者增加得到的。
所述的寨卡病毒E抗原在检测抗寨卡病毒抗体中的应用。
所述应用的方法为利用所述寨卡病毒E抗原通过免疫检测方法检测抗寨卡病毒抗体。
所述的应用中的免疫检测方法为酶联免疫法、化学发光法、胶体金法、乳胶法、放射免疫法和荧光免疫法。
所述酶联免疫法为酶联免疫吸附测定法;所述荧光免疫法为时间分辨荧光免疫法。
一种检测抗寨卡病毒抗体的试剂盒,包括所述的寨卡病毒E抗原。
所述的试剂盒,还包括免疫诊断试剂,所述免疫诊断试剂是检测人IgG、IgM或IgA的试剂。
所述检测人IgG的试剂包括碳酸盐缓冲液、PBST洗涤缓冲液、样品稀释液、显色剂A液、显色剂B液、终止液、酶标二抗。
所述酶标二抗为羊抗人抗体IgG上标记HPR酶;
碳酸盐缓冲液:碳酸氢钠2.93g,碳酸钠1.59g,加水定容至1000ml,pH9.6;
PBST洗涤缓冲液:80mmol/L的Na2HPO4、20mmol/L的KH2PO4、100mmol/L的KCl、1400mmol/L的NaCl、体积分数为0.5%的Tween-20,pH 7.4;
封闭液:1%BSA、0.01M PH7.4的PBS;
样品稀释液:1%BSA-PBST缓冲液;
终止液:2M H2SO4;
显色剂A液:柠檬酸3.2g,醋酸钠27.2g,30%的双氧水0.3ml,加纯化水至1000mL;
显色剂B液:柠檬酸1.9g,乙二胺四乙酸二钠0.4g,TMB 0.30g,加纯化水至1000mL。
本发明的有益效果为:
本发明对Zika病毒基因组及其表达蛋白进行分析,找到了能够特异性检测抗ZIKV抗体的E抗原,基于所发现的E抗原可以实现特异性检测人血中抗ZIKV抗体。
本发明检测抗ZIKV抗体的方法有效地避免了在检测过程中使用具有强传染能力的zika病毒,降低了整个实验的危险性。本发明的技术方案还具有简单、易操作、重复性好等特点,容易得到推广和应用。
附图说明
图1为zika病毒E序列抗原性分析图。
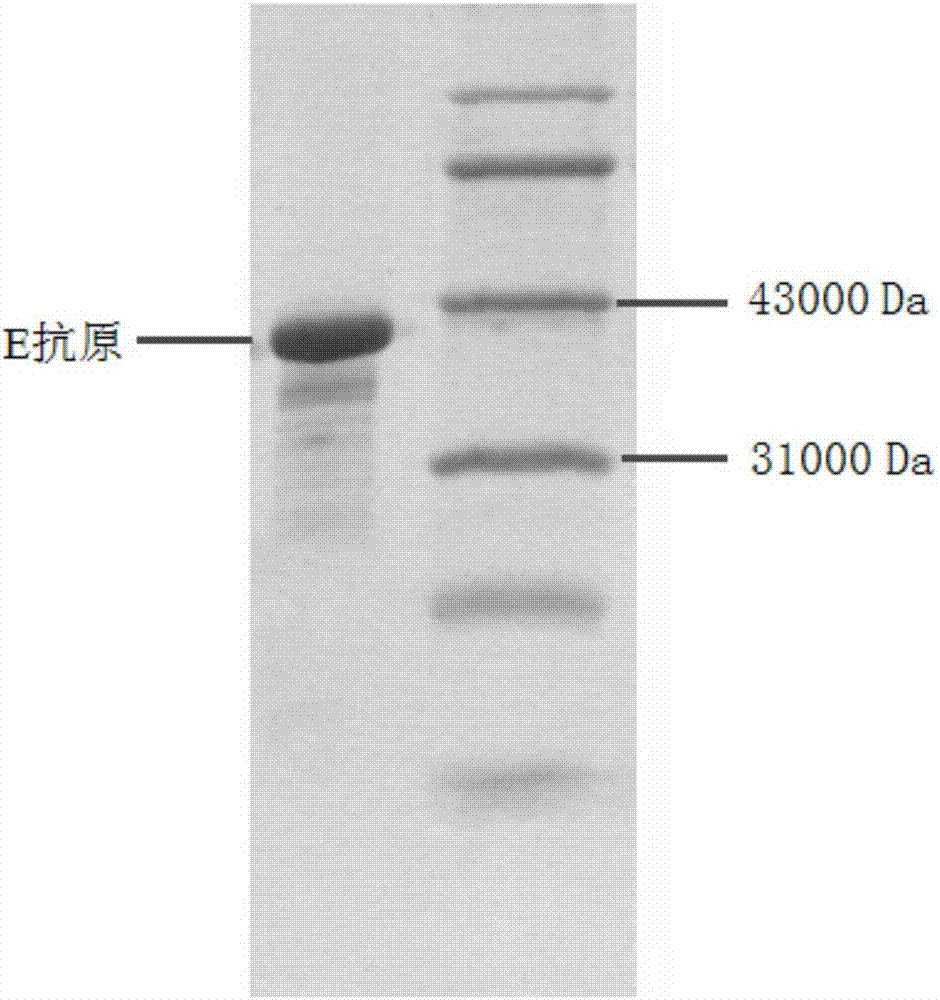
图2为实施例2中zika病毒E抗原纯化后的SDS-PAGE图。
具体实施方式
首先本发明人对E蛋白的抗原表位进行了生物信息学研究,找到了一段可能的高抗原性的抗原片段,即SEQ ID No.1所示的氨基酸序列,对该段E抗原进行了克隆表达,并且基于间接酶联免疫技术使用zika患者血清对纯化后的抗原片段的抗原特异性和灵敏度进行检验,结果发现此抗原能特异性地检测感染zika病毒后人体内的抗ziak抗体。
本领域众所周知,与某一个抗原片段具有一定相似性的另一个氨基酸序列片段会具有相同或相似的免疫反应,因此通常认为,通过替换、添加或者缺失某些氨基酸而与本发明E抗原片段具有大于80%、大于81%、大于82%、大于83%、大于84%、大于85%、大于86%、大于87%、大于88%、大于89%、大于90%、大于91%、大于92%、大于93%、大于94%、大于95%、大于96%、大于97%、大于98%、大于99%相似性的序列具有与SEQ ID No.1所示的氨基酸序列相似的免疫反应,因而这些序列片段可以用于实施本发明的方案中。
本领域亦众所周知,包含SEQ ID No.1所示的氨基酸序列的序列,或者包含与SEQ ID No.1所示的氨基酸序列具有大于80%、大于81%、大于82%、大于83%、大于84%、大于85%、大于86%、大于87%、大于88%、大于89%、大于90%、大于91%、大于92%、大于93%、大于94%、大于95%、大于96%、大于97%、大于98%、大于99%相似性的序列的序列同样具有与SEQ ID No.1所示的氨基酸序列相同或者相似的免疫反应,因而这些序列片段也可以用于实施本发明的方案中。
本发明的E抗原可以适用于任何免疫检测方法以检测感染zika病毒后人体内的抗ZIKV抗体。这些检测方法包括但不限于酶联免疫法、化学发光法、胶体金法或乳胶法。其中实施例中使用的间接免疫酶联检测技术属于酶联免疫法中的酶联免疫吸附测定法。这些方法均可以用来实施本发明。
抗体可以是IgG、IgM或者IgA亚类,因此在使用本发明的E抗原实现抗ZIKV抗体检测的过程中有时会使用到检测人IgG、IgM或者IgA的试剂,这是本领域众所周知的。而所述的这些检测试剂也是本领域众所周知的,例如但不限于诸如羊或兔抗人IgG、IgM或IgA的抗体等。因此在本发明要求保护的试剂盒中,除了本发明的E抗原片段外还包含这些检测IgG、IgM或者IgA的试剂,以及任选的其他试剂,例如缓冲液等。
以下的实施例便于更好地理解本发明,但并不限定本发明。下述实施例中的实验方法,如无特殊说明,均为常规方法。
实施例1:zika病毒E抗原的克隆、表达与活性鉴定
1、E抗原基因的设计与合成
为了使zika病毒E基因在E.coli中获得高效的表达,基于确定的zika病毒E抗原的氨基酸序列,选择大肠杆菌的偏性密码子设计E基因,并委托上海英潍捷基生物技术服务有限公司合成上述序列的基因,序列如SEQ ID No.2所示。
2、E抗原表达质粒的构建与转化
为了便于将基因克隆到表达载体中,在连接臂的两端引入Xho I和Xba I两个酶切位点,以适合表达载体pBVIL1(参见中国专利ZL00100695.9:表达载体pBVIL1及其构建方法和用途)。双酶切后插入载体pBVIL1中,构建相应的表达质粒。
(1)酶切
酶切反应体系(100μl)为:
取以上SEQ2合成基因产物及pBVIL1表达载体分别放于Eeppendorf离心管中,按照上述酶切反应体系加入各物质,37℃水浴酶切过夜。
(2)酶切产物的纯化和回收
基因产物及载体pBVIL1经双酶切后,按照《分子克隆》(科学出版社,第二版)中所述的方法用2%琼脂糖凝胶进行分离,并用百泰克生物技术有限公司的小量胶回收试剂盒进行纯化回收。即在紫外灯下分别切下含目的片段的琼脂糖凝胶,放于Eeppendorf离心管中,各加入溶胶/结合液,置65℃水浴5分钟使胶溶解,然后分别移入吸附柱后,按试剂盒说明书进行纯化。
(3)连接
连接反应体系(8μl)为:
pBVIL1载体 1μl
SEQ2合成基因 3μl
T4DNA Ligase 4μl
于灭菌Eeppendorf离心管中加入上述各物质后,16℃连接5h以上。
(4)转化
在超净工作台中,用无菌吸头取100μl HB101感受态细胞(感受态细胞按照《分子克隆》(科学出版社,第二版)的方法制备)悬液于Eppendorf中,加入(3)中的连接物8μl,轻轻旋转混匀,冰浴30min,立即转移到42℃水浴中放置2min,每管加入1ml LB培养基(不加抗生素),37℃水浴摇床培养1h后,各取0.2ml分别涂于LB琼脂培养基平皿上(含抗生素),室温晾干后,置37℃恒温箱倒置培养过夜。
(5)鉴定
挑选菌落分别接种于LB中(5ml/管),培养过夜,次日各取0.1ml转移到LB中(2ml/管),32℃培养3h,42℃水浴摇床中诱导培养4h,收菌,用SDS-PAGE鉴定,选择目的基因获得高表达菌株,并经测序鉴定载体中所插入的基因片段完全正确。
3、E抗原的表达与纯化
(1)表达菌株的培养
取-70℃保存的表达菌株20μl接种于LB培养基中(100ml LB/500ml三角瓶),37℃空气摇床培养过夜,次日按5%的比例转种于LB培养基(同上),37℃空气摇床培养约3h,当OD600值达到0.7时,立即将培养瓶转到42℃水浴摇床中,诱导培养4小时。将菌液合并,6000rpm离心20min,弃上清,收集沉淀部分。
(2)提取包涵体
将沉淀称湿重,用10倍体积的20mmol/L pH8.5TE缓冲液将沉淀悬起,加入溶菌酶(1mg/ml悬液),在室温下磁力搅拌10min。在冰浴中超声波破碎菌,每次超声3s,间隔7s,共超声20min。4℃,12000rpm,离心10min,弃上清,沉淀用1mol/L NaCl(用TE配制)洗一次,再用TE洗2次,收集沉淀。沉淀用6M脲(用pH8.5TE配制)溶解,加1%β-巯基乙醇,过滤去沉淀取上清。
(3)纯化
将上述溶解的包涵体溶液过Q-SepgEroseFF阴离子交换柱,用平衡液(pH8.5,25mmol/L TE,含6mol/L脲,0.1%β-巯基乙醇)清洗后,用不同浓度的NaCl(用平衡液配制)洗脱,收集各洗脱峰,经SDS-PAGE鉴定,收集0.05mol/L NaCl洗脱峰。再过SepgErdexG-50凝胶过滤柱,收集第一洗脱峰。纯化重组表位抗原均用SDS-PAGE鉴定。通过上述的离子交换柱和凝胶过滤纯化,获得了电泳纯的zika病毒E抗原纯品。
4、E抗原的活性鉴定
通过以下实验步骤进行活性测定:将纯化的候选抗原用pH 9.6的碳酸盐缓冲液稀释为2.5μg/ml,取100μl于酶联板中,4℃包被过夜;洗板2次,加入120μl封闭液,室温封闭6h,甩掉封闭液,拍干,室温干燥;加样品稀释液90μl,样品10μl,37℃反应30min;洗板5次,加入羊抗人IgG-HRP 100μl,37℃反应20min;洗板5次,加入A、B显示液各50μl,37℃反应10min;加入终止液50μl,终止后10min内,450nm波长测定测OD值。
试剂配制:
碳酸盐缓冲液:碳酸氢钠2.93g,碳酸钠1.59g,加水定容至1000ml,pH 9.6。
PBST洗涤缓冲液:80mmol/L的Na2HPO4、20mmol/L的KH2PO4、100mmol/L的KCl、1400mmol/L的NaCl、体积分数为0.5%的Tween-20,pH 7.4。
封闭液:1%BSA、0.01M PH7.4的PBS。
样品稀释液:1%BSA-PBST缓冲液。
终止液:2M H2SO4。
显色剂A液:柠檬酸3.2g,醋酸钠27.2g,30%的双氧水0.3ml,加纯化水至1000mL。
显色剂B液:柠檬酸1.9g,乙二胺四乙酸二钠0.4g,TMB 0.30g,加纯化水至1000mL。
本次实验对10例寨卡患者血清及10例健康对照血清进行了测定。原始测定结果如表1所示。经分析该抗原的阳性率为100%,特异性也为100%。
表1寨卡病毒E抗原活性检测数据
实施例2:抗ZIKV抗体检测
采用以下步骤:将纯化的候选抗原用pH 9.6的碳酸盐缓冲液稀释为2.5μg/ml,取100μl于酶联板中,4℃包被过夜;洗板2次,加入120μl封闭液,室温封闭6h,甩掉封闭液,拍干,室温干燥;加样品稀释液90μl,样品10μl,37℃反应30min;洗板5次,加入羊抗人IgG-HRP 100μl,37℃反应20min;洗板5次,加入A、B显示液各50μl,37℃反应10min;加入终止液50μl,终止后10min内,450nm波长测定测OD值。
对17例寨卡患者血清及53例健康对照血清进行抗ZIKV抗体进行检测。测定结果以及分析结果如表2所示:E抗原在中17例检测结果均为阳性,阳性率100%;在53例健康对照血清中,均为阴性,特异性100%。因此抗原包被作为抗体检测试剂具有较高的特异性和灵敏度,在抗ZIKV抗体诊断中具有实用价值。
表2寨卡病毒抗体检测分析结果
实施例3:酶联免疫吸附法试剂盒的制备
1、试剂的配置
碳酸盐缓冲液、PBST洗涤缓冲液、封闭液、样品稀释液、显色剂A液、显色剂B液、终止液的配置同实施例1。
2、抗原的包被
将实施例1中纯化的候选抗原用pH9.6的碳酸盐缓冲液稀释为2.5μg/ml,取100μl于酶联板中,4℃包被过夜;洗板2次,加入120μl封闭液,室温封闭6h,甩掉封闭液,拍干,室温干燥。
3、酶标二抗
在羊抗人抗体IgG上标记HPR酶,以PBST缓冲液稀释,使最终检测滴度为1:2000。
4、分装
取PBST洗涤缓冲液、样品稀释液、显色剂A液、显色剂B液、终止液、酶标二抗、包被有抗原的酶联板,分别独立包装。
实施例4:酶联免疫吸附法试剂盒的使用
取实施例3的试剂盒,以寨卡患者血清为实验组,正常人血清为阴性对照组,说明酶联免疫吸附法试剂盒的使用方法。
每个血清样品以试剂盒中提供的样品稀释液按1:90稀释后,取100μl加入包被有候选抗原的酶联板中,37℃反应30min,用PBST洗涤缓冲液洗板5次;加入羊抗人IgG-HRP 100μl,37℃反应20min,洗板5次;加入A、B显示液各50μl,37℃反应10min;加入终止液50μl,终止后10min内,450nm波长测定测OD值。
化学发光法、胶体金法、乳胶法、放射免疫法和荧光免疫法免疫诊断试剂盒分别根据其免疫检测原理制备,其中,免疫诊断试剂是检测人IgG、IgM或IgA的试剂。
SEQUENCE LISTING
<110> 中国人民解放军军事医学科学院基础医学研究所
<120> 一种寨卡病毒E抗原及其在检测抗寨卡病毒抗体中的应用
<130> 2017
<160> 2
<170> PatentIn version 3.3
<210> 1
<211> 230
<212> PRT
<213> 寨卡病毒(Zika virus)
<400> 1
Arg Ala Glu Ala Thr Leu Gly Gly Phe Gly Ser Leu Gly Leu Asp Cys
1 5 10 15
Glu Pro Arg Thr Gly Leu Asp Phe Ser Asp Leu Tyr Tyr Leu Thr Met
20 25 30
Asn Asn Lys His Trp Leu Val His Lys Glu Trp Phe His Asp Ile Pro
35 40 45
Leu Pro Trp His Ala Gly Ala Asp Thr Gly Thr Pro His Trp Asn Asn
50 55 60
Lys Glu Ala Leu Val Glu Phe Lys Asp Ala His Ala Lys Arg Gln Thr
65 70 75 80
Val Val Val Leu Gly Ser Gln Glu Gly Ala Val His Thr Ala Leu Ala
85 90 95
Gly Ala Leu Glu Ala Glu Met Asp Gly Ala Lys Gly Arg Leu Phe Ser
100 105 110
Gly His Leu Lys Cys Arg Leu Lys Met Asp Lys Leu Arg Leu Lys Gly
115 120 125
Val Ser Tyr Ser Leu Cys Thr Ala Ala Phe Thr Phe Thr Lys Val Pro
130 135 140
Ala Glu Thr Leu His Gly Thr Val Thr Val Glu Val Gln Tyr Ala Gly
145 150 155 160
Thr Asp Gly Pro Cys Lys Ile Pro Val Gln Met Ala Val Asp Met Gln
165 170 175
Thr Leu Thr Pro Val Gly Arg Leu Ile Thr Ala Asn Pro Val Ile Thr
180 185 190
Glu Ser Thr Glu Asn Ser Lys Met Met Leu Glu Leu Asp Pro Pro Phe
195 200 205
Gly Asp Ser Tyr Ile Val Ile Gly Val Gly Asp Lys Lys Ile Thr His
210 215 220
His Trp His Arg Ser Gly
225 230
<210> 2
<211> 690
<212> DNA
<213> 人工序列
<400> 2
cgtgcggaag ccaccctggg cggttttggc agcttgggtc tggattgcga gccgcgcacg 60
ggcttagact tctctgatct gtattacctt actatgaaca ataaacattg gctggtgcac 120
aaggaatggt ttcatgatat tccactcccg tggcacgcgg gtgcagacac cggcactcca 180
cattggaaca ataaagaagc tctggttgag ttcaaagatg cgcacgccaa gcgtcagacg 240
gtggtcgttc tgggttccca agaaggcgca gtacataccg ctttggcggg cgccctggaa 300
gcggagatgg acggtgcaaa aggccgctta ttttcgggtc acctgaaatg tcgtcttaag 360
atggataaac tgcgcctcaa aggcgtgagc tatagtctgt gcactgctgc gttcaccttt 420
accaaggttc cggccgaaac gctgcatggt actgtcaccg tggaagttca gtacgcaggc 480
actgatggtc catgcaaaat cccggtgcag atggctgtcg atatgcaaac gttgacccca 540
gttggccgtc tgattactgc gaacccggta atcaccgagt ctaccgaaaa ttcgaaaatg 600
atgttagaac tggacccgcc attcggcgat agctatattg tgatcggtgt tggcgataag 660
aaaattacgc atcactggca tcgcagcggt 690
- 还没有人留言评论。精彩留言会获得点赞!