壳聚糖衍生物为载体的MRI造影剂及制备方法与流程
本发明涉及一种磁共振成像用的造影剂,具体涉及一种磁共振成像造影用的基于壳聚糖的MRI造影剂及制备方法,属于医学临床磁共振成像技术领域。
背景技术:
随着科技的发展,磁共振成像已成为临床检测固体瘤的一种有效手段。相较于其其它成像技术,磁共振成像有很多优点,如无电离辐射损伤、超高的组织分辨率和三维定位能力。但为了进一步提高成像的灵敏度和准确率,通常需要造影剂来增强成像对比度。目前,临床用的造影剂一般为小分子的钆螯合物。这类小分子造影剂应用于生物体尚存在一些缺点,如血液循环时间短、弛豫率低、无靶向性,具有一定的毒性,甚至会引起生物体肾细胞的纤维化。因此高弛豫率、低毒及具有组织或肿瘤靶向性成为MRI造影剂发展的焦点。
近年来,将小分子Gd造影剂共价或者非共价的与高分子结合的研究越来越多。将小分子造影剂与高分子结合,可以增强体内稳定性、改变疏水性质、降低分子的旋转速率、提高弛豫效率、延长血液循环时间和在组织中的驻留时间,另外对高分子可进行专属性化学修饰,增强对组织或器官的靶向性,将配合物修饰为电中性,可以使渗透压与血浆相近,从而降低毒副作用。但由于大分子在体内排泄较慢限制了其在临床中的应用。因此,寻找易降解的大分子作为小分子造影剂的载体尤为重要。
技术实现要素:
本发明的主要目的在于提供一种具有生物相容性好、易生物降解和高弛豫率等特点的壳聚糖衍生物为载体的MRI造影剂及其制备方法,以克服现有技术中的不足。
为实现前述发明目的,本发明所采用的技术方案如下:
在本发明的一实施案例之中,提供了一种壳聚糖衍生物为载体的MRI造影剂的制备方法, 包括:将二乙烯三胺五乙酸和Gd3+偶联到炔基修饰的二代聚酰胺胺树形分子上,形成带有钆螯合物的二代聚酰胺胺树形分子,
以及,通过点击化学反应将带有钆螯合物的二代聚酰胺胺树形分子连接至聚乙二醇修饰的壳聚糖主链上,获得所述造影剂。
在一较优实施方式中,所述制备方法进一步包括:将壳聚糖与端羧基的聚乙二醇在室温反应得到聚乙二醇修饰的壳聚糖,所述壳聚糖的分子量为Mw 40000~50000Da,所述聚乙二醇的投量为壳聚糖结构单元的摩尔数的10~20%。
优选的,壳聚糖与端羧基的聚乙二醇在室温反应的时间为8~12h。
在一较优实施方式中,所述制备方法进一步包括:以浓度为3~6wt%的酸溶液作为反应溶剂,将叠氮化合物通过取代反应修饰到聚乙二醇修饰的壳聚糖上,反应时间为20~26h,获得修饰有叠氮基团和聚乙二醇的壳聚糖。
优选的,其中酸溶液为等体积的盐酸和醋酸的混合液。
优选的,叠氮化合物为叠氮酸或叠氮化的环氧氯丙烷。
一较优实施方式中,所述制备方法进一步包括:将二乙烯三胺五乙酸的活化酯通过缩合反应连接到二代聚酰胺胺树形分子上,获得偶联有二乙烯三胺五乙酸的树形分子。
一较优实施方式中,所述制备方法进一步包括:在pH值为5~7时,将Gd3+螯合到二乙烯三胺五乙酸(DTPA)偶联的二代聚酰胺胺树形分子上,获得偶联有二乙烯三胺五乙酸和Gd3+的二代聚酰胺胺树形分子。
在一较优实施方式中,所述制备方法进一步包括:在存在催化剂的条件下,使修饰有叠氮基团和聚乙二醇的壳聚糖与偶联有二乙烯三胺五乙酸和Gd3+的二代聚酰胺胺树形分子通过点击化学反应连接,反应时间为20~26h,获得所述造影剂,所述催化剂至少选自五水硫酸铜和抗坏血酸钠。
本发明还提供了一种采前述制备方法得到的壳聚糖衍生物为载体的MRI造影剂。
在一实施方案之中,所述壳聚糖衍生物为载体的MRI造影剂包括:
作为造影剂主体的聚乙二醇修饰的壳聚糖,
主要连接于壳聚糖主链上的带有钆螯合物的二代聚酰胺胺树形分子。
在一较佳实施方案之中,所述造影剂具有下式所示结构:
其中,n为100~300之间的整数。
该壳聚糖衍生物为载体的MRI造影剂采用壳聚糖作为造影剂主体,壳聚糖具有生物相容性好,生物毒性低和生物可降解的优点,壳聚糖的分子量大小可以不限。将钆螯合物连接在二代聚酰胺胺树形分子上,然后通过点击化学修饰到壳聚糖上,能够增加造影剂分子的尺寸,增加旋转相关时间,从而提高弛豫效率,并延长其血液循环时间。钆螯合物主要位于二代聚酰胺胺树形分子接枝的壳聚糖的侧链上,从而提高单位分子量的钆装载率。经试验发现,该造影剂弛豫率(9.53mM-1·s-1)明显高于小分子造影剂的弛豫率(4.25mM-1·s-1)。
与现有技术相比,本发明的有益效果包括:该壳聚糖衍生物为载体的MRI造影剂的生物相容性好,易生物降解,并具备高弛豫率,且其制备方法简单,反应条件温和,易于控制。
附图说明
下面结合附图和具体实施方式对本发明作进一步的阐述。
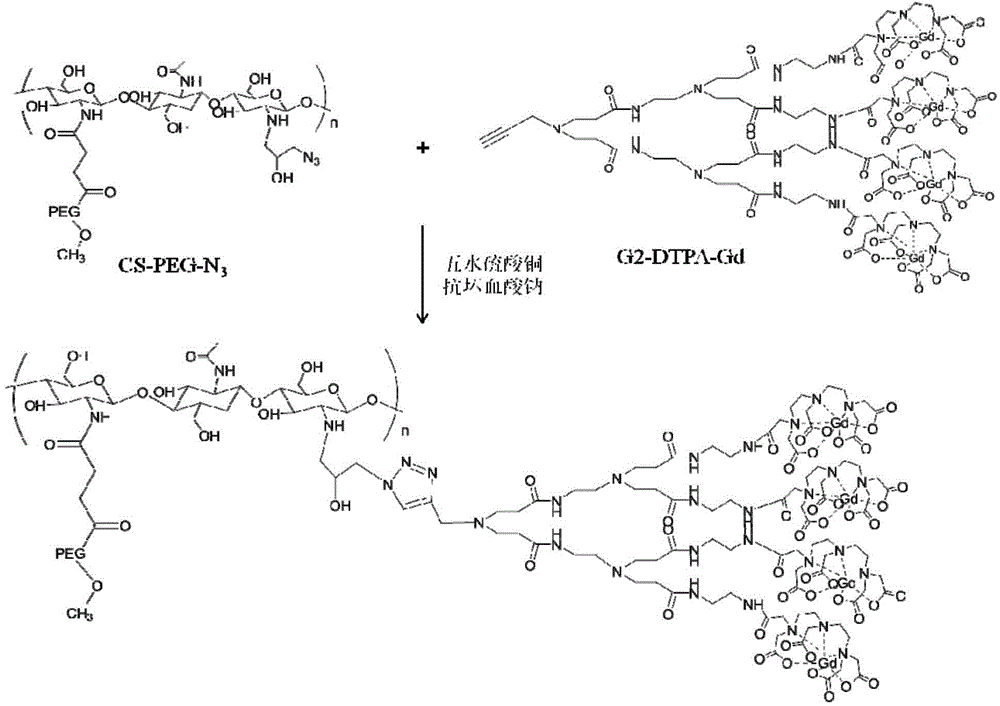
图1a是本发明实施例1中一种造影剂的制备工艺流程图;
图1b是本发明实施例1中一种造影剂的结构式;
图2是壳聚糖、CS-PEG、CS-PEG-N3及本发明造影剂的红外光谱图;
图3是本发明造影剂与Gd-DTPA弛豫率对比图;
图4是本发明高分子造影剂与Gd-DTPA的T1加权成像对比图;
图5是本发明高分子造影剂在A549细胞中的细胞毒性侧视图。
具体实施方式
以下结合具体实施例对上述方案做进一步说明。应理解,这些实施例是用于说明本发明而不限于限制本发明的范围。实施例中采用的实施条件可以根据实际需要而做进一步调整,未注明的实施条件通常为常规实验中的条件。
实施例1壳聚糖衍生物为载体的MRI造影剂的制备方法,参阅图1a,其具体步骤如下:在一实施案例中,该造影剂的制备方法可包括如下步骤:
(1)将PEG-COOH溶解配成5%(w/w)的溶液,然后将溶液的PH调节到6,然后加入NHS,搅拌5min后加入EDC使EDC:NHS:COO的摩尔比为1:1:0.8。在以上溶液搅拌30min将羧基活化后缓慢滴加到溶解在体积分数为1%CH3COOH中的壳聚糖里,反应液在室温下搅拌10h。将反应液透析后冻干,得聚乙二醇修饰的壳聚糖(CS-PEG)。
(2)将CS-PEG溶解在5wt%的冰醋酸和盐酸的等体积混合液中,加入叠氮化的环氧氯丙烷。反应液用铝箔避光,25℃反应24h。反应产物用含40%氨的甲醇溶液沉淀,过滤,并将沉淀依次用甲醇、水、丙酮洗涤,将终产物于真空干燥箱中烘干,得修饰有叠氮基团和聚乙二醇的壳聚糖(N3-CS-PEG)。
(3)取二代的聚酰胺胺树形分子,加DMF进行溶解,溶解完全后,在冰浴条件下滴加至的DTPA-NHS的DMF溶液中,滴加过程通N2保护。滴加完成后,撤去冰浴,室温反应3天。反应结束后,减压蒸馏除去溶剂DMF,最后所得粘稠物加水溶解并透析、冻干,得偶联有二乙烯三胺五乙酸的树形分子(G2-DTPA)。
(4)将G2-DTPA加水溶解,向其中滴加GdCl3·6H2O的水溶液,边滴加边用NaOH调节PH=6,42℃反应10h后,透析并冻干,得偶联有二乙烯三胺五乙酸和Gd3+的二代聚酰胺胺树形分子(G2-DTPA-Gd)。
(5)取N3-CS-PEG溶于1%的醋酸水溶液,取G2-DTPA-Gd溶于水后分别滴加至前述溶液中。反复冻融两次除氧后,继续通N2,加入抗坏血酸钠和五水硫酸铜,40℃反应24h。反应混合液透析后,冻干,即得所述造影剂PEG-CS-G2-DTPA-Gd(如下亦称本发明造影剂,如图1b所示)。
实施例2测定CS、CS-PEG、CS-PEG-N3和CS-PEG-G2-DTPA-Gd的红外光谱图,包括:采用压片法制样,分别检测壳聚糖原料、CS-PEG、CS-PEG-N3和CS-PEG-G2-DTPA-Gd的红外吸收,如图2所示。
实施例3在0.5T的MRI测试仪上测试本发明高分子造影剂与Gd-DTPA弛 豫时间T1及T1加权成像,包括:
分别配制浓度为0.1~1.0mM的上述两种样品,测试后,以浓度为横坐标,弛豫时间的倒数为纵坐标进行线性拟合得到本发明的造影剂和Gd-DTPA的弛豫率分别为9.53mM-1·s-1和4.25mM-1·s-1(图3)。本发明的造影剂弛豫率明显高于Gd-DPTA。通过两者在不同浓度下的T1加权成像(图4)可以看出,随浓度的增加,两者均有变亮的趋势,但本发明造影剂的造影效果明显亮于Gd-DTPA。
实施例4造影剂的细胞毒性检测
用WST法来测定本发明造影剂在A549细胞中的细胞毒性(图5)。在96孔板中以每孔5000~8000细胞的密度种入A549细胞悬液100μL,将96孔板置于CO2培养箱中,在37℃中培养24h。将本发明造影剂溶于完全培养基中,过滤除菌,用完全培养基将聚合物溶液稀释成0.01~2mM不同的浓度。然后再将不同浓度的聚合物溶液加入到96孔板中,每孔加100μL,对照组加入100μL完全培养基,继续培养24h。最后移出培养基,每孔加入100μL新鲜培养基,然后每孔加入10μL WST,置于培养箱中培养2h,用酶标仪测定450nm处的吸收值OD450nm。每个聚合物浓度及对照组做4个平行样。根据吸光值计算细胞的相对存活率。空白组即不加细胞及聚合物溶液,对照组即不加聚合物溶液。
细胞相对存活率(%)=100×(实验组OD-空白组OD)/(对照组OD-空白组OD)
如图5所示,A549细胞与PEG-CS-G2-DTPA-Gd孵育后的存活率与浓度相关,在Gd3+浓度低于0.1mM时,成活率均接近100%,至0.5mM时成活率在80%以上。表明本发明造影剂分子浓度在0.1mM以下时无生物毒性,0.5mM左右有较低的生物毒性。
上述实例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人是能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所做的等效变换或修饰,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!