用于活性剂递送的两亲性嵌段共聚物的制作方法
本发明涉及用于包封和体内药物递送的新型聚合物。本发明的另一方面是用于包括所述聚合物的活性成分(活性剂)的控释系统。
已知两亲性聚合物在具有疏水性核的水性环境中以胶粒形式用于包封体系中,其中可捕获疏水性药物。
携带药物的胶粒的期望特征是当在例如静脉内给药后在体内给药时,负载胶粒的高稳定性和药物的良好保留(血液中的循环延长)。
在现有技术中,已经开发了用于在聚合胶粒中药物的共价包封的方法。在共价包封中,活性成分例如药物分子与聚合物链化合键合。然而,其缺点是需要进行有机合成以将药物分子偶联至高分子量聚合物链(具有随之而来的挑战),并且需要为每种药物分子开发新的聚合物,这限制了新的聚合物平台技术的适用性。共价包封也可通过交联进行,但这可具有一些缺点。例如,药物的释放必需通过连接药物和载体的接头的降解发生,有时这难以控制从而导致在目标作用点处药物浓度不足。
即使一些系统在体外显示良好的稳定性,但其可能出现体内稳定性不足。不希望受任何理论的束缚,假设一些血清蛋白可能能够结合两亲性聚合物分子,其可以破坏胶粒和单聚体(unimers)的动态平衡。因此,难以预测特定的体系在体内测试中是否会显示足够的稳定性。
另一个重要的性质是在给药后药物在胶粒中的充分保留,这对应于包封的药物在血液中的延长的循环。许多药物通常在人体或动物体内具有短的半衰期。因此,需要多次每日注射或连续输注以具有所需的治疗效果。这就是为什么用于控制或持续释放的系统对于这种目的是非常理想的。
因此,希望提供一种适用于受控递送系统以包封特定的疏水性活性成分的聚合物,所述系统在体内具有高稳定性,并且当给药于体内时显示良好的药物保留,并且避免了药物的共价包埋的缺点。
技术实现要素:
为了解决上述需要中的至少一些,在一个方面,本发明提供了一种嵌段共聚物,其包含至少一个亲水性嵌段和至少一个疏水性嵌段,其中所述疏水性嵌段选自下组:丙烯酸酯、甲基丙烯酸酯、丙烯酰胺、甲基丙烯酰胺、乙烯基醚和它们的芳族衍生物,其中至少一个疏水性嵌段含有芳族侧基,其由或通过可降解的接头与疏水性嵌段结合,其中所述芳族侧基是芳基。
另一方面,本发明提供一种包括根据本发明的嵌段共聚物和物理包埋的活性成分的控释系统。
附图的简要说明
图1显示了根据本发明的加载胶粒的包封效率(%)和加载容量(%)与进料的ptx浓度(mg/ml)的关系图。ptx是紫杉醇,其被用作模型药物。
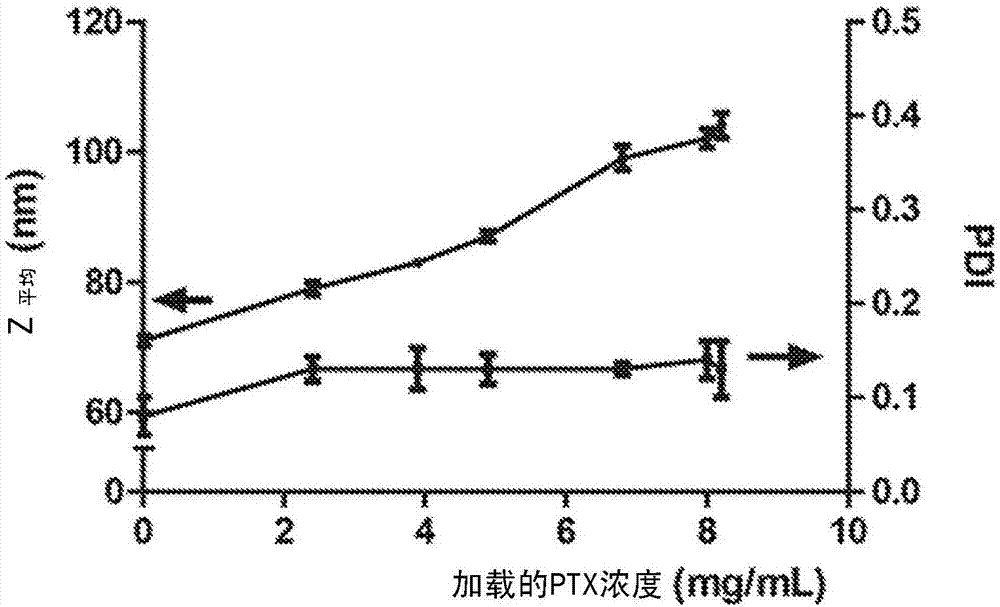
图2显示了通过动态光散射测定的根据本发明的加载胶粒的z平均流体动力学直径(z平均,nm)和多分散性指数(pdi)与加载的ptx浓度(mg/ml)的关系图。
图3显示及时测量的,在携带a431人肿瘤的雌性crl:nu-foxnu1nu小鼠中静脉内注射四种不同的ptx制剂后ptx的血浆浓度。
图4显示了加载ptx的mpeg-b-p(hpmam-bz)胶粒的静脉内注射后24小时,在小鼠不同器官中的注射剂量(id),单位为%/克器官。
图5a显示注射剂量(血液中的%id)与时间p.i(注射后)(单位为小时)的关系图。图5d显示肿瘤体积的注射剂量(%id/cm3肿瘤)与注射后时间(小时)的关系图。图5e显示了对于小鼠的不同器官的器官体积的注射剂量(%id/cm3器官)。模型药物是ptx。
图6显示在本发明的胶粒以及比较体系初始处理之后的天数内肿瘤尺寸的发展,单位为mm3,所述比较体系为
图7显示了相对于使用根据本发明的用ptx加载的胶粒与比较体系在初始处理之后的天数作图的百分比存活率,所述比较系统是
图8显示带有ptx(15mg/kg和30mg/kg)本发明的胶粒和比较体系在初始处理后的天数内肿瘤尺寸mda-mb-468异种移植的发展,单位为mm3,所述比较体系为
图9显示包封的活性剂的化学式。
图10显示mpeg-p(hpmam-bz)和mpeg-b-p(bhmpo)的化学式。
图11显示ph为7.4、6.5和5.0时对于mpeg-b-p(bhmpo)的空胶粒,通过dls测得的尺寸和光散射强度随时间的变化。
发明详述
本发明基于判断正确的认识,即当使用具有芳族侧基的特定聚合物时,可以增加聚合物胶粒的稳定性和物理包埋在所述胶粒中的疏水性药物的保留。令人惊讶的是,得到了具有在血液中长期循环的高度稳定的胶粒,用于仅物理包埋在所述胶粒中的药物。不希望受任何理论束缚,发明人相信聚合物链上的芳族侧基提供了增加的与药物分子的物理结合,特别当药物分子自身包含芳族基团时,由此产生了聚合物链和药物分子之间的芳香相互作用。聚合物链之间的芳香相互作用也有助于其在循环中的稳定性。
在本说明书和权利要求书中,术语“共聚物”是指存在至少两种类型单体的聚合物。“两亲性”是指同时具有疏水性和亲水性。
术语“活性成分”包括治疗剂和诊断剂。治疗剂是能在人体或动物体内起到预防、治疗或药理作用的化合物。预防或治疗作用通常理解为与人体或动物体内的细胞组织相互作用或对其作用的有益效果。合适的诊断相关的活性成分包括用于血管造影、mri、ct扫描成像,核磁共振成像、射线照相、x射线相衬成像、超声等的那些。特定的诊断活性成分是例如光敏剂、成像剂(例如mri造影剂)、放射性同位素化合物、荧光化合物、染料。
“疏水性”是指在辛烷-水中分配系数logp高于1。对于logp的定义参见chemicalreviews1971,第71卷,第6期。
本文所用的活性成分分子的“物理”包埋是“非共价”结合的同义词。“非共价相互作用”是指不是共价的任何相互作用,即原子或键之间的任何弱结合,其中所述结合不包括共享电子对。非共价相互作用的例子是疏水性相互作用、芳香(π-π)相互作用、氢键合相互作用、静电相互作用、立构复合相互作用和金属离子相互作用。包埋也用作活性成分的结合、加载或包封的同义词。
“接头”是指具有与分子的不同部分(或构成嵌段)(通常为两部分)连接的功能的化学基团。在本文的上下文中可降解的是指可生物降解的。“可水解的”是指可通过水解降解。“生理条件”是待用本发明的控释系统处理的生物体中存在的条件;对于人类,这些条件包括约7.4的ph和约37℃的温度。
根据本发明的共聚物是包括至少一种亲水性嵌段和至少一种疏水性嵌段的嵌段共聚物。因此,所述共聚物是两亲性嵌段共聚物。在水性溶液中,这些聚合物形成含有疏水性核的胶粒,其可被加载,具体加载疏水性药物。本发明的共聚物适用于在人体或动物体内使用的控释系统、靶向递送系统和其它系统。在一些实施方式中,这可表示本发明的共聚物是生物可吸收聚合物,或者所述共聚物在水解之后转化为生物可吸收聚合物,这意味着所述聚合物材料被人体安全地吸收并且其随时间从人体中消失。
本发明的聚合物可具有所有可能的聚合物结构,例如(多)嵌段共聚物(例如ab、aba、abab等)或接枝共聚物、无规共聚物或三元聚合物,或聚合物网络;所有这些可被接枝。
疏水性嵌段包含优选自下组的单体:丙烯酸酯、甲基丙烯酸酯、丙烯酰胺、甲基丙烯酰胺、乙烯基醚和它们的衍生物。更优选地,所述疏水性嵌段包含甲基丙烯酰胺或其衍生物,更优选为羟烷基甲基丙烯酰胺。对于衍生物,特别优选为芳族衍生物,这意味着所述衍生物包含芳族基团,更优选包含芳基或取代的芳基。优选的单体的例子包括甲基丙烯酸-2-羟乙基酯(hema)、丙烯酸-2-羟乙基酯(hea)、甲基丙烯酸甘油酯或甲基丙烯酸缩水甘油酯(gma)、丙烯酸甘油酯或丙烯酸缩水甘油酯(ga)、羟丙基甲基丙烯酰胺(hpmaam)。
本发明的共聚物的至少一种疏水性嵌段包含芳族侧基,其通过可降解的接头连接。芳族是指所述侧基含有至少一个芳环。芳族包括杂芳基和芳基。杂芳基在至少一个环中包含杂原子,例如n或s,并且被任选地取代。芳基在本说明书和权利要求书中是指通过从环碳原子中去除一个氢原子而从对应的芳烃衍生得到的单环或多环芳族烃基团,其被任选地取代。合适的芳族基团的例子是苯基、萘基、吲哚基和它们的衍生物。特别合适的芳基的例子是苯基和萘基。芳烷基也适合,例如芳甲基(特别是苯基)和其它在烷基部分中具有c1-c4碳原子的芳烷基。在一些实施方式中,所述芳族侧基优选为芳基或芳烷基。优选地,所述芳族基团是苄基、苯基或萘基或它们的衍生物,更优选为苯基或萘基。
优选地,存在的芳族基团为形成疏水性嵌段的单体的侧基的大于25mol%,更优选至少50mol%。更优选地,疏水性嵌段的单体的至少75mol%包含芳族基团,最优选地疏水性嵌段的单体的100mol%包含芳族基团。
在特定实施方式中,本发明的共聚物的疏水性嵌段不含有乳酸酯基。乳酸酯基是指单乳酸酯基、二乳酸酯基或低聚乳酸酯(oligolactate)基。乳酸酯可用于为所述共聚物提供热敏性质。含有n-(2-羟丙基)甲基丙烯酰胺单乳酸酯作为疏水性嵌段的一部分的热敏性共聚物在y.shi等,biomacromolecules,2013,14,1826-1837中报道。然而,当本发明人在体内测试这些紫杉醇加载的胶粒时,他们观察到药物的半衰期小于2分钟,表明这些热敏胶粒的快速不稳定和/或药物从胶粒的快速释放。相反,用相同药物紫杉醇加载的根据本发明的胶粒的半衰期为约8小时。参见本申请的实施例3和图3。
在本发明中,可降解的接头用于将芳族侧基连接到疏水性嵌段的聚合物主链。这确保该基团与物理包埋的活性成分一起持续释放。所述接头优选是在生理条件下可降解的,更优选是所述接头在生理条件下是可水解的。但所述接头也可通过酶的作用水解。总体来说,可使用已知接头,选自酯、原酸酯、酰胺、碳酸酯、氨基甲酸酯、酸酐、缩酮、缩醛、腙和它们的衍生物。在一些实施方式中,使用酯接头,优选为通式–c(o)-o-的接头。在这种情况中,苯基与酯接头一起形成苯甲酰基,萘基与酯接头一起形成萘甲酰基。在其它实施方式中,使用腙接头。腙接头包含基团-c=n-n-。
在本发明一个具体实施方式中,使用ph敏感的接头。优选地,所述接头在ph小于7,更优选ph为6.5或更低时水解。
ph敏感性接头的优点是,它可以选择性地在酸度增加的区域,例如一些肿瘤或炎症部位释放包埋的药物。在细胞结合和载药的胶粒的内化之后,胶粒的降解和包埋药物的释放也可在具有较低ph值的核内体或溶酶体中发生。
特别优选的是具有以下通式的腙接头:
其中r1、r2可各自独立的为h或烷基,其中r3是烷基或酮基–c(o)-。优选地,所述烷基为c1-c3烷基。更优选地,r1或r2是甲基。在优选的实施方式中,r3是酮基–c(o)-。
对于本发明的共聚物的亲水性嵌段,可使用任何合适的聚合物。优选地,所述亲水性嵌段包含聚亚烷基二醇,更优选地包含聚乙二醇(peg)。
疏水性嵌段与亲水性嵌段的重量比优选为10:90-90:10,更优选为40:60-60:40。
可通过由单体的混合物开始并进行聚合反应来制备所述共聚物。优选地,通过自由基聚合获得所述共聚物。也可首先产生共聚物并最终通过偶联合适的基团来将其官能化。本领域技术人员了解共聚物的合成方法。合成单体的合适的方法的例子在y.shi等,biomacromolecules2013,14,1826-1837中阐述。可用于聚合反应的大分子引发剂的合成的例子在d.neradovic等,macromolecules,2001,34(22),第7589–7591页中阐述。
本发明优选的实施方式是本发明的共聚物在控释系统中或作为控释系统的使用,所述控释系统还包括至少一种物理包埋的活性成分。
因此,在另一方面,本发明提供了一种包括前述权利要求中任一项所述的嵌段共聚物和至少一种物理包埋的活性成分的控释系统。
优选地,所述聚合物为具有疏水性核的聚合物胶粒的形式,并且所述活性成分物理包埋在所述胶粒的疏水性核中。本发明的两亲性嵌段共聚物特别适用于形成聚合物胶粒形式的控释系统。反过来,聚合物胶粒特别适用于疏水性活性成分的包封和控制和靶向释放,因为它们可被包埋在胶粒的疏水性核中。
本发明的胶粒还特别适用于靶向药物递送;也就是说,它们可以由于epr效应(增强的渗透性和保留效应;参考maeda,h.;nakamura,h.;fang,j.,advanceddrugdeliveryreviews,2013,65,(1),71-79)在作用点(例如发炎的组织)选择性地累积。
如在实施例中所证明的那样,加载有紫杉醇的根据本发明的胶粒显示从胶粒缓慢释放(约10天内释放加载的50%),表明药物在胶粒中的良好保留。胶粒还显示出长的血液循环时间(半衰期约8小时)。加载ptx的胶粒显示了在小鼠中完全抑制肿瘤生长,而在相等剂量下,商业使用的ptx的
本发明的聚合物胶粒是相当单分散的。在一些实施方式中,胶粒的尺寸为20-100nm。这是指通过动态光散射测量的z-平均流体动力学直径。通过动态光散射测定,多分散指数pdi优选小于0.3,更优选小于0.15。
活性成分优选是治疗剂或诊断剂。如上所述,可在相同的体系中加载(包埋)更多的活性成分。在本发明的具体实施方式中,控释系统包括两种活性成分。这些可以是例如两种治疗剂,其在组合治疗中特别有用,其中几种药物同时给药。另一个实施方式是包含治疗剂和诊断剂如成像剂(例如mri造影剂)的系统。
在一些实施方式中,优选地,所述活性成分分子包含至少一个芳族基团。在这种情况中,观察到被加载的胶粒特别稳定并具有体内药物的高保留。不希望受任何理论束缚,据信这可以通过聚合物链的芳族侧基和药物分子之间的增强的芳香相互作用来解释。
在优选的实施方式中,待包埋的活性成分的类型包括但不限于药物分子,例如(葡萄糖)皮质类固醇型或化学恒定型的药物分子、肽/蛋白质、成像剂、遗传物质或它们的组合。特别地,所述药物优选包括抗癌或细胞抑制药物、皮质类固醇、抗生素、抗病毒药物。不同化学来源的活性成分可以包埋在本发明的聚合胶粒中。特别地,本发明有利于包埋具有或不具有芳族基团的疏水性活性成分,其通常由于水溶性差而具有显著困难的递送问题。不具有芳族基团的疏水性活性成分的例子是地塞米松。具有芳族基团的疏水性活性成分的例子是贝达喹啉(bedaquiline)和紫杉醇。要被包封的疏水性活性成分优选具有至少1,更优选至少1.5的logp。活性成分的水溶性优选小于5mg/ml。
非疏水性活性成分也可被成功地包封,例如带有电荷的两亲性混合物,如盐。其例子是盐酸多柔比星。发现被成功包埋在本发明的胶粒中的活性成分的其它例子包括dapt(缺口抑制剂)和环孢菌素a(免疫抑制剂)。
在该用途特别优选的实施方式中,控释系统释放紫杉醇作为活性成分。
本发明的控释系统适用于治疗以炎症和血管通透性增加为特征的疾病。这些疾病包括但不限于选自下组的疾病:癌症、感染、眼科疾病、病毒感染、细菌感染、真菌感染、粘膜血浆感染、寄生虫感染、炎症、皮肤病、心血管疾病、中枢神经系统疾病,自身免疫性疾病、增殖性疾病、关节炎、精神病、牛皮癣、糖尿病、代谢紊乱、肺病、呼吸系统疾病、肺部疾病、copd、肌肉骨骼系统疾病、肺气肿、水肿、激素疾病。本发明的控释系统也适用于递送麻醉剂,用于疫苗接种,是治疗或预防性的。
出于清楚和简洁的目的,各特征在本发明中被描述为相同或单独的实施方式的一部分,然而,应理解本发明的范围可包括具有所有或一些所述特征的组合的实施方式。
下面通过非限制性实施例的方式描述本发明。除非另有说明,实施例和说明书中提及的份数和百分比均由重量表示。在实施例中,使用malvernalv/cgs-3测角仪,用动态光散射(dls)测定胶粒的平均粒度(z平均)和多分散指数(pdi)。用gemini300mhz光谱仪(维安联合有限公司(varianassociatesinc.),nmr仪器,美国加利福尼亚州的帕洛阿尔托市(paloalto,ca,usa))记录1h-nmr光谱。
实施例
实施例1共聚物合成
使用mpeg2-abcpa作为大分子引发剂,hpmam-bz作为单体来合成共聚物聚(乙二醇)-b-(n-(2-苯甲酰氧基丙基)甲基丙烯酰胺))(mpeg-b-p(hpmam-bz))。所述单体根据在y.shi等,biomacromolecules,2013,14,1826-1837中所述的方法合成。苯基通过酯接头连接至hpma单体。大分子引发剂合成在d.neradovic等,macromolecules,2001,34(22),第7589–7591页中阐述。
将单体以0.3g/ml的浓度溶于乙腈(在a4分子筛上干燥),单体与大分子引发剂的摩尔比为200/1。通过用氮气冲洗将溶液脱气30分钟。所述反应在氮气气氛下在70℃下进行24小时。聚合物通过在二乙醚中沉淀来纯化,并将该溶解/沉淀过程重复两次。将聚合物在室温下真空干燥24小时,收集为白色粉末。
通过凝胶渗透色谱法(gpc)分析,合成的聚合物的数均分子量(mn)为20,000da(pdi为mw/mn为1.7),而通过1hnmr分析,合成的聚合物的数均分子量(mn)为22,000da。共聚物中peg的含量为约23重量%(基于nmr分析,peg为5,000da,疏水性嵌段为17,000da)。根据langmuir,2004,20(21),第9388-9395页中报道的方法,使用芘作为探针测量,聚合物的临界胶粒浓度(cmc)为1.3μg/ml。
使用mpeg2-abcpa作为大分子引发剂,使用hpmam-nt作为单体,按照类似的方法制备萘甲酰基衍生物mpeg-b-p(hpmam-nt)。单体与大分子引发剂的摩尔比为250/1。
实施例2胶粒的制备
按照以下方法制备空mpeg-b-p(hpmam-bz)胶粒。将mpeg-b-p(hpmam-bz)以27mg/ml的浓度溶解在thf中,随后在搅拌下将1ml聚合物溶液滴加到1ml反渗透(ro)水中。将混合物在室温下孵育48小时以使thf蒸发。通过0.45μm尼龙膜
通过以下方法制备加载紫杉醇(ptx)的胶粒。将ptx和mpeg-b-p(hpmam-bz)(结构如图10所示)溶解在thf中,ptx浓度为3-12mg/ml,聚合物浓度为27mg/ml。在搅拌下将1ml聚合物溶液滴加入1ml反渗透(ro)水中。将混合物在室温下孵育48小时以使thf蒸发。通过0.45μm尼龙膜
根据y.shi等,biomacromolecules,2013,14,1826-1837中描述的方法进行加载ptx的胶粒的加载容量、包埋效率、尺寸和尺寸分布(dpi)的测量。结果见图1和2。
图1显示了加载胶粒的包封效率(%)和加载容量(%)与进料的ptx浓度(mg/ml)的关系图。
图2显示了通过动态光散射测定的加载胶粒的z平均流体动力学直径(z平均,nm)和多分散性指数(pdi)与加载的ptx浓度(mg/ml)的关系图。从图中可以看出,本发明的聚合物胶粒是相当单分散的,优选具有约70-100nm的尺寸,多分散指数pdi小于0.15。
结果表明,ptx的进料浓度最高达10mg/ml,药物包封效率非常好(>80%),使得在进料浓度为10mg/ml下得到具有高药物加载(约25%(w/w))的制剂。
实施例3体内研究
人a431肿瘤异种移植通过皮下接种建立在小鼠右侧腋下,1×106的a431细胞悬浮于100μlpbs,ph7.4中。使用数字卡尺测量肿瘤。使用公式v=
在携带a431人肿瘤的雌性crl:nu-foxnu1nu小鼠(22.5±2.5g),小鼠(n=7-8)中静脉内注射不同的ptx制剂后ptx的血浆浓度。
四种制剂包括根据实施例2得到的加载ptx的本发明的胶粒mpeg-b-p(hpmam-bz)和三种比较制剂,分别是在热敏性胶粒的mpeg-b-p(hpmam-bz30-共聚-hpmam-lac70)和mpeg-b-p(hpmam-nt25-共聚-hpmam-lac75)中加载的ptx,以及市售的
如图3中所看到的,在注射后24小时,来自接受
可以得出结论,根据本发明的两亲性嵌段共聚物形成稳定的胶粒,其具有优异的加载的ptx的保留性。
图4显示了加载ptx的mpeg-b-p(hpmam-bz)胶粒的静脉内注射后24小时,在小鼠不同器官中的注射剂量(id),单位为%/克器官。接受
实施例4体内动力学研究
在该实施例中,使用荧光团标记cy7和cy5.5在体内研究具有ptx的加载胶粒的动力学性质。cy7与聚合物链共价连接并报告注射的胶粒的命运;cy5.5物理加载在胶粒的核中并用作模式药物。
根据实施例1,相对于在聚合物的疏水嵌段中共聚的hpmam-bz,用2mol%的aemam(n-(2-氨基乙基)甲基丙烯酰胺盐酸盐)合成mpeg-b-p(hpmam-bz-共聚-aemam)。随后将mpeg-b-p(hpmam-bz-共聚-aemam)的伯胺侧基与cy7nhs酯反应。为此,将cy7nhs酯溶解于dmso(在4埃分子筛上干燥),浓度为10mg/ml。将聚合物(31mg)转移到干燥的烧瓶中,加入0.18mlcy7nhs酯溶液(10mg/ml)和1μl的tea(在4埃分子筛上干燥),反应在50℃下进行48小时。通过用thf/水(1/1,v/v)透析除去未偶联的cy7,24小时后刷新透析液总共5次。冷冻干燥后收集最终产物,冻干后作为深绿色粉末收集。
与实施例2中描述的加载ptx的mpeg-b-p(hpmam-bz)胶粒类似地制备用cy7化学标记并用cy5.5物理加载的mpeg-b-p(hpmam-bz)胶粒。简言之,在搅拌下,将26.6mg未标记的mpeg-b-p(hpmam-bz),0.4mgcy7标记的mpeg-b-p(hpmam-bz)和0.02mgcy5.5(作为物理加载的模式药物)的1mlthf溶液滴加到1ml水中。将胶粒分散体在室温下孵育48小时以使thf蒸发。随后,通过0.45μm尼龙膜
cd-1裸雌性小鼠(n=5)自由喂食无叶绿素食物颗粒和水,笼养在通风笼和临床控制的房间和大气中。动物研究按照国家规定制定的指导方针进行,经当地动物实验伦理委员会批准。在实验开始前15天,将cd-1裸小鼠皮下接种a431肿瘤细胞(4×106细胞/100μlpbs,ph7.4)至右侧腋下,致使a431肿瘤异种移植物发展,其大致尺寸为宽6-7mm。
图5显示了用cy5.5(n=5)作为模式药物加载的cy7标记的mpeg-b-p(hpmam-bz)胶粒的循环动力学、肿瘤积聚和体内生物分布。在图5a中,显示了注射剂量(血液中的%id)与时间p.i(注射后)(单位为小时)的关系图。在图5d中,显示了对于肿瘤体积的注射剂量(%id/cm3肿瘤)与注射后时间(小时)的关系图。图5e显示了对于小鼠的不同器官的器官体积的注射剂量(%id/cm3器官)。模型药物是cy5.5。
由于cy7标签与聚合物共价连接,因此报告了注射胶粒的命运。很明显,根据ptx的血浆动力学数据(图3),胶粒的半衰期约为8小时。cy5.5标签显示较短的半衰期,最有可能是因为该化合物更具亲水性,因此在胶粒中的保留比ptx少。
图6显示了在初始治疗后的几天中肿瘤尺寸的发展以mm3表示。较低的两条曲线表示用ptx加载的本发明胶粒的数据。另外三条曲线提供了作为比较数据的用市售
在雌性crl:nu-foxnu1nu小鼠(22.5±2.5g)中生长的人a431肿瘤用pbs、空mpeg-b-p(hpmam-bz)胶粒、
图7显示了根据本发明和比较系统,对具有ptx的加载胶粒初始处理后的天数绘制的百分比存活率图。
结果表明,聚合物胶粒制剂的治疗效果令人印象深刻。对于接受高剂量胶粒制剂(30mgptx/kg)的动物,在36天观察到完全肿瘤消退。此外,低剂量胶粒制剂(15mgptx/kg)显示比相等剂量的市售
实施例5体内研究,缓慢生长的肿瘤
与实施例4类似,在携带mda-mb-468乳腺癌异种移植物的小鼠中研究了加载ptx的mpeg-b-p(hpmam-bz)胶粒的治疗功效。在本研究中,小鼠接受与a431研究(实施例4)类似的处理,但是静脉内注射每周一次,而不是每隔一天注射一次。当肿瘤体积达到约100mm3时,在肿瘤细胞接种后4周开始治疗。
图8显示了在初始治疗后的几天中肿瘤尺寸的发展以mm3表示。较低的两条曲线表示用ptx加载的本发明胶粒的数据。另外三条曲线提供了作为比较数据的用市售
图8显示,
加载ptx的聚合物胶粒的重复注射通常耐受性良好,并且小鼠在治疗功效研究的整个过程中没有显著的体重减轻。此外,通过组织病理学分析代表性地评估肝脏、脾脏和肾脏,没有观察到空的或加载ptx的聚合物胶粒的器官毒性。这些观察结果表明所述胶粒制剂具有有利的毒性特征。
如这些实施例所示,本发明的控释系统是用于开发ptx-纳米药物的有吸引力的载体系统。聚合物胶粒以直接和成本有效的方式生产,而不需要化学交联或共价药物偶联,并且其特征在于优异的加载容量、增强的稳定性和强的ptx保留性。对于a431和mda-mb-468细胞,胶粒ptx的ic50值与游离药物(即
实施例6不同活性剂的包封
根据包封方法来包封下列不同的药物:地塞米松、盐酸多柔比星(dox.hcl)、贝达喹啉、dapt和环孢霉素a。使用的聚合物是mpeg-b-p(hpmam-bz),批号为j01(mn48.000,[单体]/[引发剂]=600/1)和j02(mn59.000,[单体]/[引发剂]=1000/1),和j03为mpeg-b-p(hpmam-nt)250(mn32.000,[单体]/[引发剂]=250/1)。通过nmr测得分子量mn。活性剂的化学式在图9中显示。
加载药物的胶粒制剂的制备:在搅拌下将溶解有5mg聚合物和1mg药物/候选药物的1ml四氢呋喃滴加入1ml反渗透(ro)水中,并将所述混合物再保持搅拌1分钟。将所述混合物放置在通风橱中过夜以蒸发四氢呋喃。通过0.45μm膜过滤载药的胶粒分散体(除了dox制剂),并通过dls(形成的胶粒的尺寸)分析过滤物并将过滤物溶解在乙腈中(将1体积的胶粒分散体加入到19体积的乙腈中)以用于通过紫外-可见光谱测量封装效率(ee)和加载容量(lc)(除了通过hpcl分析的紫杉醇以外的所有药物)。对于加载dox.hcl的胶粒,使用vivaspin管在10000g下将所述制剂离心5分钟,并通过紫外-可见光谱法定量过滤物中的未加载的药物以计算ee和lc。结果示于表1。
表1
该表显示,具有logp>1的药物和候选药物可以被成功地加载到具有高ee和lc的聚合物胶粒中。这些包括具有芳香族基团的药物(ptx、贝达喹啉、dox.hcl、dapt和伊马替尼游离碱),无芳香族基团的疏水性药物(地塞米松和环孢菌素a),具有芳族基团的药物(候选物)以及具有带电荷的基团的药物(dox.hcl,伊马替尼游离碱和苯乙胺)。除了具有不同分子量的苯甲酰基的聚合物之外,该表显示用萘基改性的聚合物(peg-p(hpmam-nt)250)对紫杉醇的良好ee和lc。
实施例7ph敏感的胶粒
1-[2-(2-苯甲酰肼叉)丙基氨基]-2-甲基-2-丙-1-酮(bhmpo)的合成
在180℃下干燥过夜的烧瓶中,在氮气氛中在室温下,将1-(丙酮基氨基)-2-甲基-2-丙-1-酮(ampo,677mg,4.8mmol)和4-甲氧基苯酚(聚合抑制剂,6mg;0.05mmol)溶解在146ml甲醇(在a4分子筛上干燥)中。根据acsbiomater.sci.eng.,2015,1(6),第393–404页中所述的方法合成ampo。在该溶液中加入bh(626mg,4.6mmol)。搅拌5分钟后,将7.5ml冰醋酸加入到所述溶液中,并在室温下在氮气气氛中保持搅拌该反应24小时。在减压下除去溶剂,并用己烷/乙酸乙酯(1/9,v/v)的洗脱液通过硅胶柱色谱(40g)纯化粗产物。收集含有rf为0.4的化合物(己烷/乙酸乙酯(1/1,v/v))的组分,并减压除去溶剂。收集最终产物为黄色粉末,产率为834mg(71%),熔点为164℃,用差示扫描量热法(discovery,ta仪器公司)测定。使用gemini300mhz光谱仪(维安联合有限公司,nmr仪器,美国加利福尼亚州的帕洛阿尔托市)通过1hnmr分析证实该结构,使用dmso-d6作为溶剂;使用2.52ppm处的dmso峰作为参考线。化学位移(dmso-d6):11.3(s,c=n-nh-co),8.7(t,co-nh-ch2),7.9(d,2h,芳族ch),7.5(m,3h,芳族ch),5.7和5.4(s,ch2=c),4.0(d,nh-ch2-c),2.0(s,ch3-c=c),1.9(s,ch2-c(ch3)=n)。
mpeg-b-p(bhmpo)的合成
通过大分子引发剂途径,使用mpeg2-abcpa作为大分子引发剂,bhmpo作为单体合成mpeg-b-p(bhmpo)的嵌段共聚物。将单体以0.3g/ml的浓度溶于dmso(在a4分子筛上干燥),单体与大分子引发剂的摩尔比为200/1。通过用氮气冲洗将溶液脱气30分钟。所述反应在氮气气氛下在70℃下进行24小时。聚合物通过在二乙醚中沉淀来纯化,并将该溶解/沉淀过程重复两次。将聚合物在室温下真空干燥24小时,收集为淡黄色粉末。
制剂制备
通过以下方法制备紫杉醇(ptx)加载的mpeg-b-p(bhmpo)(通过nmr测得23kda;结构在图10中显示)胶粒:在搅拌下,将1ml在thf/meoh(=四氢呋喃/甲醇)(1/1,v/v)中的ptx(4mg)和聚合物(27mg)的溶液滴加到1mlro水中,将10μl磷酸盐缓冲液ph7.4(1m)加入到混合物中以将ph调节至7.4。将胶粒分散体在室温下孵育24小时以蒸发有机溶剂。随后,通过0.45μm膜过滤所述胶粒分散体。用动态光散射分析测定形成的胶粒的尺寸并通过hplc测定ptx加载。测得的ptx浓度为3.3mg/ml,包封效率(ee)为83%,粒度为83nm,pdi为0.08。
空mpeg-b-p(bhmpo)胶粒的ph依赖稳定性
使用上述方法制备空mpeg-b-p(bhmpo)胶粒而不加入ptx。通过分别在ph5.0的150mm乙酸铵缓冲液或ph6.5的nah2po4缓冲液中将胶粒稀释5倍,将胶粒分散体的ph调节至5.0或6.5。通过由dls监测胶粒的尺寸和光散射强度,研究了在37℃和不同ph值下空mpeg-b-p(bhmpo)胶粒的ph依赖稳定性。结果示于图11。
如图11所示,苯甲酰基和聚合物主链之间的腙键对酸性ph值(6.5和5.0)敏感,而在中性ph(7.4)下稳定。因此,预期胶粒在血液循环中是稳定的,并且在肿瘤组织和细胞中特异性降解,由此可释放加载在胶粒中的ptx以杀死肿瘤细胞。
- 还没有人留言评论。精彩留言会获得点赞!