一种药物组合物及其在制备抗感染药物中的应用的制作方法
本发明属于生物医药领域,涉及一种药物组合物及其制备方法,具体涉及该药物组合物在制备抗感染疾病药物中的应用。
背景技术:
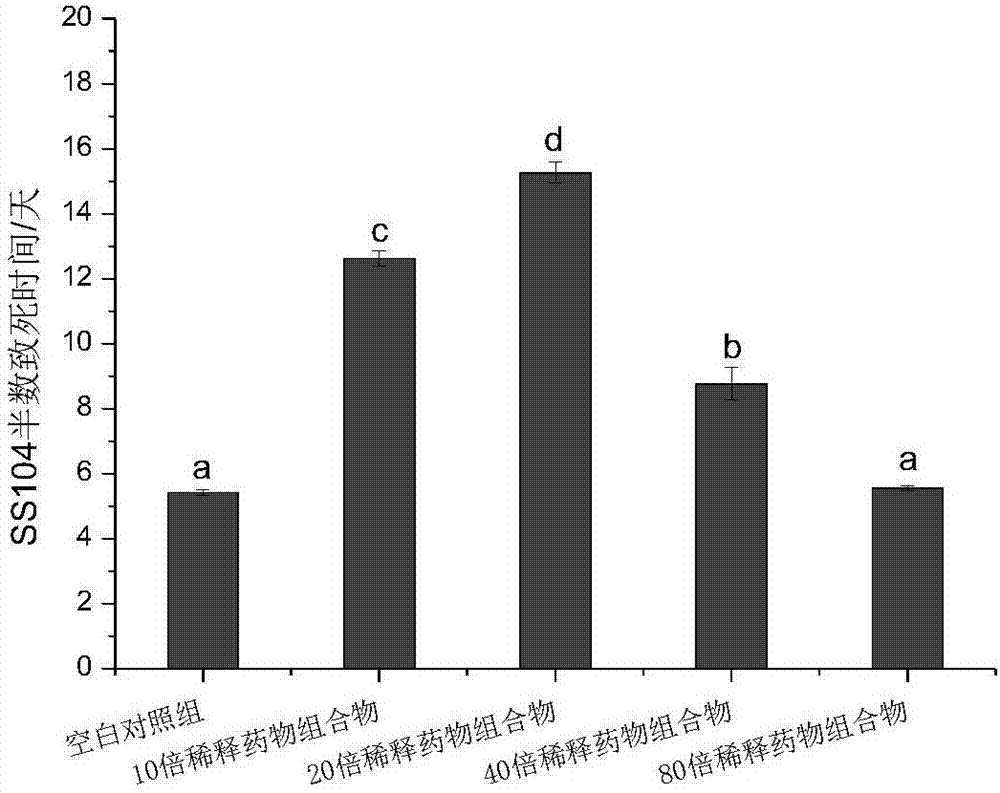
:随着抗生素的广泛应用及其滥用,越来越多的细菌对抗生素药物出现了不敏感现象,甚至是产生了严重的耐药性。尽管科学家不断研究制造抗菌谱更广、抗菌作用更强的新抗生素,但却仍然不能控制耐药菌的产生和发展。因此,寻找具有抗菌效果的新型药物迫在眉睫。ausubel实验室曾利用e.faecalisstrainsmmh594,og1rf,og1rf△fsrb,v583,vs583等感染野生型n2秀丽隐杆线虫(caenorhabditiselegans,缩写c.elegans)及glp-4(bn2ts);sek-1(km4)突变株系线虫对6000种合成药及1136种天然提取药进行抗感染药效的筛选,并成功筛选出16种具有高抗感染活性的药物。杨再昌等在ausubel的实验基础上,利用c.elegans观察了黄连中药的体内抗感染药效,发现中草药黄连具有体内抗感染作用,而黄连已在感染小鼠实验中证明具有较好的抗感染效果。因此,秀丽隐杆线虫感染模型能够对具有抗感染作用的药物进行有效的筛选。本发明公开了一种药物组合物,所述药物组合物包括炙黄芪、炙甘草,该药物组合物具有显著的体内抗感染作用,且在半数致死时间之前,与其拆方相比,药物组合物能维持更显著的药效。因此本发明所提供的药物组合物可在制备抗感染的药物中应用。技术实现要素:本发明提供了一种药物组合物,所述的药物组合物包括炙黄芪和炙甘草,按重量份,所述炙黄芪为0.1875-15份,炙甘草为0.03125-2.5份。其中,所述的炙黄芪为0.1875g,炙甘草为0.03125g。其中,所述的炙黄芪为15g,炙甘草为2.5g。其中,上述所述的药物组合物的制备方法如下:a、按比例称取药材炙黄芪,炙甘草,加蒸馏水,浸泡20min,煮沸30min;b、停止加热,冷却后,滤出即得第一次煎煮液;c、将b所得药渣加与a等体积蒸馏水,煮沸30min;d、停止加热,冷却后,滤出即得第二次煎煮液;e、合并b、d所得煎煮液,定容;f、将e所得煎煮液在12000rpm,10min条件下离心2次,沉淀药渣,留取上清液;g、将f所得上清液用0.22μm的无菌滤头过滤除菌即得。其中,所述的药物组合物的生药浓度为4.375-35g/l。本发明还提供了所述的药物组合物在制备抗感染药物中的应用。其中,所述的感染是由粪肠球菌或铜绿假单胞菌引起的。另外,本发明还提供了一种制备上述所述的药物组合物的制备方法,所述的药物组合物的制备方法如下:a、按比例称取药材炙黄芪,炙甘草,加蒸馏水,浸泡20min,煮沸30min;b、停止加热,冷却后,滤出即得第一次煎煮液;c、将b所得药渣加与a等体积蒸馏水,煮沸30min;d、停止加热,冷却后,滤出即得第二次煎煮液;e、合并b、d所得煎煮液,定容;f、将e所得煎煮液在12000rpm,10min条件下离心2次,沉淀药渣,留取上清液;g、将f所得上清液用0.22μm的无菌滤头过滤除菌即得。附图说明图1为不同浓度药物组合物对秀丽隐杆线虫ss104-e.faecalisog1rf感染模型寿命影响的药效比较。图2为不同浓度药物组合物对秀丽隐杆线虫ss104-e.faecalisog1rf感染模型寿命的半数致死时间影响的药效比较。图3为20倍稀释的药物组合物及其同倍稀释的拆方对秀丽隐杆线虫ss104-e.faecalisog1rf感染模型寿命影响的药效比较。图4为20倍稀释的药物组合物及其同倍稀释的拆方对秀丽隐杆线虫ss104-e.faecalisog1rf感染模型寿命的半数致死时间影响的药效比较。图5为20倍稀释的药物组合物对秀丽隐杆线虫ss104-p.aeruginosa感染模型寿命影响的药效比较。图6为20倍稀释的药物组合物对秀丽隐杆线虫ss104-p.aeruginosa感染模型寿命的半数致死时间影响的药效比较。具体实施方式下面结合具体实施例进一步详细描述本发明的技术方案,但本发明的保护范围不局限于所述实施例。实施例一药物组合物水煎液的制备材料:炙黄芪和炙甘草购买于兰州惠仁堂药业连锁有限责任公司。本发明的药物组合物包括炙黄芪15g,炙甘草2.5g。制备方法:所述的药物组合物的制备方法如下:a、称取药材炙黄芪15g,炙甘草2.5g,加蒸馏水150ml,浸泡20min,煮沸30min;b、停止加热,冷却后,滤出即得第一次煎煮液;c、将b所得药渣加蒸馏水150ml,煮沸30min;d、停止加热,冷却后,滤出即得第二次煎煮液;e、合并b、d所得煎煮液,定容至50ml;f、将e所得煎煮液在12000rpm,10min条件下离心2次,沉淀药渣,留取上清液;g、将f所得上清液用0.22μm的无菌滤头过滤除菌即得。实施例二药物组合物水煎液的体外抑菌作用1、生物材料(1)埃希氏菌属大肠杆菌op50(e.coliop50),购自caenorhabditisgeneticscenter(cgc)。(2)金黄色葡萄球菌staphylococcusaureusatcc29213(s.aureusatcc29213),购自美国菌种保藏中心(atcc),编号29213。(3)铜绿假单胞菌pseudomonasaeruginosaatcc27853(p.aeruginosaatcc27853)购自美国菌种保藏中心(atcc),编号27853。(4)粪肠球菌enterococcusfaecalisatcc29212(e.faecalisatcc29212)购自美国菌种保藏中心(atcc),编号29212。(5)白色念珠菌canidiaalbicansatcc10231(c.albicansatcc10231)购自美国菌种保藏中心(atcc),编号10231。2、试剂(1)药物:实施例一制备得到的药物组合物。(2)固体bhi(brainheartinfusion)培养基成分与制作(以1升为例)(bhi培养基购自青岛海博生物技术有限公司):成分含量bhi38.50g琼脂粉17.00g补充h2o至1000ml固体bhi培养基配制好后,121℃下高压恒温灭菌20min,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(3)固体lb(lysogenybroth)培养基成分与制作(以1升为例):成分含量蛋白胨10.00g酵母粉5.00gnacl10.00g琼脂粉17.00g补充h2o至1000ml固体lb培养基配制好后,121℃下高压恒温灭菌20min,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(4)固体mh(mueller-hinton)培养基成分与制作(以1升为例):成分含量牛肉浸膏6.00g可溶性淀粉1.50g酸水解酪蛋白17.50g琼脂粉17.00g补充h2o至1000ml固体mh培养基配制好后,121℃下高压恒温灭菌20min,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(5)固体改良马丁培养基成分与制作(以1升为例):成分含量蛋白胨5.00gk2hpo41.00g酵母粉2.00gmgso40.50g葡萄糖20.00g琼脂粉17.00g补充h2o至1000ml固体改良马丁培养基配制好后,121℃下高压恒温灭菌20min,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(6)固体营养肉汤培养基成分与制作(以1升为例):固体营养肉汤培养基配制好后,121℃下高压恒温灭菌20min,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。3、仪器高压灭菌锅(上海申安医疗器械厂)单人单面净化工作台(苏州净化设备厂)恒温培养摇床(上海一恒科技有限公司)连续变倍体视显微镜(上海一恒科学仪器有限公司)电子天平(北京赛多利斯仪器系统有限公司)漩涡搅拌器(上海精科仪器有限公司)离心机(ct15e,日立)4、实施步骤(1)菌液培养:取20μls.aureus的菌液在营养肉汤固体培养基上划单克隆,37℃培养48h。挑单克隆于150ml营养肉汤液体培养基中,37℃,180rpm,振荡培养至培养基混浊。4℃冷藏,备用。取20μlp.aeruginosa的菌液在lb固体培养基上划单克隆,37℃培养48h。挑单克隆于150mllb液体培养基中,37℃,180rpm,振荡培养至培养基混浊。4℃冷藏,备用。取20μle.coli的菌液在营养肉汤固体培养基上划单克隆,37℃培养48h。挑单克隆于150ml营养肉汤液体培养基中,37℃,180rpm,振荡培养至培养基混浊。4℃冷藏,备用。取20μle.faecalisatcc29212的菌液在bhi固体培养基上划单克隆,37℃培养48h。挑单克隆于150mlbhi液体培养基中,37℃,180rpm,振荡培养至培养基混浊。4℃冷藏,备用。取20μlc.albicans的菌液在改良的马丁固体培养基上划单克隆,37℃下培养48h。挑单克隆于150ml马丁液体培养基中,37℃,180rpm,振荡培养至培养基混浊。4℃冷藏,备用。(2)牛津杯法体外抑菌实验设置阴性对照组(无菌蒸馏水),阳性对照组(0.125g/l左氧氟沙星或100μg/ml制霉 素),药物组合物水煎液实验组。采用麦氏比浊法用相应菌的液体培养基将菌液稀释至0.5(即细菌数在1.5×108/ml,见表1)。在mh固体培养基板上,涂布200μl菌液,其中菌液包括:s.aureus、p.aeruginosa、e.coli、e.faecalis(每个菌株设置2~3个平行)。而在马丁固体培养基上涂布200μlc.albicans菌液,同样设置2~3个平行。待菌液被培养基吸收后,在每个培养基上各放置三个牛津杯,s.aureus、p.aeruginosa、e.coli、e.faecalis组的菌板分别加入200μl无菌蒸馏水、200μl0.125g/l左氧氟沙星、200μl药物组合物水煎液。c.albicans组的菌板分别加入200μl无菌蒸馏水、200μl100μg/ml制霉素、200μl药物组合物水煎液。放入37℃恒温箱培养,12h后进行观察。若12h后出现明显的抑菌圈,取出s.aureus、p.aeruginosa、e.coli、e.faecalis、c.albicans的各培养基,测量抑菌圈直径(mm)。当抑菌圈直径d≥20mm时定为极敏,记作“+++”;当抑菌圈直径15≤d<20mm时定为高敏,记作“++”;当抑菌圈直径10≤d<15mm时定为中敏,记作“+”;当抑菌圈直径d<10mm时定为低敏或无效,记作“-”。结果见表2。表1麦氏比浊法浊度bacl2(1.175%,g/l)h2so4(1%,v/v)细菌数×108/ml0.50.5ml99.5ml1.511.0ml99.0ml3.0表2药物组合物水煎液的体外抑菌结果表2中阴性对照组为无菌蒸馏水,阳性对照组为0.125g/l左氧氟沙星(可抑制大肠杆菌、金黄色葡萄球菌、铜绿假单胞菌、粪肠球菌生长)或100μg/ml制霉素(可抑制白色念珠菌生长),实验组为药物组合物原液。表2中所展示的是阴性对照组、阳性对照组及药物组合物水煎液抑菌圈直径的测量数值。从结果中可以看出,本发明所公开的的药物组合物水煎液在该浓度下对五种供试菌均无直接 抑制生长作用,说明本发明所公开的药物组合物水煎液在该浓度下无体外抑菌效果。实施例三药物组合物水煎液及其拆方的体内抗感染作用1、生物材料(1)c.elegansss104购自caenorhabditisgeneticscenter;基因型为glp-4(bn2)i,在温度为20℃的恒温箱里能正常生长,并繁殖后代,在温度为25℃的恒温箱里生长可诱导不育。(2)埃希氏菌属大肠杆菌op50(e.coliop50),购自caenorhabditisgeneticscenter,作为秀丽隐杆线虫的食物。(3)粪肠球菌enterococcusfaecalisog1rf(e.faecalisog1rf)购自美国菌种保藏中心(atcc),编号47077。(4)铜绿假单胞菌pseudomonasaeruginosaatcc27853(p.aeruginosaatcc27853)购自美国菌种保藏中心(atcc),编号27853。2、试剂(1)药物:实施例一制备得到的药物组合物水煎液;拆方炙黄芪;拆方炙甘草。炙黄芪:称取15g;炙甘草:称取2.5g;制备方法如下:a、按配方称取药材,加蒸馏水150ml,浸泡20min,煮沸30min;b、停止加热,冷却后,滤出即得第一次煎煮液;c、将b所得药渣加蒸馏水150ml,煮沸30min;d、停止加热,冷却后,滤出即得第二次煎煮液;e、合并b、d所得煎煮液,定容至50ml;f、将e所得煎煮液在12000rpm,10min条件下离心2次,沉淀药渣,留取上清液;g、将f所得上清液用0.22μm的无菌滤头过滤除菌即得。(2)固体ngm(nematodegrowthmedium)培养基成分与制作(以1升为例):成分含量nacl3.00gk2hpo42.34gkh2po417.23g蛋白胨2.50g琼脂粉17.00g补充h2o至1000ml固体ngm培养基配制好后,121℃下高压恒温灭菌20min,在无菌操作台下加入5g/l胆固醇1ml,1mmgso41ml,1mcacl21ml,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(3)固体bhi(brainheartinfusion)培养基成分与制作(以1升为例)(bhi培养基购自青岛海博生物技术有限公司):成分含量bhi38.50g琼脂粉17.00g补充h2o至1000ml固体bhi培养基配制好后,121℃下高压恒温灭菌20min,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(4)改良ngm培养基成分与制作(以1升为例):成分含量nacl3.00gk2hpo42.34gkh2po417.23g蛋白胨3.50g琼脂粉17.00g补充h2o至1000ml改良ngm培养基配制好后,121℃下高压恒温灭菌20min,在无菌操作台下加入5g/l胆固醇1ml,1mmgso41ml,1mcacl21ml,摇匀,趁热倒入已灭菌培养皿。静置等待培养基凝固,备用。(5)m液配方成分含量na2hpo46.00gkh2po43.00gnacl5.00g1mmgso41.00ml补充h2o至1000ml配制好m液之后,121℃下高压恒温灭菌20min,待其冷却,置于室温下,备用。(6)秀丽隐杆线虫裂解液的配制取0.32ml的naclo液体溶于4.68ml的m液,再加入5ml1m的naoh溶液,即为秀丽隐杆线虫裂解液。(7)配制不含药物的bhi培养基吸取3ml无菌蒸馏水,溶于27ml灭菌之后的bhi培养基中,再把培养基均分至10个35mm的培养皿中。(8)配制含有不同浓度药物组合物水煎液的bhi培养基吸取3ml的药物组合物水煎液溶于27ml灭菌之后的bhi培养基,即为10倍稀释的药物组合物;吸取4ml的药物组合物水煎液溶于4ml的无菌蒸馏水,记为液体1,吸取3ml液体1溶于27ml灭菌之后的bhi培养基,即为20倍稀释药物组合物;吸取4ml的液体1溶于4ml的无菌蒸馏水,记为液体2,吸取3ml液体2溶于27ml灭菌之后的bhi培养基,即为40倍稀释的药物组合物;吸取4ml的液体2溶于4ml的无菌蒸馏水,记为液体3,吸取3ml液体3溶于27ml灭菌之后的bhi培养基,即为80倍稀释的药物组合物。即分别得到生药浓度为35g/l、17.5g/l、8.75g/l、4.375g/l的10倍稀释的药物组合物、20倍稀释的药物组合物、40倍稀释的药物组合物、80倍稀释的药物组合物。将含不同浓度药物组合物的培养基均分至10个35mm的培养皿中。(9)配制含有不同药物组别水煎液的bhi培养基分别吸取2ml的不同药物组别水煎液溶于2ml的无菌蒸馏水,记为液体1,分别吸取3ml液体1溶于27ml灭菌之后的bhi培养基,即为20倍稀释的不同药物组别水煎液。将含20倍稀释的不同药物组别水煎液的培养基均分至10个35mm的培养皿中。(10)配制不含药物水煎液的改良ngm培养基吸取3ml无菌蒸馏水,溶于27ml灭菌之后的改良ngm培养基中,把培养基均分至10个35mm的培养皿中。(11)配制含有20倍稀释的药物组合物水煎液的改良ngm培养基吸取2ml的药物组合物水煎液溶于2ml的无菌蒸馏水,记为液体1,吸取3ml液体1溶于27ml灭菌之后的改良ngm培养基,即为20倍稀释药物组合物。将含20倍稀释药物组合物的培养基均分至10个35mm的培养皿中。3、仪器4、实施步骤(1)秀丽隐杆线虫的培养:将秀丽隐杆线虫接在涂布有200μl大肠杆菌op50的固体ngm培养基上,然后置于20℃的恒温箱中培养,秀丽隐杆线虫长到成虫阶段开始产卵,当固体ngm培养基表面的卵数与幼虫数比例大约1:1时,进行同步化处理。(2)秀丽隐杆线虫同步化:挑选含有大量成虫并且有部分虫卵已经孵出的ngm培养基,用m液将秀丽隐杆线虫从培养基上冲下,转移到离心管中,静置使秀丽隐杆线虫自由沉降至管底,弃上清。根据秀丽隐杆线虫数量向离心管中加入秀丽隐杆线虫裂解液,在漩祸搅拌器上振荡5-7min待秀丽隐杆线虫全部断裂时停止涡旋,并分装于1.5ml离心管中,用m液洗虫卵三次,然后把秀丽隐杆线虫的卵直接加到涂有op50的含有药物的ngm培养基上。(一)不同浓度的药物组合物水煎液的体内抗粪肠球菌感染作用同步化后的c.elegansss10425℃恒温箱内生长到l4期时,用m液冲洗下c.elegansss104,收集在1.5ml离心管中,斡旋5s,1500rpm2min离心,重复操作两次。将冲洗干净的c.elegansss104接到涂布有e.faecalisog1rf固体bhi培养基上,于25℃恒温箱内培养24h。24h之后,将被粪肠球菌感染的c.elegansss104挑至涂布有e.faecalisog1rf不含药物的直径35mm的bhi培养基(空白对照组)及各涂布有e.faecalisog1rf含有不同浓度药物组合物的bhi培养基(实验组)上,每个处理设置3个平行,每个平行35条c.elegansss104,于25℃恒温箱内培养。每隔24h进行统计各对照组及实验组c.elegansss104的死活数,直到全部c.elegansss104死亡。图1、2中10倍稀释药物组合物、20倍稀释药物组合物、40倍稀释药物组合物、80倍稀释药物组合物分别代表生药量为35g/l的药物组合物水煎液,生药量为17.5g/l的药物组合物水煎液,生药量为8.75g/l的药物组合物水煎液,生药量为4.375g/l的药物组合物水煎液。空白对照组是无菌蒸馏水。图1的纵坐标表示感染状态下不同浓度药物处理的c.elegansss104的存活比例,在同一个时间点,此值越大,表明该处理组中存活的c.elegansss104数量越多,即药物延长e.faecalisog1rf感染状态下c.elegansss104的寿命的作用越强,由 图1可以看出,在每个时间点,20倍稀释药物组合物处理的c.elegansss104存活数都最大,且从图2(图中a、b、c、d表示各组之间的差异显著性,相同标记之间没有显著性差异)中的半数致死时间可以看出,10倍、20倍、40倍稀释药物组合物与其它组别均具有显著的差异,其中20倍稀释药物组合物具有极显著的差异,说明其在延长粪肠球菌感染状态下c.elegansss104的寿命均有明显作用,即均具有较好的体内抗感染效果。其中40倍稀释的药物组合物效果最佳。(二)20倍稀释的药物组合物水煎液及其同浓度的拆方对e.faecalisog1rf的体内抗感染作用同步化后的c.elegansss10425℃恒温箱内生长到l4期时,用m液冲洗下c.elegansss104,收集在1.5ml离心管中,涡旋5s,1500rpm2min离心,重复操作两次。将冲洗干净的c.elegansss104接到涂布有e.faecalisog1rf固体bhi培养基上,于25℃恒温箱内培养24h。24h之后,将被e.faecalisog1rf感染的c.elegansss104挑至涂布有e.faecalisog1rf不含药物的直径35mm的bhi培养基(空白对照组)及各涂布有e.faecalisog1rf含有20倍稀释的不同药物的bhi培养基(实验组)上,每个处理设置3个平行,每个平行35条c.elegansss104,于25℃恒温箱内培养。每隔24h进行统计各对照组及实验组c.elegansss104的死活数,直到全部c.elegansss104死亡。图3、4中20倍稀释药物组合物、20倍稀释黄芪、20倍稀释甘草分别代表生药量为17.5g/l的药物组合物水煎液,生药量为15g/l的拆方炙黄芪水煎液,生药量为2.5g/l的拆方炙甘草水煎液。空白对照组代表无菌蒸馏水。图3的纵坐标表示感染状态下20倍稀释的不同药物处理的c.elegansss104的存活比例,在同一个时间点,此值越大,表明该处理组中存活的c.elegansss104数量越多,即药物延长e.faecalisog1rf感染状态下c.elegansss104的寿命的作用越强。由图3寿命结果及图4(图中a、b、c表示各组之间的差异显著性,相同标记之间没有显著性差异)半数致死时间的结果表明,在半数致死时间之前,20倍稀释药物组合物具有极显著的体内抗感染效果,而拆方20倍稀释黄芪与空白对照组之间无显著性差异。综合实验结果表明,20倍稀释药物组合物的体内抗感染作用起效快,并能在半数致死时间之前维持极显著的药效,因此认为20倍稀释药物组合物较其同浓度的拆方具有更好的利用价值。(三)20倍稀释的药物组合物水煎液对p.aeruginosa的体内抗感染作用为了观察药物组合物除了能体内抗革兰氏阳性菌粪肠球菌外,是否还能抗革兰氏阴性菌,因此选择铜绿假单胞菌(p.aeruginosa)进行了探究。同步化后的c.elegansss10425℃恒温箱内生长到l4期时,用m液冲洗下c.elegans ss104,收集在1.5ml离心管中,斡旋5s,1500rpm2min离心,重复操作两次。将冲洗干净的c.elegansss104接到涂布有p.aeruginosa固体改良ngm培养基上,于25℃恒温箱内培养24h。24h之后,将感染好的c.elegansss104挑至涂布有p.aeruginosa不含药物的直径35mm的改良ngm培养基(空白对照组)及涂布有p.aeruginosa含有20倍稀释的药物组合物的改良ngm培养基(实验组)上,处理设置3个平行,每个平行35条c.elegansss104,于25℃恒温箱内培养。每隔24h进行统计各对照组及实验组c.elegansss104的死活数,直到全部秀丽隐杆线虫ss104死亡。图5、6中20倍稀释药物组合物代表生药量为17.5g/l的药物组合物水煎液。空白对照组表示无菌蒸馏水。图5的纵坐标表示感染状态下20倍稀释的药物处理的c.elegansss104的存活比例,在同一个时间点,此值越大,表明该处理组中存活的c.elegansss104数量越多,即药物延长铜绿假单胞菌感染状态下c.elegansss104的寿命的作用越强,在每个时间点,20倍稀释药物组合物处理的c.elegansss104存活数都比对照组的大,且从图6(图中a、b表示20倍稀释药物组合物与空白对照组之间有显著性差异)的半数致死时间可以清晰地看出,20倍稀释药物组合物与对照组具有极显著的差异,说明其在延长铜绿假单胞菌感染状态下c.elegansss104的寿命有明显作用,即说明20倍稀释药物组合物具有较好的体内抗感染效果。本发明提供的药物组合物在体外无抑菌效果的浓度下,不仅对革兰氏阳性菌感染疾病有治疗作用,同时对革兰氏阴性菌感染疾病同样有治疗作用,说明本发明所提供的药物组合物具有很好的体内抗感染效果。同时,本发明提供的药物组合物较其拆方的体内抗感染作用起效更快,并能在半数致死时间之前维持极显著的药效,具有更好的利用价值。综上所述,本发明提供的药物组合物可在制备治疗感染疾病的药物中应用。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1