氯硝柳胺在制备抗致瘤疱疹病毒药物中的应用的制作方法
本发明涉及一种化合物的新应用,特别涉及氯硝柳胺在制备抗致瘤疱疹病毒药物中的应用。
背景技术:
卡波氏肉瘤相关疱疹病毒KSHV(Kaposi’s sarcoma-associated herpesvirus)是疱疹病毒家族中的一员。KSHV感染诱生的卡波氏肉瘤KS是艾滋病患者中常见的恶性肿瘤,大约20%的艾滋病病人会伴有卡波氏肉瘤,并且AIDS-KS病人死亡率极高,其5年生存率只有约8%。正常人群中KSHV感染后95%以上个体不表现出临床症状和患病。但在免疫抑制的患者,如艾滋病患者、器官移植患者和放化疗患者中,KSHV有很高的感染率和极大的危害,可导致卡波氏肉瘤(Kaposi’s sarcoma,KS)、原发渗出性淋巴瘤(primary effusion lymphoma,PEL)以及多中心卡斯特慢病(multicentric castleman disease,MCD)等疾病。近年来在其他疾病中(如HBV慢性肝炎、吸毒和老年性疾病)也发现很高的KSHV感染率和恶性肿瘤,正逐渐引起重视。
EB病毒(Epstein-barr virus,EBV)与KSHV同属于γ-疱疹病毒,EBV可通过唾液传播,而近年来的一些研究显示这一病毒也能通过性行为传播。目前EBV感染全世界5岁以上人群中95%以上的个体,感染之后,EBV终生存在于携带者体内,呈潜伏感染状态,可引发多种人类疾病,包括传染性单核细胞增多症(Infection Mononucleosis,IM)、口腔毛状白斑症、神经系统疾病多发性硬化症(Multiple Sclerosis,MS)、Gianotti-Crosti综合征、多形红斑(Erythema Multiforme,EM)、急性外阴溃疡以及实质器官移植后多发的淋巴组织增生性疾病。目前常用的抑制病毒DNA合成来治疗疱疹病毒感染的药物(如无环鸟苷及其相关化合物)对这两种病毒感染疗效较差,疫苗也尚处于研发阶段。
氯硝柳胺作为一种驱虫药,其安全性已经被世界卫生组织所认可,此外有研究发现氯硝柳胺可能对细菌感染的治疗有一定作用。未有明确的实验数据表明氯硝柳胺对KSHV和EBV具有药物活性的报导。
技术实现要素:
本发明的目的在于提供氯硝柳胺在制备抗致瘤疱疹病毒药物中的应用。
发明人运用Western Bolt以及Real-time quantitative PCR等技术,检测KSHV阳性细胞BCBL1中KSHV相关基因的表达、及细胞外的病毒颗粒的含量;检测EBV阳性细胞,包括淋巴细胞P3HR-1及上皮细胞HNE1-2089中EBV相关基因的表达、细胞外的病毒颗粒的含量。实验发现氯硝柳胺处理后的细胞内KSHV或EBV相关基因的表达明显降低,且细胞外的病毒颗粒释放也有明显下降。这些抑制作用呈浓度依赖性,且在没有明显毒性的浓度就有很好的抗病毒作用,为进一步的抗病毒药物研发提供强有力的理论基础和实验依据,具有重要的研发价值和开发意义。基于此,可将氯硝柳胺开发为安全有效的抗KSHV或EBV药物。
附图说明
图1:氯硝柳胺在BCBL1细胞内对KSHV潜伏期蛋白LANA、裂解期蛋白RTA、K8、ORF64的表达的影响;
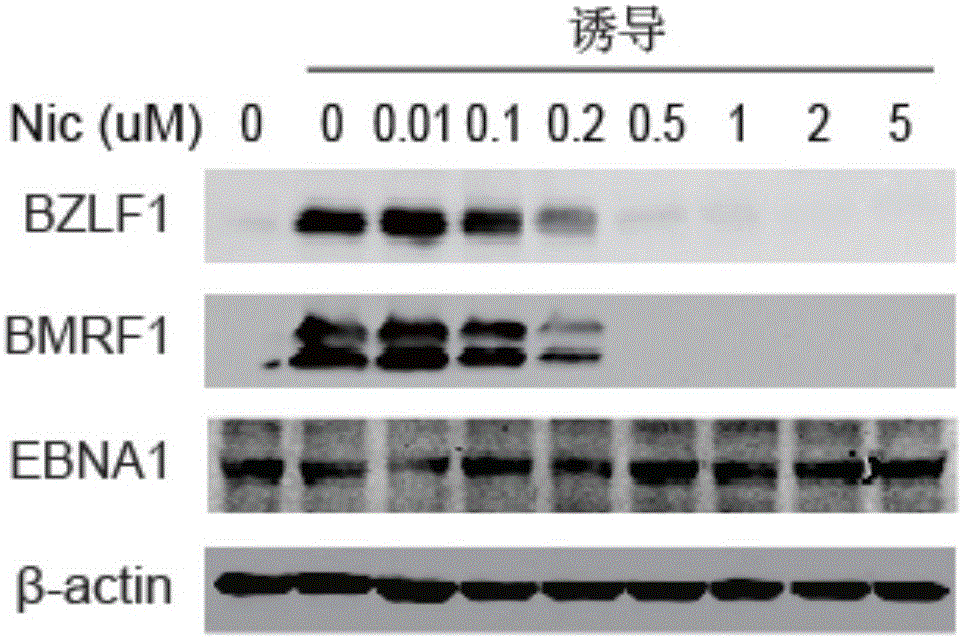
图2:氯硝柳胺在P3HR-1细胞内对EBV相关蛋白EA-D、ZTA表达的作用;
图3:氯硝柳胺在HNE1-2089细胞内对EBV相关蛋白EA-D、ZTA表达的作用;
图4:氯硝柳胺对BCBL1细胞内的病毒产量的影响;
图5:氯硝柳胺对P3HR-1细胞外的病毒产量的影响;
图6:氯硝柳胺对HNE-2089细胞外的病毒产量的影响;
图7:氯硝柳胺对PBMC细胞的存活影响。
具体实施方式
下面结合实验,进一步说明本发明的技术方案。
以下实验中,除非特别说明,本发明采用的试剂、设备和方法为本技术领域常规采购的试剂、设备和常规使用的方法。
实验原理:EBV、KSHV作为γ-疱疹病毒,生活周期都分为潜伏期和裂解期,细胞被感染后经过短暂的急性反应后迅速进入潜伏期,而经过特殊的刺激,细胞进入裂解期进行病毒扩增繁殖。因此,检测潜伏期和裂解期的相关蛋白表达可作为评估药物对于该两种病毒作用的一种手段。
本发明中简写为:TPA,大戟二萜酯;NaB,丁酸钠
实验1:在BCBL1细胞内对KSHV潜伏期蛋白LANA、裂解期蛋白RTA、K8、ORF64的表达的影响
1)取生长良好的BCBL1细胞,接种于6孔透明平底板中,每孔2×106细胞。使用的培养基是完全培养基:RPMI1640,10%胎牛血清以及1%双抗,培养条件是5%二氧化碳、37℃;
2)12h后加入诱导剂TPA,终浓度分别20ng/mL;
3)3小时后加入梯度浓度的氯硝柳胺,终浓度分别为0μM、0.1μM、0.2μM、0.5μM、1μM;
4)培养48h后,1000rpm,10min收获细胞,进行蛋白印迹实验。
结果如图1显示:在BCBL1细胞内KSHV相关蛋白RTA、K8、ORF64的表达受氯硝柳胺浓度的影响,呈一定的浓度依赖性。
实验2:氯硝柳胺在P3HR-1细胞内对EBV相关蛋白EA-D、ZTA表达的作用
1)取生长良好的P3HR-1细胞,接种于6孔透明平底板中,每孔2×106细胞。使用的培养基是完全培养基:RPMI1640,10%胎牛血清以及1%双抗,培养条件是5%二氧化碳、37℃;
2)传代12h后加入诱导剂TPA(终浓度为20μg/ml)、NaB(终浓度为3mM);
3)诱导3小时后加入氯硝柳胺,终浓度分别为0μM、0.01μM、0.1μM、0.2μM、0.5μM、1μM、2μM、5μM;
4)在加入诱导剂后的48h后,收取细胞进行蛋白印迹实验。
结果如图2显示:在P3HR-1细胞内,EBV相关蛋白ZTA、EA-D的表达受氯硝柳胺浓度的影响,呈一定的浓度依赖性。
实验3:氯硝柳胺在HNE1-2089细胞内对EBV相关蛋白EA-D、ZTA表达的作用
1)取生长良好的HNE1-2089细胞,1:4接种于6孔透明平底板中;
2)12h细胞贴壁,加入诱导剂TPA(终浓度为20μg/ml)、NaB(终浓度为3mM)
3)3h后加入梯度浓度的氯硝柳胺,终浓度分别为0μM、0.1μM、0.2μM、0.5μM、1μM、2μM、5μM;
4)培养48h后,用细胞刮板将细胞从板里刮取出来,冷的PBS漂洗,1000rpm,10min,4℃离心收集细胞进行蛋白印迹实验。
实验结果如图3所示:在HNE1-2089细胞内EBV相关蛋白ZTA、EA-D的表达受氯硝柳胺浓度的影响,呈一定的浓度依赖性。
实验4:氯硝柳胺对BCBL1细胞内的病毒产量的影响
1)取生长良好的细胞系BCBL1,种到48孔板中,细胞用量为1×105/孔,将细胞分为不诱导组(3孔)和诱导组(21孔);
2)3h后诱导组加入诱导剂TPA,终浓度为20ng/mL;
3)3h后加入相应浓度的氯硝柳胺,浓度分别0μM、0.1μM、0.2μM、0.5μM、1μM、2μM、5μM,每个浓度3个孔;
4)120h后收获细胞,10000g,4℃取上清液;
5)提取细胞外病毒DNA,方法如下:
a)取200μL上清液,加入2μL DNase I,20μL10×DNase I buffer,在37℃温箱中孵育1h;
b)向上述液体中加入0.5M EDTA 10μL,混匀,终止反应;
c)80℃水浴灭活10min;
d)加入20μL proteinase K溶液,紧接着加入200μL AL buffer,涡旋混匀,56℃水浴10min;
e)加入440μL酚氯仿抽提病毒颗粒内DNA,涡旋混匀;
f)12000rpm,4℃离心10min;
g)离心后分层,取上清液约300μL,至另一ep管中。避免抽到下层的酚氯仿;
h)加入5M NaCl溶液6μL,加入无水乙醇750μL,最后加入糖原1μL;
i)充分混匀后放入-80℃冰箱,放置1h;
j) 将样品从冰箱拿出,12000rpm,4℃,30min离心后去除上清;
k)Ep管内底部出现DNA沉淀,用1mL70%冰乙醇洗,盖上盖,上下颠倒几次;
l)12000rpm,4℃离心10min,弃上清;
m)12000rpm,4℃离心10min,除去残余的酒精;
n)打开盖子,让多余的酒精挥发;
o)3min后加入40μL ddH2O溶解DNA;
6)Real-time quantitative PCR 检测病毒含量。
结果如图4所示。结果显示,氯硝柳胺对于KSHV在BCBL1细胞外的产量呈浓度依赖性抑制。
实验5:氯硝柳胺对P3HR-1细胞外的病毒产量的影响;
1)取生长良好的细胞系P3HR-1,种到48孔板中,细胞用量为1×105/孔,将细胞分为不诱导组和诱导组;
2)3h后加入诱导组加入诱导剂TPA、NaB,终浓度分别为20ng/mL、3mM;
3)诱导3h后加入相应浓度的氯硝柳胺,浓度分别0μM、0.1μM、0.2μM、0.5μM、1μM、2μM、5μM每个浓度3个复孔;
4)120h后收获细胞,10000g离心10分钟,4℃取上清液;
5)提取病毒DNA,方法如下:
a)A.取200μL上清液,加入2μL DNase I,20μL10×DNase I buffer,在37℃温箱中孵育1h;
b)向上述液体中加入0.5M EDTA 10μL,混匀,终止反应;
c)80℃水浴灭活10min;
d)加入20μL proteinase K溶液,紧接着加入200μL AL buffer,涡旋混匀,56℃水浴10min;
e)加入440μL酚氯仿抽提病毒颗粒内DNA,涡旋混匀;
f)12000rpm,4℃离心10min;
g)离心后分层,取上清液约300μL,至另一ep管中。避免抽到下层的酚氯仿;
h)加入5M NaCl溶液6μL,加入无水乙醇750μL,最后加入糖原1μL;
i)充分混匀后放入-80℃冰箱,放置1h;
j)将样品从冰箱拿出,12000rpm,4℃,30min离心后去除上清;
k)Ep管内底部出现DNA沉淀,用1mL70%冰乙醇洗,盖上盖,上下颠倒几次;
l)12000rpm,4℃离心10min,弃上清;
m)12000rpm,4℃离心10min,除去残余的酒精;
n)打开盖子,让多余的酒精挥发;
o)3min后加入40μL ddH2O溶解DNA;
6)Real-time quantitative PCR 检测病毒含量。
结果如图5所示。结果显示,氯硝柳胺对于EBV能抑制EBV细胞外的病毒释放,且呈浓度依赖性抑制。
实验6:氯硝柳胺对HNE-2089细胞外的病毒产量的影响;
1)取生长良好的细胞系HNE1-2089,种到24孔板中,细胞用量为2×105/孔,将细胞分为不诱导组和诱导组;
2)12h后细胞贴壁,加入诱导剂TPA、NaB,终浓度分别为20ng/mL、3mM;
3)诱导3h后加入相应浓度的氯硝柳胺,浓度分别0μM、0.1μM、0.2μM、0.5μM、1μM、2μM、5μM每个浓度3个复孔;
4)120h后收获细胞,10000g离心10分钟,4℃取上清液;
5)提取病毒DNA,方法如下:
a)取200μL上清液,加入2μL DNase I,20μL10×DNase I buffer,在37℃温箱中孵育1h;
b)向上述液体中加入0.5M EDTA 10μL,混匀,终止反应;
c)80℃水浴灭活10min;
d)加入20μL proteinase K溶液,紧接着加入200μL AL buffer,涡旋混匀,56℃水浴10min;
e)加入440μL酚氯仿抽提病毒颗粒内DNA,涡旋混匀;
f)12000rpm,4℃离心10min;
g)离心后分层,取上清液约300μL,至另一ep管中。避免抽到下层的酚氯仿;
h)加入5M NaCl溶液6μL,加入无水乙醇750μL,最后加入糖原1μL;
i)充分混匀后放入-80℃冰箱,放置1h;
j)将样品从冰箱拿出,12000rpm,4℃,30min离心后去除上清;
k)Ep管内底部出现DNA沉淀,用1mL70%冰乙醇洗,盖上盖,上下颠倒几次;
l)12000rpm,4℃离心10min,弃上清;
m)12000rpm,4℃离心10min,除去残余的酒精;
n)打开盖子,让多余的酒精挥发;
o)3min后加入40μL ddH2O溶解DNA
6)Real-time quantitative PCR 检测病毒含量。
结果如图6所示。结果显示,氯硝柳胺对于感染EBV的上皮细胞,能抑制EBV细胞外的病毒产量,且呈浓度依赖性抑制。
实验7:氯硝柳胺对PBMC细胞的存活影响
MTS(3-(4,5-dimethylthiazol-2-yl)-5(3-carboymethoyphenyl)-2-(4-sulfopheny)-2H-tetrazolium, inner salt)是一种新合成的四唑类化合物,可被活细胞线粒体中的多种脱氢酶还原成各自有色的甲瓒产物,其颜色深浅与某些敏感细胞株的活细胞数在一定范围内呈高度相关。根据测得的490n的吸光度值(OD值),来判断活细胞数量,OD值越大,细胞活性越强,则表示药物毒性越小。具体实验操作如下:
1)接种细胞,用含10%胎牛血清的RPMI培养液将人外周血单核细胞PBMC以每孔10000个细胞接种到96孔板,每孔体积100ul ;
2)12h后加入氯硝柳胺,终浓度分别为0μM、0.01μM、0.1μM、0.2μM、0.5μM、1μM、2μM、5μM 、10μM 、20μM、40μM、80μM;
3)培养48h后,每孔加MTS溶液20ul,继续在培养箱中孵育2~4 h;
4)选择490nm波长,在酶联免疫监测仪上测定各孔光吸收值,观察化合物对PBMC细胞的细胞毒性。
实验结果如图7所示,实验结果表明,CC50>80μM,抗病毒化合物毒性较低,在PBMC细胞中均呈现成无细胞毒现象。
实验结果表明,氯硝柳胺处理后的细胞内KSHV或EBV相关基因的表达明显降低,且细胞外的病毒颗粒释放也有明显下降。这些抑制作用呈浓度依赖性,且在没有明显毒性的浓度就有很好的抗病毒作用,为进一步的抗病毒药物研发提供强有力的理论基础和实验依据,具有重要的研发价值和开发意义。
因此,氯硝柳胺可以通过抑制KSHV和EBV的复制和表达,对KSHV和EBV引起的疾病起到较好的治疗作用,特别是对KSHV引起的卡波氏肉瘤、原发渗出性淋巴瘤、多中心卡斯特慢病具有较好的预防及治疗作用。
氯硝柳胺可以和其他抗致瘤疱疹病毒的活性成分联合使用,通过多种途径抑制KSHV和EBV的复制和表达,对KSHV和EBV引起的疾病,特别是KSHV引起的卡波氏肉瘤、原发渗出性淋巴瘤、多中心卡斯特慢病起到更好的治疗作用。
- 还没有人留言评论。精彩留言会获得点赞!