一种负载有盐酸阿霉素的纳米粒子及其制备方法和用途与流程
本发明涉及纳米复合材料领域,尤其涉及一种负载有盐酸阿霉素的纳米粒子及其制备方法和用途。
背景技术:
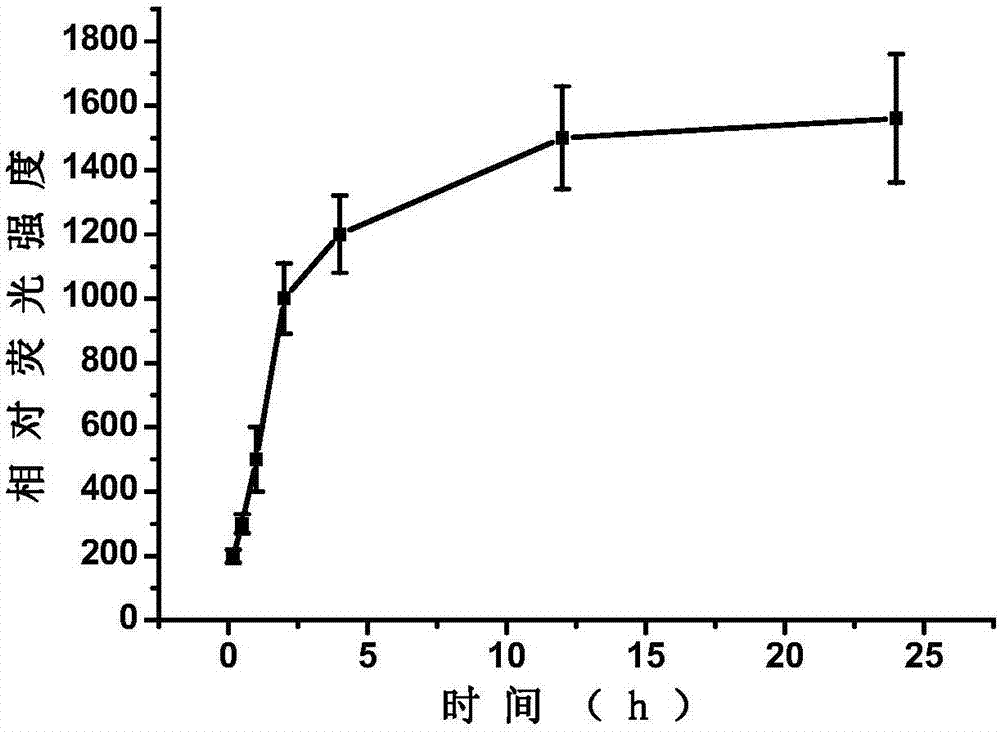
:癌症已经成为当今社会危害人类健康的严重疾病,对于癌症的治疗,化学药物治疗是目前临床上最常用的手段,化疗是一种全身的治疗手段,在药物进入人体后,化疗药物会随着血液循环系统遍布全身绝大多数组织和脏器,虽然化疗药物能够对肿瘤造成一定的杀伤,但是,化疗药物对与身体中正常的组织和器官也会造成一定的损害。利用纳米粒子对化疗药物进行负载,实现肿瘤的高效治疗,是目前常用的减弱药物毒性,提高药物靶向性的一种方法,高分子聚合物具有良好的生物相容性,因而被广泛用于抗肿瘤药物的运输,现有技术中常用的聚乙二醇-聚乳酸-聚羟基乙酸嵌段共聚物(PEG-co-PLGA)能够形成纳米胶束来包覆多种药物分子,并具有一定的生物降解性,降解过程中能够达到药物的缓释效果,故常被用于抗肿瘤药物的负载,阿霉素是一种常用的抗肿瘤药物,但是利用PEG-co-PLGA形成的纳米胶束包覆阿霉素时,其药物负载量却很低,往往需要通过一些化学手段将阿霉素与PEG-co-PLGA分子链通过化学键连接来提高载药量,上述化学手段可能会对药物活性产生影响,甚至出现毒副作用。富勒烯分子作为碳家族的“明星分子”在最近十几年引起了纳米材料研究者的广泛兴趣,富勒烯是由数十个碳原子组成中空笼状结构的碳的第三种同素异型体,在富勒烯的表面引入羟基之后,能够形成富勒烯的一种衍生物-富勒醇,富勒醇分子具有强烈的吸电子的还原特性,使其能够清除生物体中的活性氧等自由基,拮抗氧化应激引起的细胞损伤,因而具有广泛的生物医学应用前景,现有技术中的研究结果还表明,富勒醇分子具有一定的抗肿瘤活性,通过动物实验证实富勒醇分子能够有效抑制多种肿瘤细胞的生长,其作用机制不是直接杀死肿瘤细胞,而是通过对肿瘤微环境中特定组分调控,实现肿瘤的高效治疗本领域的技术人员需要利用富勒醇分子表面特殊的结构,使其能够与多种药物分子如阿霉素等相互作用,再与PEG-co-PLGA分子链结合,得到一种新的纳米结构,使其具有靶向药物递送以及可控释放的能力。技术实现要素:针对现有技术的不足,本发明的目的之一在于提供一种负载有盐酸阿霉素的纳米粒子,所述纳米粒子具有核壳结构,所述内核由富勒醇构成、所述外壳为聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物,在富勒醇内核的表面负载有盐酸阿霉素。所述富勒醇通过将富勒烯表面羟基化得到,其结构式为C2n(OH)m,其中n为30~60的正整数,m为≥6的正整数。所述富勒醇分子之间通过静电力、共轭效应和少量化学键连接,形成所述内核。所述内核表面呈负电性,盐酸阿霉素在静电力和π-π共轭效应的作用下吸附在所述内核表面,对于电中性的药物如未盐酸化的阿霉素和不含有共轭化合键的药物来说,富勒醇的吸附作用较弱,不易实现有效负载。所述外壳将富勒醇内核及其表面负载有的盐酸阿霉素紧密包覆,通过动态酯交换反应与富勒醇内核相连,位于水相体系中时,所述外壳能够自行降解,本发明通过选用聚乙二醇-聚乳酸-聚羟基乙酸嵌段外壳使其降解作用与内核表面的盐酸阿霉素的解吸附扩散作用具有协同效应,进而使得盐酸阿霉素药物释放平缓,避免突释等现象出现,降低盐酸阿霉素药物对于心脏功能的损害。优选地,所述聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物的数均分子量为6000~40000Da,例如为7000Da、10000Da、15000Da、20000Da、25000Da、30000Da、35000Da、39000Da等,进一步优选为15000~25000Da,选用上述分子量的聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物能够使得其降解速率与盐酸阿霉素的解吸附扩散作用相匹配,使得盐酸阿霉素的药物释放曲线接近于直线,避免过快释放或突然释放。优选地,所述聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物中的聚乙二醇的数均分子量为1000~10000Da,例如为1200Da、2000Da、4000Da、6000Da、8000Da、9000Da、9500Da等,进一步优选为3000~7000Da,选用上述分子量的聚乙二醇嵌段能够进一步增强所述纳米粒子的亲水性,便于分散。优选地,所述聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物中的聚乳酸-聚羟基乙酸嵌段与聚乙二醇嵌段的质量比为1:1~10,例如为1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9等,进一步优选为1:3。优选地,所述富勒醇的结构式为C2n(OH)m,其中n为30、35、36、42、50或60,m为6~26的正整数,例如为7、8、10、15、18、20、24等。优选地,所述富勒醇的结构式为C60(OH)22。优选地,所述纳米粒子的粒径为50~100nm,例如为52nm、60nm、70nm、75nm、80nm、85nm、90nm、95nm、98nm等,进一步优选为80nm,所述纳米粒子选用上述粒径使得纳米粒子在溶液中的分散性较好,使其更快进入生物组织中。本发明的目的之二在于提供一种制备所述纳米粒子的方法,所述制备方法包括如下步骤:步骤(1),将聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物溶于有机溶剂中,得到溶液A,将富勒醇溶解在极性溶剂中,得到溶液B;步骤(2),将盐酸阿霉素加入步骤(1)中得到的溶液B中,搅拌混合均匀;步骤(3),将步骤(2)中混合均匀后的溶液加入步骤(1)得到的溶液A中,得到混合液,混合液加入乳化剂进行超声破乳,经过后处理得到所述纳米粒子。优选地,步骤(1)中所述的有机溶剂为氯仿、二氯甲烷或四氢呋喃中的任意一种或至少两种的混合物,进一步优选为二氯甲烷。优选地,步骤(1)中所述的极性溶剂为水、二氯甲烷、乙醇或四氢呋喃中的任意一种或至少两种的混合物,进一步优选为水。优选地,步骤(1)中所述的溶液A中聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物的浓度为5~30mg/mL,例如为6mg/mL、8mg/mL、12mg/mL、16mg/mL、20mg/mL、24mg/mL、26mg/mL、28mg/mL等。优选地,步骤(1)中所述的溶液B中富勒醇的浓度为0.1~10μg/mL,例如为0.2μg/mL、0.5μg/mL、1μg/mL、2μg/mL、4μg/mL、5μg/mL、6μg/mL、8μg/mL、9μg/mL等,进一步优选为1~5μg/mL。优选地,步骤(2)中所述的搅拌通过磁力搅拌机进行。优选地,步骤(2)中所述的搅拌的搅拌速率为100~600转/min,例如为150转/min、200转/min、300转/min、400转/min、500转/min、550转/min、580转/min等。优选地,步骤(2)中所述的搅拌在室温无光照的条件下进行。优选地,步骤(2)中所述的搅拌的搅拌时间为12~24h,例如为13h、14h、15h、16h、17h、18h、19h、21h、23h等。优选地,步骤(2)中所述的盐酸阿霉素与溶液B中的富勒醇的质量比为1:0.1~10,例如为1:0.2、1:0.8、1:1.5、1:2、1:4、1:6、1:8、1:9、1:9.5等,进一步优选为1:3~6。优选地,步骤(3)中所述的步骤(2)中混合均匀后的溶液与步骤(1)得到的溶液A的体积比为1:1~10,例如为1:2、1:3、1:4、1:5、1:6、1:7、1:8、1:9等,进一步优选为1:5。优选地,步骤(3)中所述的乳化剂为聚乙烯醇、普郎尼克F68型或普郎尼克127型乳化剂中的任意一种或至少两种的混合物。优选地,步骤(3)中所述的超声破乳的功率为200~1000W,例如为220W、300W、400W、500W、600W、700W、800W、900W、950W等。优选地,步骤(3)中所述的超声破乳的时间为5~10min,例如为6min、7min、8min、9min等。优选地,步骤(3)中在加入乳化剂前,对混合液超声1~5min,进行预处理;优选地,所述预处理中的超声功率为200~500W,例如为220W、300W、350W、400W、450W、480W等。优选地,步骤(3)中所述的后处理为减压蒸馏。优选地,所述减压蒸馏的温度为室温。优选地,所述减压蒸馏的负压为500~800kPa,例如为520kPa、560kPa、600kPa、650kPa、700kPa、750kPa、780kPa等。本发明的目的之三在于提供一种所述纳米粒子的用途,所述纳米粒子负载有抗肿瘤药物盐酸阿霉素,释放曲线平稳,能够实现药物的缓慢释放,可以用于抗肿瘤药物的制备。与现有技术相比,本发明具有以下有益效果:本发明得到了一种新的具有核壳结构的纳米粒子,所述纳米粒子粒径合适,能够负载盐酸阿霉素,实现盐酸阿霉素的缓慢释放,释放曲线平稳,接近线性释放,相较于传统的以聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物胶束作为药物载体或者不使用载药体系的治疗方法,稳定性高,负载量高,在血清中纳米颗粒粒径两周内没有明显的变化,使用本发明制备的纳米粒子作为盐酸阿霉素的载体能够有效防止因药物突释造成的毒副作用和心肌细胞损伤,适合进一步推广使用。附图说明图1为实施例1得到的纳米粒子1的透射电镜照片。图2为实施例1得到的纳米粒子1经过药物释放细胞实验得到的药物释放曲线。图3为对于心肌细胞的毒性实验中以2mg/kg的盐酸阿霉素作为药物的实验组1、以等量的实施例1得到的纳米粒子1作为药物的实验组2、以及等量的生理盐水组作为药物的对照组治疗的小鼠的体重变化情况。图4为对于心肌细胞的毒性实验中以2mg/kg的盐酸阿霉素作为药物的实验组1、以等量实施例1得到的纳米粒子1作为药物的实验组2、以及等量的生理盐水组作为药物的对照组治疗的小鼠的心肌细胞电镜照片。具体实施方式下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。实施例1通过如下步骤制备所述纳米粒子1:步骤(1),将20mg数均分子量为25000Da的聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物(其中含有15mg数均分子量为7000Da的聚乙二醇嵌段)溶于4mL二氯甲烷中,得到溶液A,将2mg分子式为C60(OH)22的富勒醇溶解在1L水中,得到溶液B;步骤(2),将0.4mg盐酸阿霉素加入至步骤(1)中得到的溶液B中,使用磁力搅拌机在室温无光的环境中以100转/min的转速搅拌24h,混合均匀;步骤(3),取40mL步骤(2)中混合均匀后的溶液加入步骤(1)得到的溶液A中,得到混合液,混合液使用超声波细胞粉碎仪在500W的功率下预处理,之后加入1mL普郎尼克F68型乳化剂和聚乙烯醇1799质量比为1:1组成的混合乳化剂,使用超声波细胞粉碎仪在1000W的功率下超声破乳5min,经过室温下负压为800kPa的减压蒸馏处理,得到所述纳米粒子1。实施例2通过如下步骤制备所述纳米粒子2:与实施例1的区别仅在于,步骤(1)中聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物的加入量为120mg,数均分子量为15000Da,其中含有108mg数均分子量为3000Da的聚乙二醇嵌段。实施例2得到所述纳米粒子2。实施例3通过如下步骤制备所述纳米粒子3:与实施例1的区别仅在于,步骤(1)中富勒醇的加入量为5mg。实施例3得到所述纳米粒子3。实施例4通过如下步骤制备所述纳米粒子4:与实施例1的区别仅在于,步骤(2)中盐酸阿霉素的加入量为0.7mg,搅拌速率为600转/min,搅拌时间为12h。实施例4得到所述纳米粒子4。实施例5通过如下步骤制备所述纳米粒子5:与实施例1的区别仅在于,步骤(3)中得到混合液后不进行超声预处理,超声破乳的时间为10min,超声破乳的功率为200W且减压蒸馏的负压为500kPa。实施例5得到所述纳米粒子5。对照例1通过如下步骤制备胶束1:步骤(1),将200mg数均分子量为30000Da的聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物溶于40mL二氯甲烷中,得到溶液A;步骤(2),将0.4mg盐酸阿霉素加入至步骤(1)中得到的溶液A中,使用磁力搅拌机在室温无光的环境中以100转/min的转速搅拌24h,混合均匀;步骤(3),步骤(2)中混合均匀后的溶液加入1mL普郎尼克F68型乳化剂和聚乙烯醇1799质量比为1:1组成的混合乳化剂,以600转/min的转速搅拌60min,得到所述胶束1。取上述实施例和对照例中得到的纳米粒子1~5和胶束1,进行如下的表征测试,测试结果列于表1。(1)形貌表征测试各取上述实施例中和对照例中得到的纳米粒子1~5和胶束1配成含有阿霉素的浓度为25μg/mL的水溶液1~6,使用Zetasizer型激光粒度仪测定样品的水合粒径,激光粒度仪的测试参数为:测试温度25℃,测试角度90度。将上述溶液分别滴于铜网上,待其自然风干后,利用FEITecnaiG2型透射电镜测试样品的平均粒径,透射电镜的测试参数为:加速电压200kV,束斑尺寸0.2nm。(2)药物释放细胞实验将同一密度的小鼠乳腺癌细胞系4T1肿瘤细胞接种在培养皿中,待其过夜贴壁后,分别加入形貌表征测试中制备的水溶液1~6,37℃下分别在孵育10min、30min、1h、2h、4h、12h和24h后,利用PerkinElmer型光共聚焦显微镜分别观察细胞内盐酸阿霉素的荧光变化情况,作出细胞内荧光发射光强度随时间变化的曲线,即为样品的药物释放曲线,药物释放曲线经过拟合平滑后取曲线上的斜率最大值可以表征药物突释情况,数值越大则药物突释情况越严重,其中激光共聚焦显微镜的测试参数为:发射波长480nm,收集波长620nm。(3)细胞毒性实验将小鼠乳腺癌细胞系4T1以3000细胞/孔密度接种到96孔板中,待其过夜贴壁后,将形貌表征测试中制备的水溶液1~6稀释5倍,加入孔中作为实验组1~6,将同样体积的水溶液加入孔中作为对照组,培养箱中培养24h后,撤掉孔中的培养基,每孔加入110μL,含10%(体积分数)2-(2-甲氧基-4-硝苯基)-3-(4-硝苯基)-5-(2,4-二磺基苯)-2H-四唑单钠盐)(CCK-8)的细胞培养基,在培养箱中继续培养2h后,在酶标仪上测定450nm处的吸光度值,以600nm处的吸光度值作为空白溶液吸光度值,每组吸光度值扣除空白溶液吸光度值后,每实验组的吸光度值除以对照组的吸光度值作为细胞活力,细胞活力越差说明药物效果越好,即样品的缓释效果越好。(4)对于心肌细胞的毒性实验将1×106个4T1肿瘤细胞接种到小鼠腋下,待其生长3天成瘤后,分别对小鼠尾静脉注射2mg/kg的盐酸阿霉素和载有同等盐酸阿霉素含量的纳米粒子1~5和胶束1,作为实验组1~6,注射等量的生理盐水组作为对照组,每两天注射一次,每次尾静脉注射完药物后,对小鼠进行称重。治疗结束后,对小鼠进行解剖,将心脏迅速取出,放置于3%的戊二醛溶液中,用眼科剪剪成体积不超过1mm3的组织块,再转移到新的3%戊二醛溶液过夜,之后用磷酸缓冲液冲洗3次,每次10分钟,冲洗完毕后,加入1%的锇酸进行固定2小时,然后继续用磷酸缓冲液漂洗3次,每次10分钟,将组织块分别浸泡在50%、70%、80%、90%乙醇各10分钟进行梯度脱水,然后100%乙醇浸泡三次,每次10分钟,之后将组织块在体积比为1:1的乙醇和丙酮溶液中浸泡10分钟,最后浸泡100%丙酮两次,每次10分钟,用包埋剂进行渗透1小时,然后放置在渗透剂中,4℃过夜。然后将样品放在37℃、45℃和60℃烘箱中各24小时,使包埋剂固化,用超薄切片机修块、切片,切出50nm左右厚度的片层,用3%醋酸双氧铀-枸橼酸铅双染料染色后,用日立HT7700型生物透射电镜观察组织的超微结构,透射电镜测试参数为:加速电压80kV,分辨率0.2nm。表1纳米粒子1~5和胶束1的表征测试结果对比水合粒径(nm)平均粒径(nm)斜率最大值细胞活力纳米粒子1100742720.37纳米粒子21401013220.43纳米粒子3121833050.42纳米粒子4123853260.38纳米粒子5142963420.48胶束1480-7650.65其中“-”代表该值不存在。以实施例1中得到的纳米粒子1为例,图1为实施例1得到的纳米粒子1的透射电镜照片,从中可以计算出纳米粒子1的平均粒径为74nm。图2为实施例1得到的纳米粒子1经过药物释放细胞实验得到的药物释放曲线,从中可以计算出其斜率最大值为272,且药物释放曲线在0~5h内接近线性释放,之后药物释放曲线平缓,不存在突释的情况。图3为对于心肌细胞的毒性实验中以2mg/kg的盐酸阿霉素作为药物的实验组1、以等量的实施例1得到的纳米粒子1作为药物的实验组2、以及等量的生理盐水组作为药物的对照组治疗的小鼠的体重变化情况,从中可以看出,使用盐酸阿霉素治疗恶性肿瘤时,突然的药物释放能够引起剧烈的毒副作用,使得小鼠体重显著降低,但是通过本发明所述的纳米粒子1给予盐酸阿霉素方式能够明显的降低阿霉素的毒副作用,使用本发明所述的纳米粒子1治疗后的小鼠体重变化与对照组更加接近。图4为对于心肌细胞的毒性实验中以2mg/kg的盐酸阿霉素作为药物的实验组1、以等量实施例1得到的纳米粒子1作为药物的实验组2、以及等量的生理盐水组作为药物的对照组治疗的小鼠的心肌细胞电镜照片,从中可以看出,盐酸阿霉素能够导致心肌细胞线粒体损伤(如图中星形标记的线粒体脊消失的位置),而通过实施例1中得到的纳米粒子1作为药物载体载带后,心肌线粒体损伤减少,故通过本发明所述的纳米粒子给予盐酸阿霉素方式能够明显的降低阿霉素对于心脏毒性的作用。综上所述,本发明得到了一种新的具有核壳结构的纳米粒子,所述纳米粒子粒径合适,能够负载盐酸阿霉素,实现盐酸阿霉素的缓慢释放,释放曲线平稳,接近线性释放,相较于传统的以聚乙二醇-聚乳酸-聚羟基乙酸嵌段聚合物胶束作为药物载体或者不使用载药体系,使用本发明制备的纳米粒子作为盐酸阿霉素的载体能够有效防止因药物突释造成的毒副作用和心肌细胞损伤,适合进一步推广使用。申请人声明,本发明通过上述实施例来说明本发明的工艺方法,但本发明并不局限于上述工艺步骤,即不意味着本发明必须依赖上述工艺步骤才能实施。所属
技术领域:
的技术人员应该明了,对本发明的任何改进,对本发明所选用原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 具吡啶二硫功能基的磁性纳米粒子Fe3O4@SiO2@S-S-Py的制备及生物医药中的应用的制造方法与工艺
- 聚乙二醇化包裹聚多巴胺载药磁性纳米颗粒的制备方法与流程
- 一种PQQ‑DA印迹磁性纳米粒子的制备方法及其应用与制造工艺
- 一种可降解聚合物磁性纳米粒子及其制备方法与制造工艺
- 一种山梨酸-茶多酚复合纳米粒子及其应用的制造方法与工艺
- 一种实现纳米线生物传感器表面修饰的方法与制造工艺
- 磁性纳米粒子和产生自由基的酶的介孔催化剂及其使用方法与制造工艺
- 一种靶向性超顺磁性纳米探针的制备方法和应用方法与制造工艺
- 油酸包裹的超顺磁性纳米Fe3O4及其制备方法与制造工艺
- 一种贵金属纳米粒子间距可控的SERS衬底制备方法与制造工艺