一种瑞舒伐他汀钙片剂及其制备方法与流程
本发明属于医药
技术领域:
,具体涉及一种瑞舒伐他汀钙片剂及其制备方法。
背景技术:
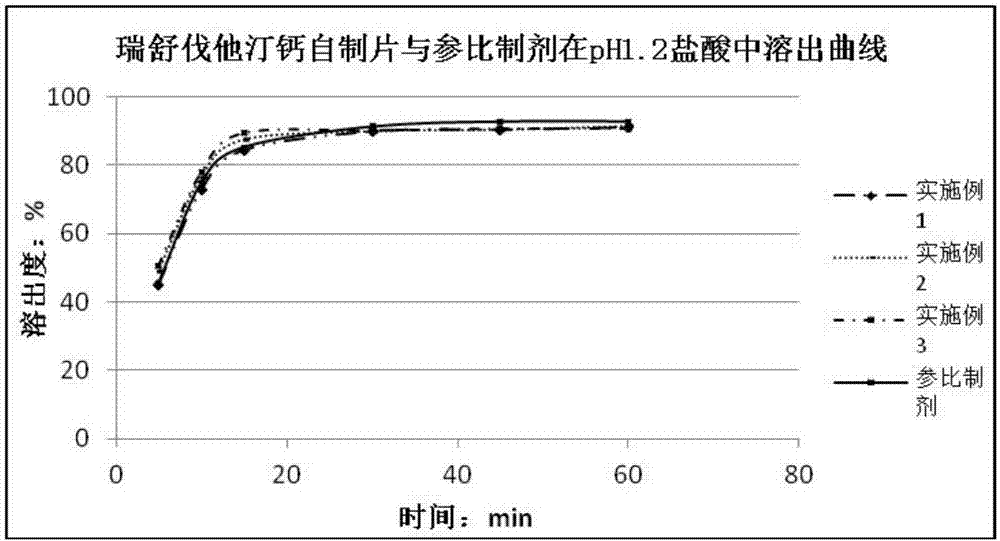
瑞舒伐他汀钙是用于经饮食控制和其它非药物治疗(如:运动治疗、减轻体重)仍不能适当控制血脂异常的原发性高胆固醇血症(iia型,包括杂合子家族性高胆固醇血症)或混合型血脂异常症(iib型)。也适用于纯合子家族性高胆固醇血症的患者,作为饮食控制和其它降脂措施(如ldl去除疗法)的辅助治疗,或在这些方法不适用时使用。瑞舒伐他汀钙属于生物药剂学分类系统三类药物,在水中的溶解度高。溶出速率较快,而阿斯利康的原研制剂在ph4.5醋酸介质和ph1.2盐酸介质中溶出较慢。研究表明,控制好原料粒径和关键辅料的水分,可以降低本品在ph4.5醋酸介质和ph1.2盐酸介质中溶出速率,使与阿斯利康的原研制剂溶出曲线较为一致。技术实现要素:本发明的目的在于通过对制剂的处方和工艺进行大量试验研究,最终获得了一种溶出与阿斯利康的原研制剂溶出较为相似的瑞舒伐他汀钙片剂。为了实现本发明的目的,制成了一种瑞舒伐他汀钙片剂,首先将瑞舒伐他汀钙原料粉碎处理,控制瑞舒伐他汀钙的粒径范围,和药学上所接受的辅料混匀后压片而成,控制所用关键辅料微晶纤维素和交联聚维酮的水分。试验结果表明采用本发明方法制备的瑞舒伐他汀钙片溶出效果较好。本发明中瑞舒伐他汀钙片由处方量的瑞舒伐他汀钙、填充剂、崩解剂、稳定剂和润滑剂组成。试验表明该口服瑞舒伐他汀钙片具有良好的溶出度,更容易被人体吸收。本发明中,所述的瑞舒伐他汀钙为经粉碎后过筛,控制粒径分布为80目~100目的占10%~40%,100目~150目占30%~80%,小于150目的占10%~40%。本发明中,单位瑞舒伐他汀钙片剂中原料与乳糖和微晶纤维素的重量比例为1:1~15:1~15。进一步优选地,上述瑞舒伐他汀钙片剂中原料与乳糖和微晶纤维素的重量比例为1:3~10:3~10。本发明中,微晶纤维素的水分控制在4.0%以下,交联聚维酮的水分控制在4.0%以下。本发明的第二个目的在于提供一种上述瑞舒伐他汀钙片剂的制备方法,该制备方法为粉末直接压片,包括如下步骤:(1)将瑞舒伐他汀钙原料粉碎。(2)称取处方量的瑞舒伐他汀钙、填充剂、崩解剂、稳定剂于混合机中进行混合。(3)将所混合物料与润滑剂混匀后压片。优选地,上述的瑞舒伐他汀钙片剂的制备方法,其中所述药学上可接受的辅料包括填充剂、稳定剂、崩解剂和润滑剂;所述的稳定剂为碳酸钙、磷酸钙、硫酸钙的一种或多种,所述的崩解剂羧甲基淀粉钠、交联羧甲基纤维素钠、交联聚维酮中的一种或多种;所述的润滑剂硬脂酸镁、微粉硅胶中的一种或多种。与现有技术相比,本发明涉及的瑞舒伐他汀钙片剂及其制备工艺具有如下优点和显著进步:(1)药物在ph1.2盐酸介质和ph4.5醋酸介质中溶出较慢,与阿斯利康的原研制剂溶出较为相似;(2)制备工艺简单,适合工业化大生产。具体实施例下面结合附图对本发明技术方案作进一步说明:附图1-2为本发明瑞舒伐他汀钙自制片与参比制剂溶出曲线对比示意图;附图3-4为本发明瑞舒伐他汀钙不同粒度分布原料所制自制片与参比制剂溶出曲线对比示意图。附图5-6为本发明瑞舒伐他汀钙不同辅料水分所制自制片与参比制剂溶出曲线对比示意图。以下实施例进一步描述本发明的制备过程和有益效果,实施例仅用于例证的目的,不限制本发明的范围,同时本领域普通技术人员根据本发明所做的显而易见的改变和修饰也包含在本发明范围之内。实施例1~3瑞舒伐他汀钙片处方工艺表1实施例1~3的瑞舒伐他汀钙片处方处方实施例1(g)实施例2(g)实施例3(g)瑞舒伐他汀钙10.410.410.4乳糖608090微晶纤维素604030碳酸钙101010交联聚维酮7.57.57.5硬脂酸镁2.12.12.1工艺:取瑞舒伐他汀钙原料进行粉碎,取处方量的瑞舒伐他汀钙原料、乳糖、微晶纤维素、交联聚维酮、碳酸钙,于混合机中混匀,再加入处方量的硬脂酸镁混匀,压片即得。对比实施例1~2不同粒度分布的瑞舒伐他汀钙原料所制片剂处方工艺表2对比实施例1~2的瑞舒伐他汀钙片处方工艺:取瑞舒伐他汀钙原料进行粉碎,收集不同粒度范围的原料,按照对比实施例1~2中各原料粒度占比称取原料,再取处方量乳糖、微晶纤维素、交联聚维酮、碳酸钙,于混合机中混匀,再加入处方量的硬脂酸镁混匀,压片即得。对比实施例3~4不同水分的微晶纤维素和交联聚维酮所制片剂处方工艺表3对比实施例3~4的瑞舒伐他汀钙片处方处方对比实施例3(g)实施例1(g)对比实施例4(g)瑞舒伐他汀钙10.410.410.4乳糖606060微晶纤维素60(水分4.3%)60(水分3.8%)60(水分2.2%)磷酸钙101010交联聚维酮7.5(水4.7%)7.5(水分3.2%)7.5(水分3.8%)硬脂酸镁2.12.12.1工艺:取瑞舒伐他汀钙原料进行粉碎,按照对比实施例3~4中微晶纤维素和交联聚维酮不同水分称取相应的微晶纤维素和交联聚维酮,再取处方量乳糖、磷酸钙,于混合机中混匀,再加入处方量的硬脂酸镁混匀,压片即得。实施例4自制品与市售参比制剂溶出行为的测定及比较。对本发明所述瑞舒伐他汀钙片与进口市售瑞舒伐他汀钙片的溶出度对比试验如下:由实施例1-3制得的瑞舒伐他汀钙自制片(采用6个计量单位即6片进行测定)、瑞舒伐他汀钙市售片(阿斯利康),参照中国药典2015年版第四部0931溶出度测定法第二法的试验装置,分别以ph1.2盐酸和ph4.5醋酸为溶出介质,转速为每分钟50转,计算除0时外,5,10,15,30,45,60分钟药物累计溶出百分比,并绘制每批样品药物累积溶出曲线,如附图1、图2所示,结果见表4、表5。表4瑞舒伐他汀钙自制片与参比制剂在ph1.2盐酸介质中溶出曲线对比取样时间点(min)实施例1实施例2实施例3参比制剂544.9448.7650.4645.561072.6378.4977.8974.901584.3287.3389.4885.263089.7989.8390.2391.284590.3290.2890.7892.746090.9691.3390.8292.78相似因子888171--表5瑞舒伐他汀钙自制片与参比制剂在ph4.5醋酸介质中溶出曲线对比取样时间点(min)实施例1实施例2实施例3参比制剂566.3868.8971.8763.191077.5579.3280.0378.761583.4184.1384.0882.443088.1089.3288.9385.574589.3689.3989.5986.876090.2691.1190.3788.36相似因子817266--实施例5不同粒度分布的原料所制自制品与市售参比制剂溶出行为的测定及比较。对本发明所述瑞舒伐他汀钙片与进口市售瑞舒伐他汀钙片的溶出度对比试验如下:由实施例1、对比实施例1-2制得的瑞舒伐他汀钙自制片(采用6个计量单位即6片进行测定)、瑞舒伐他汀钙市售片(阿斯利康),参照中国药典2015年版第四部0931溶出度测定法第二法的试验装置,分别以ph1.2盐酸和ph4.5醋酸为溶出介质,转速为每分钟50转,计算除0时外,5,10,15,30,45,60分钟药物累计溶出百分比,并绘制每批样品药物累积溶出曲线,如附图3、图4所示。结果见表6、表7。表6不同粒度分布的瑞舒伐他汀钙原料所制自制片与参比制剂在ph1.2盐酸溶液中溶出曲线比较取样时间(min)实施例1对比实施例1对比实施例2参比制剂544.9442.3341.3345.561072.6371.8968.7674.901584.3283.6681.2385.263089.7989.6287.5691.284590.3290.4689.3392.746090.9690.5990.0192.78相似因子887966---表7不同粒度分布的瑞舒伐他汀钙原料所制自制片与参比制剂在ph4.5醋酸溶液中溶出曲线比较取样时间(min)实施例1对比实施例1对比实施例2参比制剂566.3863.8962.1863.191077.5574.3373.2978.761583.4180.3679.7782.443088.1084.1883.5985.574589.3688.3987.7786.876090.2690.2889.9888.36相似因子817873---结论:通过不同粒度分布的原料所制备样品与市售参比制剂溶出曲线拟合实验结果可知,原料经粉碎过80目筛后所制备样品与市售参比制剂在上述溶出介质中溶出行为均相似。最终确定瑞舒伐他汀钙原料粒度范围控制为80目~100目的占10%~40%,100目~150目占30%~80%,小于150目的占10%~40%。实施例5不同水分的微晶纤维素和交联聚维酮所制自制品与市售参比制剂溶出行为的测定及比较。对本发明所述瑞舒伐他汀钙片与进口市售瑞舒伐他汀钙片的溶出度对比试验如下:由实施例1、对比实施例3-4制得的瑞舒伐他汀钙自制片(采用6个计量单位即6片进行测定)、瑞舒伐他汀钙市售片(阿斯利康),参照中国药典2015年版第四部0931溶出度测定法第二法的试验装置,分别以ph1.2盐酸和ph4.5醋酸为溶出介质,转速为每分钟50转,计算除0时外,5,10,15,30,45,60分钟药物累计溶出百分比,并绘制每批样品药物累积溶出曲线,如附图5、图6所示。结果见表7、表8。表8不同水分的微晶纤维素和交联聚维酮所制自制品与参比制剂在ph1.2盐酸溶液中溶出曲线比较取样时间(min)实施例1对比实施例3对比实施例4参比制剂544.9450.1745.9745.561072.6366.3871.8874.901584.3274.5983.8985.263089.7983.3789.6091.284590.3285.6490.6292.746090.9686.9590.7892.78相似因子885484---表9不同水分的微晶纤维素和交联聚维酮所制自制品与参比制剂在ph4.5醋酸溶液中溶出曲线比较取样时间(min)实施例1对比实施例3对比实施例4参比制剂566.3872.8361.7563.191077.5585.5876.5178.761583.4189.6981.6182.443088.1092.0185.3685.574589.3693.3386.2386.876090.2693.1286.9088.36相似因子815688---结论:通过不同水分的微晶纤维素和交联聚维酮所制备样品与市售参比制剂溶出曲线拟合实验结果可知,当微晶纤维素和交联聚维酮水分都控制在4.0%以下时所制备样品与市售参比制剂在上述溶出介质中溶出行为相似,而当微晶纤维素和交联聚维酮的水分都大于4.0%时,所制备样品与市售参比制剂在上述溶出介质中溶出行为相似性略差。最终确定微晶纤维素和交联聚维酮水分控制在4.0%以下。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1