一种用于鉴定AGA926-928突变的ARMS-qPCR的引物组合及其应用的制作方法
本发明属于医学分子生物学领域,具体涉及幽门螺幽杆菌16S rDNA是否存在AGA926-928突变的ARMS-qPCR的引物组、引物探针组合、PCR试剂、PCR试剂盒及其检测方法。
背景技术:
据统计全世界人群中幽门螺旋杆菌(Helicobacter pylori,Hp)感染率达50%,我国的感染率高达60%-90%。幽门螺旋杆菌感染可导致慢性胃炎、消化性溃疡、胃癌和胃黏膜相关淋巴组织组织(mucosa-associated lymphoid tissue lymphoma,MALT)淋巴瘤。另外,Hp感染还是心血管疾病、不明原因的缺铁性贫血和慢性特发性血小板减少性紫癜的独立危险因素。因此,对于这类疾病的患者,根除幽门螺旋杆菌至关重要。
根除幽门螺旋杆菌治疗的研究一直是幽门螺旋杆菌研究领域中的热点。依照国内外多个版本的幽门螺旋杆菌防治指南意见(1999年海南、2003年庐山、2005年美国胃肠病学会、2007年桐城、2009年欧洲Maastricht-III),目前质子泵抑制剂(PPI)或铋剂联合两种抗生素的三联疗法是全球推荐的幽门螺旋杆菌根除治疗一线方案,常用的抗生素主要有四环素、阿莫西林、喹诺酮、呋喃唑酮、甲硝唑、四环素等。随着根除幽门螺旋杆菌治疗在临床上的广泛应用,根除的难度逐渐增加,治疗失败的例数亦越来越多,由最初的大于90%的根除率到近期的70%左右甚至有些低于60%。其根除治疗失败的原因较多,包括宿主因素:依从性、机体免疫、胃内PH、吸烟状况;细菌因素:幽门螺旋杆菌菌株、定植、密度、球形变;环境因素(再感染);治疗方案(包括用药时间及方法);抗生素耐药。其中幽门螺旋杆菌对抗生素耐药是一线三联根除治疗失败最主要、最重要的因素。现已发现幽门螺旋杆菌对四环素、阿莫西林、喹诺酮、呋喃唑酮、甲硝唑、四环素类抗生素都有耐药菌株的产生,而且不同国家、地区对药物耐受情况也有差异。如图1所示,2007年统计的我国幽门螺旋杆菌对抗生素耐药率分别为:四环素0~40%(平均23.9%),甲硝唑50%~100%(平均73.3%),阿莫西林0~2.7%,喹诺酮类0~26.6%。
幽门螺旋杆菌抗生素耐药机制较为复杂,主要与抗生素作用靶点相关基因突变有关。其中,幽门螺旋杆菌四环素耐药主要是由16S rDNA基因AGA926-928碱基改变所致,并且其耐药程度与突变碱基数目相关,突变碱基越多,其耐药性越高,其中以TTC突变耐药性最高,而单个和两个碱基的改变往往导致幽门螺旋杆菌四环素的低度和中度耐药。检测分析患者幽门螺杆菌16S rDNA耐药突变位点,能够在短时间内迅速的得到患者四环素耐药情况,有助于临床医师采取正确的治疗手段,提高幽门螺杆菌的根除率。鉴于幽门螺旋杆菌根除失败率的不断提高和传统幽门螺旋杆菌药敏实验的缺陷,发展新型的幽门螺旋杆菌耐药检测技术极为迫切。近年来随着对幽门螺旋杆菌耐药机制认知加深,以及各抗生素(尤其是四环素、四环 素和喹诺酮类)耐药位点的鉴定,耐药突变检测在幽门螺旋杆菌耐药性检测中的作用正越来越被重视。
扩增阻碍突变系统(amplification refractory mutation system,ARMS)于1989年建立,用于对己知突变基因进行检测。该法通过设计突变ARMS引物,其3’末端碱基与待检测突变型的突变碱基匹配,用于特异性扩增突变模板。ARMS的检测灵敏度依赖于ARMS引物的特异性和反应条件如酶,馍离子浓度等的优化。为了增加寻|物的特异性,减少引物与靶DNA有错配时的错配延伸,可通过在引物3’端的第23个碱基引入另外一个或者两个错配碱基,使之与模板之间形成多重错配以阻止错误延伸。ARMSqPCR技术基于Real-time PCR平台,结合ARMS突变富集和Taqman特异性荧光检测两种技术。利用ARMS引物对突变革巴序列进行PCR扩增,Taqman探针对扩增产物进行特异性位点检测,在Real-time PCR基础上鉴定特定突变。
锁核酸(locked nucleic acid,LNA)是一种特殊的双环状核苷酸衍生物,结构中含有一个或多个2′-O,4′-C-亚甲基-β-D-呋喃核糖核酸单体,核糖的2′-O位和4′-C位通过不同的缩水作用形成氧亚甲基桥、硫亚甲基桥或胺亚甲基桥,并连接成环形,这个环形桥锁定了呋喃糖C3′-内型的N构型,降低了核糖结构的柔韧性,增加了磷酸盐骨架局部结构的稳定性。由于LNA与DNA/RNA在结构上具有相同的磷酸盐骨架,故其对DNA、RNA有很好的识别能力和强大的亲和力,并具有抗3′脱氧核苷酸酶降解的稳定性、水溶性好、体内无毒性及合成简单等优点。其能够与DNA和RNA特异性地结合从而可以制备LNA探针,与DNA探针相比,其杂交的稳定性和特异性增加,可大大提高基因诊断的效率和灵敏度。
基于上述内容,本方法用于用于幽门螺杆菌16S rDNA基因AGA926-928突变的检测,检测结果可用于指导幽门螺杆菌的根除治疗。
技术实现要素:
本发明要解决的技术问题是提供一种幽门螺杆菌16S rDNA基因突变检测试剂盒,能有效地检测幽门螺杆菌16S rDNA基因耐药突变,使临床医生能获知患者幽门螺杆菌喹诺酮类抗生素耐药情况,有助于临床医生采取正确的治疗手段,提高幽门螺杆菌的根除率。
为了解决上述技术问题,本发明通过如下技术方案实现:
在本发明的第一个目的,提供了一种用于鉴定AGA926-928突变的ARMS-qPCR的引物组,优选的提供一种用于鉴定幽门螺杆菌16S rDNA基因AGA926-928突变是否含有突变位点ARMS qPCR的引物组。
本发明提供的引物组,为如下1)或2):
1)由单独使用的16S rDNA的TTC926-928突变型的ARMS引物、16S rDNA的AGA926-928双碱基突变型的ARMS引物和16S rDNA的AGA926-928单碱基突变型的ARMS引物组成;
2)由16S rDNA的TTC926-928突变型的ARMS引物、16S rDNA的AGA926-928双碱基突变型的 ARMS引物和16S rDNA的AGA926-928单碱基突变型的ARMS引物组成:
所述16S rDNA的TTC926-928突变型的ARMS引物的核昔酸序列为SEQ ID NO:5;
所述16S rDNA的AGA926-928双碱基突变型的ARMS引物的核昔酸序列为SEQ ID NO:6-10;
所述16S rDNA的AGA926-928单碱基突变型的ARMS引物的核昔酸序列为SEQ ID NO:11-12。
本发明的第二个目的是提供一种用于鉴定AGA926-928突变的ARMS-qPCR的引物探针组合,优选的,提供一种用于鉴定幽门螺杆菌16S rDNA是否存在AGA926-928突变的ARMS-qPCR的引物探针组合。
本发明提供的所述的引物探针组合包括单独使用的引物探针组合A、引物探针组合B和引物探针组合C;
所述引物探针组合A由锁核酸阻滞探针、通用TaqMan探针、PCR通用下游引物和16S rDNA的TTC926-928突变型的ARMS引物组成;
所述引物探针组合B由锁核酸阻滞探针、通用TaqMan探针、PCR通用下游引物和16S rDNA的AGA926-928双碱基突变型的ARMS引物组成;
所述引物探针组合C由锁核酸阻滞探针、通用TaqMan探针、PCR通用下游引物和16S rDNA的AGA926-928单碱基突变型的ARMS引物组成;
所述锁核酸阻滞探针的核苷酸序列为SEQ ID NO:2;
所述通用TaqMan探针的核苷酸序列为SEQ ID NO:4;
所述16S rDNA的TTC926-928突变型的ARMS引物的核苷酸序列为SEQ ID NO:5;
所述16S rDNA的AGA926-928双碱基突变型的ARMS引物的核昔酸序列为SEQ ID NO:6-10;
所述16S rDNA的AGA926-928单碱基突变型的ARMS引物的核苷酸序列为SEQ ID NO:11-12;
所述PCR通用下游引物的核苷酸序列为SEQ ID NO:3。
上述的引物探针组合还包括所述引物探针组合D;
所述引物探针组合D由所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物和内控引物组成;
所述内控引物的核苷酸序列为SEQ ID NO:1。
上述的引物探针组合中,所述检测反应液A中,所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述16S rDNA的TTC926-928突变型的ARMS引物的摩尔比为5:2:4:4;
所述引物探针组合B中,所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述16S rDNA的AGA926-928双碱基突变型的ARMS引物的摩尔比为5:2:4:4;
所述引物探针组合C中,所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述16S rDNA的AGA926-928单碱基突变型的ARMS引物的摩尔比为5:2:4:4;
所述引物探针组合D中,所述内控引物和内控TaqMan探针的摩尔比为1:1。
所述突变位点为16S rDNA基因AGA926-928突变。
本发明的第三个目的是提供一种用于鉴定AGA926-928突变的ARMS-qPCR的PCR试剂,优选的,提供一种用于鉴定幽门螺杆菌16S rDNA基因型的ARMS-qPCR的PCR试剂。
本发明提供的PCR试剂,为:
所示的PCR试剂包括PCR试剂A、PCR试剂B和PCR试剂C组成;
所述PCR试剂A由PCR扩增反应液、所述检测反应液A和水组成;
所述PCR试剂B由PCR扩增反应液、所述检测反应液B和水组成;
所述PCR试剂C由PCR扩增反应液、所述检测反应液C和水组成;
所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述16SrDNA的TTC926-928突变型的ARMS引物在所述PCR试剂A中的终浓度分别依次为:0.4μM、0.2μΜ、0.4μΜ、0.4μM;
所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述16SrDNA的AGA926-928双碱基突变型的ARMS引物在所述PCR试剂B中的终浓度分别依次为:0.4μM、0.2μΜ、0.4μΜ、0.4μM;
所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述16SrDNA的AGA926-928单碱基突变型的ARMS引物在所述PCR试剂C中的终浓度分别依次为:0.4μM、0.2μΜ、0.4μΜ、0.4μΜ。
上述所述的PCR试剂还包括PCR试剂D:
所述PCR试剂D由PCR扩增反应液、所述检测反应液D和水组成;
所述锁核酸阻滞探针、所述通用TaqMan探针、所述PCR通用下游引物、所述内控引物在所述PCR试剂D中的终浓度分别依次为:0.4μΜ、0.2μΜ、0.4μΜ、0.4μM
所述突变位点为TTC926-928、AGA926-928双碱基或AGA926-928单碱基。
在反应体系中,上述16S rDNA的TTC926-928突变型的ARMS引物、16S rDNA的AGA926-928双碱基突变型的ARMS引物16S rDNA的AGA926-928单碱基突变型的ARMS引物在本发明的实施例中其终浓度均为0.25μM。
所述突变位点为16S rDNA基因AGA926-928突变。
本发明的第四个目的是提供一种用于鉴定AGA926-928突变的ARMS-qPCR的PCR试剂盒,优选的,提供一种用于鉴定幽门螺杆菌16S rDNA基因AGA926-928突变的ARMS-qPCR的PCR试剂盒;
本发明提供的PCR试剂盒,包括是上述的引物探针组合或上述的PCR试剂。
上述的引物探针组合或上述的PCR试剂或上述的PCR试剂盒中,所述突变位点为AGA926-928突变碱基。
上述的引物探针组合或上述的PCR试剂或上述的PCR试剂盒在鉴定或辅助鉴定幽门螺杆菌16S rDNA是否含有突变为位点中的应用或在制备鉴定或辅助鉴定幽门螺杆菌16S rDNA是否含有突变位点产品中的应用也是本发明保护的范围;
或上述的引物探针组合或上述的PCR试剂或上述的PCR试剂盒在鉴定或辅助鉴定待测样 本中含有的幽门螺杆菌16S rDNA是否含有突变位点中的应用或在制备鉴定或辅助鉴定待测样本中含有的幽门螺杆菌16S rDNA是否含有突变位点的产品中的应用;
或上述的引物探针组合或上述的PCR试剂或上述的PCR试剂盒在制备鉴定或辅助鉴定含有幽门螺杆菌的待测样本是否耐四环素中的产品中的应用;
或上述的引物探针组合或上述的PCR试剂或上述的PCR试剂盒在制备鉴定或辅助鉴定待测幽门螺杆菌是否耐四环素中的产品中的应用。
上述应用中,所述突变位点为TTC926-928、AGA926-928双碱基或AGA926-928单碱基。
本发明第五个目的是提供一种用于鉴定AGA926-928突变的ARMS-q PCR的检测方法,优选的,提供一种鉴定或辅助鉴定待测样本含有的幽门螺杆菌16SrDNA是否含有突变位点ARMS-q PCR的方法。
本发明提供的方法,包括如下步骤:
1)所示的方法包括如下步骤:
用所述PCR试剂A、所述PCR试剂B、所述PCR试剂C和所述PCR试剂D分别对待测样本进行ARMS-qPCR,检测扩增产物;
若检测孔D扩增S型曲线且Ct≤32,且检测孔A扩增S型曲线且其与检测孔D扩增曲线△Ct<12,则待测样本中幽门螺杆菌16S rDNA含有或候选含有TTC926-928突变位点;
若检测孔D扩增S型曲线且Ct≤32,且检测孔B扩增S型曲线且其与检测孔D扩增曲线△Ct<12,则待测样本中幽门螺杆菌16S rDNA含有或候选含有AGA926-928双碱基突变位点;
若检测孔D扩增S型曲线且Ct≤32,且检测孔C扩增S型曲线且其与检测孔D扩增曲线△Ct<12,则待测样本中幽门螺杆菌16S rDNA含有或候选含有AGA926-928单碱基突变位点;
若检测孔D扩增S型曲线且Ct≤32,且检测孔A、B和C均无扩增曲线;或检测孔D扩增S型曲线且Ct≤35,且检测孔A、B和C的扩增曲线与检测孔D扩增曲线△Ct>12;则待测样本中幽门螺杆菌16S rDNA不含有或候选不含有突变位点;
所述突变位点为TTC926-928、AGA926-928双碱基或AGA926-928单碱基。本发明所使用的探针两端分别标记荧光报告基团(R)和荧光淬灭基团(Q)的寡核苷酸,为5’端FAM标记的TaqMan探针。在探针完整时,即随机状态和无PCR产物杂交状态时,报告基团发出的荧光被淬灭基团吸收。在ARMS-qPCR扩增过程中,当特异的PCR产物与TaqMan探针发生杂交反应时Taq酶的5’端外切酶活性同时也把探针裂解,报告基团所释放出来的荧光就可以被内置在定量检测仪内的荧光计检测到。PCR每经过一个循环,荧光信号也和目的片段一样,有一个同步指数增长的过程,荧光信号的强弱就代表了模板DNA的拷贝数的多少。因此本发明不仅可用于简单的定性检测,亦可用做样本具体含量的定量检测。
锁核酸阻滞探针标记3’端P04。
所述待测样本为离体幽门螺杆菌患者胃粘膜组织标本、粪便或培养的幽门螺杆菌。
有益效果:本发明的实验证明,本发明设计的引物及其构成的试剂盒能快速、准确、高敏感度的检测胃粘膜组织中幽门螺杆菌16S rDNA基因AGA926-928突变,灵敏度高,可以进一步预测其对四环素耐药性。
本发明采用的锁核酸阻滞探针,其序列与幽门螺杆菌16S rDNA基因野生模板完全匹配,部分碱基锁核酸化,用于特异性结合模板DNA中的Hp16S rDNA野生型DNA,因其末端磷酸化,无法延伸从而抑制突变区野生型DNA的扩增,大大增加突变检测的灵敏度与特异性。
因此,本发明用于检测16S rDNA基因突变具有以下优势:
1、特异性强:设计的ARMS引物分别针对包括16S rDNA基因的TTC926-928、AGA926-928双碱基和AGA926-928单碱基的三种突变位点序列,能特异性扩增相应突变模板DNA;在ARMS引物的3’末端倒数2-3位增加一个或者两个碱基错配,可以增加ARMS引物的特异性;本发明技术在PCR反应体系中加入野生型16S rDNA基因特异性的锁核酸阻滞探针,通过抑制野生型基因组DNA扩增从而富集突变型DNA的扩增,进一步提高了检测的特异性。
2、敏感性高:本发明技术在引物探针组合中加入野生型16S rDNA基因阻滞探针,通过特异性地抑制野生型模板的扩增,从而达到对微量突变模板的富集作用,提高检测敏感性。本技术检测16S rDNA基因突变敏感度达0.1-1%(即突变基因组DNA达到基因总DNA的0.1-1%即可检出);而直接测序法检测16S rDNA突变的敏感度约为10%(即突变基因组DNA达到基因总DNA的10%才能检出)。
3、检测过程为闭管反应,大大降低了污染及结果偏差的可能性。
4、操作简单快速,从标本送检到得出结果可在3个小时以内完成。而直接测序法检测步骤繁琐:送检标本一提取DNA—PCR扩增一验证PCR产物(电泳)一纯化PCR产物—直接测序,且其经历两个PCR产物的电泳过程,污染机会大,不适合在医院大规模开展。
5、结果判读明确、客观;可以快速对不同突变类型进行准确分型,若需要亦可对结果进行定量分析。
6、高通量,一次最多可检测48例。
7、安全:整个体系中不包含有毒有害物质,无需PCR产物的后处理,对操作员和环境都无危害。
附图说明
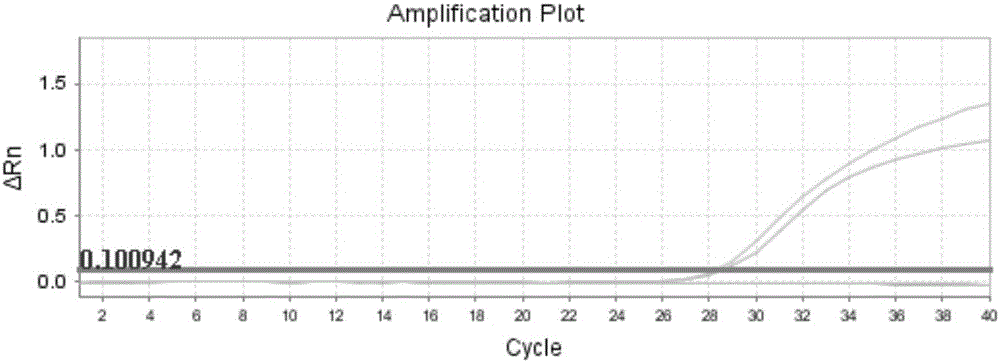
图1为用试剂盒检测幽门螺杆菌阳性样本1的TTC926-928基因突变型的扩增曲线图
图2为用试剂盒检测幽门螺杆菌阳性样本2的AGA926-928双碱基基因突变型的扩增曲线图
图3为用试剂盒检测幽门螺杆菌阳性样本3的AGA926-928单碱基基因突变型的扩增曲线图
图4为用试剂盒检测幽门螺杆菌阳性样本的16S rDNA基因野生型的扩增曲线图
具体实施方式
下面结合附图和实施例对本发明进一步说明。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1、ARMS-qPCR检测试剂盒及其专用引物和探针的设计
一、引物及探针
使用Primer Express Version3软件在两个突变的序列区域设计探针及引物。设计并筛选能特异性检测AGA926-928突变(TTC926-928、AGA926-928双碱基、AGA926-928单碱基)的ARMS引物1或多条及内控引物一条,设计通用下游引物一条,设计并筛选通用TaqMan探针一条,设计并筛选锁核酸阻滞探针一条,各探针、引物序列分别具体如下:
锁核酸阻滞探针的核苷酸序列如SEQ ID NO:2所示,其3’端标记P04;
通用TaqMan探针的核苷酸序列如SEQ ID NO:4所示,其5’端标记FAM,3’端标记BHQ;
用于检测16S rDNA的突变型ARMS引物由用于检测16S rDNA的TTC926-928突变型的ARMS引物、用于检测16S rDNA的AGA926-928双碱基突变型的ARMS引物和用于检测16S rDNA的AGA926-928单碱基突变型的ARMS引物组成,其中,
用于检测16S rDNA的TTC926-928突变型的ARMS引物的核苷酸如序列5所示;
用于检测16S rDNA的AGA926-928双碱基突变型的ARMS引物的核苷酸如序列6-10所示;
用于检测16S rDNA的AGA926-928单碱基突变型的ARMS引物的核苷酸如序列11-12所示;
内控引物为一条能够同时扩增16S rDNA野生型及突变型基因组DNA的上游引物,其核苷酸如序列1所示;
PCR通用下游引物的核苷酸如序列3所示。
将设计好的引物及探针序列交由合成公司合成,一般采用仪器自动化学合成,需提供合成检验合格报告。
二、幽门螺杆菌荧光定量PCR的试剂或试剂盒配制
1、反应体系的优化
(1)引物浓度的优化:在反应体系其它条件相同的情况下,将引物浓度分别从0.1μM至1.0μM作倍比连续稀释,通过对试验结果的分析比较,确定最佳引物浓度是0.5μΜ。
(2)探针浓度的优化:在反应体系其他条件相同的情况下,将探针浓度分别从0.05μM至0.5μM作倍比连续稀释,通过对试验结果的分析比较,确定最佳探针浓度是0.2μΜ。
(3)酶的优化:在反应体系中加入各种酶,通过对试验结果的分析比较,确定最佳酶是Ex Taq酶。
(4)Mg2+浓度的优化:在反应体系其它条件相同的情况下,将q引物探针组合组分镁离子浓度分别从0.5mM至4.0mM作倍比连续稀释,通过对试验结果的分析比较,确定最佳Mg2+浓度是2mM。
(5)退火温度的优化:在反应体系其它条件相同的情况下,进行梯度PCR(57-62℃退火温度),通过对试验结果的分析比较,确定最佳退火温度是59℃。
经优化,用于检测待测样本中的16S rDNA是否突变的PCR试剂为:
1)由PCR试剂A-D组成:
PCR试剂A为TTC926-928检测管反应体系:20μL,由qPCR混合反应液10μL、通用下游引物1μL(终浓度0.5μM)、TTC926-928的ARMS引物1μL(终浓度0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μΜ)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/μL)和水组成。
PCR试剂B为AGA926-928双碱基检测管反应体系:20μL,由qPCR混合反应液10μL、通用下游引物1μL(终浓度0.5μM)、AGA926-928双碱基的ARMS引物1μL(终浓度0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μΜ)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/y L)和水组成。
PCR试剂C为AGA926-928单碱基检测管反应体系:20μL,由qPCR混合反应液10μL、通用下游引物1μL(终浓度0.5μM)、AGA926-928单碱基的ARMS引物1μL(终浓度0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μΜ)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/y L)和水组成。
PCR试剂D为内控管的反应体系,与检测管相同,不同的是将ARMS引物替换为内控引物。
上述qPCR混合反应液组分及其终浓度见表1。
表1为qPCR组合组分
2、试剂盒组成
可以将上述的锁核酸阻滞探针、通用TaqMan探针、针对16S rDNA的TTC926-928的ARMS引物或针对16S rDNA的AGA926-928双碱基的ARMS引物或针对16S rDNA的AGA926-928单碱基的ARMS引物、内控引物、PCR通用下游引物以及水作为试剂盒的主要组成,构建获得试剂盒;
试剂盒中具体含有下列试剂和材料:
(1)引物溶液:a、锁核酸阻滞探针(序列2);b、通用TaqMan探针(序列4),;c、ARMS引物(序列5-12);d、内控引物(序列1);e、PCR通用下游引物(序列3)。
(2)qPCR反应液:包括10×PCR缓冲液;dNTPs;MgCl2溶液;Taq酶。
(3)阳性质控:为人工合成的16S rDNA基因AGA926-928突变的混合质粒DNA。
(4)阴性质控:无菌双蒸水
(5)无菌双蒸水
实施例2、幽门螺杆菌16S rDNA基因AGA926-928突变的ARMS-qPCR检测方法
一、检测
1、样本制备
从离体人胃粘膜组织标本中获取DNA,推荐使用商业化的试剂盒提取基因组DNA作为样本1-4;测定DNA浓度和纯度,要求浓度大于1ng/μL;OD260nm/OD280nm=1.8~2.0。
2、荧光PCR检测
1)ARMS引物分型检测
对于样本1-4中每个样本均在四个管A-D分别进行反应,四个管分别对应TTC926-928突变检测管(ep管A)、AGA926-928双碱基突变检测管(ep管B)、AGA926-928单碱基突变检测管(ep管C)、内控管(印管D)。检测管(A-C)内反应加入qPCR反应液、LNA阻滞探针、通用TaqMan探针、通用下游引物、模板DNA及相应的ARMS引物;内控管(D)基本相同,所不同的是加入内控引物替代ARMS引物,具体如下:
ep管A(PCR试剂A):20μl反应体系,由qPCR混合反应液10μl、通用下游引物1μL(终浓度(△5μΜ)、TTC926-928的ARMS引物1μL(终浓度(0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μΜ)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/μL)和水组成;
epB(PCR试剂B):20μL反应体系,由qPCR混合反应液10μL、通用下游引物1μL(终浓度(0.5μΜ)、AGA926-928双碱基的ARMS引物1μL(终浓度(0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μΜ)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/μL)和水组成;
epC(PCR试剂C):20μL反应体系,由qPCR混合反应液10μL、通用下游引物1μL(终浓度(0.5μΜ)、AGA926-928单碱基的ARMS引物1μL(终浓度(0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μΜ)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/μL)和水组成;
epD(PCR试剂D):20μL反应体系,由qPCR混合反应液10μL、通用下游引物1μL(终浓度0.5μΜ)、内控引物IμL(终浓度0.5μΜ)、通用TaqMan探针0.4μL(终浓度0.2μM)、锁核酸阻滞探针0.8μL(终浓度0.4μΜ)、模板DNA5μL(终浓度l-300ng/μL)和水组成。
PCR反应条件为:95℃预变性10分钟,95℃ 15秒,58℃ 40秒,扩增反应40循环,在58℃ 40秒阶段收集荧光。
ARMS-qPCR在ABI7500检测仪上进行。
3、结果判读:
若内控引物管扩增曲线阴性或Ct>32,提示该样本提取失败,需要重新提取。ARMS检测结果如图1-4所示:
对于样本1,内控引物管D扩增S型曲线且Ct≤32,ARMS引物管A有扩增S型曲线且ARMS引物管A与内控引物管D的扩增曲线△Ct<12,待测样本含有或候选含有TTC926-928突变(图1为样本1的3个ARMS引物检测管及内控管的扩增图);
对于样本2,内控引物管D扩增S型曲线且Ct≤32,ARMS引物管B有扩增S型曲线且ARMS引物管B与内控引物管D的扩增曲线△Ct<12,待测样本AGA926-928发生突变的碱基有2个(图2为样本2的3个ARMS引物检测管及内控管的扩增图);
对于样本3,内控引物管D扩增S型曲线且Ct≤32,ARMS引物管C有扩增S型曲线且ARMS引物管C与内控引物管D的扩增曲线△Ct<12,待测样本AGA926-928发生突变的碱基有1个(图3为样本3的3个ARMS引物检测管及内控管的扩增图);
对于样本4,内控引物管D扩增S型曲线且Ct≤32,三种ARMS引物管A、B、C均无扩增曲线,待测样本AGA926-928碱基未发生突变,其为16S rDNA野生型基因(图4为样本4的3个ARMS引物检测管及内控管的扩增图);
分别以样本1-4的基因组DNA为模板,用5’ATGAATGGCGTAACGA3’引物正向测序样本1-4的16S rDNA基因目的片段,结果与本发明的方法一致,证明本发明的方法正确。
二、特异性检测
用实施例1中的ARMS引物分型检测方法检测实验室保存的110株经测序已知突变类型的幽门螺杆菌临床分离株的16S rDNA序列进行扩增,结果除阴性对照外,其余对相应的DNA突变或者不突变形成呈阳性扩增,与测序结果符合率达到100%。
三、灵敏度检测
以人工合成的对应序列幽门螺杆菌16S rDNA野生型基因、幽门螺杆菌16S rDNA的AGA926-928碱基各种突变类型分别连接到pMD18-T载体为模板,浓度梯度均稀释为10~106CFU为模板。按照上述一的ARMS引物分型检测方法进行real-time PCR,每个模板浓度梯度做3个平行样本,每个模板用其突变类型对应的检测管进行检测,当体系标准模板量为10~106CFU时,每个浓度梯度的3个平行样本均扩增阳性,三种ARMS引物管A、B、C的检测下限均为10CFU,其灵敏度均为10CFU。因此,可以用实施例1中的用于检测待测样本中16S rDNA是否突变的PCR试剂A-D检测待测样本中幽门螺杆菌16S rDNA基因AGA926-928是否突变或检测待测样本是否耐四环素;并且可以对突变阳性样本进行初步的分型。
若内控引物扩增S型曲线且Ct≤32,且用于检测16S rDNA的TTC926-928突变型ARMS引物扩增S型曲线且其与内控引物的扩增曲线△Ct<12,则待测样本中幽门螺杆菌23S rDNA含有TTC926-928突变,待测样本对四环素耐药;
若内控引物扩增S型曲线且Ct≤32,且用于检测16S rDNA的AGA926-928双碱基突变型ARMS引物扩增S型曲线且其与内控引物扩增曲线△Ct<12,则待测样本中幽门螺杆菌16SrDNA含有或候选含有AGA926-928双碱基突变位点,待测样本为或候选为对四环素耐药;
若内控引物扩增S型曲线且Ct≤32,且用于检测16S rDNA的AGA926-928单碱基突变型ARMS引物扩增S型曲线且其与内控引物的扩增曲线△Ct<12,则待测样本中幽门螺杆菌16SrDNA含有或候选含有AGA926-928单碱基突变位点,△Ct<12待测样本为或候选为对四环素耐药;
若内控引物扩增S型曲线且Ct≤32,且用于检测16S rDNA的TTC926-928突变型ARMS引物、AGA926-928双碱基突变型ARMS引物和AGA926-928单碱基突变型ARMS引物均无扩增曲线或与内控引物的扩增曲线均△Ct>12,待测样本16S rDNA不含有或候选不含有AGA926-928碱基中任一个突变位点,表现为对四环素敏感。
实施例3、克拉霉素耐药基因ARMS-qPCR试剂盒的临床应用
1、样本制备
收集临床病理诊断为幽门螺杆菌阳性的100例患者的石蜡包埋胃粘膜组织切片或冰冻胃粘膜组织块,从组织中提取基因组DNA。测定DNA浓度和纯度,要求浓度大于1ng/μL;OD260nm/OD280nm=1.8~2.0。
2、荧光PCR检测
按照实施例2的方法中的ARMS引物分型检测进行荧光PCR检测。结果如下:
在临床病理诊断为幽门螺杆菌阳性的100例患者中共检测出1例16S rDNA的TTC926-928突变型阳性样本、5例16S rDNA的AGA926-928双碱基突变型突变阳性样本和9例16S rDNA的AGA926-928单碱基突变型突变阳性样本,其余为野生型样本(编号为15-50)。经测序验证,结果一致。
将上述野生型样本、TTC926-928突变阳性样本、AGA926-928双碱基突变阳性样本进行四环素培养法耐药检测,结果TTC926-928突变阳性、AGA926-928双碱基突变阳性和AGA926-928单碱基突变阳性均存在不同程度的四环素耐药现象,而野生型样本四环素敏感。
上述结果表明,应用本发明的引物、探针检测胃粘膜组织16S rDNA基因突变灵敏度高,可检测临床样本中的微量突变模板(0.1-1%);结果可靠,与突变检测“金标准”直接测序法的结果符合率为100%。此外,该方法检测速度快,操作简单,结果判读客观,闭管反应污染少,非常适合于在临床中大规模开展。
本发明不局限于上述具体的实施方式,本领域的普通技术人员从上述构思出发,不经过创造性的劳动,所作出的种种变换,均落在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!