用于集成的样品制备、反应和检测的设备与方法与流程
本申请是申请人卢米耐克斯公司的申请日为2012年5月4日、国家申请号为201280033332.9(国际申请号为pct/us2012/036491)、发明名称为“用于集成的样品制备、反应和检测的设备与方法”的中国专利申请的分案申请。
相关申请的交叉引用
本申请要求于2011年5月4日提交的名称为“automatedpcrinstrument”的美国临时申请no.61/482,494以及于2011年6月15日提交的名称为“apparatusandmethodsforintegratedsamplepreparation,reactionanddetection”的美国临时申请no.61/497,401的优先权,每个上述申请的全部内容均通过参引并入本文中。
本申请为于2011年2月23日提交的名称为“apparatusandmethodsforintegratedsamplepreparation,reactionanddetection”的美国专利申请no.13/033,129的的部分连续案,其要求于2010年2月23日提交的名称为“cassetteandinstrumentforintegratednucleicacidisolationandamplification”的美国临时申请no.61/307,281的优先权,每个上述申请的全部内容均通过参引并入本文中。
背景技术:
本文中描述的实施方式涉及用于样品制备、反应和分析的设备和方法。更具体地,本文中描述的实施方式涉及药筒和仪器,在药筒和仪器内可以在集成的过程中执行核酸的分离、扩增和分析。
一些已知的诊断程序包括分离并分析诸如dna或rna之类的核酸。用于分离样品内的核酸的已知方法通常包括数个步骤,比如:(1)通过添加蛋白酶(例如,蛋白酶k)来去除样品内的蛋白质;(2)分解剩余的大块样品以暴露其中含有的核酸(也称为细胞裂解);(3)使核酸从样品中沉淀;以及(4)洗涤和/或以其它方式制备核酸用于进一步分析。
在某些情况下,进一步的分析需要扩增经分离的核酸(例如,复制核酸以增加其拷贝数)。聚合酶链反应(pcr)过程为用于扩增核酸分子的部分的已知技术。在pcr期间,含有靶dna的输入样品与试剂相混合,所述试剂包含dna聚合酶(例如,taq聚合酶)。输入样品可以为例如通过上述程序产生的经分离的核酸样品。之后该样品在分离室内进行热循环多次以完成反应。非常小心地控制热循环的温度与时间以确保准确的结果。dna序列被充分地扩增之后,可以使用多种光学技术来对其进行分析。
用于执行核酸分离和扩增的一些已知系统包括不同的部分(例如,分离部分和扩增部分),样品必须在所述不同的部分之间通过使用可以损害样品完整性的人为干预和/或过程来传送。用于执行核酸分离和扩增的一些已知系统包括要求由有经验的实验室技术人员有效准备和/或校准的复杂控制系统。因此,这种已知的系统并非很好地适合于“工作台”应用、高容量诊断程序和/或在多种多样的实验室环境中使用。
在某些应用中,可能需要反应的多个阶段,其中一个或多个较后阶段需要在反应的阶段之间的额外试剂。例如,在反转录pcr中,反转录反应通常在执行pcr过程之前完成,其中pcr过程需要额外试剂。在一些已知的系统中反应的较后阶段所需的额外试剂通常采用可以损害样品完整性的人为干预和/或过程传送至反应室中。因此,这种已知过程可以引发错误和污染,并且也可以是对于高通量应用而言昂贵的和/或难以实施的。
尽管一些已知的系统包括容纳试剂的室,但这种室通常整合至药筒和/或反应室。因此,当这种系统和/或药筒与不同的反应和/或测定结合使用时,通常使用完全不同的药筒、盒或其它设备以促进使用试剂的特定组合,从而进行期望的反应过程。因此,这种已知的系统和/或药筒通常对于不同的反应过程和/或测定而言是不能互换使用的。
尽管一些已知的系统包括光学检测系统,以检测测试样品内的一个或多个不同的被分析物和/或靶,但是这种已知的系统通常包括位于装置的能够相对于反应室移动的一部分中的激发光来源和/或发射光的检测器。例如,一些已知的系统构造成经由可移动盖向反应室供应激发光束。因此,这种已知的系统易于受到由激发光路和/或检测光路的位置变化所造成的检测变化的影响。
因此,存在对用于执行核酸分离、扩增和检测的改进设备和方法的需求。
技术实现要素:
本文描述了执行样品分离和下游反应的药筒和仪器。在一些实施方式中,设备包括壳体、反应小瓶和传送机构。壳体限定第一流动路径和第二流动路径。该壳体具有传送端口,该传送端口限定与第二流动路径和壳体外部的容积流体连通的开口。传送端口包括流动控制构件以限制通过该开口的流动,反应小瓶联接至壳体并且限定反应容积,该反应容积经由第二流动路径与传送端口流体连通。传送机构构造成在该传送机构被致动时从分离模块的分离室经由至少第一流动路径向反应室传送样品。传送机构构造成在反应小瓶中产生真空以产生样品从分离室向反应容积的流动。
附图说明
图1和图2分别为根据实施方式的药筒处于第一构型和第二构型的示意性图示。
图3为根据实施方式的药筒的示意性图示,该药筒具有第一模块、第二模块和第三模块。
图4为根据实施方式的药筒的示意性图示,该药筒具有第一模块、第二模块和第三模块。
图5为根据实施方式的药筒的示意性图示,该药筒具有第一模块和第二模块。
图6和图7分别为根据实施方式的药筒的一部分处于第一构型和第二构型的示意性图示。
图8为根据实施方式的药筒的侧视立体图。
图9为图8中示出的药筒的俯视立体图。
图10为图8中示出的药筒的侧视剖视图。
图11为图8中示出的药筒的一部分的侧视分解图。
图12和图13为图8中示出的药筒的试剂模块的立体图。
图14为图12和图13中示出的试剂模块的一部分的立体图。
图15至图18分别为图8中示出的药筒的分离模块处于第一构型、第二构型、第三构型和第四构型的侧视剖视图。
图19为图8中示出的药筒的分离模块的侧视剖视图。
图20为图19中示出的分离模块的阀组件的一部分沿图19中的线x1-x1截取的剖视图。
图21为图19中示出的分离模块的阀组件的一部分的立体图。
图22为图8中示出的药筒的立体剖视图。
图23为图8中示出的药筒的pcr模块的立体图。
图24为图8中示出的药筒的立体剖视图。
图25为根据实施方式的药筒的侧视立体图。
图26为图25中示出的药筒的分离模块处于第一构型的侧视立体图。
图27为图26中示出的分离模块处于第一构型的侧视剖视图。
图28为图26中示出的分离模块处于第二构型的侧视立体图。
图29为图25中示出的药筒的pcr模块处于第一构型的侧视立体图。
图30为图29中示出pcr模块处于第一构型的侧视剖视图。
图31为图29中示出的pcr模块处于第二构型的侧视剖视图。
图32和图33分别为图25中示出的药筒处于第一构型和第二构型的侧视剖视图。
图34为根据实施方式的仪器的一部分的示意性图示。
图35为根据实施方式的仪器的示意性立体剖视图示。
图36为根据实施方式的仪器的立体图。
图37为图36中示出的仪器的第一致动器组件的立体图。
图38为图37中示出的第一致动器组件的立体分解图。
图39为图37中示出的第一致动器组件的后视立体图。
图40为图37中示出的第一致动器组件的一部分的立体图。
图41为图36中示出的仪器的传送致动器组件的俯视立体图。
图42为图41中示出的传送致动器组件的仰视立体图。
图43为图41中示出的传送致动器组件的后视立体图。
图44为图41中示出的传送致动器组件的一部分的立体图。
图45为图41中示出的传送致动器组件的一部分的立体图。
图46为图41中示出的传送致动器组件的蜗杆传动轴的立体图。
图47为图36中示出的仪器的第二致动器组件的俯视立体图。
图48为图47中示出的第二致动器组件的侧视立体图。
图49至图51为图47中示出的第二致动器组件的一部分的立体图。
图52为图36中示出的仪器的加热器组件的侧视立体图。
图53为图52中示出的加热器组件的接收块的立体图。
图54和图55分别为图52中示出的加热器组件的接收块的前视图和俯视图。
图56为图52中示出的加热器组件的接收块沿图54中示出的线x2-x2截取的剖视图。
图57为图52中示出的加热器组件的夹具的立体图。
图58为图52中示出的加热器组件的安装块的立体图。
图59为图52中示出的加热器组件的散热片的立体图。
图60为图52中示出的加热器组件的安装板的立体图。
图61和图62分别为图52中示出的加热器组件的第一隔离构件和第二隔离构件的立体图。
图63为图52中示出的加热器组件的加热块的立体图。
图64和图66分别为图36中示出的仪器的光学组件的前视立体图和后视立体图。
图65为图64和图66中示出的光学组件的立体分解图。
图67为图64和图66中示出的光学组件的安装构件的立体图。
图68为图64和图66中示出的光学组件的滑块的立体图。
图69为图64和图66中示出的光学组件的滑轨的立体图。
图70为图64和图66中示出的光学组件的纤维光学模块的一部分的立体图。
图71a、71b、72a、72b和73为图36中示出的仪器的电子控制系统的方块图。
图74至图76分别为根据实施方式的光学组件处于第一构型、第二构型和第三构型的示意性图示。
图77至图80为根据实施方式检测含有核酸的样品中靶分析物的方法的流程图。
图81为通过使用根据实施方式的系统和方法产生的分子信号标记。
图82为根据实施方式的分离模块的构造成接收声学能的部分的立体剖视图。
图83为根据实施方式的分离模块的构造成接收声学能的部分的立体剖视图。
图84a为图26中示出的药筒的一部分及声换能器的立体剖视图。
图84b为图84中示出的一系列声换能器的设置于图36的仪器中包括的超声致动器组件中、并与图26中示出的一组药筒接触的一部分的立体剖视图。
图85为根据实施方式的药筒的立体图。
图86为图85中示出的药筒在没有盖的情况下的立体图。
图87为图85中示出的药筒的pcr模块的立体图。
图88为根据实施方式的pcr模块的剖视图。
图89为根据实施方式的药筒的立体图。
图90为根据实施方式的药筒的立体图。
图91为根据实施方式的药筒的立体图。
图92为根据实施方式的药筒的立体图。
图93为图92中示出的药筒的立体分解图。
图94为根据实施方式的具有多个pcr小瓶的药筒的立体图。
图95为两个仪器的图像,其中,一个仪器用于分离样品,第二个仪器用于检测样品。
图96为本发明的仪器的图像。
图97a至图97c为根据一个实施方式的具有用于插入外部传送探针的端口的药筒的各种视图。
图97d为包括微孔板和在图97a至图97c中示出的外部传送探针的分析仪器的照片。
图98为根据实施方式的具有集成的流动池的药筒的立体图。
图99a和图99b为图98中示出的药筒的立体图。
图100为根据一个实施方式的流动池的立体图。
图101a和图101b分别为根据一个实施方式的具有囊的流动池处于第一构型和第二构型的示意性图示。
图102a和图102b为根据两个实施方式的流动池的示意性图示。
图103为根据一个实施方式的具有波纹管状件的流动池的示意性立体图。
图104为根据实施方式的本发明的混合设备的示意性图示。
图105为根据一个实施方式的可移动光学读取器的示意性图示。
图106为根据实施方式的具有用于阻挡珠流动的机构的流动池的示意性图示。
图107为根据实施方式的具有多个容积以利于数字pcr的药筒处于第一构型的剖视图。
图108为图107的药筒的处于第二构型中的剖视图。
具体实施方式
本文中描述了用于执行样品分离、反应和/或检测的药筒和仪器。在一些实施方式中,设备包括壳体、反应小瓶和传送机构。该壳体限定第一流动路径和第二流动路径。该壳体具有传送端口,该传送端口限定与第二流动路径和壳体外部的容积流体连通的开口。传送端口包括流动控制构件,以限制通过该开口的流量。反应小瓶联接至壳体并限定反应容积,该反应容积经由第二流动路径与传送端口流体连通。传送机构构造成当该传送机构被致动时从分离模块的分离室经由至少第一流动路径向反应室传送样品。传送机构构造成在反应小瓶中产生真空以产生样品从分离室向反应容积的流动。
在一些实施方式中,一种设备包括壳体、反应小瓶和传送机构。该壳体限定第一流动路径和第二流动路径,并且具有吸入部和可刺穿构件。吸入部和可刺穿构件限定吸入容积。反应小瓶联接至壳体,并限定经由第二流动路径与吸入容积流体连通的反应容积。传送机构构造成在该传送机构被致动时从分离模块的分离室经由至少第一流动路径向反应室传送样品。壳体的吸入部具有构造成接纳传送探针的一部分的端口。该端口构造成使得传送探针的尖端刺穿可刺穿构件以在传送探针的一部分被设置在端口内时将吸入容积安置成与端口流体连通。
在一些实施方式中,一种设备包括壳体、反应小瓶、传送机构和一组可移动构件。壳体限定流动路径。反应小瓶联接至壳体并且限定与流动路径流体连通的反应容积。传送机构构造成在该传送机构被致动时将样品从反应室传送至流动路径中。该组可移动构件可移动地联接至壳体。该组可移动构件构造成将流动路径分隔为一组pcr容积,每个pcr容积与相邻的pcr容积流体隔离。
在一些实施方式中,一种方法包括将样品从反应容积运送至由壳体限定的流动路径中。该样品包括一组靶核酸分子。一组可移动构件被移动为将流动路径划分成一组pcr容积,使得每个pcr容积包含不多于一个的靶核酸分子。加热元件被启动以对来自多个pcr容积中的各个pcr容积的内含物进行热循环。
在一些实施方式中,一种设备包括:分离模块,该分离模块可以用于例如分离核酸样品或分析物样品;和反应模块,该反应模块可以用于例如扩增核酸样品、或者测试分析物与其它化合物的结合。分离模块包括第一壳体和第二壳体。第一壳体限定第一室和第二室。至少第一室构造成容纳样品,例如含有核酸的样品。第二壳体包括侧壁和可刺穿构件,所述侧壁和可刺穿构件共同限定第一容积,该第一容积构造成容纳第一物质。第一物质可以是例如试剂、洗涤缓冲溶液,矿物油和/或待添加至样品中的任何其它物质。第二壳体的至少一部分构造成设置在第一壳体内,使得当可刺穿构件的一部分被刺穿时第一容积与第一室流体连通。反应模块限定反应室和第二容积,该第二容积构造成容纳第二物质。反应模块构造成联接至分离模块,使得反应室与第二容积各自与第一壳体的第二室流体连通。
在一些实施方式中,一种设备包括第一模块、第二模块和第三模块。第一模块限定第一室和第二室。至少第一室构造成容纳样品。第二模块限定第一容积,该第一容积构造成容纳第一物质。第一物质可以是例如试剂、洗涤缓冲溶液,矿物油和/或待添加至样品中的任何其它物质。第二模块的一部分构造成当第二模块联接至第一模块时设置在第一模块的第一室内,使得第一容积构造成选择性地安置成与第一室流体连通。第三模块限定反应室和第二容积。该第二容积构造成容纳第二物质。第三模块的一部分在第三模块联接至第一模块时设置在第一模块的第二室内,使得反应室和第二容积各自与第一模块的第二室流体连通。
在一些实施方式中,一种设备包括第一模块、第二模块和第三模块。第一模块限定第一室和第二室。第一模块包括第一传送机构,该第一传送机构构造成在第一室和第二室之间传送样品的同时维持第一室与第二室之间流体隔离。第二模块限定构造成容纳例如试剂等物质的容积。第二模块的一部分构造成在第二模块联接至第一模块时设置在第一模块的第一室内,使得该容积构造成选择性地安置成与第一室流体连通。第三模块限定反应室。该第三模块构造成联接至第一模块,使得反应室与第二室流体连通。第三模块包括第二传送机构,该第二传送机构构造成在第二室与反应室之间传送样品的一部分。
在一些实施方式中,一种设备包括第一模块和第二模块。第一模块包括反应小瓶、基底和第一传送机构。反应小瓶限定反应室并且可以是例如pcr小瓶。第一传送机构包括柱塞,该柱塞可移动地设置在壳体内,使得壳体与柱塞限定第一容积,该第一容积容纳第一物质。柱塞可以在第一位置与第二位置之间移动。第一物质可以是例如试剂、矿物油等。基底限定第一流动路径与第二流动路径的至少一部分。第一流动路径构造成与反应室、第一容积和分离模块的分离室流体连通。第二流动路径构造成与分离室流体连通。柱塞的一部分设置在第一流动路径内,使得当柱塞处于第一位置时第一容积与反应室流体隔离。柱塞的该部分设置为远离第一流动路径,使得当柱塞处于第二位置时第一容积与反应室流体连通。柱塞构造成在反应室内产生真空,以在柱塞从第一位置向第二位置移动时从分离室向反应室传送样品。第二模块包括第二传送机构并且限定第二容积,该第二容积构造成容纳第二物质。第二模块构造成联接至第一模块,使得第二容积可以选择性地安置成经由第二流动路径与分离室流体连通。第二传送机构构造成在当第二传送机构被致动时从第二容积向分离室传送第二物质。
在一些实施方式中,一种用于对容纳样品的药筒进行操纵和/或致动的仪器可以包括块体、第一光学构件、第二光学构件和光学组件。块体限定反应容积,该反应容积构造成接纳至少一部分的反应容器。块体可以包括用于促进、产生、支持和/或加快与样品相关联的反应的机构和/或附接至用于促进、产生、支持和/或加快与样品相关联的反应的机构。例如,在一些实施方式中,块体可以联接至加热元件,该加热元件构造成使样品热循环。第一光学构件设置为至少部分地位于块体内,使得第一光学构件与反应容积光学连通。第二光学构件设置为至少部分地位于块体中,使得第二光学构件与反应容积光学连通。光学组件包括激发模块和检测模块,该激发模块构造成产生多道激发光束,该检测模块构造成接收多道发射光束。光学组件联接至第一光学构件和第二光学构件,使得多道激发光束中的每道激发光束可以被传送至反应容积中并且可以从反应容积中接收多道发射光束中的每道发射光束。
在一些实施方式中,一种用于操纵和/或致动药筒的仪器包括机架、声换能器和致动机构。机架构造成容纳药筒,该药筒具有限定容积的壳体。该容积可以接纳例如包含核酸的样品之类的样品的一部分。声换能器构造成产生声能。致动机构构造成将声换能器的至少一部分移动成与药筒的一部分接触。致动机构还构造成调整由抵靠药筒的一部分的声换能器的一部分所施加的力。
术语“光束”在本文中用于描述电磁能的任何投射,无论是否在可见光谱中。例如,光束可以包括在由激光、发光二极管(led)、闪光灯等产生的可见光谱中电磁辐射的描准投射。光束可以是在预期时间段内连续的或在预期时间段内非持续的(例如,脉冲式的或间歇性的)。在某些情况下,光束可以包括诸如存在于样品中的分析物的量之类的信息(即,光束可以是光信号)和/或与所述信息相关联。
术语“平行”或在本文中用于描述两个几何结构(例如,两条线,两个平面,一条线与一个平面等)之间的关系,其中,所述两个几何结构随着其基本上延伸至无穷而基本上不相交。例如,如本文中使用的,当第一条线与第二条线随着其延伸至无穷而不相交时,第一条线被称为平行于第二条线。同样地,当平坦的表面(即,二维表面)被称为平行于一条线时,沿着该线的每个点与该表面的最靠近部分间隔开基本上相等的距离。当两个几何结构名义上彼此平行时,例如,当它们在公差内彼此平行时,它们在本文中被描述为彼此“平行”或“基本上平行”。这种公差可以包括例如制造公差、测量公差等。
术语“正交”在本文中用于描述两个几何结构(例如,两条线,两个平面,一条线与一个平面等)之间的关系,其中,所述两个几何结构在至少一个平面内以约90度的角度相交。例如,如在本文中使用的,当一条线与一个平面在平面内以约90度的角度相交时,该第一条线被描述为与该平面正交。当两个几何结构名义上正交于彼此,例如,它们在公差内彼此正交时,它们在本文中被描述为彼此“正交”或“基本上正交”。这种公差可以包括例如制造公差、测量公差等。
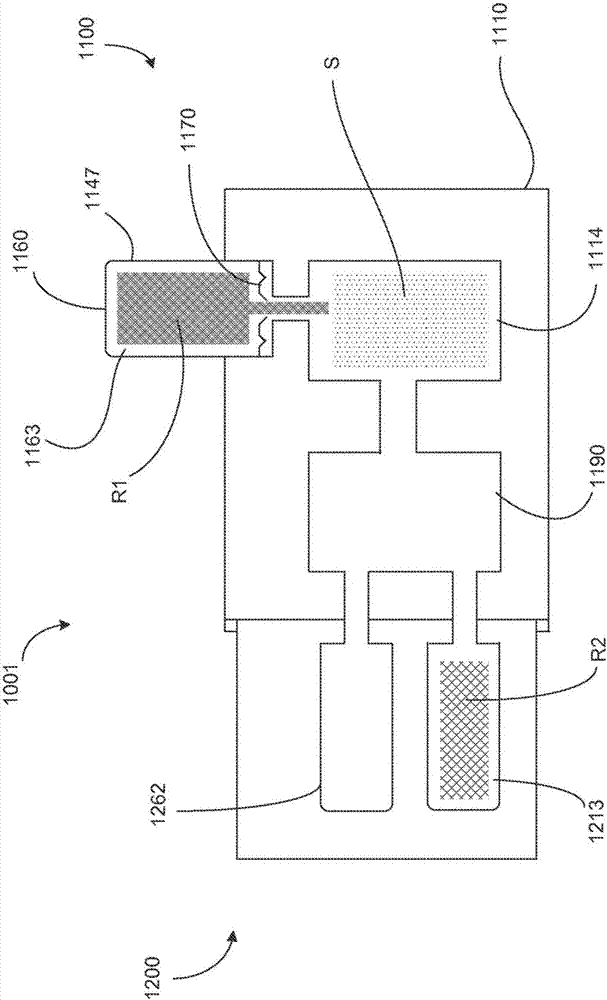
图1和图2分别为根据实施方式的处于第一构型和第二构型的药筒1001的示意性图示,该药筒1001包括分离模块1100和反应模块1200。分离模块1100和反应模块1200彼此联接,使得分离模块1100与反应模块1200能够被安置成彼此流体连通。如本文中描述的,分离模块1100与反应模块1200可以以任何适合的方式联接在一起。在一些实施方式中,例如,分离模块1100与反应模块1200可以分开地构造并联接在一起以形成药筒1001。分离模块1100与反应模块1200之间的这种布置允许分离模块1100的各种不同构型与反应模块1200的各种不同构型一起使用。分离模块1100的不同构型和/或反应模块1200的不同构型可以包括分离模块1100和/或反应模块1200内的不同的试剂和/或不同的结构。
药筒1001可以通过本文中描述的任何仪器来操作和/或致动。在一些实施方式中,药筒1001可以用来执行样品制备、对该样品执行核酸分离和/或聚合酶链反应(pcr)。在这种实施方式中,分离模块1110可以将靶核酸从容纳在分离模块1110内的样品中分离出。之后,经分离的核酸可以在反应模块1200中被扩增(例如,使用pcr),如以下进一步描述的。药筒1001的模块布置允许任何数目的不同的反应模块1200——所述不同的反应模块1200各自容纳例如不同的试剂和/或各自构造成扩增不同类型的样品——与分离模块1100一起使用,反之亦然。
分离模块1100包括第一壳体1110和第二壳体1160。如在本文中更详细地描述的,第二壳体1160联接至第一壳体1110,使得第二壳体1160可以被安置成与第一壳体1110流体连通。在一些实施方式中,第一壳体1110和第二壳体1160以模块化的方式布置,从而使得不同构型的第一壳体1110和第二壳体1160可以彼此一起使用。第一壳体1110和第二壳体1160的不同构型可以包括例如不同的化学品、试剂、样品和/或不同的内部结构。
第一壳体1110限定第一室1114和第二室1190。第一室1114或第二室1190中的至少一个可以容纳样品s。样品s可以是任何生物样品——例如含有一个或多个靶核酸的生物样品,比如尿、血液、含有组织样品的其它材料等。样品s可以通过任何适合的机构引入第一室1114或第二室1190中,这些适合的机构包括例如经由第一壳体1110中的开口或可刺穿构件(未示出)将样品s吸移或注射到第一室1114和/或第二室1190内的机构。尽管第一室1114示出为与第二室1190流体连通,但是在其它实施方式中第一室1114可以被选择性地安置成与第二室1190流体连通。换言之,在一些实施方式中,第一壳体1110可以包括任何适合的机构,比如可以将第一室1114选择性地安置成与第二室1190流体连通的阀(在图1和图2中未示出)。此外,在其它实施方式中,第一壳体1110可以具有任何适合的流量控制和/或传送机构(在图1和图2中未示出),以便于物质在第一室1114与第二室1190之间的传送和/或控制物质在第一室1114与第二室1190之间的传送,所述机构包括例如阀、毛细管流动控制装置、泵等。在另一些实施方式中,第一室1114可以与第二室1190流体隔离。
第二壳体1160包括侧壁1147和可刺穿构件1170。侧壁1147和可刺穿构件1170限定第一容积1163。第一容积1163可以被完全地或部分地用物质r1填充。物质r1可以是诸如例如矿物油、洗涤缓冲液、荧光染料、试剂等之类的生物或化学物质。如图1和图2中所示,第二壳体1160的一部分设置在第一壳体1110中,使得当可刺穿构件1170被刺穿、破坏、割断和/或破裂时,第一容积1163如图2中所示地与第一室114流体连通。类似陈述的,当可刺穿构件1170被刺穿时,分离模块1110可以从第一构型(图1)被移动至第二构型(图2)。当第一容积1163如图2中所示地与第一室1114流体连通时(即,当分离模块处于第二构型时),物质r1能够从第一容积1163传送到第一室1114中。物质r1可以通过任何适合的机构——例如,通过重力、毛细力或通过作用于第一容积1163的一些致动机构(图1和图2中未示出)——从第一容积1163传送到第一室1114中。
可刺穿构件1170可以由物质r1基本上不可渗透的和/或与物质r1基本上化学惰性的材料构造。以此方式,物质r1可以被储存在第一容积1163内延长时间段,而不损害任何期望的应用——比如本文中描述的任何实施方式——使用第二壳体1160的能力。此外,在一些实施方式中,可刺穿构件1170可以由具有某种温度特性的材料构造,使得可刺穿构件1170的期望特性和整体性在一定温度范围内得到维持。例如,在一些实施方式中,可以期望将容纳物质r1的第二壳体1160储存于制冷条件,或者可以期望通过热层压可刺穿构件1170来制造第二壳体1160。在这种实施方式中,可刺穿构件1170可以选择为使得制冷条件和/或热层压条件对于预期应用而言基本上不会使可刺穿构件的期望特性和整体性降级。在一些实施方式中,可刺穿构件1170可以由诸如任何形式的聚丙烯之类的聚合物膜构造。在一些实施方式中,可刺穿构件1170可以由双轴向聚丙烯(bop)构造。
尽管图1至图2将第二壳体1160的至少一部分示出为设置在第一壳体1110内,但在其它实施方式中,第一壳体1110和第二壳体1160可以通过使第一壳体1110的至少一部分设置在第二壳体1160内而联接在一起,或通过使第一壳体1110和第二壳体1160经由接口或配件而联接在一起而不设置在彼此内。第二壳体1160可以通过任何适合的机构联接至第一壳体1110,例如,通过粘结结合;焊接接头;卡扣配合(例如,其中设置在第一壳体上的匹配的凸起接纳在由第二壳体限定的对应的开口内或由该开口保持的布置,或者其中设置在第二壳体上的匹配的凸起接纳在由第一壳体限定的对应的开口内或由该开口保持的布置);过盈配合,其中两个部件在被推至一起后通过摩擦而紧固(例如,诸如luer-
反应模块1200限定反应室1262和第二容积1213。第二容积1213容纳物质r2。物质r2可以是诸如矿物油、洗涤缓冲液、试剂之类的任何生物物质或化学物质,其参与或以其它方式支持反应室1262内的和/或药筒1001的任何其它部分内的反应。反应模块1200联接至分离模块1100,使得反应室1262和第二容积1213能够各自被安置成与分离模块1100的第二室1190流体连通。反应模块1200可以通过任何适合的机构联接至分离模块1100,例如通过粘结结合;焊接接头;卡扣配合(例如,其中设置在第一壳体上的匹配的凸起接纳在由第二壳体限定的对应的开口内或由该开口保持的布置,或者其中设置在第二壳体上的匹配的凸起接纳在由第一壳体限定的对应的开口内或由该开口保持的布置);过盈配合,其中两个部件在被推至一起后通过摩擦而紧固(例如,诸如luer-
这种布置允许物质从反应室1262和/或第二容积1213向第二室1190传送,或反之亦然。例如,在使用中,样品、试剂和/或其它支持材料——例如样品s、物质r1或物质r2中的一种或多种——可以与期望的反应结合而传送到或传送出相联系的反应室1262。第二室1190、反应室1262和/或第二容积1213之间的流体传送可以通过重力、毛细力、液压压力等来实现。在一些实施方式中,液压压力可通过活塞泵、挡板泵或任何其它适合的传送机构来施加。在一些实施方式中,这种流体传送机构可以位于药筒1001的外部或者位于药筒1001的内部(例如,设置成至少部分地处于分离模块1100内和/或反应模块1200内)。
在一些实施方式中,物质r1和样品s或其部分可以与反转录过程结合而从第一容积1263和第一室1114通过第二室1190传送至反应室1262,从而通过使用反转录酶由核糖核酸(rna)模板产生单链互补脱氧核糖核酸(cdna)。在反转录过程完成之后,物质r2可以从第二容积1213通过第二室1190传送至反应室1262,以对新合成的cdna或样品s中存在的dna执行pcr过程。在这种实施方式中,物质r2可以包括一种或更多种包含taq聚合酶的pcr试剂。在一些实施方式中,物质r1和/或物质r2可以包括dna结合染料(例如,小沟结合物(mgb),联接至dna探针的5’-端的荧光团和mgb,其中,dna探针与靶序列特异性杂交),于是,可以通过使用本文中描述的任何仪器和/或方法检测来自反应室1262中荧光报道分子的荧光而实时监测pcr过程的进展。
在一些实施方式中,药筒1001(图1和图2)用来分离和扩增核酸样品。例如,分离可以在第一室1114中或第二室1190中发生。在一个实施方式中,物质r1包含用于核酸分离的试剂。dna、rna及其组合可通过本文中提供的药筒来分离。例如,在一个实施方式中,物质r1包含由试剂衍生的磁珠以分离dna或者rna。
单个核酸和总核酸二者均可在本文中提供的药筒中分离。例如,在一个实施方式中,物质r1包含由多聚腺苷酸(polya)序列衍生的珠,该珠设计为分离存在于样品中的信使rna总库。在另一实施方式中,物质r1包含由特定核酸序列衍生的珠,该珠设计为分离样品中的仅一部分的核酸。
一旦核酸被分离出,其就可以被扩增。在一个实施方式中,通过pcr来扩增。出于本发明的目的,参照对核酸样品的“pcr”包括反转录-pcr(rt-pcr)。具体地,当核酸样品为一个或多个靶rna或rna群体(例如,总mrna)时,将对靶rna进行rt-pcr。本文中提供的pcr主要混合物因而可以包含用于反转录的试剂。反转录步骤可以在与pcr相同的室或模块中或在不同的室或模块中发生。在一个实施方式中,反转录和pcr通过提供rt-pcr主要混合物而在同一室中进行。本领域中普通技术人员基于最初分离的核酸样品将容易了解需要rt-pcr还是pcr。本文中提供的任何药筒能够用来分离dna和/或rna,并且用来执行rt-pcr和/或pcr。
例如,在一个实施方式中,如果rna首先被分离出,则例如在第二室1190或反应室1262中对经分离的样品进行反转录反应。如果dna被分离出,则其可以例如在反应室1262中通过pcr来扩增。类似地,如果rna首先从样品s中被分离出,则其会例如在反应室1262中经受反转录反应,并且该反应的产物例如在反应室1262中用于下游pcr反应。在一些实施方式中,多靶核酸在pcr中被扩增,并且pcr反应被实时监测。在一个实施方式中,通过采用对于每个靶特异性的单个dna杂交探针监测多个靶的扩增,其中,每个探针包括在不同波长下发光或者可以在唯一波长下被激发的荧光团。在一个实施方式中,dna杂交探针在第二容积1213中作为物质r2(或其一部分)提供。
在一些实施方式中,pcr通过单链双标记检测探针来监测,即,5'端具有荧光团标记并且3'端具有猝灭剂。在另外的实施方式中,探针为水解探针,其依赖于taq聚合酶的5'→3'外切核酸酶活性以在与互补链杂交后切割双标记探针,例如
pcr反应的实时监测不限于图1与图2中示出的药筒。反而,本文中提供的任何药筒均可以采用实时pcr,例如借助以上所描述的dna杂交探针进行。
在一些实施方式中,药筒1001可以通过本文中描述的任何仪器和/或方法来操纵,以促进pcr过程在反应室1262内发生。在这种实施方式中,反应模块1200可以联接至热传递设备和/或安置成与热传递设备相接触,以允许反应室1262的内含物与pcr过程相结合地进行热循环。在这种实施方式中,反应模块1200可以进一步操作性地联接至光学设备,以允许实时监测pcr过程。在另一实施方式中,反应模块1200和/或分离模块1100可以操作性地联接至诸如光能、超声能、磁能、液力能之类的其它能源,以促进在其内发生的反应和/或分离过程。
尽管图1至图2示出反应室1262和第二容积1213各自与第二室1190流体连通,但在其它实施方式中,反应室1262、第二容积1213和/或分离模块的第二室1190之间的流体连通可以是选择性的。换言之,在一些实施方式中,反应模块1200和/或分离模块1100可以包括诸如阀、或可刺穿膜之类的可以选择性地将第二室1190安置成与第二容积1213和/或反应室1262流体连通的机构。尽管分离模块1100示出为限定一个第一容积1163,但在一些实施方式中,分离模块1100可以限定任何数目的容积和/或可以容纳任何数目的不同物质。类似地,尽管反应模块1200示出为限定一个第二容积1213,但在一些实施方式中,反应模块1200可以限定任何数目的容积并且可以容纳任何数目的不同物质。
图3为根据实施方式的药筒2001的示意性图示,该药筒2001包括第一模块2110、第二模块2160和第三模块2200。第一模块2110限定第一室2114和第二室2190。第一室2114和/或第二室2190可以容纳含有靶核酸的任何生物样品,例如尿、血、含有组织样品等的其它材料。尽管第一室2114示出为与第二室2190流体连通,但是在其它实施方式中第一室2114可以选择性地安置成与第二室2190流体连通。换言之,在一些实施方式中,第一模块2110可以包括诸如阀(图3中未示出)之类的可以选择性地将第一室2114安置成与第二室2190流体连通的任何适合的机构。此外,在其它实施方式中,第一模块2110可以具有任何适合的流量控制和/或传送机构(图3中未示出),以促进物质在第一室2114与第二室2190之间的传送和/或控制物质在第一室2114与第二室2190之间的传送,所述机构包括例如阀、毛细管流动控制装置、泵等。
第二模块2160限定第一容积2163,该第一容积2163可以完全地或部分地容纳任何生物或化学物质。该物质可以为例如矿物油、洗涤缓冲液、试剂等,其可以参与和/或以其它方式支持第一室2114内的和/或药筒2001的任何其它部分内的反应。在一个实施方式中,第一室2114中的反应为分离反应,例如核酸或肽的分离。第二模块2160可以以本文中描述的任何适合的方式联接至第一模块2110。在一些实施方式中,例如,第一模块2110和第二模块2160可以分开地构造并且联接在一起,使得第一模块2110和第二模块2160被模块化地布置。在这种模块化的布置中,第一模块2110和第二模块2160的各种不同的构型可以彼此一起使用。第一模块2110和/或第二模块2160的不同构型可以包括第一模块2110和/或第二模块2160内的不同试剂和/或不同结构。如图3中所示,第二模块2160的一部分设置在第一模块2110的第一室2114内,使得第一容积2163可以安置成与第一室2114流体连通。在其它实施方式中,第一容积2163可以选择性地安置成与第一室2114流体连通。在一些实施方式中,例如,第一模块2110和/或第二模块2160可以包括在第二模块2160联接至第一模块2110时可以将第一容积2163选择性地安置成与第一室2114流体连通的任何适合的机构,比如阀和/或本文中描述的任何适合的流体控制机构和/或流体传送机构。在一些实施方式中,可以利用如本文中描述的任何适合的流体传送机构在第一容积2163与第一室2114之间传送物质和/或样品。例如,在使用中,样品、经分离的样品(例如,经分离的dna、经分离的rna、经分离的肽、经分离的蛋白质)、试剂(例如,分离试剂)、和/或其它支持物质可以结合所需反应而被传送到和/或传送出第一室2114。在又一其它实施方式中,第一容积2163可以例如通过阀、或如本文中描述的可刺穿构件、选择性传送机构(图3中未示出)而与第一室2114流体隔离。
第三模块2200限定反应室2262和第二容积2213。反应室2262和/或第二容积2213可以完全地或部分地容纳一种或更多种生物或化学物质,比如矿物油、洗涤缓冲液、一种或多种pcr试剂、试剂等,其参与或以其它方式支持反应室2262内和/或药筒2001的其它部分内的反应。第三模块2200可以以如本文中描述的任何适合的方式联接至第一模块2110。在一些实施方式中,第一模块2110为分离模块2110,例如用于从生物样品中分离一个或多个靶核酸。在一些实施方式中,第一模块2110用于rna分离和第一链cdna合成。在该实施方式中,第一容积2163容纳分离试剂和用于反转录(rt)反应的试剂。在一些实施方式中,例如,第一模块2110和第三模块2200可以分开地构造并且联接在一起,使得第一模块2110和第三模块2200模块化地布置。在这种模块化的布置中,第一模块2110和第三模块2200的不同构型可以彼此一起使用。第一模块2110和/或第三模块2200的不同构型可以包括第一模块2110和/或第三模块2200内的不同试剂和/或不同结构。如图3中所示,第三模块2200的一部分被设置在第一模块2110的第二室2190内,使得反应室2262和第二容积2213各自与第二室2190流体连通。在其它实施方式中,反应室2262和/或第二容积2213可以选择性地安置成与第二室2190流体连通。换言之,在一些实施方式中,第一模块2110和/或第三模块2200可以包括可以将反应室2262和/或第二容积2213安置成与第二室2190选择性地流体连通的任何适合的机构,比如阀和/或本文中描述的任何适合的流体控制机构和/或传送机构。在一些实施方式中,可以利用如本文中描述的任何适合的流体传送机构在第二室2190、反应室2262和/或第二容积2213之间传送物质和/或样品。例如,在使用中,样品、试剂、和/或其它支持材料可以与所需反应相结合地传送到或传送出反应室2262。在又一其它实施方式中,反应室2262和/或第二容积2213可以例如通过如本文中描述的可刺穿构件或选择性传送机构(图中未示出)而与第二室2190流体隔离。
在一些实施方式中,药筒2001可以用来执行样品制备、对样品执行核酸分离和/或聚合酶链反应(pcr)。在这种实施方式中,靶核酸可以在第一模块2110内从样品中分离出。经分离的核酸可以是rna、dna或其组合。如以上所描述的,如果rna被分离出,则在pcr之前,在药筒2001中、例如在第一室2114中或第二室2190中进行反转录反应。之后,经分离的核酸(或新合成的cdna(如果rna被分离出))可以在第三模块2200中被扩增(例如,使用pcr),如本文中描述的,例如借助包含5'端的荧光团和mgb以及3'端的非荧光猝灭剂的dna寡核苷酸探针的实时pcr。药筒2001的模块化布置允许任何数目的不同第三模块2200与第一模块2110一起使用,所述第三模块2200各自容纳例如不同的试剂和/或各自构造成扩增不同类型的样品,或反之亦然。在一些实施方式中,药筒2001可以由本文中描述的任何仪器和/或方法来操纵,以促进反应室2262内pcr过程的发生。在这种实施方式中,第三模块2200能够被联接至热传递设备并且/或者安置成与热传递设备接触,以允许反应室2262的内含物与pcr过程相结合地热循环。在这种实施方式中,第三模块2200可以进一步地操作地联接至光学设备以监测pcr过程。在其它实施方式中,第三模块2200和/或第一模块2110可以操作性地联接至其它能源,诸如光能源、超声能源、磁能源、液压能源等,以促进本文中发生的反应过程和/或分离过程。
尽管图3将集成的药筒2001示出为限定一个第一容积2163和一个第二容积2213,但在一些实施方式中,该整合药筒2001可以限定任何数目的第一容积2163和/或第二容积2213以容纳任何数目的不同物质和/或执行额外的功能。例如,第一容积2163和/或第二容积2213可以容纳分开的洗涤缓冲液、洗脱缓冲液、用于反转录反应的试剂、pcr试剂和/或裂解缓冲液。
如上所述,在一些实施方式中,本文中描述的任何药筒可以包括一个或多个传送机构,该传送机构构造成在限定于药筒内的各个室之间传送样品。例如,图4为根据实施方式的药筒3001的示意性图示,该药筒3001包括第一模块3110、第二模块3160和第三模块3200。第一模块3110限定第一室3114和第二室3190。在一些实施方式中,第一模块3110充当分离模块,例如用于从生物样品中分离出一种或多种靶核酸、核酸群体(例如,总rna、总dna、mrna)、或者靶肽或蛋白质。第一室3114和/或第二室3190能够容纳生物样品,例如含有靶核酸的生物样品,比如尿、血、含有组织样品的其它材料等。第一室3114和第二室3190之间设置有第一传送机构3140。
在一些实施方式中,第一传送机构3140可以是选择性传送机构,以在第一室3114和第二室3190之间选择性地传送样品和/或物质。在这种实施方式中,例如,第一传送机构3140可以在第一室3114与第二室3190之间传送具有特定特性的样品和/或物质,同时限制和/或防止在第一室3114和/或第二室3190之间传送具有不同特性的样品和/或物质。在一些实施方式中,第一传送机构3140可以是使用磁性部件的设备,以基于样品和/或物质的磁性传送样品和/或物质。在其它实施方式中,第一传送机构3140可以基于样品和/或物质的表面电荷例如通过使用电泳法传送样品和/或物质。在又一实施方式中,第一传送机构3140可以基于样品和/或物质中的分子或离子的尺寸传送样品和/或物质。在这种实施方式中,第一传送机构3140可以包括用于选择性地传送样品和/或物质的反向渗透机构。换言之,在一些实施方式中,第一传送机构3140能够依靠和/或产生包括例如磁力、静电力、压力等的力,以作用于靶向样品和/或物质和/或该靶向样品和/或物质内的分子和/或离子。第一传送机构3140也可以包括任何适合的结构和/或可以组合多种选择性的传送机构(例如,以传送额外的物理运动和/或以提供额外的选择性)。在一些实施方式中,第一传送机构3140可以在第一室3114与第二室3190之间选择性地传送某些分子或离子的同时维持第一室3114与第二室3190之间大致流体隔离。在一些实施方式中,第一传送机构3140可以是如在于2006年10月17日提交的名称为“cassetteforsamplepreparation”的美国专利no.7,727,473中公开的磁阀,该专利的全部内容通过参引合并入本文中。在又一实施方式中,第一传送构件3140可以在第一室3114与第二室3190之间非选择性地传送物质和/或样品。
第二模块3160限定第一容积3163,该第一容积3163能够完全地或部分地容纳诸如矿物油、核酸分离试剂、反转录试剂、洗脱缓冲液、裂解缓冲液、洗涤缓冲液、试剂之类的的任何生物物质或化学物质,其可以参与和/或以其它方式支持第一室3114内的和/或药筒3001的任何其它部分内的反应。第二模块3160可以以如本文中描述的任何适合的方式连接至第一模块3110。在一些实施方式中,例如,第一模块3110和第二模块3160可以分开地构造并且联接在一起,使得第一模块3110和第二模块3160模块化地布置。在这种模块化的布置中,第一模块3110与第二模块3160的不同构型可以彼此一起使用。第一模块3110和/或第二模块3160的不同构型可以包括在模块内的不同试剂和/或不同结构。如图4中所示,第二模块3160的一部分设置在第一模块3110的第一室3114内,使得第一容积3163与第一室3114流体连通。在其它实施方式中,第一室3163可以选择性地安置成与第一室3114流体连通。换言之,在一些实施方式中,第一模块3110和/或第二模块3160可以包括可以将第一容积3163选择性地安置成与第一室3114流体连通的任何适合的机构,比如阀和/或本文中描述的任何适合的流体控制机构和/或传送机构。在一些实施方式中,可以使用本文中描述的任何适合的流体传送机构在第一容积3163与第一室3114之间传送物质和/或样品。例如,在使用中,样品、试剂和/或其它支持材料可以结合所需反应而传送到或传送出第一室3114。在又一其它实施方式中,第一容积3163可以例如通过本文中描述的可刺穿构件或选择性的传送机构(未示出)与第一室3114流体隔离。
第三模块3200限定反应室3262。反应室3262可以完全地或部分地容纳诸如矿物油、反转录试剂、洗脱缓冲液、裂解缓冲液、pcr试剂(例如,taq聚合酶、引物、用于监测反应的dna寡核苷酸探针、mg2+)、洗涤缓冲液、试剂等之类的任何生物物质或化学物质,其可以参与和/或以其它方式支持反应室3262内的和/或药筒3001的任何其它部分内的反应。第三模块3200可以以如本文中描述的任何适合的方式连接至第一模块3110。在一些实施方式中,例如,第一模块3110和第三模块3200可以分开地构造并且联接在一起,使得第一模块3110和第三模块3200模块化地布置。在这种模块化的布置中,第一模块3110与第三模块3200的不同构型可以彼此一起使用。第一模块3110和/或第三模块3200的不同构型可以包括在模块内的不同试剂和/或不同结构。如图4中所示,第三模块3200的一部分设置在第一模块3110的第二室3190内,使得反应室3262可以受第二传送机构3240的控制而各自与第二室3190流体连通。
第二传送机构3240可以将物质和/或试剂从第二室3190传送至反应室3262,或者反之亦然。在一些实施方式中,例如,第二传送机构可以在第二室3190与反应室3262之间传送预定容积的物质和/或试剂。类似陈述地,在一些实施方式中,第二传送机构3240可以在第二室3190与反应室3262之间以预定的容积流率传送物质和/或试剂。在一些实施方式中,例如,第二传送机构3240可以是构造成对第二室3190和/或反应室3262施加正压力或真空的泵。在这种实施方式中,第二传送机构3240可以是使用本文中描述的任何仪器和/或方法由柱塞致动的泵。在一些实施方式中,第二传送机构3240可以具有如在本文中描述的可刺穿构件,使得第二传送机构3240能够刺穿、破坏、切断、和/或破裂可刺穿构件以将容纳在反应室3262中的物质和/或样品传送到第二室3190中,或者反之亦然。在其它实施方式中,例如,第二传送机构3240可以是毛细管流动控制装置。在又一其它实施方式中,第二传送机构3240可以是如本文中描述的任何其它选择性的或非选择性的传送机构。
在一些实施方式中,药筒3001可以用来执行样品制备、核酸分离、反转录(如果rna首先被分离)、和/或对样品进行聚合酶链反应(pcr)。在这种实施方式中,靶核酸可以在第一模块3110内从样品中分离出。之后,经分离的核酸可以在第三模块3200中被扩增(例如,使用pcr),如以下进一步描述的。如本文中描述的,对多重靶的pcr可以借助本发明的例如药筒3001的药筒进行实时监测。在一个实施方式中,借助由lukhtanov等(nucleicacidsresearch35,p.e30,2007)公开的dna寡核苷酸探针来执行多重靶的扩增。药筒3001的模块化布置允许任何数目的不同的第三模块3200与第一模块3110一起使用,所述第三模块3200各自容纳例如不同的试剂和/或各自构造成扩增不同类型的样品,并且反之亦然。在一些实施方式中,药筒3001可以通过本文中描述的任何仪器和/或方法进行操作,以促进pcr过程在反应室3262内的发生。在这种实施方式中,第三模块3200可以联接至热传递设备和/或安置成与热传递设备接触,以允许反应室3262中的内含物与pcr过程相结合地热循环。在这种实施方式中,第三模块3200可以进一步操作性地联接至光学设备以监测pcr过程。在其它实施方式中,第三模块3200和/或第一模块3110可以操作性地联接至诸如光能、超声能、磁能、液压能之类的其它能源,以促进发生在其内的反应和/或分离过程。
尽管在一个实施方式中,联系图4示出及描述的药筒3001包括第一模块、第二模块和第三模块,但在其它实施方式中,药筒可以包括联接在一起的两个模块。例如,图5为根据实施方式的药筒4001的一部分的示意性图示,该药筒4001包括第一模块4200和第二模块4160。药筒4001的一部分可以联接至分离模块4110,如图5中所示。第一模块4200包括反应小瓶4260、基底4220和第一传送机构4140。反应小瓶4260限定反应室4262,反应室4262可以完全地或部分地容纳含有靶核酸的任何生物或化学样品和/或物质——比如尿、血、含有组织样品等的其它材料——和/或矿物油、洗涤缓冲液、裂解缓冲液、反转录试剂、pcr试剂等,其参与或以其它方式支持反应室4262内和/或药筒4001的任何其它部分内的反应的任何生物或化学样品和/或物质。
反应小瓶4260可以是任何适合的容器,用于容纳经分离的样品或以允许与样品有关的反应发生的其它方式的样品,例如核酸样品。在一些实施方式中,反应小瓶4260可以具有薄壁,该薄壁构造成在接纳在加热元件和/或块体(参见例如,以下描述的块体1710)和/或抵靠加热元件和/或块体设置。反应小瓶4260可以由具有与所需的反应和/或过程相容的某种特性的任何适合的材料来构造。在一些实施方式中,反应小瓶4260可以由基本上导热的材料构造,以允许在反应小瓶4260内的物质和/或样品进行热循环。在一些实施方式中,反应小瓶4260可以由基本上机械坚固的材料构造,使得在正压力或真空作用于反应小瓶4260内的容积上时反应小瓶4260的侧壁基本上保持其形状和/或尺寸。在一些实施方式中,反应小瓶4260可以由对反应小瓶4260内的反应基本上化学惰性的材料构造,使得形成反应小瓶4260的材料不会污染或以其他方式影响反应小瓶4260内的反应。
反应小瓶4260还可以是任何适合的容器,用于以允许监测这种反应(例如,检测样品内由反应所引起的或与反应相关的分析物)的方式容纳样品。在一些实施方式中,例如,反应小瓶4260可以是pcr反应小瓶,试管、微离心管等。此外,在一些实施方式中,反应小瓶4260的至少一部分可以是基本上透明的,以允许光学监测发生在其中的反应。
在一些实施方式中,反应小瓶4260可以与基底4220一体地构造。在其它实施方式中,反应小瓶4260可以通过本文中描述的任何适合的机构联接至基底4220。
基底4220限定第一流动路径4221和第二流动路径4222的至少一部分。第一流动路径4221构造成与反应室4262和分离模块的4110的分离室4114流体连通。第一传送机构4140构造成当该第一传送机构4140被致动时将样品s(或其部分)从分离室4114传送至反应室4262(如由箭头aa所示)。基底4220可以使用任何适合的结构、材料和/或制造过程限定第一流动路径4221和第二流动路径4222的一部分。在一些实施方式中,基底4220可以为单层。在其它实施方式中,基底4220可以由组合并联接在一起的分开的多层材料构造以限定结构和流动路径。在一些实施方式中,基底4220可以使用包括例如化学蚀刻、机械和/或离子研磨、压花、层压和/或硅键合的工艺进行构造。在一些实施方式中,基底4220的至少一部分可以在其上构造有加热元件、或设置在加热元件内和/或接触与加热元件,使得在使用中基底的限定第一流动路径和/或第二流动路径的部分可以被加热。例如,在一些实施方式中,基底4220可以设置在本文中公开的任何仪器内部,并且可以加热第一流动路径4221和第二流动路径4222,使得容纳在其内的物质(例如,在分离室4114与反应室4262之间传送样品的部分)能够被加热至和/或维持在近似大于50℃的温度下。如在本文中更详细地描述的,这种布置促进与pcr过程相关联的物质和/或试剂的“热启动”传送。
第一传送机构4140至少部分地容纳在第一模块4200内,并且构造成促进样品s从分离室4114传送至反应室。在一些实施方式中,第一传送机构4140可以促进样品s传送的同时维持第一流动路径4221与第一模块4200外部的区域之间的流体隔离。例如,在一些实施方式中,第一传送机构4140可以为产生力和/或促进样品s传送而不会从第一模块4200的外部区域添加物质(例如,不会添加压缩气体等)的任何机构。这种布置减少了潜在的污染、提高了过程自动化和/或以其它方式提高了样品s传送的速度和/或准确性。例如,样品s的传送可以被编程为在不同的时间步长进行,在每个时间步长传送不同数量的样品s。提高样品s传送的准确性还可以提高pcr分析的质量。第一传送机构可以是如本文中描述的任何适合的机构。例如,在一些实施方式中,第一传送机构4140可以是选择性传送机构以在分离室4114与反应室4262之间选择性地传送样品s。在一些实施方式中,第一传送机构4140可以施加磁力、静电力和/或压力以实现样品s的传送。
第一模块4200可以以本文中描述的任何适合的方式联接至分离模块4110以允许第一模块4200与分离模块4110之间的流体连通。在一些实施方式中,例如,第一模块4200和分离模块4110可以分开地构造并且联接在一起,使得第一模块4200和分离模块4110模块化地布置。在这种模块化的布置中,第一模块4200和分离模块4110的不同构型可以彼此一起使用。第一模块4200和/或分离模块4110的不同构型可以包括模块内的不同试剂和/或不同结构。
第二模块4160包括第二传送机构4240并且限定容积4163,该容积4163构造成容纳物质r1。本文中使用的物质r1和物质r2可以指的是一种或多种试剂。物质r1可以是任何的生物物质或化学物质,例如矿物油、洗涤缓冲液、荧光染料、裂解缓冲液、洗涤缓冲液、洗脱缓冲液、反转录试剂、pcr试剂(例如,一种或多种taq聚合酶、引物、dna杂交探针例如由lukhtanov等人(2007).nucleicacidsresearch35,第e30页描述的探针)、试剂等。尽管图5示出了包括一个容积4163的第二模块4160,但在其它实施方式中,第二模块4160可以包括多种物质(包括物质r1和/或不同物质)可以储存于其内的任意数目的容积4163和/或容器。第二模块4160构造成联接至第一模块4200,使得容积4163可以选择性地安置成经由第二流动路径4222与反应室4262流体连通。第二传送机构4240构造成当第二传送机构4240被致动时将物质r1的至少一部分从容积4163传送至反应室4262(如由箭头bb所示)。
第二传送机构4240可以将物质r1从第二容积4163传送至反应室4262,或者反之亦然。在一些实施方式中,例如,第二传送机构可以在第二容积4163与反应室4262之间传送预定容积的物质r1。在一些实施方式中,例如,第二传送机构可以在第二容积4163与反应室4262之间以预定的容积流率传送物质r1。在一些实施方式中,例如,第二传送机构4240可以为构造成对第二容积4163和/或反应室4262施加正压力或真空的泵。在这种实施方式中,第二传送机构4240可以为使用本文中描述的任何仪器和/或方法由柱塞致动的泵。在一些实施方式中,第二传送机构4240可以具有如本文中描述的可刺穿构件,使得当在使用中时,第二传送机构4240能够刺穿、破坏、切断、和/或破裂可刺穿构件并将容纳在反应室4262中的物质和/或样品传送到第二容积4163中,或者反之亦然。在一些其它实施方式中,例如,第二传送机构4240可以为毛细管流动控制装置。在另外的其它实施方式中,第二传送机构4240可以为本文中描述的任何其它传送机构。
在一些实施方式中,药筒4001可以用来执行样品制备、核酸分离和/或对样品或其经分离部分(例如,经分离的核酸样品)执行聚合酶链反应(pcrs)。在这种实施方式中,分离模块4110可以从容纳在分离模块4110内的样品中分离出靶核酸。之后,经分离的核酸可以在反应室4262中被扩增(例如,使用pcr),如以下将进一步描述的。替代性地或另外地,如果rna被分离出,则可以在反应室4262中进行反转录反应。在另一实施方式中,如果rna被分离出,则在反应室之一(例如反应室4262)中进行集成的反转录-pcr反应。药筒4001的模块化布置允许任何数目的不同的第二模块4160与第一模块4200一起使用,所述第二模块4160各自容纳例如不同的试剂和/或各自构造成扩增不同类型的样品或者分离不同类型的样品,且反之亦然。在一些实施方式中,药筒4001可以由本文中描述的任何仪器和/或方法来操纵,以存进在反应室4262内发生例如pcr过程之类的扩增过程。在这种实施方式中,反应小瓶4260可以联接至热传递设备和/或安置成与热传递设备接触以允许反应室4262的内含物与pcr过程相结合而进行热循环。在这种实施方式中,反应小瓶4260可以进一步操作性地联接至光学设备以监测pcr过程。在其它实施方式中,反应小瓶4260和/或分离模块4110可以操作性地联接至诸如光能、超声能、磁能、液压能等其它能源以促进在其内发生的反应和/或分离过程。
图6和图7分别为根据实施方式的药筒5001的一部分处于第一构型和第二构型的示意性图示。药筒5001的一部分包括第一模块5200和第二模块5100。第一模块5200包括反应小瓶5260、基底5220和第一传送机构5235。反应小瓶5260限定反应室5262,反应室5262可以以允许与样品s相关联的反应发生的方式容纳样品。反应小瓶5260可以具有任何适合的形状和/或尺寸,并且可以使用本文中描述的任何适合的材料构造。在一些实施方式中,例如,反应小瓶5260可以为pcr小瓶、试管等。
第一传送机构5235包括可移动地设置在壳体5230内的柱塞5240,使得壳体5230和柱塞5235限定第一容积5213。第一容积5213容纳第一物质r1。第一物质r1可以是例如试剂(例如,诸如taq聚合酶、引物之类的pcr试剂、诸如以上描述的dna杂交探针之类的dna杂交探针或者其组合)、反转录试剂、矿物油等。柱塞5240可以通过诸如本文中所述的任何仪器之类的任何适合的机构致动。
基底5220限定第一流动路径5221和第二流动路径5222的至少一部分。第一流动路径5221构造成与反应室5262、第一容积5213和分离模块5110的分离室5114(图6中以虚线的形式示出)流体连通。第二流动路径5222构造成与分离室5114流体连通。分离室5114可以为本文中所示出的和描述的类型的任何适合的分离室和/或分离模块。此外,分离室5114可以以本文中描述的任何适合的方式联接至第一模块5200。在一些实施方式中,分离室5114可以联接至第一模块5200并且如本文中描述地进行模块化地布置。分离室5114与第一模块5200之间的可移除联接可以是使用如本文中描述的任何适合的机构而流体密封的。
第二模块5100包括第二传送机构5150并限定第二容积5163,该第二容积5163构造成容纳第二物质r2。第二模块5100构造成联接至第一模块5200,使得第二容积5163可以选择性地安置成经由第二流动路径5222与分离室5114流体连通。第二模块5100可以包括构造成将第二容积5163选择性地安置成与分离室5114和/或第二流动路径5222流体连通的任何机构和/或设备。例如,在一些实施方式中,第二模块5100可以包括可刺穿构件,该可刺穿构件限定第二容积5163的边界的一部分并且将第二容积5163与分离室5114和/或第二流动路径5222流体隔离。在其它实施方式中,第二模块5100可以包括构造成将第二容积5163选择性地安置成与分离室5114和/或第二流动路径5222流体连通的阀。
第二传送机构5150构造成当该第二传送机构5150被致动时将第二物质r2的至少一部分从容积5163传送到分离室5114。第二传送机构5150可以为本文中描述的任何适合的传送机构。例如,在一些实施方式中,第二传送机构5150可以施加磁力、静电力和/或压力以实现物质r2从第二容积5163传送至分离室5114。在一些实施方式中,例如,第二传送机构5250可以为使用本文中描述的任何仪器和/或方法由柱塞致动的泵。在一些其它实施方式中,例如,第二传送机构5250可以为毛细管流动控制装置。
药筒5001可以在至少第一构型(图6)与第二构型(图7)之间移动以促进涉及样品s的反应和/或测定,该样品s最初设置在分离室5114中。当药筒5001处于第一构型时,柱塞5240处于壳体5230内的第一位置,使得柱塞5240的部分5246设置在第一流动路径5221内。因此,当药筒5001处于第一构型时,第一容积5213与反应室5262流体隔离。以此方式,当药筒5001处于第一构型时,第一物质r1维持在第一容积5213内并且被阻止运送到反应室5262中(例如,通过泄漏、重力进给、毛细作用等)。此外,当药筒5001处于第一构型时,第二容积5163与第二流动路径5222和分离室5114流体隔离。以此方式,当药筒5001处于第一构型时,第二物质r2维持在第二室5163内并且被阻止被运送到分离室5114中(例如,通过泄漏、重力进给、毛细作用等)。
通过将第二容积5163安置成经由第二流动路径5222与分离室5114流体连通、致动第二传送机构5150以将第二物质r2的至少一部分运送到分离室5114中(如由图7中箭头cc所示)、并且致动第一传送机构5235而使药筒5001移动至第二构型(图7)。更具体地,第二容积5163可以通过任何适合的机构——例如,将可刺穿构件刺穿,对阀等进行致动——被安置成经由第一流动路径5222与分离室5114流体连通。在一些实施方式中,第二容积5163可以通过致动第二传送构件5150而被安置成与分离室5114流体连通。以此方式,第二容积5163能够被安置成与分离室5114流体连通,并且第二物质r2的一部分可以在一个操作中和/或响应于单独的致动事件而被运送到分离室5114中。
第一传送机构5235通过使柱塞5240在壳体5230内移动而被致动,如由图7中箭头dd所示。类似陈述地,当第一传送机构5235被致动时,柱塞5240在壳体5230内从第一位置(如图6所示)移动至第二位置(如图7中所示)。因此,当第一传动机构5235被致动时,柱塞5240的一部分5246至少部分地从第一流动路径5221移除,由此将第一容积5213安置成经由第一流动路径5221而与反应室5262流体连通。以此方式,第一物质r1的一部分可以从第一容积5213运送到反应室5262中,如由图7中由箭头ee所示。
此外,当柱塞5240从第一位置移动至第二位置时,反应室5262内产生真空。药筒5001内的这种压差(即,在反应室5262与分离室5114之间)导致分离室5114的内含物的至少一部分(即,样品s和/或第二物质r2)经由第一流动路径5221运送到反应室5262中,如由图7中箭头ff和gg所示。以此方式,可以通过致动第一传送机构5235和/或第二传送机构5150而在分离室5114与反应室5262之间添加、混合和/或运送物质和/或样品。通过在分离室5114内执行样品s与物质r2的混合来取代将样品s与物质r2分开地运送到反应室5262中,可以消除额外的传送步骤。此外,该布置和/或方法可以改进样品s与物质r2的混合,由此提高反应室5262中反应的准确性和效率。
尽管描述为以特定的顺序发生,但在其它实施方式中,与将药筒5001从第一构型移动至第二构型相关联的操作可以以任何顺序发生,此外,在其它实施方式中,药筒5001可以被安置成涉及任何所需操作组合的任何数目的不同构型。
在一些实施方式中,药筒5001可以用于对样品s(该样品可以例如是一种或多种经分离的靶核酸)的至少一部分执行聚合酶链反应(pcr)。在这种实施方式中,经分离的核酸可以在反应室5262中被扩增(例如,使用pcr),如本文中描述的。在一些实施方式中,药筒5001可以通过本文中描述的任何的仪器和/或方法来操纵以促进反应室5262内pcr过程的发生。在这种实施方式中,反应小瓶5260可以联接至热传递设备和/或安置成与热传递设备接触以允许反应室5262的内含物与pcr过程相结合地进行热循环。在这种实施方式中,反应小瓶5260可以进一步操作性地联接至光学设备以允许实时监测pcr过程。在其它实施方式中,反应小瓶5260和/或第二模块5100可以操作性地联接至诸如光能、超声能、磁能、液压能之类的其它能源,以促进发生在其内的反应和/或分离过程。
在一些实施方式中,第一物质r1可以包括矿物油、蜡、等,使得在第一物质r1被传送到反应室5262中之后,第一物质r1可以在反应室5262中的流体混合物(即,样品s和第二物质r1)的表面上形成层。第一物质r1的表面层可以在反应过程期间(例如,在热循环期间)减少反应室5262中流体混合物的蒸发,由此提高在其内的反应的效率、准确性和/或控制。更具体地,通过减少反应室5262中的流体混合物的蒸发,反应混合物中的不同成分的相关浓度或比例可以被更准确地控制。另外,减少反应室5262中的流体混合物的蒸发还可以使反应小瓶5260的壁上的冷凝最小化,从而提高反应的光学监测或分析的准确性。
矿物油可以是具有适合特性的任何矿物油,该适合特性例如是期望的物理特性,包括例如密度和/或表面张力。矿物油等也可以选择成使得当被暴露于反应室5262内的条件下时其为化学上惰性的以及物理上稳定的。
图8至图24为根据实施方式的药筒6001的各种视图。在某些视图中,例如,图8和图9中,药筒6001的一部分示出为半透明的,使得药筒6001内的部件和/或特征可以更清晰地示出。药筒6001包括样品制备(或分离)模块6100和扩增(或pcr)模块6200,该样品制备模块6100和扩增模块6200联接在一起以形成集成的药筒6001。一个或多个药筒6001可以设置在本文中所公开的类型的任何适合的仪器(参见例如以下描述的仪器3002)内,该仪器构造成操纵、致动药筒6001和/或与药筒6001相互作用,以对容纳在药筒6001内的样品执行行核酸分离、转录和/或扩增。药筒6001通过在分离、转录和/或pcr扩增过程期间和分离、转录和/或pcr扩增过程之间限制样品处理的量而允许有效和准确地诊断测试样品。此外,分离模块6100和扩增(或pcr)模块6200的模块化布置允许任何数目的不同pcr模块6200与任何数目的不同分离模块6100一起使用,所述不同pcr模块6200各自容纳不同的试剂和/或构造成扩增不同类型的核酸,所述不同分离模块6100各自容纳不同的试剂和/或构造成分离不同类型的核酸,或者反之亦然。这种布置也允许分离模块6100与扩增模块6200分开储存。例如,在包括在分离模块6100内的试剂具有与包括在扩增模块6200内的试剂不同的储存要求(例如,过期日期、冻干要求、储存温度限制等)的情况下,则分开储存可以是有用的。
如图11中所示,分离模块6100包括第一(或分离)壳体6110和第二(或试剂)壳体6160,该第二壳体6160联接至第一壳体6110和/或至少部分地位于第一壳体6110内。第二壳体6160在图10和图22中出于清楚的目的而未示出。图11至图14示出第二壳体6160和容纳在其内的某些部件,并且图15至图18示出处于致动的各个不同阶段的第二壳体6160。第二壳体6160包括第一端部6161和第二端部6162,并且限定一系列的保持室6163a、6163b、6163c和6163d,所述一系列的保持室6163a、6163b、6163c和6163d容纳在分离过程中使用的试剂和/或其它物质。如在本文中更详细地描述的,保持室可以容纳蛋白酶(例如,蛋白酶k)、溶解大块材料的裂解溶液、使裂解室6114内残余的核酸样品带磁性电荷的结合溶液、以及结合至磁性带电核酸以协助核酸在分离模块6100和/或第一壳体6110内的运送的磁珠的溶液。
每个保持室6163a、6163b、6163c和6163d包括可移动地设置在其内的致动器6166(参见例如图14)。更具体地,如图18中所示,致动器6166a设置在保持室6163a内,致动器6166b设置在保持室6163b内,致动器6166c设置在保持室6163c内,并且致动器6166d设置在保持室6163d内。如图15中所示,可刺穿构件6170围绕第二壳体6160的第二端部6162设置,使得第二壳体6160的内部、可刺穿构件6170和致动器6166a、6166b、6166c和6166d共同包围和/或限定保持室6163a、6163b、6163c和6163d。类似陈述地,第二壳体6160的内部、可刺穿构件6170和致动器6166a、6166b、6166c和6166d共同限定流体隔离的室6163a、6163b、6163c和6163d,在所述室6163a、6163b、6163c和6163d中可以储存试剂和/或物质。可刺穿构件6170可以由诸如任何形式的聚丙烯之类的本文中描述的类型的任何适合的材料构造。在一些实施方式中,可刺穿构件6170可以由双轴向聚丙烯(bop)构造。
如图14中所示,致动器6166中的每个致动器均包括柱塞部6167、刺破部6168和一个或多个致动器开口6169。致动器开口6169构造成接纳致动器组件的一部分以便于致动器6166在如本文中所述的室(例如室6163a)中运动。特别地,致动器开口6169可以接纳诸如致动器组件3400的凸起3446a之类的凸起,如以下关于图37至图40所描述的。这种布置允许柱塞6166从第二壳体6160的第一端部6161被致动。在一些实施方式中,致动器6166可以包括保持机构(例如,凸起、卡环等),该保持机构构造成保持致动器组件(例如,致动器组件3400)的凸起以便于通过致动器组件使致动器6166往复运动。
致动器6166的柱塞部6167构造成接合第二壳体6160的限定出室(例如室6163a)的部分,在该室中,致动器6166设置成使得柱塞部6167和第二壳体6160的一部分形成基本上流体密封和/或气密封。由此,当致动器6166设置在室(例如,室6163a)内时,最小化了和/或消除了容纳在室内的物质的泄漏和/或运送。以此方式,柱塞部6167的端面限定室(例如室6163a)的边界的一部分。柱塞部6167还构造成使得当力施加在致动器6166(例如,通过以下示出和描述的致动器组件3400)上时,致动器6166将在室(例如,室6163a)内移动,以将容纳在室内的物质运送到裂解室6114中,如以下描述的。以此方式,致动器6166能够充当传送机构,以将物质从室(例如,室6163a)运送到分离模块6100的另一部分中。
致动器6166的刺破部6168构造成当致动器6166在室(例如,室6163a)内移动时刺穿、破坏、切断和/或破裂可刺穿构件6170的一部分,以将该室安置成与该室的外部区域流体连通。以此方式,各个室6163a、6163b、6163c和6163d可以选择性地安置成与分离模块6100(例如,裂解室6114)的另一部分流体连通,以允许当每个致动器6166a、6166b、6166c和6166d被致动时,容纳传送每个室6163a、6163b、6163c和6163d内的物质,如以下描述的。
第二壳体6160包括混合泵6181,该混合泵6181可以被致动(例如,通过仪器3002的致动器组件3400)以在容纳于分离模块6100的一部分(例如,裂解室6114)内的样品、试剂和/或其它物质内搅动、混合和/或产生紊流运动。如图12中所示,泵1618包括喷嘴6186,该喷嘴6186可以引导流动、增大流动的压力和/或增大分离模块6100的一部分内的紊流,以增强其内的混合。尽管混和泵6181示出为波纹管式泵,但在其它实施方式中,混合泵6181可以是用于将能量传送到裂解室6114内的溶液中的任何适合的机构。这种机构可以包括例如活塞泵、旋转构件等。在一些实施方式中,第二壳体6160可以包括用于混和分离室6114内的物质以促进容纳在其内的样品的细胞裂解和/或容纳在其内的核酸的分离的任何其它适合的机构。在一些实施方式中,第二壳体6160可以包括超声混合机构、热混合机构等。
如图11中所示,第二壳体6160设置在由第一壳体6110的第一端部部分6111限定的开口6115内。由此,当第二壳体6160设置在第一壳体6110内时,第二壳体6160的一部分限定裂解室6114的边界的至少一部分。更具体地,当第二壳体6160设置在第一壳体6110内时,可刺穿构件6170限定裂解室6114的边界的一部分。这种布置允许当可刺穿构件6170被刺破、刺穿、切断和/或破裂(参见例如图15)时容纳在第二壳体6160内的物质被运送到裂解室6114中。尽管第二壳体6160的至少一部分示出为设置在第一壳体6110内和/或裂解室6114内,但在其它实施方式中,第二壳体6160可以联接至第一壳体6110而第二壳体的任何部分不设置在第一壳体内。在另外的其它实施方式中,当第一壳体和第二壳体联接在一起时,第一壳体的一部分可以设置在第二壳体内。
如图12和图13所示,第二壳体6160包括围绕第二端部6162设置的密封件6172,使得当第二壳体6160被联接至第一壳体6110时,密封件6172和第一壳体6110的侧壁的一部分共同地形成第一壳体6110与第二壳体6160之间的基本上流体密封和/或气密封。换言之,密封件6172将裂解室6114与药筒6001的外部区域流体隔离。在一些实施方式中,密封件6172还可以将第二壳体6160与第一壳体6110声学地隔离。
第二壳体6160的第一端部6161包括凸起6171,所述凸起6171构造成接纳在由第一壳体6110限定的对应的开口6119(参见例如图10)内。由此,当第二壳体6160设置在第一壳体6110内时,凸起6171和开口6119共同地将第二壳体6160保持在第一壳体6110内。类似陈述地,凸起6171和开口6119共同地限制第二壳体6160相对于第一壳体6110的运动。
第一壳体6110和第二壳体6160的模块化布置允许任何数目的第二壳体6160(或试剂壳体)与第一壳体6110一起使用以形成分离模块6100,所述任何数目的第二壳体6160(或试剂壳体)各自容纳不同的试剂和/或物质以促进核酸分离。这种布置也允许第一壳体6110和第二壳体6160分开地储存。例如,在容纳于第二壳体6160内的试剂具有与容纳于第一壳体6110内的物质不同的储存需求(例如,过期日期、冻干要求、储存温度限制等)的情况下,分开地储存可以是有用的。
在使用中,容纳在第二壳体6160内的物质可以运送到第一壳体6110中以促进分离过程。图15至图18示出分离模块6100的一部分处于各个致动阶段的剖视图。例如,蛋白酶k可以储存于室6163d中,并且传送到如图15中所示的裂解室6114中。更具体地,致动器6166d在被任何适合的外力——例如由本文中描述的仪器3002的致动组件3400施加的力——致动时可以如由箭头hh所示地在室6163d中移动。当致动器6166d朝向裂解室6114移动时,刺破部6168d接触并刺穿可刺穿构件6170的一部分。在一些实施方式中,可刺穿构件6170可以包括穿孔部、应力集中提升部或其它结构不连续性以确保可刺穿构件6170容易地刺穿可刺穿构件6170的所需部分。以此方式,致动器6166d的运动将室6163d安置成与裂解室6114流体连通。致动器6166d的连续运动将室6163d的内含物(例如,蛋白酶k)传送到裂解室6114中。以此方式,致动器6166d充当阀和传送机构。
在另一个实施方式中,室6163d的内含物可以包括蛋白酶k(例如10mg/ml、15mg/ml或20mg/ml)、甘露醇、水和牛血清白蛋白。在进一步的实施方式中,珠经蛋白酶k包被或衍生。在另一个实施方式中,室6163d的内含物可包含蛋白酶k、甘露醇、水和明胶。在进一步的实施方式中,珠经蛋白酶k包被或衍生。在另一个实施方式中,室6163d的内含物是冻干为例如50μl的小球。
在另一个实施方式中,室6163d还提供阳性对照试剂。在一个实施方式中,阳性对照试剂为经内部对照核酸序列衍生的多个珠。在进一步的实施方式中,在甘露醇、牛血清白蛋白(bsa)和水的溶液中提供珠。在甚至进一步的实施方式中,珠和溶液提供为冻干小球,如50μl的小球。
尽管对室6163d进行了特别描述,但在其它实施方式中,包含蛋白酶k和/或阳性对照试剂的蛋白酶k溶液作为物质r1或r2存在。
以类似的方式,裂解溶液可以储存在室6163c中,并且如图16中所示传送到裂解室6114中。更具体地,致动器6166c在被任何适合的外力——例如由本文中描述的仪器3002的致动组件3400施加的力——致动时可以如由箭头ii所示地在室6163c内移动。当致动器6166c朝向裂解室6114移动时,刺破部6168c接触并刺穿可刺穿构件6170的一部分。以此方式,致动器6166c的运动将室6163c安置成与裂解室6114流体连通。致动器6166c的连续运动将室6163c的内含物(例如,裂解溶液)传送到裂解室6114中。以此方式,致动器6166c充当阀和传送机构。在一个实施方式中,储存于室6163c或另一室中的裂解溶液包含胍hcl(例如,3m、4m、5m、6m、7m或8m)、trishcl(例如,5mm、10mm、15mm、20mm、25mm或30mm)、triton-x-100(例如,1.5%、2%、2.5%、3%、3.5%、4%、4.5%或5%)、np-40(例如,1.5%、2%、2.5%、3%、3.5%、4%、4.5%或5%)、tween-20(例如,5%、10%、15%或20%)、cacl2(例如,1mm、1.5mm、2mm、2.5mm、3mm、3.5mm、4mm、4.5mm或5mm)、分子级水的过滤溶液。尽管对室6163c进行了特别描述,但在其它实施方式中,裂解溶液作为物质r1或r2存在。
以类似的方式,结合溶液可以储存在室6163b中,并且如图17中所示传送到裂解室6114中。更具体地,致动器6166b在被任何适合的外力——例如由本文中描述的仪器3002的致动组件3400施加的力——致动时可以如由箭头jj所示地在室6163b内移动。当致动器6166b朝向裂解室6114移动时,刺破部6168b接触并刺穿可刺穿构件6170的一部分。以此方式,致动器6166b的运动将室6163b安置成与裂解室6114流体连通。致动器6166b的连续运动将室6163b的内含物(例如,结合溶液)传送到裂解室6114中。以此方式,致动器6166b充当阀和传送机构。在一个实施方式中,结合溶液包含约50μl、约100μl、约125μl、约150μl、约175μl或约200μl容积的异丙醇,例如100%异丙醇、90%异丙醇、80%异丙醇、70%异丙醇。尽管对室6163b进行了特别描述,但在其它实施方式中,结合溶液作为物质r1或r2存在。
以类似的方式,一组磁珠可以储存在室6163a中,并且如图18中所示传送到裂解室6114中。更具体地,致动器6166a在被任何适合的外力——例如由本文中描述的仪器3002的致动组件3400施加的力——致动时可以如由箭头kk所示地在室6163a内移动。当致动器6166a朝向裂解室6114移动时,刺破部6168a接触并刺穿可刺穿构件6170的一部分。以此方式,致动器6166a的运动将室6163a安置成与裂解室6114流体连通。致动器6166a的连续运动将室6163a的内含物(例如,磁珠)传送到裂解室6114中。以此方式,致动器6166a充当阀和传送机构。珠在一个实施方式中是顺磁体。在一个实施方式中,珠是磁性硅珠,并且以1.0mg/ml或者1.5mg/ml、2.0mg/ml、2.5mg/ml、3.0mg/ml或3.5mg/ml的浓度提供。在进一步的实施方式中,磁性硅珠储存于异丙醇中,例如约50%异丙醇、约55%异丙醇、约60%异丙醇、约61%异丙醇、约62%异丙醇、约63%异丙醇、约64%异丙醇、约65%异丙醇、约66%异丙醇、约67%异丙醇、约68%异丙醇、约69%异丙醇、约70%异丙醇、约75%异丙醇、约80%异丙醇或约85%异丙醇。在一个实施方式中,珠提供为约50μl、约100μl、约125μl、约150μl、约175μl或约200μl的容积。尽管对室6163a进行了特别描述,但在其它实施方式中,珠作为物质r1或r2存在。
如图10中所示,第一壳体6110包括第一端部6111和第二端部6112,并且限定裂解室6114、两个洗涤室6121和6122、三个传送组件管腔6123、6124和6125、以及洗脱室6190。第一壳体6110也限定邻近分离室6114的开口6115。如图11中所示,并且如上所述,第二壳体6160设置在开口6115内,使得第二壳体6160的一部分(例如,可刺穿构件6170)限定分离室6114的边界的至少一部分。
第一端部6111还限定填充开口6116,通过该填充开口6116可以将裂解室6114安置成与分离模块6100的外部区域流体连通。如图8至图10中所示,分离模块6100包括盖6118,该盖6118围绕填充开口6116可移除地联接至填充开口6116。在使用中,含有靶核酸的样品——例如尿、血和/或含有组织样品的其它材料——可以经由填充开口6116被运送到裂解室6114中。样品可以通过任何适合的机构——包括例如经由填充开口6116将样品吸移或注射到第一室6114中之类——引入到裂解室6114中。在一些实施方式中,可以在填充开口6116内和/或填充盖6118内设置样品过滤器。过滤器可以是例如疏水的过滤器。
在样品被设置到裂解室6114中之后,可以将促进细胞裂解的试剂和/或物质添加至如以上所述的裂解室6114。此外,样品可以通过泵6181被搅动和/或混合以促进如以上所述的裂解过程。在一些实施方式中,裂解室6144的内含物可以被加热(例如,通过如以下参照仪器3002示出的和描述的第三加热模块3780)。
分离模块6100包括一系列传送组件(也称为传送机构),其在图15至图19中示出为传送组件6140a、传送组件6140b和传送组件6140c。如本文中描述的,传送组件构造成在裂解室6114、洗涤室6121、洗涤室6122和洗脱室6190之间传送物质(例如,样品的包括磁性带电颗粒的部分和附接至该磁性带电颗粒的经分离核酸)。更具体地,传送组件6140构造成在裂解室6114、洗涤室6121、洗涤室6122和洗脱室6190之间传送物质的同时维持裂解室6114、洗涤室6121、洗涤室6122和洗脱室6190与由第一壳体6110限定的其它室(例如,相邻的洗涤室)基本上流体隔离。
传送组件6140a设置在传送组件管腔6123内,使得传送组件6140a位于裂解室6114与洗涤室6121之间。因此,传送组件6140a构造成在裂解室6114与洗涤室6121之间传送物质。
传送组件6140b设置在传送组件管腔6124内,使得传送组件6140b位于洗涤室6121与洗涤室6122之间。因此,传送组件6140b构造成在洗涤室6121与洗涤室6122之间传送物质。
传送组件6140c设置在传送组件管腔6125内,使得传送组件6140c位于洗涤室6122与洗脱室6190之间。因此,传送组件6140c构造成在洗涤室6122与洗脱室6190之间传送物质。
传送组件中的每个传送组件参照图20和图21描述,其示出代表性的传送组件6140。传送组件6140包括壳体6141和可移动构件6146,该可移动构件6146可转动地设置在壳体6141内。壳体6141限定第一开口6142和第二开口6143。当传送组件6140设置在传送组件管腔(例如,传送组件管腔6123)内时,壳体6141对准成使得第一开口6142与第一室(例如,裂解室6114)对准和/或流体连通并且第二开口6143与第二室(例如,洗涤室6121)对准和/或流体连通。壳体6141可以通过任何适合的机构——例如通过机械紧固件或保持件、化学结合或粘结、过盈配合、焊接等——固定在传送组件管腔(例如,传送组件管腔6123)内。此外,壳体6141可以包括一个或多个密封件(图20和图21中未示出),使得第一室(例如,裂解室6114)与第二室(例如,洗涤室6121)维持为彼此流体隔离。类似陈述地,壳体6141和第一壳体6110可以共同形成基本上流体密封和/或气密封以消除和/或减少第一室(例如,裂解室6114)与第二室(例如,洗涤室6121)之间的物质的泄漏。
可移动构件6146包括限定凹部或空腔6148的外表面6147。可移动构件6146设置在壳体6141内,使得可移动构件6146可以如由图20和图21中箭头mm所示地转动。出于清楚的目的在图20中可移动构件6146的外表面6147示出为与壳体6141的内表面6145间隔开。外表面6147与壳体6141的内表面6145滑动地接触,使得外表面6147与内表面6145产生基本上流体密封和/或气密封。以此方式,消除了和/或减少了第一室(例如,裂解室6114)与第二室(例如,洗涤室6121)之间的物质经由壳体6141与可移动构件6146之间的界面而泄漏。
可移动构件6146进一步限定管腔6149,该管腔6149构造成接纳致动器510的一部分。致动器510可以是任何适合的致动器,比如以下参照图41至图46示出和描述的仪器3002的传送致动器组件3500的轴3510。如图20中所示,致动器510的形状可以对应于由可移动构件6146限定的管腔6149的形状,使得致动器510的转动引起可移动构件6146的转动。类似陈述地,致动器510可以匹配地设置在管腔6149内,使得致动器510与可移动构件6146之间的相对的转动运动被限制。在一些实施方式中,致动器510和管腔6149可以具有基本上相似的六边形和/或八边形形状。
在使用中,通过使可移动构件6146如由箭头mm所示地转动,可以使可移动构件6146在第一位置(未示出)与第二位置(图20)之间移动。当可移动构件6146处于第一位置时,凹部或空腔6148与第一室(例如,裂解室6114)对准或流体连通。当可移动构件6146处于第二位置时,凹部或空腔6148与第二室(例如,洗涤室6121)对准和/或流体连通。因此,通过在可移动构件6146处于第一位置时将一部分的物质捕获或设置在空腔6148内、转动可移动构件至第二位置并且从空腔6148中移除物质,可以将容纳在第一室(例如,裂解室6114)中的一种或多种物质传送至第二室(例如,洗涤室6121)。
在一些实施方式中,物质可以由磁力捕获、设置和/或维持在空腔6148中。例如,在一些实施方式中,致动器510可以包括磁性部分。在使用中,致动器510与所需的传送组件6140对准并且如图19中由箭头ll所示地移动到管腔6149中。由于致动器510的形状可以对应于管腔6149的形状,如上所述,可以在一些实施方式中执行对准操作以确保致动器510将配合在管腔6149内。当致动器510的磁性部分位于管腔6149内时,并且当可移动构件6146处于第一位置时,样品的磁性部分(例如,磁珠和附接至其的核酸)从第一室(例如,裂解室6114)移动到空腔6148中。致动器510随后被如由图20和图21中箭头mm所示地转动。当可移动构件6146处于第二位置时,可以从管腔6149中移除致动器510,由此,移除将样品的磁性部分保持在空腔6148内的磁力。因此,样品的一部分可以随后从空腔6148移动到第二室(例如,洗涤室6121)中。样品的一部分可以通过任何适合的机构——例如通过重力、流体运动等——从空腔6148移出并移动到第二室(例如,洗涤室6121)中。例如,如以下描述的,在一些实施方式中,混合机构6130a可以包括喷嘴(例如,喷嘴6131a)以压力喷射引导到空腔6148中和/或邻近空腔6148,从而将样品的一部分从空腔6148移出并移动到第二室(例如,洗涤室6121)中。
如本文中描述的传送机构6140的使用可以消除对于第一壳体6110内的分开的废物室的需要和/或对于运送废物的流动路径的需要。更确切地,如上所述,样品的靶部分在各个室之间移动(例如从洗涤室6121至洗涤室6122),而样品的其它部分维持在先前的室(例如,洗涤室6122)中。此外,由于传送机构6140维持两个室(例如洗涤室6121和洗涤室6122)之间的流体隔离,因而防止了废液与样品的靶部分一起进入该室(例如,洗涤室6122)。由此,这种布置还消除了在本文中描述的室之间和/或在由分离模块6100限定的流动路径内对于第一壳体6110内的过滤机构的需要。
如上文所述的传送机构6140的使用还允许在分离模块6100内运送样品的靶部分的同时将分离模块内的压力维持在环境压力或接近环境压力。类似陈述地,如本文中所述的传送机构6140传送样品的靶部分而不产生分离模块6100内的大幅压差。因此,这种布置可以减少样品从分离模块的泄漏。
分离模块6100包括两个混合机构6130a和6130b(也称为洗涤泵)。如本文中所描述的,混合机构6130a和6130b构造成分别产生洗涤室6121和洗涤室6122内的流体流动,以促进其内容纳的样品的一部分的洗涤和混合。类似陈述地,混合机构6130a和6130b构造成将能量分别传送到洗涤室6121和洗涤室6122中。
混合机构6130a包括致动器6132a和喷嘴6131a。混合机构6130a联接至第一壳体6110,使得喷嘴6131a的至少一部分设置在洗涤室6121内。特别地,混合机构6130a包括联接部6133a,该连接部6133a构造成联接至第一壳体6110的相对应的联接部6134a。尽管联接部6133a和6134a示出为限定螺纹联接,但在其它实施方式中,混合机构6130a可以通过任何适合的方法——例如通过机械紧固件或保持件、化学结合或粘合、过盈配合、焊接等——联接至第一壳体6110。
类似地,混合机构6130b包括致动器6132b和喷嘴6131b。混合机构6130b联接至第一壳体6110,使得喷嘴6131b的至少一部分设置在洗涤室6122内。特别地,混合机构6130b包括联接部6133b,该联接接部6133b构造成联接至第一壳体6110的相对应的联接部6134b。尽管联接部6133b和6134b示出为限定螺纹联接,但在其它实施方式中,混合机构6130b可以通过任何适合的方法——例如通过机械紧固件或保持件、化学结合或粘合、过盈配合、焊接等——联接至第一壳体6110。
致动器6132a和6132b各自分别包括顶表面6136a和6136b,所述顶表面6136a和6136b构造成通过仪器的致动组件——例如本文中描述的仪器3002的致动组件3600——接触和/或致动。在使用中,致动组件可以压下和/或移动每个致动器6132a和6132b的顶表面6136a和6136b,以在每个混合机构6130a和6130b内产生压力。该压力被传送到洗涤室6121和6122中以促进其内设置的样品之间和之内的洗涤、混合和/或其它相互作用。如上所述,在一些实施方式中,至少一个喷嘴(例如,喷嘴6131a)可以包括尖端部,其为成角度的、弯曲的和/或以其它方式设定形状的,以将由致动器(例如致动器6132a)产生的压力能和/或流动朝向洗涤室(例如洗涤室6121)内的特定区域引导。例如,在一些实施方式中,喷嘴6131a可以成形为将由致动器6132a产生的压力能和/或流动朝向传送机构6140的空腔6148引导。
尽管致动器6132a和6132b各自示出为波纹管式泵,但在其它实施方式中,混合机构6130a和/或混合机构6130b可以包括用于产生能量和/或将能量传送到洗涤室6121和6122中的任何适合的机构。这种机构可以包括,例如,活塞泵、旋转构件等。在一些实施方式中,混合机构可以包括超声能源、热能源等。
尽管混合机构6130a和6130b示出并描述为分别产生能量和/或将能量传送至洗涤室6121和6122,但在其它实施方式中,混合机构也可以限定与洗涤室流体隔离的容积,在该容积内可以储存物质(例如,洗涤缓冲溶剂)。由此,当混合机构被致动时,物质可以传送到洗涤室中。以此方式,在一些实施方式中,混合机构也可以充当传送机构。
扩增(或pcr)模块包括壳体6210(具有第一端部6211和第二端部6212)、pcr小瓶6260和传送管6250。pcr小瓶6260联接至壳体6210的第一端部6211并限定容积6262,在该容积6262内可以设置样品以促进于与该样品相关联的反应。pcr小瓶6260可以为用于以允许与样品相关联的反应发生的方式容纳该样品的任何适合的容器。pcr小瓶6260也可以为用于以允许监测这种反应(例如,检测样品内的由反应所引起的或与反应相关联的分析物)的方式容纳该样品的任何适合的容器。在一些实施方式中,pcr小瓶6260的至少一部分可以是基本上透明的,以允许其内所发生的反应的光学监测为光学系统(例如,本文中描述的仪器3002的光学组件3800)。
如图8、图9、图10和图22所示,扩增模块6200联接至分离模块6100的第一壳体6110的第二端部6112,使得传送管6250的至少一部分设置在分离模块6100的洗脱室6190内。以此方式,如本文中描述的,设置在洗脱室6190内的经分离的核酸、任何物质和/或任何pcr试剂可以具有传送管6250从洗脱室6190运送至pcr小瓶6260。
壳体6210限定一系列的试剂室6213a、6213b、6213c(参见例如图22)和泵空腔6241。试剂室6213a、6213b、6213c可以容纳与发生在pcr小瓶6260中的反应和/或过程相关联的任何适合的物质。试剂室6213a、6213b、6213c可以容纳例如洗脱流体、主要混合物、探针和/或引物以促进pcr过程。如图24中所示,壳体6210限定一系列通道6221a、6221b、6221c,所述一系列通道构造成将每个试剂室6213a、6213b、6213c安置成与分离模块6100的洗脱室6190流体连通。尽管图22中未示出,但在一些实施方式中,可刺穿构件可以设置在试剂室6213a、6213b、6213c的任何一个试剂室内和/或设置在通道6221a、6221b、6221c中的任何一个通道内,以将各个试剂室与洗脱室6190流体隔离。以与参照可刺穿构件6170的以上描述的方式相类似的方式,在这种实施方式中,可刺穿构件可以被试剂柱塞刺破以将试剂室选择性地安置成与洗脱室流体连通。
试剂柱塞6214a可移动地设置在试剂室6213a内,试剂柱塞6214b可移动地设置在试剂室6213b内,并且试剂柱塞6214c可移动地设置在试剂室6213c内。以此方式,当试剂柱塞(例如,试剂柱塞6214a)被移动时,如由图22中的箭头nn所示出的,试剂柱塞将试剂室(例如,试剂室6213a)的内含物经由相关联的通道(例如,通道6221a)传送到洗脱室6190中。以此方式,试剂柱塞充当传送机构。
试剂柱塞6214a、6214b、6214c可以由仪器的致动器组件——例如本文中描述的仪器3002的致动组件3600——接触和/或致动。在一些实施方式中,试剂柱塞6214a、6214b、6214c可以包括构造成保持致动器组件(例如,致动器组件3400)的一部分的保持机构(例如凸起、卡环等),以便于通过致动器组件使试剂柱塞6214a、6214b、6214c往复运动。
pcr模块包括传送机构6235,该传送机构6235构造成传送来自分离模块6100的洗脱室6190和pcr模块6200的pcr小瓶6260的物质和/或在分离模块6100的洗脱室6190与pcr模块6200的pcr小瓶6260之间传送物质。传送机构6235包括设置在泵空腔6241内的传送活塞6240。当传送活塞6240如由图22中箭头oo所示在泵空腔6241内移动时,在pcr容积6262内产生真空和/或正压力。pcr容积6262与洗脱室6190之间的压差导致洗脱室6190的内含物的至少一部分经由传送管6250和通道6222(参见例如图24)传送到pcr室6262中(或从pcr室6262传送)。以此方式,可以通过致动传送机构6235而在洗脱室6190与pcr容积6262之间添加、混合和/或运送物质和/或样品。传送机构6235可以由任何适合的机构——例如本文中描述的仪器3002的致动组件3600——致动。
传送活塞6240和泵空腔6241可以位于pcr模块6200内的任何适合的位置。例如,尽管传送活塞6240示出为设置在pcr小瓶6260的基本上上方,但在其它实施方式中,传送活塞6240可以设置在洗脱室6190的基本上上方。
在一些实施方式中,壳体6210限定一个或多个通气通道以将洗脱室6190和/或pcr小瓶6260流体地联接至大气。在一些实施方式中,任何这种通气口可以包括熔块以最小化地减少和/或防止样品和/或试剂从洗脱室6190和/或pcr小瓶6260中损失。
在使用中,如上所述,在分离模块6100内分离核酸并处理后,其经由传送组件6140c传送至洗脱室6190中。之后通过洗脱缓冲液将磁珠从核酸中除去(或“洗涤”)并从洗脱室6190中除去。由此,洗脱室6190容纳经分离和/或经纯化的核酸。在一些实施方式中,洗脱缓冲液容纳在洗脱室6190内。在其它实施方式中,洗脱缓冲液容纳在pcr模块6200的试剂室之一(例如,试剂室6213c)中,并且被传送至洗脱室6190中,如上所述。在一个实施方式中,洗脱缓冲液包含分子级水、trishcl(例如,约10mm、约15mm、约20mm、约25mm、约30mm、约35mm或约40mm)、氯化镁(例如,约1mm、约2mm、约3mm、约4mm、约5mm、约6mm、约7mm、约8mm、约9mm、约10mm或约20mm)、甘油(例如,约2%、约3%、约4%、约5%、约6%、约7%、约8%、约9%、约10%、约12%、约14%、约16%、约18%、约20%或约25%)的过滤溶液。在一个实施方式中,洗脱缓冲液的ph为约7.5、约7.6、约7.7、约7.8、约7.9、约8.0、约8.1、约8.2、约8.3、约8.4、约8.5、约8.6、约8.7、约8.8、约8.9或约9.0。在另一个实施方式中,洗脱缓冲液包含杀菌剂,例如,以上提供的洗脱缓冲液还包含杀菌剂。在一个实施方式中,洗脱缓冲液还充当洗涤缓冲液。虽然对洗脱室6190进行了特别描述,但在其它实施方式中,上述洗脱缓冲液作为物质r1或r2存在。
在一些实施方式中,pcr试剂随后从pcr模块6200运送到洗脱室6190中。更具体地,试剂柱塞6214a、6214b和/或6214c被致动(例如,通过仪器3002)以将通道6221a、6221b、6221c将试剂引入洗脱室6190中。pcr样品随后经由传送管6250和通道6222从洗脱室6190运送到pcr小瓶6260中。特别地,传送活塞6240可以被致动以产生pcr模块6200内的压差,从而将pcr样品从洗脱室6190运送到pcr小瓶6260中,如上所述地。以此方式,在洗脱室6190中制备pcr样品(经分离地核酸和pcr试剂)。通过在洗脱室642内执行试剂和核酸样品的混合(而不是将分离出的核酸运送到pcr小瓶6260中并在其内进行混合),避免了核酸的额外传送。这种布置可以使后-pcr分析的准确性提高,使得在一些实施方式中,该分析在本质上是半定量的。
然而,在其它实施方式中,可以在pcr小瓶6260中制备pcr样品(经分离的核酸和pcr试剂)。在这种实施方式中,例如,pcr试剂可以例如以冻干的形式储存在pcr小瓶6260中。经分离的核酸可以运送到pcr小瓶6260中,并且与冻干的pcr试剂一起混合,以在pcr小瓶6260内重构试剂。
在pcr样品处于pcr小瓶6260中后,pcr样品可以进行热循环(例如,通过仪器3002的加热器组件3700)以进行所需的扩增。在热循环结束时和/或热循环期间,pcr样品可以进行光学分析(例如,通过仪器3002的光学组件3800)以分析样品。以下提供仪器3002的描述。
图25至图33为根据实施方式的药筒7001的各种视图。药筒7001的某些特征与药筒6001的对应的特征相类似,并且因此以下未对其进行描述。在适用的情况下,对药筒6001提出的以上讨论并入对药筒7001的讨论中。例如,尽管位于第二壳体7160内的致动器(例如,致动器7163a)尺寸和/或形状不同于第二壳体6160内的致动器(例如致动器6163a)的尺寸和/或形状,第二壳体6160内的致动器的结构和功能的许多方面与壳体7160内的致动器的结构和功能的许多方面类似。因此,对于致动器(例如,致动器6160a)提出的以上描述应用于以下描述的致动器(例如,致动器7160a)。
药筒7001包括样品制备(或分离)模块7100和扩增(或pcr)模块7200,该样品制备模块7100与该扩增模块7200联接在一起以形成集成的药筒7001。盖7005围绕分离模块7100和pcr模块7200的一部分设置。一个或多个药筒7001可以设置在本文中所公开的类型(参见例如以下描述的仪器3002)的任何适合的仪器内,该仪器构造成操纵、致动药筒7001和/或与药筒7001交互作用以对容纳在药筒7001内的测试样品进行核酸分离、转录和/或扩增。
如图26至图28所示,分离模块7100包括第一(或分离)壳体7110以及联接至第一壳体7110和/或至少部分地位于第一壳体7110内的第二(或试剂)壳体7160。第二壳体7160限定了一系列保持室7163a、7163b、7163c和7163d,其容纳在分离过程中使用的试剂和/或其它物质。如本文中描述的,保持室可包含蛋白酶(例如,蛋白酶k)、溶解大块材料的裂解溶液、使裂解室7114内残余的核酸样品带磁性电荷的结合溶液、以及结合至磁性带电核酸以协助核酸在分离模块7100和/或第一壳体7110内运输的磁珠的溶液。在一个实施方式中,以上提供的上述溶液在图26至图28中提供的药筒中使用。
每个保持室7163a、7163b、7163c和7163d包括可移除地设置在其内的致动器。更具体地,如图27和图28中所示,致动器7166a设置在保持室7163a内,致动器7166b设置在保持室7163b内,致动器7166c设置在保持室7163c内,并且致动器7166d设置在保持室7163d内。每个致动器7166a、7166b、7166c和7166d与以上示出和描述的致动器6166相类似(参见例如图14)。特别地,每个致动器7166a、7166b、7166c和7166d可以充当传送机构以在沿由图28中箭头pp指示的方向移动时将物质从室(例如,室7163a)运送到分离模块7100的另一部分中。
如图27中所示,可刺穿构件7170围绕第二壳体7160的一部分设置,使得第二壳体7160的内部部分、可刺穿构件7170和致动器7166a、7166b、7166c和7166d共同地包围和/或限定保持室7163a、7163b、7163c和7163d。类似陈述地,第二壳体7160的内部部分、可刺穿构件7170和致动器7166a、7166b、7166c和7166d共同地限定流体隔离的室7163a、7163b、7163c和7163d,在所述流体隔离的室7163a、7163b、7163c和7163d中可以储存试剂和/或物质。可刺穿构件7170可以由本文中描述的类型的任何适合的材料——比如任何形式的聚丙烯——构造。在一些实施方式中,可刺穿构件7170可以由双轴向聚丙烯(bop)构造。
第二壳体7160包括混和泵7181、该混合泵7181可以被致动(例如,通过仪器3002的致动器组件3400),以在容纳于分离模块7100的一部分(例如,裂解室7114)内的样品、试剂和/或其它物质内搅动、混合和/或产生紊流运动。
如图26至图28中所示,第二壳体7160设置在由第一壳体7110限定的开口内。由此,当第二壳体7160设置在第一壳体7110内时,第二壳体7160的一部分限定裂解室7114的边界的至少一部分。更具体地,当第二壳体7160设置在第一壳体7110内时,可刺穿构件7170限定裂解室7114的边界的一部分。这种布置允许当可刺穿构件7170的一部分被刺破、刺穿、切断和/或破裂时容纳在第二壳体7160内的物质被运送到裂解室7114内。以与参照分离模块6100的以上描述相类似的方式,容纳在第二壳体7160内的物质可以在致动器7166a、7166b、7166c和7166d被致动时运送到第一壳体7110中。
如图27和图28所示,第一壳体7110包括第一(或顶部)部分7112和第二(或底部)部分7111。在一些实施方式中,上部部分7112可以与下部部分7111单独地构造,并且可以随后被联接至下部部分7111以形成第一壳体7110。第一壳体限定裂解室7114、两个洗涤室7121和7122、三个传送组件管腔(图27和图28中未示出)以及洗脱室7190。第一壳体7110还限定与分离室7114相邻的开口,第二壳体7160的一部分设置在该开口中。
如图26至图28中所示,分离模块7100包括盖7118,该盖7118可移除地联接至壳体7110。在使用中,含有靶核酸的样品——例如尿、血和/或含有组织样品的其它材料——可以在移除盖7118后经由填充开口7116运送到裂解室7114中。样品可以通过任何适合的机构——包括例如经由填充开口7116将样品吸移或注射到第一室7114中——引入裂解室7114中。
在样品被设置到裂解室7114中后,用于磁极细胞裂解的试剂和/或物质可以添加入裂解室7114中,如以上所述的。此外,样品可以通过泵7181来搅动和/或混合以磁极裂解过程,如以上所述的。在一些实施方式中,裂解室7144的内含物可以被加热(例如,通过如以下参照仪器3002所示出和描述的第三加热模块3780)。此外,第一壳体7110的第二部分7111包括声学联接部7182。因此,在一些实施方式中,声换能器的至少一部分(在图26至图28中未示出)可以设置成与声学联接部7182相接触。以此方式,由转换器产生的声学能和/或超声能可以传送通过声学联接部7182和第一壳体7110的侧壁、并进入裂解室7114内的溶液中(参见例如图82至图84b的对于超声裂解系统的描述)。
分离模块7100包括一系列的传送组件(也称为传送机构),在图26至图28中示出为传送组件7140a,传送组件7140b和传送组件7140c。如本文中描述的,传送组件构造成在裂解室7114、洗涤室7121、洗涤室7122和洗脱室7192之间传送物质(例如,样品的一部分包括磁性电荷粒子和附接至所述磁性电荷粒子的经分离的核酸)。更具体地,传送组件7140构造成在裂解室7114、洗涤室7121、洗涤室7122和洗脱室7190之间传送物质的同时维持裂解室7114、洗涤室7121、洗涤室7122和洗脱室7190与由第一壳体7110限定的其它室(例如,相邻的洗涤室)基本上流体隔离。传送组件7140a、7140b和7140c在结构和功能上类似于以上关于分离模块6100示出和描述的传送组件6140,并因而以下不进行详细描述。
分离模块7100包括两个洗涤缓冲液模块7130a和7130b,所述两个洗涤缓冲液模块7130a和7130b各自联接至第一壳体7110的上部部分7112。如本文中所述,洗涤缓冲液模块7130a和7130b各自容纳物质(例如试剂、洗涤缓冲液、矿物油和/或要被添加至样品中的任何其它物质),并且构造成当被致动时将该物质分别传送到洗涤室7121和洗涤室7122中。此外,每个洗涤缓冲液模块7130a和7130b均构造成分别产生洗涤室7121和洗涤室7122内的流体流动,以促进容纳在其内的样品的一部分的洗涤和/或混合。类似陈述地,每个洗涤缓冲液模块7130a和7130b均构造成分别向洗涤室7121和洗涤室7122内传送能量。在一个实施方式中,洗涤缓冲液模块7130a和/或7130b包含洗涤缓冲液,其含有分子级水、trishcl(例如,约10mm、约15mm、约20mm、约25mm、约30mm、约35mm或约40mm)、氯化镁(例如,约1mm、约2mm、约3mm、约4mm、约5mm、约6mm、约7mm、约8mm、约9mm、约10mm或约20mm)、甘油(例如,约2%、约3%、约4%、约5%、约6%、约7%、约8%、约9%、约10%、约12%、约14%、约16%、约18%、约20%或约25%)的过滤溶液。在一个实施方式中,洗涤缓冲液的ph为约7.5、约7.6、约7.7、约7.8、约7.9、约8.0、约8.1、约8.2、约8.3、约8.4、约8.5、约8.6、约8.7、约8.8、约8.9或约9.0。在另一个实施方式中,洗涤缓冲液包含杀菌剂,例如,以上提供的洗涤缓冲液还包含杀菌剂。
尽管对室7130a和/或7130b进行了特别描述,但在另一实施方式中以上刚描述的洗涤缓冲液作为r1和/或r2存在。
在另一个实施方式中,洗涤缓冲液模块7130a和/或7130b包含洗涤缓冲液,其含有分子级水、胍hcl(例如,约0.7mm、约0.8mm、约0.81mm、约0.82mm、约0.83mm、约0.84mm、约0.85mm、约0.9mm、约1.0mm)、trishcl(例如,约10mm、约15mm、约20mm、约25mm、约30mm、约35mm或约40mm,并且可具有约7.5、约8或约8.5的ph)、triton-x-100(例如,约0.25%、约0.5%、约0.75%、约1%)、tween-20(例如,约0.25%、约0.5%、约0.75%、约1%)、edta(例如,约0.1mm、约0.2mm、约0.3mm、约0.5mm、约0.75mm、约1mm、约2mm、约3mm、约4mm、约5mm、约6mm、约7mm、约8mm、约9mm、约10mm或约20mm)、异丙醇(例如,约10%、约20%、约30%、约40%、约50%、约60%)的过滤溶液。在一个实施方式中,洗脱缓冲液的ph为约7.5、约7.6、约7.7、约7.8、约7.9、约8.0、约8.1、约8.2、约8.3、约8.4、约8.5、约8.6、约8.7、约8.8、约8.9或约9.0。尽管对室7130a和/或7130b进行了特别描述,但在其它实施方式中,以上刚描述的洗涤缓冲液作为物质r1和/或r2存在。
洗涤缓冲液模块7130a包括致动器7150a,该致动器7150a可移动地设置在壳体7137a内。壳体7137a联接至第一壳体7110的上部部分7112,使得洗涤缓冲液模块7130a与洗涤室7121基本上对准。特别地,壳体7137a包括一对凸起7133a,该对凸起7133a构造成设置在由第一壳体7110的上部部分7112的联接部7134a限定的相对应的开口内。尽管洗涤缓冲液模块7130a示出为通过“卡扣配合”联接至第一壳体7110,但在其它实施方式中,洗涤缓冲液模块7130a可以通过任何适合的方法——例如通过螺纹联接、机械紧固件或保持件、化学结合或粘结、过盈配合、焊接等——联接至第一壳体7110。
致动器7150a包括柱塞部7151a、刺破部7152a和接合部7153a。接合部7153a构造成接合致动器组件的一部分、可移除地联接至致动器组件的一部分和/或接纳在致动器组件的一部分内,以便于致动器7150a在壳体7137a运动,如本文中描述的。致动器7150a可以通过任何适合的仪器——比如以下关于图47至图51描述的致动器组件3600——操纵和/或致动。
致动器7150a的柱塞部7151a设置在壳体7137a内。可刺穿构件7135a围绕壳体7137a的端部设置,使得柱塞部7151a的端面、壳体7137a和可刺穿构件7135a共同限定在其内设置物质的容积。壳体7137a的内表面和柱塞部7151a构造成形成基本上流体密封的和/或气密封。在一些实施方式中,柱塞部7151a可以包括密封构件、o形圈等。
致动器7150a的刺破部7152a构造成当致动器7150a在壳体7137a内沿由图28中箭头qq指示的方向移动时,致动器7150a的刺破部7152a刺穿、破坏、切断和/或破裂可刺穿构件7135a的一部分。以此方式,致动器7150的运动将该室安置成与洗涤室7121流体连通。类似陈述地,洗涤缓冲液模块7130a可以在致动器7150a被致动时选择性地安置成与洗涤室7121流体连通。在洗涤缓冲液模块7130a内的物质被运送到洗涤室7121中之后,致动器7150a可以在壳体7137a内往复运动以产生压力,该压力被传送到洗涤室7121内,以促进设置在其内的样品之间的洗涤、混合和/或与设置在其内的样品的其它交互作用。第一壳体7110的上部部分7112包括喷嘴7131a,该喷嘴7131a构造成将由致动器7150a产生的压力能和/或流动朝向洗涤室7121内的特定区域引导。
洗涤缓冲液模块7130b包括致动器7150b,该致动器7150b可移动地设置在壳体7137b内。壳体7137b联接至第一壳体7110的上部部分7112,使得洗涤缓冲液模块7130b与洗涤室7122基本上对准。特别地,壳体7137b包括一对凸起7133b,该对凸起7133b构造成设置在由第一壳体7110的上部部分7112的联接部7134b限定的相对应的开口内。尽管洗涤缓冲液模块7130b示出为通过“卡扣配合”联接至第一壳体7110,但在其它实施方式中,洗涤缓冲液模块7130b可以通过任何适合的方法——例如通过螺纹联接、机械紧固件或保持件、化学结合或粘结、过盈配合、焊接等——联接至第一壳体7110。
致动器7150b包括柱塞部7151b、刺破部7152b和接合部7153b。接合部7153b构造成接合致动器组件的一部分、可移除地联接至致动器组件的一部分和/或接纳在致动器组件的一部分内,以便于致动器7150b在壳体7137a内运动,如本文中描述的。致动器7150b可以通过任何适合的仪器——比如以下关于图47至图51描述的致动器组件3600——操纵和/或致动。
致动器7150b的柱塞部7151b设置在壳体7137b内。可刺穿构件7135b围绕壳体7137b的端部设置,使得柱塞部7151b的端面、壳体7137b和可刺穿构件7135b共同限定在其内设置物质的容积。壳体7137b的内表面和柱塞部7151b构造成形成基本上流体密封和/或气密封。在一些实施方式中,柱塞部7151b可以包括密封构件、o形圈等。
致动器7150b的刺破部7152b构造成当致动器7150b在壳体7137b内沿由图28中箭头qq指示的方向移动时,致动器7150b的刺破部7152b刺穿、破坏、切断和/或破裂可刺穿构件7135b的一部分。以此方式,致动器7150b的运动将该室安置成与洗涤室7122流体连通。类似陈述地,洗涤缓冲液模块7130b可以在致动器7150b被致动时选择性地安置成与洗涤室7122流体连通。在洗涤缓冲液模块7130b内的物质被运送到洗涤室7122中之后,致动器7150b可以在壳体7137b内往复运动以产生压力,该压力被传送到洗涤室7122内,以促进设置在其内的样品之间的洗涤、混合和/或与设置在其内的样品的其它交互作用。第一壳体7110的上部部分7112包括喷嘴7131b,该喷嘴7131b构造成将由致动器7150b产生的压力能和/或流动朝向洗涤室7122内的特定区域引导。
如图29至图31中所示,扩增(或pcr)模块7200包括基底7220,该基底7220由第一(或上)层7227和第二(或底)层7228构造。pcr模块7200包括pcr小瓶7260,该pcr小瓶7260联接至第二层7228、传送机构7235、第一试剂模块7270a和第二试剂模块7270b。pcr小瓶7260联接至壳体7210的第一端部7211并限定容积7262,在该容积7262内可以设置有样品以促进与该样品相关联的反应。pcr小瓶7260可以为用于以允许发生与该样品相关联的反应的方式容纳该样品的任何适合的容器。pcr小瓶7260也可以为用于以允许监测这种反应(例如,检测样品内反应引起的或与反应相关联的分析物)的方式容纳该样品的任何适合的容器。在一些实施方式中,pcr小瓶7260的至少一部分可以是基本上透明的,以允许其内发生的反应的光学监测为光学系统(例如,本文中描述的仪器3002的光学组件3800)。
如图32和图33中所示,扩增模块7200联接至分离模块7100的第一壳体7110,使得传送管7250的至少一部分设置在分离模块7100的洗脱室7190内。以此方式,如本文中描述的,设置在洗脱室7190内的经分离核酸、任何物质和/或任何pcr试剂可以经由传送管7250从洗脱室7190运送至pcr小瓶7260。更具体地,基底7220限定流动通道7222,该流动通道7222在pcr模块7200联接至分离模块7100时将pcr小瓶7260安置成与洗脱室7190流体连通。如图30和图31中所示,流动通道7222的一部分限定在传送管7250中以及基底7220的第二层7228的传送端口7229中。尽管流动通道7222示出为主要由基底7220的第二层7228限定,但在其它实施方式中,流动通道7222可以由第一层7227来限定或限定在第一层7227和第二层7228二者的部分中。
基底7220还限定流动通道7223、流动通道7221a和流动通道7221b。如本文中更详细地描述的,流动通道7223构造成将限定在传送机构7235内的容积7237安置成经由传送端口7229与pcr小瓶7260流体连通。流动通道7221a构造成将由试剂模块7270a限定的容积安置成经由传送管7250与洗脱室7190流体连通。流动通道7221b构造成将由试剂模块7270b限定的容积安置成经由传送端口7229和/或通道7222的一部分与pcr小瓶7260流体连通。流动通道7223、流动通道7221a和/或流动通道7221b中的任何一者可以由第一层7227、第二层7228来限定或限定在第一层7227和第二层7228二者的部分中。
pcr模块7200包括两个试剂模块7270a和7270b,所述两个试剂模块7270a和7270b各自联接至基底7220的上层7227。如本文中描述的,每个试剂模块7270a和7270b均分别容纳物质r1和物质r2。试剂模块7270a构造成将物质r1通过如本文中描述的流动通道7221a运送到洗脱室7190中。试剂模块7270b构造成将物质r2经由流动通道7221b运送到pcr小瓶7260中,如本文中描述的。以此方式,每个模块7270a和7270b均充当试剂储存装置和传送机构。
物质r1和r2可以例如为试剂、洗脱缓冲溶液、洗涤缓冲溶液、矿物油和/或要被添加至样品中的任何其它物质,如本文中描述的。在一些实施方式中,物质r1可以包括洗脱缓冲液和矿物油。在一些实施方式中,物质r2可以包括促进pcr小瓶7260内的pcr过程的反应试剂。在一些实施方式中,pcr主要混合物可以以冻干的状态设置在pcr小瓶7260中,使得物质r2的添加和/或物质r1与靶向样品的混合物重构经冻干的主要混合物,以促进pcr过程。
在一些实施方式中,通过单链双标记检测探针来监测pcr,即5'端具有荧光团标记和3'端具有猝灭剂。在进一步的实施方式中,探针为水解探针,其依赖于taq聚合酶的5'→3'外切核酸酶活性以在杂交后将双标记探针切成互补链,例如
在另一个实施方式中,主要混合物包含冻干试剂,以对三种靶和内部对照进行多重pcr。在进一步的实施方式中,靶核酸为对流感a特异的核酸、对流感b特异的核酸和对rsv特异的核酸。在甚至进一步的实施方式中,实时监测多重反应,例如通过提供对各个靶序列特异的杂交寡核苷酸探针,各个探针包含在5'端的荧光团和mgb以及在3'端的非荧光猝灭剂。
在另一个实施方式中,冻干的主要混合物包含用于pcr和反转录反应的试剂。例如,在一个实施方式中,冻干的主要混合物包含反转录酶和taq聚合酶二者、dntp、rnase抑制剂、kcl、bsa以及引物,以执行第一链cdna合成和pcr。
主要混合物包含不同的引物和探针,这取决于要被扩增的靶。每种靶将与特异引物和探针组相关联,并且该特异引物和探针组可以与上述的其它pcr试剂一起冻干,以形成冻干的主要混合物。组分的浓度还取决于扩增的特异性靶以及是否扩增多个靶而变化。
试剂模块7270a包括致动器7280a,该致动器7280a可移动地设置在壳体7277a内。壳体7277a联接至基底7220的上层7227,使得试剂模块7270a与通道7221a、传送管7250和/或洗脱室7190基本上对准。如图29中所示,壳体7277a包括一对凸起7273a,该对凸起7273a构造成设置在由基底7220的上层7227的联接部7234a限定的相对应的开口内。尽管试剂模块7270a示出为通过“卡扣配合”联接至基底7220,但在其它实施方式中,试剂模块7270a可以通过任何适合的方法——例如通过螺纹联接、机械紧固件或保持件、化学结合或粘结、过盈配合、焊接等——联接至基底7220。
致动器7280a包括柱塞部7281a、刺破部7282a和接合部7283a。接合部7283a构造成接合致动器组件的一部分、可移除地联接至致动器组件的一部分和/或接纳在致动器组件的一部分内,以便于致动器7280a在壳体7277a内运动,如本文中描述的。致动器7280a可以通过任何适合的仪器——诸比如以下关于图47至图51描述的致动器组件3600——操纵和/或致动。
致动器7280a的柱塞部7281a设置在壳体7277a内。可刺穿构件7275a围绕壳体7277a的端部设置,使得柱塞部7281a的端面、壳体7277a和可刺穿构件7275a共同限定于其内设置物质r1的容积。壳体7277a的内表面和柱塞部7281a构造成形成基本上流体密封和/或气密封。在一些实施方式中,柱塞部7281a可以包括密封构件、o型圈等。
致动器7280a的刺破部7282a构造成当致动器7280a在壳体7277a内沿由图31中箭头ss指示的方向移动时,致动器7280a的刺破部7282a刺穿、破坏、切断和/或破裂可刺穿构件7275a的一部分。以此方式,致动器7280a的运动将其内的容积安置成与通道7221a流体连通、并因而与洗脱室7190流体连通。类似陈述地,试剂模块7270a可以在致动器7280a被致动时选择性地安置成与洗脱室7190流体连通。
试剂模块7270b包括致动器7280b,该致动器7280b可移动地设置在壳体7277b内。壳体7277b联接至基底7220的上层7227,使得试剂模块7270b与通道7221b基本上对准。如图29中所示,壳体7277b包括一对凸起7273b,该对凸起7273b构造成设置在由基底7220的上层7227的联接部7234b限定的相对应的开口内。尽管试剂模块7270b示出为通过“卡扣配合”联接至基底7220,但在其它实施方式中,试剂模块7270b可以通过任何适合的方法——例如通过螺纹联接、机械紧固件或保持件、化学结合或粘结、过盈配合、焊接等——联接至基底7220。
致动器7280b包括柱塞部7281b、刺破部7282b和接合部7283b。接合部7283b构造成接合致动器组件的一部分、可移除地联接至致动器组件的一部分和/或接纳在致动器组件的一部分内,以便于致动器7280b在壳体7277b内运动,如本文中描述的。致动器7280b可以通过任何适合的仪器——比如以下关于图47至图51所描述的致动器组件3600——操纵和/或致动。
致动器7280b的柱塞部7281b设置在壳体7277b内,可刺穿构件7275b围绕壳体7277b的端部设置,使得柱塞部7281b的端面、壳体7277b和可刺穿构件7275b共同限定于其内设置物质r2的容积。壳体7277b的内表面和柱塞部7281b构造成形成基本上流体密封的和/或气密封。在一些实施方式中,柱塞部7281a可以包括密封构件、o型圈等。
致动器7280b的刺破部7282b构造成当致动器7280b在壳体7277b内沿由图31中箭头ss指示的方向移动时,致动器7280b的刺破部7282b刺穿、破坏、切断和/或破裂可刺穿构件7275b的一部分。以此方式,致动器7280b的运动将其内的容积安置成与通道7221b流体连通、并因而与pcr室7260流体连通。
pcr模块7200包括传送机构7235,该传送机构7235构造成传送来自分离模块7100的洗脱室7190和pcr模块7200的pcr小瓶7260的物质和/或在分离模块7100的洗脱室7190和pcr模块7200的pcr小瓶7260之间传送物质。如本文中所述的,传送机构7235还构造成限定容积7237,在该容积7237内可以容纳物质,并且选择性地将容积7237安置成与pcr小瓶7260流体连通。以此方式,传送机构7235还充当流动控制机构。
传送机构7235包括设置在壳体7236内的致动器7240。壳体7236联接至基底7220的上层7227的一部分和/或为基底7220的上层7227的一部分。壳体7236限定容积7237,在该容积7237内可以储存例如矿物油的物质。尽管未示出为包括可刺穿构件,但在其它实施方式中,容积7237的一部分可以由可刺穿构件包围和/或被可刺穿构件流体隔离如本文中所述的。
致动器7240包括柱塞部7241、阀部7242和接合部7243。接合部7243构造成接合致动器组件的一部分、可移除地联接至致动器组件的一部分和/或接纳在致动器组件的一部分内,以便于致动器7240在壳体7236内运动,如本文中描述的。致动器7240可以通过任何适合的仪器——比如以下关于图47至图51描述的致动器组件3600——操纵和/或致动。
致动器7240的柱塞部7241设置在壳体7236内。壳体7236的内表面和柱塞部7241构造成形成基本上流体密封和/或气密封。在一些实施方式中,柱塞部7241可以包括密封构件、o型圈等。另外,密封件7244设置在壳体7236的顶部处。
致动器7240构造成在壳体7236内在第一位置(图30)与第二位置(图31)之间移动。当致动器7240处于第一位置时,致动器7240的阀部7242设置成至少部分地位于流动通道7223内,使得容积7237与流动通道7223和/或pcr小瓶7260基本上流体隔离。类似陈述地,当致动器7240处于第一位置时,阀部7242的一部分与上层7227接触,以产生基本上流体密封和/或气密封。当致动器7250在壳体7236内沿由图31中箭头rr指示的方向移动时,阀部7242与上层7227间隔开和/或从流动通道7223中移除,由此,将容积7237安置成与通道7223流体连通、并因此与pcr室7260流体连通。以此方式,当致动器7240移动时,容积7237内的物质可以被运送到由pcr小瓶7260限定的pcr容积7262中。
此外,当致动器7240在壳体7236内移动时,如由图31中箭头rr所示,在pcr小瓶7260的pcr容积7262内产生真空。pcr容积7262与洗脱室7190之间的压差引起洗脱室7190的内含物的至少一部分具有传送管7250和通道7222(参见例如图24)传送到pcr容积7262中。以此方式,通过致动传送机构7235可以在洗脱室7190与pcr容积7262之间添加、混合和/或运送物质和/或样品。传送机构7235可以通过任何适合的机构——例如本文中所述的仪器3002的致动组件3600——致动。
在使用中,如上所述,在一个或多个靶核酸或核酸群体在分离模块7100内被分离出并被处理之后,其通过传送组件7140c被传送到洗脱室7190中。试剂模块7270a可以随后被致动,以将物质r1传送到洗脱室7190中。例如,在一些实施方式中,试剂模块7270a可以被致动,以将含有洗脱缓冲液和矿物油的溶液运送到洗脱室7190中。磁珠随后通过洗脱缓冲液从核酸中移除(或“洗涤”),并且从洗脱室7190中移除(例如,通过传送组件7140c)。由此,洗脱室7190容纳经分离和/或经纯化的核酸。
试剂模块7270b可以被致动,以将物质r2运送到pcr容积7262中。例如,在一些实施方式中,试剂模块7270b可以被致动,以将含有各种反应试剂的溶液运送到pcr小瓶7260中。在一些实施方式中,pcr小瓶7260可以容纳处于冻干状态的额外试剂pcr和/或物质,例如主要混合物。因此,当物质r2运送到pcr小瓶7260中时冻干的内含物可以在制备中重构用于反应。
靶向样品s可以经由传送管7250和通道7222从洗脱室7190(在致动上述的试剂模块7270b之前或之后)运送到pcr小瓶7260中。特别地,传送机构7235的致动器7240可以被致动,以在pcr模块7200内产生压差,从而将pcr样品经由通道7222从洗脱室7190运送到pcr小瓶7260中,如上所述的。以此方式,pcr样品(分离出的核酸和pcr试剂)可以部分地在洗脱室7190中制备。此外,当传送机构7235被致动时,限定在其内的容积7237被安置成经由通道7223与pcr容积7262流体连通,如上所述的。因此,在一些实施方式中,额外的物质(例如,矿物油)可以通过与样品传送操作相同的操作被添加至pcr小瓶中。
在pcr样品处于pcr小瓶7260中之后,pcr样品s的至少一部分可被热循环(例如,通过仪器3002的加热器组件3700)以执行所需的扩增。在热循环完成后和/或在热循环期间,可任选地分析pcr样品(例如,通过仪器3002的光学组件3800)以分析样品。或者,如通篇所述的,可以在pcr期间例如利用各自与mgb和荧光团缀合的dna杂交探针进行任选地分析pcr样品。以下提供了仪器3002和用于操纵药筒的其它适合的仪器的描述。
本文中描述的任何药筒可以由任何适合的仪器操纵和/或致动,以对容纳在药筒内的样品执行分离过程和/或反应。例如,在一些实施方式中,本文中描述的任何药筒可以由仪器操纵和/或致动,以对药筒内的测试样品执行实时核酸分离和扩增。以此方式,系统(例如,药筒或一系列药筒和仪器)可以用于许多不同测定,例如来自鼻咽样本的流感(flu)a、flub和呼吸道合胞体病毒(rsv)的快速检测。
在一些实施方式中,仪器可以构造成促进、产生、支持和/或加快由本文中示出和描述的类型的药筒限定的反应室中容纳的样品中的反应。这种仪器也可以包括光学组件,以在反应之前、反应期间和/或反应之后检测样品中的一种或多种不同的物质和/或分析物。例如,图34为根据实施方式的仪器1002的示意性图示。仪器1002包括块体1710、第一光学构件1831、第二光学构件1832和光学组件1800。块体1710限定反应容积1713,该反应容积1713构造成接纳反应容器260的容纳样品s的至少一部分261。反应容器260可以为用于以允许与样品s相关联的反应发生的方式容纳该样品s的任何适合的容器。反应容器260也可以是用于以允许监测这种反应(例如,检测样品s内由反应所引起的或与反应相关联的分析物)的方式容纳该样品s的任何适合的容器。在一些实施方式中,例如,反应容器260可以是pcr小瓶,试管等。此外,在一些实施方式中,反应容器260的至少该部分261能够为基本上透明的,以允许光学监测在其内发生的反应。
块体1710可以为用于促进、产生、支持和/或加快与反应容器260中的样品s相关联的反应的任何适合的结构,和/或可以联接至用于促进、产生、支持和/或加快与反应容器260中的样品s相关联的反应的任何适合的机构。例如,在一些实施方式中,块体1710可以联接至和/或可以包括用于循环加热反应容器260中的样品s的机构。以此方式,块体1710可以产生样品s的热诱导反应,例如pcr过程。在其它实施方式中,块体1710可以联接至和/或可以包括用于将一种或多中物质引入反应容器260中以产生与样品s相关联的化学反应的机构。
反应容积1713可以具有用于容纳反应室260的部分261的任何适合的尺寸和/或形状。在一些实施方式中,例如,反应容积1713的形状可以基本上对应于反应室260的部分261的形状(例如,如图34中所示)。然而,在一些实施方式中,反应容积1713的形状可以与反应室260的部分261的形状不同。尽管反应室260的部分261在图34中示出为与块体1710的限定反应容积1713的侧壁间隔开,但在其它实施方式中,反应室260的部分261可以与块体1710的一部分接触。在又一些其它实施方式中,反应容积1713可以容纳设置在反应室260的部分261与块体1710的一部分(例如,侧壁)之间的物质(例如,盐水溶液、导热胶等)。
尽管块体1710在图34中示出为仅容纳反应容积1713内的反应室260的部分261,但在其它实施方式中,块体1710可以构造成使得整个反应室260被接纳在反应室1713内。在一些实施方式中,例如,块体1710可以包括将整体的反应室260基本上保留在反应容积1713内的盖或其它机构(图34中未示出)。此外,在一些实施方式中,块体1710可以基本上围绕整个反应室260。在其它实施方式中,块体1710可以基本上围绕设置在反应容积1713内的反应室260的部分261。
如图34中所示,第一光学构件1831设置成至少部分地位于块体1710内,使得第一光学构件1831与反应容积1713光学连通。以此方式,光束(和/或光信号)可以通过第一光学构件1831而在反应容积1713与块体1710的外部区域之间传送。第一光学构件1831可以为光束可以通过其或从其传送的任何适合的结构、装置和/或机构。在一些实施方式中,第一光学构件1831可以为用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。在其它实施方式中,第一光学构件1831可以包括构造成修改和/或转化光束的机构,例如光学放大器、光学信号转换器、透镜、光学过滤器等。在又一些其它实施方式中,第二光学构件1832可以包括发光二极管(led)、激光或构造成产生光束的其它装置。
第二光学构件1832设置至少部分地位于块体1710内,使得第二光学构件1832与反应容积1713光学连通。以此方式,光束(和/或光信号)可以通过第二光学构件1832而在反应容积1713与块体1710的外部区域之间传送。第二光学构件1832可以为光束可以通过其或从其传送的任何适合的结构、装置和/或机构。在一些实施方式中,第二光学构件1832可以为用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。在其它实施方式中,第二光学构件1832可以包括构造成修改和/或转化光束的机构,例如光学放大器、光学信号转换器、透镜、光学过滤器等。在又一些其它实施方式中,第二光学构件1832可以包括光电二极管或构造成接收和/或检测光束的其它装置。
光学组件1800包括激发模块1860和检测模块1850。激发模块1860构造成产生一系列的激发光束(和/或光学信号,图34中未示出)。因此,激发模块1860可以包括用于产生一系列激发光束的任何适合的装置和/或机构,例如激光、一个或多个发光二极管(led)、闪光灯等。在一些实施方式中,由激发模块1860产生的每道光束可以具有与由激发模块1860产生的其它光束中的每道光束基本上相同的特性(例如,波长、幅值和/或能量)。然而,在其它实施方式中,由激发模块1860产生的第一光束可以具有不同于由激发模块1860产生的其它光束中的一道光束的特性(例如,波长、幅值和/或能量)。在一些实施方式中,例如,激发模块1860可以包括一系列的led,其各自构造成产生具有与由其它led产生的光束的波长不同的波长的光束。
检测模块1850构造成接收一系列的发射光束(和/或光学信号,图34中未示出)。因此,检测模块1850可以包括任何适合的光检测器,例如光学检测器、光敏电阻、光生伏打电池、光敏二极管、光电管、ccd相机等。发射光束可以通过任何适合的光源产生,例如通过激发样品s的成分。在一些实施方式中,检测模块1850可以构造成选择性地接收每道发射光束而不管每道光束是否具有与其它发射光束中的每道光束相同的特性(例如,波长、幅值和/或能量)。然而,在其它实施方式中,检测模块1850可以构造成基于光束的特定特性(例如,波长、幅值和/或能量)选择性地接收每道发射光束。例如,在一些实施方式中,检测模块1850可以包括一系列的光检测器,所述一系列的光检测器各自构造成接收具有与由其它光检测器接收的光束的的波长不同的波长的光束。
如图34中所示,第一光学构件1831和第二光学构件1832联接至光学组件1800。以此方式,成系列的激发光束中的每道光束可以被传送到反应容积1713中和/或反应容器260的部分261中,并且可以从反应容积1713和/或反应容器260的部分261中接收成系列的发射光束中的每道光束。更具体地,第一光学构件1831联接至激发模块1860,使得由激发模块1860产生的成系列的激发光束可以传送到反应容积1713中和/或反应容器260的部分261中。类似地,第二光学构件1832联接至检测模块1850,使得可以从反应容积1713和/或从反应容器260的部分261接收多道发射光束中的每道发射光束。
由激发模块1860产生的成系列的光束通过第一光学构件1831、并沿第一光路1806传送到反应容积1713中和/或反应容器260的部分261中。由此,由激发模块1860产生的成系列的光束中的每道光束在基本上恒定的位置处传送到反应室1713和/或反应容器260的部分261中。类似地,由检测模块1850接收的成系列的光束从反应容积1713和/或反应容器260的部分261由第二光学构件1832沿第二光路1807接收。由此,由检测模块1850接收到的成系列的光束中的每道光束在基本上恒定的位置处从反应容积1713和/或反应容器260的部分261接收。通过在反应容积1713的恒定的位置处分别传送激发光束和接收发射光束,能够减少与从多个不同的位置传送激发光束和/或从多个不同的位置接收发射光束相关联的多通道分析内的检测变动。
此外,通过在块体1710内包括第一光学构件1831和第二光学构件1832,第一光学构件1831(和第一光路1806)的位置和/或第二光学构件1832(和第二光路1807)的位置相对于反应容积1713是恒定的。这种布置通过最小化和/或消除第一光学构件1831、第二光学构件1832和/或反应容积1713之间的相对运动也可以减少与光路和/或光学构件相关联的测试间的检测变动。
在一些实施方式中,成系列的激发光束可以顺序地传送到反应容积1713中,并且成系列的发射光束能够顺序地从反应容积1713中接收。例如,在一些实施方式中,激发模块1860可以以顺序(或分时段)的方式产生各自具有不同波长的一些列的光束。每道光束被传送到反应容积1713,在反应容积1713中光束可以例如激发容纳在反应容器260内的样品s。类似地,在这种实施方式中,照射光束以顺序(或分时段)的方式产生(由于样品s内的某些分析物和/或靶的激发)。由此,检测模块1850可以以顺序(或分时段)的方式接收具有不同波长的一系列的光束。以此方式,仪器1802能够可以用来检测样品s内的多种不同的分析物和/或靶。
尽管设置在块体1710内的第一光学构件1831的一部分以及设置在块体1710内的第二光学构件1832的一部分在图34中示出为基本上平行和/或在相同的平面内,但在其它实施方式中,块体可以包括相对于第二光学构件处于任何位置和/或方向的第一光学构件。类似陈述地,尽管第一光路1806在图34中示出为基本上平行于第二光路1807和/或处于与第二光路1807相同的平面内,但在其它实施方式中,仪器可以构造成产生相对于第二光路处于任何位置和/或方向的第一光路。
例如,图35示出根据实施方式的仪器2002的一部分的局部剖视的示意性图示。仪器2002包括块体2710、第一光学构件2831、第二光学构件2832和光学组件(图35中未示出)。块体2710限定反应容积2713,该反应容积2713构造成接纳容纳样品s的反应容器260的至少一部分261。反应容器260可以为用于以允许与样品s相关联的反应发生并允许监测这种反应的方式容纳样品s的任何适合的容器,如本文中描述的。在一些实施方式中,例如,反应容器260可以是pcr小瓶、试管等。此外,在一些实施方式中,反应容器260的至少部分261可以是基本上透明的,以允许光学监测在其内发生的反应。
块体2710可以为促进、产生、支持和/或加快与反应容器260中的样品s相关联的反应的任何适合的结构和/或可以联接至用于促进、产生、支持和/或加快与反应容器260中的样品s相关联的反应的任何适合的机构。例如,在一些实施方式中,块体2710可以联接至和/或可以包括用于对反应容器260中的样品s进行循环加热的机构。以此方式,块体2710可以产生样品s的热诱导反应,例如pcr过程。在其它实施方式中,块体2710可以联接至和/或可以包括用于将一种或多种物质引入到反应容器260中以产生与样品s相关联的化学反应的机构。
反应容积2713可以具有用于容纳反应室260的部分261的任何适合的尺寸和/或形状。如图35中所示,反应容积2713限定纵向轴线la并且当部分261设置在反应容积2713内时反应容积2713基本上围绕反应室260的部分261。以此方式,由块体2710或附接至块体2710的任何机构提供至样品s的任何刺激(例如,加热或制冷)可以以空间上基本上均匀的方式提供。
如图35中所示,第一光学构件2813设置成至少部分地位于块体2710内,使得第一光学构件2813限定第一光路2806并且与反应容积2713光学连通。以此方式,光束(和/或光学信号)经由第一光学构件2831可以在反应容积2713与块体2710的外部区域之间传送。第一光学构件2831可以为本文中所示出和描述的类型的、可以通过其或从其传送光束的任何适合的结构、装置和/或机构。在一些实施方式中,第一光学构件2831可以为用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。
第二光学构件2832设置成至少部分地位于块体2710内,使得第二光学构件2832限定第二光路2807并且与反应容积2713光学连通。以此方式,光束(和/或光学信号)可以经由第二光学构件2832在反应容积2713与块体2710的外部区域之间传送。第二光学构件2832可以为本文中所示出和描述的类型的、可以通过其或从其传送光束的任何适合的结构、装置和/或机构。在一些实施方式中,第二光学构件2832可以为用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。
如上所述,第一光学构件2831和第二光学构件2832联接至光学组件(图35中未示出)。光学组件可以产生一道或多道激发光束,并且可以检测一道或多道发射光束。由此,一道或多道激发光束可以被传送到反应容积2713和/或反应容器260中,并且一道或多道发射光束可以从反应容积2713和/或反应容器260的部分261中接收。更具体地,第一光学构件2831可以将激发光束从光学组件传送到反应容积2713中,以激发容纳在反应容器260内的样品s的一部分。类似的,第二光学构件2832可以将由样品s内的分析物或其它靶产生的发射光束从反应室2713传送至光学组件。以此方式,光学组件可以监测发生在反应容器260内的反应。
如图35中所示,第一光学构件2831的一部分和第一光路2806基本上设置在第一平面pxy内。第一平面pxy基本上平行于反应容积2713的纵向轴线la和/或包括反应容积2713的纵向轴线la。然而,在其它实施方式中,第一平面pxy无需基本上平行于反应容积2713的纵向轴线la和/或包括反应容积2713的纵向轴线la。第二光学构件2832的一部分和第二光路2807基本上设置在第二平面pyz内。第二平面pyz基本上平行于反应容积2713的纵向轴线la和/或包括反应容积2713的纵向轴线la。然而,在其它实施方式中,第二平面pyz无需基本上平行于反应容积2713的纵向轴线la和/或包括反应容积2713的纵向轴线la。此外,如图35中所示,第一光路2806和第二光路2807限定大于约75度的偏移角θ。更具体地,第一光路2806和第二光路2807限定在从基本上平行于反应容积2713的纵向轴线la的方向(即,在基本上正交于第一平面pxy和第二平面pyz的平面内)观察时大于约75度的偏移角θ。以类似的方式,第一光学构件2831和第二光学构件2832限定大于约75度的偏移角θ。这种布置使由第二光学构构件2832(即,“检测”光学构件)接收的激发光束的量最小化,由此,提高了光学检测和/或光学监测的准确性和/或灵敏度。
在一些实施方式中,仪器2002的一部分可以产生反应容积2713内的第一光路2806和第二光路2807,使得偏移角θ介于约75度与约105度之间。在一些实施方式中,仪器2002的一部分可以产生反应容积2713内的第一光路2806和第二光路2807,使得偏移角θ为约90度。
尽管仪器2002的一部分示出为产生基本上平行并且在反应容积2713内的点pt处相交的第一光路2806和第二光路2807,但在其它实施方式中,块体2713、第一光学构件2831和/或第二光学构件2832可以构造成使得第一光路2806与第二光路2807不平行和/或不相交。例如,在一些实施方式中,第一光路2806和/或第一光学构件2831可以与第二光路2807和/或第二光学构件2831平行且偏移(即,倾斜)。类似陈述地,在一些实施方式中,第一光学构件2831和第二光学构件1832可以与由块体2710限定的基准平面分别间隔开距离y1和距离y2,其中y1不同于y2。由此,沿着纵向轴线la的、第一光学构件2831和/或第一光路2806与反应容积2713相交的位置不同于沿着纵向轴线la的、第二光学构件2832和/或第二光路2807与反应容积2713相交的位置。以此方式,第一光路2806和/或第一光学构件2831可以相对于第二光路2807和/或第二光学构件2831倾斜。
在其它实施方式中,由纵向轴线la与第一光路2806和/或第一光学构件2831限定的角度γ1可以不同于由纵向轴线la与第二光路2807和/或第二光学构件2832限定的角度γ2(即,第一光路2806可以不平行于第二光路2807)。在又一实施方式中,块体2713、第一光学构件2831和/或第二光学构件2832可以构造成使得第一光路2806与第二光路2807在反应容积2713外部的位置处相交。
距离y1和距离y2可以为如下的任何适合距离,该任何适合距离使得第一光学构件2831和第二光学构件1832构造成在反应容器260的所需部分中分别产生和/或限定第一光路2806和第二光路2807。例如,在一些实施方式中,距离y1可以为如下距离,该距离使得当反应容器260设置在块体2710内时第一光学构件2831和/或第一光路2806在样品s的填充线fl位置下方的位置处进入反应容积2713和/或与反应容积2713相交。以此方式,由第一光学构件2831传送的激发光束将进入填充线下方的样品s中。这种布置可以通过减少因经由反应容器的顶部空间(即,反应容器260的在填充线lf上方的基本上不含样品s的部分)传输激发光束而可能发生的激发光束减弱来改善样品内分析物的光学检测。然而,在其它实施方式中,距离y1可以是如下距离,该距离使得当反应容器260设置在块体2710内时第一光学构件2831和/或第一光路2806在样品s的填充线fl位置上方的位置处进入反应容积2713。
类似地,在一些实施方式中,距离y2可以为如下距离,该距离使得当反应容器260设置在块体2710内时第二光学构件2832和/或第二光路2807在样品s的填充线fl位置下方的位置处进入反应容积2713和/或与反应容积2713相交。以此方式,由第二光学构件2832接收的发射光束将离开填充线下方的样品s。这种布置可以通过减少因经由反应容器的顶部空间接收发射光束而可能发生的发射光束减弱来改善样品内分析物的光学检测。然而,在其它实施方式中,距离y2可以是如下距离,该距离使得当反应容器260设置在块体2710内时第二光学构件2832和/或第二光路2807在样品s的填充线fl位置上方的位置处进入反应容积2713和/或与反应容积2713相交。
图36至图70示出构造成操纵、致动一系列的药筒和/或与一系列的药筒相互作用以对药筒内的测试样品执行核酸分离和扩增过程的仪器3002和/或仪器的一部分的各种视图。药筒可以包括本文中示出和描述的任何药筒,例如药筒6001。该系统可以用于许多不同的测定,例如,快速检测来自鼻咽样本的流感(flu)a、flub和呼吸道合胞体病毒(rsv)。仪器3002示出为不包括壳体3002和/或仪器3002的某些部分,以更清晰地示出其内的部件。例如,图47示出不带光学组件3800的仪器3002。
如图36中所示,仪器3002包括机架和/或框架3300、第一致动器组件3400、样品传送组件3500、第二致动器组件3600、加热器组件3700和光学组件3800。框架3300构造成容置、容纳本文中描述的仪器3002的每个部件和/或组件和/或为其提供安装。第一致动器组件3400构造成致动药筒的分离模块(例如,分离模块6100)的致动器或传送机构(例如,致动器或传送机构6166),以将一种或更多种试剂和/或物质运送到分离模块内的裂解室中。传送致动器组件3500构造成致动传送组件(例如,传送组件6140a),以在分离模块(例如,分离模块7100)内的各个室和/或容积之间传送样品的一部分。第二致动器组件3600构造成致动分离模块(例如,分离模块6100)的混合机构(例如,混合机构6130a)和/或洗涤缓冲液模块(例如,洗涤缓冲液模块7130a)和/或pcr模块(例如,pcr模块6200),以将一种或更多种试剂和/或物质运送到分离模块和/或pcr模块内的室内和/或在分离模块和/或pcr模块的室内混合。加热器组件3700构造成加热药筒的一个或多个部分(例如,pcr小瓶7260、基底7220和/或与壳体7110的邻近裂解室7114的区域)以促进和/或利于药筒内的过程(例如,以加快、促进和/或产生“热启动”过程、加热的裂解过程和/或pcr过程)。光学组件3800构造成监测在药筒内发生的反应。更具体地,光学组件3800构造成检测药筒中测试样品内的一种或多种不同的分析物和/或靶。这些组件中的每个组件在以下分开地讨论,接着是可以由仪器3002执行的各种方法的描述。
如图36中所示,框架3300包括基座框架3310、前构件3312、两个侧构件3314和后构件3320。基座构件3310支持本文中描述的功能性组件,并包括六个安装或支撑腿。在一些实施方式中,支撑腿能够被调整,以允许仪器3302在被安装和/或安置在实验台上时被水平地对准。后构件3320联接至基座构件3310并且构造成支撑或保持动力供给组件3361。后构件3320还可以为与仪器3302的操作相关的任何其它部件——例如处理器、控制元件(例如,马达控制器、加热系统控制器等)、通信接口、冷却系统——提供安装支撑。图71至图73为仪器3002的控制和计算机系统的方框图。
侧构件3314中的每个侧构件包括上部部分3316和下部部分3315。前构件3312联接至每个侧构件3314并限定开口,在该开口内可以设置用于处理的容纳多个测定药筒的盒3350。在一些实施方式中,盒3350可以被构造成容纳本文中所示出和描述的类型(例如在图36中示出为药筒6001)的六个药筒。在使用中,容纳多个药筒的盒3350设置在仪器3002内并且在分离和/或扩增过程期间相对于机架3300维持在固定位置。由此,容纳样品的药筒不在各个站之间移动以进行分析。反而,如本文中所述的,样品、试剂和/或其它物质通过如本文中所述的仪器3002而在药筒的各个部分内运送、处理和/或操纵。尽管仪器3002示出为构造成接纳容纳六个药筒的一个盒3350,但在其它实施方式中,仪器可以被构造成接纳任何数目的盒3350,盒3350容纳任何数目的药筒。
图37至图40示出仪器3002的第一致动器组件3400的各个视图。第一致动器组件3400构造成致动和/或操纵药筒的分离模块(例如,分离模块6100)的传送机构和/或试剂致动器(例如,试剂致动器6166a、6166b、6166c和6166d)以将一种或更多种试剂和/或物质运送到分离模块内的裂解室中。特别地,第一致动器组件3400可以致动来自设置在盒3350内的每个药筒的试剂致动器中的第一试剂致动器(例如,试剂致动器6166d),并随后在不同的时间致动来自每个药筒的试剂致动器中的第二试剂致动器(例如,试剂致动器6166c)。
第一致动器组件包括接合杆3445、由框架组件3410支撑的第一(或x轴)马达3440和第二(或y轴)马达3441。如图38和图40中所示,接合杆3445包括一系列的凸起3346a、3346b、3346c、3346d、3346e和3346f。每个凸起构造成接合分离模块(例如,分离模块6100)的一个或多个试剂致动器(例如,试剂致动器6166a)、设置在分离模块(例如,分离模块6100)的一个或多个试剂致动器(例如,试剂致动器6166a)内和/或致动分离模块(例如,分离模块6100)的一个或多个试剂致动器(例如,试剂致动器6166a),其中该分离模块(例如,分离模块6100)设置在仪器3002内。在一些实施方式中,接合杆3445和/或凸起(例如,凸起3346a)可以包括保持机构(例如,凸起、卡环等),该保持机构构造成保持致动器(例如,试剂致动器6166a)的凸起和/或开口以便于在分离模块内往复移动试剂致动器。
框架组件3410包括第一轴(或x轴)安装框架3420,该第一轴安装框架3420可移动地联接至第二轴(或y轴)安装框架3430。特别地,第一轴安装框架3420可以沿着y轴相对于第二轴安装框架3430移动,如由图37中箭头aaa所示。类似陈述地,第一轴安装框架3420可以沿着“对准方向”(即,沿着y轴)相对于第二轴安装框架3430移动,以便于接合杆3445和/或凸起(例如凸起3346a)与所需系列的致动器和/或传送机构对准。
第一轴安装框架3420为第一(或x轴)马达3440提供支撑,该第一轴安装框架3420构造成沿着x轴移动接合杆3445和/或凸起(例如,凸起3346a),如由图37中箭头bbb所示的。类似陈述地,第一轴马达3440联接至第一轴安装框架3420,并且构造成沿着“致动方向”(即,沿着x轴)移动安装杆3445和/或凸起(例如凸起3346a)以致动所需系列的致动器和/或传送机构。接合杆3445的运动由两个x轴引导轴3421来引导,每个x轴引导轴3421可移动地设置在相对应的支承件3422内。支承件3422相对于第一轴安装框架3420和/或第一马达3440由支承件安装构件3423来定位。
第二轴安装框架3430联接至框架组件3300的两个侧框架构件3314且位于其之间。第二轴安装框架3430为第二(或y轴)马达3441和第一轴安装框架3420提供支撑。第二马达3441构造成沿着y轴(或沿着对准方向)移动第一轴安装框架3420、并因而移动接合杆3445,如图37中由箭头bbb所示的。以此方式,接合杆3445和/或凸起(例如,凸起3346a)可以在对致动器和/或传送机构进行致动之前与所需系列的致动器和/或传送机构对准。第一轴安装框架3420通过一对支承块3432联接至第二轴安装框架3430,该对支承块3432围绕相对应的一对y轴引导轴3431可滑动地设置。
在使用中,第一致动组件3400可以顺序地致动设置在仪器3001内的一组药筒(例如,药筒6001)的一系列的传送机构和/或试剂致动器(例如,致动器6166a、6166b、6166c和6166d)。首先,通过沿着对准方向(即,沿着y轴)移动第一框架构件3420可以使接合杆3445与所需的传送机构和/或试剂致动器(例如,致动器6166d)对准。接合杆3445可以随后沿着致动方向(即,沿着x轴方向)移动以致动来自每个药筒的所需的传送机构和/或试剂致动器(例如,致动器6166d)。以此方式,第一致动器组件3400可以以并行(或同时)的方式致动和/或操纵来自仪器3002内设置的每个药筒的试剂致动器。然而,在其它实施方式中,致动器组件3400和/或接合杆3445可以构造成以顺序的(或连续的)方式顺序地致动设置在仪器3002内的每个药筒的相对应的试剂致动器。
第一致动器组件3400可以通过沿着x轴在第一方向上移动接合杆3445来致动所需的传送机构和/或试剂致动器。然而,在其它实施方式中,第一致动器组件3400可以通过沿着x轴往复移动(即,在第一方向和第二方向上交替地移动接合杆3445)接合杆3445而致动所需的传送机构和/或试剂致动器。当所需的传送机构和/或试剂致动器已被致动时,第一致动器组件3400可以以如上述的类似方式致动另一传送机构和/或试剂致动器(例如致动器6166c)。
尽管第一致动器组件3400示出和描述为致动传送机构和/或试剂致动器,但在其它实施方式中,第一致动器组件3400可以致动本文中描述的任何药筒的任何适合的部分。例如,在一些实施方式中,第一致动器部件3400可以致动、操纵和/或移动超声转换器以促进超声裂解。
图41至图46示出了仪器3002的传送致动器组件3500的各种视图。传送致动器组件3500构造成致动和/或操纵传送组件或机构,例如,以上参照图20和图21示出和描述的传送组件6140。特别地,传送致动器组件3500可以致动来自盒3350内设置的每个药筒的第一个传送组件(例如,传送组件6140a),并且随后在不同的时间致动来自每个药筒的第二个传送组件(例如,传送组件6140b)。
传送致动器组件3500包括一系列的致动器轴3510。尽管传送致动器组件3500包括六个致动器轴,但图41至图46中仅标出一个。每个致动器轴3510构造成接合分离模块(例如,分离模块6100)的一个或多个传送组件(例如,传送组件6140a)、设置在分离模块(例如,分离模块6100)的一个或多个传送组件(例如,传送组件6140a)内和/或致动分离模块(例如,分离模块6100)的一个或多个传送组件(例如,传送组件6140a),该分离模块(例如,分离模块6100)设置在仪器3002内。如图44中所示,每个致动器轴3510具有第一端部3511和第二端部3512。第一端部3511联接至传动齿轮3513(参见图41至图42),该传动齿轮3513进而由蜗杆驱动轴3541驱动。如图41和图42所示,转动位置指示器3542联接至致动器轴3510中的一个致动器轴的第一端部3511。转动位置指示器3542限定狭槽和/或开口3543,该狭槽和/或开口3543的旋转位置可以(例如,通过光学感测机构)感测到,以提供关于致动器轴3510的转动位置的反馈。
每个轴3510的第二端部3512包括接合部3514,该接合部3514构造成被接纳在设置于仪器3002内的药筒(例如,药筒6001)的传送组件(例如,传送组件6140a)内和/或与其接合。以此方式,接合部3514可以操纵和/或致动传送组件以便于传送药筒内样品的一部分,如上所述的。接合部3514的形状对应于传送组件的一部分(例如,由可移动构件6146限定的管腔6149)的形状,使得致动器轴3510的转动引起一部分传送组件的转动。特别地,如图44中所示,接合部具有八边形形状。在一些实施方式中,接合部3514可以包括保持机构(例如,凸起、卡环等),该保持机构构造成保持传送组件的凸起和/或开口,以便于在分离模块内往复移动传送组件的一部分。
接合部3514限定管腔3515,在该管腔3515内可以设置有磁体(未示出)。以此方式,致动器轴3510可以对设置在药筒(例如,药筒6001)内的内含物(即,磁珠)的一部分产生和/或施加力(即,磁力),以便于通过传送组件传送样品的一部分,如以上所述的。
致动器轴3510由第一(或x轴)马达5380、第二(或y轴)马达3560和第三(或旋转)马达3540移动。如在以下更详细地描述的,x轴马达3580由支撑框架3571支撑,y轴马达3560由接合框架组件3550支撑,并且,旋转马达3540由旋转框架组件3530支撑。
旋转框架组件3530为旋转马达3540提供支撑,该旋转马达3540构造成绕y轴转动致动器轴3510,如由图41中箭头ccc所示的。类似陈述地,旋转马达3540联接至旋转框架组件3530,并且构造成沿着“致动方向”(即,绕y轴)转动致动器轴3510以致动所需系列的传送组件。旋转框架组件3530包括旋转板3531、一对涡杆驱动支承座3533、以及蜗杆驱动轴3541。蜗杆驱动轴3541通过带轮组件联接至旋转马达3540,并且由两个涡杆驱动支承座3533来支撑。蜗杆驱动轴3541与每个致动器轴3510的驱动齿轮3513接合。因此,当蜗杆驱动轴3541在第一方向上(即,绕z轴)旋转时,每个致动轴3510在第二方向(即,如由图41中箭头ccc所示地绕y轴)旋转。
旋转框架组件3530也包括y轴位置指示器3534,该y轴位置指示器3534可滑动地设置在接合框架组件3550上的一对相对应的滑动构件3553内。以此方式,当旋转框架组件3530沿着y轴(例如,沿接合方向)平移时,如由图41中箭头ddd所示,y轴位置指示器3534和相对应的滑动构件3553可以引导线性运动和/或提供关于旋转框架组件3530的位置的反馈。
接合框架组件3550为y轴马达3560提供支撑,该y轴马达3560构造成沿着y轴移动框架组件3530、并因此移动致动轴3510,如由图41中箭头ddd所示的。类似陈述地,y轴马达3560联接至接合框架组件3550,并且构造成沿“接合方向”(即,沿着y轴)移动致动器轴3510,以致动所需系列的传送机构。接合框架组件3550包括支撑框架3551,该支撑框架3551为驱动连杆3561提供支撑(该驱动连杆3561将y轴马达的旋转运动转化为旋转框架组件3530的线性运动)。旋转框架组件3530的运动由两个y轴引导轴3552引导,每个y轴引导轴3552可移动地设置在相对应的支承件3554内。轴承3554联接至旋转板3531,如图43中所示。
支撑框架3571联接至框架组件3300的两个侧框架构件3314的下端部3315且位于其之间。支撑框架3571为x轴马达3580和接合框架组件3550提供支撑。x轴马达3580构造成沿着x轴(或沿着对准方向)移动接合框架组件3550、并因而移动致动轴3510,如由图41中箭头eee所示的。以此方式,致动器轴3510可以在致动传送机构之前与所需系列的传送机构对准。支撑框架3571通过一对支承座3573联接至接合框架组件3550,该对支承座3573绕相对应的一对x轴引导轴3572可滑动地设置。
在使用中,传送致动器组件3500可以顺序地致动设置在仪器3001内的一组药筒(例如药筒6001)的一系列的传送机构(例如传送组件6140a、6140b和6166c)。首先,通过沿着对准方向(即,沿着x轴)移动接合框架组件3550可以使致动器轴3510与所需的传送机构对准。致动器轴3510可以随后沿着接合方向(即,沿着y轴方向)移动以接合来自每个药筒的所需的传送机构(例如,传送组件6140a)。致动器轴3510可以随后沿着致动方向(即,绕y轴旋转)移动以致动来自每个药筒的所需的传送机构(例如,传送组件6140a)。以此方式,传送致动器组件3500可以以并行(或同时)的方式致动和/或操纵来自仪器3002内设置的每个药筒的传送机构。然而,在其它实施方式中,传送致动器组件3500和/或致动轴3510可以构造成以顺序的(或连续的)方式顺序地致动仪器3002内设置的每个药筒的相对应的传送机构。
图47至图51示出仪器3002的第二致动器组件3600的各种视图。第二致动器组件3600构造成致动和/或操纵本文中所示出和描述的任何药筒的传送机构(例如,传送机构7235)、洗涤缓冲液模块(例如,洗涤缓冲液模块7130a)、混合机构(例如、混合机构6130a)和/或试剂模块(例如,试剂模块7270a)。特别地,第二致动器组件3600可以致动来自盒3350内设置的每个药筒的第一个传送机构、混合机构(例如,混合机构6130a)等,并且随后在不同的时间致动来自每个药筒的第二个传送机构、混合机构(例如,混合机构6130b)等。
第二致动器组件3600包括接合杆3645、由框架组件3610支撑的第一(或x轴)马达3640和第二(或y轴)马达3641。如图48中所示,接合杆3645包括一系列的凸起3346。尽管接合杆3645包括六个凸起(一个凸起对应于盒3350内的每个药筒),但仅一个凸起3346被标记出。每个凸起构造成接合药筒的一个或多个传送机构(例如,传送机构7235)、洗涤缓冲液模块(例如,洗涤缓冲液模块7130a)、混合机构(例如,混合机构6130a)和/或试剂模块(例如,试剂模块7270a),设置在药筒的一个或多个传送机构(例如,传送机构7235)、洗涤缓冲液模块(例如,洗涤缓冲液模块7130a)、混合机构(例如,混合机构6130a)和/或试剂模块(例如,试剂模块7270a)内,操纵和/或致动药筒的一个或多个传送机构(例如,传送机构7235)、洗涤缓冲液模块(例如,洗涤缓冲液模块7130a)、混合机构(例如,混合机构6130a)和/或试剂模块(例如,试剂模块7270a),其中该药筒设置在仪器3002内。在一些实施方式中,接合杆3645和/或凸起3346可以包括保持机构(例如,凸起、卡环等),该保持机构构造成保持致动器的一部分(例如,以上参照图27和图28示出和描述的致动器7150a的接合部7153a)以便于在药筒的一部分往复移动致动器。
框架组件3610包括第二轴(或y轴)安装框架3630,该第二轴安装框架3630可移动地联接至第一轴(或x轴)安装框架3620。特别地,第二轴安装框架3630可以沿着x轴相对于第一轴安装框架3620移动,如由图47中箭头ggg所示的。类似陈述地,第二轴安装框架3630可以沿“对准方向”(即,沿着x轴)相对于第一轴安装框架3620移动,以便于使接合杆3645和/或凸起3346与所需系列的传送机构、混合机构、试剂模块等对准。
第二轴安装框架3620为第二(或y轴)马达3641提供支撑,该第二马达3641构造成沿着y轴移动接合杆3645和/或凸起3346,如由图47中箭头fff所示的。类似陈述地,第二轴马达3641联接至第二轴安装框架3620,并且构造成沿“致动方向”(即,沿着y轴)移动接合杆3645和/或凸起3346,以致动所需系列的传送机构、混合机构、试剂模块等。接合杆3645的运动由两个y轴引导轴3631引导,每个y轴引导轴3631可移动地设置在联接于第二轴安装框架3620的相对应的支承件内。
第一轴安装框架3630联接至框架组件3300的两个侧框架组件3314的上部3316并位于其之间。第一轴安装框架3630为第一(或x轴)马达3640和第二轴安装框架3620提供支撑。第一马达3640构造成沿着x轴(或沿着对准方向)移动第二轴安装框架3620、并因此移动接合杆3645,如由图47中箭头ggg所示的。以此方式,接合杆3645和/或凸起3346a可以在对这种机构进行致动之前与所需系列的传送机构、混合机构、试剂模块等对准。第二轴安装框架3620通过一对支承座3622联接至第一轴安装框架3630,该对支承座3622绕相对应的一对x轴引导轴3631可滑动地设置。第一(或x轴)马达3640通过安装构件3624(参见例如图51)联接至第二轴安装框架3620。
在使用中,第二致动器组件3600可以顺序地致动设置在仪器3001内的一组药筒(例如,药筒6001)的一系列的传送机构(例如,传送机构7235)、洗涤缓冲液模块(例如,洗涤缓冲液模块7130a)、混合机构(例如、混合机构6130a)和/或试剂模块(例如,试剂模块7270a)。首先,可以通过沿着对准方向(即,沿着x轴)移动第二框架构件3630而使接合杆3645与所需的机构(例如,混合机构6130a)对准。接合杆3645可以随后沿着致动方向(即,沿着y轴方向)移动以致动来自每个药筒的所需的机构(例如,混合机构6130a)。以此方式,第二致动器组件3600可以以并行(或同时)的方式致动和/或操纵来自仪器3002内设置的每个药筒的传送机构、洗涤缓冲液模块、混合机构和/或试剂模块。然而,在其它实施方式中,第二致动器组件3600和/或接合杆3645可以构造成以顺序的(或连续的)方式顺序地致动仪器3002内设置的每个药筒的相对应的机构。
第二致动器组件3600可以通过沿着y轴在第一方向上移动接合杆3645而致动所需的机构。然而,在其它实施方式中,第二致动器组件3600可以通过沿着y轴往复移动接合杆3645(即,在第一方向和第二方向上交替地移动接合杆3645)而致动所需的传送机构或试剂致动器。当所需的机构已被致动时,第二致动器组件3600可以以如上所述的类似方式致动另一机构和/或致动器(例如,混合机构6130b)。
尽管第二致动器组件3600示出和描述为致动传送机构和/或试剂致动器,但在其它实施方式中,第二致动器组件3600可以致动本文中描述的任何药筒的任何适合的部分。例如,在一些实施方式中,第二致动器组件3600可以致动、操纵和/或移动超声转换器以便于将超声能传输到药筒的一部分中。
图52至图63示出仪器3002的加热器组件3700的各种视图。加热器组件3700构造成加热药筒的一个或多个部分(例如,pcr小瓶7260、基底7200和/或壳体7110的邻近裂解室7114的区域),以加快或促进药筒内的过程(例如,加快、促进和/或产生用于pcr的“热启动”过程、加热裂解过程和/或热循环过程)。特别地,加热器组件3700可以致动和/或加热盒3350内设置的每个药筒的第一部分(例如,pcr小瓶6260),并且随后在不同的时间致动和/或加热来自每个药筒的第二部分(例如,分离模块6100的邻近裂解室6114的部分)。
加热器组件3700包括一系列的接收块3710(一个接收块对应于盒3350内的每个药筒)、定位组件3770、第一加热模块3730、第二加热模块3750和第三加热模块3780。接收块3710构造成接纳药筒的反应室的至少一部分,比如药筒6001的pcr小瓶6260。如图53至图56所示,接收块3710包括安装表面3714并限定反应容积3713。反应容积3713的尺寸和/或形状基本上对应于药筒6001的pcr小瓶6260的尺寸和/或形状。如图54和图56所示,反应室3713限定纵向轴线la,并且当pcr小瓶6260设置在反应容积3713内时基本上围绕pcr小瓶6260的一部分。以此方式,通过加热器组件3700提供给pcr小瓶6260内的样品的任何刺激(例如,加热或冷却)可以以基本上空间上均匀的方式提供。此外,如图56中所示,接收块3710的一部分——该部分限定反应容积3713——的侧壁具有基本上一致的壁厚。这种布置允许反应容积3713与加热器组件3700的剩余部分之间的热传递以空间上基本上均匀的方式发生。
接收块3710通过夹持块3733(参见例如图57)联接至安装块3734(参见例如图58),使得热电装置3731与安装表面3714接触。以此方式,反应容积3713和容纳在该反应容积3713中的样品可以被循环地加热以产生样品s的热诱导反应,例如pcr过程。
每个接收块3710限定第一(或激发)管腔3711、第二(或发射)管腔3712和第三(或温度监测)管腔3715。邻近pcr小瓶可以经由第三管腔3715设置有热电耦或其它适合的温度测量装置。如图52中所示,激发纤维3831设置成至少部分地位于第一管腔3711内,使得激发纤维3831和/或第一管腔3711限定第一光路3806并且与反应容积3713光学连通。以此方式,光束(和/或光学信号)可以经由激发纤维3831和/或第一管腔3711而在反应容积3713与块体3710的外部区域之间传送。激发纤维3831可以为本文中所示出的和描述的类型的任何适合的结构、装置和/或机构,通过其或从其可以传送光束。在一些实施方式中,激发纤维3831可以为用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。
检测纤维3832设置至少部分地位于第二管腔3712内,使得检测纤维3832和/或第二管腔3712限定第二光路3807并且与反应容积3713光学连通。以此方式,光束(和/或光学信号)可以经由检测纤维3832和/或第二管腔3712而在反应容积3713与块体3710的外部区域之间传送。检测纤维3832可以为本文中所示出和描述的类型的任何适合的结构、装置和/或机构,通过其或从其可以传送光束。在一些实施方式中,检测纤维3832可以为用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。
如以下所述,激发纤维3831和检测纤维3832联接至光学组件3800。光学组件3800可以产生一道或多道激发光束,并且可以检测一道或多道发射光束。由此,激发纤维3831可以将激发光束从光学组件传送到反应容积3713中,以激发容纳在pcr小瓶6260内的样品s的一部分。类似地,检测纤维3832可以将由样品s内的分析物或其它靶产生的发射光束从pcr小瓶6260传送到光学组件3800。
如图55中所示,第一管腔3711和第二管腔3712限定约90度的偏移角度θ。类似陈述地,第一光路3806和第二光路3807限定约90度的偏移角度θ。更具体地,当在基本上平行于反应容积3713的纵向轴线la的方向上观察时,第一光路3806和第二光路3807限定约90度的偏移角度θ。以类似的方式,分别设置在第一管腔3711和第二管腔3712内的激发纤维3831和检测纤维3832限定约90度的偏移角度θ。这种布置使由检测纤维3832接收的激发光束的量最小化,从而提高了光学检测和/或监测的准确性和/或灵敏性。
在一些实施方式中,第一管腔3711和第二管腔3712可以定位成使得偏移角度θ大于约75度。在其它实施方式中,第一管腔3711和第二管腔3712可以定位成使得偏移角度θ介于约75度与约105度之间。
如图54中所示,第一管腔3711的中心线与第二管腔3712的中心线基本上平行且偏移(即倾斜)。类似陈述地,激发纤维3831(并且因而第一光路3806)倾斜于检测纤维3832(并且因而第二光路3807)。换言之,第一管腔3711(和/或激发纤维3831)和第二管腔3712(和/或检测纤维3832)可以与由接收块3710限定的基准平面分别间隔开距离y1和距离y2,其中y1不同于y2。因此,沿纵向轴线la的、在其上激发纤维3831和/或第一光路3806与反应容积3713相交的位置不同于沿纵向轴线la的、在其上检测纤维3832和/或第二光路3807与反应容积3713相交的位置。以此方式,第一光路3806和/或激发纤维3831可以相对于第二光路3807和/或第二光学构件3831倾斜。
距离y1和距离y2可以为如下的任何适合的距离,该距离使得激发纤维3831和检测纤维3832构造成分别在pcr小瓶6260的所需部分中产生和/或限定第一光路3806和第二光路3807。例如,在一些实施方式中,距离y1可以为如下的距离,该距离使得第一管腔3711、激发纤维3831和/或第一光路3806在设置于接收块3710内的pcr小瓶6260内的样品的填充线的位置下方的位置处进入反应容积3713和/或与反应容积3713相交。以此方式,由激发纤维3831传送的激发光束将进入填充线下方的样品中。然而,在其它实施方式中,距离y1可以是如下的距离,该距离使得第一管腔3711、激发纤维3831和/或第一光路3806在pcr小瓶6260内的样品的填充线的位置上方的位置处进入反应容积3713。
类似地,在一些实施方式中,距离y2可以是如下的距离,该距离使得第二管腔3712、检测纤维3832和/或第二光路3807在设置于接收块3710内的pcr小瓶6260内的样品的填充线的位置下方的位置处进入反应容积3713和/或与反应容积3713相交。然而,在其它实施方式中,距离y2可以是如下的距离,该距离使得第二管腔3712、检测纤维3832和/或第二光路3807在pcr小瓶6260内的样品的填充线的位置上方的位置处进入反应容积3713和/或与反应容积3713相交。
第一加热模块3730包括一系列的热电装置3731(一个热电装置对应于每个药筒和/或每个接收块3710)、安装块3734、一系列的夹持块3733和散热片3732。如图58所示,安装块3734包括第一部分3735和第二部分3737。第一部分3735包括成角度的表面3736,每个热电装置3731联接至成角度的表面3736。以此方式,每个接收块3710通过相对应的夹持块3733联接至安装块3734,使得热电装置3731与接收块3710的安装表面3714接触。
安装块3734的第二部分3737联接至散热片3732。散热片(参见例如图59)可以为用于促进接收块3710与仪器3002的外部区域之间热传递的任何适合的装置。在一些实施方式中,散热片3732可以包括主动地冷却安装块3734(即,移除来自安装块3734的热量)的装置和/或机构。
定位组件3770联接至散热片3732和框架组件3300的一部分,并且构造成在沿着y轴的方向上线性地移动加热器组件3700。由此,当被致动时,定位组件3770可以相对于盒3350和/或其内的药筒移动加热器组件3700,使得pcr小瓶(例如,pcr小瓶6260)设置在接收块3710内,如以上所述的。定位组件3770包括马达3771和连杆组件3772,连杆组件3772构造成将马达3771的旋转运动转化成线性运动。加热器组件3700的运动由y轴引导轴3773引导。
在使用中,第一加热模块3730可以循环地加热设置在仪器3001内的每个药筒的pcr小瓶,以加快容纳在所述pcr小瓶内的内含物的pcr过程和/或混合。在一些实施方式中,第一加热模块3730可以利用任何适合的pcr升温速率(例如,块体3710、pcr小瓶和/或样品的温度的改变率)对本文中所示出和描述的任何pcr小瓶进行热循环。例如,在一些实施方式中,第一加热模块3730可以构造成以每秒8.1摄氏度的pcr升温速率加热接收块体3710和/或pcr小瓶(例如,pcr小瓶7260)。在这种实施方式中,第一加热模块3730可以构造成以每秒-4.8摄氏度的pcr升温速率冷却和/或降低接收块3710和/或pcr小瓶的温度。以此方式,第一加热块体3730、接收块3710和pcr小瓶(例如,pcr小瓶7260)构造成使得由加热器产生的热能的一部分传递至pcr样品。类似陈述地,pcr小瓶将热能的一部分从第一加热模块3730传递至容纳在pcr小瓶内的样品,使得pcr样品以所需的pcr升温速率进行热循环。例如,在一些实施方式中,接收块3710和/或pcr小瓶的每秒8.1摄氏度的pcr升温速率对应于pcr样品的每秒3.85摄氏度的pcr升温速率(升温速率的降低除此之外相关于接收块3710的热质量)。类似地,在一些实施方式中,用于冷却接收块3710和/或pcr小瓶的-4.8摄氏度每秒的pcr升温速率对应于用于冷却pcr样品的每秒-3.57摄氏度的pcr升温速率。
此外,由于每个药筒经由分开的接收块3710被分开的热电装置3731加热,因而在一些实施方式中,第一药筒的热循环可以在与第二药筒的热循环不同的时间点执行。此外,由于每个药筒可以独立于仪器中的其它药筒进行热循环,因而在一些实施方式中,用于第一药筒的热循环方案(例如,热循环事件的时间和温度)可以不同于用于第二药筒的热循环方案。在一些实施方式中,第一加热模块3730不用于热循环,而是保持在恒定的温度,例如用于对rna样品执行反转录的温度。
第二加热模块3750包括一系列的电阻加热器3751(一个电阻加热器对应于每个药筒和/或每个接收块3710)、安装板3754、第一绝缘构件3752和第二绝缘构件3753。如图60中所示,安装板3754包括第一部分3755和第二部分3760。第一部分3755为每个电阻加热器3751提供安装支撑。类似陈述地,每个电阻加热器3731联接至安装板3754。
安装板3754联接至第一加热模块3730的安装块3734,使得第一绝缘构件3752设置在安装块3734与安装板3754的第一部分3755之间,而第二绝缘构件3753设置在安装块3734与安装板3754的第二部分3760之间。以此方式,第二加热模块3750可以基本上独立于第一加热模块3730而起作用。类似陈述地,这种布置减少和/或限制安装板3754与安装块3734之间的热传递。
安装板3754的第一部分3755包括顶表面3758,并且限定凹部3756和一系列的管腔3757(一个管腔对应于盒3350内的每个药筒)。在使用中,当加热器组件3700移动到仪器3002内的每个药筒周围的位置时,每个pcr小瓶被设置穿过相对应的管腔3757并进入由相对应的接收块3710限定的反应容积3713中。由此,在一些实施方式中,当加热器组件3700定位在每个药筒周围时,安装板3754的限定管腔3757的侧壁定位在每个pcr小瓶6260的一部分周围和/或基本上围绕每个pcr小瓶6260的一部分。然而,在其它实施方式中,pcr小瓶6260可以与管腔3757间隔开和/或不驻留于管腔3757内。例如,在一些实施方式中,在当加热器组件3700定位在每个药筒周围时,仅传送端口(比如以上参照图30和图31示出和描述的pcr模块7200的传送端口7229)可以设置在安装板3754的管腔3737内。
如图60中所示,安装板3754的第二部分3760限定一系列的凹部和/或空腔3761(一个凹部和/或空腔对应于盒3350内的每个药筒)。在使用中,当加热器组件3700移动到仪器3002内的每个药筒周围的位置时,药筒的一部分设置在安装板3754的相对应的凹部3761内。更具体地,如图52中所示,分离模块(例如,分离模块6100)的对应于洗脱室6190(在图52中未标出)的一部分设置在相对应的凹部3761内。由此,当加热器部件3700定位在每个药筒周围时,安装板3754的第二部分3760——其限定凹部3761——的侧壁定位在洗脱室6190的一部分周围和/或基本上围绕洗脱室6190的一部分。以此方式,第二加热模块3750可以对每个药筒的洗脱室6190内容纳的样品的一部分进行加热和/或热循环。
在使用中,第二加热模块3750可以加热设置在仪器3001内的每个药筒的一部分以加快、提高和/或促进在药筒内发生的反应过程。例如,在一些实施方式中,第二加热模块3750可以加热pcr模块的基底的一部分(例如,以上参照图29至图31示出和描述的pcr模块7200的基底7220)。在一个实施方式中,完成由第二加热模块3750进行的加热以促进反转录反应或用于“热启动”pcr。
更具体地,在一些实施方式中,第二加热模块3750可以促进与pcr过程相关联的“热启动”方法。热启动方法涉及“热启动酶”(聚合酶)的使用,以降低核酸在扩增反应中的非特异性引发。更具体地,当酶维持处于环境温度(例如,大约50℃以下)下时,会发生非特异性杂交,这可以导致在聚合酶的存在下的非特异性引发。由此,热启动酶为在环境温度下惰性、并且直到被加热至预定的温度才变得活跃的酶。这种预定的温度可以是约40℃、50℃、70℃、或95℃以上的温度。为促进“热启动”方法,第二加热模块3750可以在将混合物添加至pcr小瓶(例如,pcr小瓶7260)之前加热洗脱室(例如,洗脱室7190),以将经洗脱的核酸样品维持在升高温度(例如,处于约40℃、50℃、70℃、或95℃以上的温度)。例如,在一些实施方式中,第二加热模块3750可以将洗脱室7190内的样品的温度维持至介于约50℃与约95℃之间的温度。通过以这种方式加热经洗脱的核酸,可以消除和/或减少在酶的存在下的非特异性杂交和/或错误引发。
反应试剂(例如,以上在图30和图31中示出的试剂模块7270b中容纳的物质r2)可以随后被添加至pcr小瓶(例如,pcr小瓶7260)中而被添加至容纳在其内的冻干的主要混合物。来自洗脱室(例如,洗脱室7190)的加热的核酸样品可以随后被传送到pcr小瓶中,如以上所描述的。此外,第二加热模块7250还可以加热洗脱室与pcr小瓶之间的流动路径(例如,通道7222),使得流动路径内的内含物(例如,从洗脱室传送至pcr小瓶的经洗脱的核酸样品)可以维持在升高温度(例如,约40℃、50℃、70℃、或95℃以上的温度)。例如,在一些实施方式中,第二加热模块3750可以将流动通道内的样品的温度维持在介于约50℃与约95℃之间的温度。在加热的洗脱样品被运送到pcr小瓶中之后,通过(由第一加热模块3730产生的)温度循环混合溶液,并且随后启动pcr反应。
第三加热模块3780包括至少一个加热器(未示出)和一个加热器块3784。如图63中所示,加热器块3784限定一系列的凹部和/或空腔3786a、3786b、3786c、3786d、3786e、3786f,每个凹部或空腔对应于盒3350内的每个药筒)。在使用中,当加热器组件3700被移动到仪器3002内的每个药筒周围的位置时,药筒的一部分设置在加热器块3784的相对应的凹部(例如,凹部3786a)内。更具体地,如图52中所示,分离模块(例如,分离模块6100)的对应于裂解室6114(图52中未识别出)的一部分设置在相对应的凹部内。由此,当加热器组件3700定位在每个药筒周围时,加热器块体3784的限定凹部3786的侧壁定位在裂解室6114的一部分周围和/或基本上围绕裂解室6114的一部分。以此方式,第三加热器模块3780可以加热和/或热循环容纳在每个药筒的裂解室6114内的样品的一部分。在一个实施方式中,通过第三加热模块3780进行的加热在反转录和/或pcr反应期间发生。
图64至70示出仪器3002的光学组件3800的各种视图。光学组件3800构造成监测在仪器3002内设置的药筒内发生的反应。更具体地,光学组件3800构造成在发生在药筒的pcr小瓶(例如pcr小瓶6260)内的pcr反应之前、期间和/或之后检测测试样品内的一种或多种不同的分析物和/或靶。如本文中描述的,光学组件3800可以以顺序和/或分时段的方式和/或实时地分析样品。光学组件3800包括激发模块3860、检测模块3850、滑动组件3870和光学纤维组件3830。
例如,在一个实施方式中,光学组件用来实时地监测核酸扩增反应。在另一实施方式中,扩增反应为pcr。在另一实施方式中,光学组件用来测量来自结合测定——-例如,酶与基底或者配体与受体之间的结合——的结果。
光学纤维组件3830包括一系列的激发光学纤维(在图64中标示为激发纤维3831a、3831b、3831c、3831d、3831e、3831f、3831g)。每个激发纤维3831a、3831b、3831c、3831d、3831e和3831f均构造成将来自激发模块3860的光束和/或光学信号传送至相对应的接收块3710。因此,每个激发纤维3831a、3831b、3831c、3831d、3831e和3831f的第一端部均设置在如以上描述的接收块3710的管腔3711内。激发纤维3831g为校准纤维并且构造成将来自激发模块3860的光束和/或光学信号传送至光学校准模块(未示出)。激发光学纤维3831可以是用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。
光学纤维组件3830包括一系列的检测光学纤维(在图64中标示为检测纤维3832a、3832b、3832c、3832d、3832e、3832f、3832g)。每个检测纤维3832a、3832b、3832c、3832d、3832e和3832f均构造成将来自接收块3710的光束和/或光学信号传送至检测模块3850。因此,每个检测纤维3832a、3832b、3832c、3832d、3832e和3832f的第一端部均设置在如以上描述的接收块3710的管腔3712内。检测纤维3832g为校准纤维并且构造成接收来自光学校准模块(未示出)的光束和/或光学信号。检测光学纤维3832可以是用于传送光束的任何适合的光学纤维,例如多模纤维或单模纤维。
光学纤维组件3830还包括纤维安装块3820。如图70中示出的,纤维安装块3820限定一系列的管腔3825a至3625g和一系列的管腔3824a至3824g。每个管腔3824均构造成接纳相对应的激发光学纤维(例如,如在图65中标示的激发纤维3831a)的第二端部。类似地,每个管腔3825均构造成接收相对应的检测光学纤维(例如,如在图65中标示的检测纤维3832a)的第二端部。纤维安装块3820联接至滑动组件3870的滑轨3890,以将激发纤维3831光学地联接至激发模块3860,并且将检测纤维3832光学地联接至检测模块3850,如以下更详细地描述的。
如图65中所示,光学纤维组件3830包括一系列的间隔件、透镜和密封构件,以便于本文中描述的光学连接、和/或修改、约束和/或改变由光学纤维组件3830所传送的光束。更具体地,光学纤维组件3830包括一系列的激发间隔件3833和检测间隔件3834,所述激发间隔物件3833和检测间隔件3834构造成设置在纤维安装块3820和/或滑板3890内。光学纤维组件3830还包括一系列的激发透镜3835和检测透镜3836,所述激发透镜3835和检测透镜3836构造成设置在纤维安装块3820和/或滑板3890内。光学纤维组件3830还包括一系列的激发密封构件3837和检测密封构件3838,所述激发密封构件3837和检测密封构件3838构造成设置在纤维安装块3820和/或滑板3890内。激发密封构件3837和检测密封构件3838构造成密封由光学组件3800限定的光路和/或防止污染物进入由光学组件3800限定的光路。
如图64至图66所示,光学组件3800包括激发模块3860,该激发模块3860构造成产生一系列的激发光束(和/或光学信号,未示出)。激发模块3860包括激发电路板3861,在该激发电路板3861上安装有一系列的激发光源3862。光源3862可以是用于产生一系列激发光束的任何适合的装置和/或机构,例如激光、发光二极管(led),闪光灯等。在一些实施方式中,由每个光源3862产生的光束可以具有与由其它光源3862产生的光束的特性基本上相同的特性(例如,波长、幅值和/或能量)。然而,在其它实施方式中,第一光源3862可以产生具有第一组特性(与红色光束相关联的波长)的光束,并且第二光源3862可以产生具有不同的第二组特性(例如,与绿色光束相关联的波长)的光束。这种布置允许每道不同的光束(即,具有不同特性的光束)以顺序的方式传送至每个接收块3710,如本文中所更详细地描述的。如图65中所示,激发模块3860包括一系列的间隔件3863、过滤器3864和透镜3865,以便于本文中描述的光学连接、和/或修改、约束和/或改变由激发模块3860所产生的并且由激发纤维3831所传送的光束。
如图64至图66中所示,光学组件3800包括检测模块3850,该检测模块3850构造成接收和/或检测一系列的发射光束(和/或光学信号,未示出)。检测模块3850包括检测电路板3851,在该电路板3851上安装有一系列的发射光检测器3852。发射光检测器3852可以为用于检测一系列发射光束的任何适合的装置和/或机构,例如光学检测器、光敏电阻、光生伏打电池、发光二极管、光电管、ccd相机等。在一些实施方式中,每个检测器3852可以构造成地择性地接收发射光束而不管发射光束的特性(例如,波长、幅值和/或能量)如何。然而,在其它实施方式中,检测器3852可以构造(或“调谐”)成对应于具有特定组特性(例如,与红色光束相关联的波长)的发射光束。例如,在一些实施方式中,每个检测器3852可以构造成在被激发模块3860的相对应的光源3862激发时接收通过激发样品的一部分所产生的发射光。这种布置允许每道不同的发射光束(例如,具有不同特性的光束)从每个接收块3710以顺序的方式被接收,如本文中所更详细地描述的。如图65中所示,检测模块3850包括一系列的间隔件3853、过滤器3854和透镜3855,以便于本文中描述的光学连接、和/或修个、约束和/或改变由检测模块3850接收到的发射光束。
滑动组件3870包括安装构件3840、滑块3880和滑轨3890。滑块3880联接至安装构件3840,并且可滑动地安装至滑轨3890。如以下更详细地描述的,在使用中,由步进马达3873旋转的传动螺杆3872可以在滑块3880的一部分内旋转,以引起滑块3880(并因此引起安装构件3840)相对于滑轨3890移动,如由图64和图66中箭头hhh所示的。以此方式,可以使安装构件3840相对于滑轨3890移动,以顺序地将每个激发光源3862和发射光检测器3852移动成分别与每个激发纤维3831的第二端部和每个发射纤维3832的第二端部光学连通。以下提供滑动组件3870的进一步的详细描述和光学模块3800的操作。
如图67中所示,安装构件3840限定一系列的激发管腔3844a至3844f和一系列的发射管腔3845a至3845f。如图65中所示,每个激发光源3862设置在相对应的激发管腔3844内,并且每个发射光检测器3852设置在相对应的发射管腔3845内。安装构件3840联接至滑块3880,使得滑块3880的运动引起安装构件3840(并且因而引起激发光源3862和发射光检测器3852)的运动。
如图68中所示,滑块3880包括第一部分3881和第二部分3882。第一部分3881包括引导凸起3886,并限定一系列的激发管腔3884a至3884f和一系列的发射管腔3855a至3855f。当滑块3880联接至安装构件3840时,滑块3880的每个激发管腔3884均与安装构件3840的相对应的激发管腔3844对准。类似地,滑块3880的每个发射管腔3885均与安装构件3840的相对应的发射管腔3845对准。引导凸起构造成可滑动地设置在滑轨3890上的相对应的凹槽3896内。
滑块3880的第二部分3882限定一对引导管腔3887和导向螺杆管腔3888。在使用中,传动螺杆3872在导向螺杆管腔3888内旋转,以相对于滑轨3890移动滑块3880。滑块3880的移动由导轨3871引导,所述滑轨3871可滑动地设置在相对应的引导管腔3887内。
如图69中所示,滑轨3890限定七个激发开口3894a、3894b、3894c、3894d、3894e、3894f、3894g和七个检测开口3895a、3895b、3895c、3895d、3895e、3895f、3895g。纤维安装块3820联接至滑轨3890,使得激发纤维3831与每个相对应的激发开口光学连通,并且检测纤维3832与每个相对应的激发开口光学连通。以此方式,当滑块3880和安装构件3840相对于滑轨3890共同移动时,滑块3880的每个激发开口和检测开口以及安装构件3840分别顺序地与滑轨3890的每个激发开口3894和检测开口3895对准。
在使用中,在扩增过程期间或扩增过程之后,滑动组件3870可以可控制地移动滑块3880,使得光源3862和光学检测器3852对顺序地经过每对激发纤维3931和检测纤维3832。以此方式,光学组件3800可以以分时段和/或多路复用的方式分析六个pcr小瓶(例如,pcr小瓶6260)中的每个pcr小瓶内的样品。
图71a、71b、72a、72b和73为用于仪器3002的电子控制和计算机系统的示意性方框图。
尽管光学组件3800示出为包括邻近激发模块3860的检测模块3850,但在其它实施方式中,仪器的光学组件可以包括相对于激发模块的位置定位的检测模块。例如,图74至图76为光学组件4800的示意性图示,该光学组件4800构造成执行一系列样品的分时段的光学检测,如以上参照光学组件3800所描述的。光学组件4800为仪器(例如,本文中示出和描述的任何仪器)的构造成容纳六个反应小瓶260的一部分。光学组件4800包括激发模块4860、检测模块4850和纤维组件4830。激发模块4860包括四个激发光源4862a、4862b、4862c和4862d。每个激发光源构造成产生具有不同波长的光束。例如,光源4862a构造成产生具有颜色#1(例如,红色)的光束,光源4862b构造成产生具有颜色#2(例如,绿色)的光束,光源4862c构造成产生具有颜色#3(例如,蓝色)的光束,光源4862d构造成产生具有颜色#4(例如,黄色)的光束。
检测模块4850包括四个检测器4852a、4852b、4852c和4852d。每个检测器构造成接收具有不同波长的发射光束。例如,检测器4852a构造成接收用激发颜色#1激发分析物产生的光束,检测器4852b构造成接收用激发颜色#2激发分析物产生的光束,检测器4852cv构造成接收用激发颜色#3激发分析物产生的光束,检测器4852d构造成接收用激发颜色#4激发分析物产生的光束。
纤维组件4830包括一系列的激发纤维4831和一系列的检测纤维4832。特别地,一根激发纤维用于将每个反应小瓶260光学地联接至激发模块4860,并且一根检测纤维4832用于将每个反应小瓶260光学地联接至检测模块4850。激发模块4860和检测模块4850构造成相对于纤维组件4830移动。以此方式,每个光源及其相对应的检测器(例如,光源4862a和检测器4852a)可以顺序地与用于特定反应小瓶260的激发纤维和检测纤维对准。
在使用中,当光学组件4800处于如图74中所示的第一构型时,,光源4862a和检测器4852a与第一反应小瓶260光学连通。由此,容纳在第一反应小瓶中的样品可以用具有颜色#1的激发光进行分析。随后使激发模块4860和检测模块4850如由图75中箭头iii所示地移动,以将光学组件安置于第二构型。当光学组件4800处于如图75中所示的第二构型时,光源4862a和检测器4852a与第二反应小瓶260光学连通,并且光源4862b和检测器4852b与第一反应小瓶260光学连通。由此,容纳在第一反应小瓶中的样品可以用具有颜色#2的激发光进行分析,并且容纳在第二反应小瓶中的样品可以用具有颜色#1的激发光进行分析。随后使激发模块4860和检测模块4850如由图76中箭头jjj所示地移动,以将光学组件安置于第三构型。当光学组件4800处于如图76中所示的第三构型时,光源4862a和检测器4852a与第三反应小瓶260光学连通,光源4862b和检测器4852b与第二反应小瓶260光学连通,并且光源4862c和检测器4852c与第一反应小瓶260光学连通。因此,容纳在第一反应小瓶中的样品可以用具有颜色#3的激发光进行分析,容纳在第二反应小瓶中的样品可以用具有颜色#2的激发光进行分析,容纳在第三反应小瓶中的样品可以用具有颜色#1的激发光进行分析。
图75为根据实施方式的检测生物样品中的核酸的方法100的流程图。特别地,图示的方法为“单阶段靶检测”方法,其可以使用本文中所示出的和描述的任何药筒以及本文中所示出和描述的任何仪器来执行。更具体地,以下描述的方法100的操作可以在在药筒中执行而无需打开药筒和/或以其它方式将样品、试剂和/或pcr混合物暴露于外部环境。类似陈述地,以下所描述的方法100的操作可以在药筒中执行而无需人为干预来传送样品和/或试剂。出于描述的目的,方法100描述为用以上参照图25至图33示出和描述的药筒7001的分离模块7100和pcr模块7200来执行。
该方法包括从洗脱室内的磁性捕获珠中洗脱核酸,102。该过程可以例如在分离模块7100的洗脱室7190内发生。更具体地,参照图29至图31,洗脱缓冲液可以储存在试剂模块7270a内,并且可以如上所述地传送到洗脱室7190内,以完成洗脱操作。洗脱缓冲液可以为本文中描述的洗脱缓冲液和/或与核酸扩增(例如,通过pcr和反转录)相容的任何适合的洗脱缓冲液。
随后将经洗脱的核酸从洗脱室传送到pcr室,104。pcr室可以是,例如图29至图31中示出的pcr小瓶7260。尽管洗脱室7190和pcr小瓶7260以上示出为位于不同的模块和/或壳体中,但在其它实施方式中,洗脱室和pcr室能够位于整体构造的壳体或结构中。如以上所述,在一些实施方式中,pcr室可以包括冻干的扩增试剂,使得在核酸传送后,试剂被重构。经洗脱的核酸随后使用如上所述的传送机构7235或任何其它适合的机构传送到pcr小瓶7260中。
pcr混合物随后在pcr室内热循环和/或加热,106。pcr混合物可以使用如上示出的仪器3002在任何适合的温度范围之间循环。在一些实施方式中,pcr混合物可以升高至恒定的温度,以激活用于扩增的酶。
实时监测扩增反应,108。在一些实施方式中,扩增反应可以通过结合至产物(即,扩增子)的、具有荧光标签的小沟结合物(mgb)和/或任何其它基于亲和力的杂交相互作用来监测。监测可使用以上所示出和描述的仪器3002的光学组件3800来执行。
完成扩增后,检测探针(例如,mgb)可以与靶扩增子相结合,110。这提供了终点检测。
在一些实施方式中,该方法包括进行解链分析和/或退火分析,112。可以执行该操作以鉴别或确证特异性或错配序列的分子靶。
图76为根据实施方式检测生物样品中的核酸的方法200的流程图。具体地,图示的方法为“两阶段靶检测”方法,该方法可以用本文中所示出和描述的任何药筒和本文中所示出和描述的任何仪器来执行。更具体地,以下描述的方法200的操作可以在药筒中执行而无需打开药筒和/或以其它方式将样品、试剂和/或pcr混合物暴露于外部环境。类似陈述地,以下描述的方法200的操作可以在药筒中进行而无需人为干预来传送样品和/或试剂。出于描述的目的,方法200描述为用以上参照图8至图24示出的和描述的分离模块6100和pcr模块6200来执行。
该方法包括从洗脱室内的磁性捕获珠中洗脱核酸,202。该过程可以发生在例如分离模块6100的分离室6190内。更具体地,参照图8至图10,洗脱缓冲液可以储存在试剂室6213c内,并且可以如上所述地传送到洗脱室中,以完成洗脱操作。洗脱缓冲液可以为本文中描述的洗脱缓冲液和/或与核酸扩增(例如,通过pcr和反转录)相容的任何适合的洗脱缓冲液。
随后将经洗脱的核酸从洗脱室传送至pcr室,204。pcr室可以是例如图8中所示的pcr小瓶6260。如上所述,在一些实施方式中,pcr室可包含冻干的扩增试剂,使得在传送核酸后,该试剂被重构。之随后使用如上所述的传送机构6235或任何其它适合的机构传送经洗脱的核酸。
pcr混合物随后在pcr室内热循环和/或加热,206。pcr混合物可以使用如上所示的仪器3002在任何适合的温度范围之间循环。在一些实施方式中,pcr混合物可以升高至恒定的温度,以激活用于扩增的酶。
实时监测扩增反应,208。在一些实施方式中,扩增反应可通过结合产物(即,扩增子)的、具有荧光标签的小沟结合物(mgb)和/或任何其它基于亲和力的杂交相互作用来监测。监测可使用以上所示出和描述的仪器3002的光学组件3800来执行。
在完成扩增后,检测探针(例如,mgb)可以与靶扩增子相结合,210。这提供了终点检测。该方法包括执行解链分析和/或退火分析,212。可以执行该操作以鉴别或确证特异性或错配序列的分子靶。如本文中使用的,mgb本身可用作探针,或者可以缀合至另一分子并用作探针。例如,在一个实施方式中,mgb与荧光染料一起缀合至特异性dna寡核苷酸探针的5'端。在该实施方式中,探针在3'端包含非荧光猝灭剂。当探针在溶液中时,5'-荧光染料的荧光被猝灭。然而,当探针与其补体相结合时,荧光不再被猝灭。因此,由探针产生的荧光的量与产生靶的量成正比。通过将不同荧光染料(即,当被激发时每种荧光染料会发出不同波长的光,或者可以以独特波长被激发)缀合至各个探针,这些探针在反应中可以是“多重的”。
随后将第二组探针递送至pcr室,214。在一些实施方式中,第二组探针可以包括配制成与在高于约70摄氏度下解链(破坏亲和作用的解离能)的特异性或错配靶序列相结合的第二组mgb探针或其它探针。在一些实施方式中,第二组mgb探针配制成与在高于约75摄氏度下解链的特异性或错配靶序列相结合。在其它实施方式中,第二组mgb探针配制成与在高于约80摄氏度下解链的特异性或错配靶序列相结合。在另外其它实施方式中,第二组mgb探针配制成与在高于约85摄氏度下解链的特异性或错配靶序列相结合。
在一些实施方式中,第二组探针可以储存在试剂室6213b内,并且可以直接地传送到pcr小瓶6260中或者经由洗脱室6190传送到pcr小瓶6260中,如上所述的。以此方式,第二组探针可以添加至pcr混合物而无需打开药筒或pcr小瓶或以其它方式将pcr混合物暴露于污染物。
该方法随后包括进行第二解链分析和/或退火分析,216。可以执行该操作以鉴别或确证特异性或错配序列的分子靶。
图77为根据实施方式检测生物样品中核酸的方法300的流程图。特别地,示出的方法为“伴随单阶段靶检测的两步反转录pcr(rt-pcr),”方法,该方法可以使用本文中示出和描述的任何药筒以及本文中所示出和描述的任何仪器来执行。更具体地,以下所描述的方法300的操作可以在药筒中执行而无需打开药筒和/或以其它方式将样品、试剂和/或pcr混合物暴露于外部环境。类似陈述地,以下描述的方法300的操作可以在药筒中执行而无需人为干预来传送样品和/或试剂。出于描述的目的,方法200被描述为用以上参照图8至图24示出和描述的分离模块6100和pcr模块6200来执行。
本方法包括从洗脱室内的磁性捕获珠中洗脱核酸,302。该过程可以例如在分离模块600的洗脱室6190中发生。更具体地,参照图8至图10,洗脱缓冲液可以储存在试剂室6213c内,并且可以被传送到如以上描述的洗脱室内,以完成洗脱操作。洗脱缓冲液可以为本文中描述的洗脱缓冲液和/或与核酸扩增(例如,通过pcr和反转录)相容的任何适合的洗脱缓冲液。
随后将经洗脱的核酸从洗脱室传送到pcr室,304。pcr室可以是例如图8中示出的pcr小瓶6260。如以上所描述的,在一些实施方式中,pcr室可以包括冻干的扩增试剂,使得在核酸被传送后,试剂被重构。经洗脱的核酸随后使用如以上描述的注射泵或任何其它适合的机构来传送。
混合物随后在pcr室中加热至基本上恒定的温度,306。以此方式,可以激活用于反转录的酶。
当完成反转录时,pcr试剂被传送到pcr室,308。pcr试剂可以储存在试剂室6213b和/或6213a内,并且可以直接地传送到pcr小瓶6260中或者经由洗脱室6190传送到pcr小瓶6260中,如以上描述的。以此方式,pcr试剂可以在完成反转录之后添加至pcr混合物而无需打开药筒或pcr小瓶、或以其它方式将pcr混合物暴露于污染物。
实时监测扩增反应,310。在一些实施方式中,扩增反应可以通过结合至产物(即,扩增子)的、具有荧光标签的小沟结合物(mgb)和/或任何其它基于亲和力的杂交相互作用来监测。然而,任何dna结合剂可用于实时监测pcr反应。监测可使用以上所示和描述的仪器3002的光学组件3800来执行。
如在本文中使用的,“dna结合剂”是指能够结合双链或单链dna的任何可检测分子,例如,可通过荧光检测。在一个实施方式中,dna结合剂为荧光染料或者在与双链或单链dna相结合时能够直接或间接产生信号的其它发色团、酶或物质。该试剂可以直接结合,即,dna结合剂可以附着于直接结合dna的另一试剂。仅需要该试剂在与双链核酸或单链dna相结合时能够产生可检测信号,该可检测信号能够与在同一试剂在溶液中时产生的信号相区分。
在一个实施方式中,dna结合剂为嵌入剂。嵌入剂如溴化乙锭和sybr氯在嵌入双链dna中时比在与单链dna、rna结合或在溶液中时更强烈地发出荧光。另一些嵌入剂在与双链dna结合时在荧光光谱中展现出变化。例如,放线菌素d在与单链核酸结合时发出红色荧光,而在与双链模板结合时发出绿色荧光。无论可检测信号增加、减少或是转变,如放线菌素d的情况,在试剂与双链dna结合或未结合时提供可区分的可检测信号的任何嵌入剂适合用于实践所公开的发明。
在另一个实施方式中,dna结合剂为采用荧光共振能量传送的外切核酸酶探针。例如,在一个实施方式中,dna结合剂为在5'和3'端分别具有报道基因和猝灭剂染料的寡核苷酸探针,并且特异性地与靶核酸分子相结合。在溶液中且当完整时,报道基因染料的荧光被淬灭。然而,某些taq聚合酶的外切核酸酶活性用来在pcr期间切割探针,而报道基因不再被淬灭。因此,荧光发射与产生的靶量成正比。
在另一个实施方式中,dna结合剂采用与寡核苷酸探针5'端缀合的mgb。除了5'端的mgb之外,报道基因染料还与探针的5'端缀合,并且猝灭剂染料位于3'端。例如,在一个实施方式中,采用由lukhtanov描述的dna探针(lukhtavon(2007).nucleicacidsresearch35,第e30页)。在一个实施方式中,mgb直接缀合至寡核苷酸探针。在另一实施方式中,mgb缀合至报道基因染料。当探针在溶液中时,5'-荧光染料的荧光被淬灭。然而,当探针与其补体相结合时,荧光不再被淬灭。因此,由探针产生的荧光量与产生的靶量成正比。通过将不同荧光染料(即,当被激发时每种荧光染料会发出不同波长的光,或者可以以独特波长被激发)与各个探针缀合,这些探针在反应中可以是“多重的”。
在又一个实施方式中,小沟结合物用于实时监测pcr反应。例如hoechst33258(searle&embrey,1990,nuc.acidsres.18(13):3753-3762)展现出随着增加的靶量而改变的荧光。用于与本发明一起使用的另一些mgb包括偏端霉素和纺锤菌素。
根据本文中描述的一些实施方式,dna结合剂直接或间接产生可检测信号。信号比如能够通过荧光或吸光度直接检测,或者能够经由附着至dna结合剂的结合配体或取代标签部分间接检测。
根据本文中描述的一些实施方式,dna结合剂直接或间接地产生可检测信号。信号比如能够通过荧光或吸光度直接检测;或者能够经由附着至dna结合剂的结合配体或取代标签部分间接检测。例如,在一个实施方式中,采用与荧光报道基因染料缀合的dna探针。dna探针在报道基因染料的相反端具有猝灭剂染料,并且仅当与其互补序列相结合时会发荧光。在进一步的实施方式中,dna探针在5'端具有mgb和荧光染料二者。
与本发明一起使用的其它非限制性dna结合剂包括但不限于molecularbeacons、scorpions和fret探针。
在完成扩增后,检测探针(例如,mgb)可以结合至靶扩增子,312。这提供了终点检测。该方法包括执行解链分析和/或退火分析,314。可以执行该操作以鉴别或确证特异性或错配序列的分子靶。
图78为根据实施方式检测生物样品中的核酸的方法400的流程图。特别地,示出的方法为以上示出的和描述的方法100的替代性“单阶段靶检测”方法。方法400可以使用本文中示出和描述的任何药筒以及本文中示出和描述的任何仪器来执行。更具体地,以下描述的方法400的操作可以在药筒中执行而无需打开药筒和/或以其它方式将样品、试剂和/或pcr混合物暴露于外部环境中。类似陈述地,以下描述的方法400的操作可以在药筒中执行而无需人为干预来传送样品和/或试剂。出于描述的目的,方法400描述为用本文中参照图85至图87示出和描述的分离模块10100和pcr模块10200来执行。
方法400不同于方法100之处在于,洗脱缓冲液储存于壳体的洗脱室中而非储存于如方法100描述的试剂室6213c中。因此,该方法包括从洗脱室内的磁性捕获珠中洗脱核酸,402。该过程发生在分离模块10100的洗脱室内。洗脱缓冲液可以是与核酸扩增(例如,通过pcr和反转录)相容的任何适合的洗脱缓冲液。
随后将经洗脱的核酸从洗脱室传送至pcr室,404。pcr室可以例如是图85至图87中示出的pcr小瓶10260。尽管洗脱室10190和pcr小瓶10260示出为位于不同的模块和/或壳体中,但在其它实施方式中,洗脱室和pcr室可以位于整体构造的壳体或结构中。如以上描述的,在一些实施方式中,pcr室可以包括冻干的扩增试剂,使得在核酸被传送后,试剂被重构。经洗脱的核酸随后使用如以上描述的注射泵或任何其它适合的机构来传送。
pcr混合物随后在pcr室内热循环和/或加热,406。pcr混合物可以使用如上所示的仪器3002而在任何适合的温度范围之间循环。在一些实施方式中,pcr混合物可以升高至恒定的温度以激活用于扩增的酶。
实时监测扩增反应,408。在一些实施方式中,扩增反应可以通过与产物(即,扩增子)相结合的检测探针(例如,标记有mgb的单链寡核苷酸探针,或者单链双标记检测探针,即在5'端具有荧光团标记并且在3'端具有猝灭剂)来监测。监测可使用以上示出和描述的仪器3002的光学组件3800来执行。
完成扩增后和/或在扩增期间,检测探针(例如,mgb)可以与靶扩增子相结合,410。这提供了终点检测。在一些实施方式中,本方法包括执行解链分析和/或退火分析,412。可以执行该操作以鉴别或确证特异性或错配序列的分子靶。
使用本文中描述的系统和方法所产生的数据可以使用任何数目的不同方法进行分析。例如,可以通过使用亲和探针的解链分析或退火分析来分析该数据,用于经扩增核酸的序列鉴别。用独特“亲和探针”或分子标签(由经改性碱基和mgb-fluor组成,mgb-fluor具有与靶分子-亲和常数-kd定向结合的亲和力)的解链/退火谱分析-分子谱表分析指示/产生特异性遗传状态谱。例如,图81为指示由与源于生物样品的扩增核酸相结合的一组探针产生的分子信号的谱图。该分子信号表示与生物样品回复相关的病变状态(或独特核酸序列的存在)。分子信号或图谱取决于分子标签与靶核酸的特异性相互作用,这仅可以用药筒内的分子标签而产生。换言之,光谱是指纹踪迹(即,指示病变状态(肿瘤学、传染病)或遗传状态的峰或“光谱响应”的独特序列)。
光谱内的多重-超过一种病变状态-(多重标志)-随(特定波长内的)温度和时间、随独特“探针”或多探针(独特分子实体-分子反应物、指示剂、标签)而多重。
可以在鉴别过程使用多于一种的指纹踪迹(指纹组)。对指纹的多面板指纹光谱测定可用于确定结果。用于产生多通道或阵列数据的变量为所用的波长差异荧光、退火或解离(解链)的温度范围以及数据采集率(时间依赖性域)。
对加热和冷却亲和探针和扩增靶的控制可以用于产生识别疾病所需的指纹。对于数据生成(退火和解链),温度范围可以在70至100摄氏度范围内。
尽管以上分离模块6001示出为包括具有用于促进裂解过程的混合泵6181的分离模块6100,但在其它实施方式中,可以使用用于将能量传送到溶液以加快和/或提高细胞裂解的任何适合的机构。例如,在一些实施方式中,可以使用声学能。
例如,图82示出根据实施方式的分离模块的第二壳体8160,该分离模块构造成将声学能传送到分离模块(例如分离模块6100、分离模块7100等)的分离室(未示出)内容纳的样品中,以加快包含在其内的核酸的细胞裂解和/或分离。第二壳体8160可以以与以上参照图11的描述相类似的方式联接至对应的第一壳体和/或设置在相对应的第一壳体(图82中未示出)内。更具体地,第二壳体8160包括类似于上文示出和描述的密封件6172——基本上将第二壳体8160与第一壳体声学隔离——的密封件(未示出)。
第二壳体8160限定了容纳分离过程中使用的试剂和/或其它物质的一系列保持室8163a、8163b、8163c和8163d。特别地,保持室可以容纳蛋白酶(例如,蛋白酶k)、溶解大块材料的裂解溶液、使核酸带磁性电荷的结合溶液、以及结合至磁性带电核酸以协助核酸在分离模块和/或第一壳体内运输的磁珠的溶液。
第二壳体8160还限定开口8185,超声转换器8195的一部分可以设置在该开口8185内。声学联接构件8182联接至开口8185内的第二壳体8160的侧壁的一部分。因此,在使用中,声换能器8195的至少一部分可以设置在开口8185内并且与声学联接构件8182接触。以此方式,由转换器8195产生的声学和/或超声能可以传送通过声学联接构件8182和壳体8160的侧壁、并进入裂解室的溶液内。超声转换器8195可以为任何适合的声换能器(例如,包括压电元件和报警器),并且可以构造成在20khz与300khz之间共振。在一些实施方式中,声换能器8195可以构造成在介于40khz与45khz之间的频率下产生超声能。
超声转换器8195可以通过仪器——比如本文中描述的仪器3002——的致动器移动到开口8185中。这种致动器可以包括例如构造成将超声转换器8195移动预定的距离使其与声学联接构件8182接触的步进马达。在一些实施方式中,例如,仪器可以包括与以上参照图37至图40示出和描述的第一致动器组件3400类似的致动器组件。在这种实施方式中,第一致动器组件可以包括通过类似于接合杆3445的接合杆而被移动到开口中的一系列超声转换器。
在一些实施方式中,致动器可以构造成改变由超声转换器8195施加在声学联接构件8182上的力。这可以例如通过在超声转换器被致动时相对于联接构件8182移动超声转换器8195来完成。这种布置可以允许动态地调整通过声学联接构件8182的超声能传输和/或由通过声学联接构件8182的超声能传输产生的热。
在一些实施方式中,声学联接构件8182由绝热材料构造。以此方式,可以使从声学联接构件8182至第二壳体8160的邻近侧壁的热传递最小化。这种布置可以使第二壳体8160的侧壁在声换能器8195被致动并与侧壁接触时的变形和/或解链最小化和/或防止第二壳体8160的侧壁在声换能器8195被致动并与侧壁接触时的变形和/或解链。另外,在一些实施方式中,声学联接构件8182可以构造成和/或构建成具有声阻抗以促进超声能传送通过声学联接构件8182并进入分离室中。
图83示出根据实施方式的分离模块的第二壳体9160,该第二壳体9160构造成将超声能传送到分离模块的分离室(未示出)内容纳的样品中,以加快包含在其内的核酸的细胞裂解和/或分离。第二壳体9160可以以如上述类似的方式联接至相对应的第一壳体(图83中未示出)和/或设置在相对应的第一壳体中。更具体地,第二壳体9160包括与上文示出和描述的密封件6172相类似的密封件(未示出),其将第二壳体9160与第一壳体基本上声学地隔离。
第二壳体9160限定了容纳在分离过程中使用的的试剂和/或其它物质的一系列保持室9163a、9163b、9163c和9163d。第二壳体9160还限定开口9185,超声转换器9195的一部分可以设置在该开口9185内。相比于以上所述的开口8185,开口9185可以具有第二壳体9160的侧壁中的开口与分离室流体连通。
声学联接构件9183设置在开口9185内,并且通过第二壳体9160的侧壁的一部分。更具体地,声学联接构件9183联接至侧壁,使得声学联接构件9183的第一部分9186位于开口9185内,并且声学连接构件9183的第二部分9184位于分离室内。密封件9184设置在第二壳体9160的侧壁与声学联接构件9183之间,以将分离室与第二壳体基本上流体隔离和/或将声学联接构件9183与第二壳体基本上声学地隔离。
在使用中,声换能器8195的至少一部分可以设置在开口9185内并且与声学联接构件9183的第一部分9186接触。以此方式,由转换器9195产生的声学能和/或超声能可以被传送通过声学联接构件9183并进入分离室内的溶液中。
超声转换器8195可以通过仪器——比如本文中描述的仪器3002——的致动器移动到开口9185中。这种致动器可以包括例如构造成将超声转换器8195移动预定距离使其与声学联接构件9183接触的步进马达。在一些实施方式中,例如,仪器可以包括与以上参照图37至图40示出和描述的第一致动器组件3400类似的致动器组件。在这种实施方式中,第一致动器组件可以包括通过类似于接合杆3445的接合杆而被移动到开口中的一系列转换器。
在一些实施方式中,致动器可以构造成改变由超声转换器5195施加在声学联接构件5183上的力。这可以例如通过在超声转换器被致动时相对于联接构件9183移动超声转换器8195来完成。这种布置可以允许动态地调整通过声学联接构件9183的超声能传输和/或由通过声学联接构件9183的超声能传输产生的热量。
如以上所述,在一些实施方式中,声学联接构件5183可以构造成具有声阻抗,以促进超声能传送通过声学联接构件9183并进入分离室中。
尽管图82和图83示出分离模块的第二壳体,其构造成将超声能传送到容纳在分离模块内的样品中,但在其它实施方式中,药筒的任何部分可以构造成将超声能传输到样品中。例如,图84a和图84b示出分离模块7100(参见例如图26至图28)和超声转换器7195。转换器7195可以为任何适合的转换器并且可以包括例如压电叠堆和报警器。特别地,如上所述,壳体7110包括声学联接部7182。在使用中,声换能器7195的至少一部分可以设置成与声学联接部7182接触。以此方式,由转换器产生的声学和/或超声能可以传送通过声学联接部7182和第一壳体7110的侧壁、并进入裂解室7114内的溶液中。
如图84b中示出的,超声转换器7195可以通过仪器3002’的致动器组件3191移动成与声学联接部7182接触。致动器组件3191包括例如步进马达7192,该步进马达7192构造成将该组超声转换器7195移动预定的距离以将包括在超声转换器7195内的超声报警器7197安置成与声学联接部7182(参见图84a)接触。在一些实施方式中,例如,致动器组件3191类似于以上参照图37至图40示出和描述的第一致动器组件3400。在这种实施方式中,致动器组件3191包括类似于接合杆3445的壳体7193,在该壳体7193内设置有所述系列的超声转换器7195。特别地,超声转换器7195在壳体7195内由一系列的弹簧或贝氏(belleville)垫圈7196“弹簧加载”的或偏置。以此方式,可以朝向声学联接部7182迫压超声转换器7195,使得当转换器7195的超声报警器7197移动成与声学联接部7182接触时,贝氏垫圈可以确保在超声报警器7197与声学联接部7182之间的接触得以维持。
在一些实施方式中,致动器组件3191可以构造成改变由超声转换器7195和/或超声报警器7197施加在声学联接部7182上的力。这可以例如通过在超声转换器7195被致动的同时相对于声学联接部7182移动超声转换器7195来完成。这种布置可以允许动态地调整通过声学联接部7182的超声能传输和/或通过声学联接部7182的超声能传输产生的热量。如在图84a中最佳示出的,弹簧7196或其它偏置构件构造成相对于仪器3002的致动器组件3191维持和/或偏置超声转换器7195。
尽管pcr模块6200在上文示出和描述为包括在其内可以储存pcr试剂、洗脱缓冲液等的三个试剂室6213a、6213b和6213c,但在其它实施方式中,pcr模块可以包括任何数目的试剂室。在一些实施方式中,pcr模块可以没有任何试剂室。例如,图85至图87示出根据实施方式的药筒10001。药筒10001包括联接在一起以形成集成的药筒10001的核酸分离模块10100和扩增(或pcr)模块10200。该集成的药筒10001在许多方面与上文示出和描述的药筒6001和/或药筒7001相似,并因此在本文中未详细描述。如在图86中所示,图86示出不含盖10005的药筒,pcr模块10200包括壳体10210、pcr小瓶10260和传送管10250。扩增模块10200联接至分离模块10100,使得传送管的至少一部分被设置在分离模块10100的洗脱室内。
壳体10210包括传送端口10270。传送端口10270限定一个或多个管腔和/或通道,经分离的核酸和/或其它物质或试剂可以通过所述一个或多个管腔和/或通道运送到pcr小瓶10260中。壳体10210和/或传送端口10270可以限定一个或多个通气通道,以将洗脱室和/或pcr小瓶10260流体地联接至大气。在一些实施方式中,任何这种通气口可以包括熔块、阀和/或其它适合的机构,以使样品和/或试剂从洗脱室和/或pcr小瓶10260中的损失最小化和/或防止样品和/或试剂从洗脱室和/或pcr小瓶10260中损失。
传送端口10270的第一端部10271设置在pcr小瓶10260外部,并且传送端口10270的第二端部10272设置在pcr小瓶内。更具体地,第二端部分10272设置在pcr小瓶10260内,使得可以在其内设置样品的pcr小瓶10260的容积v不大于预定量级。以此方式,由于pcr小瓶10260内样品之上存在有限的“顶部空间”,因而可以使热循环期间可能形成在pcr小瓶10260的壁上的冷凝最小化和/或得以消除。
pcr模块10200包括传送活塞10240,该传送活塞10240构造成在洗脱室和/或pcr小瓶10260内产生压力和/或真空,以将洗脱室内的样品和/或试剂的至少一部分如上所述地传送至pcr小瓶10260。
与药筒1001一起使用的洗脱缓冲液储存在分离室10100的洗脱室(图85至图87未示出)中。pcr试剂以冻干的形式储存在pcr小瓶10260中,如上所述。在使用中,经分离的核酸从洗脱室中的捕获珠中洗脱。经洗脱的核酸随后如上所述地传送到pcr小瓶10260中,并且与pcr小瓶10260内的pcr试剂混合。
尽管pcr模块6200示出和描述为包括邻近壳体6210(参见例如图8)的第一端部6211设置的三个试剂室6213a、6213b和6213c,但在其它实施方式中,pcr模块可以包括以任何位置和/或方向设置的任何数目的试剂室或模块。此外,在一些实施方式中,可以偏置试剂柱塞(例如,柱塞6214a)和/或本文中描述的任何传送机构。例如,图88为联接至分离模块6100’的pcr模块11200的剖视图。pcr模块11200包括壳体11210,该壳体11210限定其内可以储存本文中描述的类型的物质和/或试剂的三个试剂室11213。每个试剂室11213内设置有柱塞11214和弹簧11215(在图88中仅示出和标记出一个)。以此方式,柱塞(或传送机构)被偏置在非致动位置中。然而,在其它实施方式中,可以将柱塞偏置在致动位置中,并且可以通过锁定突片等保持就位。以此方式,柱塞的致动可以由弹簧力辅助。
pcr模块还包括经由喷嘴11131与洗脱室6190’流体连通的混合机构(或传送机构)11130。吸移管11250将洗脱室6190安置成与pcr小瓶11260流体连通
在一些实施方式中,pcr模块可以包括邻近分离模块的洗脱室设置的pcr小瓶或反应室。例如,图89示出药筒12001,该药筒12001具有联接至pcr模块12200的分离模块6100’。pcr模块12200包括邻近洗脱室6190’的pcr室12260。类似陈述地,当pcr模块12200联接至分离模块6100’时,pcr小瓶12260设置在pcr试剂室12231与分离模块6100’之间。
尽管本文中示出和描述的药筒包括分离模块,该分离模块包括联接至pcr模块的洗脱室(例如,洗脱室7190),使得在使用中经分离的样品的一部分传送到pcr小瓶中(例如,pcr小瓶7260),但在其它实施方式中,pcr模块无需包括pcr小瓶。例如,在一些实施方式中,药筒可以包括也构造为其内可以发生pcr的反应容积的洗脱室。例如,图90示出了根据实施方式的药筒13001,该药筒13001包括分离模块6100’和pcr模块13200。pcr模块13200包括基底13220和一系列的试剂模块13270。在使用中,试剂模块13270构造成将本文中所示出和描述的类型的一种或更多种试剂和/或物质经由流动管13229传送到分离模块6100’的洗脱室6190’中。以此方式,pcr可以在洗脱室6190’中发生。在这种实施方式中,类似于仪器3002的仪器可以构造成热循环洗脱室6190’以促进pcr。此外,仪器可以包括光学组件,该光学组件构造成光学地监测洗脱室6190’内的反应。在一些实施方式中,壳体6110’可以包括设置在壳体6110’内邻近洗脱室6190’的位置处的激发光学构件(未示出)和/或检测光学构件(未示出)。
尽管本文中示出和描述的药筒通常包括与分离模块串联联接的pcr模块,但在其它实施方式中,药筒可以包括以任何方向、位置和/或定位联接至分离模块的pcr模块。类似陈述地,尽管药筒在本文中示出和描述为包括联接至分离模块的端部的pcr模块,但在其它实施方式中,pcr模块可以以任何方式与分离模块整合和/或联接至分离模块。例如,图91示出药筒14001,该药筒14001包括分离模块14100和pcr模块14200。分离模块14100包括与上文描述类似的一系列的洗涤机构14130。pcr模块包括一系列的试剂模块14270。试剂模块14270设置成邻近洗涤机构14130和/或位于洗涤机构14130之间。
在使用中,试剂模块14270构造成将本文中示出和描述的类型的一种或多种试剂和/或物质经由流动管14229传送到分离模块14100的洗脱室14190中。以此方式,pcr可以在洗脱室14190中发生。
图92和图93示出另一实施方式,其中,pcr模块15200的试剂模块15270设置成邻近分离模块15100的洗涤机构15130和/或位于分离模块15100的洗涤机构15130之间。药筒15001不同于药筒14001之处在于容纳在试剂模块15270内的物质经由一系列的内部流动路径15228传送到pcr小瓶15260中。pcr模块包括用于将经分离的样品的一部分从洗脱室15190传送到pcr小瓶15260中的传送机构15235。
尽管本文中示出和描述的pcr模块包括单个pcr小瓶,但在其它实施方式中,pcr模块可以包括任何数目的pcr小瓶。图94中示出了一个示例,其示出具有四个pcr小瓶16260的pcr模块16200。
尽管以上描述了各种实施方式,但应当理解的是,这些实施方式仅通过示例而并非限制的方式呈现。其中,以上描述的方法和/或简图指示以某顺序发生的某些事件和/或流线图,可以修改某些事件和/或流型的顺序。另外,当可能的情况下,某些事件可以并行的过程同时进行,以及可以顺序地进行。尽管已经具体地示出和描述了实施方式,将会理解的是,可以在形式上和细节上作出各种改变。
尽管本文中描述的许多室——例如室6163a、洗涤缓冲液模块7130a和试剂模块7270a——被描述为容纳物质、样品和/或试剂,许多室通过可刺穿构件(例如,可刺穿构件6170、可刺穿构件7135a和可刺穿构件7275)维持流体隔离,但在一些实施方式中,本文中的任何室可以仅部分地填充有所需的物质、样品和/或试剂。更具体地,本文中描述的任何室可以包括第一容积的所需物质(其通常为液体状)和第二容积的诸如氧气、氢气之类的气体。这种布置减小了在破裂可刺穿构件之前用于在室内移动传送机构或刺破构件(例如,致动器6166的刺破部6168)的力。更具体地,通过包括室容积的一部分作为气体,当传送机构在室内移动时,气体被压缩以减小室的容积,由此允许刺破构件与可刺穿构件接触。在一些实施方式中,在本文中描述的任何室都可以包括其内容积的约百分之十的气体。
尽管分离模块6100在上文示出和描述为包括传送组件6140a,其构造成在裂解室6114与洗涤室6121之间传送物质的的同时维持裂解室6114与洗涤室6121基本上流体隔离,但在其它实施方式中,本文中描述的任何模块可以包括在这些室之间传送物质的同时允许这些室之间流体连通的传送机构。例如,在一些实施方式中,模块可以包括构造成选择性地控制物质在第一室与第二室之间流动的传送机构。这种传送机构可以包括例如阀。
尽管药筒在本文中示出和描述为包括在被设置在操纵药筒的仪器内之前联接在一起的多个模块(例如,分离模块和反应模块),但在其它实施方式中,药筒可以包括多个模块,所述多个模块中的至少一个模块构造成在仪器内联接至另一模块和/或通过仪器联接至另一模块。类似地,在一些实施方式中,仪器可以被构造成将一个模块(例如,试剂模块)联接至另一模块(例如,反应模块、分离模块等)作为药筒的处理的一部分。
尽管诸如传送组件6140之类的传送机构在本文中示出和描述为使用磁力来促进样品的靶部分在药筒内的运动,但在其它实施方式中,本文中示出的和描述的任何传送机构可以使用任何适当类型的力来促进样品的靶部分在药筒内的运动。例如,在一些实施方式中,传送机构可以包括泵。在其它实施方式中,传送机构可以产生样品的靶部分的蠕动运动。
尽管第一加热模块3730在上文中描述为构造成产生特定的pcr温度升温速率,但在其它实施方式中,第一加热模块可以通过任何适合的pcr升温速率热循环pcr小瓶或pcr样品。例如,尽管描述为产生基本上比用于冷却样品的pcr升温速率大的用于加热样品的pcr升温速率,但在其它实施方式中,第一加热模块可以产生基本上与用于冷却的pcr升温速率相同的用于加热的pcr升温速率。在又一实施方式中,用于冷却样品的pcr升温速率可以基本上大于用于加热的pcr升温速率。此外,第一加热模块3730操作性地联接至仪器的控制系统(参见例如图71至图73),使得pcr样品的pcr升温速率可以被精确地且准确地控制。在一些情况下,控制可以基于第一加热模块3730的一部分——例如块体3710——的温度测量值。
尽管描述了药筒和/或其部分主要用于与核酸分离和扩增反应一起使用、并且用于与本文中的所描述的特定仪器一起使用,但药筒并不限于此。尽管描述了仪器和/或仪器的部分主要用于与核酸分离和扩增反应一起使用、并且与本文中描述的特定的药筒一起使用,但该仪器并不限于此。
在一些实施方式中,一种设备包括第一模块、第二模块和第三模块。第一模块限定第一室和第二室,至少第一室构造成容纳样品。第二模块限定第一容积,该第一容积构造成容纳第一物质。第二模块的一部分构造成在第二模块联接至第一模块时设置在第一模块的第一室内,使得第一容积构造成选择性地安置成与第一室流体连通。第三模块限定反应室和第二容积,该第二容积构造成容纳第二物质。第三模块的一部分设置成在第三模块联接至第一模块时位于第一模块的第二室内,使得反应室和第二容积各自与第一模块的第二室流体连通。
在一些实施方式中,本文中描述的任何模块可以包括构造成将声学能传送到由模块限定的室中的声学联接构件。
在一些实施方式中,本文中描述的任何模块可以包括构造成在模块内的第一室与模块内的第二室之间传送样品的传送机构。这种传送机构可以使用用于传送包括溶液流、磁力等的物质的任何适合的机构。
在一些实施方式中,本文中描述的任何模块可以包括构造成在模块内的第一室与模块内的第二室之间传送样品的阀。在一些实施方式中,这种阀可以构造成维持第一室与第二室之间的流体隔离。
在一些实施方式中,一种设备包括第一模块、第二模块和第三模块。第一模块限定第一室和第二室。第一模块包括第一传送机构,该第一传送机构构造成在在第一室与第二室之间传送样品的同时维持第一室和第二室之间流体隔离。第二模块限定构造成容纳物质的容积。第二模块的部分构造成在第二模块联接至第一模块时设置在第一模块的第一室内,使得该容积构造成选择性地安置成与第一室流体连通。第三模块限定反应室,第三模块构造成联接至第一模块,使得反应室与第二室流体连通。第三模块包括第二传送机构,该第二传送机构构造成在第二室与反应室之间传送样品的一部分。
在一些实施方式中,一种设备包括第一模块和第二模块。第一模块包括反应小瓶、基底和第一传送机构。反应小瓶限定反应室。第一传送机构包括柱塞,该柱塞可移动地设置在壳体内,使得壳体和柱塞限定第一容积,该第一容积容纳第一物质。基底限定第一流动路径和第二流动路径的至少一部分。第一流动路径构造成与反应室流体连通。第一容积和分离模块的分离室、第二流动路径构造成与分离室流体连通。柱塞的一部分设置在第一流动路径内,使得当柱塞处于壳体内的第一位置时第一容积与反应室流体隔离。柱塞的该部分设置成与第一流动路径间隔开,使得当柱塞处于壳体内的第二位置时第一容积与反应室流体连通。柱塞构造成在反应室内产生真空,以在柱塞从第一位置移动至第二位置时将样品从分离室传送至反应室。第二模块包括第二传送机构并限定第二容积,该第二容积构造成容纳第二物质。第二模块构造成联接至第一模块,使得第二容积可以选择性地放置为经由第二流动路径与分离室流体连通。第二传送机构构造成在第二传送机构被致动时将第二物质从第二容积传送至分离室。
在一些实施方式中,一种仪器包括块体、第一光学构件、第二光学构件和光学组件。块体限定反应容积,该反应容积构造成接纳反应容器的至少一部分。第一光学构件设置成至少部分地位于块体内,使得第一光学构件限定第一光路并且与反应容积光学连通。第二光学构件设置成至少部分地位于块体内,使得第二光学构件限定第二光路并且与反应容积光学连通。包括第一光路的第一平面和包括第二光路的第二平面限定大于约75度的角度。光学组件联接至第一光学构件和第二光学构件,使得激发光束可以传送到反应容积中并且可以从反应容积中接收照射光束。
尽管仪器(例如,仪器3002)在上文示出和描述为构造成操纵和/或致动一个或多个药筒(例如,药筒7001)以产生单个仪器内的和/或单个药筒内的核酸分离、pcr和光学检测,但在其它实施方式中,本文中描述的任何步骤和/或功能可以通过多个不同的仪器和/或多个不同的药筒来执行。例如,在一些实施方式中,第一仪器可以操纵和/或致动药筒以进行核酸分离和/或pcr,第二仪器可以操纵药筒或药筒内的样品室以光学地分析样品。类似陈述地,在一些实施方式中,系统可以包括处理子系统,该处理子系统与检测子系统分开,其中,处理子系统和检测子系统各自构造成接收和/或操纵普通样品药筒。
例如,本文中提供的药筒、仪器和/或其部分可用于下一代测序(ngs)平台。已经报道了ngs技术用于产生比sanger法多出三至四个数量级的序列,并且还更低廉地进行。ngs技术包括但不限于基因组鸟枪法测序、细菌人工染色体(bac)末端测序、单核苷酸多态性发现和再测序、其它突变发现、染色质免疫沉淀(chip)、微rna发现、大规模表达序列标签测序、引物步移、或基因表达系列分析(sage)。
在一个实施方式中,本文中描述的任何pcr模块可构造成在ngs平台仪器内使用、用于核酸序列分析。替代性地,在其它实施方式中,pcr模块可构造成与样品传送模块(例如,自动液体操作仪器)配合以将pcr模块内的核酸扩增产物传送至流动池或ngs仪器的其它检测装置。
在一个实施方式中,模块提供为使得本发明的药筒可以构造成与一个下述ngs平台一起使用:roche454gs-flx平台、illumina测序平台(例如,hiseq2000、hiseq1000、miseq、基因组分析仪iix)、illuminasolexaig基因组分析仪、appliedbiosystems3730xl平台、abisolidtm(例如,5500xl或5500solidtm系统)。该模块可配合到前述装置之一,或者可以构造成与样品传送模块相配合,所述样品传送模块将核酸扩增反应的产物从pcr模块移动至ngs仪器。
在一个实施方式中,本发明的药筒用于基因组鸟枪法测序、细菌人工染色体(bac)末端测序、单核苷酸多态性发现和再测序、其它突变发现、染色体免疫沉淀(chip)、微rna发现、大规模表达序列标签测序、引物步移、或基因表达系列分析(sage)。
在一个实施方式中,如本文中描述的,在本发明的药筒和仪器中进行核酸分离和/或扩增(例如,pcr)。在进一步的实施方式中,在扩增反应结束时,样品传送模块将扩增产物传送至各ngs仪器的流动池,用于文库制备和随后的测序。
在另一个实施方式中,如本文中描述的,在本发明的药筒和/或仪器中进行核酸分离和/或扩增(例如,pcr)。在进一步的实施方式中,在完成扩增反应后,将药筒传送至可负责与以上提供的ngs仪器之一一起使用的模块中。核酸扩增产物随后传送至各ngs仪器的流动池,用于文库制备和随后的测序。
例如,图95示出了包括分离/pcr仪器10,002、检测仪器10,003和中央计算机10,004的系统10,000。分离/pcr仪器10,002和检测仪器10,003各自包括构造成接收普通药筒的接收部10,319(图95未示出)。该药筒可以是本文中示出和描述的任何药筒。分离/pcr仪器10,002可以包括本文中描述的仪器(例如,仪器6002和/或仪器7002)的任何部件和/或功能。检测仪器10,003也可以包括本文中描述的仪器(例如,仪器6002和/或仪器7002)的任何部件和/或功能。然而,在一些实施方式中,检测仪器10,003可以包括流通式基于珠的流体系统,该系统可以允许对药筒中的每个样品井顺序采样。包括在每个子系统中使用的普通样品处理药筒的这种布置可以允许不同的检测系统与分离/pcr仪器一起使用,并且反之亦然。
尽管系统10,000示出为包括单独的分离/pcr仪器10,002和检测仪器10,003,但在其它实施方式中,系统可以在单个仪器内包括分离/pcr部件和检测部件二者。例如,仪器7002构造成操纵一系列的药筒,以进行核酸分离、pcr和检测。尽管仪器7002构造成在pcr操作与检测操作之间将药筒维持在基本上固定的位置处,但在其它实施方式中,集成的系统可以包括用于在分离和/或pcr操作和检测操作之间移动药筒的机构。例如,图96示出仪器11,002,该仪器11,002构造成在分析的各个阶段之间移动药筒和/或容纳在其内(图96中未示出)的样品。
示例
本发明通过参照以下示例进一步说明。然而,应当指出的是,这些示例与上文中描述的实施方式类似,都是说明性的而不应解释为以任何方式限制本发明的范围。
示例1-用于对药筒和容纳多个药筒的盒进行操纵的仪器
在一些实施方式中,包括多个药筒(例如,两个、三个、四个、五个、六个、七个、八个、九个或十个药筒)的盒被插入到对盒内的每个单独的药筒进行操纵的仪器中。取决于仪器的结构,多个盒可以被插入到仪器中。
该仪器包括在每个盒处理模块中的九个部件(也称为子组件)。如以上所述,仪器可以具有多个处理模块(即,每个盒关联于单个处理模块)。子组件包括:(1)热控制电子器件;(2)侧泵子组件,(3)cpu和硬盘驱动器;(4)运动控制电子器件;(5)底架子组件;(6)光学子组件;(7)顶泵子组件;(8)用于盒/药筒插入的模块;(8)超声裂解模块和/或(10)pcr热子组件。
如以上所提供的,仪器包括用于各盒的分开的处理模块。另外,每个仪器包括用于对每个单独的药筒或盒的一个或多个室进行热循环的加热和冷却元件。因此,热循环对于每个盒或对于盒内的每个药筒独立地进行。
每个药筒在插入到仪器中之前容纳要被在药筒室的一个室中分析的特定样品。仪器包括用于操作药筒或多个药筒、以及容纳在药筒内的样品和溶液的结构和部件。一旦样品药筒或多个药筒装载到仪器中,样品就在药筒内被操作,例如,通过裂解样品、从整个样品中分离核酸、以及将成分在药筒内从室传送至室或从一个药筒传送至另一个药筒。这种过程可以使用本文中描述的任何药筒和/或仪器来执行。例如,仪器包括设计成将全部的或部分的样品从一个药筒室传送至另一药筒室、或传送至分开的药筒中的室的一个或多个传送组件。仪器也包括一个或多个超声报警器,并且该各超声报警器与各药筒或盒相关联。
在一些实施方式中,例如鼻咽样品的样品通过在药筒内将裂解剂传送到样品室中或将样品传送到裂解剂室中或通过将裂解剂从一个药筒传送到另一药筒中的样品室或将样品从一个药筒传送到另一药筒中的裂解剂室而裂解。仪器包括用于混合试剂或将试剂从药筒的一个区域移动至另一区域的结构。例如,仪器包括一个或多个柱塞,以在药筒内将试剂从室传送至室。
在该示例中,首先从样品中分离(例如从鼻咽样品中分离)核酸(核酸的子集,例如特异性核酸序列,或者总核酸如总dna、mrna、rrna或总rna)。在该示例中,磁珠用于结合核酸。核酸随后传送至药筒的另一部分用于下游处理,例如核酸的扩增和检测。
核酸的扩增和检测在药筒中执行,例如,通过检测之后进行的聚合酶链反应(pcr),或在pcr(实时pcr)过程期间进行检测。仪器包括与一个或多个药筒的一个或多个室接触的个或多个加热/冷却元件。因此,在多个药筒的情况下,热循环对于每个药筒——即,对于每个pcr反应——可以独立地进行。
检测选项
在pcr发生的室中、或在不同的室中(在同一药筒中、同一盒的不同药筒中或者仪器的分开的室中)进行pcr产物的检测。此外,pcr产物的检测可以在反应期间进行(实时检测)或当pcr反应结束时进行(结束点检测)。
相同药筒内的检测
可以与仪器3002相似的仪器包括至少四个荧光激发通道和四个荧光发射过滤器,以允许检测多个靶(即,每个用荧光分子标记的靶与唯一的发射和激发过滤器组合相关联)。激发通道包括发光二极管(led)和独特的过滤器,使得每个激发通道发射不同波长的光。为了检测一个样品中的多个产物,药筒定位成以串联方式邻近每个led,通过使用步进运动驱动的导向螺杆来移动药筒或光学检测模块。因此,光学检测模块可以从药筒至药筒移动,或替代性地,药筒可以在仪器内移动以与光学检测模块对准。荧光强度通过特定发射过滤器(例如通过ccd相机)测量。结果会被上传至计算机。
示例2-在一个仪器中的核酸处理和扩增以及在第二个仪器中的检测
在一些实施方式中,方法包括如在示例1中所提供的制备和扩增样品。此外,在pcr期间,采用了荧光标记的引物使得反应产物被荧光标记。引物设计成使得反应产物包括突出序列,使得最终双链产物包括单链的部分。
方法还包括使单链部分与经互补于各pcr产物的单链部分的序列衍生的磁珠相杂交。磁珠可以在pcr之前或在pcr之后添加至样品中。所述珠可以被添加至药筒的其内进行pcr的同一室中或分开的室中。例如,在一些实施方式中,磁珠可以设置在药筒的洗脱室内(例如,类似于以上描述的室7190的室),使得当样品被传送至pcr小瓶(例如,pcr小瓶7260)中时存在用于如下文描述的pcr后检测操作的磁珠。在其它实施方式中,磁珠可以储存和/或设置在pcr小瓶(例如,小瓶7260)内,使得当样品传送到pcr小瓶中时存在用于pcr后检测操作的磁珠。在又一些其它实施方式中,磁珠可以储存和/或设置在试剂模块(例如,试剂模块7270a和/或7270b)内或储存和/或设置在由传送机构(例如,传送机构7235)限定的容积内。以此方式,磁珠可以在任何适合的时间或以任何适合的方式运送到pcr小瓶中,以促进如本文中描述的pcr后检测操作。
用于pcr后检测操作的磁珠可以是任何适合的珠或颗粒。例如,珠可以包括多种不同类型的珠,每种类型具有不同的结合能力和/或构造成产生不同的光学信号。例如,在一些实施方式中,珠可以由聚苯乙烯和磁铁构成。珠可以包括例如第一组和第二组,第一组杂交和/或配制成具有第一结合能力(例如,结合单个靶分子的能力),第二组杂交和/或配制成具有第二结合能力(例如,结合两个靶分子的能力)。此外,不同的珠类型各自可以具有不同的染料或标记,使得在下述光学检测期间可以区分不同的类型。
一旦pcr产物被标记,将将盒(例如,包含六个药筒的盒)传送至另一阅读器,例如,经修改的luminex
在一些实施方式中,药筒壳体限定开口和吸入端口(例如,可刺破隔板),在该开口和吸入端口内可以设置外部探针以吸入用于检测的pcr产物。药筒可以是本文中示出和描述的类型的任何适合的药筒。例如,图97a至图97d示出药筒7001’,该药筒7001’在许多反面类似于上文示出和描述的药筒7001,并因而在本文中不进行详细描述。药筒7001’包括壳体7220’(也称为基底),该壳体7220’具有吸入部(或“传送端口”)7277c。吸入部7277c限定吸入空腔或容积7278,并且具有构造成如本文中所描述地接纳传送探针10,006的端口。可以包括多个层的壳体7220’限定第一流动路径7222’和第二流动路径7221b’。pcr小瓶7260联接至壳体7220’,使得pcr小瓶7260与分离模块的分离室7190’如以上所述地流体连通。吸入空腔经由第二流动路径与pcr小瓶7260流体连通。
如图97a中所示,传送探针10,006沿箭头kkk的方向移动,以接合壳体7220的吸入部7277c的端口或设置在接合壳体7220的吸入部7277c的端口内,从而将传送探针安置成处于第二构型(图97b)。更具体地,传送探针10,006可以包括刺破端10,007,该刺破端10,007构造成接合设置在壳体7220内和/或位于壳体由其构造的层之间的可刺穿构件7275c(参见图97c)。因此,如图97b和图97c所示,吸入部7277c和可刺穿构件7275c可以共同形成吸入空腔7278的边界。此外,可刺穿构件7275c将第二流动路径7221b’和/或pcr小瓶7260与吸入部7277c的开口流体隔离。因此,传送探针10,006沿箭头kkk(图97a)方向的运动使得刺破端10,007刺破和/或移动穿过可刺穿构件7275c并且设置在吸入空腔7278内(参见图97c)。
随着刺破端10,007设置在吸入空腔7278内,传送探针可以经由第二流动路径7221b’并且通过由传送探针限定的管腔10,008从pcr小瓶7260吸入pcr样品的一部分。类似陈述地,传送探针10,006可以将负压引入吸入空腔7278中使得pcr样品的一部分从pcr小瓶7260被抽出并进入由传送探针10,006限定的管腔10,008中。以此方式,传送探针10,006可以被致动和/或在仪器(例如,仪器3002或仪器10,003)内移动以将pcr样品的一部分传送到光学阅读装置中。所传送的样品可以随后经由传送探针10,006运送到阅读仪器的样品检测室(例如,图97d中示出的样品检测室10,009)中。在传送针或传送探针10,006将标记的pcr产物传送至第二仪器10,003的光学模块(样品检测室、磁体、led、ccd相机)之后,根据用于阅读仪器(例如
在一些实施方式中,药筒7001’包括类似于传送探针10,006、构造成与吸入部配合的集成的传送探针。在这种实施方式中,第二仪器(例如,第二仪器10,003)无需包括类似于将pcr产物从药筒7001’传送到检测室10,009中的传送探针10,006的传送探针。
在一些实施方式中,可刺穿构件无需设置在壳体7220的层之间。例如,在一些实施方式中,吸入部可以包括与上文描述的试剂壳体7277b相类似的端口。在这种实施方式中,端口可以包括设置在端口的底部与壳体7220的上表面之间的可刺穿构件(类似于可刺穿构件7275b)。因此,可刺穿构件7275c围绕“端口壳体”7277b的端部设置,使得传送探针10,006的刺破端10,007可以刺穿、破坏、刺破和/或以其它方式移动通过可刺穿构件7275c。
如在图97a至97d中所示,药筒7001’还包括类似于上文示出和描述的传送机构7235的传送机构7235’。此外,壳体7220限定第三流动路径7221a’,物质(例如,矿物油、硅油、磁珠或用于在标记pcr产物中使用的物质等)可以通过该第三流动路径7221a’从传送机构7235’运送到pcr小瓶7260中,如以上参照传送机构7235的操作所描述的。
示例3-在集成的仪器中的核酸处理、扩增和检测
在该示例中,样品处理和pcr产物标记如对于示例2所描述地进行。然而,代替在标记pcr产物后将药筒和/或盒传送至其它仪器,采用了单个仪器并且样品制备和检测在该单个仪器中进行(比如图96示出的集成的仪器11,002)。由此,该仪器被整合并且包括样品制备模块、pcr模块、和光学模块(可以与存在于luminex’s
传送针(或如示例2中描述的传送探针)将标记的pcr产物传送至仪器的光学模块。随后根据
示例4-在单个药筒和集成的仪器中的核酸处理、扩增和流动池检测
尽管某些实施方式在上文示出和描述为包括在其内执行(例如,通过仪器3001)pcr和光学检测的单个室(例如,pcr小瓶7260),但在其它实施方式中,方法包括在反应容积中执行pcr、将标记的pcr产物传送至检测容积、并且随后执行pcr产物的分析(例如,光学分析)。此外,在一些实施方式中,该过程可以在单个药筒中或模块中执行,使得样品在从pcr小瓶(或反应室)传送至检测容积时未由外部部件(例如,传送探针、吸移器等)处理和/或暴露于药筒的外部环境。
例如,图98、图99a和图99b示出药筒17001,该药筒17001具有区别于(例如,在不同的空间位置区别于)检测容积的反应容积。在一些实施方式中,药筒17001可以用于如以上对于示例2和示例3所描述地处理样品和执行pcr产物标记。药筒17001可以基本上类似于以上描述的药筒7001,因而在本文中不进行详细描述。例如,药筒17001可以包括任何适合的试剂模块,例如与上文示出和描述的试剂模块7270c类似的试剂模块17270c。药筒17001可以包括传送机构,比如与上文示出和描述的传送机构7235类似的传送机构17235。此外,药筒17001包括与本文中描述的pcr小瓶7260基本上类似的pcr小瓶17260。以此方式,药筒17001可以以本文中描述的方式类似的方式被操纵(例如,通过仪器3002)。
然而,药筒17001与药筒7001不同之处在于药筒17001包括流动池部17903,在该流动池部17903内可以发生检测和/或分析。进一步展开,药筒17001包括壳体17220、第一传送机构17235、第二传送机构17904。壳体17220包括延伸部或端部17902,该延伸部或端部17902构造成从药筒17001的一部分延伸,使得药筒17001的流动池部17903可以通过光学检测系统(未示出)接合。类似陈述地,如以下描述的,流动池部17903包括在突出端部17902内,由此提供基本上无障碍地通向流动池部17903的检测容积17910。
如图99a中所示,壳体17220包括第一层(或基体)17907和第二层17909。壳体17220(和/或第一层17907和第二层17909)限定第一流动路径17906和第二流动路径17905。更具体地,第一流动路径17906与pcr小瓶17260(即,反应容积)和检测容积17910流体连通。由此,样品可以从反应容积经由第一流动路径17906运送至检测容积17910。第二流动路径17905与传送机构17904和流动池部17903的检测容积17910流体连通。以此方式,当传送泵17904被致动时,pcr小瓶17260内的样品的一部分(例如,标记的pcr产物)可以被运送到流动池部17903中和/或检测容积17910中。
如图99a中所示,第一流动路径17906和/或第二流动路径17905限定多个方向的流动路径。以此方式,当传送机构被致动时,标记的pcr产物的第一部分在第一流动路径17906内沿第一方向流动,并且标记的pcr产物的第二部分(和/或废产物)在第二流动路径17905内沿与第一方向相反的第二方向流动。以此方式,延伸部17902的延伸超过药筒17901的该部分的距离可以控制成容置其内放置药筒17001的仪器(该仪器在图98中未示出)的检测设备。在一些实施方式中,延伸部17902可以构造成从药筒17001的一部分延伸所需的距离,使得延伸部可以与光学模块等配合。
如上所述,传送机构17904将标记的产物从pcr小瓶17260移动至流动池17903,该流动池17903整合在药筒17001中。特别地,传送机构包括柱塞,该柱塞如由图99a中箭头zzz所示地向上移动,这在流动池部17903的检测容积17910内产生真空。此外,柱塞的运动开放传送机构17904内的容积,样品的一部分和/或废产物可以在穿过流动池部17903之后流动到该容积内。在使用中,在标记的pcr产物的一部分已被运送到检测容积17910中之后,pcr产物可以通过任何适合的机构来检测。
例如,在一些实施方式中,如以上所描述的,pcr产物用磁珠来标记和/或附接至磁珠。所述珠可以包括以上在示例2中描述的类型的一系列杂交检测珠。在这种实施方式中,检测可以包括向限定检测容积17910(例如,第一层17907的一部分)第一表面施加磁场。以此方式,磁性粒子以及粘附至和/或结合至所述磁性粒子的样品可以维持于抵着表面(第一表面或层17907或相反的第二表面,例如,第二层17909)。尽管离子维持在抵着表面的位置,但样品可以由具有任何所需波长的一个或多个光源激发。光学检测系统(例如,ccd相机,光电二极管等)可以随后测量从样品发射出的光,这可以用于产生驻留于检测容积17910内的样品的映射。光学组件可以包括如本文中描述的任何部件。光学组件可以包括例如磁体、一系列的led,ccd相机等。为了允许检测流动池17903中pcr产物,如本文中描述的光学模块3800的结构可以被修改。
在一些实施方式中,例如,样品和珠可以由具有不同波长的多个不同的光源来激发。这可以引起由样品和/或珠产生的不同的光发射,并且可以允许样品的量化和/或准确的特性。
在一些实施方式中,药筒17001可以包括试剂室中的杂交检测珠、pcr小瓶和/或药筒17001的传送机构。例如,在一些实施方式中,珠可以包括在传送机构17904中。因此,在使用中,当传送机构17904的柱塞如由图99中箭头zzz所示向上移动时,样品被吸入传送机构中并且与储存在传送机构中的珠混合。柱塞可以随后沿相反的方向移动以将样品和珠运送到检测容积17910中用于光学检测。在其它实施方式中,珠可以包括在试剂模块17270c中,该试剂模块17270c用本文中描述的可刺穿构件密封。以此方式,珠以及将所述珠容纳在内的溶液可以与药筒17001的结构分开地包装,并且可以随后联接至如本文中描述的药筒。
传送机构17904为以上在示例2中描述的类型的一系列的杂交检测珠。
流动池17903设计成使得标记的产物积聚在读取区域17910中的同时仍允许流动发生(例如,通过第一流动路径17905和第二流动路径17906)。类似陈述地,以上提出的布置允许废物和/或回流积聚在传送机构17904内、pcr小瓶17260内或药筒17001内的任何其它适合的室内。在一些实施方式中,流动池部17903可以包括流动结构(例如,障碍物,产生弯曲路径等的一系列结构),该流动结构限制和/或控制磁性离子穿过检测容积。以此方式,流动池部17903可以构造成基于流式细胞技术原理与检测系统一起使用。
示例5-解链退火分析
除了荧光检测外,本文中提供的仪器用于解链/退火分析。这种分析在非流动池(示例2和示例3)中进行或者在具有流动池部(示例4)的药筒中进行。在这种实施方式中,加热元件定位成使得该加热元件与药筒的一部分——该部分容纳被检测的标记的pcr产物——接触。然而,元件可以被构造成允许光学通向标记的产物。各加热元件的温度以逐渐的方式增大并且荧光在阶梯式增大之后测量。为了减小少背景荧光,在每个检测阶段之间施行洗涤步骤,以洗掉非杂交的产物。在这种实施方式中,冲洗溶液可以经由以上描述的机构从试剂模块(例如。模块17270c)运送到流动池部(例如,流动池部17903)中。替代性地,洗涤缓冲液可以在解链/退火分析期间连续地施加至流动池17903,以洗涤掉非杂交产物。
洗涤缓冲液和非杂交产物经由出口和/或第二流动路径17905流出流动池17903,或流出流动池17903的读取区域17910进入囊状件或波纹管状件。然而,在一些实施方式中,珠在洗涤后保持就位于检测容积17910中,使得pcr产物未被洗涤掉(例如,存在有磁体以将珠保持就位,或珠由于流动池17903内的结构元件而被保持就位)。
示例6-流动池设计-压纹壁
在一些实施方式中,限定流动池17903的检测容积17910的侧壁(例如,第一层17907和/或第二层17909)可以在其内具有压纹孔(well)以将珠定位在表面上的紧密阵列中。以此方式,流动池部17903的设计在读取标记产物的荧光时能够增大信噪比。孔的尺寸由使用的珠的直径和/或仪器的检测极限来确定。孔中可以存在有多个珠,或者每个孔中可以存在一个珠。所述珠由磁力或压力(例如,通过真空)保持就位。由此,尽管本文中称为流动池部17903,但光学检测无需在样品和/或珠移动(例如,“流动”)时发生,而是可以在由外力(例如,磁力)、压纹孔和/或任何其它适合的机构将样品和/或珠维持在基本上静止的位置的情况下发生。
示例7-流动池设计-柔性壁
在一些实施方式中,流动池部17903和/或检测容积17910可以不包括出口、但可以替代地具有用于积聚流体(例如,废弃流体、载送流体等)的可膨胀的和/或柔性的构件。例如,图100至图103中示出流动池部的多种示例,其中,限定检测容积的一个或多个壁由柔性的和/或顺性的材料构成。以此方式,流动池部的容积和/或检测容积可以在样品于其内运送时增大。特别地,图100、图101a和图101b示出包括柔性壁17908的流动池部17903’,该柔性壁17908至少部分地限定检测容积17910’。出于成像的目的,这种柔性允许壁17908变形成平坦表面。压力(例如,真空、磁力等)用于通过抵靠平坦表面或基体17907’拉动流动池壁17908来保持壁17908平坦,该基体17907’限定流动池17903’的检测容积17910‘的边界的一部分。在成像期间施加压力,并且也可以在如由图100中箭头lll所指示地将标记的pcr产物传送至流动池部17903’期间施加压力。在一些实施方式中,成像的方向可以与由箭头mmm所指示的施加压力的方向基本上相反。在一些实施方式中,基体17907’可以为基本上刚性的(例如,不构造成在仪器内变形)。
示例8-流动池的容纳
在一些实施方式中,流动池部17903的壁17908是可膨胀的(例如,流动池17903的壁17908限定可膨胀的囊状件)。如图101a中所示,当样品引入流动池部17903”中时,壁17908”被移动成膨胀的构型。流动池17903的读取区域17910可以是压纹的或者可以是柔性的,如以上所述。标记的样品可以通过真空压力、泵送机构(例如,传送泵17904),或者任何其它方式进入囊状件。在一些实施方式中,囊状件的尺寸通过一组容纳壁17909”和/或围绕限定囊状件的壁17908”的表面来控制,如图102a中所示。因此,在这种实施方式中,囊状件仅膨胀到由容纳表面17909”和基体17907”的表面所允许的尺寸。
在一些实施方式中,替代性囊状件的尺寸不由围绕囊状件的容纳表面17909容纳。而是,囊状件的尺寸基于标记的产物的流动率和/或囊状件的原始尺寸来控制。
在流动池中使用的另一囊状件用于当珠被拉动流动池的读取区域17910”中时或当珠被泵送到流动池17903”’的读取区域17910”(图102b)中时捕获过量的试剂。进一步扩展地,在这种实施方式中,读取区域17910”’可以由基部17907”’(或壳体的第一层)中的凹部限定。以此方式,标记的产物可以如由箭头nnn所指示地流动通过第一流动路径17906”’而进入检测容积17910”’。过量的试剂可以流动通过第二流动路径17905”’而进入由流动池17903”’的壁17908”’限定的囊状件。在这种实施方式中,成像方向可以基本上与囊状件相反,如由箭头ooo所指示的。此外,囊状件并不包含用于使过量流体离开的出口而是流体积聚在囊状件中。
如图103中所示,在一些实施方式中,流动池部19903包括波纹管状件19911以便捕获流入到流动池19903中的过量的试剂。波纹管状件19911用于在珠被运送到检测容积或流动池部19903的读取区域19910中时捕获过量的试剂。在一些实施方式中,联接机构19912用于将波纹管状件19911膨胀至所需的容积。联接机构19912可以为任何适合的构型。在其它实施方式中,任何适合的装置均能够被用于膨胀波纹管状件19911。此外,流动池19903无需包括用于使过剩的流体离开的出口,因此,流体积聚在波纹管状件内。
示例9-将标记的产物传送至流动池
为了在将珠传送至流动池部(例如,以上在示例4至示例8中描述的)之前和/或在将珠传送至流动池部期间保持珠悬浮在样品内,在一些实施方式中,仪器可以包括磁性地联接的混合物。例如,在一些实施方式中,磁性地联接的混合物17913可以定位在pcr小瓶17260正下方,如图104中示出的。在一些实施方式中,小的混合物体放置在珠被杂交的隔室中并且可以构造成沿箭头ppp所示的方向旋转。如以上所述,珠在pcr小瓶17260中或药筒的一些其它隔室(图104中未示出)中被杂交。在不希望受理论限制的情况下,混合可以加速珠与pcr产物的杂交。混合物17913在传送到流动池(图104中未示出)中之前也可以用于使珠悬浮在溶液中。在一些实施方式中,如上文描述地完成传送(例如,通过传送泵17904)。
在其它实施方式中,如上所述,可以在传送机构17904内对珠和样品进行搅动以确保珠悬浮在溶液中。
示例10-检测标记的pcr产物
如在之前示例中描述的,存在于药筒中的标记的pcr产物通过传送泵17904(参见图98)传送至集成在药筒17001内的流动池部17903中。在一些实施方式中,仪器可以容纳多个药筒(例如,如本文中所描述地设置在多个药筒的盒中)用于并行处理。一旦标记的pcr产物被合成并传送至流动池部17903,所述产物通过沿着从一个药筒17001到下一个药筒的轴线移动的光学阅读器17914来检测,如由图105中箭头qqq所示。在一些实施方式中,光学阅读器17914具有与本文中描述的其它阅读器相同的部件(例如,led、过滤器、镜子),并且可以在相邻的药筒之间移动。以此方式,光学阅读器17914可以以顺次的方式读取流动池17903的每个读取区域17910。在其它实施方式中,光学阅读器17914可以通过与上文示出和描述的光学系统3800的设计类似的一系列的光学纤维而光学地和/或电子地联接至每个检测容积17910。
示例11-流动池内的截留珠
如图106中所示,在一些实施方式中,流动池17903可以包括任何适合的结构(例如,柱或销),以在仍然允许流体的一部分流动通过流动池17903的同时截留珠和/或限制珠在检测容积17910内的运动。更具体地,包括标记的产物的溶液可以经由第一流动路径17906流动到检测容积17910中(如由箭头rrr指示的),并且溶液的一部分可以经由第二流动路径17905离开检测容积17910(如由箭头sss指示的)。特别地,检测容积17910和/或流动池部17903的其它部分可以容纳定位在读取区域17910下游的柱17915,以阻挡标记的珠17916从流动池17903中逃逸、并因而逸出读取区域17910。
柱17915可以根据被使用的珠的尺寸来制造。此外,柱17915和/或流动结构能够被定位成产生用于维持珠的位置的任何适合的弯曲路径。
示例12-数字pcr
尽管药筒6001和7001在上文中示出和描述为包括在其内(例如,分别在pcr小瓶6260和7260)进行pcr的单个反应室,但在其它实施方式中,药筒或药筒的一部分可以包括可在其内进行pcr的一系列反应室。以这种方式,本文中示出和描述的任何药筒可以用于进行数字pcr。数字pcr是在各反应室中进行一个或零个靶核酸分子扩增的过程。因此,数字pcr对于每个独立反应室提供给使用者是/否的答案,即在样品中是否存在或不存在靶。这个过程还允许绝对拷贝数检测。在一个实施方式中,本文中提供的药筒和仪器用于通过数字pcr对一个或多个核酸分子进行绝对拷贝数检测。在另一个实施方式中,本文中提供的药筒和仪器用于通过数字pcr检测靶核酸中的突变数目。
在一些实施方式中,例如,药筒可以包括扩增模块(比如上述的扩增模块6200或7200),该扩增模块包括与一系列数字pcr反应室流体连接的数字pcr小瓶。数字pcr反应室的容积可以是例如约20微升、约10微升、约1微升、约500nl、小于10微升、小于5微升、小于1微升、小于500纳升、约500nl至约10微升、约500nl至约5微升。在一些这样的实施方式中,数字pcr小瓶包括含有pcr试剂的冻干物质,如上文对于pcr小瓶6260的内含物描述的。在数字pcr实施方式中,核酸模板在一个实施方式中为dna模板。在另一个实施方式中,核酸模板为rna。在又一实施方式中,rna为病毒rna。在一个实施方式中,数字pcr试剂与核酸模板相混合,并且将混合物分装到数字pcr室中和/或运送到数字pcr室中。反应混合物被分装为使得在每个室中可以存在一个或零个核酸靶分子。在分析多个靶的情况下,每个室包含对于每个特异性靶而言的零个或一个核酸分子。
可使用荧光探针实时地监测各反应。例如,在一些实施方式中,该反应通过单链荧光共振能量传送探针(例如,
在一些实施方式中,使用本文中描述的任何药筒和仪器对各室中的多个靶进行数字pcr,并且实时监测反应的过程。在一些实施方式中,靶是来自一种或更多种下述病毒的基因序列:流感a、流感b、呼吸道合胞病毒(rsv)、单纯疱疹病毒1(hsv1)或者单纯疱疹病毒2(hsv2)。在一些实施方式中,在pcr之前,在本文中提供的药筒和/或仪器中进行反转录反应。
图107和图108示出根据实施方式构造成促进数字pcr的药筒18920的示意性图示。数字pcr药筒18920包括第一端部18921、第二端部18922以及基底或壳体18923。第一端部18921构造成接纳pcr小瓶18260和/或联接至pcr小瓶18260。pcr小瓶能够类似于本文中示出和描述的任何pcr小瓶。更具体地,第一端部18921可以通过任何适合的方法联接至pcr小瓶18260。例如,在一些实施方式中,第一端部18921可以与pcr小瓶18260的一部分形成卡扣配合。在其它实施方式中,第一端部18921和pcr小瓶18260的一部分可以形成摩擦配合、螺纹配合等。
第二端部18922包括传送机构18930,该传送机构包括壳体18925和设置在壳体18925内的致动器18926。致动器18926的一部分可以基本上类似于本文中描述的传送机构的一部分(例如,以上参照图29至图31描述的传送机构7235)。由此,致动器18926可以包括下述部分,该部分构造成由仪器接合使得仪器可以在第一构型(图107)与第二构型(图108)之间移动致动器18926。致动器18926还包括密封构件18927,该密封构件18927构造成当致动器18926设置于壳体18925内时接合壳体18925的内表面。由此,密封构件18927形成与壳体18925的内表面的基本上流体紧密密封,如本文中进一步描述的。
数字pcr药筒18920的基底18923构造成基本上在第一端部18921与第二端部18922之间延伸。基底18922的一部分可以基本上类似于上文示出和描述的基底或壳体7220。例如,基底18922可以包括多个层。此外,基底18922限定流动路径18924,该流动路径18924构造成将第一端部18921安置成与第二端部18922流体连通,如本文中进一步描述的。
数字pcr药筒18920还包括一组柱塞(或可移动构件)18928,该组柱塞可移动地设置在数字pcr药筒18920的一部分内。更具体地,该组柱塞18928构造成当数字pcr药筒从第一构型移动至第二构型时选择性地接合仪器的一部分。特别地,柱塞18928可以通过类似于以上描述的致动器组件3400和3600来致动。
在使用中,pcr样品可以以诸如例如本文中描述的方式之类的任何适合的方式在pcr小瓶18260内制备。在充足地制备好pcr样品后,pcr小瓶18260可以联接至数字pcr药筒18920,并且数字pcr药筒18920可以设置在仪器(例如,用于进行数字pcr处理的仪器,包括至少致动器部分、加热部分、光学部分或任何其它适合的部分)内。以此方式,仪器可以选择性地接合数字pcr药筒18920以将数字pcr药筒18920移动至第二构型,如图108所示。
更具体地,仪器的一部分可以接合传送机构18930的致动器18926以将致动器18926沿箭头ttt的方向移动。密封构件18927和壳体18925的这种布置使得致动器模块18926的运动在壳体18925内引入负压,并且因此吸入力施加至由基底18923限定的流动通道18924。以此方式,致动器模块18226的运动将设置在pcr小瓶18260内容积v1的pcr样品的一部分吸取通过流动路径18924并进入壳体18925。
在pcr样品的一部分设置在流动路径18924内的情况下,仪器可以选择性地接合该组柱塞18928。在一些实施方式中,仪器构造成依次接合柱塞18928。在一些实施方式中,仪器构造成以给定的顺序接合柱塞18928。例如,如由箭头uuu所示,在一些实施方式中,仪器首先接合末端柱塞18928。在一些实施方式中,仪器同时地接合末端柱塞18928,如由箭头uuu所示的。在末端柱塞18928处于第二构型的情况下,仪器依次地接合相邻的如由箭头vvv、www、xxx和yyy所指示的柱塞18928。尽管示出为包括一组10个的柱塞18928,但在一些实施方式中,数字pcr药筒可以包括任何适合数目的柱塞18928。此外,柱塞18928的数目不需要是偶数(例如,柱塞18928的致动可以对每个柱塞单独地进行)。此外,尽管描述为自外向内的方式致动,但在其它实施方式中,柱塞可以以任何适合的顺序致动。例如,在一些实施方式中,柱塞18926可以致动为使得仪器首先致动如由箭头yyy所示的柱塞,随后按照顺序致动如由箭头xxx、www、vvv和uuu所示的柱塞。
在柱塞18928处于第二构型的情况下,容积v1的pcr样品的一部分分隔成设置在相邻的柱塞18928(例如,容纳在反应室18929之内的)之间的流动路径18924内的较小的基本上相等的容积v2。类似陈述地,当柱塞18928处于第二位置或第二构型时,流动路径18924划分成和/或分隔成一系列的pcr容积18928。每个pcr容积18928均可以具有任何适合的容积。例如,在一些实施方式中,反应室18929的容积v2可以为5微升。在其它实施方式中,反应室18929的基本上相等的容积v2可以介于5微升与10微升之间。以此方式,容积v2的反应室18292构造成容纳基本上单杂交的链的样品和给定组的探针。在容积v2的pcr样品设置在反应室18929内的情况下,仪器可以对数字pcr药筒18920的反应室18929进行热循环。该仪器可以构造成以诸如本文中描述的方式之类的任何适合的方式对反应室18929进行热循环。以此方式,对容积v2的pcr样品执行数字pcr过程,并且可以使用本文中描述的任何适合的光学方法对其进行分析。
尽管数字pcr药筒18920示出为基本上线性的(例如,具有基本上线性的流动路径),但在其它实施方式中,数字pcr药筒可以是任何适合的构型。例如,在一些实施方式中,数字pcr药筒可以包括多个基底,所述多个基底从pcr小瓶径向地延伸并且联接至基本上环状外圈。在其它实施方式中,基底可以从pcr小瓶沿螺旋方向延伸使得流动路径分隔成以螺旋状绕pcr小瓶延伸的一系列容积。
尽管药筒18920在上文中描述为具有如下pcr小瓶18260,该pcr小瓶18260在样品制备好之后(例如,用pcr试剂等分离、组合)联接至壳体18923、并且随后被安置在仪器内,但在其它实施方式中,数字pcr药筒可以包括联接至分离模块(比如分离模块7100)的pcr小瓶并且还包括类似于流动路径18924的流动路劲,经分离且经制备的样品可以在该流动路径18924内流动,如以上描述的。类似陈述地,在一些实施方式中,pcr药筒可以包括与本文中公开的任何其它pcr模块的结构和功能(例如,pcr模块6200、7200等)集成的药筒18920的结构和功能。
尽管以上未描述,但在一些实施方式中,pcr样品可以在其内的样品被传送到流动路径中之前部分地加热。例如,在一些实施方式中,可能期望pcr样品处于升高温度下以促进与如本文中描述的pcr过程相关联的物质和/或试剂的“热启动”传送。
尽管多种实施方式已描述为具有特定特征和/或部件的组合,但其它实施方式也可以具有来自如上所述的任何实施方式的任何特征和/或部件的组合。
- 还没有人留言评论。精彩留言会获得点赞!