一种三亚胺噻唑衍生物的制备方法与流程
本发明属于有机合成技术领域,具体涉及一种三亚胺噻唑衍生物的制备方法。
背景技术:
在农药领域,三亚胺噻唑衍生物表现出良好的杀螨作用,三亚胺噻唑类农药如德国拜耳公司生产的氟螨噻(Flubenzimine)(Bayer AG.DE2210882A1,1972.),对仁果类、李树上的螨属害虫防治效果显著,对辣根猿叶甲幼虫100%有效。因此合成三亚胺噻唑衍生物具有重要意义。
三亚胺噻唑衍生物的制备方法有:
1)Bayer合成法:以硫脲和全氟代二甲基乙二胺为起始原料,在氟化钠作用下合成三亚胺噻唑衍生物。
利用上述方法在实验室中制备三亚胺噻唑衍生物,具有明显的缺点:1)全氟化合物具有持久性和生物积累性,污染严重,不符合绿色化学的要求。2)全氟化合物具有多种毒性,如抑制免疫系统,影响线粒体代谢,导致肝细胞损伤、生殖细胞受损等,对人体健康极为不利。
技术实现要素:
为了克服上述现有技术的不足,本发明提供了一种三亚胺噻唑衍生物的制备方法。
一种三亚胺噻唑衍生物的制备方法,所述三亚胺噻唑衍生物具有式Ⅰ所示的结构:
式Ⅰ中,其中R1、R2选自苯基、取代苯基、苄基、萘基、环己基、甲基、吡啶、噻吩、炔基、羟基和酯基,取代苯基取代原子是三氟甲基、氟原子、氯原子、溴原子、甲基、甲氧基;R3选自取代苯基、环己基、叔丁基、正丁基,取代苯基取代原子是甲基;其特征在于,由硫脲和异腈,在乙酰丙酮镍(Ni(acac)2)的作用下,50℃搅拌至反应完毕,有大量固体析出,过滤,并用甲醇洗涤,干燥得到目标化合物;其化学过程见反应式Ⅱ:
所述的硫脲、异腈和Ni(acac)2的摩尔比值为1:2.5:0.03,溶剂选自丙酮(分析纯),且在使用前无需进一步处理;反应时间为1h,反应温度为50℃。
本发明的有益效果为:本发明提供的三亚胺噻唑衍生物的合成方法科学合理,并且具有溶剂绿色,合成方法简单,反应时间短,产率较高,后处理简单,产品易于纯化等特点。
附图说明
图1为实施例1制备的化合物3a的1H NMR图谱;
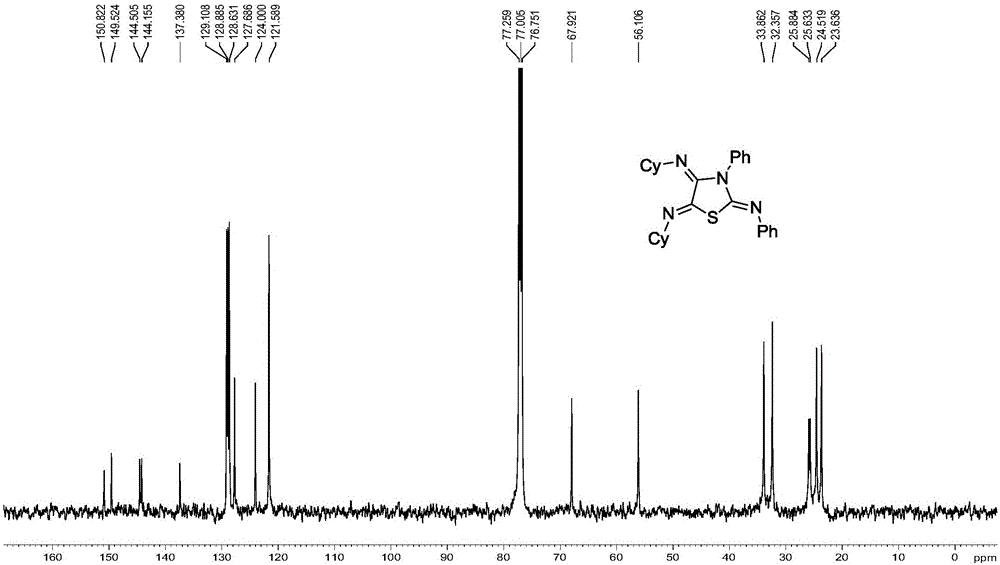
图2为实施例1制备的化合物3a的13C NMR图谱;
图3为实施例4制备的化合物3d的1H NMR图谱;
图4为实施例4制备的化合物3d的13C NMR图谱;
图5为实施例10制备的化合物3j的1H NMR图谱;
图6为实施例10制备的化合物3j的13C NMR图谱。
具体实施方式
下面结合附图和具体的实施例对本发明进一步详细的说明:
下述实施例中所述试验方法,如无特殊说明,均为常规方法;所述试剂和材料,如无特殊说明,均可从商业途径获得。
实施例1
1)三亚胺噻唑衍生物3a的制备
将二苯基硫脲(0.6mmol,137mg),环己基异腈(1.50mmol,164mg)加入到25mL单口瓶中,加入催化剂Ni(acac)2(0.018mmol,5mg)作催化剂,2mL丙酮作溶剂,50℃搅拌1h。体系析出固体,抽滤得到白色粉末状固体,用甲醇溶液进行洗涤即可得到纯净的目标产物。经NMR,HRMS证实为三亚胺噻唑衍生物3a,其收率为93%。
谱图解析数据3a:
1H NMR(CDCl3,500MHz):δ7.48–7.45(m,2H),7.40–7.39(m,2H),7.36–7.33(m,1H),7.29–7.26(m,2H),7.08(t,J=7.35Hz,1H),6.87(d,J=7.80Hz,2H),4.71(br s,1H),3.06(br s,1H),1.77–1.72(m,4H),1.66–1.64(m,4H),1.58–1.52(m,4H),1.41–1.35(m,3H),1.29–1.18(m,5H);13C NMR(CDCl3,125MHz):δ150.8,149.5,144.6,144.2,137.4,129.1,128.9,128.6,127.7,124.0,121.6,67.9,56.1,33.9,32.4,25.9,25.6,24.5,23.7;HRMS(ESI)m/z calcd for C18H13ClN3OS+[M+H]+445.2426,found 445.2419.
实施例2
用1b代替实例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据3b:
1H NMR(CDCl3,500MHz):δ7.40–7.37(m,2H),7.30–7.28(m,3H),4.69(br s,1H),3.18(br s,1H),3.08(br s,1H),1.81–1.79(m,4H),1.68–1.61(m,8H),1.57–1.55(m,2H),1.44–1.43(m,3H),1.28–1.22(m,11H),0.89–0.87(m,2H);13C NMR(CDCl3,125MHz):δ145.5,145.0,144.4,138.1,129.3,128.1,126.9,67.7, 62.6,55.8,34.0,33.8,32.4,29.7,25.9,25.7,25.5,24.6,23.8;HRMS(ESI)m/z calcd for C27H39N4S+[M+H]+451.28899,found 451.28915.
实施例3
用1c代替实例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据3c:
1H NMR(CDCl3,500MHz):δ7.45–7.42(m,2H),7.34–7.31(m,1H),7.27–7.25(m,2H),4.68(br s,1H),3.22–3.19(m,1H),3.12(s,3H),1.83–1.82(m,4H),1.63–1.58(m,7H),1.53–1.45(m,4H),1.27–1.15(m,5H);13C NMR(CDCl3,125MHz):δ150.3,144.4,144.3,137.9,129.2,128.6,127.5,67.9,55.9,39.6,34.0,33.2,32.4,25.9,25.7,25.1,24.6,23.7;HRMS(ESI)m/z calcd for C22H31N4S+[M+H]+383.22639,found 383.22647.
实施例4
用1d代替实例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据3d:
1H NMR(CDCl3,500MHz):δ7.46–7.43(m,2H),7.34–7.28(m,5H),7.23–7.19(m,3H),4.71(br s,1H),4.58(s,2H),3.20–3.17(m,1H),1.82–1.81(m,4H),1.66–1.60(m,7H),1.53(br s,1H),1.45(br s,3H),1.28–1.21(m,5H);13C NMR(CDCl3,125MHz):δ150.2,144.3,144.1,139.7,137.9,129.2,128.5,128.2,127.3,127.1,126.5,68.0,56.4,56.0,33.9,32.3,25.9,25.7,24.6,23.7;HRMS(ESI)m/z calcd for C28H35N4S+[M+H]+459.25769,found 459.25763.
实施例5
用1e代替实例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据3e:
1H NMR(CDCl3,500MHz):δ7.87–7.83(m,2H),7.59–7.57(m,1H),7.52(t,J=7.72Hz,1H),7.45–7.37(m,3H),4.68–4.64(m,1H),3.26(br s,1H),3.08–3.05(m,1H),1.85–1.76(m,5H),1.64–1.61(m,7H),1.51–1.45(m,8H),1.25–0.98(m,10H); 13C NMR(CDCl3,125MHz):δ145.1,144.9,144.6,135.6,134.3,130.4,128.2,128.1,127.7,125.7,125.5,123.6,67.7,62.7,55.8,33.9,33.7,32.5,32.3,25.8,25.4,24.6,23.8;HRMS(ESI)m/z calcd for C31H41N4S+[M+H]+501.30464,found 501.30463.
实施例6
用1f代替实例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据3f:
1H NMR(CDCl3,500MHz):δ8.39(d,J=3.57Hz,1H),7.58–7.55(m,1H),7.48–7.45(m,2H),7.38–7.34(m,3H),6.97–6.94(m,1H),6.91(d,J=8.10Hz,1H),4.76(br s,1H),3.34–3.31(m,1H),1.81–1.80(m,4H),1.67–1.59(m,7H),1.54–1.52(m,1H),1.47–1.42(m,3H),1.31–1.16(m,5H);13C NMR(CDCl3,125MHz):δ159.1,152.4,147.2,143.5,137.8,137.6,129.2,128.4,127.5,120.3,119.1,67.0,56.0,33.8,32.6,25.9,25.7,24.5,23.7;HRMS(ESI)m/z calcd for C26H32N5S+[M+H]+446.23729,found 446.23663.
实施例7
用1g代替实例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据3g:
1H NMR(CDCl3,500MHz):δ7.45–7.42(m,2H),7.34–7.31(m,1H),7.28–7.26(m,2H),4.68(br s,1H),4.11(d,J=2.46Hz,2H),3.22–3.19(m,1H),2.23(t,J=2.35Hz,1H),1.83–1.81(m,4H),1.64–1.59(m,7H),1.53–1.44(m,4H),1.26–1.15(m,5H);13C NMR(CDCl3,125MHz):δ153.4,144.0,143.4,137.5,129.1,128.6,127.6,80.5,71.4,68.2,56.0,41.1,33.8,32.4,25.8,25.7,24.5,23.7;HRMS(ESI)m/z calcd for C24H31N4S+[M+H]+407.22639,found 407.22638.
实施例8
用2b代替实例1中的2a,其他条件同实例1,实验结果见表1。
谱图解析数据3h:
1H NMR(CDCl3,500MHz):δ7.45–7.42(m,2H),7.35–7.30(m,3H),7.27–7.24(m,2H),7.05(t,J=7.38Hz,1H),6.87(d,J=7.70Hz,2H),1.36(s,9H),1.27(s,9H);13C NMR(CDCl3,125MHz):δ150.8,149.3,143.0,140.8,138.3,129.3,128.8,128.4,127.3,123.8,121.8,58.6,54.8,29.8,27.9;HRMS(ESI)m/z calcd for C23H29N4S+(M+H)+393.21074,found 393.21078.
实施例9
用2c代替实例1中的2a,其他条件同实例1,实验结果见表1。
谱图解析数据3i:
1H NMR(CDCl3,500MHz):δ7.51–7.48(m,2H),7.40–7.36(m,3H),7.30–7.27(m,2H),7.10–7.07(m,1H),6.88(d,J=7.70Hz,2H),3.99(t,J=7.05Hz,2H),3.37(t,J=6.68Hz,2H),1.76–1.70(m,2H),1.52–1.40(m,4H),1.33–1.26(m,2H),0.95(t,J=7.35Hz,3H),0.86(t,J=7.32Hz,3H);13C NMR(CDCl3,125MHz)δ150.4,149.4,148.1,145.6,137.2,129.0,128.9,128.0,124.1,121.5,59.1,49.7,33.3,32.1,20.6,13.8;HRMS(ESI)m/z calcd for C23H29N4S+[M+H]+393.21074,found 393.21094.
实施例10
用2d代替实例1中的2a,其他条件同实例1,实验结果见表1。
谱图解析数据3j:
1H NMR(CDCl3,500MHz):δ7.58(br s,4H),7.44(br s,1H),7.24–7.21(m,2H),7.05–7.03(m,1H),6.92–6.83(m,7H),6.74–6.72(m,1H),2.12(s,6H),1.91(s,6H);13C NMR(CDCl3,125MHz):δ149.7,149.2,148.6,148.4,146.4,145.1,136.5,129.4,129.0,128.8,128.3,127.3,125.0,124.6,122.2,121.1,18.4,17.6;HRMS(ESI)m/z calcd for C31H29N4S+[M+H]+489.21074,found 489.21063.
表1
。
- 还没有人留言评论。精彩留言会获得点赞!