以碱性橙‑溴化十六烷基三甲基铵为探针检测DNA的方法与流程
本发明涉及DNA检测方法技术领域,尤其涉及一种以碱性橙-溴化十六烷基三甲基铵(CTMAB)为探针检测DNA的方法。
背景技术:
核酸是遗传信息的载体,是生命的最基本物质之一。核酸分析技术是分子生物学领域研究的基础,对于研制新药物和疾病治疗具有非常重要的意义,是生命科学中受到广泛关注和研究的课题。
目前,核酸分析测定的方法有很多。紫外分光光度法操作简单,被广泛使用;但由于灵敏度低﹑易受干扰,使其在应用上受到限制。荧光分析法具有较好的选择性和灵敏度,近些年应用较多;但荧光试剂价格昂贵,部分荧光试剂被证实具有致癌性。1993年,Pasternack等人第一次使用普通荧光分光光度计建立了共振光散射技术。核酸的共振光散射分析方法在普通荧光分光光度计即可实现,具有灵敏度高﹑选择性好﹑操作简便﹑应用安全﹑试剂便宜等优点。近年来,共振光散射技术在核酸分析中得到迅速发展,受到越来越广泛的关注。
碱性橙为闪绿色结晶,遇硫酸呈黄色,稀释呈橙色。熔点Mp为118-118.5℃,可溶于水,乙醇。碱性橙广泛应用于染色,其结构式为:溴化十六烷基三甲基铵(CTMAB)为一种常见的阳离子表面活性剂。
技术实现要素:
本发明提供了一种以碱性橙-CTMAB为探针检测DNA的方法。
一种以碱性橙-CTMAB为探针检测DNA的方法,包括以下步骤:
A、于10mL容量瓶中依次加入适量的碱性橙、BR缓冲液和CTMAB,然后用水定容至刻度,混匀,静置15分钟后进行测试;在200-800nm的波长范围内,在Δλ=0nm的条件下同步扫描激发和发射单色器,狭缝宽度为5.0nm,波长扫描速度为200nm/min,得到共振光散射光谱,然后在最大共振光散射峰处(λ=560.0nm)测量溶液的共振光散射强度;
B、于10mL容量瓶中依次加入适量的碱性橙、BR缓冲液、CTMAB和DNA,然后用水定容至刻度,混匀,静置15分钟后进行测试;在200-800nm的波长范围内,在Δλ=0nm的条件下同步扫描激发和发射单色器,狭缝宽度为5.0nm,波长扫描速度为200nm/min,得到共振光散射光谱,然后在最大共振光散射峰处(λ=560.0nm)测量溶液的共振光散射强度;
C、通过检测得到的DNA加入前后碱性橙-CTMAB体系的共振光散射峰强度增加值来计算DNA浓度大小。
DNA对碱性橙-CTMAB体系共振光散射峰强度的增加程度用ΔIRLS=IRLS–I0RLS表示,其中,I0RLS和IRLS分别代表DNA加入前后体系的共振光散射强度。ΔIRLS值反映DNA浓度大小,ΔIRLS值越大说明DNA浓度越高。
以下为本发明提供的检测方法的原理:对下列体系进行检测,得到共振光散射光谱。
分别配置下列体系:ctDNA,CTMAB,CTMAB-ctDNA,碱性橙,碱性橙-ctDNA,碱性橙-CTMAB,碱性橙-CTMAB-ctDNA,测定各体系的共振光散射光谱,实验结果如图1所示。(a)ctDNA;(b)CTMAB;(c)CTMAB-ctDNA;(d)碱性橙(e)碱性橙-ctDNA;(f)碱性橙-CTMAB;(g)碱性橙-CTMAB-ctDNA。
检测条件为:碱性橙,3.0×10-4mol/L;CTMAB,1.6×10-5mol/L;ctDNA,1.0×10-6g/mL;pH=7.50。
由检测结果可知:碱性橙在303nm和560nm处有两个弱的共振光散射峰。从图1(曲线a,b)可以看出,ctDNA和CTMAB的共振光散射强度很弱,在实验条件下没有共振光散射峰。从图1(曲线c)可以看出,CTMAB-ctDNA复合体系在300nm处有一个共振光散射峰,说明CTMAB与核酸发生作用,其作用力为静电引力和疏水作用力。图1(曲线d,e)说明ctDNA对碱性橙的共振光散射光谱几乎没有影响,表明ctDNA和碱性橙间的静电力和疏水作用力比较弱。从图1(曲线f)可以看出,CTMAB能明显增强碱性橙的共振光散射强度。通过静电力和疏水作用力,碱性橙溶于CTMAB胶束中而形成聚集体。图1(曲线g)说明ctDNA能使碱性橙-CTMAB复合物的共振光散射光强度明显增强,这表明以CTMAB为媒介,ctDNA能与碱性橙-CTMAB复合体系发生作用形成离子缔合物。ctDNA对碱性橙-CTMAB复合体系共振光散射峰强度的增加程度(ΔIRLS)能反映ctDNA浓度大小。
通过进一步的检测,确定最佳实验条件。
1、确定碱性橙的最佳浓度
当碱性橙浓度低于1.6×10-4mol/L时,随着碱性橙浓度的增大,碱性橙-CTMAB和碱性橙-CTMAB-ctDNA体系的共振光散射峰从475nm左右红移至560nm处。当碱性橙浓度大于1.6×10-4mol/L时,随着碱性橙浓度的增加,位于560nm处的共振光散射峰位置不再发生变化。
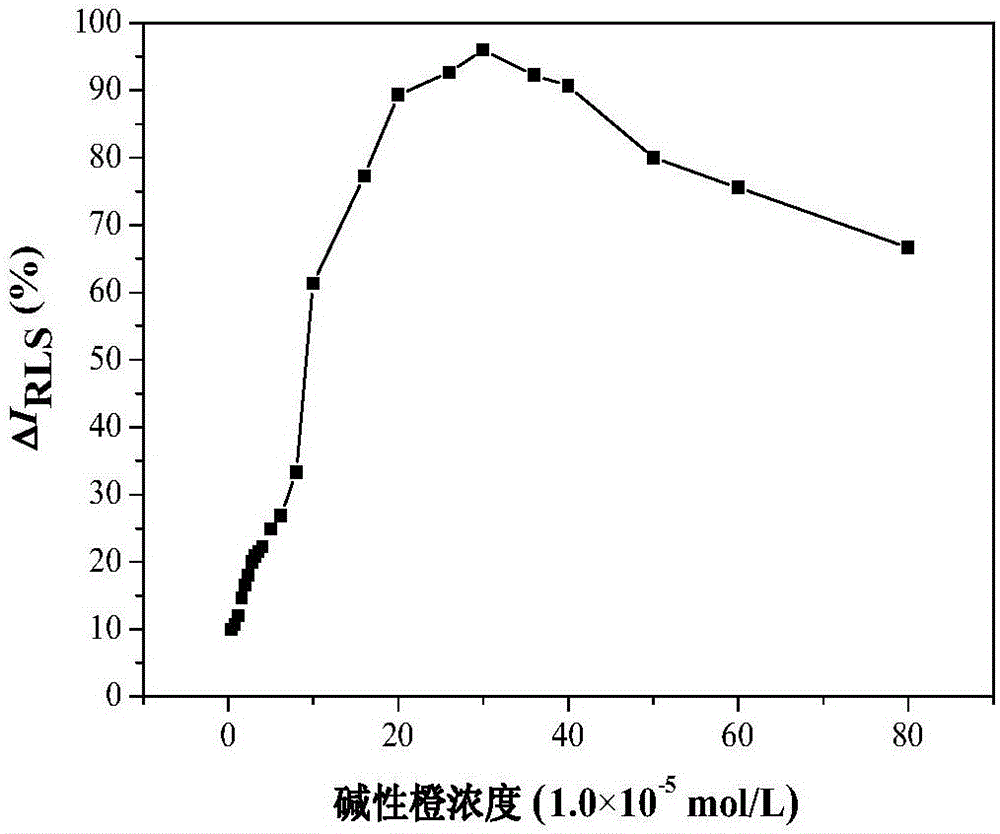
碱性橙浓度对ΔIRLS的影响如图2所示。随着碱性橙浓度的增加,ΔIRLS先增强,后减弱。当碱性橙浓度为3.0×10-4mol/L时,ΔIRLS最强。实验条件为:CTMAB,1.6×10-5mol/L;ctDNA,1.0×10-6g/mL;pH=7.50。
2、确定CTMAB的最佳浓度
CTMAB浓度对ΔIRLS的影响如图3所示。同样,随着CTMAB浓度的增加,ΔIRLS先增强后减弱。当CTMAB浓度为1.6×10-5mol/L时,体系ΔIRLS达最大值。实验条件为:碱性橙,3.0×10-4mol/L;ctDNA,1.0×10-6g/mL;pH=7.50。
3、确定最佳pH值
通过改变BR缓冲液的pH值,我们考察了pH对△IRLS的影响,结果如图4所示。在4.10-10.20pH范围内,随着pH增大,△IRLS逐渐增强,在pH为中性7.00时达到最大值并保持稳定。在考察范围内,pH值7.50最接近中性pH,为最佳pH值。实验条件为:碱性橙,3.0×10-4mol/L;CTMAB,1.6×10-5mol/L;ctDNA,1.0×10-6g/mL。
4、确定最佳孵育时间
体系的稳定性和孵育时间对一种分析方法的推广应用具有重要意义。实验表明,当体系各成分混合后,△IRLS在15min达到最大(最佳孵育时间),并能在90分钟内保持稳定,稳定性良好。
5、工作曲线和检测限
在最佳实验条件下(碱性橙浓度为3.0×10-4mol/L,CTMAB浓度为1.6×10-5mol/L,pH为7.50,稳定时间15min),绘制ctDNA的工作曲线,得到如下分析参数:线性范围:2.5×10-8~5×10-7g/mL(相关性系数=0.989),5×10-7~3×10-5g/mL(相关性系数=0.991),检测限:8.5ng/mL(S/N=3)。可见,该方法线性范围宽且有较高的灵敏度。
本方案的有益之处在于:本发明以碱性橙-溴化十六烷基三甲基铵(CTMAB)为探针,建立了测定DNA的灵敏的共振光散射方法。测试在普通的荧光分光光度计上选择合适的激发和发射狭缝宽度,采用相等的激发和发射波长同时扫描激发和发射单色器(Δλ=0nm)即可得到。本发明以DNA加入前后碱性橙-CTMAB体系共振光散射强度出现的灵敏信号(共振光散射峰强度增加值,ΔIRLS)为检测信号,建立其与DNA浓度之间的关系。本研究方法具有操作简单﹑测定灵敏度高等特点,检测限可达纳克级,为生化和临床分析提供了一条新的途径,具有广泛的应用前景。
附图说明
图1:共振光散射光谱图。
图2:碱性橙浓度对ΔIRLS的影响图。
图3:CTMAB浓度对ΔIRLS的影响图。
图4:pH对ΔIRLS的影响图。
具体实施方式
实施例
一种以碱性橙-CTMAB为探针检测DNA的方法,包括以下步骤:
A、于10mL容量瓶中依次加入适量的碱性橙、BR缓冲液和CTMAB,然后用水定容至刻度,混匀,静置15分钟后进行测试;在200-800nm的波长范围内,在Δλ=0nm的条件下同步扫描激发和发射单色器,狭缝宽度为5.0nm,波长扫描速度为200nm/min,得到共振光散射光谱,然后在最大共振光散射峰处(λ=560.0nm)测量溶液的共振光散射强度;
B、于10mL容量瓶中依次加入适量的碱性橙、BR缓冲液、CTMAB和DNA,然后用水定容至刻度,混匀,静置15分钟后进行测试;在200-800nm的波长范围内,在Δλ=0nm的条件下同步扫描激发和发射单色器,狭缝宽度为5.0nm,波长扫描速度为200nm/min,得到共振光散射光谱,然后在最大共振光散射峰处(λ=560.0nm)测量溶液的共振光散射强度;
C、通过检测得到的DNA加入前后碱性橙-CTMAB体系的共振光散射峰强度增加值来计算DNA浓度大小。
DNA对碱性橙-CTMAB体系共振光散射峰强度的增加程度用ΔIRLS=IRLS–I0RLS表示,其中,I0RLS和IRLS分别代表DNA加入前后体系的共振光散射强度。ΔIRLS值反映DNA浓度大小,ΔIRLS值越大说明DNA浓度越高。
利用标准加入法测定了合成样品中核酸的含量,实验结果见表1。从表中结果可见,该方法对合成样品中核酸含量的测定结果令人满意。
表1合成样品中核酸的测定
实验条件:BSA:1.0×10-6g/mL;Mg2+:1.0×10-6mol/L;K+:6.0×10-6mol/L;Na+:1.0×10-5mol/L;pH=7.50
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,根据本发明的技术方案及其发明构思加以等同替换或改变,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!