酪蛋白‑多糖纳米凝胶的超声制备方法及功能食品的应用与流程
本发明涉及蛋白质-多糖纳米凝胶
技术领域:
,特指一种以酪蛋白酸钠和海藻酸钠为原料、采用扫频超声处理或者多模式频率超声波技术制备纳米凝胶体系并对β-胡萝卜素进行包埋制备功能食品的方法。
背景技术:
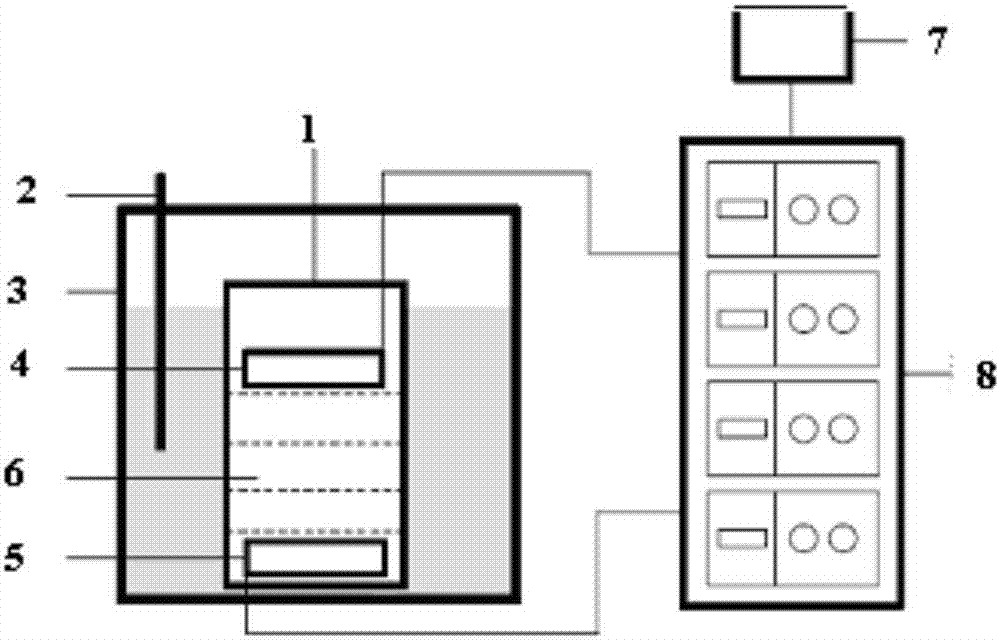
:功能食品因含有维生素、不饱和脂肪酸、多酚类化合物或益生菌等生物活性成分,具有调节人体生理机能的功能,可以延缓和预防慢性疾病的发生。然而,许多活性成分对食品加工和储藏过程中温度、氧、光、ph和金属离子等因素敏感,易于发生氧化、异构化、聚集或降解等结构改变,导致生物活性降低或丢失。而且,疏水性和两亲性活性成分在水中溶解度非常低。这些在很大程度上限制了活性成分在食品和医药工业中的应用。天然的生物大分子(如蛋白质、多糖等)不但具有高的营养价值,而且具有多种功能特性,已被广泛用作包埋技术中的原料。因此,开发天然大分子(蛋白质和多糖)的凝胶体系对生物活性成分进行包埋和保护,是发展功能性食品和药品的关键。酪蛋白约占牛乳蛋白总量的80%,是牛乳蛋白的主要成分。酪蛋白含有人体必需的8种氨基酸,是一种全价含磷蛋白质,主要由αs1-酪蛋白、αs2-酪蛋白、β-酪蛋白及k-酪蛋白组成,平均分子量在75000-350000之间,等电点约为4.6。酪蛋白酸钠,亦称酪蛋白酸钠、酪蛋白钠、酪酸钠或干酪素,是酪蛋白和钠的化合物。是将酪蛋白和氢氧化钠加热回流制备,将水不溶性的酪蛋白转变成可溶性的蛋白盐,即形成酪蛋白酸钠。酪蛋白酸钠具有增稠性、乳化性、起泡性、热稳定性以及界面特性等诸多特性,是一种安全无害的增稠剂和乳化剂,因此被广范地用作食品(例如冰激淋、咖啡增白剂、人造稠黄油等)的乳化稳定剂。酪蛋白酸钠分子中具有亲水基团和疏水基团,因而具有一定的乳化性。可受一定的环境条件所影响,例如ph的变化即可明显影响其乳化性能,酪蛋白酸钠在等电点时的乳化力最小,低于等电点时其乳化力可增大,而在碱性条件下其乳化力较大,且随ph增高而加大。值得特别注意的是,由于酪蛋白酸钠很耐热,在特定的ph条件下对其进行热处理时可大大提高乳化力。通常,应用酪蛋白酸钠制成的乳化剂,其稳定性比乳清蛋白、大豆蛋白等所制备的乳化剂更好。海藻酸钠(sodiumalginate),别名褐藻酸钠,是海藻酸(由α-l-古罗糖醛酸(g)和β-d-甘露糖醛酸(m)聚合而成)的钠盐,大量存在于褐藻中,具有高度的安全性,是无毒食品,早在1938年就已被收入美国药典。海藻酸钠溶于水后,有良好的凝胶特性和成膜能力,在医药和食品等行业有广泛的研究和应用。海藻酸钠的水溶液具有较高的黏度,已被用作食品的增稠剂、稳定剂、乳化剂等。海藻酸钠含有大量的-coo-,在水溶液中可表现出聚阴离子行为,具有一定的黏附性,可用作治疗黏膜组织的药物载体。在酸性条件下,-coo-转变成-cooh,电离度降低,海藻酸钠的亲水性降低,分子链收缩,ph值增加时,-cooh基团不断地解离,海藻酸钠的亲水性增加,分子链伸展。因此,海藻酸钠具有明显的ph敏感性。海藻酸钠可以在极其温和的条件下快速形成凝胶,当有ca2+、sr2+等阳离子存在时,g单元上的na+与二价阳离子发生离子交换反应,g单元堆积形成交联网络结构,从而形成水凝胶。海藻酸钠形成凝胶的条件温和,这可以避免敏感性药物、蛋白质、细胞和酶等活性物质的失活。研究发现蛋白质与多糖之间相互作用形成复合凝胶可以克服单一组分ph敏感、稳定性差、包埋效率低的不足,对生物活性成分起到很好的包埋和保护作用。因此国内外学者进行了大量的有关蛋白质-多糖复合凝胶的制备方法及其对生物活性成分包埋的研究。乳化法是制备复合凝胶的常用方法,此法的不足表现在复合凝胶的制备过程中需要添加有机溶剂、表面活性剂、戊二醛交联剂等,这些试剂的残留使复合凝胶具有一定毒性;去溶剂法和化学交联法也涉及有毒交联剂的引入;以上三种方法不是制备复合凝胶的理想方法。离子交联法和自组装法制备复合凝胶,条件温和,不需要有毒的交联剂,不生成化合键,仅依靠非共价键连接,因而被广泛使用。特别是自组装法,对于营养递送系统设计而言,安全性等相对更佳。然而蛋白质与多糖毕竟是不同性质的两种大分子,仅仅通过简单自组装法进行凝聚,凝聚效果差,凝聚物对生物活性成分的包埋效率低。为了解决这一问题,本发明引进先进的扫频式超声波处理和多模式超声波处理技术,希望超声波能激发蛋白质与多糖两种生物大分子溶液产生与其自身固有频率相匹配的共振频率,产生交联,获得了一种包埋效率高、ph稳定、粒径均一的蛋白质-多糖复合凝胶,利用所得的蛋白质-多糖复合凝胶对生物活性成分进行包埋和保护。技术实现要素:为解决上述问题,本发明通过对酪蛋白酸钠-海藻酸钠进行复合凝聚,添加β-胡萝卜素,利用扫频式超声波处理和多模式超声波处理等技术手段制备酪蛋白酸钠-海藻酸钠复合凝胶,并研究其对β-胡萝卜素的包埋效果。本发明酪蛋白酸钠-海藻酸钠复合凝胶,是由以下重量份的原料制备而成:酪蛋白酸钠:2~40份;海藻酸钠:2.5~25份。优选以下重量份的原料制备而成:酪蛋白酸钠:10份;海藻酸钠:4份。酪蛋白酸钠-海藻酸钠复合凝胶的制备方法,按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为(2-40)mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为(2.5-25)mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例为:(2~40):(2.5~25),然后调节混合溶液的ph=4-7。(4)将步骤(3)得到的混合溶液进行双频扫频超声波处理,超声条件为:上下板间距为10cm,扫频周期300s,间歇比1:1(超声5s,间歇5s),上下每块振板功率为600w。(5)超声结束后,室温下静置1h,即得酪蛋白酸钠-海藻酸钠复合凝胶溶液,喷雾干燥或者冷冻干燥后得酪蛋白酸钠-海藻酸钠复合凝聚物。其中步骤(3)中优选调节混合溶液的ph=5。其中步骤(3)中所述的酪蛋白酸钠和海藻酸钠的质量比例优选为10:4。其中步骤(4)中所述的双频频率组合为:40khz/68khz、28khz/40khz、68khz/28khz、33khz/40khz;优选频率组合为40khz/68khz。酪蛋白酸钠-海藻酸钠复合凝胶负载β-胡萝卜素的制备方法,按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为(2-40)mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为(2.5-25)mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例为:(2~40):(2.5~25),然后调节混合溶液的ph=4-7。(4)将浓度为(1-5)mg/ml的β-胡萝卜素的乙醇溶液逐滴加入步骤(3)制备的酪蛋白酸钠和海藻酸钠复合凝胶溶液中,使得酪蛋白酸钠和β-胡萝卜素的质量比例为1:0.5;(5)室温下将步骤(4)得到的混合溶液进行双频扫频超声波处理,超声条件为:上下板间距为10cm,扫频周期300s,间歇比1:1(超声5s,间歇5s),上下每块振板功率为600w;(6)超声结束后,即得负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,喷雾干燥或者冷冻干燥后得到负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝聚物。其中步骤(3)中优选调节混合溶液的ph=5。其中步骤(3)中所述的使得酪蛋白酸钠和海藻酸钠的质量比例优选为10:4。其中步骤(5)中所述的双频频率组合为:40khz/68khz、28khz/40khz、68khz/28khz、33khz/40khz;优选频率组合为40khz/68khz。酪蛋白酸钠-海藻酸钠复合凝胶的制备方法,或者按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为(2-40)mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为(2.5-25)mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例为:(2~40):(2.5~25),然后调节混合溶液的ph=4-7。(4)对步骤(3)的混合溶液进行多频模式超声处理,其中所述的多频超声处理模式为:三频同步超声处理或者双频同步超声处理或者单频超声处理,超声功率密度100~150w/l;超声脉冲工作时间10s;脉冲间歇时间5s,超声处理时间为40min。(5)超声结束后,室温下静置1h,即得酪蛋白酸钠-海藻酸钠复合凝胶溶液,喷雾干燥或者冷冻干燥后得酪蛋白酸钠-海藻酸钠复合凝聚物。其中步骤(3)中优选调节混合溶液的ph=5。其中步骤(3)中酪蛋白酸钠和海藻酸钠的质量比例优选为10:4。其中步骤(4)中三频同步超声处理或者双频同步超声处理或者单频超声处理的超声波频率组合为:28khz、35khz、35/40khz或者28/35/40khz,优选28/35/40khz。酪蛋白酸钠-海藻酸钠复合凝胶负载β-胡萝卜素的制备方法,或者按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为(2-40)mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为(2.5-25)mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例为:(2~40):(2.5~25),然后调节混合溶液的ph=4-7。(4)将浓度为(1-5)mg/ml的β-胡萝卜素乙醇溶液逐滴加入步骤(3)制备的酪蛋白酸钠和海藻酸钠复合凝胶溶液中,使得酪蛋白酸钠和β-胡萝卜素的质量比例为1:0.5;(5)对步骤(4)的混合溶液进行多频模式超声处理,其中所述的多频超声处理模式为:三频同步超声处理或者双频同步超声处理或者单频超声处理,超声功率密度100~150w/l;超声脉冲工作时间10s;脉冲间歇时间5s,超声处理时间为40min。(6)超声结束后,室温下静置1h,即得负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,喷雾干燥或者冷冻干燥后得到负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝聚物。其中步骤(3)中优选调节混合溶液的ph=5。其中步骤(3)中酪蛋白酸钠和海藻酸钠的质量比例优选为10:4。其中步骤(5)中三频同步超声处理或者双频同步超声处理或者单频超声处理的超声波频率组合为:28khz、35khz、35/40khz或者28/35/40khz,优选28/35/40khz。负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶,具有稳定性好、生物相容性好、缓释时间长、包载率高等优点,可应用于制作保健食品、食品或者药品。本发明的有益效果在于:(1)本发明向酪蛋白酸钠中添加海藻酸钠,改变酪蛋白酸钠的高级结构,使其结构打开,暴露活性基团,同时蛋白质和多糖形成小的聚集体,从而促进各聚集体通过疏水相互作用形成凝胶为包埋生物活性成分提供基础。(2)本发明在利用酪蛋白酸钠-海藻酸钠复合凝胶包埋β-胡萝卜素的过程中,使用扫频超声波处理技术或者多模式超声波技术,通过超声波的物理力促进了蛋白质和多糖交联成聚集体,从而促进各聚集体通过疏水相互作用形成凝胶,为包埋生物活性成分提供基础。(3)本发明中包埋β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶的制备方法,工艺操作简单,制备过程中未涉及有机试剂,适宜工业化生产,且酪蛋白酸钠和海藻酸钠原料价格便宜,制备工艺简单。(4)本发明的包埋β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶具有稳定性好、生物相容性好、缓释时间长、包载率高等优点,可应用于食品、保健品、药品及化妆品等多个领域。附图说明图1是本发明的多模式超声波生物处理设备结构图,其中1、2、3为超声振板,4为盛液器,5为水浴锅,6为温度探头,7为循环泵,8为电脑程序控制器,9、10、11为超声控制器。图2是扫频双频超声预处理装置的设备图,1-超声池,2-温度计,3-恒温水浴池,4-超声波上振板,5-超声波下振板,6-样品处理区域,7-电脑控制器,8-超声波发生器。具体实施方式在本发明中所使用的术语,除非另外说明,一般都能被本领域普通技术人员理解。下面结合具体的实施例,并参照数据进一步详细地描述本发明。特此说明:这些实施例只是为了举例说明本发明,而非以任何方式限制本发明的范围。图1为本发明的多模式超声波生物处理设备,该设备配有一台电脑程序控制器8,可设定超声工作参数(超声功率密度、频率、脉冲工作时间、间歇时间和处理总时间)分别控制三个超声控制器9、10、11,分别连接三支不同频率的超声振板1、2、3,可实现单一频率/两个频率/三个频率超声波处理;将需要处理的溶液投入盛液器4中进行单频/双频/多频超声处理,启动循环泵7对溶液进行循环。通过水浴锅5和温度探头6实现溶液温度的自动控制。图2为本发明使用的扫频双频超声预处理装置的设备图,为江苏大学自主研制。超声发生器8能发出定频和扫频两种模式的超声波,单台超声波发生器功率为600w。在超声池1中上下对称放置超声波振板上板4和超声波下板5,通过超声波发生器8控制超声波振板上板4和超声波下板5;电脑控制器7设定超声波各参数后,控制超声波发生器8,发出符合要求的超声波;3为本发明中设备的恒温水浴池,通过温度计2实时监控温度,并根据工作需要调节介质温度;将需要处理的液原料置于样品袋中置于处理液区域6中进行超声波处理。本发明中的酪蛋白酸钠和海藻酸钠均为市售产品,食品级产品。本发明中的β-胡萝卜素为市售产品,食品级产品,纯度大于90%。实施例1-6(不加超声)酪蛋白酸钠-海藻酸钠复合凝胶负载β-胡萝卜素的制备方法,按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为(2-40)mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为(2.5-25)mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例见表1,然后调节混合溶液的ph=5。(4)将浓度为2mg/ml的β-胡萝卜素乙醇溶液逐滴加入步骤(3)制备的酪蛋白酸钠和海藻酸钠复合凝胶溶液中,使得酪蛋白酸钠和β-胡萝卜素的质量比例为1:0.5;(5)室温下静置1h,即得负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,喷雾干燥或者冷冻干燥后得到负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝聚物。(6)β-胡萝卜素包封率和负载率的测定取负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,采用旋转蒸发仪在40℃的温度下浓缩至40ml,取浓缩液1ml加5ml正己烷,混匀后在4℃下以5000rpm离心10分钟。测定正己烷相在波长为450nm处的吸光值,并计算游离β-胡萝卜素(未包埋和松散吸附的β-胡萝卜素)的质量。根据下式计算β-胡萝卜素的包封率和负载率:β-胡萝卜素的包封率(%)=(β-胡萝卜素总质量-游离β-胡萝卜素质量)×100/β-胡萝卜素总质量;β-胡萝卜素的负载率(%)=(β-胡萝卜素总质量-游离β-胡萝卜素质量)×100/样品总质量。实施例1-6制备过程相同,只是酪蛋白酸钠/海藻酸钠质量比不同,具体见表1不同质量比的酪蛋白酸钠/海藻酸钠对β-胡萝卜素包封率和负载率的影响。通过表1中对比实施例1-6不同质量比的酪蛋白酸钠/海藻酸钠对β-胡萝卜素包封率和负载率的影响可以看出,与对照相比(不加海藻酸钠,即实施例6),添加海藻酸钠可以显著提高酪蛋白酸钠包埋β-胡萝卜素的包封率;酪蛋白酸钠/海藻酸钠质量比为2:2.5时即可使β-胡萝卜素的包封率提高46.1%,酪蛋白酸钠/海藻酸钠质量比为10:4时则使β-胡萝卜素的包封率提高了88.5%。表1不同酪蛋白酸钠/海藻酸钠质量比对β-胡萝卜素包封率和负载率的影响实施例7-10(扫频双频超声波处理)酪蛋白酸钠:2份;海藻酸钠:2.5份。酪蛋白酸钠-海藻酸钠复合凝胶负载β-胡萝卜素的制备方法,按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为2mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为2.5mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例为2:2.5,然后调节混合溶液的ph=5。(4)将浓度为(1-5)mg/ml的β-胡萝卜素的乙醇溶液逐滴加入步骤(3)制备的酪蛋白酸钠和海藻酸钠复合凝胶溶液中,使得酪蛋白酸钠和β-胡萝卜素的质量比例为1:0.5;(5)室温下将步骤(4)得到的混合溶液进行双频扫频超声波处理,超声条件为:上下板间距为10cm,扫频周期300s,间歇比1:1(超声5s,间歇5s),上下每块振板功率为600w;双频频率组合见表1。(6)超声结束后,即得负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液。(7)β-胡萝卜素包封率和负载率的测定取负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,采用旋转蒸发仪在40℃的温度下浓缩至40ml,取浓缩液1ml加5ml正己烷,混匀后在4℃下以5000rpm离心10分钟。测定正己烷相在波长为450nm处的吸光值,并计算游离β-胡萝卜素(未包埋和松散吸附的β-胡萝卜素)的质量。根据下式计算β-胡萝卜素的包封率和负载率:β-胡萝卜素的包封率(%)=(β-胡萝卜素总质量-游离β-胡萝卜素质量)×100/β-胡萝卜素总质量;β-胡萝卜素的负载率(%)=(β-胡萝卜素总质量-游离β-胡萝卜素质量)×100/样品总质量。实施例7-10制备过程相同,只是超声参数略有改变,表2不同超声波模式对β-胡萝卜素包封率和负载率的影响。表2不同超声波模式对β-胡萝卜素包封率和负载率的影响实施例超声频率或模式包封率%负载率%对比例(即实施例1)不超声43.15.4实施例740khz/68khz63.86.0实施例840khz/28khz56.45.5实施例968khz/28khz52.35.2实施例1033khz/40khz56.75.6通过表2中对比实施例7-10不同频率组合的扫频超声波对β-胡萝卜素包封率和负载率的影响,可以发现扫频超声波处理可以显著提高酪蛋白酸钠-海藻酸钠复合凝胶包埋β-胡萝卜素的包封率,与对照相比(不超声),双频扫频超声波处理即可使β-胡萝卜素的包封率提高21.3%~48.0%,而40/68khz的双频扫频超声波处理则使β-胡萝卜素的包封率提高了48.0%。实施例11-14(多模式频率超声波处理)酪蛋白酸钠:2份;海藻酸钠:2.5份。酪蛋白酸钠-海藻酸钠复合凝胶负载β-胡萝卜素的制备方法,按照下述步骤进行:(1)将酪蛋白酸钠溶解到蒸馏水中,磁力搅拌至蛋白完全溶解;得到酪蛋白酸钠浓度为2mg/ml溶液;(2)将海藻酸钠溶解到水溶液中,磁力搅拌至完全溶解;得到浓度为2.5mg/ml海藻酸钠溶液;(3)将步骤(2)海藻酸钠溶液按体积比为1:1比例逐滴加入到步骤(1)酪蛋白酸钠溶液中,使得酪蛋白酸钠和海藻酸钠的质量比例为2:2.5,然后调节混合溶液的ph=5。(4)将浓度为(1-5)mg/ml的β-胡萝卜素的乙醇溶液逐滴加入步骤(3)制备的酪蛋白酸钠和海藻酸钠复合凝胶溶液中,使得酪蛋白酸钠和β-胡萝卜素的质量比例为1:0.5;(5)对步骤(4)的混合溶液进行多频模式超声处理,其中所述的多频超声处理模式为:三频同步超声处理或者双频同步超声处理或者单频超声处理,超声功率密度150w/l;超声脉冲工作时间10s;脉冲间歇时间5s,超声处理时间为40min;三频同步超声处理或者双频同步超声处理或者单频超声处理的超声波频率组合见表3。(6)超声结束后,室温下静置1h,即得负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,喷雾干燥或者冷冻干燥后得到负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝聚物。(7)β-胡萝卜素包封率和负载率的测定取负载β-胡萝卜素的酪蛋白酸钠-海藻酸钠复合凝胶溶液,采用旋转蒸发仪在40℃的温度下浓缩至40ml,取浓缩液1ml加5ml正己烷,混匀后在4℃下以5000rpm离心10分钟。测定正己烷相在波长为450nm处的吸光值,并计算游离β-胡萝卜素(未包埋和松散吸附的β-胡萝卜素)的质量。根据下式计算β-胡萝卜素的包封率和负载率:β-胡萝卜素的包封率(%)=(β-胡萝卜素总质量-游离β-胡萝卜素质量)×100/β-胡萝卜素总质量;β-胡萝卜素的负载率(%)=(β-胡萝卜素总质量-游离β-胡萝卜素质量)×100/样品总质量。实施例11-14制备过程相同,只是超声参数略有改变,表3不同超声波模式对β-胡萝卜素包封率和负载率的影响。表3不同超声波模式对β-胡萝卜素包封率和负载率的影响通过表3中对比实施例11-14不同模式多频率组合的超声波对β-胡萝卜素包封率和负载率的影响,可以发现多模式频率超声波处理可以显著提高酪蛋白酸钠-海藻酸钠复合凝胶包埋β-胡萝卜素的包封率,与对照相比(不超声),双频扫频超声波处理即可使β-胡萝卜素的包封率提高16.5%~44.1%,而28khz/35khz/40khz的三频组合超声波处理则使β-胡萝卜素的包封率提高了44.1%。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1