含咔唑基噻唑烷酮及其制备方法与流程
本发明属于化学合成领域,特别涉及一种含咔唑基噻唑烷酮及其制备方法。
背景技术:
咔唑(又名苯并吡咯),具有较大的共轭体系,良好的刚性平面结构以及很好的给电子能力,因此,咔唑及其衍生物在光电材料方面有着很好的应用。天然咔唑生物碱自身对微生物的具有一定的抗原性,研究者对天然咔唑生物碱的结构进行一定的修饰,使它获得了更好的生物活性,因而在医药领域也有着广泛应用。schiff碱结构中通常含有共轭双键,具有一定的荧光性效应,利用荧光性质来进行微量分析,schiff碱不仅具有易于控制的空间构型、多齿的配位能力,还具有独特的光、电、磁等物理材料性能。现如今,已报道的噻唑烷酮类化合物的合成温度过高,操作复杂。
技术实现要素:
本发明的目的在于提供一种含咔唑基噻唑烷酮及其制备方法,该方法具有操作简单,反应条件温和,反应时间较短,产率高的优点。
为实现上述目的,本发明采用如下技术方案:
含二茂铁基噻唑烷酮,其结构通式为:
其中,r为甲基、乙基、十二烷基、十四烷基、十六烷基等烷基;r1包括h、甲基;r2包括h、烷基、苯基、对氟苯基、邻氯苯基、对氯苯基、2,4-二氯苯基、邻溴苯基、间溴苯基、对溴苯基、2,4-二溴苯基、邻硝基苯基、间硝基苯基、对硝基苯基、3,5-二硝基苯基、邻甲基苯基、间甲基苯基、对甲基苯基、邻甲氧基苯基、间甲氧基苯基、对甲氧基苯基、邻羟基苯基、间羟基苯基、对羟基苯基、呋喃基、噻吩基、2-吡啶基、3-吡啶基或4-吡啶基。
含咔唑基噻唑烷酮的制备方法,包括以下步骤:
于反应容器中,加入amol含咔唑噻二唑schiff碱,bmol巯基乙酸和cmol催化剂,以n,n-二甲基甲酰胺为溶剂,加热反应,tlc监控至反应完全,然后将反应混合液冷却至室温,通过乙酸乙酯进行萃取,减压蒸除溶剂,经柱色谱分离得含咔唑基噻唑烷酮;其中,a:b:c=1:(1.0~1.4):(1.3~1.7)。
进一步的,所述的催化剂为路易斯酸,用量为cmol,a:c=1:(1.3~1.7)。
进一步的,所述的含咔唑基schiff碱的结构通式为:
其中,r为甲基、乙基、十二烷基、十四烷基、十六烷基等烷基;r1包括h、甲基;r2包括h、烷基、苯基、对氟苯基、邻氯苯基、对氯苯基、2,4-二氯苯基、邻溴苯基、间溴苯基、对溴苯基、2,4-二溴苯基、邻硝基苯基、间硝基苯基、对硝基苯基、3,5-二硝基苯基、邻甲基苯基、间甲基苯基、对甲基苯基、邻甲氧基苯基、间甲氧基苯基、对甲氧基苯基、邻羟基苯基、间羟基苯基、对羟基苯基、呋喃基、噻吩基、2-吡啶基、3-吡啶基或4-吡啶基。
进一步的,反应完全的时间为6~8h。
进一步的,反应温度为84~120℃。
进一步的,n,n-二甲基甲酰胺的用量为dml,a:d=1:(100~300)。
进一步的,反应过程用tlc进行监测,当发现咔唑基噻二唑schiff碱的原料点消失时表示反应完全,其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液。
与现有技术相比,本发明的有益效果在于:
本发明提供合成了一系列新型含咔唑基噻唑烷酮,以咔唑基噻二唑schiff碱、巯基乙酸为原料,以路易斯酸为催化剂,制备出含咔唑基噻唑烷酮。操作过程简单,后处理较简单,催化剂廉价易得。本发明通过将咔唑衍生物基及噻二唑基schiff碱与巯基乙酸的环合,得到的噻唑烷酮类衍生物,使其化合物具有更好的生物活性,其在农业,医药,光电信息等领域均具有更好的应用。
附图说明
图1为实施例1所制备的2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮的红外光谱图;
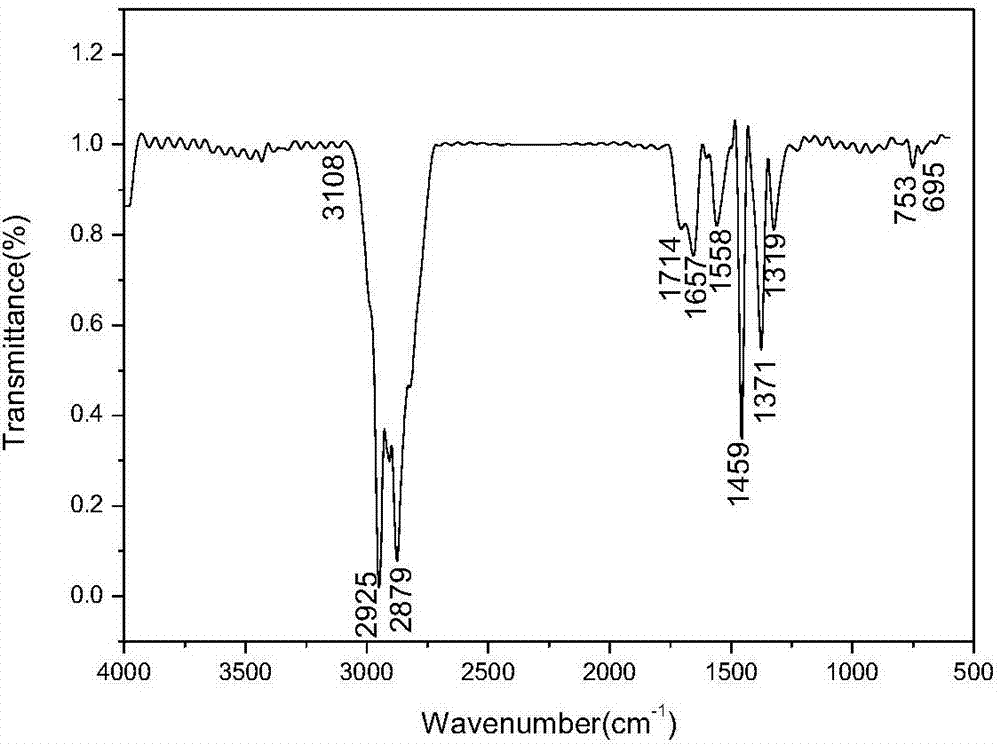
图2为实施例2所制备的2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮的红外光谱图;
图3为实施例3所制备的2-甲基-2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮的的红外光谱图;
图4为实施例4所制备的2-甲基-2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮的红外光谱图。
具体实施方式
以下结合实施例对本发明做进一步详细说明:
本发明是以咔唑基噻二唑schiff碱、巯基乙酸为原料,以路易斯酸为催化剂,dmf为溶剂,制备一系列含二茂铁基噻唑烷酮,其反应方程式如式(3)所示。
其中,r为甲基、乙基、十二烷基、十四烷基、十六烷基等烷基;r1包括h、甲基;r2包括h、烷基、苯基、对氟苯基、邻氯苯基、对氯苯基、2,4-二氯苯基、邻溴苯基、间溴苯基、对溴苯基、2,4-二溴苯基、邻硝基苯基、间硝基苯基、对硝基苯基、3,5-二硝基苯基、邻甲基苯基、间甲基苯基、对甲基苯基、邻甲氧基苯基、间甲氧基苯基、对甲氧基苯基、邻羟基苯基、间羟基苯基、对羟基苯基、呋喃基、噻吩基、2-吡啶基、3-吡啶基或4-吡啶基。
实施例1
于干燥的带有回流冷凝管的三口烧瓶中,加入50mg(0.17mmol)的n-甲基咔唑甲酰氨基噻二唑schiff碱,19.3mg(0.21mmol)的巯基乙酸,10ml的dmf为溶剂,搅拌过程中,加入37.0mg(0.27mmol)氯化锌,升温至90℃,tlc监控,(其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液),反应7h,将反应液冷却,乙酸乙酯进行萃取(3×10ml),再经柱层析分离,减压蒸馏除去溶剂,即得深蓝色2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮,产率69%。
ir(kbr,v/cm-1):2968,2931,2874(饱和c-h);1710(c=o);1527,1454(苯环骨架振动);1377(甲基弯曲振动);1315(c-n伸缩振动);893(=c-h);737(苯环1,2-取代);706(c-s)。
实施例2
于干燥的带有回流冷凝管的三口烧瓶中,加入50mg(0.14mmol)的n-甲基咔唑甲酰-2-氨基-5-苯基噻二唑schiff碱,15.6mg(0.17mmol)的巯基乙酸,10ml的dmf为溶剂,搅拌过程中,加入28.6mg(0.21mmol)氯化锌,升温至90℃,tlc监控,(其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液),反应7h,将反应液冷却,乙酸乙酯进行萃取(3×10ml),再经柱层析分离,减压蒸除溶剂,即得深蓝色2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮,产率68%。
ir(kbr,v/cm-1):3018(苯环c-h);2925,2879(饱和c-h);1714(c=o);1657(c=n);1558,1459(苯环骨架振动);1371(甲基弯曲振动);1319(c-n伸缩振动);753(苯环1,2-取代);695(c-s)。
实施例3
于干燥的带有回流冷凝管的三口烧瓶中,加入50mg(0.16mmol)的n-甲基咔唑乙酰氨基噻二唑schiff碱,17.5mg(0.19mmol)的巯基乙酸,10ml的dmf为溶剂,搅拌过程中,加入32.6mg(0.24mmol)氯化锌,升温至90℃,tlc监控,(其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液),反应7h,将反应液冷却,乙酸乙酯进行萃取(3×10ml),再经柱层析分离,减压蒸除溶剂,即得棕色2-甲基-2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮,产率73%。
ir(kbr,v/cm-1):2958,2879(饱和c-h);1715(c=o);1549,1455(苯环骨架振动);1408,1371(甲基弯曲振动);1288(c-n伸缩振动);898(=c-h);748(苯环1,2-取代);665(c-s)。
实施例4
于干燥的带有回流冷凝管的三口烧瓶中,加入50mg(0.13mmol)的n-甲基咔唑乙酰-2-氨基-5-苯基噻二唑schiff碱,14.7mg(0.16mmol)的巯基乙酸,10ml的dmf为溶剂,搅拌过程中,加入27.2mg(0.20mmol)氯化锌,升温至90℃,tlc监控,(其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液),反应7h,将反应液冷却,乙酸乙酯进行萃取(3×10ml),再经柱层析分离,减压蒸除溶剂,即得棕色2-甲基-2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮,产率74%。
ir(kbr,v/cm-1):3051(苯环c-h);2921,2776(饱和c-h);1715(c=o);1554,1470(苯环骨架振动);1382(甲基弯曲振动);1252(c-n伸缩振动);889(=c-h);758(苯环1,2-取代);685(c-s)。
实施例5
于干燥的带有回流冷凝管的三口烧瓶中,加入0.1mmol的n-甲基咔唑乙酰氨基噻二唑schiff碱,0.14mmol的巯基乙酸,30ml的dmf为溶剂,搅拌过程中,加入0.13mmol氯化锌,升温至84℃,tlc监控,(其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液),反应7h,将反应液冷却,乙酸乙酯进行萃取(3×10ml),再经柱层析分离,减压蒸除溶剂,即得棕色2-甲基-2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮,产率73%。
实施例6
于干燥的带有回流冷凝管的三口烧瓶中,加入0.1mmol的n-甲基咔唑乙酰-2-氨基-5-苯基噻二唑schiff碱,0.1mmol的巯基乙酸,10ml的dmf为溶剂,搅拌过程中,加入0.17mmol氯化锌,升温至120℃,tlc监控,(其中tlc所用的展开剂是体积比为1:2的石油醚和乙酸乙酯的混合液),反应6h,将反应液冷却,乙酸乙酯进行萃取(3×10ml),再经柱层析分离,减压蒸除溶剂,即得棕色2-甲基-2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮,产率74%。
由图1所示,在2968cm-1、2931cm-1和2874cm-1处为饱和c-h伸缩振动的吸收峰,1710cm-1处为c=o振动吸收峰,1527cm-1和1454cm-1处的峰为芳环骨架振动的吸收峰,1377cm-1处为饱和甲基c-h的吸收峰,1315cm-1处为c-n的吸收峰,893cm-1处可能为不饱和氢弯曲振动吸收峰,737cm-1处为苯1,2-取代振动吸收峰,706cm-1处可能为c-s-c振动吸收峰。综上所述,可以证实合成得到了2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮。
由图2所示,3018cm-1处为苯环c-h的振动吸收峰,2925cm-1和2879cm-1处为饱和c-h伸缩振动的吸收峰,1714cm-1处为c=o振动吸收峰,在1657cm-1处的峰为c=n伸缩振动的吸收峰,1558cm-1和1459cm-1处的峰为芳环骨架振动的吸收峰,1371cm-1处为饱和甲基c-h的吸收峰,1319cm-1处为c-n的吸收峰,753cm-1处为苯1,2-取代振动吸收峰,695cm-1处可能为c-s-c振动吸收峰。综上所述,可以证实合成得到了2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮。
由图3所示,在2958cm-1和2879cm-1处为饱和c-h伸缩振动的吸收峰,1715cm-1处为c=o振动吸收峰,1549cm-1和1455cm-1处的峰为芳环骨架振动的吸收峰,1408cm-1和1371cm-1处为饱和甲基c-h的吸收峰,1288cm-1处为c-n的吸收峰,898cm-1处可能为不饱和氢弯曲振动吸收峰,748cm-1处为苯1,2-取代振动吸收峰,665cm-1处可能为c-s-c振动吸收峰。综上所述,可以证实合成得到了2-甲基-2-(9”-甲基咔唑)-3-(1’3’4’-噻二唑)-1,3-噻唑-4-酮。
由图4所示,3051cm-1处为苯环c-h的振动吸收峰,2921cm-1和2776cm-1处为饱和c-h伸缩振动的吸收峰,1715cm-1处为c=o振动吸收峰,1554cm-1和1470cm-1处的峰为芳环骨架振动的吸收峰,1382cm-1处为饱和甲基c-h的吸收峰,1252cm-1处为c-n的吸收峰,889cm-1处可能为不饱和氢弯曲振动吸收峰,758cm-1处为苯1,2-取代振动吸收峰,685cm-1处可能为c-s-c振动吸收峰。综上所述,可以证实合成得到了2-甲基-2-(9”-甲基咔唑)-3-(5’-苯基-1’3’4’-噻二唑)-1,3-噻唑-4-酮。
- 还没有人留言评论。精彩留言会获得点赞!