一种KRAS基因突变检测的引物探针组合及其应用的制作方法
本发明属于分子生物学技术领域,涉及一种基因突变的检测产品,具体涉及一种KRAS基因突变检测的引物探针组合及其应用。
背景技术:
肺癌、结直肠癌是当今世界各国常见的恶性肿瘤,并已成为绝大多数国家癌症死亡的主要原因。其中肺癌以非小细胞肺癌(NSCLC)最常见。KRAS基因位于染色体12p12.1,是重要的癌基因之一,编码一种21kD的KRAS蛋白,参与细胞内的信号传递,主要包括RAS/P13K/PTEN/AKT和RAS/RAF/MEK/ERK 信号转导途径,这些转导途径是当前肿瘤靶向药物研究的热点,靶向药物通过抑制这些途径发生药理作用。研究表明,非小细胞肺癌、结直肠癌组织存在 KRAS基因突变,KRAS基因第12和13密码子发生突变,将导致KRAS蛋白变异并处于持续激活状态,使药物失效。
KRAS基因突变可导致EGFR信号通路下游持续激活,是TKI原发耐药机制之一。大量临床研究表明,靶向药物对于未发生KRAS基因突变的患者有效率可达到60%,而对已发生KRAS基因突变的患者则完全无效。但是,2010年 10月最新研究发现第13密码子上的G13D突变亦对抗体类药物有治疗反应性。通过检测K-ras基因有没有突变,可以筛选出抗EGFR(表皮生长因子受体)靶向药物治疗有效的大肠癌患者,实现肿瘤病人的个体化治疗,从而延长患者生存期。对于没有突变的患者,则能减少不必要的治疗费用和毒副作用。KRAS 基因突变对癌症的发生、形成过程起重要作用。最常见的突变位点90%-97%发生在在外显子1的12和13密码子,其中70%发生于第12密码子,30%发生于13密码子。
对K-ras突变的检测方法有直接测序法、突变体富集PCR、ARMS-PCR、高分辨率熔解曲线(HRM)以及TaqMan-MGB法等,直接测序敏感性低,费用高;突变富集体PCR容易造成PCR的污染而导致假阳性;HRM对模板的要求高,敏感度不高;TaqMan-PCR在敏感度和准确性上均有所提高,但是 ARMS-MGB法要比TaqMan-PCR敏感度、准确性还高,且特异性很高。
ARMS-PCR(Amplification Refractory Mutation System,突变扩增阻滞系统) 技术,是一种利用序列特异性引物对模板进行选择性扩增而达到检测基因突变的方法。ARMS技术利用Taq DNA聚合酶缺少3'→5'外切酶活性,PCR引物的3'端末位碱基必须与其模板DNA互补才能有效扩增的原理,针对不同的已知突变,设计适当的引物以检测出突变基因(即利用特异引物对突变靶序列进行高精准的PCR扩增放大);同时利用探针对扩增产物进行检测,在实时荧光定量PCR平台上实现对样品DNA中稀有突变的检测。
市场上已有采用ARMS-PCR的检测试剂,CN 105567854 A公开了一种检测人EGFR、KRAS、KRAS基因突变的ARMS引物,其在ARMS实时荧光定量技术中引入了双内参系统,还增加了和突变位点一致的正常位点参照,使其成为双内参系统和双重判读规则的试剂盒。CN 102367478 A公开了一种用于 KRAS基因突变分型的ARMS-qPCR检测试剂盒及检测方法。该试剂盒包括 qPCR混合反应液、锁核酸阻滞探针、参照引物、ARMS引物和阳性对照样品。但现有的方法ARMS-PCR的检测试剂检测精准度和特异性不够高,难以在大范围内普及使用。
近年非常令人兴奋的是预测性基因检测的开展,利用基因检测技术在疾病发生前发现疾病发生的风险,提早预防,由于大部分肿瘤突变是体细胞突变,突变细胞常常与野生型细胞混合在一起,因此所获得的的DNA往往含大量的野生型背景,对体细胞突变的检测就需要一种高特异性和高灵敏度的检测方法。
因此,利用与ARMS-MGB法荧光定量PCR技术检测K-ras突变能够可以筛选出抗EGFR(表皮生长因子受体)靶向药物治疗有效的大肠癌患者,实现肿瘤病人的个体化治疗,从而延长患者生存期。
技术实现要素:
针对现有技术的不足,本发明的目的是提供一种KRAS基因突变检测的引物探针组合及其应用,所述试剂盒能够检测速度快,具有很高的特异性和灵敏度。
为达此目的,本发明采用以下技术方案:
第一方面,本发明提供了一种KRAS基因突变检测的引物探针组合,所述引物探针组合包括检测引物探针,所述检测引物探针包括对KRAS基因突变检测特异性引物对、KRAS基因特异性探针、扩增阻断探针和内参系统;
其中,所述KRAS基因的突变检测的位点为外显子1的12和13密码子,具体为G12S、G12C、G12R、G12D、G12A、G12V和G13D突变位点。
本发明中,由于大部分肿瘤突变是体细胞突变,突变细胞常常与野生型细胞混合在一起,因此所获得的DNA往往含大量的野生型背景,因此引物、探针设计必须非常特异,特异的选择了12和13密码子的这7个突变位点,增加了扩增阻碍探针,沉默了样本中的野生型背景,很大程度提高了检测的灵敏度和特异性。
根据本发明,所述KRAS基因突变检测特异性引物对的错配率为15-30%,例如可以是15%、16%、17%、18%、19%、20%、21%、22%、23%、24%、25%、 26%、27%、28%、29%或30%,,优选为20-25%。
本发明中,发明人发现通过调节KRAS基因突变检测特异性引物的错配率,使得绝大部分野生型背景与突变型检测无法结合,且通过增加G-C碱基的错配,使得20bp左右的引物就能达到与Taqman MGB探针5-10℃的Tm差值,使得引物和探针的Tm差异符合MGB探针的设计原则,从而实现对样本中非特异性序列进行阻断扩增的目的,进一步提高检测的准确度和特异性,且仅仅只需要10ng 的DNA样品就能够完成检测,检测灵敏度达到0.5%。
根据本发明,所述扩增阻断探针与KRAS基因突变检测特异性引物对中的下游引物的碱基重叠序列为3-10bp,例如可以是3bp、4bp、5bp、6bp、7bp、 8bp、9bp或10bp,优选为6-9bp。
本发明中,阻碍探针与突变型的引物碱基长度基本一致,且序列3’端最后一个碱基与野生型序列一致,且3’端用磷酸基团封闭,从而抑制KRAS基因突变区野生型模板的非特异性扩增,大大增加KRAS突变检测的灵敏度和特异性。
根据本发明,发明人发现将扩增阻断探针的3’端进行磷酸化,有效的抑制了野生型基因的扩增,沉默了样本中非特异的连接,进一步提高检测的准确率。
优选地,所述KRAS基因特异性探针和所述扩增阻断探针的5’端带有荧光基团,所述荧光基团为FAM、HEX、TET、JOE、NED、VIC、CY3、CY5、ROX 或TAMRA中的任意一种或至少两种的组合,优选为FAM和/或NED。
优选地,所述KRAS基因特异性探针和所述扩增阻断探针的3’端带有淬灭集团,所述淬灭基团选自MGB、BHQ-1、BHQ-2、BHQ-3或Phosphorothioate(PS) 中的任意一种的组合,优选为MGB,所述MGB修饰在3’端。
本发明中,发明人发现采用MGB作淬灭基团可以将探针的Tm值提高 6-10℃左右,提高配对与非配对模板间的Tm值差异,用这种探针可以降低本底,因此检测的重复性和准确度得以大大提高。
根据本发明,所述KRAS基因突变检测特异性引物对的核苷酸序列如SEQ ID NO.1-9所示,具体序列如下:
G12S突变位点的上游引物(SEQ ID NO.1)为:GCGTTGCCTACGCCACT;
G12C突变位点的上游引物(SEQ ID NO.2)为:CCCTGCCTACGCCACA;
G12R突变位点的上游引物(SEQ ID NO.3)为:GCGTTGCCTACGCCACG;
G12D突变位点的上游引物(SEQ ID NO.4)为:CGGTGCCTACGCCAT;
G12A突变位点的上游引物(SEQ ID NO.5)为:GCGCTTGCCTACGCCAG;
G12V突变位点的上游引物(SEQ ID NO.6)为:GCGCTTGCCTACGCCAA;
KRAS基因外显子1的12密码子的通用下游引物(SEQ ID NO.7),即上述 SEQ ID NO.1-6的通用下游引物为: TGTGTGACATGTTCTAATATAGTCACATTTTC;
G13D突变位点的上游引物(SEQ ID NO.8)为: GGGGAGTTGGAGCTGGTGA;
G13D突变位点的下游引物(SEQ ID NO.9)为: GGTCCTGCACCAGTAATATGCATA.
根据本发明,所述KRAS基因特异性探针的核苷酸序列如SEQ ID NO.10-11 所示,具体序列如下:
KRAS基因外显子1的12密码子的特异性探针(SEQ ID NO.10)为: CCTGCTGAAAATGACTGA;
KRAS基因外显子1的13密码子的特异性探针(SEQ ID NO.11)为: TCGTCCACAAAATGATTCTGA.
优选地,所述扩增阻断探针的核苷酸序列如SEQ ID NO.12-14所示,具体序列如下:
KRAS基因外显子1的12密码子扩增阻断探针(SEQ ID NO.12-13)为:
G12S、G12C和G12R突变位点的扩增阻断探针(SEQ ID NO.12): CCACCAGCTCCAACT;
G12D、G12A和G12V突变位点的扩增阻断探针(SEQ ID NO.13): CCACCAGCTCCAAC;
KRAS基因外显子1的13密码子扩增阻断探针(SEQ ID NO.14)为: TGGTGGCGTAGGCAAG.
优选地,所述内参系统包括内参引物对和内参探针。
优选地,所述内参引物对的核苷酸序列如SEQ ID NO.15-16所示,具体序列如下:
正向引物(SEQ ID NO.15):GCGGGTTGTCCTTGAGAAAC;
反向引物(SEQ ID NO.16):AATGGTCCACCCGGTACATC.
优选地,所述内参探针的核苷酸序列如SEQ ID NO.17所示,具体序列如下: CACAGAACTCGGGACC.
第二方面,本发明提供一种检测KRAS基因突变的试剂盒,所述试剂盒包括第一方面所述的引物探针组合物。
根据本发明,所述试剂盒还包括阴性质控、阳性质控和辅助试剂。
优选地,所述阴性质控为TE缓冲液。
优选地,所述阳性质控为KRAS基因G12A突变质粒,所述突变质粒的核苷酸序列如SEQ ID NO.18所示,具体序列如下:
AAGAACTGTCTATGTAGCATTTATGCATTTTTCTTAAGCGTCGATGGAG GAGTTTGTAAATGAAGTACAGTTCATTACGATACACGTCTGCAGTCAACTG GAATTTTCATGATTGAATTTTGTAAGGTATTTTGAAATAATTTTTCATATAAA GGTGAGTTTGTATTAAAAGGTACTGGTGGAGTATTTGATAGTGTATTAACCT TATGTGTGACATGTTCTAATATAGTCACATTTTCATTATTTTTATTATAAGGCC TGCTGAAAATGACTGAATATAAACTTGTGGTAGTTGGAGCTGCTGGCGTAG GCAAGAGTGCCTTGACGATACAGCTAATTCAGAATCATTTTGTGGACGAAT ATGATCCAACAATAGAGGTAAATCTTGTTTTAATATGCATATTACTGGTGCA GGACCATTCTTTGATACAGATAAAGGTTTCTCTGACCATTTTCATGAGTACT TATTACAAGATAATTATGCTGAAAGTTAAGTTATCTGAAATGTACCTTGGGT TTCAAGTTATATGTAACCATTAATATGGGAACTTTACTTTCCTTGGGAGTAT GTCAGGGTCCATGATGTTCACTCTCTGTGCATTTTGA.
优选地,所述辅助试剂为Taq酶、dNTPs、MgCl2和PCR反应缓冲液。
第三方面,本发明提供一种利用如第二方面所述的试剂盒用于检测KRAS 基因突变的方法,包括以下步骤:
(1)提取样本DNA;
(2)向步骤(1)样本DNA中加入PCR缓冲液、Taq酶、dNTPs、MgCl2、 KRAS基因突变检测特异性引物对、KRAS基因特异性探针、扩增阻断探针、内参引物对、内参探针、阳性质控和阴性质控;
(3)PCR扩增。
根据本发明,所述MgCl2的浓度为1-5mM,例如可以是1mM、2mM、3mM、 4mM或5mM,优选为2-4mM。
优选地,所述dNTPs的浓度为0.1-1mM,例如可以是0.1mM、0.2mM、 0.3mM、0.4mM、0.5mM、0.6mM、0.7mM、0.8mM、0.9mM或1mM,优选为0.1-0.8mM。
优选地,所述Taq酶的浓度为0.5-2U/μl,例如可以是0.5U/μl、0.6U/μl、 0.7U/μl、0.8U/μl、0.9U/μl、1U/μl、1.2U/μl、1.3U/μl、1.4U/μl、1.5U/μl、 1.6U/μl、1.7U/μl、1.8U/μl、1.9U/μl或2U/μl。
优选地,所述KRAS基因突变检测特异性引物对的浓度为100-900nM,例如可以是100nM、150nM、180nM、200nM、250nM、280nM、300nM、320 nM、350nM、380nM、400nM、420nM、450nM、480nM、500nM、550nM、 580nM、600nM、650nM、680nM、700nM、750nM、800nM、850nM、880 nM或900nM,优选为200-600nM。
优选地,所述KRAS基因特异性探针的浓度为100-400nM,例如可以是100 nM、150nM、180nM、200nM、250nM、280nM、300nM、320nM、350nM、 380nM或400nM,优选为100-200nM。
优选地,所述扩增阻断探针的浓度为100-300nM,例如可以是100nM、150 nM、180nM、200nM、250nM、280nM或300nM,优选为100-200nM。
优选地,所述内参引物对的浓度为300-900nM,例如可以是300nM、320 nM、350nM、380nM、400nM、420nM、450nM、480nM、500nM、550nM、 580nM、600nM、650nM、680nM、700nM、750nM、800nM、850nM、880 nM或900nM,优选为400-600nM。
优选地,所述内参探针的浓度为100-400nM,例如可以是100nM、150nM、 180nM、200nM、250nM、280nM、300nM、320nM、350nM、380nM或400 nM,优选为100-200nM。
优选地,所述阳性质控的浓度为200-1000copies/μl,例如可以是 200copies/μl、230copies/μl、250copies/μl、280copies/μl、300copies/μl、320 copies/μl、350copies/μl、380copies/μl、400copies/μl、420copies/μl、450copies/μl、480copies/μl、500copies/μl、520copies/μl、550copies/μl、580copies/μl、600 copies/μl、620copies/μl、650copies/μl、680copies/μl、700copies/μl、720copies/μl、 750copies/μl、780copies/μl、800copies/μl、820copies/μl、850copies/μl、880 copies/μl、900copies/μl、920copies/μl、950copies/μl、980copies/μl或1000 copies/μl,优选为300-800copies/μl。
根据本发明,步骤(3)所述的PCR扩增的条件为:
a)95℃预变性2min;
b)95℃变性15s,58℃延伸1min,5个循环;
c)95℃变性15s,60℃延伸1min,40个循环。
1)试剂盒有效性的判定:
阳性对照组有效:阳性对照组在ABI7500的FAM通道下均有典型的扩增曲线,确认无误后通过调节阈值将PC的Ct值均调至24±0.2,并将此阈值作为待检样本的阈值;
阴性对照组有效:阴性对照组在ABI7500的FAM通道下均无典型的扩增曲线或无Ct值,否则可能为试剂受到污染或操作过程中的污染,请排除污染源后重新检测。
2)检测样本有效性的判定:
若Ct值在18-25之间,表明加入的DNA量正常;
若Ct≤18,表明所加样本DNA过量,需稀释后在检测;
若Ct>25,说明加入的样本DNA含有PCR抑制剂或DNA加入量不够,需重新提取DNA后再检测。
3)根据本发明,所述PCR结果突变的判定如下:
对于G12S突变位点,若结果检测通道的Ct值不大于28,则为阳性结果;若结果检测通道的Ct值大于28,则为阴性结果;
对于G12C、G12D和G12A突变位点,若结果检测通道的Ct值不大于31,则为阳性结果;若结果检测通道的Ct值大于31,则为阴性结果;
对于G12R和G12V突变位点,若结果检测通道的Ct值不大于32,则为阳性结果;若结果检测通道的Ct值大于32,则为阴性结果;
对于G13D突变位点,若结果检测通道的Ct值不大于30,则为阳性结果;若结果检测通道的Ct值大于30,则为阴性结果。
第四方面,本发明提供一种如第一方面所述的引物探针组合和/或如第二方面所述的试剂盒用于制备辅助临床诊断、肿瘤相关靶向药物选择或甲状腺癌分子诊断试剂和/或药物中的应用。
与现有技术相比,本发明具有的有益效果:
(1)本发明通过特异选择了12和13密码子的这7个突变位点,增加了扩增阻碍探针,有效的抑制了野生型基因的扩增,可从野生型背景中检测到1%突变等位基因,增加了一根3‘端进行磷酸化修饰的阻断探针,沉默了样本中非特异的连接,实现了高度的反应特异性和灵敏度沉默了样本中的野生型背景,很大程度提高了检测的灵敏度和特异性;
(2)本发明调节KRAS基因突变检测特异性引物的错配率,使得引物和探针的Tm有差异,实现对样本中非特异性序列进行阻断扩增的目的,进一步提高检测的准确度和特异性,且仅仅只需要10ng的DNA样品就能够完成检测,检测灵敏度达到0.5%;
(3)本发明试剂盒包含内参系统,更具有科学性和可靠性,更高的特异性和灵敏度,且本发明试剂盒检测速度快,全部检测过程只需要两个小时即可完成,检测通量大,一台仪器一次可完成48人份的检测;
(4)本发明对仪器设备的要求低,两通道的荧光定量PCR仪即可胜任检测工作,利于大规模的市场推广应用。
附图说明
图1本发明阳性样本G12D突变检测结果;
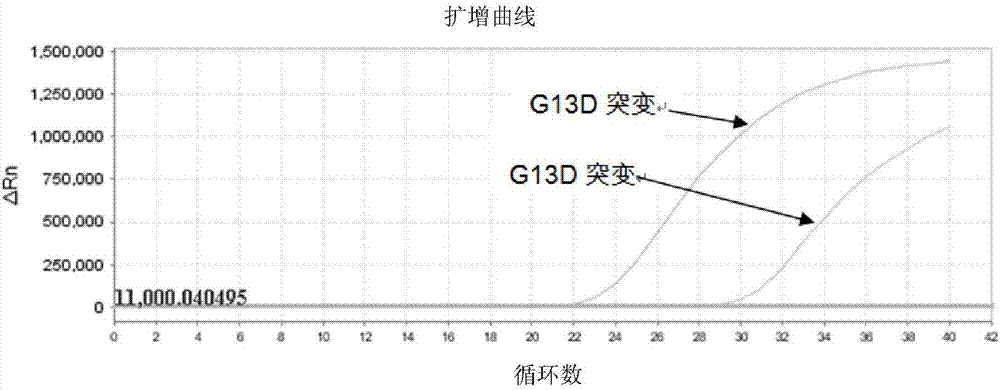
图2本发明阳性样本G13D突变检测结果;
图3本发明阳性样本G12C、G12D和G12V突变检测结果;
图4为本发明G12S突变位点检测灵敏度结果图;
图5为本发明G12C突变位点检测灵敏度结果图;
图6为本发明G12R突变位点检测灵敏度结果图;
图7为本发明G12D突变位点检测灵敏度结果图;
图8为本发明G12A突变位点检测灵敏度结果图;
图9为本发明G12V突变位点检测灵敏度结果图;
图10为本发明G13D突变位点检测灵敏度结果图。
具体实施方式
为更进一步阐述本发明所采取的技术手段及其效果,以下结合本发明的优选实施例来进一步说明本发明的技术方案,但本发明并非局限在实施例范围内。
实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
实施例1试剂盒的组装
引物探针组合的设计,具体序列如下表1所示:
表1
其中,所述KRAS基因突变检测特异性引物对的错配率为22%,所述扩增阻断探针与KRAS基因突变检测特异性引物对中的下游引物的碱基重叠序列为 9bp;
阴性质控品:所述阴性质控为TE缓冲液;
阳性质控品:KRAS基因突变质粒,所述突变质粒的核苷酸序列如SEQ ID NO.18所示,具体序列如下:
AAGAACTGTCTATGTAGCATTTATGCATTTTTCTTAAGCGTCGATGGAG GAGTTTGTAAATGAAGTACAGTTCATTACGATACACGTCTGCAGTCAACTG GAATTTTCATGATTGAATTTTGTAAGGTATTTTGAAATAATTTTTCATATAAA GGTGAGTTTGTATTAAAAGGTACTGGTGGAGTATTTGATAGTGTATTAACCT TATGTGTGACATGTTCTAATATAGTCACATTTTCATTATTTTTATTATAAGGCC TGCTGAAAATGACTGAATATAAACTTGTGGTAGTTGGAGCTGCTGGCGTAG GCAAGAGTGCCTTGACGATACAGCTAATTCAGAATCATTTTGTGGACGAAT ATGATCCAACAATAGAGGTAAATCTTGTTTTAATATGCATATTACTGGTGCA GGACCATTCTTTGATACAGATAAAGGTTTCTCTGACCATTTTCATGAGTACT TATTACAAGATAATTATGCTGAAAGTTAAGTTATCTGAAATGTACCTTGGGT TTCAAGTTATATGTAACCATTAATATGGGAACTTTACTTTCCTTGGGAGTAT GTCAGGGTCCATGATGTTCACTCTCTGTGCATTTTGA;
辅助试剂:Taq酶、dNTPs、MgCl2和PCR反应缓冲液;
将上述组分、说明书及离心管组装后装入试剂盒中。
实施例2KRAS基因突变检测
采用实施例1中的试剂盒进行KRAS基因突变检测,包括如下步骤:
(1)样本DNA提取:
取非小细胞肺癌肿瘤(样本1)、甲状腺癌(样本2)和结直肠癌(样本3) 的石蜡包埋病理组织切片,使用QIAGEN的QIAamp DNA FFPE Tissue Kit (Cat.no.56404)提取石蜡包埋组织切片样本,所提DNA需用紫外分光光度计测定浓度和纯度,其DNA OD260/OD280的值应在1.8~2.0,浓度应在3.3~ 13.2ng/ul之间;
(2)配制体系,具体的体系组成如下表2所示:
表2
向上述反应体系中加入步骤(1)提取的DNA样本,DNA样本量小于15ng,加入至对应的PCR反应孔中,封上荧光定量PCR级别的封闭膜或盖上管盖,以2000rpm/min,离心30s,以确保反应混合液全部离入管底;
(3)将步骤(2)体系放入PCR仪,进行PCR扩增,具体的扩增条件如表3所示:
表3
阶段2的检测荧光通道为FAM,运行PCR反应程序,保存文件;
(4)结果判定:
1)试剂盒有效性的判定:
阳性对照组有效:阳性对照组在ABI7500的FAM通道下应均有典型的扩增曲线,确认无误后通过调节阈值将PC的Ct值均调至24±0.2,并将此阈值作为待检样本的阈值;
阴性对照组有效:阴性对照组在ABI7500的FAM通道下应均无典型的扩增曲线或无Ct值,否则可能为试剂受到污染或操作过程中的污染,请排除污染源后重新检测;
2)检测样本有效性的判定:
若Ct值在18-25之间,表明加入的DNA量正常;
3)根据本发明,所述PCR结果突变的结果如图1-3所示;
从图1-3可以看出,KRAS基因突变检测试剂盒检测非小细胞肺癌肿瘤(样本1)、甲状腺癌(样本2)和结直肠癌(样本3)的阳性样本时,有典型的扩增曲线,其中针对各位点具体如下:
G12S突变位点,Ct值<28;
G12C、G12D和G12A突变位点,Ct值<31;
G12R和G12V突变位点,Ct值<32;
G13D突变位点,Ct值<30;
无非特异性扩增,且准确度达到0.5%;
从图4-图10可以看出,在293细胞基因组DNA中加入1%、2%、10%、 50%的KRAS基因G12A突变质粒时,有典型的扩增曲线,其中针对各位点具体如下:
G12S突变位点,Ct值<28;
G12C、G12D和G12A突变位点,Ct值<31;
G12R和G12V突变位点,Ct值<32;
G13D突变位点,Ct值<30;
无非特异性扩增。
实施例3
与实施例1-2相比,仅仅所述扩增阻断探针与KRAS基因突变检测特异性引物对中的下游引物的碱基重叠序列为2bp,其他组分和条件与实施例1-2相同。
结果显示,则检测样本出现非特异性扩增。
实施例4
与实施例1-2相比,仅仅所述扩增阻断探针与KRAS基因突变检测特异性引物对中的下游引物的碱基重叠序列为12bp,其他组分和条件与实施例1-2相同。
结果显示,则阻断探针与下游引物结合性增强,导致下游引物与上游引物结合率降低,扩增曲线荧光高度下降。
实施例5
与实施例1-2相比,仅仅所述淬灭基团选自BHQ-1,其他组分和条件与实施例1-2相同。
结果显示,猝灭基团BHQ-1的特异性没有MGB好,检测样本会出现轻微的非特异性。
对比例1
与实施例1-2相比,仅仅所述KRAS基因突变检测特异性引物对的错配率为10%,其他组分和条件与实施例1-2相同。
结果显示,则检测样本检测限高,准确度降低,达到3%。
对比例2
与实施例1-2相比,仅仅所述KRAS基因突变检测特异性引物对的错配率为35%,其他组分和条件与实施例1-2相同。
结果显示,发现该对比例PCR结果无荧光,无法完成PCR。
综上所述,本发明通过调节KRAS基因突变检测特异性引物的错配率,使得引物和探针的Tm有差异,实现对样本中非特异性序列进行阻断扩增的目的,进一步提高检测的准确度和特异性,且仅仅只需要10ng的DNA样品就能够完成检测,检测灵敏度达到0.5%。
申请人声明,本发明通过上述实施例来说明本发明的详细方法,但本发明并不局限于上述详细方法,即不意味着本发明必须依赖上述详细方法才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
序列表
<110> 无锡禾盛医疗器械有限公司
<120> 一种KRAS基因突变检测的引物探针组合及其应用
<130> 2018
<160> 18
<170> SIPOSequenceListing 1.0
<210> 1
<211> 17
<212> DNA
<213> 人工合成序列()
<400> 1
gcgttgccta cgccact 17
<210> 2
<211> 16
<212> DNA
<213> 人工合成序列()
<400> 2
ccctgcctac gccaca 16
<210> 3
<211> 17
<212> DNA
<213> 人工合成序列()
<400> 3
gcgttgccta cgccacg 17
<210> 4
<211> 15
<212> DNA
<213> 人工合成序列()
<400> 4
cggtgcctac gccat 15
<210> 5
<211> 17
<212> DNA
<213> 人工合成序列()
<400> 5
gcgcttgcct acgccag 17
<210> 6
<211> 17
<212> DNA
<213> 人工合成序列()
<400> 6
gcgcttgcct acgccaa 17
<210> 7
<211> 32
<212> DNA
<213> 人工合成序列()
<400> 7
tgtgtgacat gttctaatat agtcacattt tc 32
<210> 8
<211> 19
<212> DNA
<213> 人工合成序列()
<400> 8
ggggagttgg agctggtga 19
<210> 9
<211> 24
<212> DNA
<213> 人工合成序列()
<400> 9
ggtcctgcac cagtaatatg cata 24
<210> 10
<211> 18
<212> DNA
<213> 人工合成序列()
<400> 10
cctgctgaaa atgactga 18
<210> 11
<211> 21
<212> DNA
<213> 人工合成序列()
<400> 11
tcgtccacaa aatgattctg a 21
<210> 12
<211> 15
<212> DNA
<213> 人工合成序列()
<400> 12
ccaccagctc caact 15
<210> 13
<211> 14
<212> DNA
<213> 人工合成序列()
<400> 13
ccaccagctc caac 14
<210> 14
<211> 16
<212> DNA
<213> 人工合成序列()
<400> 14
tggtggcgta ggcaag 16
<210> 15
<211> 20
<212> DNA
<213> 人工合成序列()
<400> 15
gcgggttgtc cttgagaaac 20
<210> 16
<211> 20
<212> DNA
<213> 人工合成序列()
<400> 16
aatggtccac ccggtacatc 20
<210> 17
<211> 16
<212> DNA
<213> 人工合成序列()
<400> 17
cacagaactc gggacc 16
<210> 18
<211> 606
<212> DNA
<213> 人工合成序列()
<400> 18
aagaactgtc tatgtagcat ttatgcattt ttcttaagcg tcgatggagg agtttgtaaa 60
tgaagtacag ttcattacga tacacgtctg cagtcaactg gaattttcat gattgaattt 120
tgtaaggtat tttgaaataa tttttcatat aaaggtgagt ttgtattaaa aggtactggt 180
ggagtatttg atagtgtatt aaccttatgt gtgacatgtt ctaatatagt cacattttca 240
ttatttttat tataaggcct gctgaaaatg actgaatata aacttgtggt agttggagct 300
gctggcgtag gcaagagtgc cttgacgata cagctaattc agaatcattt tgtggacgaa 360
tatgatccaa caatagaggt aaatcttgtt ttaatatgca tattactggt gcaggaccat 420
tctttgatac agataaaggt ttctctgacc attttcatga gtacttatta caagataatt 480
atgctgaaag ttaagttatc tgaaatgtac cttgggtttc aagttatatg taaccattaa 540
tatgggaact ttactttcct tgggagtatg tcagggtcca tgatgttcac tctctgtgca 600
ttttga 606
- 还没有人留言评论。精彩留言会获得点赞!
- 用于检测CYP2C19基因多态性的引物、探针及检测试剂盒的制造方法与工艺
- 分子信标探针及引物对、GC基因SNPs位点检测方法与流程
- 一种表面修饰分子印迹固相微萃取探针及其制备与应用的制造方法与工艺
- 一种木瑚菌属食用菌鉴别用分子标记及引物和探针的制造方法与工艺
- 一种用于检测样品中牛凸隆病毒的荧光RT-PCR引物、探针和试剂盒及检测方法与制造工艺
- CYP2C19基因多态性检测引物、探针及试剂盒的制造方法与工艺
- 检测CYP2C9和VKORC1基因多态性的引物、探针和试剂盒的制造方法与工艺
- 一种用于检验临床样本中活菌体的荧光PCR引物探针组及试剂盒的制造方法与工艺
- 含反义碱基的探针法实时荧光PCR的制造方法与工艺
- PCR反应管及包含其的固相载具的制造方法与工艺
- 一种用于评估皮肤抗过敏情况的引物和探针及试剂盒的制作方法
- 一种用于评估皮肤防御情况的引物和探针及试剂盒的制作方法
- 一种荧光定量PCR检测猪delta冠状病毒的引物、探针、试剂盒及方法
- 一种快速区分HP-PRRS疫苗GDr180株与野毒株的引物、探针及方法
- 一种用于检测样品中猪凸隆病毒的荧光rt-pcr引物和探针和试剂盒及检测方法
- 一种阿胶中驴、马、牛和猪源性巢式荧光pcr检测引物、探针、试剂盒、检测方法及应用
- 一种用于评估皮肤防晒情况的引物和探针及试剂盒的制作方法
- 一种用于评估皮肤抗皱情况的引物和探针及试剂盒的制作方法
- 一种用于检测car-t转导效率的引物、探针和方法
- 用于微嵌合检测和个体识别的引物、探针、试剂盒及方法