一种C12、C13位取代齐墩果酸衍生物及其制备和应用的制作方法
本发明属于医药技术领域,具体涉及c12、c13位取代齐墩果酸衍生物及其制备和应用。
背景技术:
齐墩果酸(oa)是植物化学成分,毒性很低,具有抗病毒、消炎、增强免疫和抑制免疫(免疫双向调解作用)、抑制血小板凝集、降血脂、降糖、保肝、护肾、抗艾滋病毒等多种生物活性。齐墩果酸对恶性肿瘤化疗造成的免疫功能下降的恢复和对抗结核药物的肝损害的保护意义重大。
近年来,末期官能化为医药研究提供了一条新的途径,其通过改造先导化合物某些活性位点的基团来合成一系列多样化的结构,以便于找出其中具有活性的化合物。天然产物多样化不需要通过从头合成,而是选择合适的催化剂直接对其修饰,获得目标产物。本发明针对齐墩果酸12号、13号碳,通过一步反应直接构建了c-x键,合成并获得了具有较高活性的抗肿瘤类药天然骨架小分子。
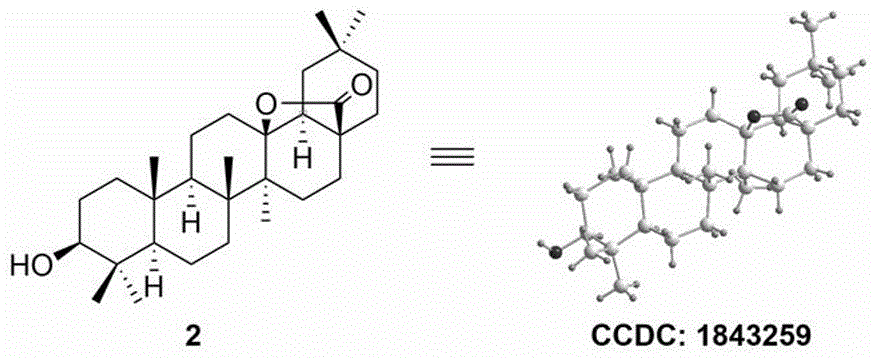
有关齐墩果酸结构修饰的研究很多,antoniomartinez等人报道了与本发明所述的的齐墩果酸衍生物相似的化合物,其用br2溴化齐墩果酸及用n-溴代琥珀酰亚胺与偶氮二异丁腈处理齐墩果酸两种方法,得到的是x为br的齐墩果酸衍生物(tetrahedron.2015,71,792-800)。banitapattnaik等人报道以ccl4作溶剂,用n-溴代琥珀酰亚胺处理齐墩果酸得到x为h的齐墩果酸衍生物(bioorg.chem.2016,68,152-158),即本发明中的化合物2,但是我们重复此实验,得到产物后进行x-射线单晶衍射分析实验,结果却表明产物并非x为h的齐墩果酸衍生物,而是x为br的齐墩果酸衍生物。在我们前期研究工作中,我们采用n-碘代丁二酰亚胺处理oa,得到x为i的齐墩果酸衍生物。然而这些含溴或者碘的齐墩果酸衍生物类药性较差,而含氯的衍生物由于缺少合适的合成条件无法通过常规的合成方法得到。本发明通过筛选超过50多种反应溶剂和混合溶剂和多种氯化试剂,得到一种优秀反应条件,一步反应以高产率得到c12、c13位取代齐墩果酸衍生物,该制备方法简单,反应条件温和,无需复杂的柱层析,能耗低,收率高,实用性强,且所合成的化合物,类药性高,相对分子质量在500以下,细胞实验证明其具有较高的体外抗肿瘤活性,有望用于制备治疗肺癌、肝癌和乳腺癌的药物,同时也为其他同类化合物的合成提供新的解决思路和方案。
技术实现要素:
本发明的目的在于提供一种c12、c13位取代齐墩果酸衍生物及其制备方法和应用,该化合物能够选择性的抑制a549细胞(人非小细胞肺癌细胞)和hepg2细胞(人肝癌细胞)的生长,具有较好的药理活性,且其制备方法简单,实验条件温和,不要求高温高压等苛刻条件,反应收率高。
为实现上述目的本发明采用如下技术方案:
一种c12、c13位取代齐墩果酸衍生物,其结构式如下:
其具体制备步骤包括:
称取齐墩果酸(1当量)于合适的反应瓶中,加入添加剂(0.2-1.3当量,包括n-氯代琥珀酰亚胺、氯胺-t、苯基三甲基三溴化铵、n-碘代丁二酰亚胺、三乙基硅烷中的一种或多种混合)和适量的溶剂(乙二醇二甲醚或2,2,2-三氟乙醇),反应体系在常温下搅拌反应。
应用:c12、c13位取代齐墩果酸衍生物在制备抗肺癌、肝癌和乳腺癌药物中的应用。
本发明的显著优点在于:
(1)本发明通过一步反应高效合成目标化合物,其合成方法简单,操作简便,实验条件温和,反应收率高。
(2)本发明所得的c12、c13位取代齐墩果酸衍生物相对分子质量都小于500,属于小分子化合物,类药性评价高,且生物细胞实验证实该化合物具有较高的抗癌活性,因此该化合物具有用于制备治疗肺癌和肝癌药物的前景。
附图说明
图1为化合物2的球棍模型图。
具体实施方式
为了使本发明所述的内容更加便于理解,下面结合具体实施方式对本发明所述的技术方案做进一步的说明,但是本发明不仅限于此。
实施例1(化合物1)
方法一:
在室温条件下,将齐墩果酸(0.5mmol,228mg)和n-氯代琥珀酰亚胺(0.55mmol,74mg)称至反应瓶中,加入10ml乙二醇二甲醚(dme),反应体系在常温下搅拌反应4天。反应液旋干后,加入5ml乙醇,然后将混悬液直接加入200ml水中,得到白色固体沉淀,过滤后干燥,可得到237mg白色固体产物,收率96%。
方法二:
在室温条件下,将齐墩果酸(0.5mmol,228mg)、氯胺-t(0.65mmol,148mg)和苯基三甲基三溴化铵(ptatb,0.1mmol,38mg)称至反应瓶中,加入10ml2,2,2-三氟乙醇,反应体系在常温下搅拌反应4天。反应液直接加入200ml水中,白色固体沉淀过滤后干燥,可得到184mg白色固体产物,收率75%。
物理状态:白色固体;熔点:218.4–219.1oc.
tlc:rf=0.56(pe/etoac=4:1).
1hnmr(400mhz,cdcl3)δ4.18(s,1h),3.28–3.21(m,1h),2.29–2.12(m,3h),2.01(d,j=5.6hz,2h),1.98–1.90(m,1h),1.73(t,j=11.6hz,3h),1.66–1.61(m,3h),1.55(d,j=11.9hz,3h),1.46(d,j=13.7hz,2h),1.39(s,3h),1.37–1.28(m,3h),1.28–1.23(m,2h),1.20(s,3h),1.08–1.03(m,1h),0.99(s,6h),0.90(s,3h),0.89(s,3h),0.79(s,1h),0.78(s,3h).
13cnmr(101mhz,cdcl3)δ179.02,91.61,78.72,65.10,55.24,51.96,45.32,44.80,43.03,42.38,39.79,38.90,38.52,36.52,34.48,33.92,33.24,31.81,29.34,28.99,27.98,27.50,27.19,23.63,21.31,20.20,18.86,17.71,16.74,15.40.
hrms(esi):calcdforc30h47clo3[m+h]+m/z491.3286,found491.3292.
实施例2(化合物2)
在室温条件下,将齐墩果酸(0.5mmol,228mg)和n-碘代丁二酰亚胺(0.525mmol,118mg)称至反应瓶中,加入10ml2,2,2-三氟乙醇和三乙基硅烷(70mg,0.6mmol),反应体系在常温下搅拌反应3.5小时。反应液直接加入200ml水中,白色固体沉淀过滤后干燥,可得到224mg白色固体产物,收率98%。
物理状态:白色固体;熔点:312.7–313.2oc.
tlc:rf=0.47(pe/etoac=4:1).
1hnmr(400mhz,cdcl3)δ3.22–3.15(m,1h),2.25–2.19(m,1h),1.89–1.81(m,3h),1.80–1.70(m,2h),1.68–1.60(m,3h),1.59–1.53(m,3h),1.51(d,j=5.9hz,1h),1.46(d,j=11.0hz,3h),1.43–1.35(m,2h),1.34–1.29(m,1h),1.25–1.17(m,4h),1.14(s,3h),1.12(s,3h),1.10–0.99(m,1h),0.96(s,3h),0.92(s,1h),0.86(s,3h),0.86(s,3h),0.81(s,3h),0.75(s,3h),0.67(d,j=10.8hz,1h).
13cnmr(101mhz,cdcl3)δ179.25,89.65,78.88,55.12,50.04,47.32,44.96,43.79,41.38,38.98,38.88,36.91,36.14,35.19,34.73,33.03,31.60,29.86,27.99,27.70,27.31,26.56,25.95,23.09,19.52,18.17,18.02,17.79,16.22,15.39.
hrms(esi):calcdforc30h48o3[m+h]+m/z457.3676,found457.3679.
活性测试
(1)化合物对a549肿瘤细胞增殖和存活的抑制作用
材料:人非小细胞肺癌细胞株a549;
受试药物:最终化合物1、2和齐墩果酸;
细胞培养方法:取出液氮中冻存的a549细胞,在37℃的温水中解冻,将细胞悬液移入1.5ml离心管中,置于离心机中,1500rpm离心5min,弃去上清液,加入1mlrpmi1640完全培养液,轻轻吹打均匀,将细胞悬液加入培养皿中,补加3mlrpmi1640完全培养液,将培养皿置于5%co2、37℃培养箱中培养。
细胞毒性实验:将a549细胞以2×104个细胞/孔的密度接种到96孔培养板中,加入不同浓度的化合物,将其置于37℃、5%二氧化碳培养箱中培养72小时。取出培养板,每孔加入10μlcck-8试剂,将培养板继续置于37℃、5%二氧化碳培养箱中孵育3小时后,终止培养,小心吸弃上清液,每孔加入150μl二甲基亚砜,避光振荡10min使结晶物充分溶解;以酶标仪检测450nm处的吸收度od450,并按照以下公式计算细胞存活率:细胞存活率%=(处理组od450/对照组od450)×100%,然后使用spss13.0软件对数据进行处理,并计算癌细胞增殖的半数抑制浓度(ic50)。
(2)化合物对hepg2肿瘤细胞增殖和存活的抑制作用
材料:人肝癌细胞株hepg2;
受试药物:最终化合物1、2和齐墩果酸;
细胞培养方法:取出液氮中冻存的hepg2细胞,在37℃的温水中解冻,将细胞悬液移入1.5ml离心管中,置于离心机中,1500rpm离心5min,弃去上清液,加入1mlrpmi1640完全培养液,轻轻吹打均匀,将细胞悬液加入培养皿中,补加3mlrpmi1640完全培养液,将培养皿置于5%co2、37℃培养箱中培养。
细胞毒性实验:将hepg2细胞以2×104个细胞/孔的密度接种到96孔培养板中,加入不同浓度的化合物,将其置于37℃、5%二氧化碳培养箱中培养。取出培养板,每孔加入10μlcck-8试剂,将培养板继续置于37℃、5%二氧化碳培养箱中孵育3小时后,终止培养,小心吸弃上清液,每孔加入150μl二甲基亚砜,避光振荡10min使结晶物充分溶解;以酶标仪检测450nm处的吸收度od450,并按照以下公式计算细胞存活率:细胞存活率%=(处理组od450/对照组od450)×100%,然后使用spss13.0软件对数据进行处理,并计算癌细胞增殖的半数抑制浓度(ic50)。
(3)化合物对mda-mb-231肿瘤细胞增殖和存活的抑制作用
材料:人乳腺癌细胞株mda-mb-231;
受试药物:最终化合物1、2和齐墩果酸;
细胞培养方法:取出液氮中冻存的231细胞,在37℃的温水中解冻,将细胞悬液移入1.5ml离心管中,置于离心机中,1500rpm离心5min,弃去上清液,加入1mlrpmi1640完全培养液,轻轻吹打均匀,将细胞悬液加入培养皿中,补加3mlrpmi1640完全培养液,将培养皿置于5%co2、37℃培养箱中培养。
细胞毒性实验:将231细胞以2×104个细胞/孔的密度接种到96孔培养板中,加入不同浓度的化合物,将其置于37℃、5%二氧化碳培养箱中培养。取出培养板,每孔加入10μlcck-8试剂,将培养板继续置于37℃、5%二氧化碳培养箱中孵育3小时后,终止培养,小心吸弃上清液,每孔加入150μl二甲基亚砜,避光振荡10min使结晶物充分溶解;以酶标仪检测450nm处的吸收度od450,并按照以下公式计算细胞存活率:细胞存活率%=(处理组od450/对照组od450)×100%,然后使用spss13.0软件对数据进行处理,并计算癌细胞增殖的半数抑制浓度(ic50)。
实施例1、实施例2所得最终化合物1、2和齐墩果酸的活性参数如表1所示,ic50值为化合物1、2和齐墩果酸作用于癌细胞72小时后对应癌细胞半数有效抑制浓度。
表1.化合物的活性参数
由表1可见,修饰过的齐墩果酸衍生物更好抑制了癌细胞的生长,对a549细胞、hepg2细胞、mda-mb-231细胞均表现较好的活性,与齐墩果酸比,其半数抑制浓度ic50降低了约24-100倍。
缩略词说明:
dme(乙二醇二甲醚);ptatb(苯基三甲基三溴化铵);cf3ch2oh(2,2,2-三氟乙醇);tesh(三乙基硅烷)。
以上所述仅为本发明的较佳实施例,凡依本发明申请专利范围所做的均等变化与修饰,皆应属本发明的涵盖范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 用于生产化学品及其衍生物的组合物和方法与制造工艺
- 7‑OH‑8‑[(1‑胺基‑1‑苯基衍生物)‑次甲基]‑黄酮化合物及其制备方法及其应用与制造工艺
- 联苯胺衍生物、其制造方法和电子照相感光体与制造工艺
- 包含环糊精衍生物的可注射美法仑组合物及其制备和使用方法与制造工艺
- 含D型非天然氨基酸的抗菌肽类似物及其合成与应用的制造方法与工艺
- 一种黄芪甲苷衍生物及其制备方法和应用与制造工艺
- (Z,E)5‑OH‑3‑(苯基衍生物‑次甲基)‑二氢黄酮‑7‑O‑糖苷及其制备及其应用的制造方法与工艺
- 喹唑啉衍生物的制造方法与工艺
- 一种白杨素氨基酸衍生物的制备方法与制造工艺
- Harrisotone A衍生物的组合物在防治肝脏损伤药物中的应用的制造方法与工艺
- 联苯胺衍生物、其制造方法和电子照相感光体与制造工艺
- 包含环糊精衍生物的可注射美法仑组合物及其制备和使用方法与制造工艺
- 一种黄芪甲苷衍生物及其制备方法和应用与制造工艺
- (Z,E)5‑OH‑3‑(苯基衍生物‑次甲基)‑二氢黄酮‑7‑O‑糖苷及其制备及其应用的制造方法与工艺
- 喹唑啉衍生物的制造方法与工艺
- 吡唑衍生物及其作为大麻素受体介体的用途的制造方法与工艺
- Harrisotone A衍生物的组合物在防治肝脏损伤药物中的应用的制造方法与工艺
- 水生态处理中淤泥及衍生物的再利用处理系统的制造方法与工艺
- Schiglautone A衍生物的组合物用于制备抗缺氧药物的制作方法
- Schiglautone A衍生物的组合物用于制备抗红细胞低下性贫血药物的制作方法
- Harrisotone A衍生物的组合物在防治肝脏损伤药物中的应用的制造方法与工艺
- 水生态处理中淤泥及衍生物的再利用处理系统的制造方法与工艺
- 一种新型罗汉果醇衍生物单体的制作方法
- Schiglautone A衍生物的组合物用于制备抗鼻炎药物的制作方法
- Schiglautone A衍生物的组合物用于制备防治肾纤维化药物的制作方法
- Artalbic acid衍生物的组合物用于制备抗心衰药物的制作方法
- Artalbic acid衍生物的组合物用于制备抗慢性阻塞性肺病药物的制作方法
- Schiglautone A 衍生物的组合物用于制备抗慢性阻塞性肺病药物的制作方法
- Artalbic acid的衍生物的组合物用于制备抗慢性阻塞性肺病药物的制作方法
- Artalbic acid的衍生物的组合物用于制备防治胰腺纤维化药物的制作方法