具有选择性抗铜绿假单胞菌活性的灭菌肽及其活性优化修饰物的制作方法
本发明涉及抗菌肽领域,特别是一种具有选择性抗铜绿假单胞菌活性的灭菌肽及其活性优化修饰物。
背景技术:
作为现代医学的一大支柱,抗生素在处理感染起到了巨大的作用。然而,近三十多年来,各种各样的感染仍然是人类健康的最大敌人之一。2017年9月,世卫组织正式发布了“全球濒临抗生素枯竭”的报告。由于对抗生素的使用不当或过度使用,许多细菌产生耐药性或快速进化成致命性的超级细菌,如在德国引发重大疫情的出血性大肠杆菌素、在美国被称为杀手的耐碳青霉烯的肠杆菌。当前,由于抗生素耐药性的产生,细菌感染发生的死亡总人数已经超过癌症和艾滋病的总和。更为重要的是,一旦发生细菌恐怖袭击,将是对国家、民族甚至全人类最可怕的灾难。澳大利亚首席科学家伊恩·查布曾指出,抗生素耐药性很可能会成为全球面临的最严重公共卫生挑战之一,这需要科学界、企业界和公众共同应对。
近年来,抗菌肽的开发与应用成为研究的热点。具有广谱抗微生物活性的抗菌肽,不仅对细菌毒素有中和作用,还能抗真菌、抗病毒、抑制或杀伤肿瘤细胞、杀灭寄生虫和原虫等。其作用机制独特,不易产生耐药性,抗菌肽只对原核生物细胞和真核生物病变细胞有抗菌作用,对正常的真核生物细胞不起作用。
在饲料中添加抗菌肽代替传统抗生素。抗菌肽不仅能够耐受饲料加工过程中高温高压的剧烈条件,并且可以在饲料保存过程中持续发挥其功能,保持饲料品质,延长贮存期限。比如,利用抗菌肽的抑菌活性,可以抑制产品在加工及销售中滋生的有害菌,延长产品货架期;在饲料中添加可以起到天然防霉防腐剂的作用,能抑制致病菌,如大肠杆菌、沙门氏菌、金黄色葡萄球菌等,以及引起饲料霉变的多种霉菌。抗菌肽杀菌机理独特,病原菌不易对抗菌肽产生耐药性。再者,抗菌肽产品具广谱抗菌作用,对畜禽具有促生长、保健和治疗疾病的功能,属无毒副作用、无残留、无致细菌耐药性的一类环保型制剂。据美国学者报道,抗菌肽可以作为饲料防霉剂。
在医药方面抗菌肽就成为其中最有前途的选择之一。新型抗菌药物抗菌肽由于其作用机理不同于传统抗生素,不会使细菌产生耐药性。而且除抗菌作用之外,还有促进伤口的快速愈合,消炎,抗感染的功能。抗菌肽可谓抗菌药物中的新秀。
抗菌肽还可作为新型的天然防腐剂,因为抗菌肽表现出的良好的热稳定性,可以用于热加工食品。其强大的抗菌活性可以防止食品生产,发酵过程中的杂菌污染。因此,把抗菌肽用作食品防腐剂是广阔的。
学界公认,抗菌肽是当前替代化学抗生素的最佳替代品。然而,到目前为止,全球极少有抗菌肽药物达到临床使用的要求。市场需要开发人源天然抗菌肽成药,本发明解决这样的问题。
技术实现要素:
为解决现有技术的不足,本发明的目的在于提供一种具有选择性抗铜绿假单胞菌活性的灭菌肽及其活性优化修饰物,本发明从人体足跟角质层脚屑中提取、分离并纯化得到选择性抑制铜绿假单胞菌的抗菌肽,并对氨基酸序列进行修饰,得到几种灭菌效果更强的修饰序列,也得到几种灭菌效果较好,但是长度短,成本低的修饰序列,扩大使用范围。
为了实现上述目标,本发明采用如下的技术方案:
具有选择性抗铜绿假单胞菌活性的灭菌肽,抗菌肽是具有选择性抑制铜绿假单胞菌活性的人源天然蛋白,抗菌肽的氨基酸序列由12-22个氨基酸残基组成,其氨基酸序列为:seqidno.1;
seqidno.1:grhgsglghssshgqhgsgsgr。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽,抗菌肽从人体足跟角质层脚屑中提取、分离、纯化得到。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽,
提取的过程为:
收集人体足跟角质层脚屑,采用酸性乙酰乙酸缓冲液提取总蛋白;
分离、纯化的过程为:
提取的总蛋白经超滤管以三羟甲基氨基甲烷柠檬酸盐缓冲液膜渗滤后,用肝素琼脂糖凝胶柱进行亲和层析;
附着肝素的蛋白先通过含氯化钠的三羟甲基氨基甲烷柠檬酸盐缓冲液洗脱,再用三氟乙酸进行膜渗滤;
渗出液通过制备柱以反向高效液相色谱方式进行分离纯化,富集的蛋白经冷冻干燥后溶解于乙酸水溶液中保存;
富集的蛋白通过制备柱以反向高效液相色谱方式进行再一次分离纯化,分别收集各个峰值区的蛋白并用质谱仪进行分子量鉴定和氮末端蛋白测序。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽,抗菌肽seqno.1对铜绿假单胞菌的最小杀菌浓度mbc90达到0.038μg/ml。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽,抗菌肽seqno.1对铜绿假单胞菌的杀菌效果依赖于酸性环境。
具有选择性抗铜绿假单胞菌活性的灭菌肽的活性优化修饰物,根据选择性抑制铜绿假单胞菌活性的灭菌肽seqidno.1多肽合成得到;包括:氨基酸序列:seqidno.2-6;
seqidno.1:grhgsglghssshgqhgsgsgr,
seqidno.2:ghhggggghggghgghgggggh,
seqidno.3:rgsgsghqghssshglgsghrg,
seqidno.4:slssghgsghghqrgghrsgsg,
seqidno.5:grhgsglghssshgqh,
seqidno.6:hahsghgqstqr。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽的活性优化修饰物,seqno.2、seqno.3和seqno.4的杀菌效果相比seqidno.1的杀菌效果强,最小杀菌浓度mbc90都小于0.019μg/ml。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽的活性优化修饰物,seqno.5的最小杀菌浓度mbc90达到0.3μg/ml。
前述的具有选择性抗铜绿假单胞菌活性的灭菌肽的活性优化修饰物,seqno.6的最小杀菌浓度mbc90达到0.15μg/ml。
本发明的有益之处在于:
本发明从人体足跟角质层脚屑中提取、分离并纯化得到选择性抑制铜绿假单胞菌的抗菌肽,实现对铜绿假单胞菌具有选择性的抑制活性,因为提取源头是人体,所以不会具有排斥现象;
本发明对抗菌肽的氨基酸序列进行修饰得到得到几种灭菌效果更强的修饰序列,也得到几种灭菌效果较好,但是长度短,成本低的修饰序列,具有改良为成药的潜力;
抗菌肽及其活性优化修饰物应用范围广,可以应用于抗生素、消毒剂、防腐剂或包装材料中;
抗菌肽与传统抗生素联合用药会产生协同作用,可以实现更好的抗菌效果,同时可以有效降低抗生素的使用剂量。
附图说明
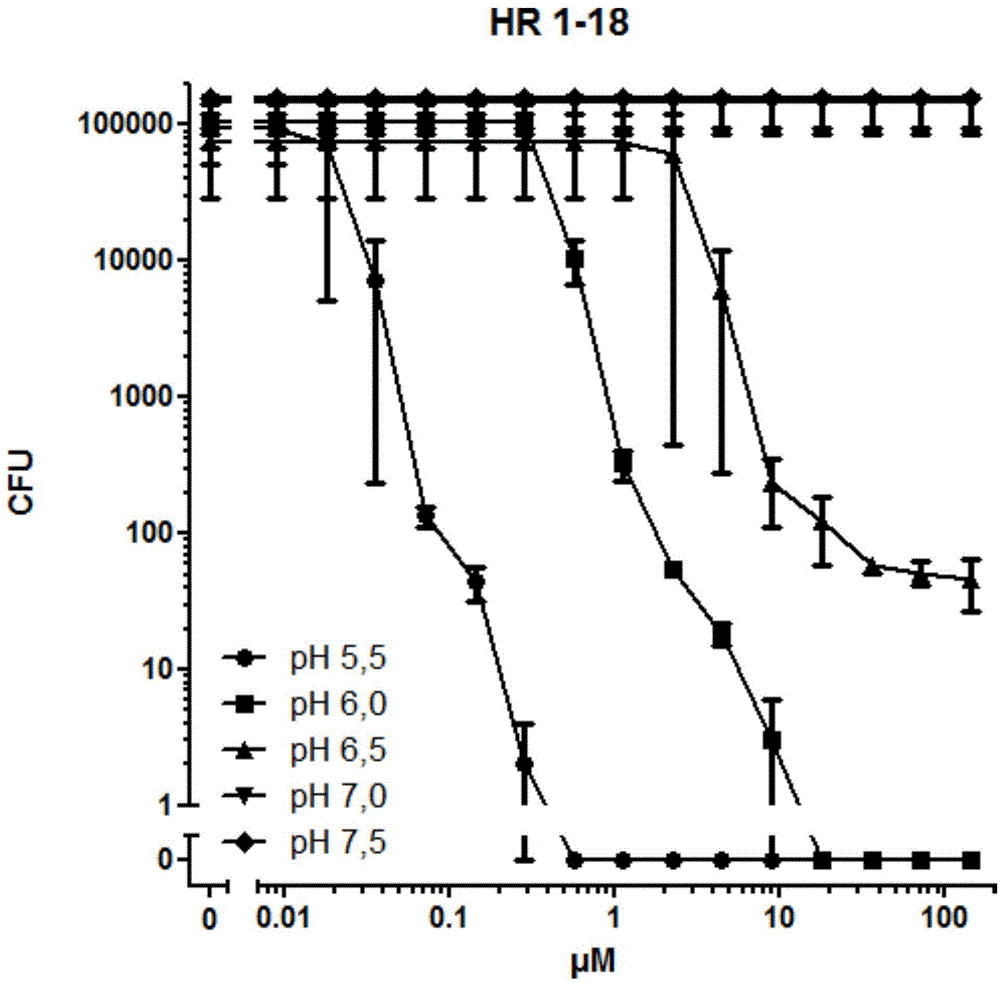
图1是ph值对本发明的角蛋白小肽hr1-18(seqno.1)杀菌效率的影响示意图,cfu指菌落形成单位;
图2是显示角蛋白小肽hr1-18对铜绿假单胞菌的杀菌机理的透射电镜照片;a)铜绿假单胞菌经hr1-18处理2小时后的透射电镜照片;b)免疫胶体金电镜照片。
具体实施方式
以下结合附图和具体实施例对本发明作具体的介绍。
具有选择性抗铜绿假单胞菌活性的灭菌肽,抗菌肽是具有选择性抑制铜绿假单胞菌活性的人源天然蛋白,抗菌肽的氨基酸序列由12-22个氨基酸残基组成,其氨基酸序列为:seqidno.1;
seqidno.1:grhgsglghssshgqhgsgsgr。
抗菌肽从人体足跟角质层脚屑中提取、分离、纯化得到。
提取的过程为:
收集80-120克人体足跟角质层脚屑,采用酸性乙酰乙酸缓冲液按照参考方法(schroeder,1997)提取总蛋白;
分离、纯化的过程为:
提取的总蛋白经amicon公司超滤管(3000道尔顿)以10毫摩尔三羟甲基氨基甲烷柠檬酸盐缓冲液(ph8.0)膜渗滤后,采用pharmacia公司肝素琼脂糖凝胶柱进行亲和层析;
附着肝素的蛋白先通过含2摩尔氯化钠的100毫摩尔三羟甲基氨基甲烷柠檬酸盐缓冲液(ph8.0)洗脱,再用0.1%三氟乙酸进行膜渗滤;
渗出液通过macherey&nagel公司的c8制备柱(300x7mm,c8nucleosil,250x12.6mm)以反向高效液相色谱(rp-hplc)方式进行分离纯化,富集的蛋白经冷冻干燥后溶解于5毫升0.01%(v/v)乙酸水溶液中保存;
富集的蛋白通过macherey&nagel公司的c2-c18制备柱以反向高效液相色谱(rp-hplc)方式进行再一次分离纯化,分别收集各个峰值区的蛋白并采用micromass公司的质谱仪进行分子量鉴定和氮末端蛋白测序。
具有选择性抗铜绿假单胞菌活性的灭菌肽的活性优化修饰物,根据选择性抑制铜绿假单胞菌活性的灭菌肽seqidno.1多肽合成得到;包括:氨基酸序列:seqidno.2-6;
seqidno.1:grhgsglghssshgqhgsgsgr,
seqidno.2:ghhggggghggghgghgggggh,
seqidno.3:rgsgsghqghssshglgsghrg,
seqidno.4:slssghgsghghqrgghrsgsg,
seqidno.5:grhgsglghssshgqh,
seqidno.6:hahsghgqstqr。
抗菌肽修饰的过程:因为所有小肽的氨基酸序列长度为12-23,都可以采用市场已有的多肽合成仪快速人工合成,如美国appliedbiosystems公司的abi433peptidesynthesizer、csbio公司的cs336无死角多肽合成仪和proteintechnologies公司的tribute双通道多肽合成仪。
验证实验部分:
实验一:角蛋白小肽hr1-18(seqno.1)对铜绿假单胞菌的杀菌效率实验;
实验过程:首先吸取经过活化的铜绿假单胞菌(pseudomonasaeruginosa)atcc10145菌液接入营养肉汤培养基中,置于恒温振荡培养箱中振荡培养至对数期作为原菌液;吸取1ml原菌液离心富集后用含有1%胰蛋白酶大豆汤(tsb)的10毫摩尔磷酸钠缓冲液(ph值5.5)清洗并倍比稀释成105cfu/ml的菌悬液,同时配备倍比稀释成104cfu/ml、103cfu/ml、102cfu/ml稀释菌悬液待用。每100μl菌悬液滴加10μl角蛋白小肽hr1-18及其活性改良小肽蛋白液(蛋白浓度初始为19ng/ml,依次2倍叠加,直到100μg/ml),另设2组平行实验组,设溶菌酶为阳性对照组,0.01%乙酰乙酸为阴性对照组。每个菌悬处理液在恒温恒湿培养箱中,37℃培养2小时后均匀涂布于营养肉汤培养基固体平板上,后倒置于恒温恒湿培养箱中,37℃培养16小时。采用日本biokobe公司的菌落计数仪统计菌落数。杀菌效率采用最小杀菌浓度mbc90或mbc100表示,指杀死90%或100%的供试铜绿假单胞菌所需的最低角蛋白小肽浓度。
实验结果:
实验结果分析:
由所得结果可以知道角蛋白小肽hr1-18(seqno.1)对铜绿假单胞菌的杀菌效果很强,最小杀菌浓度mbc90达到0.038μg/ml。经对hr1-18氨基酸序列进行优化后,seqno.2、seqno.3和seqno.4的杀菌效果更强,mbc90都小于0.019μg/ml,超过多数抗生素的药效。另外,经对hr1-18氨基酸序列进行缩小改装,seqno.5和seqno.6的杀菌效果也较好,其中seqno.6的mbc90达到0.15μg/ml。由于seqno.6只有12个氨基酸残基长度,化学合成成本低。由此可知,角蛋白小肽hr1-18及其活性改良为成药的潜力。
实验二:ph值对角蛋白小肽hr1-18(seqno.1)杀菌效率的影响;
首先吸取经过活化的铜绿假单胞菌(pseudomonasaeruginosa)atcc10145菌液接入营养肉汤培养基中,置于恒温振荡培养箱中振荡培养至对数期作为原菌液;吸取1ml原菌液离心富集后用含有1%胰蛋白酶大豆汤(tsb)的10毫摩尔磷酸钠缓冲液(ph值5.5)清洗并倍比稀释成105cfu/ml的菌悬液,同时配备倍比稀释成104cfu/ml、103cfu/ml、102cfu/ml稀释菌悬液待用。每100μl菌悬液滴加10μl角蛋白小肽hr1-18(蛋白浓度初始为19ng/ml,依次2倍叠加,直到100μg/ml),另设2组平行实验组,设溶菌酶为阳性对照组,0.01%乙酰乙酸为阴性对照组。每个菌悬处理液在恒温恒湿培养箱中,37℃培养2小时后均匀涂布于营养肉汤培养基固体平板上,后倒置于恒温恒湿培养箱中,37℃培养16小时。采用日本biokobe公司的菌落计数仪统计菌落数。
实验结果如表二所示:
表二ph值对hr1-18杀菌效率的影响
注:a、hr1-18用量单位μg/ml;
b、原始数据为2次重复实验;数据结果表示为菌落统计上的菌落行程单位(cfu)数值;
c、该表格图形表示为图2.
结果分析:
由所得结果可以知道角蛋白小肽hr1-18(seqno.1)对铜绿假单胞菌的杀菌效果依赖于酸性环境。由于,皮肤表面和胃肠道环境的实际ph值极低(小于3),hr1-18在临床应用上很有意义。
实验三:电镜照片显示角蛋白小肽hr1-18对铜绿假单胞菌的杀菌机理;
首先吸取经过活化的铜绿假单胞菌atcc10145菌液接入营养肉汤培养基中,置于恒温振荡培养箱中振荡培养至对数期作为原菌液;吸取1ml原菌液离心富集后用含有0.25%葡萄糖的10毫摩尔磷酸钠缓冲液(ph5.5)清洗并倍比稀释成od600值为2.0的菌悬液待用。每109cfu/ml菌悬液滴加角蛋白小肽hr1-18至浓度100μg/ml,在恒温恒湿培养箱中,37℃培养2小时后,采用2.5%戊二醛在4℃下过夜固定。然后,3220g离心10min,取沉淀并在44℃下悬浮于2%nobel琼脂溶剂中。再经离心冷却后,含菌琼脂块进行系列乙醇脱水,并逐步过渡到聚羟基芳族丙烯酸树脂替代,60℃下包埋。硬化的树脂切成5nm小块.置于网格中备用。样品用透射电镜(飞利浦tem208)进行分析。
如图2所示为透射电镜照片显示角蛋白小肽hr1-18对铜绿假单胞菌的杀菌机理。a)铜绿假单胞菌经hr1-18处理2小时候后,透射电镜照片显示胞浆内含物出现聚集成团;b)免疫胶体金电镜照片显示hr1-18不附着在膜上而在胞内。
本发明从人体足跟角质层脚屑中提取、分离并纯化得到选择性抑制铜绿假单胞菌的抗菌肽,实现对铜绿假单胞菌具有选择性的抑制活性,因为提取源头是人体,所以不会具有排斥现象;本发明对抗菌肽的氨基酸序列进行修饰得到得到几种灭菌效果更强的修饰序列,也得到几种灭菌效果较好,但是长度短,成本低的修饰序列,具有改良为成药的潜力;抗菌肽及其活性优化修饰物应用范围广,可以应用于抗生素、消毒剂、防腐剂或包装材料中;抗菌肽与传统抗生素联合用药会产生协同作用,可以实现更好的抗菌效果,同时可以有效降低抗生素的使用剂量。
以上显示和描述了本发明的基本原理、主要特征和优点。本行业的技术人员应该了解,上述实施例不以任何形式限制本发明,凡采用等同替换或等效变换的方式所获得的技术方案,均落在本发明的保护范围内。
序列表
<110>浙江长兴亮肽生物技术有限公司
<120>具有选择性抗铜绿假单胞菌活性的灭菌肽及其活性优化修饰物
<141>2018-11-19
<160>6
<170>siposequencelisting1.0
<210>1
<211>22
<212>prt
<213>nativeproteins
<400>1
glyarghisglyserglyleuglyhisserserserhisglyglnhis
151015
glyserglyserglyarg
20
<210>2
<211>22
<212>prt
<213>artificialsequence
<400>2
glyhishisglyglyglyglyglyhisglyglyglyhisglyglyhis
151015
glyglyglyglyglyhis
20
<210>3
<211>22
<212>prt
<213>artificialsequence
<400>3
argglyserglyserglyhisglnglyhisserserserhisglyleu
151015
glyserglyhisarggly
20
<210>4
<211>22
<212>prt
<213>artificialsequence
<400>4
serleuserserglyhisglyserglyhisglyhisglnargglygly
151015
hisargserglysergly
20
<210>5
<211>16
<212>prt
<213>artificialsequence
<400>5
glyarghisglyserglyleuglyhisserserserhisglyglnhis
151015
<210>6
<211>12
<212>prt
<213>artificialsequence
<400>6
hisalahisserglyhisglyglnserthrglnarg
1510
- 还没有人留言评论。精彩留言会获得点赞!