一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物及其制备方法和用途与流程
本发明属于药物化学领域,具体涉及一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物及其制备方法和用途。
背景技术:
阿尔茨海默症(alzheimer’sdisease,ad)是老年人中发病率和致死率最高的疾病之一。阿尔茨海默症国际协会(alzheimer’sdiseaseinternational,adi)发布的《2015全球阿尔茨海默症报告》指出,2015年全球已有超过4600万人患上痴呆症,据预测,到2050年,全球将有1.315亿人口受到痴呆的困扰,其中中国痴呆症患者的发病率已达到6.61%。随着人均生存年龄的延长,本病已发展为社会和医疗保健系统的主要负担,并且为社会、患者及家属带来了沉重的精神和经济压力。因而,研究开发新型老年痴呆治疗药物意义重大。从市场需求来看,阿尔茨海默症国际协会预测,到2050年老年痴呆症治疗药物的全球销售额将达6000亿美元;在我国,随着老年痴呆症发病率的迅速上升,这类药物的市场也快速膨胀。
ad是一种慢性的、以进行性记忆和认知功能损害为特征的多病因、多环节参与的复杂神经退行性疾病,其主要病理学特征为β-淀粉样肽(β-amyloidpeptide,aβ)大量沉积形成的老年斑(senileplaque,sp)、tau蛋白过度磷酸化形成的神经纤维缠结(neurofibrillarytangle,nft),并伴随神经元的凋亡和神经突触的退化等。近年来,许多研究者致力于从分子和细胞水平来揭示ad的发病机理,提出了多种假说,如:胆碱能神经元损伤、淀粉样蛋白的沉积、tau蛋白过度磷酸化、炎症、自由基氧化、金属离子失调等,因此,针对这些发病机制来发展的新型治疗途径和手段,将有希望缓解和改善ad患者的病情。目前临床上有效治疗ad的药物主要是基于神经递质乙酰胆碱不足导致认知功能失调的胆碱能假说,采用乙酰胆碱酯酶抑制剂来提高病人脑内乙酰胆碱水平,如:tacrine、donepezil、ravastigmine、galantamine。但长期临床使用表明,这些药物可短期内缓解ad的症状,但不能从根本上有效阻止或逆转病程,而且还会导致经典的胆碱能毒性,如引起幻觉、意识混沌、头晕、恶心、肝脏毒性、食欲不振以及大便频繁等。因此,临床上迫切需要研发具有新型作用机制的ad治疗药物。
ad病因复杂,至今尚未完全阐明其发病机制,但研究表明,患者脑内乙酰胆碱水平降低、β-淀粉样蛋白的过度生成与沉积、金属离子代谢紊乱、ca2+平衡失调、tau-蛋白过度磷酸化导致的神经纤维缠结、谷氨酸受体活性过高、氧化应激产生大量活性氧(ros)和自由基以及神经炎症反应等多种因素在ad的发病过程中扮演重要角色。针对上述发病因素,研究人员采用传统的“一药一靶”药物设计策略,发现了大量对某一靶点具有高活性和高选择性的药物,如:胆碱酯酶抑制剂和nmda受体拮抗剂等,这些药物存在作用靶点单一、临床使用毒副作用较多,对ad患者的长期疗效欠佳等问题。
近年来,随着对ad致病机理的不断阐明,发现ad的发生和发展具有多机制、多因素作用的特点,不同机制之间有相互关联相互影响,构成了ad发生和发展过程复杂的网络调控系统。基于上述结果,研究人员提出了“多靶点导向药物(multitarget-directedligands,mtdls)”策略来研发抗神经退行性疾病药物。所谓“多靶点药物”是指单一化学实体同时作用于疾病网络中的多个靶点,对各靶点的作用可产生协同效应,使总效应大于各单效应之和,此类药也称为“multifunctional”或“multipotential”药物。多靶点药物与多药联合应用以及复方药物的主要区别在于:可减少服药量、提高治疗效果、避免药物之间的相互作用及由此带来的毒副作用,均一的药代动力学特性,便于使用等。因此,研究开发具有新型化学结构、新型作用机制,具有多靶点作用、低毒副作用的抗神经退行性疾病治疗药物不仅符合社会老龄化进程的迫切需求,而且具有良好的市场前景。在前期报道中,发现了灯盏乙素苷元氨基甲酸酯类衍生物(cn10337956a、cn102603698a)、二苯乙烯或乙烷氨基甲酸酯类化合物(cn102816090a)、异黄酮氨基甲酸酯类化合物(cn102827131a),阿魏酸氨基甲酸酯类化合物(cn105837497a、ca105601540a、cn105646289a)这些化合物虽具有较好的乙酰胆碱酯酶(ache)抑制活性和抗氧化活性,且对aβ聚集有一点的抑制作用,同时对丁酰胆碱酯酶(buche)的抑制活性非常差,导致这些化合物在动物模型中对ad的治疗疗效欠佳。研究表明,buche是与ache密切相关的酶,作为胆碱能神经传递的辅助调节因子可水解乙酰胆碱(ach),随着ad的发展,ache水平逐渐降低,而buche活性度增加到了正常水平的165%,buche抑制剂可使ach水平增加了5倍,进一步动物实验表明,buche的缺失几乎没有健康方面的副作用。因此,设计并发现同时具有乙酰胆碱酯酶和丁酰胆碱酯酶的双靶点抑制剂对ad治疗将极具潜力。
血管性痴呆(vasculardementia,vd)是由缺血性脑血管病、出血性脑血管疾病、急性和慢性缺氧性脑血管疾病等各种类型的脑血管疾病所致的智能及认知功能障碍的临床综合征,其主要临床表现包括:认知能力、记忆力和社会生活能力的减退以及情感、性格的改变,是一种慢性进行性疾病。在中国、日本等亚洲国家血管性痴呆是老年期痴呆的第一位原因;随着世界人口向老龄化的不断推进,脑血管病日益增多,血管性痴呆发病率有逐渐上升的趋势,严重影响老年人的工作和生活质量,并给社会和家庭带来沉重的经济和精神负担。因此,vd已成为当今老年医学与精神医学领域中一个重要的研究热点。血管性痴呆由于发病机制复杂,尚无能够阻断疾病发展的药物,目前临床治疗以改善脑部血液循环和脑代谢,加强脑部营养为主。
近年来,国内外研究表明,在vd患者表现认知功能损伤的同时也经常伴有胆碱能系统的异常。vd患者海马区chat阳性神经元及纤维密度降低,脑内不同部位的chat活性下降,在vd患者脑脊液中的ach浓度明显低于正常水平,并且其浓度降低的程度与痴呆的严重程度呈正相关;而脑缺血可以导致脑内乙酰胆碱酯酶活性上升;同时也发现乙酰胆碱酯酶抑制剂如:huperzinea和revastigmine可以保护缺血造成的神经元损伤,且可以促进脑缺血后神经损伤和脑功能的恢复,这表明乙酰胆碱酯酶抑制剂也可用于血管性痴呆的治疗。
技术实现要素:
为克服上述缺陷,本发明的目的在于提供一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物。
本发明的第二目的的还在于提供一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物的制备方法。
本发明的第三目的还在于提供一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物在制备治疗神经退行性疾病药物中的用途。
本发明的第四目的还在于提供一种治疗神经退行性疾病的药物,包括4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物或者其与酸合成的药学上可接受的盐。
为实现上述目的,本发明采用如下技术方案:
一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物,其化学结构通式为:
其中,r为h、c1~c6烷基、羟基或者c1~c6烷氧基;
c=x为ch2、c=o、c=s或者c-ph;
y为c或者n;
z为h、-f、-cl、-br、-i、c1-4烷基、c1-4烷氧基、三氟甲基、三氟甲氧基、硝基、氰基和苯氧基中任意一种、两种、三种或者四种基团;
r1nr2表示n-甲基-n-乙基、二甲基、二乙胺、二异丙氨、二丁胺、二烯丙氨、吗啉环、哌啶环、4-苄基哌啶环、4-取代苄基哌啶环、4-苯基哌啶环、4-取代苯基哌啶环、苄基哌嗪环、取代苄基哌嗪环、四氢吡咯环或者4-位被c1~c12烷基取代的哌嗪环。
一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物的制备方法,包括以下步骤:
a.以4-羟基肉桂酸或阿魏酸为起始原料,在第一溶剂和缩合剂作用下与取代4-苄基哌啶反应,得到相应的肉桂酰胺类化合物;
b.肉桂酰胺类化合物在第二溶剂和碱条件下,与氨基甲酰氯发生酰化反应,得到产物4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物。
其化学反应通式为:
其中,r、x、y、z的取代与上述化学结构通式中表达一样。
优选地,所述步骤a中的第一溶剂为四氢呋喃、n,n-二甲基甲酰胺、二甲基亚砜、c3-8脂肪酮、苯、甲苯、乙腈、二氯甲烷、氯仿、c1-8醇和c5-8烷烃中一种或几种。
优选地,所述步骤a中的缩合剂为二环己基碳二亚胺、4-二甲氨基吡啶、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐edci和1-羟基苯并三唑hobt中一种或几种。
优选地,所述步骤a中4-羟基肉桂酸或阿魏酸、取代4-苄基哌啶与缩合剂的摩尔比为1:1~5:1~10,反应温度为25~100℃,反应时间为12~48h。
优选地,所述步骤b中的第二溶剂为c3-8脂肪酮、n,n-二甲基甲酰胺、乙醚、异丙醚、甲基叔丁基醚、四氢呋喃、乙二醇二甲醚、c1-6脂肪酸与c1-6脂肪醇所形成酯、二氯甲烷、氯仿、1,2-二氯乙烷、苯、甲苯、二甲苯、氯苯、邻二氯苯、乙腈、二甲基亚砜和吡啶中一种或几种。
优选地,所述步骤b中的碱为碱金属氢氧化物、碱土金属氢氧化物、碱金属或碱土金属碳酸盐、碱金属或碱土金属碳酸氢盐、c1-6脂肪酸碱金属盐、哌啶、四氢吡咯、三乙胺、三丁胺、三辛胺、吡啶、n-甲基吗啉、n-甲基哌啶、三乙烯二胺和四丁基氢氧化铵中一种或几种。
优选地,所述步骤b中肉桂酰胺类化合物、氨基甲酰氯、碱的摩尔比为比1:1~10:1~20,反应温度为25℃~100℃,酰化反应时间为10~24h。
一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物在制备治疗神经退行性疾病药物中的应用。
优选地,所述的神经退行性疾病为阿尔茨海默氏病、血管性痴呆、帕金森症、亨廷顿症、hiv相关痴呆症、多发性硬化症、进行性脊髓侧索硬化症、神经性疼痛或者青光眼。
一种治疗神经退行性疾病药物,包括上述4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物或者由其与酸合成的药学上可接受的盐。
优选地,所述的4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物或者由其与酸合成的药学上可接受的盐的重量百分比10%~99.5%。
优选地,所述的酸为盐酸、氢溴酸、硝酸、硫酸、磷酸、c1-6脂肪羧酸、草酸、苯甲酸、水杨酸、马来酸、富马酸、琥珀酸、酒石酸、柠檬酸、c1-6烷基磺酸、樟脑磺酸、苯磺酸或者对甲苯磺酸。
本发明的积极有益效果:
1.本发明化合物结构上引用氨基甲酸酯基团,基于多靶点原则,对乙酰胆碱酯酶和丁酰胆碱酯酶的ic50分别为0.18μm~17.3μm和0.11μm~7.6μm,在25.0μm浓度下对aβ1-42自身聚集的抑制率在46.7%以上,对乙酰胆碱酯酶、丁酰胆碱酯酶和自身诱导的aβ聚集均具有显著抑制作用,可广泛用于治疗神经退行性疾病的治疗。
2.本发明化合物对alcl3诱导的斑马鱼ad模型的运动功能和反应能力具有显著的改善作用,与模型对照组比较均具有统计学差异;本发明化合物对东莨菪碱致小鼠获得记忆障碍具有剂量依赖性的改善作用,与模型组比较均具有统计学差异。
附图说明
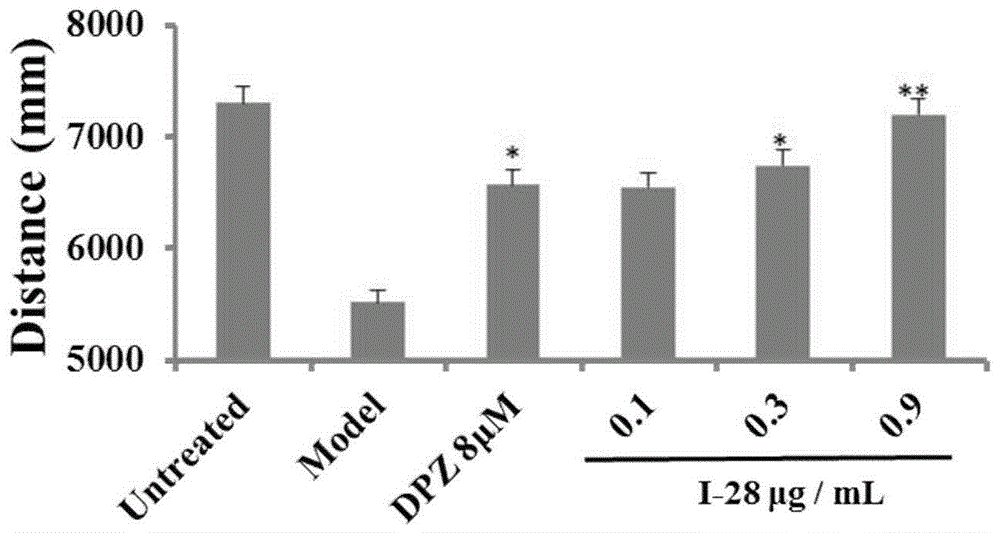
图1为本发明化合物对alcl3诱导斑马鱼ad的运动功能的检测结果图;
图2为本发明化合物对alcl3诱导斑马鱼ad的反应能力的检测结果图;
图3为本发明化合物对东莨菪碱致小鼠获得记忆障碍影响的检测结果图。
具体实施方式
下面结合一些具体实施例对本发明进一步说明。
一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物,其化学结构通式为:
其中,实施例1-29中,r、x、y、z和r1nr2取代基详细见表1。
以化合物1为例,一种4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物(i-1)的制备方法,包括以下步骤:
a.在反应瓶中加入50mmol阿魏酸、100ml干燥thf、75mmoledci、75mmolhobt、50mmol4-苄基哌啶,25℃搅拌反应24h;反应结束后,减压蒸除溶剂,残余物中加入250ml二氯甲烷,依次用饱和碳酸钠水溶液和饱和氯化钠水溶液洗涤,有机层经无水硫酸钠干燥后过滤,减压蒸除溶剂,残余物经柱层析纯化(洗脱液中二氯甲烷:甲醇=30:1v/v),得相应的肉桂酰胺类化合物;
b.将步骤a肉桂酰胺类化合物全部溶于100ml乙腈中,加入75mmol碳酸钾、55mmol氨基甲酰氯,升温至60℃搅拌反应12h;反应结束后,减压蒸除溶剂,残余物中加入200ml二氯甲烷,依次用饱和碳酸钠水溶液和饱和氯化钠水溶液洗涤,有机层经无水硫酸钠干燥后过滤,减压蒸除溶剂,残余物经柱层析纯化(洗脱液中二氯甲烷:甲醇=10:1v/v),得到产物i-1,收率为82.5%,其化学结构均经1h-nmr,13c-nmr和esi-ms确证。
上述实施例2-10的4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物的制备方法与实施例1相似,相同部分不重述,不同之处见表2和表3。
表1本发明实施例1-29的4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物
本发明化合物结构分析数据
4-n-甲基-n-乙基氨基甲酸酯-(4-苄基哌啶)阿魏酰胺(i-1):lightyellowoil,82.5%yield,98.6%hplcpurity.1hnmr7.59(d,j=15.2hz,1h,c=ch),7.28(t,j=7.6hz,2h,2×ar-h),7.20(t,j=7.2hz,1h,1×ar-h),7.14(d,j=7.2hz,2h,2×ar-h),7.08(d,j=7.2hz,2h,2×ar-h),7.04(s,1h,ar-h),6.81(d,j=15.2hz,1h,c=ch),4.69(d,j=11.2hz,1h,1/2phch2),4.07(d,j=11.6hz,1h,1/2phch2),3.85(s,3h,och3),3.48(q,j=6.8hz,1h,1/2nch2),3.39(q,j=6.8hz,1h,1/2nch2),3.08(s,3/2h,1/2nch3),3.03(t,j=9.6hz,1h,1/2nch2),2.61(t,j=9.6hz,1h,1/2nch2),2.98(s,3/2h,1/2nch3),2.56(t,j=6.0hz,2h,nch2),1.83-1.79(m,1h,ch),1.73(d,j=12.6hz,2h,ch2),1.26-1.16(m,5h,ch3+ch2).13cnmr165.3,154.2,151.9,141.8,140.0,133.8,133.7,129.1(2c),128.3(2c),126.1,123.6,120.3,117.5,111.6,56.0,46.2,44.2,43.0(2c),42.7,38.3(2c),32.8,31.8.hr-esi-ms:calcd.forc26h32n2o4[m+h]+:437.2396,found:437.2430。
4-二甲氨基氨基甲酸酯-(4-苄基哌啶)阿魏酰胺(i-2):lightyellowoil,90.3%yield,98.2%hplcpurity.1hnmr7.59(d,j=15.2hz,1h,ch=ch),7.29(t,j=7.6hz,2h,2×ar-h),7.21(d,j=7.2hz,1h,ar-h),7.15-7.12(m,2h,2×ar-h),7.10(s,1h,ar-h),7.07(s,1h,ar-h),7.05(s,1h,ar-h),6.80(d,j=15.2hz,1h,ch=ch),4.71-4.67(m,1h,1/2phch2),4.08-4.05(m,1h,1/2phch2),3.86(s,3h,och3),3.11(s,3h,nch3),3.07-3.05(m,1h,1/2nch2),3.00(s,3h,nch3),2.65-2.61(m,1h,1/2nch2),2.56(t,j=5.6hz,2h,nch2),1.83-1.77(m,1h,ch),1.74(d,j=13.6hz,2h,ch2),1.25-1.19(m,2h,ch2).13nmr165.3,154.5,151.8,141.9,141.7,139.9,133.8,129.1(2c),128.3(2c),126.1,123.6,120.2,117.6,111.6,56.1,46.3,43.0,42.7,38.3,36.8,36.6,32.8,31.8.hr-esi-ms:calcd.forc25h30n2o4[m+h]+:423.2239,found:423.2256。
4-二乙胺基氨基甲酸酯-(4-苄基哌啶)阿魏酰胺(i-5):lightyellowoil,84.7%yield,98.8%hplcpurity.1hnmr7.59(d,j=15.6hz,1h,ch=ch),7.31-7.26(m,2h,2×ar-h),7.22-7.18(m,1h,ar-h),7.14(d,j=7.2hz,2h,2×ar-h),7.10-7.08(m,2h,2×ar-h),7.04(s,1h,ar-h),6.80(d,j=15.6hz,1h,ch=ch),4.70(d,j=7.6hz,1h,1/2phch2),4.08(d,j=10.4hz,1h,1/2phch2),3.85(s,3h,och3),3.46-3.43(m,2h,ch2),3.39-3.36(m,2h,ch2),3.04(t,j=10.0hz,1h,1/2ch2),2.62(t,j=11.8hz,1h,1/2ch2),2.57(t,j=7.2hz,2h,ch2),1.83-1.79(m,1h,ch),1.74(d,j=13.6hz,2h,ch2),1.28-1.24(m,6h,2×ch3),1.21-1.19(m,2h,ch2).13nmr165.3,153.8,151.9,142.0,141.8,140.0,133.7,129.1(2c),128.3(2c),126.1,123.6,120.2,117.4,111.7,56.0,43.0,42.7,42.3(2c),42.1,38.3(2c),29.7,14.0,13.4.hr-esi-ms:calcd.forc27h34n2o4[m+h]+:451.2552,found:451.2591。
4-二苯甲基氨基甲酸酯-(4-苄基哌啶)阿魏酰胺(i-8):lightyellowoil,73.9%yield,98.9%hplcpurity.1hnmr7.57(d,j=15.6hz,1h,ch=ch),7.38-7.30(m,8h,8×ar-h),7.26(t,j=7.2hz,2h,2×ar-h),7.19(t,j=8.4hz,3h,3×ar-h),7.11(d,j=7.2hz,2h,2×ar-h),7.06(s,2h,2×ar-h),7.03(s,1h,ar-h),6.79(d,j=15.6hz,1h,ch=ch),4.67(d,j=10.0hz,1h,1/2phch2),4.03(d,j=9.6hz,1h,1/2phch2),3.86(s,3h,och3),2.98(t,j=7.2hz,1h,1/2ch2),2.57(t,j=7.2hz,1h,1/2ch2),2.52(t,j=7.2hz,2h,ch2),1.77-1.75(m,1h,ch),1.69(d,j=13.6hz,2h,ch2),1.19-1.16(m,2h,ch2).13nmr165.2,152.7,151.7,142.5,141.7,141.4,140.0,134.2,129.2,129.0,128.4,126.9,126.4,126.1,123.3,120.3,117.9,111.7,56.2,46.2,43.0,38.3,32.9,31.9.hr-esi-ms:calcd.forc35h34n2o4[m+h]+:547.2552,found:547.2584。
表2本发明实施例1-10的4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物制备方法参数之一
表3本发明实施例1-10的4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物制备方法参数之二
4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物(i)与酸合成盐制备
在反应瓶中加入按照上述实施例1所得4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物(i)2.0mmol和丙酮50ml,搅拌均匀后加入6.0mmol酒石酸,升温至回流搅拌反应20min,反应结束后冷却至室温,减压蒸除溶剂,残余物用丙酮重结晶,过滤析出的固体,即得4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物(i)的盐,其化学结构经1h-nmr和esi-ms确证。
生物活性测试
1.本发明制备的4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物(i)对乙酰胆碱酯酶和丁酰胆碱酯酶抑制活性
向96孔板中依次加入1.0mmol/l碘化硫代乙酰胆碱或硫代丁酰胆碱(均购自sigma公司)30μl,ph7.4的pbs缓冲液40μl,待测化合物溶液20μl(dmso含量小于1%)和10μl电鳗乙酰胆碱酯酶(eeache)或马血清丁酰胆碱酯酶(eqbuche),加毕混匀后,37℃孵育15min,向各孔中加入质量分数为0.2%的5,5'-二硫代-双(2-硝基)苯甲酸(dtnb,购自sigma公司)溶液30μl显色,用酶标仪测定405nm处各孔的光密度(od值),与不加待测样品的空白孔比较,计算化合物对酶的抑制率[酶抑制率=(1-样品组od值/空白组od值)×100%];选择化合物的五至六个浓度,测定其酶抑制率,并以该化合物摩尔浓度的负对数与酶的抑制率线性回归,求得50%抑制率时的摩尔浓度即为该化合物的ic50,以卡巴拉汀为阳性对照.每个化合物每次测定3个复孔,检测结果见表4。
表4本发明化合物对胆碱酯酶抑制活性和自身诱导aβ1-42聚集抑制活性
测定结果表明,本发明化合物对乙酰胆碱酯酶和丁酰胆碱酯酶的ic50分别为0.18μm~17.3μm和0.11μm~7.6μm,与阳性对照药物rivastigmine检测结果相当或者更好,本发明化合物对乙酰胆碱酯酶和丁酰胆碱酯酶均具有显著抑制作用。
2.本发明制备的4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物(i)对抑制aβ聚集活性测定
取20μl的aβ1-42溶液+20μl的待测化合物溶液(待测化合物溶液为本申请化合物溶液或者阳性对照姜黄素溶液)、20μl的aβ1-42溶液+20μlpbs缓冲液(含2%dmso)、20μlpbs缓冲液(含2%dmso)+20μlpbs缓冲液(含25%dmso)于黑色96孔板中,化合物和aβ1-42的最终浓度均为25μm。37℃孵育24h,然后加入160μl含有5μm硫黄素t的50mm的甘氨酸-naoh缓冲液(ph=8.5),振摇5s后立即用varioskanflashmultimodereader(thermoscientific)多功能酶标仪在446nm激发波长和490nm发射波长下测定荧光值;aβ1-42+待测化合物溶液的荧光值记录为ifi,aβ1-42+pbs缓冲液的荧光值记录为ifc,只含有pbs缓冲液的荧光值记录为if0,由化合物抑制aβ1-42自身聚集的抑制率计算公式为:100-(ifi-if0)/(ifc-if0)*100。每个化合物每个浓度测定两个复孔,检测结果见表4。
测定结果表明,本发明化合物对aβ1-42自身诱导的聚集均具有显著抑制作用,在25.0μm浓度下对aβ1-42自身聚集的抑制率在46.7%以上;而姜黄素在相同浓度下的抑制率为43.1%,说明本发明化合物对aβ1-42自身诱导的聚集均具有显著抑制作用。
3.本发明制备的4-氨基甲酸酯-阿魏酸酰胺-4-苄基哌啶类化合物(i)对alcl3诱导斑马鱼阿尔茨海默症模型的防治作用(以i-28为例说明)。
随机选取3dpf野生型ab系斑马鱼于六孔板中,用三氯化铝(alcl3)诱发斑马鱼阿尔兹海默症模型(以下简称ad斑马鱼),分别水溶给予i-28化合物0.1μg/ml、0.3μg/ml和0.9μg/ml浓度,阳性对照组给药多奈哌齐dpz8μm,同时设置正常对照组和模型对照组,每实验浓度组30尾斑马鱼。给药3天后,用行为分析仪分别观察记录各实验组斑马鱼在60min内3个明暗周期(即:黑暗10min、光照10min交替3个周期)的运动距离和速度差值,分析斑马鱼60min的运动距离和速度差值,以运动距离和速度差值与模型对照组进行统计分析,以统计学意义评价化合物对斑马鱼阿尔兹海默症模型的防治作用,结果见图1和图2。
由图1可知,模型对照组斑马鱼的运动距离(5513mm)与正常对照组(7304mm)比较p<0.01,表明模型建立成功;阳性对照组运动距离(6566mm)与模型对照组比较p<0.05,其运动改善作用为59%,说明dpz对ad斑马鱼的运动功能有改善作用。浓度为0.1μg/ml、0.3μg/ml和0.9μg/ml的i-28运动距离分别为6544、6741和7159mm,与模型对照组比较p>0.05、p<0.05和p<0.01,说明化合物i-28能够显著的改善alcl3诱导斑马鱼ad的运动功能。
由图2可知,模型对照组斑马鱼的速度改变(1.15mm/s)与正常对照组(2.35mm/s)比较p<0.01,表明模型建立成功;阳性对照组速度改变(1.97mm/s)与模型对照组比较p<0.01,其反应能力改善作用为68%,说明dpz对ad斑马鱼的反应能力有改善作用。浓度为0.1μg/ml、0.3μg/ml和0.9μg/ml的i-28速度改变分别为1.80、2.14和2.28mm/s,与模型对照组比较p>0.05、p<0.05和p<0.01,说明化合物i-28能够显著的改善alcl3诱导斑马鱼ad的反应能力。
4.本发明制备的4-氨基甲酸酯-肉桂酰胺-4-苄基哌啶类化合物(i)对东莨菪碱所致小鼠记忆获得障碍的影响(以i-28为例说明)。
spf级icr雄性小鼠,25-30g,随机分为:正常组、模型组、阳性对照组、受试药高、中、低剂量组,每组10只动物。一次性灌胃给予受试药物,正常组和模型组给予溶媒0.5%cmc-na,给药体积均为0.1ml/10g,阳性对照组灌胃rivastigmine6.0mg/kg,受试药高、中、低剂量组分别灌喂本发明化合物20.0、10.0、5.0mg/kg;药后45min,正常组小鼠腹腔注射生理盐水,其余各组动物均注射东莨菪碱5mg/kg;造模30min后,将小鼠放入非电刺激y迷宫进行行为学测试。测试时将小鼠放于一臂末端,让其在迷宫内自由穿行8min,记录其进入各臂的次数和交替次数,按照以下公式计算交替率:交替率%=[交替次数/(总进入次数-2)]×100,结果以均数±标准差表示,组间差异采用单因素方差分析,结果见图3。
测定结果表明,正常组的交替率为65.3%,模型组的交替率为40.8%,与模型组相比,阳性对照组(rivastigmine)的交替率为60.2%,说明该模型运行成功。在该实验条件下,本发明所公开的化合物(i-28)对东莨菪碱致小鼠获得记忆障碍具有剂量依赖性的改善作用,其中中剂量组(10.0mg/kg)显示了最高的交替率62.2%(p<0.01),与阳性对照组比较没有统计学差异。说明所公开化合物i-28能够显著的改善东莨菪碱致小鼠获得记忆障碍。
最后说明的是,以上实施例仅用以说明本发明的技术方案而非限制,本领域普通技术人员对本发明的技术方案所做的其他修改或者等同替换,只要不脱离本发明技术方案的精神和范围,均应涵盖在本发明的权利要求范围当中。
- 还没有人留言评论。精彩留言会获得点赞!
- N-取代-3,5-二(2-(三氟甲基)亚苄基)哌啶-4-酮衍生物及其制备方法与应用
- 一种n-(4-氟苄基)-n-(1-甲基哌啶-4-基)-n’-(4-异丁氧基苄基)脲的酒石酸盐的合成方法
- N-(4-氟苄基)-n-(1-甲基哌啶-4-基)-n’-(4-(2-甲基丙氧基)-苯基甲基)脲半酒石酸盐 ...的制作方法
- N-(1-苄基哌啶-4-氨基)-2-(4-苯甲酰苯氧基)乙酰胺的新用图
- 一种苄基哌啶衍生物的制备方法
- 一种手性2-取代基-4-哌啶酮-1-羧酸叔丁酯的合成方法
- N-烃基取代-3-哌啶酮的合成方法
- (2s
- 含哌啶基吡喃酮化合物在制备抗真菌感染药物中的应用的制作方法
- 可连续回收丙酮的哌啶酮连续精制生产方法及装置的制作方法
- 一种光稳定剂中间体2,2,6,6-四甲基-4-哌啶酯类化合物及其制备方法
- 一种2-芳基氟代哌啶衍生物及其制备方法
- N-(4-氟苄基)-n-(1-甲基哌啶-4-基)-n’-(4-(2-甲基丙氧基)苯基甲基)脲酒石酸盐晶型 ...的制作方法
- 3,5-双(芳基亚甲基)-1-取代-4-哌啶酮系列化合物及其在制备抗食管癌药物的应用
- 哌啶脲衍生物的制作方法
- 一种(s)-(+)-1-(2-哌啶苯基)-3-甲基正丁胺的制备方法
- 一种哌啶化合物及其制备方法
- 用作gpr120激动剂的取代的螺哌啶基化合物的制作方法
- 一类膦功能化聚醚哌啶盐离子液体及其在烯烃氢甲酰化反应中的应用
- 一种合成1-(N-Boc-4-哌啶)-4-吡唑硼酸频哪醇酯的方法
- 一种光稳定剂中间体2,2,6,6-四甲基-4-哌啶酯类化合物及其制备方法
- 一种2-芳基氟代哌啶衍生物及其制备方法
- N-(4-氟苄基)-n-(1-甲基哌啶-4-基)-n’-(4-(2-甲基丙氧基)苯基甲基)脲酒石酸盐晶型 ...的制作方法
- 3,5-双(芳基亚甲基)-1-取代-4-哌啶酮系列化合物及其在制备抗食管癌药物的应用
- 哌啶脲衍生物的制作方法
- 一种(s)-(+)-1-(2-哌啶苯基)-3-甲基正丁胺的制备方法
- 一种哌啶化合物及其制备方法
- 用作gpr120激动剂的取代的螺哌啶基化合物的制作方法
- 一类膦功能化聚醚哌啶盐离子液体及其在烯烃氢甲酰化反应中的应用
- 一种合成1-(N-Boc-4-哌啶)-4-吡唑硼酸频哪醇酯的方法