活性物质、非水电解质电池、组电池、电池包、汽车及车辆的制作方法
本发明的实施方式涉及电池用活性物质、非水电解质电池、组电池、电池包、汽车及车辆。
背景技术:
近年来,随着电子领域中的技术的快速发展,在进行电子设备的小型化及轻量化。其结果是,进行电子设备的便携化及无线化,对于成为其驱动源的二次电源也渴望小型化、轻量化及高能量密度化。为了应对这样的要求,在开发可显示出高的能量密度的锂二次电池。最近,还在进行外包装材料使用了铝层压薄膜的超薄型-轻量二次电池的开发及商品化。
采用了这样的铝层压外包装材料的二次电池因伴随着充放电的电极的体积膨胀及收缩而使电池厚度变化。因该原因而出现电池变形、或电极间距扩大、电池电阻增大、电池特性下降的问题。
作为能够回避这样的问题的材料系,提出了使用钛酸锂作为负极活性物质的电池。钛酸锂几乎没有伴随着充放电的体积变化,其结果是,电池厚度的变化非常小。通过将该化合物用作负极活性物质,解决了上述问题。
钛酸锂因大约在1.55V(相对于Li/Li+)进行锂的嵌入脱嵌反应,因此在正极例如使用LiMn2O4的电池中,该电池电压大约为2.5V。此电压低于广泛商用化的锂离子二次电池即具备碳负极及LiMn2O4正极的电池的电池电压即3.9V。即,在由含有钛酸锂的非水电解质电池构成可显示出与由碳负极/LiMn2O4正极的电池构成的组电池或电池包相同的电压的组电池或电池包时,与使用含有碳负极的电池时相比,需要增加串联连接数量(电池个数)。
技术实现要素:
发明要解决的问题
本发明的目的是,提供能够实现可显示出优异的输入输出特性、优异的寿命特性及高电压的非水电解质电池的电池用活性物质、能够显示出优异的输入输出特性及高电压的非水电解质电池、具备该非水电解质电池的组电池、具备前面的非水电解质电池的电池包及具备该电池包的汽车。
用于解决问题的手段
根据第1实施方式,提供一种电池用活性物质。该活性物质含有用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的含钛氧化物。通式中,下标w、x、y及z分别在0≤w≤6、0<x<2、0≤y≤3、0≤z≤3的范围内。M1为选自Sr、Ba及Pb中的至少1种金属元素。M2为选自金属元素M(除去Ti及M1)和P中的至少1种元素。
根据第2实施方式,提供一种非水电解质电池。该非水电解质电池具备正极、负极和非水电解质。负极含有第1实施方式涉及的电池用活性物质。
根据第3实施方式,提供一种组电池。该组电池具备多个第2实施方式涉及的非水电解质电池。多个非水电解质电池彼此串联及/或并联地连接。
根据第4实施方式,提供一种电池包。该电池包具备第2实施方式涉及的非水电解质电池。
根据第5实施方式,提供一种具备第4实施方式涉及的电池包的汽车。该电池包配置在汽车的发动机舱内。
根据第6实施方式,提供一种车辆。该车辆具备第4实施方式涉及的电池包。
根据1个实施方式,能够提供一种电池用活性物质,其能够实现可显示出优异的输入输出特性、优异的寿命特性及高电压的非水电解质电池。
附图说明
图1是3种含钛氧化物的充电曲线。
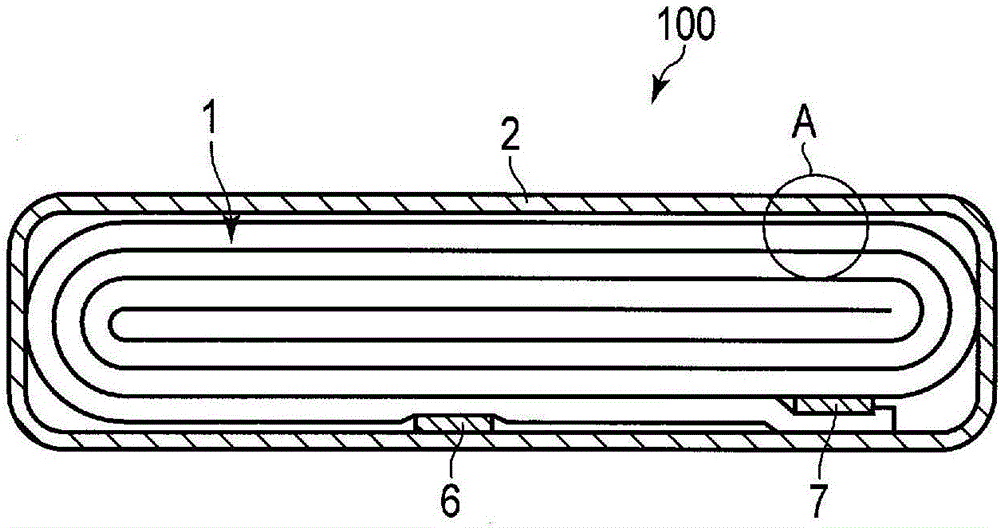
图2是表示第2实施方式涉及的非水电解质电池的一个例子的概略剖视图。
图3是图2的非水电解质电池的A部的放大剖视图。
图4是表示第3实施方式涉及的组电池的一个例子的概略立体图。
图5是表示第4实施方式涉及的电池包的一个例子的分解立体图。
图6是表示图5的电池包的电路的方框图。
图7是表示第5实施方式涉及的汽车的一个例子的概略剖视图。
具体实施方式
以下,参照附图对实施方式进行说明。再者,贯通实施方式对于通用的构成标记同一符号,并将重复的说明省略。此外,各图是用于促进实施方式的说明和其理解的示意图,其形状及尺寸、比例等有与实际装置不同的地方,但这些可参酌以下的说明和公知的技术适宜地进行设计变更。
(第1实施方式)
根据第1实施方式,提供一种电池用活性物质。该活性物质含有用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的含钛氧化物。通式中,下标w、x、y及z分别在0≤w≤6、0<x<2、0≤y≤3、0≤z≤3的范围内。M1为选自Sr、Ba及Pb中的至少1种金属元素。M2为选自金属元素M(除去Ti及M1)和P中的至少1种元素。M1可以是选自Sr、Ba及Pb中的1种金属元素,或者也可以是选自Sr、Ba及Pb中的2种以上的金属元素。M2可以是选自金属元素M(除去Ti及M1)和P中的1种元素,或者也可以是选自金属元素M(除去Ti及M1)和P中的2种以上的元素。
第1实施方式涉及的电池用活性物质能够在比钛酸锂低的电位下进行锂的嵌入脱嵌反应。此外,第1实施方式涉及的电池用活性物质能够在与钛酸锂同等的大范围的SOC(State of charge,充电状态)内显示出平稳的电位变化。另外,第1实施方式涉及的电池用活性物质能够实现优异的寿命性能。其结果是,第1实施方式涉及的电池用活性物质能够实现可显示出优异的输入输出特性及高电压的非水电解质电池。以下对这些理由进行说明。
图1中示出3种含钛氧化物的充电曲线。图1所示的充电曲线将锂脱嵌的方向作为充电方向。图1中示出充电曲线的含钛氧化物为含钛氧化物Li2NaSr0.5Ti6O14(A)、含钛氧化物Li2Na2Ti6O14(B)及含钛氧化物Li2SrTi6O14(C)。含钛氧化物(A)为可用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14(0<x<2,M1为选自Sr、Ba及Pb中的至少1种金属元素)表示的氧化物。另一方面,含钛氧化物(B)及(C)为不能用x在0<x<2的范围内的通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的氧化物。
如图1所示的那样,含钛氧化物Li2SrTi6O14(C)示出多段的充电曲线。含钛氧化物Li2SrTi6O14(C)的放电曲线也为多段。因此,含钛氧化物Li2SrTi6O14(C)难在大范围的SOC内得到稳定的输出。另一方面,含钛氧化物Li2Na2Ti6O14(B)如图1所示的那样,充电曲线不是多段,在大范围的SOC内电位连续平稳地变化。含钛氧化物Li2Na2Ti6O14(B)的放电曲线也同样在大范围的SOC内电位连续平稳地变化。因此,含钛氧化物Li2Na2Ti6O14(B)可在大范围的SOC内得到稳定的输出。但是,从图1弄清楚,含钛氧化物Li2Na2Ti6O14(B)与含钛氧化物Li2SrTi6O14(C)的容量相比容量较低。
与此相对,含钛氧化物Li2NaSr0.5Ti6O14(A)如图1所示的那样,与含钛氧化物Li2Na2Ti6O14(B)同样,能够在大范围的SOC内示出电位连续平稳变化的充电曲线。即使在含钛氧化物Li2NaSr0.5Ti6O14(A)的放电曲线中,电位也同样能够在大范围的SOC内连续平稳地变化。此外,含钛氧化物Li2NaSr0.5Ti6O14(A)如图1所示的那样,能够显示出接近含钛氧化物Li2SrTi6O14(C)的容量的容量。因而,含钛氧化物Li2NaSr0.5Ti6O14(A)能够在大范围的SOC内以高容量显示出稳定的输入及输出。
另外,尽管图1中未示出,但含钛氧化物Li2NaSr0.5Ti6O14(A)能够显示出比含钛氧化物Li2Na2Ti6O14(B)及含钛氧化物Li2SrTi6O14(C)更优异的循环寿命。此点在本说明书的实施例中得到实证。
而且,含钛氧化物Li2NaSr0.5Ti6O14(A)如图1所示的那样,能够在比1.5V(相对于Li/Li+)低的电位下进行锂的嵌入反应。尽管图1中未示出,但含钛氧化物Li2NaSr0.5Ti6O14(A)也能在比1.5V(相对于Li/Li+)低的电位下进行锂的脱嵌反应。也就是说,含钛氧化物Li2NaSr0.5Ti6O14(A)能够在比钛酸锂低的电位下进行锂的嵌入脱嵌反应。
多亏于此,含钛氧化物Li2NaSr0.5Ti6O14(A)能够实现可显示出优异的输入输出特性及高电压的非水电解质电池。
在通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14中,下标w根据用该通式表示的含钛氧化物的充放电状态,在0≤w≤6的范围内变化。
此外,下标x表示在用通式Li(2+w)Na2Ti(6-y)M2zO14表示的含钛复合氧化物中的Na的位点中,被选自Sr、Ba及Pb中的至少1种金属元素即M1置换的部分的比例。
另外,下标y表示在用通式Li(2+w)Na(2-x)M1(x/2)Ti6O14表示的含钛复合氧化物中的Ti的位点中,被选自金属元素M(除去Ti及金属元素M1)和P中的至少1种元素即M2置换的部分的比例。下标z表示用上述通式表示的1mol的含钛复合氧化物含有的元素M2的物质量。这里,M2由于也可以含有与Ti的价数不同的元素,所以下标y和下标z也可以彼此不同。或者,在元素M2为与Ti相同的价数的元素时,下标y及z的值可彼此相同。再者,下标y及z的值以及元素M2能以用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的含钛氧化物达到电中性的方式组合地进行选择。
下标w在0≤w≤6的范围内、下标x在0<x<2的范围内、下标y在0≤y≤3的范围内、下标z在0≤z≤3的范围内、M1为选自Sr、Ba及Pb中的至少1种金属元素、M2为选自金属元素M(除去Ti及金属元素M1)和P中的至少1种元素的用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)O14表示的含钛氧化物与图1中示出充电曲线的含钛氧化物Li2NaSr0.5Ti6O14(A)同样,能够在大范围的SOC内以高容量示出稳定的高输入及高输出,能够显示出优异的循环寿命,能够在比钛酸锂低的电位下进行锂的嵌入脱嵌反应。此点在本说明书的实施例中得到实证。
基于以上理由,含有用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的含钛氧化物的第1实施方式涉及的电池用活性物质能够实现可显示出优异的输入输出特性、优异的寿命特性及高电压的非水电解质电池。
金属元素M1从能量密度的观点出发,优选为Sr或Ba中的至少1种金属元素,更优选为Sr。金属元素M1为2价的金属,因而能够将用通式Li(2+w)Na2Ti(6-y)M2zO14表示的含钛复合氧化物中的Na在xmol方面置换为x/2mol的金属元素M1。下标x优选在0.1≤x≤1.9的范围内。如果下标x在此范围,则能够兼顾更高的容量及更优异的寿命特性。更优选的下标x的范围为0.25≤x≤1.8。
通过用元素M2置换用通式Li(2+w)Na(2-x)M1(x/2)Ti6O14表示的含钛氧化物中的Ti的位点的一部分,即,使下标y及z大于0,能够大幅度提高含钛氧化物的电子传导性,能够兼顾更优异的大电流特性和更优异的寿命特性。但是,如果下标y及z的值超过3,则有生成阻碍寿命特性的异相的顾虑。下标y及z优选分别为0.01以上,更优选在0.01≤y≤1及0.01≤z≤1的范围内。如果下标y及z大于0,则能够实现更高的输出性能。优选M2为选自Zr、V、Nb、Ta、Mo、W及P中的至少1种元素。元素M2更优选为V及Nb中的至少1种元素。
在第1实施方式涉及的电池用活性物质中,含钛氧化物例如能够采用粒子的形态。处于粒子形态的含钛氧化物例如可以是一次粒子(单粒子),也可以是一次粒子凝聚而成的二次粒子。在含钛氧化物的粒子为二次粒子时,从寿命性能的观点出发,二次粒子的压缩断裂强度优选为10MPa以上。
在第1实施方式涉及的电池用活性物质含有含钛氧化物的二次粒子时,其平均二次粒径优选为1μm以上且100μm以下。如果二次粒子的平均粒径在此范围内,则工业生产上容易处理,此外,在用于制作电极的涂膜中,能够使质量及厚度均匀,而且能够防止电极的表面平滑性的下降。二次粒子的平均粒径更优选为3μm以上且30μm以下。
电池用活性物质含有二次粒子,例如可通过扫描式电子显微镜(SEM)观察来确认。
含在二次粒子中的一次粒子优选平均一次粒径为1nm以上且10μm以下。如果平均一次粒径在此范围内,则工业生产上容易处理,此外,能够促进含钛氧化物的固体内的锂离子的扩散。平均一次粒径更优选为10nm以上且1μm以下。
优选一次粒子为各向同性状。在本说明书中所谓各向同性状的一次粒子,指的是纵横尺寸比为3以下的粒子。一次粒子为各向同性状粒子,可通过扫描式电子显微镜(SEM)观察来确认。
二次粒子优选用BET法测定的比表面积为5m2/g以上且50m2/g以下。在比表面积为5m2/g以上时,可充分确保锂离子的嵌入及脱嵌位点。在比表面积为50m2/g以下时,工业生产上容易处理。
第1实施方式涉及的电池用活性物质还能包含含钛氧化物的粒子和形成于该粒子表面的至少一部分上且含有碳或氮中的至少一种元素的表层。
含有碳元素的表层能够显示锂离子透过性,同时能够显示比含钛氧化物优异的导电性。因此,含有碳元素的表层能够具有提高含钛氧化物的粒子的电子传导性的效果。此外,含有碳元素的表层还能够具有抑制与诱发电池电阻上升的电解液的副反应的效果。电池用活性物质中的碳元素的含量相对于电池用活性物质的质量优选在0.01质量%以上且10质量%以下的范围内。如果在此范围内,则可得到充分确保容量、同时提高电子传导的效果。更优选碳元素的含量相对于活性物质材料的质量为0.01质量%以上且3质量%以下。进一步优选碳元素的含量相对于活性物质材料的质量为1质量%以上且3质量%以下。电池用活性物质中的碳元素的含量例如可通过高频加热-红外线吸收法来定量。此外,通过采用TEM-EDX等取得活性物质截面的碳分布图(mapping),能够得知碳元素的存在区域。
含有氮元素的表层能够显示锂离子透过性,同时能够显示比含钛氧化物优异的导电性。因此,含有氮元素的表层能够具有提高含钛氧化物的粒子的电子传导性的效果。电池用活性物质中的氮元素的含量相对于活性物质材料的质量优选在0.01质量%以上且3质量%以下的范围内。如果在此范围内,则可得到充分确保容量、同时提高电子传导的效果。关于电池用活性物质中的氮元素的含量,例如可通过将其溶解于不活泼气体中,用热传导率检测器(例如LECO公司制造的ONH836)来测定。此外,通过采用TEM-EDX等来取得活性物质截面的氮分布图,能够得知氮元素的存在区域。
第1实施方式涉及的电池用活性物质除上述元素以外,还能以1000质量ppm以下的量含有制造上不可避免的杂质。
电池用活性物质中的各元素的含量可用ICP发光分光法进行测定。
第1实施方式涉及的电池用活性物质例如可按以下制造。
首先,作为Li源,准备氢氧化锂、氧化锂、碳酸锂等锂盐。此外,作为Na源,准备氢氧化钠、氧化钠、碳酸钠等钠盐。按规定量将它们溶解于纯水中,调制起始溶液。在该溶液中,以锂、钠、钛、M1及M2的原子比达到规定比率的方式,投入氧化钛、金属元素M1的氧化物和任意的元素M2的氧化物,调制混合溶液。例如,在合成组成式Li2NaSr0.5Ti6O14的含钛氧化物时,以混合溶液中的锂∶钠∶锶∶钛的原子比达到2∶1∶0.5∶6的方式混合起始原料。
接着,一边搅拌得到的混合溶液一边使其干燥,得到烧成前体。作为干燥方法,可列举喷雾干燥、造粒干燥、冷冻干燥或它们的组合。接着,对得到的烧成前体进行烧成,得到含钛氧化物。烧成可在大气中进行,或者,也可以在氧气氛、采用氩等的不活泼气氛中进行。
在上述工序中,也可以不将Li源及Na源溶于纯水中而只混合粉末,但为了更均匀地混合原料,抑制杂质相的生成,优选经由上述工序。
烧成前体(混合的原料)的烧成只要在680℃以上且1200℃以下进行30分钟以上且24小时以下即可。优选在720℃以上且1100℃以下将烧成进行1小时以上且10小时以下。
如果烧成温度低于680℃,则氧化钛和锂化合物的反应不充分,锐钛矿型TiO2、金红石型TiO2、Li2TiO3等杂质相增大,电容量减小。如果烧成温度超过1200℃,则通过烧结的进展微晶粒径过剩地生长,使大电流性能降低。
还可在以下说明的条件下对通过上述烧成而得到的含钛氧化物进行粉碎及再烧成。
作为粉碎方法,例如可采用乳钵、球磨机、砂磨机、振动球磨机、行星球磨机、喷射磨机、反转喷射磨机、旋转气流式喷射磨机或筛子等。粉碎时也能够采用使水、乙醇、乙二醇、苯或己烷等公知的液体粉碎助剂共存的湿式粉碎。粉碎助剂对于改善粉碎效率及增加微粉生成量是有效果的。更优选的方法是使用氧化锆制球作为介质的球磨机,优选加入液体粉碎助剂的湿式粉碎。另外,作为粉碎助剂也可以添加可提高粉碎效率的多元醇等有机物。多元醇的种类没有特别的限定,可单独或组合地使用季戊四醇、三羟乙基乙烷、三羟甲基丙烷等。
再烧成也可在大气中进行,或者也可以在氧气氛、采用氩等的不活泼气氛中进行。再烧成只要在250℃以上且900℃以下进行1分钟以上且10小时以下即可。如果为900℃以上,则粉碎的粉末的烧成进展,即使是短时间的热处理也压坏细孔。如果低于250℃则不能将湿式粉碎时附着的杂质(有机物)除去,使电池性能下降。优选在400℃以上且700℃以下将再烧成进行10分钟以上且3小时以下。
此外,含钛氧化物的pH值优选在10.0~11.2的范围内。其理由如下。在含钛氧化物的烧成过程中,碳酸锂、碳酸钠、氢氧化锂及氢氧化钠等碱性化合物是起因于未进入含钛氧化物中的未反应的Li成分及/或Na成分而副生成的。在起因于未反应的Li成分及/或Na成分的这些碱性化合物残存在含钛氧化物粒子的表面时,这些碱性化合物被电化学还原,或与非水电解质反应,而产生二氧化碳或烃气体。另外,通过这些副反应,可在活性物质表面形成成为电阻成分的有机皮膜。在含钛氧化物粒子的pH值小于11.2时,含钛氧化物粒子的表面中的上述碱性化合物的量非常小。通过采用含有这样的含钛氧化物粒子的电池用活性物质,能够提高电池性能,特别是提高高温循环性能及输出性能。
但是,在按上述的条件机械地粉碎含钛氧化物时,有未反应的Li成分及Na成分变得在表面露出,pH值大于11.2,电池性能下降的倾向。所以,优选在粉碎工序后进行再烧成工序。通过进行再烧成,表面显露的未反应Li成分及Na成分进入到活性物质内部,能够减少表面残存的未反应的Li成分及Na成分。即,通过实施粉碎后的再烧成工序,可将pH值控制在11.2以下。
在将成为含钛氧化物的原料的氢氧化锂及氢氧化锂等Li源、碳酸钠及碳酸钠等Na源与钛氧化物(例如锐钛矿型TiO2、金红石型TiO2)进行反应的阶段,通过降低Li源及Na源的比率,可减少副生成的碳酸锂及碳酸钠等剩余Li成分及Na成分。但是,如果降低Li源及Na源的比率,则得到的活性物质中的锂及钠的比率下降,其结果是,含钛氧化物的电容量降低。因此,为了使电容量保持在高容量,优选在不使Li源及Na源减量的情况下,使得到的活性物质的pH值在10以上。
此外,考虑到维持电容量和降低副反应,更优选pH值在10.3~11.1的范围。
再者,含钛氧化物的pH值可按以下步骤进行测定。即,将含钛氧化物1g分散在50mL的纯水(25℃)中,在搅拌大约10分钟后,过滤活性物质,得到滤液。将该滤液的pH值作为含钛氧化物的pH值。pH值的测定方法及测定装置遵循JIS标准(JIS Z8802、JIS Z8805)。
[电池用活性物质的分析方法]
接着,对有关电池用活性物质的利用ICP发光分光法的元素含量的测定方法、碳量的测定方法、氮量的测定方法、二次粒子的平均粒径的测定方法、一次粒子的平均粒径的确认方法及比表面积的测定方法进行说明。
再者,电池用活性物质在装入电池中时,例如可按以下方式取出。首先,使电池形成放电状态。例如,通过将电池在25℃环境下以0.1C电流放电到额定终止电压,可将电池形成放电状态。接着,将放电状态的电池解体,取出电极(例如负极)。例如用碳酸甲乙酯清洗取出的电极。将洗净的电极放入水中,在水中使电极层失活。通过采用离心分离装置等,可从失活的电极中提取电池用活性物质。
提取的电池用活性物质有时依然含有粘结剂及导电剂。例如,在提取的电池用活性物质中作为粘结剂含有聚偏氟乙烯的情况下,在通过用N-甲基-2-吡咯烷酮等清洗将粘结剂成分除去后,可用具有适当的网眼尺寸的筛孔将导电剂除去。在这些成分微量残存时,通过大气中的加热处理(例如在250℃加热处理30分钟等)就可将其除去。
(利用ICP发光分光法的元素含量的测定方法)
利用ICP发光分光法的元素含量的测定例如可按以下方法进行。在容器中称取按前面的步骤提取的电池用活性物质,通过酸溶解或碱溶解得到测定溶液。通过用测定装置(例如SII-Nanotechnology公司制造的SPS-1500V)对该测定溶液进行ICP发光分光,可测定电池用活性物质中的元素的含量。
利用这样的发光分析装置,能够测定活性物质中的添加元素的含量。另一方面,在电极中还含有其它活性物质时,元素的含量可按以下进行测定。将从电极中提取的负极活性物质供给TEM-EDX,通过限制视野的衍射法鉴定各个粒子的晶体结构。选定具有归属于通式Li(2+w)Na2Ti6O14的衍射图案的粒子,通过对选定的粒子进行EDX分析,可测定各元素的含量。再者,在用上述通式表示的化合物的粒子的衍射图案中,依赖于通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14中的下标x、y及z的值以及金属元素M1及元素M2,有时峰的位置从归属于Li(2+w)Na2Ti6O14的衍射图案稍微偏离。但是,用上述通式表示的化合物的粒子能够作为与归属于通式Li(2+w)Na2Ti6O14的衍射图案同样的图案进行相鉴别。
(碳量的测定方法)
活性物质中的碳元素的含量例如可按前面说明的那样从由电极提取的电池用活性物质中将导电剂除去,将如此得到的电池用活性物质在150℃干燥12小时,在称取到容器中后,可用测定装置(例如LECO公司制CS-444LS)进行测定。
在电极中含有其它活性物质时,可按以下进行测定。将从电极中取出的活性物质供给TEM-EDX,用限制视野的衍射法鉴定各个粒子的晶体结构。选定具有归属于含钛氧化物的衍射图案的粒子,对选定的粒子测定碳含量。此外,此时,如果通过EDX取得碳分布图,则能够得知碳元素的存在区域。
(氮量的测定方法)
活性物质中的氮元素的含量例如可将从电极中提取的电池用活性物质在不活泼气体中溶解,用热传导率检测器(例如,LECO公司制造的ONH836)进行测定。
在电极中含有其它活性物质时,可按以下进行测定。将从电极中取出的活性物质供给TEM-EDX,用限制视野的衍射法鉴定各个粒子的晶体结构。选定具有归属于钛复合氧化物的衍射图案的粒子,对选定的粒子测定氮含量。此外,此时如果用EDX取得氮分布图,能够得知氮元素的存在区域。
(二次粒子的平均粒径的测定方法)
二次粒子的平均粒径的测定方法如下。作为测定装置,采用激光衍射式分布测定装置(岛津SALD-300)。首先,在烧杯中添加大约0.1g的试样、表面活性剂和1~2mL的蒸馏水,充分搅拌注入到搅拌水槽中,在此调制试样溶液。采用该试样溶液,以2秒为间隔测定64次光度分布,解析粒度分布数据。
(一次粒子的平均粒径的确认方法)
平均一次粒径可通过扫描式电子显微镜(SEM)观察来确认。求出从典型的视野提取的典型的10个粒子的平均值,确定平均一次粒径。
(比表面积的测定方法)
比表面积的测定可采用在液体氮的温度下使吸附占有面积已知的分子吸附在粉体粒子表面上,从其量求出试样的比表面积的方法。经常利用的方法是采用不活泼气体的低温低湿物理吸附的BET法。BET法是将单分子层吸附理论即Langmuir理论扩张到多分子层吸附的、作为比表面积的计算方法最有名的理论。将用BET法求出的比表面积称为BET比表面积。
接着,对活性物质的晶体结构的确认方法进行说明。
活性物质的晶体结构可通过广角X射线衍射(XRD)来确认。
活性物质的广角X射线衍射测定按以下进行。首先,将对象试样粉碎到平均粒径达到5μm左右。平均粒径可按前面说明的那样,例如利用激光衍射法等来求出。将粉碎的试样填充在形成于玻璃试样板上的深0.2mm的托盘部分中。此时,注意要将试样充分填充在托盘部分中。此外,注意不要因试样的填充不足而发生裂纹、空隙等。接着,从外部充分压紧另一玻璃板,使填充的试样平滑化。注意不要因填充量过于不足而由托盘的基准面产生凹凸。接着,将填充了试样的玻璃板设置在广角X射线衍射装置中,采用Cu-Kα射线取得衍射图案。
再者,在试样的取向性高时,因试样的填充方法而有峰位置偏移或强度比变化的可能性。将那样的试样形成颗粒形状进行测定。颗粒例如最好为直径10mm、厚度2mm的压粉体。这样的压粉体可通过对试样施加15分钟的大约250MPa的压力来制作。将得到的颗粒设置在X射线衍射装置中,测定其表面。通过采用这样的方法进行测定,能够排除由操作者带来的测定结果的差异,提高再现性。
在对含在电极中的活性物质进行广角X射线衍射测定时,例如可按以下进行。
首先,为了把握活性物质的结晶状态,形成锂离子从活性物质完全脱嵌的状态。例如在作为负极使用时,按前面说明的步骤,使电池形成完全放电状态。但是,即使在放电状态也有时存在残留的锂离子。接着,在填充了氩的手套箱中将电池分解,用适当的溶剂进行清洗。例如最好使用碳酸甲乙酯等。可以将洗净的电极切成与广角X射线衍射装置的托盘的面积同等程度,直接粘贴在玻璃托盘上进行测定。此时,根据电极集电体的金属箔的种类预先测定好XRD,把握在哪个位置出现源自集电体的峰。此外,还预先把握好有无导电剂及粘结剂等合剂的峰。在集电体的峰和活性物质的峰重叠时,优选将活性物质从集电体剥离进行测定。这是为了在定量地测定峰强度时将重叠的峰分离。当然,如果事前能把握好这些,也能够将此操作省略。可以物理地剥离电极,但如果在溶剂中施加超声波则容易剥离。通过测定如此回收的电极,能够进行活性物质的广角X射线衍射测定。
用特沃尔德法(Rietveld method)对如此得到的广角X射线衍射的结果进行解析。在特沃尔德法中,将从预先推定的晶体结构模型计算的衍射图案与实测值进行全拟合,能够使有关晶体结构的参数(晶格常数、原子坐标、占有率等)精密化,能够调查测定对象活性物质的晶体结构的特征及添加元素的存在位置(位点)。
以上说明的第1实施方式涉及的电池用活性物质在非水电解质电池的负极或正极中都能使用。此外,无论用于负极或正极中都无变化,能够在大范围的SOC内以高容量显示出稳定的输出及输入,能够显示出高电压,能够实现循环特性优异的非水电解质电池。
在将第1实施方式涉及的电池用活性物质用于正极时,作为对电极的负极的活性物质例如可使用金属锂、锂合金或石墨、焦炭等碳系材料。
在负极中使用第1实施方式涉及的电池用活性物质作为负极活性物质时,可以单独使用,也可以与其它活性物质一同使用。所谓那样的其它活性物质,例如为具有尖晶石型晶体结构的锂钛复合氧化物(Li4Ti5O12等)、具有锐钛矿型、金红石型或单斜晶系β型晶体结构的钛复合氧化物(a-TiO2、r-TiO2、TiO2(B)等)及铁复合硫化物(FeS、FeS2等)。
同样,在正极中使用第1实施方式涉及的电极用活性物质作为正极活性物质时,可以单独使用,也可以与其它活性物质一同使用。所谓那样的其它活性物质,例如为具有尖晶石型晶体结构的锂钛复合氧化物(Li4Ti5O12等)、具有锐钛矿型、金红石型或单斜晶系β型晶体结构的钛复合氧化物(a-TiO2、r-TiO2、TiO2(B)等)及铁复合硫化物(FeS、FeS2等)。
根据以上说明的第1实施方式,可提供一种电池用活性物质。该活性物质含有用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的含钛氧化物。M1为选自Sr、Ba及Pb中的至少1种金属元素。M2为选自金属元素M(除去Ti及金属元素M1)和P中的至少1种元素。该电池用活性物质能够在大范围的SOC内以高容量显示出稳定的输入及输出,能够在比钛酸锂低的电位下进行锂的嵌入脱嵌反应。多亏于此,第1实施方式涉及的电池用活性物质能够实现可显示出优异的输入输出特性、优异的寿命特性及高电压的非水电解质电池。
(第2实施方式)
根据第2实施方式,可提供一种非水电解质电池。该非水电解质电池具备正极、负极和非水电解质。负极含有第1实施方式涉及的电池用活性物质。
第2实施方式涉及的非水电解质电池还能进一步具备配置在正极与负极之间的隔膜。正极、负极及隔膜可构成电极组。非水电解质保持在电极组中。
电极组例如可具有层叠型的结构。在层叠型的电极组中,中间夹着隔膜地交替层叠多个正极和多个负极。
或者,电极组还可具有卷绕型的结构。卷绕型的电极组可通过卷绕由层叠正极、隔膜和负极而成的层叠体来形成。
第2实施方式涉及的非水电解质电池也可以进一步具备收纳电极组及非水电解质的外包装材料、负极端子和正极端子。
正极及负极通过中间夹着隔膜可空间上分离。负极端子可与负极电连接。正极端子可与正极电连接。
以下,对外包装材料、负极、正极、非水电解质、隔膜、正极端子及负极端子详细地进行说明。
1)外包装材料
外包装材料例如可由厚度0.5mm以下的层压薄膜形成。或者,外包装材料例如也可以是厚度1.0mm以下的金属制容器。金属制容器的厚度更优选为0.5mm以下。
外包装材料的形状可从扁平型(薄型)、方型、圆筒型、硬币型、钮扣型中选择。作为外包装材料的例子,根据电池尺寸,例如可包括搭载于便携用电子设备等中的小型电池用外包装材料、搭载于二轮至四轮的汽车等中的大型电池用外包装材料等。
层压薄膜可使用包含两片树脂层和夹在其间的金属层的多层薄膜。金属层为了轻量化优选为铝箔或铝合金箔。树脂层例如可使用聚丙烯(PP)、聚乙烯(PE)、尼龙、聚对苯二甲酸乙二醇酯(PET)等高分子材料。层压薄膜可通过利用热熔融粘合进行密封而成形成外包装材料的形状。
金属制容器例如可由铝或铝合金等制作。铝合金优选为含有镁、锌、硅等元素的合金。在合金中含有铁、铜、镍、铬等过渡金属时,优选使其量在100质量ppm以下。
2)负极
负极可具备集电体和形成在该集电体的一面或两面上的负极层。
集电体优选为在比1V(相对于Li/Li+)高的电位范围中电化学上稳定的铝箔或含有Mg、Ti、Zn、Mn、Fe、Cu、Si这样的元素的铝合金箔。由此可防止过放电循环中的负极集电体的溶解、腐蚀劣化。为铝合金箔时,优选使铁、铜、镍、铬等过渡金属的含量在1%以下。
负极层可含有负极活性物质、导电剂及粘结剂。
第1实施方式涉及的电池用活性物质可含在负极活性物质中。负极活性物质如第1实施方式的说明中所述的那样,也可以含有第1实施方式涉及的电池用活性物质以外的负极活性物质。
负极活性物质的比表面积优选为0.5m2/g以上且50m2/g以下。在比表面积为0.5m2/g以上时,可充分确保锂离子的嵌入及脱嵌位点。在比表面积为50m2/g以下时,工业生产上容易处理。更优选比表面积为3m2/g以上且30m2/g以下。
导电剂除了能提高负极活性物质的集电性能以外,还可抑制活性物质和集电体的接触电阻。作为导电剂,例如可使用碳材料、铝粉末等金属粉末、TiO等导电性陶瓷。作为碳材料,例如可列举出乙炔黑、碳黑、焦炭、碳纤维、石墨。更优选热处理温度为800~2000℃的平均粒径10μm以下的焦炭、石墨、TiO的粉末、平均粒径1μm以下的碳纤维。有关碳材料的利用N2吸附的BET比表面积优选为10m2/g以上。
粘结剂能使负极活性物质和导电剂粘结。粘结剂的例子包括聚四氟乙烯(PTFE)、聚偏氟乙烯(PVdF)、氟系橡胶及丁苯橡胶。
负极层中的负极活性物质、导电剂及粘结剂优选分别按70质量%以上且96质量%以下,2质量%以上且28质量%以下及2质量%以上且28质量%以下的比例进行配合。通过将导电剂的量规定为2质量%以上,可提高负极层的集电性能,提高非水电解质电池的大电流特性。此外,通过将粘结剂的量规定为2质量%以上,可提高负极层和集电体的粘结性,提高循环特性。另一方面,使导电剂及粘结剂分别在28质量%以下在谋求高容量化上是优选的。
负极例如可通过将负极活性物质、导电剂及粘结剂悬浮在通用的溶剂中,调制浆料,将该浆料涂布在集电体上并使其干燥,然后实施加压来制作。负极也可以通过将活性物质、导电剂及粘结剂形成为颗粒状,然后形成负极层,将其形成在集电体上来制作。
3)正极
正极可具备集电体和形成在该集电体的一面或两面上的正极层。
集电体例如优选为铝箔或含有Mg、Ti、Zn、Mn、Fe、Cu、Si这样的元素的铝合金箔。
正极层可含有正极活性物质、导电剂及粘结剂。
作为正极活性物质,可使用例如氧化物、聚合物等。
氧化物例如可使用嵌入锂的金属氧化物,例如二氧化锰(MnO2)、氧化铁、氧化铜及氧化镍、锂锰复合氧化物(例如LixMn2O4或LixMnO2)、锂镍复合氧化物(例如LixNiO2)、锂钴复合氧化物(LixCoO2)、锂镍钴复合氧化物(例如LiNi1-yCoyO2)、锂锰钴复合氧化物(例如LixMnyCo1-yO2)、锂镍锰钴复合氧化物(例如Lix(NiaMnbCoc)O2、这里a+b+c=1)、具有尖晶石型晶体结构的锂锰镍复合氧化物(LixMn2-yNiyO4)、具有橄榄石型晶体结构的锂磷酸化物(例如LixFePO4、LixFe1-yMnyPO4、LixCoPO4)、硫酸铁(Fe2(SO4)3)或钒氧化物(例如V2O5)。上述的x及y优选为0<x≤1、0≤y≤1。
作为聚合物,例如可使用聚苯胺及聚吡咯这样的导电性聚合物材料或二硫化物系聚合物材料。还可使用硫(S)、氟化碳作为活性物质。
在优选的正极活性物质的例子中,包括正极电压高的锂锰复合氧化物(LixMn2O4)、锂镍复合氧化物(LixNiO2)、锂钴复合氧化物(LixCoO2)、锂镍钴复合氧化物(LixNi1-yCoyO2)、锂镍锰钴复合氧化物(例如Lix(NiaMnbCoc)O2,这里a+b+c=1)、具有尖晶石型晶体结构的锂锰镍复合氧化物(LixMn2-yNiyO4)、锂锰钴复合氧化物(LixMnyCo1-yO2)及具有橄榄石型晶体结构的磷酸铁锂(LixFePO4)。上述的x及y优选为0<x≤1、0≤y≤1。
从高温耐久性的观点出发,更优选的正极活性物质为锂锰复合氧化物(LixMn2O4)、锂镍锰钴复合氧化物(例如Lix(NiaMnbCoc)O2,这里a+b+c=1)、磷酸铁锂(LixFePO4)。这些活性物质结构稳定性高、充放电的可逆性优异,因而在与上述的负极活性物质的组合中,可得到更高的寿命性能。
此外,具备含有第1实施方式涉及的电池用活性物质的负极、含有具有尖晶石型晶体结构的锂锰复合氧化物(LixMn2O4)的正极或含有锂镍锰钴复合氧化物(例如Lix(NiaMnbCoc)O2,这里a+b+c=1)的正极的非水电解质电池能够5个串联地构成可显示出与铅蓄电池的优异的互换性的12V系统。另外,具备含有第1实施方式涉及的电池用活性物质的负极和含有具有橄榄石型晶体结构的磷酸铁锂(LixFePO4)的正极的非水电解质电池能够6个串联地构成可显示出与铅蓄电池的优异的互换性的12V系统。通过这样的构成,可提供高温耐久性优异、可在发动机舱中使用的组电池及电池包。
导电剂除了能提高活性物质的集电性能以外,还能够抑制活性物质和集电体的接触电阻。导电剂的例子包含乙炔黑、碳黑及石墨等碳质物。
粘结剂能够使活性物质和导电剂粘结。粘结剂的例子包含聚四氟乙烯(PTFE)、聚偏氟乙烯(PVdF)及氟系橡胶。
正极层中的正极活性物质、导电剂及粘结剂优选分别按80质量%以上且95质量%以下、3质量%以上且18质量%以下及2质量%以上且17质量%以下的比例进行配合。通过使导电剂为3质量%以上的量,能够发挥上述的效果。通过使导电剂为18质量%以下的量,能够降低高温保存下的导电剂表面的非水电解质的分解。通过使粘结剂为2质量%以上的量,可得到充分的正极强度。通过使粘结剂为17质量%以下的量,可减少正极中的绝缘材料即粘结剂的配合量,减小内部电阻。
正极例如可通过将正极活性物质、导电剂及粘结剂悬浮在通用的溶剂中来调制浆料,将该浆料涂布在集电体上并使其干燥,然后实施加压来制作。正极也可以通过将正极活性物质、导电剂及粘结剂形成为颗粒状,然后形成正极层,将其形成在集电体上来制作。
4)非水电解质
非水电解质例如可使用通过将电解质溶解于有机溶剂中而调制的液状非水电解质,或者将液状电解质和高分子材料复合化而成的凝胶状非水电解质。
液状非水电解质优选将电解质以0.5M以上且5.0M以下的浓度溶解于有机溶剂中。
电解质的例子包含高氯酸锂(LiClO4)、六氟磷酸锂(LiPF6)、四氟硼酸锂(LiBF4)、六氟砷酸锂(LiAsF6)、三氟甲磺酸锂(LiCF3SO3)、双三氟甲磺酰亚胺锂[LiN(CF3SO2)2]等锂盐或它们的混合物。电解质优选在高电位也难氧化的物质,更优选LiPF6。
有机溶剂的例子包含碳酸亚丙酯(PC)、碳酸亚乙酯(EC)、碳酸亚乙烯酯等环状碳酸酯;碳酸二乙酯(DEC)、碳酸二甲酯(DMC)、碳酸甲乙酯(MEC)等链状碳酸酯;四氢呋喃(THF)、2-甲基四氢呋喃(2MeTHF)、二氧杂戊环(DOX)等环状醚;二甲氧基乙烷(DME)、二乙氧基乙烷(DEE)等链状醚;或γ-丁内酯(GBL)、乙腈(AN)、环丁砜(SL)。这些有机溶剂能够单独使用或以混合溶剂的形态使用。
高分子材料的例子包含聚偏氟乙烯(PVdF)、聚丙烯腈(PAN)、聚环氧乙烷(PEO)。
优选的有机溶剂为将碳酸亚丙酯(PC)、碳酸亚乙酯(EC)及碳酸二乙酯(DEC)中的至少两种以上混合而成的混合溶剂或含有γ-丁内酯(GBL)的混合溶剂。通过使用这些混合溶剂,可得到高温特性优异的非水电解质电池。
5)隔膜
隔膜例如可使用包含聚乙烯、聚丙烯、纤维素或聚偏氟乙烯(PVdF)的多孔质薄膜或使用合成树脂制无纺布。优选的多孔质薄膜由聚乙烯或聚丙烯制成,能够在一定温度下熔融并切断电流,所以能够提高安全性。
6)负极端子
负极端子例如可使用在相对于锂离子金属的电位为1V以上且3V以下的范围中具备电稳定性和导电性的材料。具体地讲,可列举铝或含有Mg、Ti、Zn、Mn、Fe、Cu、Si等元素的铝合金。负极端子为了降低与负极的集电体的接触电阻,而优选与负极的集电体相同的材料。
7)正极端子
正极端子例如可使用在相对于锂离子金属的电位为3~4.25V的范围中具备电稳定性和导电性的材料。具体地讲,可列举铝或含有Mg、Ti、Zn、Mn、Fe、Cu、Si等元素的铝合金。正极端子为了降低与正极的集电体的接触电阻,而优选与正极的集电体相同的材料。
接着,参照附图对第2实施方式涉及的非水电解质电池的例子进行说明。
首先,参照图2及图3,对第1实施方式涉及的非水电解质电池的一个例子即扁平型非水电解质电池进行说明。
图2是表示第2实施方式涉及的非水电解质电池的一个例子的概略剖视图。图3是图2的非水电解质电池的A部的放大剖视图。
图2及图3所示的非水电解质电池100具备扁平状的卷绕电极组1。扁平状的卷绕电极组1如图3所示的那样,具备负极3、隔膜4及正极5。隔膜4介于负极3与正极5之间。这样的扁平状的卷绕电极组1例如可通过以隔膜4介于负极3与正极5之间的方式层叠负极3、隔膜4、正极5及另一片隔膜4而形成层叠物,以负极3在外侧的方式如图2所示的那样将该层叠物卷绕成涡卷状,然后进行加压成型来形成。
负极3包含负极集电体3a和负极层3b。最外壳的负极3如图3所示,具有只在负极集电体3a中的朝着电极组的中心的一面上形成负极层3b的构成。其它的负极3在负极集电体3a的两面上形成有负极层3b。
正极5在正极集电体5a的两面上形成有正极层5b。
如图2所示的那样,在卷绕电极组1的外周端附近,负极端子6与最外壳的负极3的负极集电体3a连接,正极端子7与内侧的正极5的正极集电体5a连接。
卷绕电极组1被收纳在袋状容器2内,袋状容器2由在两片树脂层之间夹着金属层的层压薄膜构成。
负极端子6及正极端子7从袋状容器2的开口部伸出到外部。例如液状非水电解质从袋状容器2的开口部被注入,收纳在袋状容器2内。
通过将袋状容器2的开口部以夹着负极端子6及正极端子7的方式热密封,从而通过袋状容器2将卷绕电极组1及液状非水电解质完全密封。
第2实施方式涉及的非水电解质电池包含第1实施方式涉及的电池用活性物质,所以能够显示出优异的输入输出特性、优异的寿命特性及高电压。
(第3实施方式)
根据第3实施方式,提供一种组电池。第3实施方式涉及的组电池具备第2实施方式涉及的多个非水电解质电池。
在第3实施方式涉及的组电池中,各单电池能够以串联或并联的方式电连接来配置,或者也能够以组合串联连接及并联连接的方式进行配置。
例如,第3实施方式涉及的组电池可具备6m个非水电解质电池,该非水电解质电池具备含有第1实施方式涉及的电池用活性物质的负极和含有具有橄榄石型晶体结构的含铁磷酸化合物的正极和非水电解质。这里,m为1以上的整数。6m个非水电解质电池可相互以串联的方式连接,构成组电池。如第2实施方式中说明的那样,此例组电池具备的非水电解质电池能够6个串联地构成可显示出与铅蓄电池的优异的互换性的12V系统,且高温耐久性优异。因此,此例组电池能够与铅蓄电池一同在发动机舱中使用。
此外,例如,第3实施方式涉及的组电池可具备5n个非水电解质电池,该非水电解质电池具备含有第1实施方式涉及的电池用活性物质的负极、含有选自具有尖晶石型晶体结构的锂锰复合氧化物及具有层状结构的锂镍锰钴复合氧化物中的至少1种的正极、和非水电解质。这里,n为1以上的整数。5n个非水电解质电池可相互以串联的方式连接,构成组电池。如第2实施方式中说明的那样,此例组电池具备的非水电解质电池能够5个串联地构成可显示出与铅蓄电池的优异的互换性的12V系统,且高温耐久性优异。因此,此例组电池能够与铅蓄电池一同在发动机舱中使用。
接着,参照附图对第3实施方式涉及的组电池的一个例子进行说明。
图4是表示第3实施方式涉及的组电池的一个例子的概略立体图。图4所示的组电池23具备5个单电池21。5个单电池21分别为第2实施方式涉及的一个例子的非水电解质电池。
图4所示的组电池23进一步具备4根引线20。1根引线20连结1个单电池21的负极端子6和相邻的另1个单电池21的正极端子7。如此,5个单电池21通过4根引线20串联地连接。即,图4所示的组电池23为5个串联的组电池。
如图4所示的那样,5个单电池21中的1个单电池21的正极端子7与外部连接用的正极侧引线28连接。此外,5个单电池21中的1个单电池21的负极端子6与外部连接用的负极侧引线30连接。
第3实施方式涉及的组电池由于具备第2实施方式涉及的非水电解质电池,所以能够显示出优异的输入输出特性、优异的寿命特性及高电压。
(第4实施方式)
第4实施方式涉及的电池包具备第2实施方式涉及的非水电解质电池。
第4实施方式涉及的电池包可以具备1个非水电解质电池,也可以具备多个非水电解质电池。此外,在第4实施方式涉及的电池包具备多个非水电解质电池时,各单电池能够以串联或并联的方式电连接来配置,或者也能够以组合串联连接及并联连接的方式进行配置。多个非水电解质电池也能以串联、并联、或组合串联及并联的方式电连接,构成组电池。第4实施方式涉及的电池包也可以包含多个组电池。
第4实施方式涉及的电池包可进一步具备保护电路。保护电路具有控制非水电解质电池的充放电的功能。或者,使用电池包作为电源的装置(例如电子设备、汽车等)中所包含的电路也能作为电池包的保护电路使用。
此外,第4实施方式涉及的电池包还可进一步具备通电用的外部端子。通电用的外部端子是用于将来自非水电解质电池的电流输出到外部及将电流输入给非水电解质电池的。换句话讲,在使用电池包作为电源时,将电流通过通电用的外部端子供给外部。此外,在对电池包进行充电时,将充电电流(包含汽车等车辆的动力的再生能量)通过通电用的外部端子供给电池包。
或者,第4实施方式涉及的电池包还可具备第3实施方式涉及的组电池。
接着,参照附图对第4实施方式涉及的电池包的一个例子进行说明。
图5是第4实施方式涉及的一个例子的电池包的分解立体图。图6是表示图5所示的电池包的电路的方框图。
图5及图6所示的电池包200包含具有图2及图3所示的结构的多个扁平型电池21。即,图5及图6所示的电池包200包含多个第2实施方式涉及的一个例子的非水电解质电池。
多个单电池21按照使延伸出到外部的负极端子6及正极端子7朝着相同方向聚齐的方式层叠,用粘接胶带22捆紧,从而构成了组电池23。这些单电池21如图6所示的那样相互以串联的方式电连接。
印制电路布线基板24与多个单电池21的负极端子6及正极端子7延伸出的侧面相对地配置。如图6所示的那样,在印制电路布线基板24上搭载有热敏电阻25、保护电路26及向外部设备通电用的端子27。另外,在与组电池23相对的印制电路布线基板24的面上,为了避免与组电池23的布线发生不必要的连接而安装有绝缘板(未图示)。
正极侧引线28与位于组电池23的最下层的单电池21的正极端子7连接,其前端插入至印制电路布线基板24的正极侧连接器29中而进行电连接。负极侧引线30与位于组电池23的最上层的单电池21的负极端子6连接,其前端插入至印制电路布线基板24的负极侧连接器31中而进行电连接。这些连接器29及31通过形成在印制电路布线基板24上的布线32及33而与保护电路26连接。
热敏电阻25检测各个单电池21的温度,并将其检测信号发送至保护电路26。保护电路26在规定条件下可以将保护电路26与向外部设备通电用的端子27之间的正(plus)侧布线34a及负(minus)侧布线34b切断。规定条件的一个例子例如是从热敏电阻25接收到单电池21的温度达到规定温度以上的信号时。此外,规定条件的其它例子是检测到单电池21的过充电、过放电、过电流等时。该过充电等的检测是对每个单电池21或单电池21整体进行。当检测每个单电池21时,可以检测电池电压,也可以检测正极电位或负极电位。在后者的情况下,要在每个单电池21中插入作为参比电极使用的锂电极。在图5及图6的电池包200中,在单电池21上分别连接用于电压检测的布线35。检测信号通过这些布线35被发送至保护电路26。
在除了正极端子7及负极端子6所突出的侧面以外的组电池23的三个侧面上都分别配置有由橡胶或树脂形成的保护片材36。
组电池23与各保护片材36及印制电路布线基板24一起被收纳于收纳容器37内。即,在收纳容器37的长边方向的两个内侧面和短边方向的内侧面分别配置保护片材36,在短边方向的相反侧的内侧面配置印制电路布线基板24。组电池23位于被保护片材36及印制电路布线基板24所围成的空间内。盖38安装于收纳容器37的上面。
另外,对于组电池23的固定,也可以使用热收缩带来代替粘接胶带22。此时,在组电池的两侧面配置保护片材,用热收缩管绕圈后,使热收缩管热收缩而将组电池捆扎。
图5及图6所示的电池包200具有串联连接多个单电池21的形态,但第4实施方式涉及的电池包为了增大电池容量,也可以以并联的方式连接多个单电池21。或者,第4实施方式涉及的电池包也可以具备以组合串联连接和并联连接的方式连接的多个单电池21。还可以将组装好的电池包200再以串联或并联的方式连接。
此外,图5及图6所示的电池包200具备多个单电池21,但第4实施方式涉及的电池包也可以具备1个单电池21。
此外,电池包的实施方式可以根据用途而适当变更。本实施方式涉及的电池包适合用于取出大电流时要求循环特性优异的用途。具体地讲,可作为数码相机的电源使用,或作为例如两轮至四轮的混合动力电动汽车、两轮至四轮的电动汽车、及助力自行车的车载用电池使用。特别适合作为车载用电池使用。
在搭载了第4实施方式涉及的电池包的车辆中,电池包例如可回收车辆的动力的再生能量。作为车辆,例如可列举两轮至四轮的混合动力电动汽车、两轮至四轮的电动汽车、助力自行车及电车。
第4实施方式涉及的电池包由于具备第2实施方式涉及的非水电解质电池,所以能够显示出优异的输入输出特性、优异的寿命特性及高电压。
(第5实施方式)
第5实施方式涉及的汽车具备第4实施方式涉及的电池包。
作为这里所说的汽车,可列举两轮至四轮的搭载了怠速停止机构(start-stop system)的汽车、两轮至四轮的混合动力电动汽车、两轮至四轮的电动车、助力自行车等。
图7中示出第5实施方式的汽车的一个例子。如图7所示的那样,第5实施方式的汽车41将第4实施方式涉及的电池包42搭载在发动机舱中。通过在成为高温环境下的汽车的发动机舱中设置电池包,可缩短从电池包到电动机、变换器等电动驱动系装置的距离,从而降低输入输出的损失,提高燃料消耗效率。
再者,在图7所示的汽车中,电池包搭载在发动机舱中。但是,汽车中的电池包的搭载位置并不局限于发动机舱内。例如,电池包也可搭载在汽车的车体后方或座位下。
根据第5实施方式,由于具备第4实施方式涉及的电池包,能够提供一种搭载了能显示出优异的输入输出特性、优异的寿命特性及高电压的电化学装置的汽车。
[实施例]
以下对实施例进行说明,但只要不超出本发明的主旨,本发明并不限定于以下记载的实施例。
<活性物质的合成>
(实施例1)
在实施例1中,通过以下的步骤合成实施例1的活性物质。
以Li∶Na∶Sr∶Ti的摩尔比达到2∶1∶0.5∶6的方式混合作为起始原料的碳酸锂(Li2CO3)、碳酸钠(Na2CO3)、碳酸锶(SrCO3)、锐钛矿结构的二氧化钛(TiO2),调制混合溶液。一边搅拌得到的混合溶液一边使其干燥,得到烧成前体。将得到的烧成前体在900℃烧成3小时。用以氧化锆微珠(φ5mm)为介质的珠磨机对通过烧成得到的烧成体进行粉碎。如此得到实施例1的电池用活性物质的粉末。
将实施例1的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例1的电池用活性物质为具有组成式Li2NaSr0.5Ti6O14的含钛氧化物。实施例1的电池用活性物质的粉末的平均粒径为1.7μm,比表面积为4.2m2/g,pH为10.9。
(实施例2~15、比较例1~2)
在实施例2~15及比较例1~2中,除了如下表1所示的那样变更混合溶液中的Na∶Sr的摩尔比以外,用与实施例1相同的方法,分别合成实施例2~15及比较例1~2的活性物质。
实施例2~15及比较例1~2的各个活性物质的粉末的组成分析的结果、以及平均粒径及比表面积的测定结果与实施例1的结果一同示于下表1中。再者,在表1中,按通式Li2Na(2-x)Sr(x/2)TiO14中的下标x的值的升序,记载了有关实施例1~15以及比较例1及2的信息。此外,实施例2~15及比较例1~2的各个活性物质的pH值都在10.6~11.0的范围内。
表1
(实施例21)
在实施例21中,使用碳酸钡BaCO3代替起始原料中的碳酸锶SrCO3,并以Li∶Na∶Ba∶Ti的摩尔比达到2∶1∶0.5∶6的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例21的活性物质。
将实施例21的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例21的电池用活性物质为具有组成式Li2NaBa0.5Ti6O14的含钛氧化物。实施例21的电池用活性物质的粉末的平均粒径为2.1μm,比表面积为4.0m2/g,pH为10.9。
(实施例22~35及比较例3)
在实施例22~35及比较例3中,除了如下表2所示的那样变更混合溶液中的Na∶Ba的摩尔比以外,用与实施例21相同的方法,分别合成了实施例22~35及比较例3的活性物质。
实施例21~35及比较例3的各个活性物质的粉末的组成分析的结果以及平均粒径及比表面积的测定结果与实施例21及比较例1的结果一同示于下表2中。再者,表2中,按通式Li2Na(2-x)Ba(x/2)TiO14中的下标x的值的升序,记载有关实施例21~35及比较例1及3的信息。此外,实施例21~35及比较例3的各个活性物质的pH值都在10.6~11.1的范围内。
表2
(实施例41)
在实施例41中,作为起始原料进一步使用氧化铌Nb2O5,并以Li∶Na∶Sr∶Ti∶Nb的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例41的活性物质。
将实施例41的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例41的电池用活性物质为具有组成式Li2NaSr0.5Ti5NbO14的含钛氧化物。此外,实施例41的活性物质的pH值为10.8。
(实施例42)
在实施例42中,作为起始原料进一步使用氧化钒V2O5,并以Li∶Na∶Sr∶Ti∶V的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例42的活性物质。
将实施例42的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例42的电池用活性物质为具有组成式Li2NaSr0.5Ti5VO14的含钛氧化物。此外,实施例42的活性物质的pH值为10.8。
(实施例43)
在实施例43中,作为起始原料进一步使用氧化锆ZrO2,并以Li∶Na∶Sr∶Ti∶Zr的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例43的活性物质。
将实施例43的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例43的电池用活性物质为具有组成式Li2NaSr0.5Ti5ZrO14的含钛氧化物。此外,实施例43的活性物质的pH值为10.9。
(实施例44)
在实施例44中,作为起始原料进一步使用氧化钽Ta2O5,并以Li∶Na∶Sr∶Ti∶Ta的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例44的活性物质。
将实施例44的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例44的电池用活性物质为具有组成式Li2NaSr0.5Ti5TaO14的含钛氧化物。此外,实施例44的活性物质的pH值为10.9。
(实施例45)
在实施例45中,作为起始原料进一步使用氧化钼MoO2,并以Li∶Na∶Sr∶Ti∶Mo的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例45的活性物质。
将实施例45的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例45的电池用活性物质为具有组成式Li2NaSr0.5Ti5MoO14的含钛氧化物。此外,实施例45的活性物质的pH值为10.9。
(实施例46)
在实施例46中,作为起始原料进一步使用氧化钨WO3,并以Li∶Na∶Sr∶Ti∶W的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例46的活性物质。
将实施例46的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例46的电池用活性物质为具有组成式Li2NaSr0.5Ti5WO14的含钛氧化物。此外,实施例46的活性物质的pH值为10.8。
(实施例47)
在实施例47中,作为起始原料进一步使用五氧化二磷P2O5,并以Li∶Na∶Sr∶Ti∶P的摩尔比达到2∶1∶0.5∶5∶1的方式混合起始原料并调制混合溶液,除此以外,用与实施例1相同的方法,合成了实施例47的活性物质。
将实施例47的电池用活性物质的一部分供于利用ICP的组成分析,结果得知实施例47的电池用活性物质为具有组成式Li2NaSr0.5Ti5PO14的含钛氧化物。此外,实施例47的活性物质的pH值为10.9。
实施例41~47的活性物质的组成、平均粒径及比表面积与实施例1的一同示于下表3中。
表3
(实施例51~53)
在实施例51~53中,按以下步骤合成了实施例51~53的活性物质。
首先,准备实施例1的活性物质的粉末。在其中加入麦芽糖,与纯水一同装入烧杯中进行混合。在采用转子将该混合物在搅拌器中充分分散后,使其蒸发干燥。如此,在实施例1的活性物质的粉末上均匀地涂布有机物。接着,将涂布的活性物质在氩气流中的不活泼气氛内,在500℃下烧成(碳化热处理)1小时,谋求有机物的碳化。如此得到实施例51~53的活性物质。
再者,在实施例51~53中,通过变化麦芽糖的添加量来控制碳量。
对实施例51~53的活性物质,按前面说明的步骤测定了碳元素的含量。实施例51、52及53的活性物质的碳元素的含量分别为0.3质量%、1质量%及3质量%。
将实施例51~53的活性物质的一部分供于TEM-EDX分析,确认了活性物质中的碳元素的存在区域,结果得知在实施例51~53的活性物质中,在含钛氧化物的粒子的表面上形成有含碳元素的表层。
(实施例61~63)
在实施例61~63中,按以下步骤合成了实施例61~63的活性物质。
首先,准备实施例1的活性物质的粉末。将其分成4份。将它们分别经过不同的烧成时间,在氨气流中(100mL/min)在550℃下进行烧成。将烧成时间为1小时的活性物质作为实施例61的活性物质、将烧成时间为3小时的活性物质作为实施例62的活性物质、将烧成时间为6小时的活性物质作为实施例63的活性物质、将烧成时间为12小时的活性物质作为实施例64的活性物质。
对实施例61~64的活性物质,按前面说明的步骤测定了氮元素的含量。实施例61、62、63及64的活性物质的氮元素的含量分别为0.02质量%、0.25质量%、1.2质量%及2.8质量%。
将实施例61~64的活性物质的一部分供于TEM-EDX分析,确认了活性物质中的氮元素的存在区域,结果得知在实施例61~64的活性物质中,在含钛氧化物的粒子的表面上形成有含氮元素的表层。
<烧杯电池的制造>
采用各实施例及各比较例的活性物质,按以下的步骤,制作各实施例及各比较例的烧杯电池。以下,对采用实施例1的活性物质制作实施例1的烧杯电池的步骤进行说明,但对于其它的实施例及比较例,也按同样的步骤分别制作烧杯电池。
(电极的制作)
首先,将90质量%的实施例1的活性物质、作为导电剂的5质量%的乙炔黑和5质量%的聚偏氟乙烯(PVdF)加入N-甲基吡咯烷酮(NMP)中进行混合,调制浆料。接着,将该浆料涂布在由厚度12μm的铝箔构成的集电体的两面上,并使其干燥。然后,对干燥的涂膜进行加压,由此得到电极密度(不含集电体)为2.2g/cm3的电极。
(液状非水电解质的调制)
按1∶2的体积比率混合碳酸亚乙酯(EC)及碳酸二乙酯(DEC),形成混合溶剂。以1M的浓度使电解质即LiPF6溶解于该混合溶剂中,得到液状非水电解质。
(烧杯电池的制造)
对使用制作的电极作为工作电极,使用锂金属作为对电极及参比电极的电池单元进行组装。在该电池单元中注入上述液状非水电解质,完成实施例1的烧杯电池。
<电池性能的评价>
(实施例1~15及实施例21~35)
按以下的步骤对实施例1~15及实施例21~35以及比较例1~3的烧杯电池进行评价。以下,将各实施例及各比较例的烧杯电池简称为烧杯电池。
首先,对于烧杯电池,在25℃的环境下,以0.2C及1V进行了10小时的恒电流-恒电压放电后(锂嵌入),进行将0.2C恒电流充电(锂脱嵌)进行到3V的充放电。
图1所示的有关含钛氧化物Li2NaSr0.5Ti6O14(A)的充电曲线、有关含钛氧化物Li2Na2Ti6O14(B)的充电曲线、及有关含钛氧化物Li2SrTi6O14(C)的充电曲线,分别为通过以上说明的0.2C恒电流充电得到的实施例1、比较例1及比较例2的各烧杯电池的充电曲线。
从图1弄清楚,实施例1的烧杯电池(A)能够显示出在大范围的SOC内不是多段的、而是电位连续平稳地变化的充电曲线,且能够显示出接近比较例2的烧杯电池(C)的容量。实施例2~15、实施例21~35的烧杯电池也与实施例1的相同,能够显示出在大范围的SOC内不是多段的、而是电位连续平稳地变化的充电曲线。
另一方面,从图1弄清楚,比较例1的烧杯电池(B)显示出显著低于实施例1的烧杯电池(A)的容量。此外,比较例2的烧杯电池(C)显示出多段的充电曲线。比较例3的烧杯电池也与比较例2的烧杯电池同样地显示出多段的充电曲线。
接着,对于烧杯电池,以1C及1V进行了3小时的恒电流-恒电压放电后(锂嵌入),将1C恒电流充电(锂脱嵌)进行到3V,将此充放电重复100次。将第100次充电容量相对于初次充电容量的比率作为循环容量维持率(%)算出。
以下的表4及表5中分别示出实施例1~15、实施例21~35以及比较例1~3的烧杯电池的平均工作电位、容量及循环容量维持率。
表4
表5
实施例1~15及实施例21~35的烧杯电池为通式Li2Na(2-x)M1(x/2)TiO14中的下标x的值及金属M1的种类彼此不同的例子。从表4及5所示的结果得知:实施例1~15及实施例21~35的烧杯电池尽管活性物质的组成彼此不同,但是同样能够显示出比比较例1的烧杯电池优异的容量及优异的循环容量维持率。此外得知:实施例1~15的烧杯电池尽管活性物质中的Sr的含量彼此不同,但是同样能够显示出比比较例2的烧杯电池优异的循环容量维持率。而且得知:实施例21~35的烧杯电池尽管活性物质中的Ba的含量彼此不同,但是同样能够显示出比比较例3的烧杯电池优异的循环容量维持率。
(实施例41~47、实施例51~53及实施例61~64)
对于实施例41~47、实施例51~53及实施例61~64的烧杯电池,用与实施例1相同的方法进行评价。
有关实施例41~47、实施例51~53及实施例61~64的烧杯电池的充电曲线,与实施例1的充电曲线同样,在大范围的SOC内示出不是多段的、而是电位连续平稳地变化的充电曲线。
对于实施例41~47、实施例51~53及实施例61~64的烧杯电池,进一步按以下的步骤进行速率特性评价。对实施例1的烧杯电池也同样地进行速率特性评价。
对于烧杯电池,以1C及1V进行了3小时的恒电流-恒电压放电后(锂嵌入),将1C恒电流充电(锂脱嵌)进行到3V,测定1C容量。接着,对于烧杯电池,以1C及1V进行了3小时的恒电流-恒电压放电后(锂嵌入),将10C恒电流充电(锂脱嵌)进行到3V,测定10C容量。将如此测定的10C容量相对于1C容量的比率作为10C/1C容量比(%)算出。
在以下的表6、表7及表8中,将实施例41~47、实施例51~53及实施例61~64的各个烧杯电池的容量及10C/1C容量比与实施例1的烧杯电池一同示出。此外,表6中将实施例41~47的各个烧杯电池的平均工作电位与实施例1的烧杯电池的平均工作电位一同示出。
表6
表7
表8
表6中示出结果的实施例1及实施例41~47的烧杯电池为通式Li2NaSr0.5Ti(6-y)M2(z)O14中的下标y及z的值以及元素M2的种类彼此不同的例子。从表6所示的结果得知:活性物质含有元素M2的实施例41~47的烧杯电池尽管平均工作电位及容量与实施例1的相同,但是能够显示出比实施例1的烧杯电池更优异的速率特性。特别是得知:在作为元素M2含有Nb、V、Ta及Zr时(实施例41~44)改善速率特性的效果大,得到了比作为元素M2使用Nb时(实施例41)更显著的效果。
表7中示出结果的实施例1及实施例51~53的烧杯电池为活性物质中的碳元素的含量彼此不同的例子。从表7所示的结果得知:包含用含有碳元素的表层被覆的含钛氧化物粒子的实施例51~53的烧杯电池与实施例1的烧杯电池相比,能够显示出高的容量及优异的速率特性。
表8中示出结果的实施例1及实施例61~64的烧杯电池为活性物质中的氮元素的含量彼此不同的例子。从表8所示的结果得知:含有氮处理过的含钛氧化物的实施例61~64的烧杯电池可显示出比实施例1的烧杯电池优异的速率特性。此外,得知实施例61~64的烧杯电池可显示出比实施例1的烧杯电池高的容量。
从以上说明的实施例1~15、实施例21~35、实施例41~47、实施例51~53及实施例61~64和比较例1~3的结果的比较得知:实施例1~15、实施例21~35、实施例41~47、实施例51~53及实施例61~64的各个活性物质能够实现可显示出优异的输入输出特性、优异的寿命特性及比1.55V(相对于Li/Li+)低的工作电压的烧杯电池。此外得知:由于各实施例的活性物质能够实现如此低的工作电压,所以具备作为负极活性物质含有各实施例的活性物质的负极的非水电解质电池能够显示出高电压。
<非水电解质电池的制作>
(实施例71)
在实施例71中,按以下的步骤制作实施例71的非水电解质电池。
使用实施例1的活性物质作为负极活性物质,制作负极。
此外,使用具有尖晶石型晶体结构的锂锰复合氧化物(Li1.1Mn1.9Al0.1O4)作为正极活性物质,制作正极。
另一方面,按1∶2的体积比混合碳酸亚丙酯(PC)及γ-丁内酯(GBL),调制混合溶剂。使LiBF4溶解于该混合溶剂中,达到1.5M的浓度。如此调制非水电解液。
使用按以上得到的负极、正极及非水电解液和作为外包装材料的层压薄膜,制作具有厚4mm×宽72mm×高100mm的尺寸、容量为2Ah的实施例71的电池。实施例71的电池的电压为2.7V。即,确认实施例71的非水电解质电池的电池电压为5个串联的铅酸电池互换电压。
(实施例72)
在实施例72中,按以下步骤制作实施例72的非水电解质电池。
负极与实施例71同样地制作。正极除了将具有尖晶石型晶体结构的锂镍锰钴复合氧化物(LiNi0.6Mn0.2Co0.2O2)作为正极活性物质以外,与实施例71同样地制作。非水电解液与实施例71同样地调制。
使用按以上得到的负极、正极及非水电解液和作为外包装材料的层压薄膜,制作具有厚3.4mm×宽72mm×高100mm的尺寸、容量为2Ah的实施例72的电池。确认实施例72的电池的电压为2.5V。即,实施例72的非水电解质电池的电池电压为5个串联的铅酸电池互换电压。
(实施例73)
在实施例73中,按以下步骤制作实施例73的非水电解质电池。
负极与实施例71同样地制作。正极除了将具有橄榄石型晶体结构的磷酸铁锂(LiFePO4)作为正极活性物质以外,与实施例71同样地制作。非水电解液与实施例71同样地调制。
使用按以上得到的负极、正极及非水电解液和作为外包装材料的层压薄膜,制作具有厚3.6mm×宽72mm×高100mm的尺寸、容量为2Ah的实施例73的电池。实施例73的电池的电压为2.1V。即,确认实施例73的非水电解质电池的电池电压为6个串联的铅酸电池互换电压。
(比较例71)
在比较例71中,按以下步骤制作比较例71的非水电解质电池。
负极除了将石墨作为负极活性物质以外与实施例71同样地制作。正极与实施例73同样地制作。非水电解质与实施例71同样地调制。
使用按以上得到的负极、正极及非水电解液和作为外包装材料的层压薄膜,制作具有厚3.6mm×宽72mm×高100mm的尺寸、容量为2Ah的比较例71的电池。比较例71的电池电压为3.4V。
<评价>
在80℃环境下,将实施例71~73及比较例71的电池供于充电1C/放电1C的充放电循环试验,测定了500个循环后的循环容量维持率(%)。结果示于下表9。
表9
从表9所示的结果得知,负极中使用实施例1的活性物质的实施例71~73的电池与使用石墨作为负极活性物质的比较例71的电池相比,显示出明显优异的容量维持率,具有优异的高温耐久性。特别是,使用磷酸铁锂(LiFePO4)作为正极活性物质、使用1.5M的LiBF4-PC/GBL(1∶2)电解液的实施例73的非水电解质电池可显示出非常好的循环容量维持率。另一方面,使用石墨作为负极活性物质的比较例71的非水电解质电池尽管将磷酸铁锂(LiFePO4)作为正极活性物质,但是在十几个循环时容量剧减,500个循环后的容量大约为零。
以上说明的至少一个实施方式及实施例涉及的电池用活性物质含有用通式Li(2+w)Na(2-x)M1(x/2)Ti(6-y)M2zO14表示的含钛氧化物。M1为选自Sr、Ba及Pb中的至少1种金属元素。M2为选自金属元素M(除去Ti及M1)和P中的至少1种元素。该活性物质能够在大范围的SOC内以高容量显示出稳定的输入及输出,能够以比钛酸锂低的电位进行锂的嵌入脱嵌反应。多亏于此,该活性物质能够实现可显示出优异的输入输出特性及高电压的非水电解质电池。
对本发明的几个实施方式进行了说明,但这些实施方式是作为例子而提示的,其意图并非限定发明的范围。这些新颖的实施方式能够以其它各种方式实施,在不脱嵌发明的主旨的范围内,可以进行各种省略、置换、变更。这些实施方式和其变形包含于发明的范围、主旨中,同时包含于权利要求书中记载的发明和其均等的范围内。
- 还没有人留言评论。精彩留言会获得点赞!