杂环化合物及包含其的有机发光器件的制作方法
本申请要求于2014年5月22日在韩国知识产权局提交的韩国专利申请No.10-2014-0061428的优先权和权益,其全部内容通过引用并入本文。本说明书涉及杂环化合物以及包含其的有机发光器件。
背景技术:
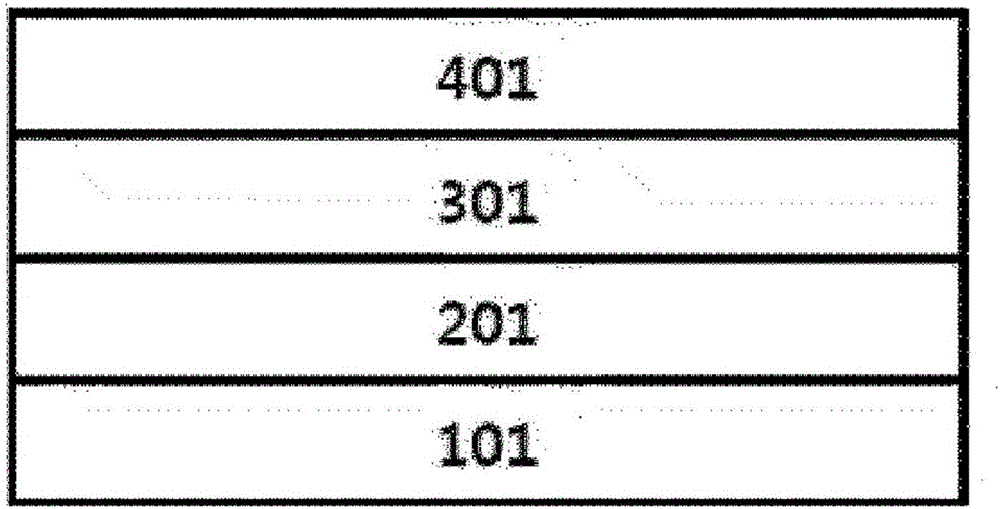
:通常,有机发光现象意指通过使用有机材料将电能转换成光能的现象。利用有机发光现象的有机发光器件具有这样的结构,其通常包括阳极、阴极和介于其间的有机材料层。本文中,在很多情况下,有机材料层具有由不同材料构成的多层结构以提高有机发光器件的效率和稳定性,例如,有机材料层可由空穴注入层、空穴传输层、发光层、电子传输层和电子注入层等形成。在有机发光器件的结构中,如果在两个电极之间施加电压,则空穴从阳极注入有机材料层并且电子从阴极注入有机材料层,当注入的空穴与电子彼此相遇时形成激子,并且当激子再次返回基态时发光。一直需要开发用于上述有机发光器件的新材料。技术实现要素:技术问题本说明书的一个目的是提供杂环化合物以及包含其的有机发光器件。技术方案本说明书的一个示例性实施方案提供了由下式1表示的杂环化合物。[式1]在式1中,X和Y各自独立地为O或S,R1至R12各自独立地为氢;氘;卤素基团;腈基;硝基;羟基;经取代或未经取代的烷基;经取代或未经取代的环烷基;经取代或未经取代的烷氧基;经取代或未经取代的芳氧基;经取代或未经取代的烷基硫基;经取代或未经取代的芳基硫基;经取代或未经取代的烷基磺酰基;经取代或未经取代的芳基磺酰基;经取代或未经取代的芳基;经取代或未经取代的芴基;经取代或未经取代的咔唑基,或者经取代或未经取代的包含N、O和S原子中一者或更多者的杂环基,其条件为R1至R4中至少之一各自独立地由-(L)n-A表示,n为0至4的整数,L包括经取代或未经取代的亚芳基,以及选自以下的一种或更多种:经取代或未经取代的包含N、O和S原子中一者或更多者的二价杂环基;并且当n为2至4时,多个L任选地彼此相同或不同,并且A为包含一个或更多个N的经取代或未经取代的单环杂环基;或者经取代或未经取代的三亚苯基。另外,本说明书的一个示例性实施方案提供了一种有机发光器件,包括:第一电极;设置成面对所述第一电极的第二电极;以及设置在所述第一电极和所述第二电极之间的包括发光层的一个或更多个有机材料层,其中所述有机材料层中的一个或更多个包含所述杂环化合物。有益效果根据本说明书的新化合物可用作用于有机发光器件的有机材料层的材料,并且可通过使用所述新化合物在有机发光器件中提高效率,获得低驱动电压,和/或改善使用寿命特点。附图说明图1示出了由基底101、阳极102、发光层301和阴极401构成的有机发光器件的实例。图2示出了由基底101、阳极201、空穴注入层501、空穴传输层601、发光层301、电子传输层701、电子注入层801和阴极401构成的有机发光器件的实例。具体实施方式下文中,将更详细地描述本说明书。本说明书的一个示例性实施方案提供了由式1表示的化合物。以下将描述取代基的实例,但不限于此。在本说明书中,术语“经取代或未经取代的”意指通过选自以下的一个或更多个取代基进行取代:氢;卤素基团;腈基;硝基;羟基;烷基;环烷基;烯基;胺基;烷基胺基;芳烷基胺基;芳基胺基;杂环基胺基;芳基;芴基;咔唑基;以及包含N、O和S原子中一者或更多者的杂环基,或者通过以上例示的取代基中的两个或更多个取代基连接的取代基进行取代,或者不具有取代基。例如,术语“两个或更多个取代基连接的取代基”可为联苯基,即,联苯基也可为芳基,并且可解释为两个苯基连接的取代基。术语“取代”意指与化合物的碳原子键合的氢原子变为另一个取代基,并且不限制取代的位置,只要该位置为氢原子被取代的位置即可,即,取代基可被取代的位置,并且当两个或更多个被取代时,两个或更多个取代基可彼此相同或不同。在本说明书中,卤素基团的实例包括氟、氯、溴或碘。在本说明书中,烷基可为直链或支化的,并且其碳原子数没有特别限制,但优选为1至50。其具体实例包括甲基、乙基、丙基、正丙基、异丙基、丁基、正丁基、异丁基、叔丁基、仲丁基、1-甲基-丁基、1-乙基-丁基、戊基、正戊基、异戊基、新戊基、叔戊基、己基、正己基、1-甲基戊基、2-甲基戊基、4-甲基-2-戊基、3,3-二甲基丁基、2-乙基丁基、庚基、正庚基、1-甲基己基、环戊基甲基、环己基甲基、辛基、正辛基、叔辛基、1-甲基庚基、2-乙基己基、2-丙基戊基、正壬基、2,2-二甲基庚基、1-乙基-丙基、1,1-二甲基-丙基、异己基、2-甲基戊基、4-甲基己基、5-甲基己基等,但并不限于此。在本说明书中,环烷基没有特别限制,但其碳原子数优选为3至60,并且其具体实例包括环丙基、环丁基、环戊基、3-甲基环戊基、2,3-二甲基环戊基、环己基、3-甲基环己基、4-甲基环己基、2,3-二甲基环己基、3,4,5-三甲基环己基、4-叔丁基环己基、环庚基、环辛基等,但并不限于此。在本说明书中,烷氧基可为直链、支化或环状的。烷氧基的碳原子数没有特别限制,但优选为1至20。其具体实例可包括甲氧基、乙氧基、正丙氧基、异丙氧基(isopropoxy)、异丙基氧基(i-propyloxy)、正丁氧基、异丁氧基、叔丁氧基、仲丁氧基、正戊氧基、新戊氧基、异戊氧基、正己氧基、3,3-二甲基丁氧基、2-乙基丁氧基、正辛氧基、正壬氧基、正癸氧基、苄氧基、对甲基苄氧基等,但并不限于此。在本说明书中,烯基可为直链或支化的,其碳原子数没有特别限制,但优选为2至40。其具体实例包括乙烯基、1-丙烯基、异丙烯基、1-丁烯基、2-丁烯基、3-丁烯基、1-戊烯基、2-戊烯基、3-戊烯基、3-甲基-1-丁烯基、1,3-丁二烯基、烯丙基、1-苯基乙烯基-1-基、2-苯基乙烯基-1-基、2,2-二苯基乙烯基-1-基、2-苯基-2-(萘基-1-基)乙烯基-1-基、2,2-双(二苯基-1-基)乙烯基-1-基、芪基、苯乙烯基等,但并不限于此。在本说明书中,芳基可为单环芳基或多环芳基,并且包括具有1至25个碳原子的烷基或具有1至25个碳原子的烷氧基被取代的情况。另外,在本说明书中,芳基可意指芳香环。当芳基为单环芳基时,碳原子数没有特别限制,但优选为6至25。单环芳基的具体实例可包括苯基、联苯基、三联苯基、芪基等,但不限于此。当芳基为多环芳基时,碳原子数没有特别限制,但优选为10至24。多环芳基的具体实例可包括萘基、蒽基、菲基、三亚苯基、芘基、苝基、基、荧蒽基、芴基等,但并不限制于此。在本说明书中,芴基可被取代,并且两个取代基可彼此键合形成螺环结构。当芴基被取代时,芴基可以是等。但是,芴基并不限于此。在本说明书中,甲硅烷基的具体实例包括三甲基甲硅烷基、三乙基甲硅烷基、叔丁基二甲基甲硅烷基、乙烯基二甲基甲硅烷基、丙基二甲基甲硅烷基、三苯基甲硅烷基、二苯基甲硅烷基、苯基甲硅烷基等,但并不限于此。在本说明书中,胺基的碳原子数没有特别限制,但优选为1至30。胺基的具体实例包括甲胺基、二甲胺基、乙胺基、二乙胺基、苯基胺基、萘胺基、联苯基胺基、蒽基胺基、9-甲基-蒽基胺基,二苯基胺基、苯基萘基胺基、二甲苯基胺基、苯基甲苯基胺基、三苯基胺基等,但并不限于此。在本说明书中,杂环基为包含N、O和S中一者或更多者作为杂原子的杂环基。并且其碳原子数没有限制,但优选为2至60。杂环基的实例包括噻吩基、呋喃基、吡咯基、咪唑基、噻唑基、唑基、二唑基、三唑基、吡啶基、联吡啶基、嘧啶基、三嗪基、三唑基、吖啶基、哒嗪基、吡嗪基、喹啉基、喹唑啉基、喹喔啉基、酞嗪基、吡啶并嘧啶基、吡啶并吡嗪基、吡嗪并吡嗪基、异喹啉基、吲哚基、咔唑基、苯并唑基、苯并咪唑基、苯并噻唑基、苯并咔唑基、苯并噻吩基、二苯并噻吩基、苯并呋喃基基、菲咯啉基、噻唑基、异唑基、二唑基、噻二唑基、苯并噻唑基、吩噻嗪基、二苯并呋喃基等,但并不限于此。在本说明书中,芳氧基、芳基胺基、芳烷基胺基、杂芳基胺基、芳基硫基、芳基磺酰基和芳基烯基的芳基与芳基的上述实例相同。具体地,芳氧基的实例包括苯氧基、对甲苯氧基、间甲苯氧基、3,5-二甲基苯氧基、2,4,6-三甲基苯氧基、对叔丁基苯氧基、3-联苯氧基、4-联苯氧基、1-萘氧基、2-萘氧基、4-甲基-1-萘氧基、5-甲基-2-萘氧基、1-蒽氧基、2-蒽氧基、9-蒽氧基、1-菲氧基、3-菲氧基、9-菲氧基等,芳基硫基的实例包括苯基硫基、2-甲基苯基硫基、4-叔丁基苯基硫基等,并且芳基磺酰基的实例包括苯磺酰基,对甲苯磺酰基等,但实例并不限于此。在本说明书中,烷基硫基、芳烷基胺基和烷基磺酰基的烷基与烷基的上述实例相同。具体地,烷基硫基的实例包括甲基硫基、乙基硫基、叔丁基硫基、己基硫基、辛基硫基等,并且烷基磺酰基的具体实例包括甲基磺酰基、乙基磺酰基、丙基磺酰基、丁基磺酰基等,但实例并不限于此。在本说明书中,亚芳基意指在芳基中存在两个键合位置,即,二价基团。芳基的上述描述可适用,不同之处在于这些各自为二价基团。在本说明书中,“*”意指键合至另一个取代基的部分。根据本说明书的一个示例性实施方案,X可以是O。根据本说明书的另一个示例性实施方案,R2或R3由-(L)n-A表示,n为0或1,L为经取代或未经取代的亚苯基、经取代或未经取代的亚联苯基、经取代或未经取代的二价萘基,或者经取代或未经取代的亚蒽基,并且A可以是经取代或未经取代的杂环基,或者经取代或未经取代的芳基。根据本说明书的一个示例性实施方案,R5和R6可以是具有1至10个碳原子的经取代或未经取代的烷基。根据本说明书的一个示例性实施方案,R5和R6可以是甲基。根据本说明书的一个示例性实施方案,R10可以是氢,或者具有6至20碳原子的经取代或未经取代的芳基。根据本说明书的一个示例性实施方案,R10可以是氢、经取代或未经取代的苯基、经取代或未经取代的联苯基,或者经取代或未经取代的萘基。根据本说明书的一个示例性实施方案,A可以是经取代或未经取代的吡啶基、经取代或未经取代的嘧啶基、经取代或未经取代的哒嗪基、经取代或未经取代的吡嗪基、经取代或未经取代的三嗪基、经取代或未经取代的四嗪基、五嗪基、经取代或未经取代的咔唑基、经取代或未经取代的二苯并呋喃基、经取代或未经取代的二苯并噻吩基、经取代或未经取代的苯基、经取代或未经取代的联苯基、经取代或未经取代的萘基、经取代或未经取代的菲基、经取代或未经取代的蒽基、经取代或未经取代的芴基、经取代或未经取代的螺二芴基、经取代或未经取代的荧蒽基,或者经取代或未经取代的三亚苯基。根据本说明书的一个示例性实施方案,A可以是经取代或未经取代的三嗪基、经取代或未经取代的嘧啶基、经取代或未经取代的咔唑基、经取代或未经取代的二苯并呋喃基、经取代或未经取代的二苯并噻吩基、经取代或未经取代的苯基、经取代或未经取代的联苯基、经取代或未经取代的萘基、经取代或未经取代的菲基、经取代或未经取代的蒽基、经取代或未经取代的芴基、经取代或未经取代的螺二芴基、经取代或未经取代的荧蒽基,或者经取代或未经取代的三亚苯基。根据本说明书的一个示例性实施方案,当A另外地经取代时,另外的取代基可以是经选自以下的一个或更多个取代基取代的取代基:卤素基团;具有1至10个碳原子的烷基;具有6至20个碳原子的芳基,以及具有2至20个碳原子的包含N、O和S原子中一者或更多者作为杂原子的杂环基。根据本说明书的一个示例性实施方案,当A另外地经取代时,A可以经苯基取代。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的三嗪基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的三嗪基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的嘧啶基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的嘧啶基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的咔唑基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的咔唑基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的二苯并呋喃基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的二苯并呋喃基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的二苯并噻吩基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的二苯并噻吩基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的萘基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的萘基的苯基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的萘基的萘基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的菲基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的菲基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的蒽基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的蒽基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的芴基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的芴基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的螺二芴基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的螺二芴基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的荧蒽基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的荧蒽基的苯基。根据本说明书的一个示例性实施方案,R2可以是经取代或未经取代的三亚苯基。根据本说明书的一个示例性实施方案,R2可以是其中取代有经取代或未经取代的三亚苯基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的三嗪基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的三嗪基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的嘧啶基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的嘧啶基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的咔唑基。根据本说明书的一个示例性实施方案,R3可以是其中经取代有取代或未经取代的咔唑基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的二苯并呋喃基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的二苯并呋喃基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的二苯并噻吩基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的二苯并噻吩基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的萘基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的萘基的苯基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的萘基的萘基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的菲基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的菲基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的蒽基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的蒽基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的芴基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的芴基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的螺二芴基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的螺二芴基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的荧蒽基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的荧蒽基的苯基。根据本说明书的一个示例性实施方案,R3可以是经取代或未经取代的三亚苯基。根据本说明书的一个示例性实施方案,R3可以是其中取代有经取代或未经取代的三亚苯基的苯基。根据本说明书的一个示例性实施方案,由式1表示的化合物可由下式1-1或1-2表示:[式1-1][式1-2]式1-1和1-2中的R1至R4和R7至R12与式1中所限定的那些相同。根据本说明书的一个示例性实施方案,-(L)n-A可以是以下经取代或未经取代的取代基1-1至1-41中的任一取代基。然而,-(L)n-A并不限于此。根据本说明书的一个示例性实施方案,当以下取代基1-1至1-41另外地经取代时,另外的取代基可以是经选自以下的一个或更多个取代基取代的取代基:卤素基团;具有1至10个碳原子的烷基;具有6至20个碳原子的芳基,以及具有2至20个碳原子的包含N、O和S原子中一者或更多者作为杂原子的杂环基。根据本说明书的一个示例性实施方案,由式1表示的所述化合物由下式2-1至2-81中任一者表示。然而,所述化合物并不限于此。根据本说明书的一个示例性实施方案,由式1表示的化合物的一般合成例可如下。具体地,根据本说明书的一个示例性实施方案,在一般合成例中,由K表示的化合物可通过使用由Q表示的化合物和苯甲酸酯类化合物经由闭环反应产生,并且此外,由L表示的化合物可通过使用卤化物制备。由式1表示的化合物可通过使用合成例制备,并且如果必要的话,调整多个取代基或取代基位置。本说明书的一个示例性实施方案提供了一种包含所述杂环化合物的有机发光器件。本说明书的一个示例性实施方案提供了一种有机发光器件,包括:第一电极;设置成面对所述第一电极的第二电极;以及设置在所述第一电极和所述第二电极之间的包括发光层的一个或更多个有机材料层,其中所述有机材料层中的一个或更多个层包含所述杂环化合物。本说明书的有机发光器件的有机材料层除了可由其中堆叠有两个或更多个有机材料层的多层结构构成之外,还可由单层结构构成。例如,本发明的有机发光器件可具有包括空穴注入层、空穴传输层、发光层、电子传输层、电子注入层等作为有机材料层的结构。然而,有机发光器件的结构并不限于此,而是可包括更少数量的有机层。在本说明书的一个示例性实施方案中,所述有机材料层可包括空穴传输层、空穴注入层,或同时注入和传输空穴的层,并且所述空穴传输层、所述空穴注入层,或所述同时注入和传输空穴的层可包含所述杂环化合物。在另一个示例性实施方案中,发光层可包含杂环化合物。具体地,根据本说明书的一个示例性实施方案,所述杂环化合物可以是发光基质。在本说明书的一个示例性实施方案中,所述有机材料层可包括电子传输层、电子注入层,或同时传输和注入电子的层,并且所述电子传输层、所述电子注入层,或所述同时传输和注入电子的层可包含所述杂环化合物。在本说明书的一个示例性实施方案中,所述电子传输层、所述电子注入层,或所述同时传输和注入电子的层可仅包含所述杂环化合物。在本说明书的一个示例性实施方案中,有机材料层除了可包括包含所述杂环化合物的有机材料层之外,还可包括空穴注入层或空穴传输层,所述空穴注入层或空穴传输层包含含有芳基胺基、咔唑基或苯并咔唑基的化合物。在本说明书的一个示例性实施方案中,包含所述杂环化合物的有机材料层可包含所述杂环化合物作为基质,并且可包含另外的有机化合物、金属或金属化合物作为掺杂剂。在本说明书的一个示例性实施方案中,有机材料层可包括电子阻挡层,并且电子阻挡层可包含所述杂环化合物。在本说明书的一个示例性实施方案中,有机材料层还可包括选自以下的一个或两个或更多个层:空穴注入层、空穴传输层、电子阻挡层、电荷产生层、空穴阻挡层、电子传输层,和电子注入层。在另一个示例性实施方案中,有机发光器件可为具有其中阳极、一个或更多个有机材料层和阴极按顺序堆叠在基底上的结构(正常型)的有机发光器件。在又一个示例性实施方案中,有机发光器件可为具有其中阴极、一个或更多个有机材料层和阳极按顺序堆叠在基底上的反向结构(倒置型)的有机发光器件。例如,根据本说明书示例性实施方案的有机发光器件的结构示于图1和2中。图1示出了由基底101、阳极102、发光层301和阴极401构成的有机发光器件的实例。在该结构中,所述杂环化合物可包含于发光层301中。图2示出了由基底101、阳极201、空穴注入层501、空穴传输层601、发光层301、电子传输层701、电子注入层801和阴极401构成的有机发光器件的实例。在该结构中,所述杂环化合物可包含于空穴注入层501、空穴传输层601、发光层301、电子传输层701和电子注入层801中的一个或更多个层中。本说明书的有机发光器件可通过本领域已知的材料和方法来制造,不同之处在于有机材料层的一个或更多个层包含本说明书的化合物,即,所述杂环化合物。当有机发光器件包括多个有机材料层时,所述有机材料层可由相同材料或不同材料形成。本说明书的有机发光器件可通过本领域已知的材料和方法来制造,不同之处在于有机材料层的一个或更多个层包含所述杂环化合物,即,由式1表示的化合物。例如,本说明书的有机发光器件可通过将第一电极、有机材料层和第二电极按顺序堆叠在基底上来制造。在这种情况下,有机发光器件可通过以下过程来制造:通过使用物理气相沉积(PVD)法(如溅射法或电子束蒸发法)使金属或具有导电性的金属氧化物、或其合金沉积在基底上形成阳极,在其上形成包括空穴注入层、空穴传输层、发光层和电子传输层的有机材料层,然后使可以用作阴极的材料沉积在其上。除了上述方法之外,有机发光器件可通过使阴极材料、有机材料层和阳极材料按顺序沉积在基底上来制造。另外,当制造有机发光器件时,式1的化合物不仅可通过真空沉积法还可通过溶液涂覆法形成为有机材料层。在此,溶液涂覆法意指旋涂、浸涂、刮涂、喷墨印刷、丝网印刷、喷涂法、辊涂等,但并不限于此。除了上述方法外,有机发光器件可通过使阴极材料、有机材料层和阳极材料按顺序沉积在基底上来制造(国际专利公开第2003/012890号)。但是,制备方法并不限于此。在本说明书的一个示例性实施方案中,第一电极为阳极,且第二电极为阴极。在另一个示例性实施方案中,第一电极为阴极,且第二电极为阳极。作为阳极材料,通常优选的是具有大功函数的材料以使空穴顺利注入有机材料层。本发明中可使用的阳极材料的具体实例包括:金属如钒、铬、铜、锌和金,或其合金;金属氧化物如氧化锌、氧化铟、氧化铟锡(ITO)和氧化铟锌(IZO);金属和氧化物的组合如ZnO:Al或SnO2:Sb;导电聚合物例如聚(3-甲基噻吩)、聚[3,4-(亚乙基-1,2-二氧基)噻吩](PEDOT)、聚吡咯和聚苯胺等,但并不限于此。作为阴极材料,通常优选的是具有小功函数的材料以使电子容易注入有机材料层。阴极材料的具体实例包括金属如镁、钙、钠、钾、钛、铟、钇、锂、钆、铝、银、锡和铅,或其合金;多层结构材料例如LiF/Al或LiO2/Al等,但并不限于此。空穴注入材料是注入来自电极的空穴的层,并且空穴注入材料优选为这样的化合物,其具有传输空穴的能力从而在阳极具有空穴注入效应且对发光层或发光材料具有优异的空穴注入效应,防止发光层中产生的激子迁移到电子注入层或电子注入材料,并且具有优异的薄膜形成能力。优选的是,空穴注入材料的最高占据分子轨道(HOMO)介于阳极材料的功函数与周边有机材料层的HOMO之间。空穴注入材料的具体实例包括金属卟啉、低聚噻吩、芳胺类有机材料、六腈六氮杂三亚苯基类有机材料、喹吖啶酮类有机材料、苝类有机材料、蒽醌、聚苯胺、聚噻吩类导电聚合物等,但并不限于此。空穴传输层是接收来自空穴注入层的空穴并将空穴传输到发光层的层,且空穴传输材料为可以接收来自阳极或空穴注入层的空穴并将空穴传输到发光层的材料,对空穴具有高迁移率的材料是合适的。其具体实例包括芳胺类有机材料、导电聚合物、同时存在共轭部分和非共轭部分的嵌段共聚物等,但并不限于此。发光材料为可以接收分别来自空穴传输层和来自电子传输层的空穴和电子并使空穴与电子结合以在可见光区发光的材料,并且优选地为对荧光和磷光具有良好量子效率的材料。其具体实例包括:8-羟基喹啉铝络合物(Alq3);咔唑类化合物;二聚苯乙烯基化合物;BAlq;10-羟基苯并喹啉-金属化合物;苯并唑、苯并噻唑和苯并咪唑类化合物;聚(对苯乙炔)(PPV)类聚合物;螺环化合物;聚芴、红荧烯等,但并不限于此。发光层可包含基质材料和掺杂剂材料。基质材料的实例包括缩合芳香环衍生物、或包含杂环的化合物等。具体地,缩合芳香环衍生物的实例包括蒽衍生物、芘衍生物、萘衍生物、并五苯衍生物、菲化合物、荧蒽化合物等,而包含杂环的化合物的具体实例包括咔唑衍生物,二苯并呋喃衍生物,梯型呋喃化合物,嘧啶衍生物等,但其实例并不限于此。掺杂剂材料的实例包括有机化合物、金属或金属化合物。作为掺杂剂材料的有机化合物的实例包括芳香族胺衍生物、苯乙烯胺化合物、硼络合物、荧蒽化合物等。具体来说,芳香族胺衍生物为具有经取代或未经取代的芳基氨基的缩合芳香环衍生物,并且其实例包括具有芳基氨基的芘、蒽、和二茚并芘等;苯乙烯胺化合物为其中经取代或未经取代的芳基胺被至少一个芳基乙烯基取代的化合物,并且选自芳基、甲硅烷基、烷基、环烷基和芳氨基中的一个或两个或更多个取代基是经取代或未经取代的。其具体实例包括苯乙烯胺、苯乙烯二胺、苯乙烯三胺、苯乙烯四胺等,但是并不限于此。另外,作为金属或金属化合物,可使用典型的金属或金属化合物,并且具体地,可使用金属络合物。金属络合物的实例包括铱络合物、铂络合物等,但并不限于此。电子传输材料为接收来自电子注入层的电子并将电子传输至发光层的层,电子传输材料为可以很好地从阴极注入电子并将电子迁移到发光层的材料,对电子具有高迁移率的材料是合适的。其具体实例包括8-羟基喹啉Al络合物;包含Alq3的络合物;有机自由基化合物;羟基黄酮-金属络合物等,但并不限于此。所述电子传输层可以与如根据现有技术所使用的任何期望阴极材料一起使用。特别地,合适阴极材料的实例包括具有小功函数的常规材料,后接铝层或银层。其具体实例包括铯、钡、钙、镱和钐,在每种情况中均后接铝层或银层。电子注入层为注入来自电极的电子的层,并且优选这样的化合物:具有传输电子的能力,具有由阴极注入电子的效应以及优异的向发光层或发光材料注入电子的效应,防止发光层中产生的激子迁移至空穴注入层,并且还具有优异的薄膜形成能力。其具体实例包括芴酮、蒽醌二甲烷、联苯醌、噻喃二氧化物、唑、二唑、三唑、咪唑、苝四羧酸、亚芴甲烷、蒽酮及其衍生物,金属络合物化合物,含氮五元环衍生物等,但并不限于此。金属络合物化合物的实例包括8-羟基喹啉锂、双(8-羟基喹啉)锌、双(8-羟基喹啉)铜、双(8-羟基喹啉)锰、三(8-羟基喹啉)铝、三(2-甲基-8-羟基喹啉)铝、三(8-羟基喹啉)镓、双(10-羟基苯并[h]喹啉)铍、双(10-羟基苯并[h]喹啉)锌、双(2-甲基-8-喹啉)氯镓、双(2-甲基-8-喹啉)(邻甲酚)镓、双(2-甲基-8-喹啉)(1-萘酚)铝、双(2-甲基-8-喹啉)(2-萘酚)镓等,但并不限于此。空穴阻挡层为阻挡空穴到达阴极的层,并且可一般地在与空穴注入层相同的条件下形成。其具体实例包括二唑衍生物或三唑衍生物、邻二氮杂菲衍生物、BCP、铝络合物等,但并不限于此。电子阻挡层为这样的层,其用于通过阻挡电子同时传输空穴来提高电子和空穴复合的可能性,并且电子传输能力明显较低的材料是合适的。作为用于电子层的材料,如果必要的话,可使用用于空穴传输层的前述材料,并且可使用公知的电子阻挡层而不受限于此。根据所用材料,根据本说明书的有机发光器件可为顶部发光型、底部发光型或双侧发光型。在本说明书的一个示例性实施方案中,除有机发光器件之外,杂环化合物还可包含在有机太阳能电池或有机晶体管中。发明模式在以下实例中将详细描述由式1表示的杂环化合物及包含所述杂环化合物的有机发光器件的制造。但是,陈述以下实施例用于举例说明本说明书,但是本说明书的范围并不限于此。[制备例1]化合物P2的制备将P1(20g,99.8mmol)、2-溴-5-氯苯甲酸甲酯(36g,144mmol)、CuI(5.2g,27.3mmol)和Cs2CO3(64g,196mmol)悬浮于二甲基甲酰胺(DMF)(150mL)中。在氮气氛下搅拌混合物同时回流约12小时,然后冷却至室温。在0℃下向其中缓慢地添加200mL2M的HCl,然后过滤通过在常温下将得到的混合物搅拌1小时所产生的固体。将滤出的固体溶解于500mL的CHCl3中,然后用水清洗。将产物放在无水硫酸镁上干燥,然后通过减压移除溶剂。产生的固体通过柱色谱法使用己烷/乙酸乙酯(10/1,v/v)来纯化,从而获得白色固体P2(20g,产率54%)。MS:[M+H]=353[制备例2]化合物P3的制备将化合物P2(20.0g,54.3mmol)溶解于无水四氢呋喃(THF)(300mL)中,然后在0℃下在氮气氛下向其中缓慢地添加MeMgBr溶液(3M,在醚溶液中55mL)。将得到的溶液在常温下搅拌12小时,然后缓慢地添加到饱和的NH4Cl溶液(500mL)中。在将混合溶液用乙酸乙酯萃取之后,将得到的产物在无水硫酸镁上干燥,然后通过减压移除溶剂。将产生的固体悬浮于AcOH中而不进行进一步纯化,然后逐滴向其中添加0.5mL的硫酸。搅拌混合物同时在氮气下回流约12小时,然后冷却至室温。移除溶剂,然后向其中添加水。在将混合溶液用乙酸乙酯萃取之后,将得到的产物在无水硫酸镁上干燥,然后通过减压移除溶剂。产生的固体通过柱色谱法使用己烷/乙酸乙酯(10/1,v/v)来纯化,从而获得白色固体P3(13g,产率68%).MS:[M+H]=351[制备例3]化合物P4的制备将化合物P3(12.0g,34.2mmol)、双频哪醇二硼(10.1g,39.7mmol)、Pd(dba)2(0.7g,1.2mmol)、PCy3(0.8g,2.8mmol)和KOAc(12.5g,127.0mmol)悬浮于1,4-二氧六环(150mL)中。在氮气氛下搅拌混合物同时回流约12小时,然后冷却至室温。移除溶剂,然后将得到的产物溶解于氯仿。将溶液在无水硫酸镁上干燥并且过滤,然后通过减压移除溶剂。产生的固体通过使用EtOH纯化,从而得到P4(13.7g,产率90%)。MS:[M+H]=443[制备例4]式P5的制备化合物P5(14.1g,81%)通过以与制备例1中制备化合物P2相同的方式进行制备来获得,不同之处在于使用2-溴-4-氯苯甲酸甲酯(11.7g,46.9mmol)代替2-溴-5-氯苯甲酸甲酯。MS:[M+H]=369[制备例6]式P6的制备化合物P6(8.1g,77.9%)通过以与制备例2中制备化合物P3相同的方式进行制备来获得,不同之处在于使用P5(10.9g,29.5mmol)代替P2。MS:[M+H]=351[制备例7]式P7的制备化合物P7(6.1g,84.5%)通过以与制备例3中制备化合物P4相同的方式进行制备来获得,不同之处在于使用P6(5.7g,16.2mmol)代替P3。MS:[M+H]=443[制备例8]式P9的制备化合物P9(16.1g,46.6%)通过以与制备例1中制备化合物P2相同的方式进行制备来获得,不同之处在于使用P8(18.0g,97.7mmol)代替P1。MS:[M+H]=353[制备例9]式P10的制备化合物P10(7.7g,82.6%)通过以与制备例2中制备化合物P3相同的方式进行制备来获得,不同之处在于使用P9(9.8g,27.7mmol)代替P2。MS:[M+H]=335[制备例10]式P11的制备化合物P11(5.1g,78.2%)通过以与制备例3中制备化合物P4相同的方式进行制备来获得,不同之处在于使用P10(5.1g,15.2mmol)代替P3。MS:[M+H]=427[制备例11]式P12的制备化合物P12(13.4g,58%)通过以与制备例1中制备化合物P2相同的方式进行制备来获得,不同之处在于使用P8(12.0g,65.1mmol)代替P1,并且使用2-溴-4-氯苯甲酸甲酯(15.5g,62.1mmol)代替2-溴-5-氯苯甲酸甲酯。MS:[M+H]=353[制备例12]式P13的制备化合物P13(8.9g,80.0%)通过以与制备例2中制备化合物P3相同的方式进行制备来获得,不同之处在于使用P12(11.7g,33.1mmol)代替P2。MS:[M+H]=335[制备例13]式P14的制备化合物P14(6.5g,79.5%)通过以与制备例3中制备化合物P4相同的方式进行制备来获得,不同之处在于使用P13(6.4g,19.1mmol)代替P3。MS:[M+H]=427[制备例14]式2-2的制备将P4(12.0g,27.1mmol)、2-氯-4,6-二苯基-1,3,5-三嗪(7.5g,28.0mmol)、Pd(PPh3)4(0.7g,1.2mmol)和K2CO3(12g,86.8mmol)悬浮于四氢呋喃(THF)(100mL)中。在氮气氛下搅拌混合物同时回流约24小时,然后冷却至室温。移除溶剂,然后将得到的产物溶解于氯仿中。将溶液在无水硫酸镁上干燥并且过滤,然后通过减压移除溶剂。产生的固体用THF/甲苯纯化,从而获得由式2-2表示的白色固体化合物(10.3g,产率69%)。MS:[M+H]=548[制备例15]式2-8的制备化合物2-8(8.9g,64.8%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用2-(3-溴苯基)-4,6-二苯基-1,3,5-三嗪(9.7g,21.9mmol)代替2-氯-4,6-二苯基-1,3,5-三嗪。MS:[M+H]=624[制备例16]式2-18的制备化合物2-18(7.3g,74.0%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用P14(7.9g,18.5mmol)代替P4。MS:[M+H]=532[制备例17]式2-31的制备化合物2-31(8.9g,64.8%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用P7(9.7g,21.9mmol)代替P4,并且使用2-(4-溴苯基)-4,6-二苯基-1,3,5-三嗪(9.7g,21.9mmol)代替2-氯-4,6-二苯基-1,3,5-三嗪。MS:[M+H]=624[制备例18]式2-56的制备化合物2-56(6.3g,70.0%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用P14(6.7g,15.7mmol)代替P4,并且使用9-溴-10-苯基蒽(5.4g,16.2mmol)代替2-氯-4,6-二苯基-1,3,5-三嗪。MS:[M+H]=567[制备例19]式2-72的制备化合物2-72(6.0g,64.4%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用P11(7.1g,16.6mmol)代替P4,并且使用3-溴-9苯基-9H-咔唑(5.4g,16.7mmol)代替2-氯-4,6-二苯基-1,3,5-三嗪。MS:[M+H]=558[制备例20]式2-76的制备化合物2-76(7.5g,75.0%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用P11(7.0g,16.4mmol)代替P4,并且使用2-([1,1’-联苯基]-4-基)-4-氯-6-苯基-1,3,5-三嗪(5.7g,16.5mmol)代替2-氯-4,6-二苯基-1,3,5-三嗪。MS:[M+H]=608[制备例21]式2-79的制备化合物2-79(7.7g,75.1%)通过以与制备例14中制备化合物2-2相同的方式进行制备来获得,不同之处在于使用P11(7.9g,18.5mmol)代替P4,并且使用9-溴-10-苯基蒽(6.5g,19.5mmol)代替2-氯-4,6-二苯基-1,3,5-三嗪。MS:[M+H]=553[实施例1]将薄薄地涂覆有厚度为的氧化铟锡(ITO)薄膜的玻璃基底(康宁7059玻璃)放入其中溶解有清洁剂的蒸馏水中,并超声清洗。使用Fischer公司制造的产品作为清洁剂,使用用Millipore公司制造的过滤器过滤两次的蒸馏水作为蒸馏水。在将ITO清洗30分钟后,使用蒸馏水重复进行两次超声清洗10分钟。用蒸馏水清洗完成后,按顺序使用异丙醇、丙酮和甲醇溶剂进行超声清洗,然后进行干燥。通过加热使六腈六氮杂三亚苯基以的厚度真空沉积在由此制备的透明ITO电极上,从而形成空穴注入层。在其上真空沉积作为传输空穴的材料的HT-1然后真空沉积制备例18中合成的作为发光层基质的化合物2-56和掺杂剂D1化合物至厚度为然后,通过加热按顺序使E1化合物真空沉积为电子注入层和电子传输层。负电极通过在电子传输层上按顺序分别沉积氟化锂(LiF)和铝至厚度为和形成,从而制造有机发光器件。在前述过程中,分别保持有机材料、氟化锂和铝的沉积速率为和至[六腈六氮杂三亚苯基][实施例2]实验以与实施例1中相同的方式进行,不同之处在于,作为发光层的基质,使用化合物2-79代替制备例18中合成的化合物2-56。[比较例1]实验以与实施例1中相同的方式进行,不同之处在于,作为发光层的基质,使用H1代替制备例18中合成的化合物2-56。实验结果示于下表1中。[表1]实验例(50mA/cm2)基质材料电压(V)电流效率(Cd/A)比较例1H16.135.85实施例12-565.56.01实施例22-795.615.9如表1所示,根据本发明的式的化合物衍生物在包括有机发光器件的有机电子器件中可表现出优良的效率和驱动电压特性。[实施例3]将薄薄地涂覆有厚度为的氧化铟锡(ITO)薄膜的玻璃基底(康宁7059玻璃)放入其中溶解有清洁剂的蒸馏水中,并超声清洗。使用Fischer公司制造的产品作为清洁剂,使用用Millipore公司制造的过滤器过滤两次的蒸馏水作为蒸馏水。在将ITO清洗30分钟后,使用蒸馏水重复进行两次超声波清洗10分钟。用蒸馏水清洗完成后,按顺序使用异丙醇、丙酮和甲醇溶剂进行超声清洗,然后进行干燥。通过加热使六腈六氮杂三亚苯基以的厚度真空沉积在由此制备的透明ITO电极上,从而形成空穴注入层。在其上真空沉积作为传输空穴的材料的NPB然后以10%的浓度真空沉积制备例14中合成的作为发光层基质的化合物2-2和Ir(ppy)3掺杂剂化合物至厚度为然后,通过加热按顺序使E1化合物真空沉积为电子注入层和电子传输层。负电极通过在电子传输层上按顺序分别沉积氟化锂(LiF)和铝至厚度为和形成,从而制造有机发光器件。在前述过程中,分别保持有机材料、氟化锂和铝的沉积速率为和至[实施例4]实验以与实施例3中相同的方式进行,不同之处在于,作为发光层的基质,使用化合物2-8代替制备例14中合成的化合物2-2。[实施例5]实验以与实施例3中相同的方式进行,不同之处在于,作为发光层的基质,使用化合物2-18代替制备例14中合成的化合物2-2。[实施例6]实验以与实施例3中相同的方式进行,不同之处在于,作为发光层的基质,使用化合物2-32代替制备例14中合成的化合物2-2。[实施例7]实验以与实施例3中相同的方式进行,不同之处在于,作为发光层的基质,使用化合物2-76代替制备例14中合成的化合物2-2。[实施例8]实验以与实施例3中相同的方式进行,不同之处在于,作为发光层的基质,使用化合物2-76和2-72代替制备例14中合成的化合物2-2。[比较例2]实验以与实施例3中相同的方式进行,不同之处在于,作为发光层的基质,使用H2代替制备例14中合成的化合物2-2。实验结果示于下表2。[表2]如表2所示,根据本发明的式的化合物衍生物在包括有机发光器件的有机电子器件中可表现出优良的效率和驱动电压特性。[附图标记说明]101:基底201:阳极301:发光层401:阴极501:空穴注入层601:空穴传输层701:电子传输层801:电子注入层当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1