一种催化α‑蒎烯二聚反应的方法与流程
本发明涉及一种催化α-蒎烯二聚反应的方法,具体说来是采用具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40为催化剂,催化α-蒎烯二聚反应的方法。
背景技术:
松节油是世界上最丰富的可再生天然资源之一,我国松节油年产量10万吨,居世界之首,发展对其深加工技术替代不可再生资源具有巨大环境效益和经济价值。α-蒎烯是松节油最主要组分,含量可达80%以上,可提供C10骨架和多元环及桥环、环内双键等,具有活泼的化学反应性能,是许多高附加值精细化工产品的重要原料。传统上,α-蒎烯在酸催化条件下发生聚合反应,主要用于萜烯树脂生产,因而在催化方法研究时,主要集中在如何能增加α-蒎烯聚合度和提高萜烯树脂质量上(Shiwei Liu,Congxia Xie,Shitao Yu,et al.Polymerization ofα-pinene using Lewis acidic ionic liquid as catalyst[J].Catalysis Communications,2009,10,986-988),对其聚合机理认识不深刻,也很少有蒎烯低聚反应研究。直至近些年出现将环萜烯等生物质原料替代化石资源制备高性能可再生燃料的报道,尤其是以蒎烯和柠檬烯等纯碳氢化合物为代表的重要单萜原料,其低聚氢化产物被认为是开发新型航空航天高能量密度燃料(High Energy Density Fuel,HEDF)的理想替代品(Tracy NI,Chen D,Crunkleton DW and Price GL.Hydrogenated monoterpenes as diesel fuel additives[J].Fuel,2009,88,2238-2240;Peralta-Yahya PPOuellet M,Chan R,Mukhopadhyay A,Keasling JD and Lee TS.Identification and microbial production of a terpene-based advanced biofuel[J].Nature Comm,2011,2,483)。因此研究α-蒎烯二聚反应不仅具有理论意义,还有重要的环境效益和商业应用价值。
Harvey等采用离子交换树脂Amberlyst-15、全氟磺酸树脂Nafion和酸性蒙脱土MMT-K-10催化β-蒎烯异构及二聚反应,发现酸性较弱的Amberlyst-15难以催化得到二聚物,而用酸性较强的Nafion和MMT-K-10可获得较高收率的二聚物(B.G.Harvey,M.E.Wright,R.L.Quintana.High-Density Renewable Fuels Based on the Selective Dimerization of Pinenes[J].Energy Fuels.2010,24,267-273;Heather A.Meylemans,Roxanne L.Quintana,Benjamin G.Harvey.Efficient conversion of pure and mixed terpene feedstocks to high density fuels[J].Fuel,2012,97,560-568)。邹吉军等也发现,Al-MCM-41介孔分子筛的酸性是影响β-蒎烯二聚反应催化效果的最直接因素,总酸量越多,酸强度越高,催化效果越好(Jijun Zou,Na Chang,Xiangwen Zhang,et al.Isomerization and dimerization of pinene using Al-incorporated MCM-41mesoporous materials[J].ChemCatChem,2012,4,1289-1297)。上述技术中采用的易分离和可回收利用的固体酸催化剂在很多酸催化反应中取得了一定进展。但同时,树脂类催化材料的化学稳定性,以及蒙脱土和介孔分子筛材料的制备重现性、酸位分布等问题也一直是限制其在酸催化反应工艺中投入实际应用的关键问题。此外,上述背景技术主要的研究对象皆为β-蒎烯的二聚反应,因此,开发一种制备简单、结构明确、稳定高效的催化剂用于生物质松节油 主要成分α-蒎烯的二聚反应,从而为新型生物质基HEDF提供原料,是松脂深加工领域和能源绿色化领域的现实需求。
技术实现要素:
本发明目的是提供一种制备简单、结构确定的,具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40催化剂,应用于α-蒎烯二聚反应制备二聚物的方法,从而为生物质高能量密度航空燃料提供原料。
本发明的技术方案如下:
本发明技术方案中所述的具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40催化剂催化α-蒎烯二聚反应在间歇式常压反应器中进行,原料为α-蒎烯,采用甲苯作为溶剂:
在装有冷凝回流管、温度计的100mL三口烧瓶中加入0.60g具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40催化剂、10mL甲苯,在N2的保护下,机械搅拌并升温至80℃,缓慢滴加10mLα-蒎烯(10-12d/min),滴加完毕后反应16h。反应结束后静置,催化剂沉降至反应器底部,可用倾析的方法分离并直接循环使用,上层反应混合物清液经蒸馏除去溶剂甲苯后,可直接作为后续松节油基生物质高密度燃料的原料。
上述技术方案中所述的具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40催化剂,其制备方法为:
(1)有机中间体合成:
在配有机械搅拌、温度计、恒压滴液漏斗和回流冷凝管的250mL反应瓶中加入0.3mol1,3-丙烷磺内酯和150mL乙酸乙酯,将混合液升温至50℃,缓慢滴加(6~7d/min)与1,3-丙烷磺内酯等物质的量的N-甲基咪唑,滴加完毕后,保温反应2h,减压过滤,滤饼用乙酸乙酯洗涤3次,于110℃下干燥2h,得到中间体1-甲基-3-(3-磺酸基)丙基咪唑盐白色粉末。
(2)具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40的合成
将步骤(1)得到的中间体1-甲基-3-(3-磺酸基)丙基咪唑盐、磷钨酸按物质的量比2:1加入到三口烧瓶(100mL)中,加入20mL去离子水使其溶解,室温(25℃)机械搅拌12h后,加入1/4倍磷钨酸物质的量的氯化锰,同时升高温度至50℃,继续搅拌12h后,减压蒸馏除水,110℃干燥6h,所得灰白色固体为催化剂Mn0.5[MIMPS]2PW12O40。
本发明所制备的具有双酸性的无机-有机复合杂多酸盐Mn0.5[MIMPS]2PW12O40,采用类似酸功能化离子液体的设计思路和制备方法,具有制备方法简单、结构明确的特点;催化剂结构中酸中心和Lewis酸中心分别以共价键和离子键的形式引入,活性组分稳定不易流失。该催化剂在α-蒎烯二聚反应中表现出良好的催化活性和稳定性,催化工艺简单,易于分离和重复使用,为α-蒎烯高附加值利用提供一条有效途径。
附图说明
图1为实施例1所制备催化剂Mn0.5[MIMPS]2PW12O40的制备反应式。
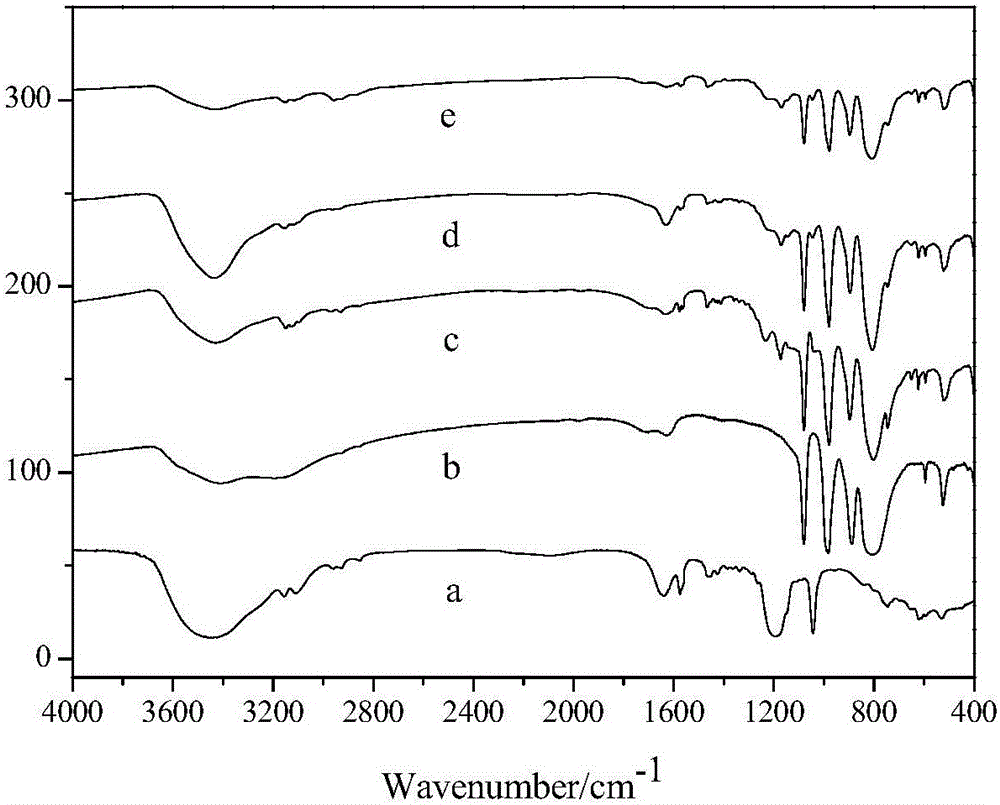
图2为实施例1、对比例2所制备催化剂及其原料以及实施例3回收催化剂的FT-IR谱图;其中(a)MIMPS(b)H3PW12O40(c)H[MIMPS]2PW12O40(d)Mn0.5[MIMPS]2PW12O40(e)回收Mn0.5[MIMPS]2PW12O40。
图3为实施例1所制备催化剂及其原料的XRD谱图;其中(a)H3PW12O40(b)Mn0.5[MIMPS]2PW12O40(c)MnCl2、MIMPS、H3PW12O40三者机械混合物。
图4为实施例1所制备催化剂的TG-DTG谱图。
图5为实施例1所制备催化剂的Py-IR谱图。
具体实施方式
下面结合具体实施例对本发明方法进一步说明,但并不是对本发明的限定。
实施例1
在配有机械搅拌、温度计、滴液漏斗和回流冷凝管的250mL反应瓶中加入0.3mol 1,3-丙烷磺内酯和150mL乙酸乙酯,将混合液升温至50℃,缓慢滴加(6~7d/min)与1,3-丙烷磺内酯等物质的量的N-甲基咪唑,滴加完毕后,保温反应2h,减压过滤,滤饼用乙酸乙酯洗涤3次,于110℃下干燥2h,得到中间体1-甲基-3-(3-磺酸基)丙基咪唑盐白色粉末。
在配有机械搅拌、温度计的三口烧瓶(100mL)中加入2.50mmol磷钨酸,5.00mmol中间体1-甲基-3-(3-磺酸基)丙基咪唑盐,加入20mL去离子水使其溶解,室温(25℃)搅拌12h后,加入1.25mmol氯化锰,同时升高温度至50℃,继续搅拌12h,减压蒸馏除水,110℃干燥6h,得Mn0.5[MIMPS]2PW12O40灰白色固体。其熔点>300℃,不溶于甲苯,不溶于α-蒎烯。如图2(d)所示,IR(KBr,v/cm-1)表征结果为:1574,1463,1181,1086,976,885,811,742;如图2(b)所示的XRD图谱,因阳离子组分取代磷钨酸中的氢质子,导致其衍射峰减弱,证明了Mn0.5[MIMPS]2PW12O40结构的形成;如图3所示的TG-DTG图谱,160℃质量损失为催化剂中所含的结晶水,450℃质量损失为中间体阳离子分解导致,621℃、712℃质量损失为磷钨酸根阴离子分解;采用吡啶-IR(KBr,v/cm-1)表征酸中心类型,如图5所示:1540附近峰指示 中心,1450附近峰指示Lewis中心,证明该催化剂具有双酸性。
表1双酸性无机-有机复合杂多酸盐对α-蒎烯二聚反应的催化性能
实施例2
在装有回流冷凝管、温度计的100mL三口烧瓶中加入0.60g催化剂Mn0.5[MIMPS]2PW12O40,10mL甲苯,在N2的保护下,机械搅拌并升温至80℃,缓慢滴加10mLα-蒎烯(10-12d/min),反应16h。反应结束冷却静置,催化剂沉降到反应器底部,倾析分出上层反应混合物清液,用气相色谱分析其组成,催化反应结果见表1。
实施例3-10
实施例2中与上层有机反应混合物分离的固体催化剂,于同一反应装置中,未经处理直接进行循环使用:加入10mL甲苯,在N2的保护下,机械搅拌并升温至80℃,缓慢滴加10mL(10-12d/min)α-蒎烯,反应16h,反应结束冷却静置,催化剂沉降到反应器底部,倾析分出上层反应混合物清液,用气相色谱分析其组成,如此进行催化剂循环使用实验八次,所得催化剂循环使用结果见表2。
表2双酸型无机-有机复合杂多酸盐催化剂Mn0.5[MIMPS]2PW12O40的重复使用性能
对比例1
在配有机械搅拌、温度计、滴液漏斗和回流冷凝管的250mL反应瓶中加入0.3mol 1,3-丙烷磺内酯和150mL乙酸乙酯,将混合液升温至50℃,缓慢滴加(6~7d/min)与1,3-丙烷磺内酯等摩尔的N-甲基咪唑,滴加完毕后,保温反应2h,减压过滤,滤饼用乙酸乙酯洗涤3次,于110℃下干燥2h,得到中间体1-甲基-3-(3-磺酸基)丙基咪唑盐白色粉末。
在配有机械搅拌、温度计的三口烧瓶(100mL)中加入2.50mmol磷钨酸,2.50mmol中间体1-甲基-3-(3-磺酸基)丙基咪唑盐,加入20mL去离子水使其溶解,室温(25℃)搅拌12h后,取2.50mmol氯化锰加入三口烧瓶中,同时升高温度至50℃,继续搅拌12h,减压蒸馏除水,110℃干燥6h,所得灰白色固体为对比催化剂Mn[MIMPS]PW12O40。其熔点>300℃,不溶于甲苯,不溶于α-蒎烯。
对比例2
在配有机械搅拌、温度计、滴液漏斗和回流冷凝管的250mL反应瓶中加入0.3mol1,3-丙烷磺内酯和150mL乙酸乙酯,将混合液升温至50℃,缓慢滴加(6~7d/min)与1,3-丙烷磺内酯等物质的量的N-甲基咪唑,滴加完毕后,保温反应2h,减压过滤,滤饼用乙酸乙酯洗涤3次,于110℃下干燥2h,得到中间体1-甲基-3-(3-磺酸基)丙基咪唑盐白色粉末。
在配有机械搅拌、温度计的三口烧瓶(100mL)中加入2.50mmol磷钨酸,5.00mmol中间体1-甲基-3-(3-磺酸基)丙基咪唑盐,加入20mL去离子水使其溶解,室温(25℃)搅拌24h,减压蒸馏除水,110℃干燥6h,所得白色固体为对比催化剂H[MIMPS]2PW12O40,其熔点135.6-137.5℃,不溶于甲苯,不溶于α-蒎烯。如图2(c)所示,IR(KBr,v/cm-1)表征结果为:1576,1467,1180,1076,981,888,793,734。
对比例3
在配有机械搅拌、温度计、回流冷凝管的三口烧瓶(100mL)中加入N-甲基咪唑0.10mo1和1-溴代正丁烷0.12mol,机械搅拌下,70℃保温反应36h,减压蒸馏除未反应的1-溴代正丁烷,得到淡黄色透明液体为中间体溴化1-丁基-3-甲基咪唑盐。
在配有机械搅拌、温度计的三口烧瓶(100mL)中加入2.50mmol磷钨酸,5.00mol中间体溴化1-丁基-3-甲基咪唑盐,加入20mL去离子水使其溶解,室温(25℃)搅拌12h后,取1.25mmol氯化锰加入三口烧瓶中,同时升高温度至50℃,继续搅拌12h,减压蒸馏除水,110℃干燥6h,所得灰白色固体为对比催化剂Mn0.5[BMIM]2PW12O40,其熔点>300℃,不溶于甲苯,不溶于α-蒎烯。
对比例4
在装有冷凝回流管、温度计的100mL三口烧瓶中加入0.60g对比例1中制备的催化剂Mn[MIMPS]PW12O40、10mL甲苯,在N2的保护下,机械搅拌并升温至80℃,缓慢滴加10mLα-蒎烯(10-12d/min),反应16h。反应结束冷却静置,催化剂沉降到反应器底部,倾析分出上层反应混合物清液,用气相色谱分析其组成,催化反应结果见表1。
对比例5
在装有冷凝回流管、温度计的100mL三口烧瓶中加入0.60g对比例2中制备的催化剂H[MIMPS]2PW12O40、10mL甲苯,在N2的保护下,机械搅拌并升温至80℃,缓慢滴加10mLα-蒎烯(10-12d/min),反应16h。反应结束冷却静置,催化剂沉降到反应器底部,倾析分出上层反应混合物清液,用气相色谱分析其组成,催化反应结果见表1。
对比例6
在装有冷凝回流管、温度计的100mL三口烧瓶中加入0.60g对比例3中制备的催化剂Mn0.5[BMIM]2PW12O40、10mL甲苯,在N2的保护下,机械搅拌并升温至80℃,缓慢滴加10mLα-蒎烯(10-12d/min),反应16h。反应结束冷却静置,催化剂沉降到反应器底部,倾析分出上层反应混合物清液,用气相色谱分析其组成,催化反应结果见表1。
- 还没有人留言评论。精彩留言会获得点赞!