一种β‑葡萄糖苷酶及其制备方法和应用与流程
本发明属于基因工程技术及生物医药领域,具体涉及一种β-葡萄糖苷酶及其制备方法和应用。
背景技术:
人参的主要活性成分为人参皂苷。人参皂苷是由糖和苷元相连而成的糖苷类化合物,属于三萜类皂苷。人参皂苷中含量最多的是原人参二醇型(protopanaxdiol)皂苷和原人参三醇型(protopanaxtriol)皂苷,原人参二醇型皂苷包括人参皂苷rb1、rb2、rc、rd、f2、rg3、rh2、人参皂苷化合物k(ck)等;原人参三醇型皂苷包括人参皂苷re、rg1、rf、rg2、rh1等。其中人参皂苷rb1、rb2、rc、re、rg1、rd的含量较高,而人参皂苷rg2、rg3、rh1、rh2、ck等在天然人参中含量只有十万分之几或不存在,为稀有人参皂苷。许多药理研究表明,稀有人参皂苷药理效果更好、更容易吸收入血、生物利用度更高。因此,获得大量的稀有人参皂苷具有重要的社会价值,是众多科研人员研究的热点。传统的炮制方法可以提高这些稀有人参皂苷的含量,但其含量仍然非常低。因此,亟待开展新型绿色环保生产工艺的研究以提高这些稀有人参皂苷的转化率和中药材资源的利用效率,降低稀有人参皂苷的生产成本。
常用的水解皂苷的方法有酸水解法、碱水解法和生物转化法。但是它们的水解条件都十分剧烈,不易控制,而且由于在水解过程中能使皂苷元发生脱水、环合、双键位移、取代基位移、构型转化等变化,使水解的副产物增多,目标产物很难得到。更重要的是酸、碱水解法对环境造成很大程度上的危害,所以需要寻找新的转化技术和方法,即能更有效的将低活性、高含量的植物皂苷转化成高活性、天然含量低的单体皂苷,又能做到不给环境造成负担的转化技术和方法。生物转化尤其是酶的区域和立体选择性强、反应条件温和、操作简便、成本较低、公害少,且能完成一些化学合成难以进行的反应,克服了传统酸、碱水解方法的缺陷,又减少了污染物的产生,符合从末端治理向源头控制转化的新型现代生产模式,因而越来越受到重视。
技术实现要素:
本发明的目的是为了解决现有的水解皂苷的方法副产物多且对环境有害的问题,而提供一种β-葡萄糖苷酶及其制备方法和应用。
本发明首先提供一种β-葡萄糖苷酶,是如下1)或2)的蛋白质:
1)序列如seqidno.1所示的氨基酸组成的蛋白质;
2)将1)所示的蛋白质的氨基酸残基序列经过一个或几个氨基酸残基的取代和/或缺失和/或添加且具有糖苷酶活性的蛋白质。
本发明还提供一种编码上述β-葡萄糖苷酶dna,核苷酸序列如seqidno.2所示。
本发明还提供含有上述β-葡萄糖苷酶dna的重组载体。
本发明还提供由上述重组载体转化寄主细胞得到的重组菌。
本发明还提供一种β-葡萄糖苷酶的制备方法,该方法包括:
将seqidno.2所示的dna片段插入表达载体获得重组载体,将重组载体转化寄主细胞,培养转化体,从培养物中获得β-葡萄糖苷酶。
优选的是,所述的方法包括:
步骤一:以提取thermotoganeapolitanadsm4359的基因组dna为模板,用具有seqidno.3所示的核苷酸序列的上游引物和具有seqidno.4所示的核苷酸序列的下游引物进行pcr扩增,得到seqidno.2所示的dna分子;
步骤二:将步骤一获得的dna分子用nhei和ecori进行双酶切,酶切产物与经相同酶切的表达载体用t4连接酶16℃连接过夜,得到重组载体;
步骤三:将步骤二获得的重组载体转化表达寄主菌感受态细胞,得到重组菌;
步骤四:将步骤三得到的重组菌和iptg加入新鲜培养基中,30℃进行诱导发酵16h,离心收集菌体,破碎菌体后离心,得到β-葡萄糖苷酶。
本发明还提供上述β-葡萄糖苷酶在制备人参皂苷rg2或含人参皂苷rg2混合物中的应用。
本发明还提供上述β-葡萄糖苷酶在制备人参皂苷rh1、含人参皂苷rh1混合物、原人参三醇苷元单体或含原人参三醇苷元单体的混合物中的应用。
本发明还提供上述β-葡萄糖苷酶在制备人参皂苷rg3、含人参皂苷rg3混合物、原人参二醇苷元单体或含原人参二醇苷元单体的混合物中的应用。
优选的是,所述的β-葡萄糖苷酶在ph3-10,温度为40℃-100℃条件下反应。
本发明的有益效果
(1)本发明提供的β-葡萄糖苷酶具有良好的热稳定性和较宽的ph酶解范围;
(2)本发明提供的β-葡萄糖苷酶具有高效、专一、副产物少、产率高、产物易于纯化、成本低的优点。
(3)本发明提供的β-葡萄糖苷酶用于生产稀有人参皂苷及其混合物,其具有较强的水解能力,可以将把人参皂苷转化成在人参等植物中微量存在的生物活性更高,更容易被人体高效吸收的稀有人参皂苷,所述稀有人参皂苷的药理效果得到了认证,可以应用在医药健康等多种领域。
附图说明
图1为本发明β-葡萄糖苷酶最适反应温度的折线图;
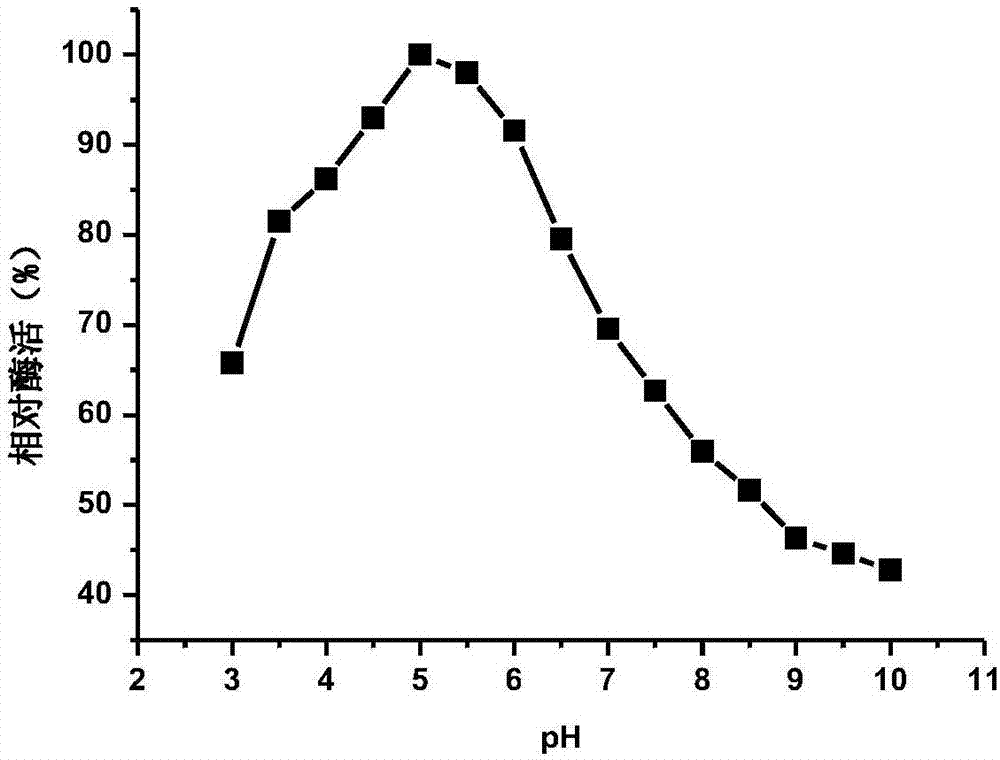
图2为本发明β-葡萄糖苷酶最适反应ph的折线图;
图3为本发明β-葡萄糖苷酶水解人参皂苷re的薄层图;
图4为本发明β-葡萄糖苷酶水解人参皂苷rg1的薄层图;
图5为本发明β-葡萄糖苷酶水解人参皂苷rc、rd、rb1、rb2的薄层图。
具体实施方式
本发明首先提供一种β-葡萄糖苷酶,是如下1)或2)的蛋白质:
1)序列如seqidno.1所示的氨基酸组成的蛋白质;
2)将1)所示的蛋白质的氨基酸残基序列经过一个或几个氨基酸残基的取代和/或缺失和/或添加且具有糖苷酶活性的蛋白质。
上述一个或几个氨基酸残基的取代和/或缺失和/或添加且具有糖苷酶活性的蛋白质为不超过40个氨基酸残基的取代和/或缺失和/或添加。
本发明还提供一种编码上述β-葡萄糖苷酶dna,核苷酸序列如seqidno.2所示。
本发明还提供含有上述β-葡萄糖苷酶dna的重组载体。
本发明还提供由上述重组载体转化寄主细胞得到的重组菌。
本发明还提供一种β-葡萄糖苷酶的制备方法,该方法包括:
将seqidno.2所示的dna片段插入表达载体获得重组载体,将重组载体转化寄主细胞,培养转化体,从培养物中获得β-葡萄糖苷酶。
按照本发明,所述的制备方法步骤如下:
步骤一:以提取thermotoganeapolitanadsm4359的基因组dna为模板,用具有seqidno.3所示的核苷酸序列的上游引物和具有seqidno.4所示的核苷酸序列的下游引物进行pcr扩增,得到seqidno.2所示的dna分子;所述的扩增条件优选为:先95℃预变性4min,然后95℃50s,55℃45s,72℃1min30s,共30个循环,最后72℃延伸10min,回收上述pcr反应产物,进行琼脂糖凝胶电泳检测;
步骤二:将步骤一获得的dna分子用nhei和ecori进行双酶切,酶切产物与经相同酶切的表达载体用t4连接酶16℃连接过夜,得到重组载体;所述的表达载体优选为pet28a载体;
步骤三:将步骤二获得的重组载体转化表达寄主菌感受态细胞,得到重组菌;所述的转化表达寄主菌为大肠杆菌表达菌株,优选为大肠杆菌escherichiacolibl21(de3)菌株;
步骤四:将步骤三得到的重组菌和iptg加入新鲜培养基中,30℃进行诱导发酵16h,离心收集菌体,破碎菌体后离心,得到β-葡萄糖苷酶。
按照本发明,所述的重组菌在加入新鲜培养基前,优选将重组菌单菌落接种至含有50μg/ml卡那霉素的lb液体培养基中,37℃培养12h,收集发酵液,将发酵液按照1%(v/v)的接种量转接至100ml新鲜的lb液体培养基中,37℃培养至od600达到0.6,再在培养基中加入无菌的iptg进行诱导发酵;所述的iptg在培养基中的终浓度优选为0.4mm。
按照本发明,所述的离心收集菌体,破碎菌体后离心的手段为本领域常规的技术,没有特殊限制,优选为:将发酵液离心10min收集菌体,将得到的大肠杆菌菌体用浓度为50mmol/lph值为5.0的醋酸-醋酸钠缓冲溶液吹打悬浮,在冰水浴的条件下进行超声波细胞破碎(200w,工作3s暂停3s,工作100次),离心(15700g,4℃,30min)去除细胞碎片,收集上清液,即为β-葡萄糖苷酶液。
本发明还提供上述β-葡萄糖苷酶在制备人参皂苷rg2或含人参皂苷rg2混合物中的应用,所述的应用方法具体为:将本发明所述的β-葡萄糖苷酶在ph3-10,温度40℃-100℃条件下水解转化人参皂苷单体re或含人参皂苷re的混合物制备得到rg2或含rg2的混合物。
本发明还提供上述β-葡萄糖苷酶在制备人参皂苷rh1、含人参皂苷rh1混合物、原人参三醇苷元单体或含原人参三醇苷元单体的混合物中的应用。所述的应用方法具体为:将本发明所述的β-葡萄糖苷酶在ph3-10,温度40℃-100℃条件下水解转化人参皂苷单体rg1或含人参皂苷rg1的混合物制备得到人参皂苷rh1、含人参皂苷rh1混合物、原人参三醇苷元单体或含原人参三醇苷元单体的混合物。
本发明还提供上述β-葡萄糖苷酶在制备人参皂苷rg3、含人参皂苷rg3混合物、原人参二醇苷元单体或含原人参二醇苷元单体的混合物中的应用。所述的应用方法具体为:将本发明所述的β-葡萄糖苷酶在ph3-10,温度40℃-100℃条件下水解转化人参皂苷单体rc、rd、rb1、rb2单体及含人参皂苷rc、rd、rb1、rb2两种及两种以上的混合物制备得到人参皂苷rg3、含人参皂苷rg3混合物、原人参二醇苷元单体或含原人参二醇苷元单体的混合物。
下面结合具体实施例对本发明做进一步详细的描述,实施例中涉及到的各种反应原料和反应试剂均可通过商业渠道购买得到。
实施例1β-葡萄糖苷酶的制备
提取thermotoganeapolitanadsm4359(来源为德国微生物菌种保藏中心,编号为4359)的基因组dna并以其为模板,用p1和p2为引物,引物由上海生工生物工程技术服务有限公司合成,引物序列如下:
p1:
5’-cgcggcagccatatggctagcatgaagatggaaaaggtgaatga-3’
(forward),下划线表示nhei位点(p1核苷酸序列如seqidno.3所示);
p2:
5’-ttgtcgacggagctcgaattctcacggtttgaatcttctctcct3’
(reverse),下划线表示ecori位点(p2核苷酸序列如seqidno.4所示);
用seqidno.3所示核苷酸序列的上游引物和具有seqidno.4所示的核苷酸序列的下游引物进行pcr扩增,pcr扩增条件为:先95℃预变性4min,然后95℃50s,55℃45s,72℃1min30s,共30个循环,最后72℃延伸10min,回收上述pcr反应产物,进行琼脂糖凝胶电泳检测,结果获得约2170bp大小的片段dna,其核苷酸序列如seqidno.2所示;
将上述获得的pcr产物用nhei和ecori双酶切,酶切产物与经相同酶切的pet28a载体用t4连接酶16℃连接过夜,得到重组载体;
将上述重组载体转化大肠杆菌escherichiacolibl21(de3)感受态细胞,获得重组菌;
将上述获得的thermotoganeapolitanadsm4359β-葡萄糖苷酶重组菌单菌落接种至含有50μg/ml卡那霉素的lb液体培养基中,37℃培养12h,收集发酵液,将发酵液按照1%(v/v)的接种量转接至100ml新鲜的lb液体培养基中,37℃培养至od600达到0.6,再在培养基中加入无菌的iptg,使iptg在培养基中的终浓度为0.4mm,在30℃进行诱导发酵16h。将发酵液4000g离心10min收集菌体。将得到的大肠杆菌菌体用浓度为50mmol/lph值为5.0的醋酸-醋酸钠缓冲溶液吹打悬浮,在冰水浴的条件下进行超声波细胞破碎(200w,工作3s暂停3s,工作100次),离心(15700g,4℃,30min)去除细胞碎片,收集上清液,即为β-葡萄糖苷酶液。
实施例2β-葡萄糖苷酶酶学性质测定
酶活定义为:1min内催化产生1μmol对硝基苯酚(pnp)所需的酶量。
1、β-葡萄糖苷酶的最适反应温度的测定
分别测定ph5.0,40-100℃温度条件的稀释酶液的酶活力,每个温度设三个平行,以酶活力最高者定为100%,以相对酶活力对温度作图。结果如图1所示。
从图1可以看出,本发明所述的β-葡萄糖苷酶的最适反应温度为85℃。
2、β-葡萄糖苷酶的最适反应ph的测定
分别取不同ph的50mm的缓冲液(ph范围3.0-10.0)配置成5mm的pnpg溶液,加入25μl稀释酶液,设置三个平行,测定85℃下各ph值条件下的酶活。以酶活力最高者定义为100%,以相对酶活力对ph作图。结果如图2所示。
从图2可以看出,本发明所述的β-葡萄糖苷酶最适反应的ph为5.0。
实施例3β-葡萄糖苷酶水解转化人参皂苷单体re制备得到rg2
将200μl上述得到的酶液加入200μl人参皂苷re,使re终浓度2mg/ml进行反应,反应在ph值为5.0的条件下进行,85℃反应15-60min。
反应后真空干燥样品并用甲醇重新溶解,进行薄层色谱检测。图3为本发明β-葡萄糖苷酶水解人参皂苷re的薄层图(薄层条件:展开剂为三氯甲烷:甲醇:水=65:35:10,展开后65℃烘干,喷显色剂,显色剂为10%硫酸-乙醇,低温吹干显色剂后于110℃烘至显色,以下实施例均为此条件),从图中可以看出,人参皂苷re在40min就几乎被全部转化为rg2,随着反应时间的延长,人参皂苷re被水解转化为人参皂苷rg2,转化率为99%。
实施例4β-葡萄糖苷酶水解转化人参皂苷单体rg1制备得到人参皂苷rh1或原人参三醇苷元单体
将200μl上述得到的酶液加入200μl人参皂苷rg1,使rg1终浓度2mg/ml进行反应,反应在ph值为5.0的条件下进行,85℃反应25min-8h。
反应后真空干燥样品并用甲醇重新溶解,进行薄层色谱检测。图4为本发明β-葡萄糖苷酶水解人参皂苷rg1的薄层图,从图中可以看出,人参皂苷rg1在25min就几乎被全部转化为rh1,同时有少量原人参三醇苷元(ppt)产生,随着反应时间的延长,到8h时,rh1又全部转化为ppt,转化率为99%。
实施例5β-葡萄糖苷酶水解转化人参皂苷单体rc、rd、rb1、rb2单体制备得到人参皂苷rg3或原人参二醇苷元单体
将200μl上述得到的酶液加入200μl人参皂苷rc、rd、rb1、rb2,使rc、rd、rb1、rb2终浓度2mg/ml进行反应,反应在ph值为5.0的条件下进行,85℃反应5-10h。
反应后真空干燥样品并用甲醇重新溶解,进行薄层色谱检测。图5为本发明β-葡萄糖苷酶水解人参皂苷rc、rd、rb1、rb2的薄层图,从图中可以看出,人参皂苷在酶的作用下转化为rg3和原人参二醇苷元(ppd),并且随着时间的延长产物增加。
实施例6β-葡萄糖苷酶水解转化人参皂苷混合物制备得到人参皂苷rg2、rh1及原人参三醇苷元混合物
将1ml上述得到的酶液加入1ml三醇组人参皂苷(三醇组人参茎叶皂苷或三醇组三七皂苷),使皂苷终浓度5mg/ml进行反应,反应在ph值为5.0的条件下进行,85℃反应6h。
实施例7β-葡萄糖苷酶水解转化人参皂苷混合物制备得到人参皂苷rg3及原人参二醇苷元混合物
将1ml上述得到的酶液加入1ml二醇组人参皂苷(二醇组人参茎叶皂苷或二醇组三七皂苷),使皂苷终浓度5mg/ml进行反应,反应在ph值为5.0的条件下进行,85℃反应6h。
sequencelisting
<110>吉林农业大学
<120>一种β-葡萄糖苷酶及其制备方法和应用
<160>4
<210>1
<211>723
<212>prt
<213>人工序列
<400>1
metlysmetglulysvalasngluileleuserglnleuthrleuglu
151015
glulysvallysleuvalvalglyvalglyleuproglyleuphegly
202530
asnprohisserargvalalaglyalaalaglygluthrhisproval
354045
proargvalglyleuproalaphevalleualaaspglyproalagly
505560
leuargileasnprothrarggluasnaspgluasnthrtyrtyrthr
65707580
thralapheprovalgluilemetleualaserthrtrpasnargglu
859095
leuleuglugluvalglylysalametglyglugluvalargglutyr
100105110
glyvalaspvalleuleualaproalametasnilehisargasnpro
115120125
leucysglyargasnpheglutyrtyrsergluaspprovalleuser
130135140
glyglumetalaserserphevallysglyvalglnserglnglyval
145150155160
glyalacysilelyshisphevalalaasnasnglngluthrasnarg
165170175
metvalvalaspthrilevalsergluargalaleuarggluiletyr
180185190
leuargglyphegluilealavallyslysserlysprotrpserval
195200205
metseralatyrasnlysleuasnglylystyrcysserglnasnglu
210215220
trpleuleulyslysvalleuarggluglutrpglyphegluglyphe
225230235240
valmetserasptrptyralaglyaspasnprovalgluglnleulys
245250255
alaglyasnaspleuilemetproglylysalatyrglnvalasnthr
260265270
gluargargaspgluileglugluilemetglualaleulysglugly
275280285
lysleuserglugluvalleuaspglucysvalargasnileleulys
290295300
valleuvalasnalaproserphelysasntyrargtyrserasnlys
305310315320
proaspleuglulyshisalalysvalalatyrglualaglyalaglu
325330335
glyvalvalleuleuargasngluglualaleuproleusergluasn
340345350
serlysilealaleupheglythrglyglnilegluthrilelysgly
355360365
glythrglyserglyaspthrhisproargtyralaileserileleu
370375380
gluglyilelysgluargglyleuasnpheaspglugluleualalys
385390395400
thrtyrgluasptyrilelyslysmetarggluthrgluglutyrlys
405410415
proargargaspsertrpglythrileilelysprolysleuproglu
420425430
asnpheleuserglulysgluilehislysleualalyslysasnasp
435440445
valalavalilevalileserargileserglygluglytyrasparg
450455460
lysprovallysglyaspphetyrleuseraspaspgluthraspleu
465470475480
ilelysthrvalserarggluphehisgluglnglylyslysvalile
485490495
valleuleuasnileglyserprovalgluvalvalsertrpargasp
500505510
leuvalaspglyileleuleuvaltrpglnalaglyglngluthrgly
515520525
argilevalalaaspvalleuthrglyargileasnproserglylys
530535540
leuprothrthrpheproargasptyrseraspvalprosertrpthr
545550555560
pheproglygluprolysaspasnproglnlysvalvaltyrgluglu
565570575
aspiletyrvalglytyrargtyrtyraspthrpheglyvalglupro
580585590
alatyrglupheglytyrglyleusertyrthrthrpheglutyrser
595600605
aspleuasnvalserpheaspglygluthrleuargvalglntyrarg
610615620
ilegluasnthrglyglyargalaglylysgluvalserglnvaltyr
625630635640
ilelysalaprolysglylysileasplyspropheglngluleulys
645650655
alaphehislysthrargleuleuasnproglygluserglugluval
660665670
valleugluileprovalargaspleualaserpheasnglygluglu
675680685
trpvalvalglualaglyglutyrgluvalargvalglyalaserser
690695700
argasnilelysleulysglythrpheservalglyglugluargarg
705710715720
phelyspro
<210>2
<211>2172
<212>dna
<213>人工序列
<400>2
atgaagatggaaaaggtgaatgaaatcctgtctcaactcactctggaagaaaaagtgaaa60
cttgtagtgggggtaggacttccggggttgtttggaaatccccattcccgggtggcgggt120
gccgctggagagacgcatcctgtcccaagagtgggtcttcctgctttcgttctggcggat180
ggcccagcaggacttagaataaatcctacgagagaaaacgatgagaacacctattacacc240
accgcttttcctgttgagatcatgcttgcttccacctggaacagagagctcctcgaagaa300
gtgggaaaggcaatgggtgaagaggtgagagagtacggtgtggatgtgctccttgctcct360
gcgatgaacatacacagaaatccactttgtggaagaaactttgaatactactcggaagat420
cctgtcctctccggtgagatggcctcttcctttgtgaagggagtccagtcacagggagtt480
ggtgcgtgtataaagcacttcgtggcgaacaaccaggagacgaacagaatggtcgtggac540
acgatcgtgtccgaacgtgctctcagagagatatatctcaggggattcgagatcgctgtg600
aagaaatcaaaaccgtggagcgtgatgagtgcttacaacaaactcaatgggaagtactgc660
tcgcagaacgagtggctcctgaagaaggttctcagggaagaatggggtttcgaaggtttc720
gttatgagcgactggtacgctggagacaatccggtagaacagctcaaagcaggtaacgat780
ctcatcatgcctggaaaggcctaccaggtgaacacagaacgaagagacgaaatagaagag840
atcatggaggccctgaaagaaggaaaactcagcgaagaagttctcgatgaatgtgtaaga900
aacatcttgaaagtccttgtgaacgcaccttctttcaaaaactacagatactccaacaaa960
cccgatcttgagaagcacgcaaaggttgcttatgaagcaggagcagaaggtgttgtcctt1020
ttgaggaacgaagaggctcttcctctttctgaaaactcgaaaatagccctctttggaacg1080
ggccagatcgaaacgataaaaggtggaacaggaagcggcgacacccatccaaggtacgct1140
atttccatccttgaggggataaaagaaaggggtctgaatttcgacgaagaactcgcaaaa1200
acctacgaagactacatcaagaagatgagagaaacagaagagtacaaaccaagaagggat1260
tcctggggaacgatcataaaaccaaaacttccagaaaacttcctttcggagaaggaaata1320
cacaaactggcgaaaaagaacgacgtggcggtcatcgtgatcagcaggatttccggagaa1380
ggctatgacagaaagccggtgaagggagacttttacctttctgacgatgagactgatctc1440
ataaagactgtctccagagagttccatgaacagggcaagaaagtgatcgttcttctcaac1500
ataggaagtcctgttgaggttgttagctggagagatctggtggatgggattctccttgtg1560
tggcaggcagggcaggaaaccggcaggatcgttgccgatgttctcactggaaggatcaat1620
ccatctggaaaacttccaaccacctttccgagagactactctgatgtaccctcctggacc1680
tttcctggagagccaaaggacaatccacagaaggtggtctacgaagaggacatctacgtg1740
ggatacaggtactacgacaccttcggtgtggagccggcgtacgagttcggatacggcctt1800
tcttacacgacctttgagtacagtgacctgaacgtttcgttcgacggtgaaacactcaga1860
gttcagtacagaatagaaaacacgggcggtcgtgcaggaaaggaagtctcgcaggtttac1920
atcaaggcaccgaaaggaaaaatcgacaaacccttccaggaactcaaggcgtttcacaaa1980
accagacttttgaatcctggagagtctgaagaagtggtgcttgagatacctgtcagagat2040
cttgcaagtttcaacggtgaagaatgggttgtcgaagcgggtgaatacgaagtaagggtt2100
ggtgcgtcttcgaggaacataaaacttaaaggaacgttttccgtcggtgaggagagaaga2160
ttcaaaccgtga2172
<210>3
<211>44
<212>dna
<213>人工序列
<400>3
cgcggcagccatatggctagcatgaagatggaaaaggtgaatga
<210>4
<211>44
<212>dna
<213>人工序列
<400>4
ttgtcgacggagctcgaattctcacggtttgaatcttctctcct
- 还没有人留言评论。精彩留言会获得点赞!