KDM5B抑制剂及其制备方法与流程
本发明属于药物化学领域,具体涉及一种kdm5b抑制剂及其制备方法。
背景技术:
癌症是一种严重威胁人类健康与生命的疾病,根据世界卫生组织公布的全球癌症统计数据显示,2012年全球新增约1410万癌症病例和820万死亡病例,其中肺癌是全球最为常见且死亡率最高的癌症。肺癌严重威胁人类健康,由于人口老龄化、吸烟及环境污染等外界因素的影响,肺癌的发生率和死亡率远高于其他癌症。kdm5b作为一类重要的组蛋白去甲基化酶,在肺癌病人组织中高表达,与肺癌的增殖、侵袭与转移、不良预后及多重耐药等密切相关。虽已有kdm5b抑制剂报道,但均未进入临床研发阶段。因此,开发新型肺癌靶向的kdm5b小分子化合物具有重大的创新性和科学意义。
组蛋白赖氨酸特异性去甲基化酶可分为fad依赖的单胺氧化酶lsd1和包含jmjc结构域的jmjd蛋白家族。lsd1特异性去除h3k4、h3k9单双甲基化,进而激活或抑制基因表达,而jmjd家族蛋白依赖fe2+和a-酮戊二酸(2-og)催化去甲基化修饰,包括kdm2a/b,kdm3a/b,kdm4a-e,kdm5a-d(或jarid1a-d),kdm6a-b,jhdm1d,kdm8等多个亚家族,选择性催化不同底物。jmjd家族蛋白jmjc结构域高度保守,有2个组氨酸(his)和1个谷氨酸(glu),在2-og和o2的参与下,无需氢供体即可催化组蛋白甲基赖氨酸生成不稳定的羟基化中间体,同时产生1分子co2和琥珀酸盐,中间体进一步分解生成去甲基化赖氨酸和甲醛。在jmjd家族中,kdm5分为kam5a-d四个亚型,是研究最多的亚家族,特异性去除h3k4甲基化修饰,其中kdm5c/d与肿瘤关联的研究报道较少。去甲基化酶kdm5在病人肺癌组织中高表达,并远高于癌旁组织和正常组织,与肺癌的侵袭与转移密切相关,sirna诱导的kdm5b表达量降低可抑制肿瘤细胞生长、侵袭与转移。kdm5在乳腺癌、前列腺癌、黑色素瘤、胃癌等多种肿瘤组织中过表达,对增殖、周期调控、转移与侵袭、分化等过程发挥关键作用,且其表达水平与肿瘤的恶化程度相关,kdm5表达水平降低或敲出可明显抑制肿瘤的转移与侵袭等。基于kdm5b重要的肿瘤生物学功能及其在克服肿瘤耐药方面的潜力,其已成为重要的表观遗传调控靶点,设计靶向kdm5b的小分子化合物已成为肿瘤靶向药物开发领域的一个重要方向。
kdm5作为一类重要的表观调控去甲基化酶,在肺癌病人组织中高表达,与肺癌的增殖、侵袭与转移及不良预后、多重耐药等密切相关,kdm5敲除或小分子抑制剂可有效清除肺癌耐药细胞,抑制增殖、转移与侵袭、凋亡、分化等过程。虽已有不同结构骨架类型的kdm5a/b抑制剂报道,但因选择性差、作用机制不明确、脱靶效应明显、缺乏细胞内活性或较差的pd/pk属性等,尚无小分子抑制剂进入临床研发阶段。因此,开发高活性高选择性类药属性好的kdm5b小分子化合物是肿瘤靶向药物研究领域的重要方向。
技术实现要素:
有鉴于此,本发明确有必要提供一种新型的kdm5b抑制剂及其制备方法。
本发明提供一种kdm5b抑制剂,化学名称为4,5,6,7-四氢-8h-环戊二烯并[d][1,2,4]三唑并[1,5-a]嘧啶-8-酮,其结构式为
本发明还提供一种kdm5b抑制剂的制备方法,该方法包括步骤:将化合物m(3-氨基-4-氢-1,2,4-三氮唑)与2-氧代环戊烷羧酸甲酯c4h7(co)2och3在酸性溶剂的作用下,于115℃-125℃的温度下进行反应,合成所述kdm5b抑制剂,其中,所述酸性溶剂为冰醋酸、盐酸、硫酸、三氟乙酸或三氟甲磺酸等有机酸。其中,所述kdm5b抑制剂的制备路线如下所示:
基于上述,所述kdm5b抑制剂的制备方法还包括步骤:3-氨基-4-氢-1,2,4-三氮唑与2-氧代环戊烷羧酸甲酯反应完全后得到kdm5b抑制剂混合液;然后除去所述酸性溶剂,得到kdm5b抑制剂半成品;将该kdm5b抑制剂半成品于55℃-65℃干燥,得到kdm5b抑制剂纯品。
因此,本发明提供的kdm5b抑制剂的化学名称为4,5,6,7-四氢-8h-环戊二烯并[d][1,2,4]三唑并[1,5-a]嘧啶-8-酮,其结构式中具有嘧啶并1,2,4–三氮唑的基团结构单元,可以基于嘧啶并1,2,4–三氮唑基本骨架制备系列靶向kdm5b的具有抗肿瘤活性的化合物,同时为寻找靶向kdm5b为靶点的新型抗肿瘤药物开辟新途径。另外,本发明提供的kdm5b抑制剂的合成方法可行,收率高,收率达82%以上。
附图说明
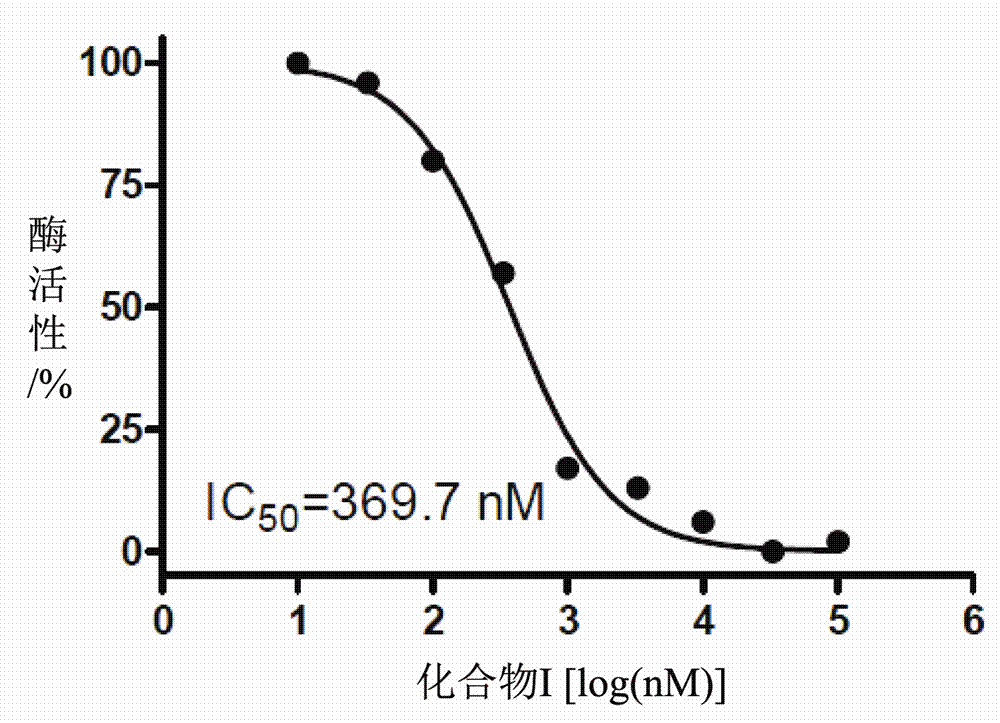
图1是本发明提供的抑制剂对kdm5b酶活性的抑制曲线图。
图2是本发明提供的抑制剂对kdm5b酶活性的抑制曲线图。
具体实施方式
下面通过具体实施方式,对本发明的技术方案做进一步的详细描述。
本发明实施例提供一种kdm5b抑制剂,化学名称为4,5,6,7-四氢-8h-环戊二烯并[d][1,2,4]三唑并[1,5-a]嘧啶-8-酮,结构式为
将1g(约11.89mmol)3-氨基-4-氢-1,2,4-三氮唑加入至反应瓶,再加入20ml冰醋酸,然后缓慢滴加2.22ml(约17.84mmol)2-氧代环戊烷羧酸甲酯并在120℃加热回流,采用tlc监测反应。反应结束后,将反应体系投入冰水中,有大量白色固体析出,直接抽滤得白色固体。丙酮清洗白色固体后,置于60℃烘箱中干燥6h得到上述kdm5b抑制剂纯品。经称量计算可得,产率82.70%,白色固体,熔点211.2-216.6℃;1hnmr(400mhz,dmso-d6)δ13.39(s,1h),8.16(s,1h),2.91(t,j=7.7hz,2h),2.68(t,j=7.3hz,2h),2.17-1.99(m,2h);13cnmr(100mhz,dmso-d6)δ155.83,154.93,152.11,151.43,110.37,31.78,27.21,22.20;hrms(esi):m/zcalcdforc8h9n4o(m+h)+,177.07764;found,177.07671,因此可以确认本发明实施例提供的kdm5b抑制剂的结构如上所示。
抑制活性测定
抑制活性实验方法反应体系为10μl,包括检测缓冲液、组蛋白h3多肽底物、去甲基化酶kdm5b和待测化合物kdm5b抑制剂,反应在384孔板中进行,室温反应60min。先将3μlkdm5b抑制剂和4μl去甲基化酶kdm5b室温预孵育30min,然后再加入3μl组蛋白h3多肽底物,5μl包被有兔抗的受体微珠和5μl组蛋白赖氨酸甲基化一抗;反应体系中dmso含量是1%;室温缓慢振摇孵育30min。最后加入10μl耦联有链霉亲和素的供体微珠(perkin,以1:1稀释1:125检测缓冲液)。在30min内,样品在alphascreen中测量数值(enspirealpha2390multilabelreader,perkinelmer)。
1.1实验方法可行性验证
选用文献报道的kdm5b抑制剂kdoam-25为对照,在用酶量为100ng和h3多肽的浓度为10μm的条件下,利用上述抑制活性实验方法测定抑制剂kdoam-25的活性为36nm,与之前文献报道的活性数据一致,验证了该方法的可行性。其中,报道kdm5b抑制剂kdoam-25的文献名称为“potentandselectivekdm5inhibitorstopscellulardemethylationofh3k4me3attranscriptionstartsitesandproliferationofmm1smyelomacells”,作者为a.tumber等人,报道于《cellchembiol》,2017,24(3):371-380。
1.2本发明实施例提供的kdm5b抑制剂的活性实验
本发明实施例提供的kdm5b抑制剂4,5,6,7-四氢-8h-环戊二烯并[d][1,2,4]三唑并[1,5-a]嘧啶-8-酮,以下简称化合物i。
样品为所合成的kdm5b抑制剂化合物i纯品,样品储备液:称取1-2mg样品于1.5ml的ep管中,用dmso配制成浓度为10mm的溶液,4℃保存,实验过程中,再用dmso稀释至所需浓度。采用上述抑制活性实验方法测定化合物i对kdm5b的抑制活性,检测数据如表1所示。
表1化合物i对kdm5b酶活性的抑制活性结果表
依据表1的数据绘制化合物i对kdm5b酶活性的抑制曲线,如图1和图2所示。从图1中可以看出:化合物i在重复实验1中的半抑制浓度ic50为369.7nm,化合物i在重复实验2中的半抑制浓度ic50为236.3nm,两者的平均ic50为303.0nm,均差为66.7;而且化合物i在重复实验1和2时的抑制曲线图形是一致的,从而可以证明本发明实施例提供的化合物i对kdm5b酶有抑制作用,可以用作kdm5b抑制剂。
最后应当说明的是:以上实施例仅用以说明本发明的技术方案而非对其限制;尽管参照较佳实施例对本发明进行了详细的说明,所属领域的普通技术人员应当理解:依然可以对本发明的具体实施方式进行修改或者对部分技术特征进行等同替换;而不脱离本发明技术方案的精神,其均应涵盖在本发明请求保护的技术方案范围当中。
- 还没有人留言评论。精彩留言会获得点赞!
- SPNP‑I在制备Nav1.7通道工具试剂中的应用的制造方法与工艺
- SPNP‑I在制备Nav1.2通道工具试剂中的应用的制造方法与工艺
- SPNP‑IX在制备Nav1.3通道抑制剂中的应用的制造方法与工艺
- SPNP‑IX在制备Kv4.2通道工具试剂中的应用的制造方法与工艺
- SPNP‑IX在制备Kv4.3通道工具试剂中的应用的制造方法与工艺
- SPNP‑27在制备Nav1.5通道抑制剂中的应用的制造方法与工艺
- SPNP‑27在制备Nav1.3通道抑制剂中的应用的制造方法与工艺
- 一种多肽在制备Nav1.3钠通道工具试剂中的应用的制造方法与工艺
- SPKP‑XI在制备Kv4.2通道抑制剂中的应用的制造方法与工艺
- SGLT‑2糖尿病抑制剂及其中间体的制备方法与流程
- 一种天然气水合物的复合抑制剂及其应用的制作方法与工艺
- 一种作为CYP11B、CYP17、CYP21抑制剂的化合物的制作方法与工艺
- 一种胃酸分泌抑制剂的新用途的制作方法与工艺
- 一种可以表达HIV‑1入侵抑制剂ECLD而抑制HIV‑1感染的重组腺相关病毒的制作方法与工艺
- 一株抑制镰刀菌生长及产毒的粘质沙雷氏菌SerEW01及其应用的制作方法与工艺
- 一种miRNA‑71抑制剂及其用途的制作方法与工艺
- 一种lncRNA-MSR的抑制剂及其应用的制作方法与工艺
- 一种TMSB4基因的抑制剂及其应用的制作方法与工艺
- 吡啶类IRAK4抑制剂、其制备方法及应用与流程
- 一种miRNA‑182抑制剂及其在制备防治心脏移植免疫排斥反应药物中的应用的制造方法与工艺