一种基于生物质多孔碳的C@Fe3O4@Bi复合光催化剂的制备方法及用途与流程
本发明属于环境材料制备技术领域,具体涉及一种基于生物质多孔碳的C@Fe3O4@Bi复合光催化剂的制备方法及用途。
背景技术:
环境污染是现今社会亟待解决的问题,其中大气污染和水污染与我们生活息息相关。抗生素是一类用于治疗各种非病毒感染的药物,常用于医学中的各种病菌的抑制和灭杀,但由于抗生素自身的因素,导致在人或动物体内不能完全吸收,从而大量的抗生素以代谢物甚至原态排入环境中,对水体环境造成污染。许多专家学者通过物理、化学和生物等多种方法来去除解决上述问题,但这些方法效率较低,又易造成二次污染,因此,人们发现一种新型的处理技术-光催化,光催化技术通常以太阳能为光源,成本较低,且通过光催化技术可将环境中的抗生素降解为二氧化碳、水等无机物,因此它是一种理想的绿色环保技术。在众多光催化剂中,二氧化钛(TiO2)具有价格相对低廉、化学性质稳定无毒等优点而被广泛使用,但是它的带隙较宽,光吸收范围相对狭窄,太阳能利用率不高,致使光催化活性降低,铋系光催化剂由于其具有较高的光催化活性而引起了人们的广泛关注。
Bi是一种半金属材料,兼具金属性和非金属性,半金属Bi具有高度各向异性费米表面,较小的有效电子质量,低载流子密度和较长的自由程等优点,使半金属Bi成为研究的热点(J.Zhao,Q.F.Han,J.W.Zhu,X.D.Wu,X.Wang,Synthesis of Bi nanowire networks and their superior photocatalytic activity for Cr(VI)reduction,Nanoscale,6(2014)10062-10070),同时半金属Bi具有较小的带隙能,可作为一个直接等离子体光催化剂(F.Dong,T.Xiong,Y.J.Sun,Z.W.Zhao,Y.Zhou,X.Feng,Z.B.Wu,A semimetal bismuth element as a direct plasmonic photocatalyst,Chem.Commun,50(2014)10386-10389),应用于光催化技术。然而半金属Bi对污染物的吸附能力较弱,为了提高吸附性,本文引入了生物质炭(玉米芯),将其处理为多孔碳材料。多孔碳材料比表面较大,其独特的多孔结构不仅会使光能利用率增加,而且可以增加污染物的吸附。将生物质炭(玉米芯)作为载体材料与半金属Bi复合,可以将污染物吸附到半导体粒子的周围,增加局部浓度加快反应速度,从而进一步提高光催化效率。此外,考虑到经济成本,我们选用磁性材料(Fe3O4)与半金属Bi和由玉米芯所制备的多孔碳材料进行复合,本发明所制备的复合光催化剂具有良好的磁分离特性,极大的提高了回收成本和二次利用率。
技术实现要素:
本文以高温煅烧法为制备手段,制备出一种基于生物质多孔碳C@Fe3O4@Bi复合光催化剂的制备方法,能够很好的降解环境废水中的四环素,具有合成简单和降解速率高的特点。
本发明的技术方案是:
一种基于生物质多孔碳的C@Fe3O4@Bi复合光催化剂的制备方法,包括如下步骤:
步骤1、多孔碳的制备:首先将玉米芯用去离子水洗涤三次,除去表面杂质后烘干,将烘干后的玉米芯置于管式炉内,在N2氛围下煅烧,待反应结束降至室温后取出,得到产物A;
称取适量的KOH,加入适量去离子水,得到KOH溶液,将产物A加入到KOH溶液中,搅拌,随后进行过滤所得物质放入烘箱中烘干,记为产物B;
将产物B置于管式炉中,在N2氛围下进行煅烧,待反应结束降至室温后取出,用去离子水洗涤,所得的样品即为多孔碳(C);
步骤2、修饰后的多孔碳的制备:将步骤1得到的多孔碳浸没于HNO3中,磁力搅拌下进行恒温水浴反应,反应完毕后将固体混合物进行抽滤并洗涤,直至洗涤液呈中性,放入真空烘箱中烘干,所得样品为修饰后的多孔碳;
步骤3、C@Fe3O4@Bi复合光催化剂的制备:将步骤2中制得的修饰后的多孔碳加入到乙二醇中,混匀,然后加入五水合硝酸铋,超声混匀,随后进行磁力搅拌,搅拌结束后加入九水合硝酸铁,继续进行搅拌,搅拌结束,得到混合物D,放入烘箱中烘干;将烘干的混合物D置于管式炉内,在N2氛围下煅烧,最后所得样品即为C@Fe3O4@Bi复合光催化剂。
步骤1中,煅烧玉米芯时的升温速率为4~6℃/min,煅烧温度为400~500℃,煅烧时间为20~60min。
步骤1中,KOH溶液的浓度为1mol/L,KOH的质量与步骤1所得的物质A的质量比为1:2.5~1:3.5。
步骤1中,煅烧产物B时的升温速率为4℃~6℃/min,煅烧温度为600~800℃,煅烧时间为50~120min。
步骤2中,所述HNO3的浓度为63wt.%,磁力搅拌时恒温水浴反应温度为80℃,恒温水浴反应时间为3h。
步骤3中,磁力搅拌时间均为1h。
步骤3中,制备混合物D时,所使用的修饰后的多孔碳、五水合硝酸铋、九水合硝酸铁和乙二醇的用量比为0.3g:1.44g~3.36g:0.8g:20mL。
步骤3中,所述煅烧的升温速率为4℃~6℃/min,煅烧温度为300~600℃,煅烧时间为1~3h。
步骤1~3中,所述的烘干温度均为60℃。
所述的方法制备的C@Fe3O4@Bi复合光催化剂用于光催化降解四环素。
有益效果:
本发明所制备的C@Fe3O4@Bi复合光催化剂的分离回收更加便捷、高效;该C@Fe3O4@Bi复合光催化剂具有较好的光催化活性和稳定性,同时以生物质玉米芯作为碳源,实现了废物合理利用,节省资源。
附图说明
图1:为实施例1的C@Fe3O4@Bi复合光催化剂的XRD图,其中a为实施例9中当五水合硝酸铋的加入量为1.44g时制备的C@Fe3O4@Bi复合光催化剂;b为实施例9中当五水合硝酸铋的加入量为1.92g时制备的C@Fe3O4@Bi复合光催化剂;c为实施例1制备的C@Fe3O4@Bi复合光催化剂;e为为实施例9中当五水合硝酸铋的加入量为2.88g时制备的C@Fe3O4@Bi复合光催化剂;f为实施例9中当五水合硝酸铋的加入量为3.36g时制备的C@Fe3O4@Bi复合光催化剂,其中灰色圆圈代表Fe3O4的XRD峰;
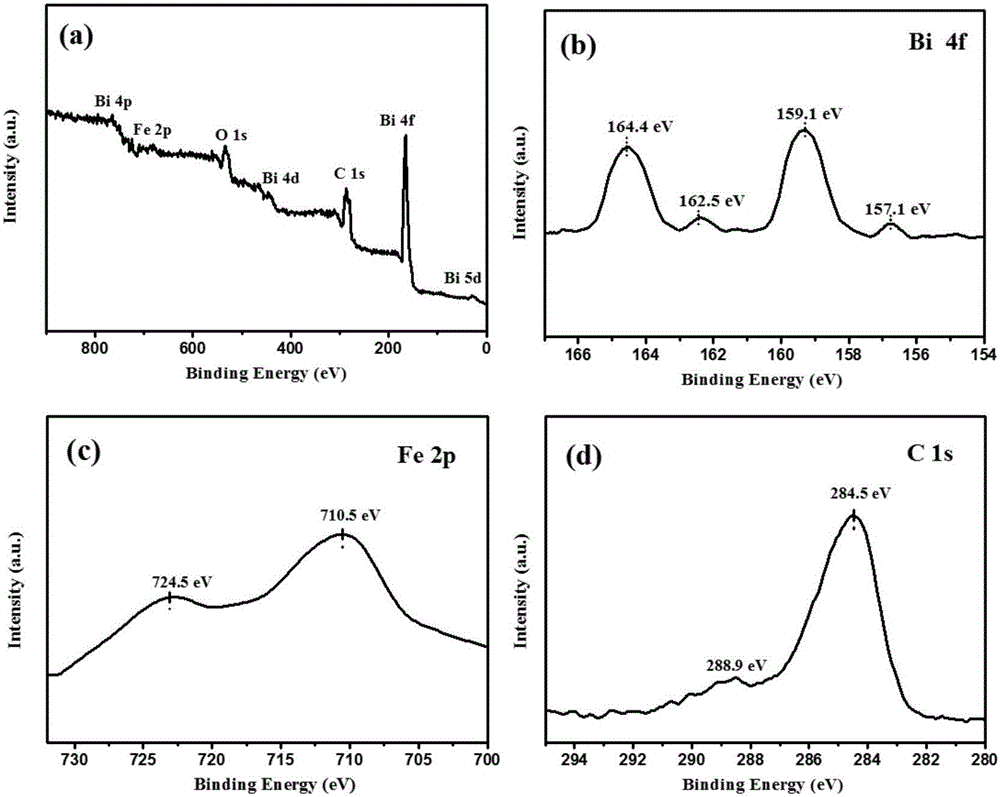
图2:为样品的XPS谱图,其中a为实施例1制备的C@Fe3O4@Bi复合光催化剂,b-d分别为Bi 4f,Fe 2p和C 1s的高分辨XPS谱图;
图3:为不同样品的SEM和TEM图,其中a为实施例1制备的多孔碳的SEM图;b及其插图为实施例1制备的多孔碳的TEM图;c、e为实施例1制备的C@Fe3O4@Bi复合光催化剂的SEM图;d、f为实施例1制备的C@Fe3O4@Bi复合光催化剂的TEM图;
图4:为实施例1所制备的多孔碳的比表面积图,插图为实施例1制备的多孔碳的孔径分布图;
图5:为不同合成样品的DRS图,其中a为实施例10制备的单质Bi光催化剂,b为实施例1制备的C@Fe3O4@Bi复合光催化剂;
图6:为不同合成样品的吸附图,其中a为实施例1制备的多孔碳;b为实施例9中当五水合硝酸铋的加入量为1.44g时制备的C@Fe3O4@Bi复合光催化剂;c为实施例9中当五水合硝酸铋的加入量为2.4g时制备的C@Fe3O4@Bi复合光催化剂;d为实施例9中当五水合硝酸铋的加入量为1.92g时制备的C@Fe3O4@Bi复合光催化剂;e为实施例9中当五水合硝酸铋的加入量为2.88g时制备的C@Fe3O4@Bi复合光催化剂;f为实施例9中当五水合硝酸铋的加入量为3.36g时制备的C@Fe3O4@Bi复合光催化剂;g为实施例10制备的单质Bi光催化剂;
图7:不同煅烧温度的样品在可见光下光降解四环素的考察图,其中a为实施例12中当煅烧温度为400℃时制备的C@Fe3O4@Bi复合光催化剂;b为实施例1中制备的C@Fe3O4@Bi复合光催化剂;c为实施例12中当煅烧温度为600℃时制备的C@Fe3O4@Bi复合光催化剂;
图8:不同样品在可见光下光降解四环素的考察图,其中a为实施例9中当五水合硝酸铋的加入量为3.36g时制备的C@Fe3O4@Bi复合光催化剂;b为实施例9中当五水合硝酸铋的加入量为1.92g时制备的C@Fe3O4@Bi复合光催化剂;c为实施例1制备的C@Fe3O4@Bi复合光催化剂;d为实施例9中当五水合硝酸铋的加入量为2.88g时制备的C@Fe3O4@Bi复合光催化剂;e为实施例9中当五水合硝酸铋的加入量为1.44g时制备的C@Fe3O4@Bi复合光催化剂;f为实施例10制备的Bi光催化剂;
图9:为加入不同捕获剂后,实施例1制备的C@Fe3O4@Bi复合光催化剂光催化降解四环素图,其中TEOA为三乙醇胺;BQ为对苯醌;TEA为叔丁醇;
图10:为实施例1制备的C@Fe3O4@Bi复合光催化剂光催化降解四环素溶液的5次循环光催化效果图。
具体实施方式
下面结合具体实施例对本发明作进一步描述:
光催化活性评价:在D1型光化学反应仪(购自扬州大学教学仪器厂)中进行,将100mL20mg/L的四环素模拟废水加入反应瓶中,再加入磁子和0.1g光催化剂,打开可见光电源和曝气装置进行动态吸附,启动外接超级恒温水浴控制反应体系温度为30℃。到达吸附平衡后进行光照反应,每隔10分钟取样一次,离心分离,测上清液中四环素的浓度,通过C/C0来判断四环素的降解效果。其中,C0为吸附平衡后四环素的浓度,C为反应时间T时四环素的浓度。
实施例1:
(1)多孔碳的制备:首先将玉米芯用去离子水洗涤三次,除去表面杂质后烘干,将烘干后的玉米芯置于管式炉内,以5℃/min的升温速率在在N2氛围下于450℃下煅烧30分钟,待反应结束降至室温后取出。称取适量的KOH,加入去离子水将KOH配制成浓度为1mol/L的溶液,将炭化后的物质加入到KOH溶液中,使KOH与炭化后的物质质量比为1:3.5,搅拌30分钟,随后进行过滤并放入烘箱中干燥。然后将烘干的物质置于管式炉中,以5℃/min的升温速率在在N2氛围下于750℃下煅烧90分钟,待反应结束降至室温后取出,并用去离子水多次洗涤,所得的样品即为多孔碳。
(2)多孔碳的修饰:量取适量的63wt.%的HNO3,然后加入上述多孔碳,使多孔碳浸没于硝酸中,并于80℃下进行水浴加热搅拌,然后将混合物进行抽滤并洗涤,直至溶液呈中性,放入真空烘箱中烘干,所得样品为修饰后的多孔碳。
(3)C@Fe3O4@Bi复合光催化剂的制备:将0.3g修饰后的多孔碳加入到20ml乙二醇中,搅拌均匀,然后加入2.4g五水合硝酸铋,超声混匀,随后进行磁力搅拌,搅拌结束后加入0.8g九水合硝酸铁,继续进行搅拌,搅拌结束,将混合物放入烘箱中于80℃烘箱中干燥。最后将干燥的混合物置于管式炉内,以5℃/min的升温速率在在N2氛围下于500℃下煅烧2h,最后所得样品即为C@Fe3O4@Bi复合光催化剂。
(4)取0.1g(2)中样品在光化学反应仪中进行光催化降解试验,实验结果用紫外分光光度计分析,测得该C@Fe3O4@Bi复合光催化剂对四环素的光降解效果明显,表明该C@Fe3O4@Bi复合光催化剂具有较强的光催化活性。
实施例2:
按实施例1制备工艺同样步骤进行,不同的是步骤(1)中管式炉的温度设置为400℃和500℃来制备不同的炭化碳材料,进而合成C@Fe3O4@Bi复合光催化剂。
实施例3:
按实施例1制备工艺同样步骤进行,不同的是步骤(1)中管式炉的煅烧时间设置为20min和60min来制备不同的炭化碳材料,进而合成C@Fe3O4@Bi复合光催化剂。
实施例4:
按实施例1制备工艺同样步骤进行,不同的是步骤(1)中管式炉的升温速率分别为4℃/min、6℃/min,来制备不同的炭化碳材料,进而合成C@Fe3O4@Bi复合光催化剂。
实施例5:
按实施例1制备工艺同样步骤进行,不同的是步骤(2)中KOH与炭化后的物质的质量比分别为1:2.5和1:3,进而合成C@Fe3O4@Bi复合光催化剂。
实施例6:
按实施例1制备工艺同样步骤进行,不同的是步骤(3)管式炉的温度设置为600℃和800℃来制备不同的多孔碳样品,进而合成C@Fe3O4@Bi复合光催化剂。
实施例7:
按实施例1制备工艺同样步骤进行,不同的是步骤(3)管式炉的时间设置为50min和120min来制备不同的多孔碳样品,进而合成C@Fe3O4@Bi复合光催化剂。
实施例8:
按实施例1制备工艺同样步骤进行,不同的是步骤(3)管式炉的升温速率分别为4℃/min、6℃/min,来制备不同的多孔碳样品,进而合成C@Fe3O4@Bi复合光催化剂。
实施例9:
按实施例1制备工艺同样步骤进行,不同的是步骤(5)中五水合硝酸铋的加入量取1.44g、1.92g、2.88g和3.36g,来制备不同的C@Fe3O4@Bi复合光催化剂,考察五水合硝酸铋的加入量对C@Fe3O4@Bi复合光催化剂光催化活性的影响。
图1图2中证明了本申请所制备的样品确实为C@Fe3O4@Bi复合光催化剂。图5中可以看出,Bi光催化剂在靠近紫外光区域和可见光区域波长为350nm左右具有较强的吸收,表明Bi光催化剂可同时对紫外光和可见光产生响应,而复合之后C@Fe3O4@Bi复合光催化剂在可见光区域具有较强的吸收。在可见光照射下,不同五水合硝酸铋的加入量对C@Fe3O4@Bi复合光催化剂降解的影响结果如图8所示,当五水合硝酸铋的加入量为2.4g时,所制备的样品具有较好的光催化降解四环素性质。当五水合硝酸铋的加入量为1.44g、1.92g、2.88g和3.36g时,所制备的样品都表现出较好的活性。当五水合硝酸铋的加入量小于2.4g时,随着五水合硝酸铋的加入量的增加,C@Fe3O4@Bi复合光催化剂的光催化剂活性逐渐增加,当五水合硝酸铋的加入量大于2.4g时,随着五水合硝酸铋的加入量的增加,C@Fe3O4@Bi复合光催化剂的光催化剂活性逐渐下降,考虑到样品的光催化活性,本申请选取的五水合硝酸铋的加入量为2.4g时制备C@Fe3O4@Bi复合光催化剂。
实施例10:
按实施例1制备工艺同样步骤进行,不同的是步骤(5)中不加入修饰后的多孔碳和九水合硝酸铁,来制备Bi光催化剂,考察单质Bi光催化剂光催化活性,结果如图8所示,纯单质Bi光催化剂光催化活性较低,而复合之后的C@Fe3O4@Bi复合光催化剂的光催化剂活性增大,表明复合体系有利于光催化剂催化降解性能的提升。
实施例11:
按实施例1制备工艺同样步骤进行,不同的是步骤(5)管式炉的升温速率分别为4℃/min、6℃/min,来制备不同C@Fe3O4@Bi复合光催化剂。
实施例12:
按实施例1制备工艺同样步骤进行,不同的是步骤(5)管式炉的温度分别设置为300℃、400℃和600℃,来制备不同C@Fe3O4@Bi复合光催化剂,结果如图7所示,煅烧温度为500℃时制备的C@Fe3O4@Bi复合光催化剂的降级活性最高,当煅烧温度为600℃时制备的C@Fe3O4@Bi复合光催化剂的光催化降解活性小于煅烧温度为400℃时制备的复合光催化剂,考虑到样品的活性,反应物的合理利用和经济价值,本申请选取煅烧温度为500℃制备C@Fe3O4@Bi复合光催化剂。
实施例13:
按实施例1中(4)步骤考察C@Fe3O4@Bi复合光催化剂5次循环光催化降解四环素抗生素废水的光化学稳定性,结果如图10所示,从图10中可以看出5次循环后,C@Fe3O4@Bi复合光催化剂的光催化活性没有明显的下降,说明本申请所制备的C@Fe3O4@Bi复合光催化剂具有良好的光化学稳定性,能够多次的回收利用。
图1为不同C@Fe3O4@Bi复合光催化剂的XRD图,从图中可以看出,所制备的复合光催化剂的衍射峰2θ=22.6°、27.2°、38.1°、39.7°和48.8°分别与标准卡片库中Bi(JCPDS No.44-1246)的(003)、(012)、(104)、(110)和(202)晶面相对应,图中灰色的圆圈代表Fe3O4的衍射峰,说明通过一部煅烧法成功的合成了C@Fe3O4@Bi复合光催化剂。通过图中可以看出,五水合硝酸铋的加入量的不同,对C@Fe3O4@Bi复合光催化剂的衍射峰没有产生影响。图中未发现杂峰,表明C@Fe3O4@Bi复合光催化剂的具有较高的纯度。
图2是样品的XPS谱图,图a为C@Fe3O4@Bi复合光催化剂的XPS图,从图中可以得出合成的复合光催化剂中具有C、O、Fe和Bi等元素,表明复合光催化剂被成功的合成,图b、c和d中分别是Bi 4f、Fe 2p和C 1s的高倍XPS图。在159.1eV和164.4eV处的峰对应于Bi 4f自旋轨道分裂峰,即Bi 4f7/2和5/2,对应于Bi-O键,其主要来源于复合光催化剂表面的一些被空气氧化的物质,而在Bi 4f 7/2和5/2的低结合能侧出现了157.1eV和162.5eV两个肩峰,其主要对应于金属Bi,图c中Fe 2p峰表明合成的复合光催化剂中含有Fe3O4,图d中C1s的两个峰的结合能分别为284.5eV和288.9eV,对应于sp2-C和C=O键。
图3为不同样品的SEM和TEM图,从a、b图中可以看出,成功的制备了基于生物质玉米芯的多孔碳,结合不同样品的比表面数据(图4)可得到,多孔碳的孔径主要约2nm左右。
图4为多孔碳的吸附脱附曲线图,插图为孔径分布,从图中可以看出,这个等温曲线是I型(典型的微孔碳原子)和IV型(介孔材料的特性)的组合,这表明大量的微孔和中孔的存在,这与TEM结果相符合,本申请制备的多孔碳的比表面积达893.4m3g-1,复合之后比表面积下降为58.92m3g-1,由此进一步说明C@Fe3O4@Bi复合光催化剂被成功合成。
图6为不同合成样品的吸附图,从图中可以看出,多孔碳吸附性较好,纯单质Bi光催化剂的吸附性较差,吸附量较小。当Bi光催化剂与C@Fe3O4复合之后,复合光催化剂的吸附性均有所提升,随着五水合硝酸铋的量的增加,复合光催化剂的吸附量,逐渐减小。
图9为加入不同捕获剂后C@Fe3O4@Bi复合光催化剂光催化降解四环素图,从图中可以看出,与不加捕获剂相比,加入不同的捕获剂后,复合光催化剂的光降解四环素性能均有所下降,表明在本申请中,羟基自由基,空穴和超氧自由基均为光催化降解四环素过程中的活性物种。加入三乙醇胺捕获剂之后可以最大程度的抑制复合光催化剂的活性,表明本申请所制备的复合光催化剂在光催化剂降解四环素的过程中,空穴是主要的活性物种。
- 还没有人留言评论。精彩留言会获得点赞!