辨识与鉴别来自栽培种苹果的尿苷二磷酸葡萄糖:根皮素的4’-O-葡萄糖基转移酶的方法与流程
在本发明的一些实施例中,本发明涉及a’-o-糖基转移酶,更具体地但不限于,涉及其用于生产三叶苷和用于改造具有增加的三叶苷含量的细胞和植物的用途。
苹果(malusxdomesticaborkh)是一种农业和经济上重要的食品和饮料来源。苹果积累了高含量的多种酚类抗氧化剂,包括类黄酮和联苯植物抗毒素,其含量可能取决于许多因素,如基因型、发育阶段或生物刺激。
在常见的苯丙烷类衍生物中,苹果的特征在于存在二氢查耳酮(dhcs),这种结构与常见的类黄酮前体密切相关,即查耳酮。与其他类黄酮一样,dhcs表现出多种羟基和葡萄糖基取代模式。3-oh-根皮素、根皮苷(根皮素-2’-o-葡萄糖苷)(图4中的第7号说明)、三叶苷(根皮素-4’-o-葡萄糖苷)(图1和4中的第6号说明)和三羟基根皮素糖苷化衍生物(3-羟基卟啉-4’-o-葡萄糖苷)在苹果植物的茎、叶、花和果实中以不同的组合积累。
dhcs在植物中的生理功能仍未得到解决。他们被认为可以作为叶子中的紫外线过滤剂,或者起到作为有效的抗氧化剂和抗病原体的作用,但仍然缺乏确凿的证据。例如根皮素-在植物界中发现的一种简单的二氢查耳酮,(图1和4中的第5号说明)具有对葡萄糖共同运输蛋白1的抑制活性和已证实的抗氧化活性。据报导,dhcs具有抗癌活性,抑制心血管疾病或成为阿兹海默症的潜在药物。尽管它们作为药物和食品添加剂具有很高的潜力,但由于不具水溶性和低生物利用度,dhcs的使用仍然有限,其部分可通过糖基化来改善。
在根皮素的4’-位置的葡萄糖基化(图1和4中的第5号说明)产生甜味化合物,三叶苷(图1和4中的第6号说明),也称为修饰的二氢查耳酮。先前已在多穗石栎(lithocarpuspolystachyus)的葡萄属(vitis)物种的叶子中检测到三叶苷,并且还存在于不同的苹果属物种中,包括苹果树(m.domestica)和裂叶桑(m.trilobata)。其他二氢查耳酮衍生物也是甜味的,新橙皮苷二氢查耳酮(nhdc)和柚皮苷二氢查耳酮,后者发现在棘豆中积累,比蔗糖每重量单位甜1000倍,并且在加热和大的ph值范围内稳定。二氢查耳酮还被证明可用作苦味阻滞剂和增味剂,在食品、饮料和制药工业中具有多种用途。总共,从30个植物家族中已知大约200种不同的二氢查耳酮,包括山茶属、草莓属、多穗石栎属、豆科植物和柑橘属植物。
达到植物中三叶苷的生物合成途径尚未完全解开。通过查耳酮合成酶催化一分子的4-二氢香豆酰-辅酶a(图1中的第3号说明)和三分子的丙二酰基辅酶a的缩合,得到根皮素(如图1所示)。
葡萄糖基团在4’位置与根皮素的连接被认为是形成三叶苷的最后一步。欧诺等人,[欧诺等人,美国国家科学院院刊,美国(2006)103:11075-11080]已经指出,查耳酮的糖基化可以通过从金鱼草(aelrrhinummajus)分离的重组查耳酮4’-o-葡萄糖基转移酶催化。最近,已显示来自细菌(地衣芽孢杆菌)的功能性表现的udp-葡萄糖基转移酶(ugt)催化根皮素转化为三叶苷[佩迪等人,应用及环境微生物学期刊,(2013)79,3516-3521]。
美国专利申请号us20110030098公开了通过用编码具有根皮素糖基转移酶活性的多肽的多核苷酸转化植物细胞或植物来生产具有增加的根皮苷或根皮素糖基转移酶活性的植物细胞或植物的方法。us200110030098还提供了经遗传修饰以包含及/或表现多核苷酸的宿主细胞、植物细胞和植物。
技术实现要素:
根据本发明的一些实施例的一目的,提供一种产生三叶苷的方法,所述方法包括:在允许形成三叶苷的多个条件下,使包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列的一多肽与根皮素和尿苷二磷酸葡萄糖进行接触,从而产生三叶苷。
根据本发明的一些实施例的一目的,提供一种制备产生三叶苷的一植物的方法,所述方法包括:在所述植物中上调包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列的一多肽的表现量,其中所述植物包括根皮素和尿苷二磷酸葡萄糖,从而制备所述植物。
根据本发明的一些实施例的一目的,提供一种基因转殖的植物或植物细胞,包括:编码一多肽的一外源核酸序列,所述多肽包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列。
根据本发明的一些实施例的一目的,提供一种产生一基因转殖的植物的方法,所述方法包括:向所述植物的一细胞中引入核酸建构体,所述核酸建构体包含编码一多肽的一核酸序列,所述多肽包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列。
根据本发明的一些实施例的一目的,提供一种如本发明的一些实施例所述的细胞的细胞裂解物。
根据本发明的一些实施例的一目的,提供一种组合物,包括如本发明的一些实施例所述的细胞裂解物的三叶苷。
根据本发明的一些实施例的一目的,提供一种组合物,包括如本发明的一些实施例所述的方法所产生的三叶苷。
根据本发明的一些实施例,所述方法是在体内进行。
根据本发明的一些实施例,所述体内是在一植物细胞内。
根据本发明的一些实施例,所述体内是在一微生物内。
根据本发明的一些实施例,所述微生物选自酵母菌和细菌所组成的群组中。
根据本发明的一些实施例,所述方法是在体外进行。
根据本发明的一些实施例,所述体外是一无细胞系统。
根据本发明的一些实施例,所述方法更包括:纯化所述三叶苷。
根据本发明的一些实施例,所述上调包括基因工程。
根据本发明的一些实施例,所述上调包括:与表现所述多肽的一植物杂交,所述多肽包含与seqidno:8至少90%相同的氨基酸序列。
根据本发明的一些实施例,所述植物细胞包含一受质,所述受质选自下列所组成的群组:根皮素、三叶苷、根皮苷、槲皮素、柚皮素和叶黄素。
根据本发明的一些实施例,所述植物细胞包含一尿苷二磷酸葡萄糖受质。
根据本发明的一些实施例,所述植物细胞包含一根皮素受质和一尿苷二磷酸葡萄糖受质。
根据本发明的一些实施例,当所述基因转殖的植物或植物细胞包含所述根皮素与所述尿苷二磷酸葡萄糖时,所述基因转殖的植物或植物细胞产生三叶苷。
根据本发明的一些实施例,所述的方法或所述的基因转殖的植物或植物细胞还包括:选择所述细胞或所述植物以表现所述seqidno:8或与所述seqidno:8至少90%相同的所述多肽的产物。
根据本发明的一些实施例,所述的方法或所述的基因转殖的植物或植物细胞还包括:选择具有a’-o-糖基转移酶活性的所述细胞或所述植物。
根据本发明的一些实施例,所述的方法或所述的基因转殖的植物或植物细胞还包括:选择产生所述三叶苷的所述细胞或所述植物。
根据本发明的一些实施例,所述植物细胞选自下列所组成的群组之中:一叶子的一细胞、一花的一细胞、一果实的一细胞。
根据本发明的一些实施例,所述植物属于蔷薇科。
根据本发明的一些实施例,所述植物选自下列所组成的群组之中:苹果、海棠、三叶海棠、复叶葡萄、甘葛、多穗石柯、白檀、墨西哥菝葜以及草莓。
根据本发明的一些实施例,所述的细胞裂解物包括三叶苷。
根据本发明的一些实施例,所述组合物为一食品、一饲料或一饮料产品。
根据本发明的一些实施例,所述组合物为选自下列所组成的群组之中的一形式:颗粒形式、粉末形式、糊剂形式和液体形式。
根据本发明的一些实施例,所述组合物选自下列所组成的群组之中:果冻、酱汁、糖浆、调味品、酒类、谷物、薄片饼、条状物、零食、涂抹酱、糊状物、浸渍物、面粉、粥、饮料、输液、汤剂、药酒、萃取物以及果汁。
根据本发明的一些实施例,所述组合物选自下列所组成的群组之中:果干、新鲜水果、冷冻水果、烘焙水果、煮沸的水果、蒸水果、搅拌干果和烤水果。
根据本发明的一些实施例,所述组合物被配制成一药物组合物。
根据本发明的一些实施例,所述药物组合物用于治疗一致癌疾病。
根据本发明的一些实施例,所述药物组合物用于治疗一心血管疾病。
根据本发明的一些实施例,所述药物组合物用于治疗糖尿病。
根据本发明的一些实施例,所述药物组合物用于治疗神经退化性疾病。
除非另有定义,否则本文使用的所有技术及/或科学术语具有与本发明所属领域的普通技术人员通常理解的相同的含义。虽然在本发明实施例的实施或测试中可以使用与本文所述方法和材料类似或等同的方法和材料,下面描述的方法和/或材料为例示性的。如果发生矛盾,专利说明书包括其定义,将受到限制。另外,这些材料、方法和实例仅是说明性的,并非用以限制。
附图说明
这里仅通过举例的方式参考附加的图式来描述本发明的一些实施例。现在具体参照附图详细说明,强调的是,所示出的细节是作为例示并且出于对本发明实施例的说明性讨论的目的。就这一点而言,对于本领域技术人员而言,利用附图进行的描述对于可以如何实践本发明的实施例是显而易见的。
在附图中:
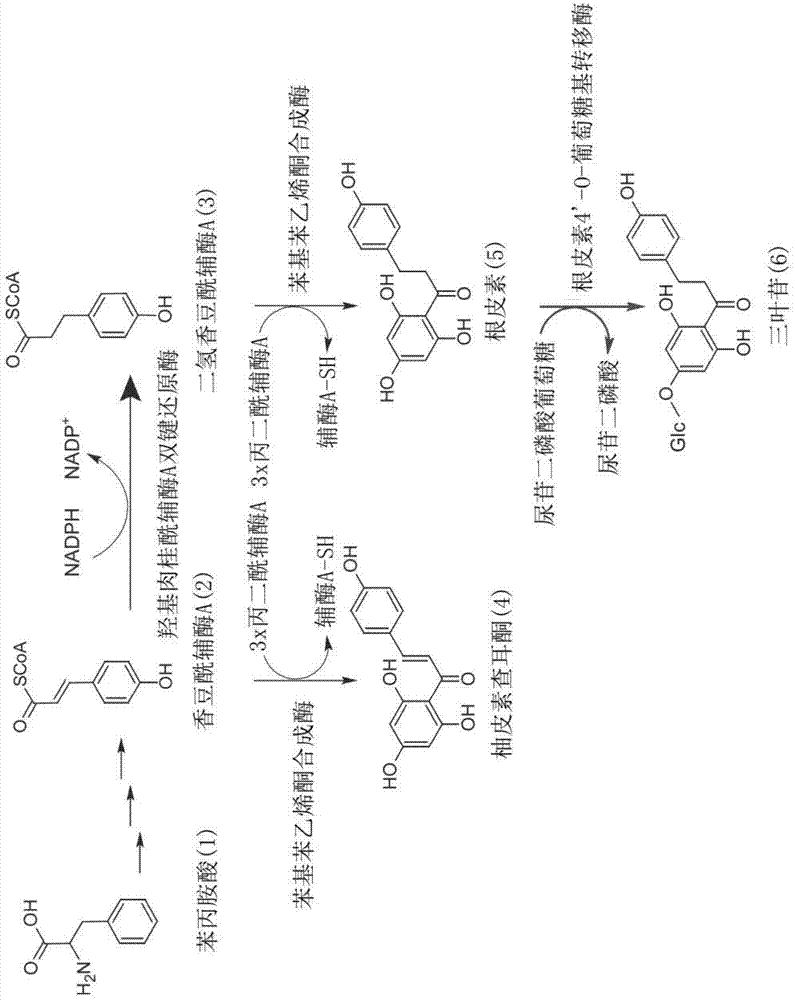
图1是提出的生物合成途径的示意图,其产生苹果中的二氢查耳酮糖苷。chs,苯基苯乙烯酮合成酶;chi,查耳酮异构酶;hcdbr,羟基肉桂酰辅酶a双键还原酶;mdph-4’-ogt,根皮素-4’-o-葡糖基转移酶,用红色字体显示。
图2是植物的推定的氨基酸序列和一些细菌udp-葡萄糖基转移酶蛋白的演化树示意图。本研究中鉴定根皮素-4’-o-葡糖基转移酶蛋白用粗体下标线文字突出显示。推导方法重复进行1000次。
图3a至3h是图解说明重组根皮素-4’-o-葡糖基转移酶与根皮素(图1中的第5号说明)和udp-葡萄糖反应产物的质谱联用-液相色谱法分析。(图3a)重组根皮素-4’-o-葡糖基转移酶与根皮素作为受质的酶活性。(图3b)煮沸的重组根皮素-4’-o-葡糖基转移酶与udp-葡萄糖作为共同受质的酶活性。(图3c)根皮素水平。(图3d)三叶苷(图1中的第6号图示)水平。(图3e)根皮苷(图4中的第7号图示)水平。(图3f)根皮素的质谱。(图3g)三叶苷的质谱。(图3h)根皮苷的质谱。质荷比=质量-电荷比。插图显示了根皮素、三叶苷和根皮苷的结构。
图4说明his标记的亲和层析纯化的重组根皮素-4’-o-葡糖基转移酶的受质特异性。值得注意的是,对于含有500奈克的酶于1小时的反应,将根皮素的活性任意设定为100%。辨识了分析出的多种受质。酶测定在含有50mm三羟甲基氨基甲烷盐酸盐(tris-hcl)于ph7.5和2mm2-巯基乙醇,50μm受质和2mmudp-葡萄糖的缓冲液中进行。
图5a至5d图解说明重根皮素-4’-o-葡糖基转移酶蛋白的根皮素-4’-o-糖基转移酶活性。所述图显示了使用根皮素作为变量的共同受质(图5a)或使用udp-葡萄糖作为变量的共同受质(图5b)的根皮素-4’-o-葡糖基转移酶的稳态动力学测量。用根皮素和udp-葡萄糖受质测定根皮素-4’-o-葡糖基转移酶活性的最适ph值(图5c)和最适温度(图5d)。
图6是说明根皮素-4’-o-葡糖基转移酶在不同苹果品种金冠(goldendelicious)组织中的表达模式的图。通过实时qrt-pcr分析测量根皮素-4’-o-葡糖基转移酶转录物含量的定量并相对于肌动蛋白标准化。用不同字母标记的多个条状体表示由jmp统计软件确定的显着差异(p≤0.05;tukey-kramer确实显着差异检验)。使用三个生物学方法重复进行所有分析。
图7显示了根皮素-4’-o-葡糖基转移酶(udp-葡萄糖:类黄酮7-o-葡萄糖基转移酶)的开放读取区域和编码蛋白的序列。值得注意的是,根皮素-4’-o-葡糖基转移酶的核酸序列如seqidno:7所示,根皮素-4’-o-葡糖基转移酶的氨基酸序列如seqidno:8所示。
图8显示了来自苹果的根皮素-4’-o-葡萄糖基转移酶(udp葡萄糖:类黄酮7-o-葡萄糖基转移酶,aax16493)(在seqidno:8中列出),栽培种苹果花青素5,3-o-葡萄糖基转移酶(xm_008382233)的氨基酸序列的多重比对。(在seqidno:10中列出)和来自地衣芽孢杆菌的udp-葡萄糖基转移酶(wp_003182014)(在seqidno:9中列出)[pandeyrp等人,(2013),同上)]。
图9是说明纯化的重组根皮素-4’-o-葡萄糖基转移酶的sds-page分析的照片。泳道1:分子量标记;泳道2:ni-nta基质层析后来自重组根皮素-4’-o-葡萄糖基转移酶的可溶性提取物。
图10a至10f是说明重组根皮素-4’-o-葡萄糖基转移酶与三叶苷或根皮苷和udp-葡萄糖的反应产物的质谱联用-液相色谱法分析的图。(图10a)重组根皮素-4’-o-葡萄糖基转移酶与根皮苷作为受质的酶活性。(图10b)煮沸的重组根皮素-4’-o-葡萄糖基转移酶与根皮苷的酶活性。(图10c)重组根皮素-4’-o-葡萄糖基转移酶与三叶苷作为受质的酶活性。(图10d)煮沸的重组根皮素-4’-o-葡萄糖基转移酶与三叶苷的酶活性。(图10e)根皮苷二-o-葡萄糖苷的质谱。(图10f)三叶苷二-o-葡糖苷的质谱。质荷比=质量-电荷比。s=受质;p=产物。
图11a至11e是说明重组根皮素-4’-o-葡萄糖基转移酶与柚皮素和udp-葡萄糖的反应产物的质谱联用-液相色谱法分析的图。(图11a)重组根皮素-4’-o-葡萄糖基转移酶的酶活性,其中柚皮素作为受质,udp-葡萄糖作为共同受质。(图11b)煮沸的重组根皮素-4’-o-葡萄糖基转移酶与柚皮素作为受质的酶活性。(图11c)柚皮素水平。(图11d)柚皮素-7-o-葡萄糖苷水平。(图11e)柚皮素-7-o-葡萄糖苷的质谱。质荷比=质量-电荷比。
图12a至12d是说明重组根皮素-4’-o-葡萄糖基转移酶与槲皮素和udp-葡萄糖的反应产物的质谱联用-液相色谱法分析的图。(图12a)重组根皮素-4’-o-葡萄糖基转移酶的酶活性,其中槲皮素作为受质,udp-葡萄糖作为共同受质。(图12b)用槲皮素作为受质的煮沸的重组根皮素-4’-o-葡萄糖基转移酶的酶活性。(图12c)槲皮素-7-o-葡糖苷水平。(图12d)槲皮素-7-o-葡糖苷的质谱。质荷比=质量-电荷比。
具体实施方式
在本发明的一些实施例中,本发明涉及a’-o-葡萄糖基转移酶,更具体地但不限于,涉及其用于生产三叶苷和用于改造具有增加的三叶苷含量的细胞和植物的用途。
参考附图和后附的描述可以更好地理解本发明的原理和操作。
在详细解释本发明的至少一个实施例之前,应理解本发明不一定限于应用于以下描述中阐述的或通过实施例列举的说明的细节。本发明能够具有其他实施例或者能够以各种方式执行或实施。而且,应当理解的是,这里采用的措辞和术语是为了描述的目的,不应该被认为是限制性的。
苹果(malusxdomesticabrokh)是世界上最重要的农业和经济重要的食品和饮料来源。苹果的许多有益健康特性被认为是由于多酚代谢物,包括各种二氢查耳酮(dhcs)。dhcs表现出多种羟基和葡萄糖基取代模式,并在苹果植物的茎、叶、花和果实中以不同的组合积累。尽管许多植物物种中已知许多参与多酚生物合成的基因和酶,但导致甜味二氢查耳酮(例如三叶苷)生物合成的特定反应尚不清楚。
本发明人已经鉴定了一种新的位置特异性葡萄糖基转移酶,其在udp-葡萄糖存在下糖基化根皮素以形成三叶苷。所述葡萄糖基转移酶命名为苹果属udp-葡萄糖:根皮素a’-o-葡萄糖基转移酶(mdph-4’-ogt)。从栽培种苹果属的叶中被复制并表征编码根皮素4’-o-葡萄糖基转移酶的基因。进一步发现根皮素4’-o-葡萄糖基转移酶在苹果果实和叶片中表现,与苹果组织中三叶苷的积累一致。这种新基因可用于代谢基因工程细胞和作物植物,以含有三叶苷作为天然甜味剂、营养补充剂,用于改善植物抗病性和治疗性。
因此,根据本发明的一幕的,提供了产生三叶苷的方法,所述方法包括:使包含与seqidno:8至少90%相同并具有a’-o-葡萄糖基转移酶活性的氨基酸序列的一多肽与根皮素和尿苷二磷酸葡萄糖进行接触,从而产生三叶苷。
本发明进一步提供了制备产生三叶苷的植物的方法,所述方法包括:在所述植物中上调包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列的一多肽的表现量,其中所述植物包括根皮素和尿苷二磷酸葡萄糖,从而制备所述植物。
本文所用术语“三叶苷”是指二氢查耳酮糖苷,也称为根皮素-4’-o-葡萄糖苷或1-丙酮,1-(4-(β-d-吡喃葡萄糖氧基)-2,6-二羟基苯基)-3-(4-羟基苯基),其结构如下所示(式i):
本文所用术语“根皮素”是指二氢查耳酮,也称为二氢柚皮素、根皮素或3-(4-羟基苯基)-1-(2,4,6-三羟基苯基)-1-丙酮,其结构如图所示。下面(式ii):
本文所用的术语“udp-葡萄糖”是指尿苷二磷酸葡萄糖,也称为尿嘧啶-二磷酸葡萄糖,为一核苷酸糖,其结构如下所示(式iii):
本文所用的术语“具有4’-o-葡萄糖基转移酶活性”是指葡萄糖基团在4-羟基团上与受质的连接。
三叶苷生物合成通常需要共同受质为根皮素和udp-葡萄糖,并且涉及葡萄糖基团与4-羟基团上的根皮素的连接。葡萄糖基团在4-羟基团上与根皮素的连接通常通过具有4’-o-葡萄糖基转移酶活性的酶实现。这种葡萄糖基转移酶催化糖部分(例如葡萄糖)从活化的核苷酸糖(例如udp-葡萄糖)转移到受体分子的4-羟基(例如根皮素)。本发明人已发现所述酶为苹果属udp-葡萄糖:根皮素4’-o-葡萄糖基转移酶(在本文中也称为mdph-4’-ogt)。
根据一个实施例,催化三叶苷生物合成的多肽包含与seqidno:8至少90%相同的氨基酸序列。根据一些实施例,氨基酸序列与seqidno:8至少90%同源。
根据一个实施例,催化三叶苷生物合成的多肽包含具有至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%的氨基酸序列与seqidno:8同源性或同一性。
根据一个实施例,催化三叶苷生物合成的多肽包含具有至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、97%、至少98%、至少99%或100%的氨基酸序列与seqidno:8的同源性或同一性。
根据一个具体实施例,催化三叶苷生物合成根皮素4’-o-葡萄糖基转移酶多肽的氨基酸序列如seqidno:8所示。在一些情况下,seqidno:8也称为udp-葡萄糖:类黄酮7-o-葡萄糖基转移酶(如登录号aax16493中所述)。
根据本发明,同源序列包括直系同源序列和旁系同源序列。
如本文所用术语“旁系同源”涉及导致旁系同源基因的物种的基因组内的基因重复。如本文所用术语“直系同源”涉及由于先祖关系而在不同生物中的同源基因。因此,直系同源物是衍生自给定两个物种的最后共同祖先中的单个祖先基因的进化对应物,因此很大的可能性具有相同功能。
鉴定单子叶植物物种中的直系同源物的一种选择是通过进行相互blast搜索。这可以通过涉及针对任何序列数据库对感兴趣序列进行比对的第一次比对来完成,例如公众可获得的ncbi数据库,其可以在以下处找到:ncbi.nlm.nih.gov。如果寻找水稻中的直系同源物,则可以针对例如来自栽培稻品种日本晴(nipponbare)的28,469个全长cdna复制体(例如ncbi获得的)来对感兴趣的序列进行比对。可以过滤比对结果。然后将过滤结果或未过滤结果的全长序列针对从中获得目标序列的生物体的序列进行回头比对(第二次比对)。然后比较第一次和第二次比对的结果。当在第一次比对中导致最高得分(最佳命中)的序列在第二次比对中识别出查询序列(原始感兴趣序列)作为最佳命中时,识别出直系同源物。使用相同的理性(paralogue)(同一生物体中基因的同源物)分析可以发现。在大序列族的情况下,可以使用clustalw程序[ebi.ac.uk/tools/clustalw2/index.html],然后使用演化树(wikipedia.org/wiki/neighbor-joining)有助于可视化群集。
可以使用计算成对序列比对的任何同源性比较软件来确定同源性(例如同源性百分比、序列同一性和序列相似性)。
如本文所用术语,“序列同一性”或“同一性”在上下文中两个核酸或多肽序列包括提及的两个序列中的残基,其在比对时是相同的。当使用序列同一性百分比参考蛋白质时,认识到不相同的残基位置通常因氨基酸的保留取代而不同,其中氨基酸残基取代具有相似化学性质的其他氨基酸残基(例如电荷或疏水性)因此不改变分子的功能特性。当序列在保留取代方面不同时,可以向上调整序列同一性百分比以校正取代的保留性质。通过这种保留取代而不同的序列被认为具有“序列相似性”或“相似性”。进行这种调节的方法是本领域技术人员所熟知的。通常,这涉及将保留取代评分作为部分而非完全序列错配参考,从而增加序列同一性百分比。因此,例如当给予相同的氨基酸得分为1并且给予非保留取代而得分为零时,保留取代被给予0和1之间的得分。例如,根据henikoffs和henikoffjg的算法计算保守置换的得分。[来自蛋白质块的氨基酸取代基质,美国国家科学院院刊,美国,1992,89(22):10915-9]。
可以使用任何同源性比较软件确定同一性(例如同源性百分比),包括例如国家生物技术信息中心(ncbi)的blastn软件,例如通过使用默认参数。
根据本发明的一些实施例,同一性是整体同一性,即与本发明的整个氨基酸或核酸序列的同一性,而不是其部分。
根据本发明的一些实施例,术语“同源性”或“同源的”是指两个或更多个核酸序列的同一性,或两个或多个氨基酸序列的同一性,或氨基酸序列与一个或多个核酸序列的同一性。
可以使用wo2014/102774中描述的各种已知序列比较工具确定两个或更多个序列之间的同源性或同一性程度。
可以使用的局部比对工具包括但不限于tblastx算法,其将核苷酸查询序列(两条链)的六框架概念转译产物与蛋白质序列数据库进行比较。预设参数包括:最大目标序列:100;预期阈值:10;字体大小:3;查询范围内的最大匹配数:0;评分参数:matrix-blosum62;过滤器和屏蔽:过滤器-低复杂性区域。
通常,产生三叶苷的方法可以在体外或体内进行。应当理解,本发明的一些步骤可以在体外进行,而其他步骤可以在体内进行。这确认为完全在本领域技术人员的能力范围内。
当所述方法在体内进行时,所述方法使用至少一种表现本发明酶的宿主细胞。
适于产生三叶苷的宿主细胞包括例如微生物(例如细菌、真菌、酵母细胞)、昆虫细胞、哺乳动物细胞和植物细胞。
根据具体实施例,宿主细胞是植物细胞或微生物。
根据一个实施例,产生三叶苷的方法在外源表现多肽的细胞中进行,所述多肽包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列。
根据一个实施例,包含与seqidno:8至少90%相同并且具有4’-o-葡萄糖基转移酶活性的氨基酸序列的多肽也可以由细胞内源表现,在这种情况下,多肽表现是与不表现外源多肽的细胞相比上调至少约5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%或更多。
根据一个实施例,本发明多肽的表现包括通过向细胞中引入外源核酸序列来实现包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列。所述外源核酸序列包括一多肽其包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列。
如本文所用术语“多肽”是指线性有机聚合物,其由通过直链中的肽键键合在一起的大量氨基酸残基组成,形成蛋白质分子的一部分(或全部)。多肽的氨基酸序列是指包含多肽或其部分的氨基酸的线性连续排列。
如本文所用术语“多核苷酸”是指单股或双股核酸序列,其以rna序列、互补多核苷酸序列(cdna)、基因组多核苷酸序列及/或复合多核苷酸序列(例如,上述的组合)的形式分离和提供。
如本文所用术语“表现”是指mrna和任选的多肽的表现水平。
如本文所用术语“内源的”是指在野生型基因组位置(例如植物细胞、微生物)和野生型等级的细胞内天然表现的任何化合物、多核苷酸或多肽。
如本文所用术语“外源的”被期待是指可能不在细胞内天然表现的多核苷酸或多肽(例如来自不同物种的核酸序列)或在细胞中过表现的多核苷酸或多肽(例如植物细胞、微生物)。
当在细胞中表达外源多核苷酸时,可以以稳定或瞬时方式将外源多核苷酸引入植物中,以产生核糖核酸(rna)分子及/或多肽分子。应注意的是,外源多核苷酸可包含与细胞的内源核酸序列(例如植物细胞、微生物)相同或部分同源的一核酸序列。
适用于本发明方法的多核苷酸包括但不限于包含编码与seqidno:8至少90%相同的氨基酸序列的核酸序列的多核苷酸,或其功能同源物。
上述多肽的功能同源物也适用于本文所述的方法。功能同源物是与参考多肽具有序列相似性的多肽,并且其执行参考多肽的一种或多种生物化学或生理学功能。因此,本文所述酶的功能同源物是与参考酶具有序列相似性的多肽,并且其能够催化本发明方法的相同步骤或部分步骤作为参考酶。根据一个实施例,本文所述酶的功能同源物是能够具有4’-o-葡萄糖基转移酶活性的多肽。
根据本发明的一些实施例,本发明的多核苷酸包含编码一多肽的一核酸序列,所述多肽包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列。
根据一实施例,本发明的多核苷酸包含与seqidno:7至少90%相同的一核酸序列。根据一些实施例,所述多核苷酸包含与seqidno:7至少90%同源的核酸序列。
根据一实施例,本发明的多核苷酸包含具有至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%或100%的核酸序列与seqidno:7同源性或同一性。
根据一具体实施例,本发明的多核苷酸包含编码根皮素4’-o-葡萄糖基转移酶多肽的核酸序列(即包含seqidno:8所示的氨基酸序列)如seqidno:7所示。
根据具体实施例,本发明的多核苷酸包含编码udp-葡萄糖:类黄酮7-o-葡萄糖基转移酶的核酸序列(如登录号aax16493和seqidno:7所示)。
根据一实施例,与对照植物相比,通过提高植物天然基因的表现水平可以实现上调多肽植物的表现。这可以通过例如下文进一步描述的基因组编辑来完成,例如通过在(多个)调节组件中引入(多个)突变(例如增强子、启动子、非转译区、内含子区),及/或通过同源定向修复(hdr),例如用于引入编码目的多肽的“修复模板”,导致天然基因表现的上调。
另外及/或可替代地,通过重组dna技术,例如使用包含多核苷酸的核酸构建体来编码目标多肽的多核苷酸,通过增加由于外源多核苷酸的表现引起的目的多肽的含量,可以实现多肽植物表现的上调。
根据一个实施例,外源多核苷酸在用于转化宿主细胞的核酸构建体中提供。如上所述,合适的宿主细胞包括例如细菌、酵母和其他微生物、植物细胞和其他真核细胞。
可以使用本领域技术人员熟知的重组dna技术构建根据本发明一些实施例的方法中有用的构建体。基因构建体可以插入载体中,载体可以是市售的,适于转殖入细胞(例如植物细胞)并适于在被转殖的细胞中表现目标基因。遗传构建体可以是表现载体,其中核酸序列与一个或多个调节序列可操作地连接,从而允许在细胞(例如植物细胞)中表现。
在本发明一些实施例的一个具体实施例中,调节序列是植物可表现的启动子。
如本文所用术语“植物可表现的”是指启动子序列,包括添加到其中或包含在其中的任何其他调节组件,至少能够在植物细胞、组织或器官中诱导,赋予、激活或增强表现,优选单子叶植物或双子叶植物细胞、组织或器官。可用于本发明一些实施例的方法的优选启动子的实例列于表i,ii,iii和iv中。
表i
用于实施本发明一些实施例的示例性组成型启动子
表ii
用于实施本发明一些实施例的示例性优选种子启动子
表iii
用于实施本发明的示例性的花特异性启动子
表iv
用于实施本发明的替代水稻启动子
根据一个实施例,多个构建体被使用以允许多肽在包含多个受质的植物组织中表现。
可优化本发明一些实施例的多肽的核酸序列用于植物表现。此类序列修饰的实例包括但不限于改变g/c含量以更接近通常在感兴趣的植物物种中发现的含量,并且去除通常在植物物种中发现的密码子,通常称为密码子优化。
如本文所用术语“密码子优化”是指选择适当的dna核苷酸用于使用在一结构基因或片段,所述dna核苷酸接近目的植物内感兴趣的密码子。因此,优化的基因或核酸序列是指其中天然或天然存在的基因的核苷酸序列已经被修饰为在植物中利用统计学上优选的或统计学上有利的密码子的基因。通常在dna水平上检查核苷酸序列,并且编码区使用任何合适的方法被优化以确认的在植物物种中的表现,例如如sardana等人所述。(1996,植物细胞学报,15:677-681)。在所述方法中,密码子使用的标准偏差,即密码子使用偏差的量度),可以通过首先找到天然基因的每个密码子的使用的平方比例偏差相对于高度表现的植物基因的比例偏差来计算,然后计算平均偏差的平均值。使用的公式是:1sdcu=n=1n[(xn-yn)/yn]2/n,其中xn是指在高度表现的植物基因中使用密码子n的频率,其中yn表示目的基因中密码子n的使用频率,n表示目的基因中密码子的总数。目的基因中的密码子n和n指的是目的基因中密码子的总数。来自双子叶植物高度表现基因的密码子使用表使用murray等人的数据汇编而成。(1989,核酸研究,17:477-498)。
优化核酸序列以根据特定植物细胞类型的优选密码子做为利用基础的直接使用而不进行任何额外的统计计算的一种方法是基于密码子优化表,例如通过nias(国家农业生物科学研究所)、日本dna银行(www.kazusa.or.jp/codon/)在线提供的密码子使用数据库。密码子使用数据库包含许多不同物种的密码子使用表,每个密码子使用表已根据基因库中存在的数据进行统计学确定。
通过使用上述的表来确定特定物种(例如水稻)中每种氨基酸的最优选或最有利的密码子,可以对编码有一目的蛋白质的天然存在的核苷酸序列进行密码子优化以用于所述特定植物物种。这通过用特定物种基因组中具有低统计学发生率的密码子替换对应的氨基酸的密码子来实现,所述密码子在统计学上更受青睐。然而,可以选择一个或多个不太受欢迎的密码子来删除现有的限制性位点,以创造潜在有用的连接处(5’和3’末端创建新的密码子以添加信号肽或终止盒,可能用于切割的内部位点和将片段拼接在一起以产生正确的全长序列),或消除可能对mrna稳定性或表达产生负面影响的核苷酸序列。
在任何修饰之前,天然存在的编码的核苷酸序列可能已含有许多密码子,这些密码子对应于特定植物物种中的统计学上有利的密码子。因此,天然核苷酸序列的密码子优化可以包括确定天然核苷酸序列中哪些密码子对于特定植物在统计学上不受青睐,并且根据特定植物的密码子使用表来修饰这些密码子以产生密码子优化的衍生物。修饰的核苷酸序列可以完全或部分地优化用于植物密码子使用,条件是由修饰的核苷酸序列编码的蛋白质的产生水平高于由相应的天然存在的或天然基因编码产生的蛋白质。通过改变密码子使用来构建合成基因例如描述于pct专利申请号93/07278中。
因此,本发明的一些实施例包括上文描述的核酸序列及其片段、与其杂交的序列、与其同源的序列、与其直系同源的序列、编码具有不同密码子使用的相似多肽的序列、以突变为特征的改变序列,例如天然存在的或人工诱导的一个或多个核苷酸的缺失、插入或取代,无论是随机还是有针对性的。
植物细胞可以用本发明的一些实施例的核酸建构体稳定或暂时转型。在稳定转型中,本发明的一些实施例的核酸分子整合到植物基因组中,因此它代表稳定和遗传的性状。在暂时转型中,核酸分子由转型的细胞表现,但它没有整合到基因组中,因此它代表了一种短暂的性状。
将外源基因引入单子叶植物和双子叶植物中的方法有多种(potrykus,植物生理研究期刊,植物分子生物。(1991)42:205-225;shimamoto等人,自然期刊(1989)338:274-276)。
使外源dna稳定整合到植物基因组dna中的主要方法包括两种主要方法:
(i)农杆菌主导的基因转移:klee等人,(1987)annu植物生理研究期刊,38:467-486;克利和罗杰斯,细胞培养和植物体细胞遗传学,卷6,植物核基因的分子生物学编辑;schell、j和vasil,l.k.,学术出版社,圣地亚哥,(1989)页2-25;gatenby,植物生物技术编辑。kungs和arntzenc.j巴特沃思出版社,波士顿,(1989),页93-112。
(ii)直接dna摄入:paszkowski等人,在植物的细胞培养和体细胞遗传学,卷6,植物核基因的分子生物学;schell、j和vasil,l.k.,学术出版社,圣地亚哥,(1989)页52-68;包括将dna直接摄入原生质体的方法,toriyamak等人,(1988)生物技术,卷6:1072-1074。植物细胞短暂电击诱导的dna摄取:zhang等人,植物细胞研究,(1988)7:379-384;fromm等人,自然期刊(1986)319:791-793;通过粒子轰击将dna注入植物细胞或组织,klein等人,生物技术(1988)6:559-563;mccabe等人,生物技术(1988)6:923-926;桑福德,植物生理学,(1990)79:206-209;通过使用微量移液管系统:neuhaus等人,应用遗传学,(1987)75:30-36;neuhaus和spangenberg,植物生理学,(1990)79:213-217;玻璃纤维或碳化硅晶须转化细胞培养物,胚胎或愈伤组织,美国专利号5,464,765或通过dna与发芽花粉直接孵育,dewet等人,胚胎组织的实验操作编辑;chapmang、p.和mantells.h.和danielsw,伦敦,(1985),页197-209;以及ohta,美国国家科学院院刊,美国(1986)83:715-719。
农杆菌系统包括使用质体载体,其含有整合到植物基因组dna中的定义的dna片段。接种植物组织的方法根据植物种类和土壤杆菌递送系统而变化。一种广泛使用的方法是叶盘方法,其可以用任何组织外植体进行,所述组织外植体提供引发全植物分化的良好来源。horsch等人,植物分子生物学手册a5,kluwer学术出版社,德雷赫特(1988),页1-9。补充方法采用土壤杆菌递送系统与真空渗透相结合。农杆菌系统在基因转殖双子叶植物的产生中特别可行。
有多种直接dna转移到植物细胞中的方法。在电穿孔中,原生质体短暂地暴露于强电场。在显微注射中,使用非常小的微量移液管将dna机械地直接注射到细胞中。在微粒轰击中,dna被吸附在诸如硫酸镁晶体或钨颗粒的微粒上,并且微粒被物理加速到细胞或植物组织中。
在稳定转型之后,进行植物繁殖。最常见的植物繁殖方法是种子。然而,种子繁殖的再生具有缺陷,即由于杂合性,作物缺乏均一性,因为种子是由植物根据门德尔规则控制的遗传变异产生的。基本上,每个种子在遗传上都是不同的,并且每个种子都会以其自身的特定性状生长。因此,优选制造转型的植物,使得再生的植物具有与母本转型基因植物相同的性状和特征。因此,优选通过微体繁殖再生转型的植物,其提供转型植物的快速、一致的繁殖。
微体繁殖是从已从选定的母本植物或栽培种中切除的单片组织培育新一代植物的过程。所述方法允许大量繁殖具有表现融合蛋白的优选组织的植物。生产的新一代植物在遗传上与原始植物相同,并具有原始植物的所有特征。微体繁殖允许在短时间内大量生产优质植物材料,并且在保持原始转型基因植物或转型植物的特征方面提供所选栽培种的快速繁殖。复制植物的优点是植物繁殖的速度和植物的质量和均匀性。
微体繁殖是一个多阶段的过程,需要改变培养基或多个阶段之间的生长条件。因此,微体繁殖过程涉及四个基本阶段:第一阶段,初始组织培养;第二阶段,组织培养增殖;第三阶段,分化和植物形成;以及第四阶段,温室培养和成形化。在第一阶段,初始组织培养期间,建立组织培养物并且证明无污染物。在第二阶段期间,将初始组织培养物倍增,直到产生足够数量的组织样品以满足生产目标。在第三阶段期间,将在第二阶段生长的组织样品分开并生长成单独的小植株。在第四阶段,将转型的小植株转移到温室中进行成形化,其中植物对光的耐受性逐渐增加,从而可以在自然环境中生长。
尽管目前优选稳定转型,但本发明的一些实施例还设想了叶子细胞、分生组织细胞或整株植物的暂时转型。
暂时转型可以通过上述任何直接dna转型方法或使用修饰的植物病毒进行病毒感染来实现。
已显示可用于转型植物宿主的病毒包括camv、tmv和bv。使用植物病毒的植物转型描述于美国专利号us4,855,237(bgv)、ep-aus67,553(tmv);日本公开申请号63-14693(tmv)、epa194,809(bv)、epa278,667(bv);以及gluzmany等人,分子生物学通讯:病毒载体,冷泉港实验室,纽约,页172-189(1988)。用于在许多宿主(包括植物)中表现外源dna的假病毒颗粒描述于wo87/06261中。
用于在植物中引入和表现非病毒外源核酸序列的植物rna病毒的建构体,通过上述参考文献以及dawsonw.o.等人,病毒学(1989)172:285-292;takamatsu等人,胚胎期刊,(1987)6:307-311;french等人,科学期刊(1986)231:1294-1297;以及高松等人,febsletters(1990)269:73-76。
当病毒是dna病毒时,可以对病毒本身进行适当的修改。或者,可首先将病复制隆到细菌质体中,以便于用外源dna建构所需的病毒载体。然后可以从质体中切除病毒。如果病毒是dna病毒,细菌复制起点可以附着在病毒dna上,然后由细菌复制。所述dna的转录和转译将产生外壳蛋白,其将包裹病毒dna。如果病毒是rna病毒,通常将病毒复制为cdna并插入质体中。然后将质体用于制备建构体的整体。然后通过转录质体的病毒序列和病毒基因的转译产生rna病毒,以产生包裹病毒rna的(多个)外壳蛋白。
用于在植物中引入和表现非病毒外源核酸序列的植物rna病毒的建构体,例如包括在本发明的一些实施例的建构体中的那些,通过上述参考文献以及美国专利号us5,316,931中证实。
在一个实施例中,提供了植物病毒核酸,其中天然外壳蛋白编码序列已从病毒核酸中删除。非天然植物病毒外壳蛋白编码序列以及非天然启动子已插入,优选为能够在植物宿主中表达的非天然外壳蛋白编码序列的亚基因组启动子,能够在植物宿主中表现非天然外壳蛋白编码序列,重组植物病毒核酸的包装,以及确保重组植物病毒核酸对宿主的全身感染。或者,可以通过在其中插入非天然核酸序列使外壳蛋白基因失活,从而产生蛋白质。重组植物病毒核酸可含有一种或多种另外的非天然亚基因组启动子。每个非天然亚基因组启动子能够在植物宿主中转录或表现相邻基因或核酸序列,并且不能彼此重组以及不能与天然亚基因组启动子重组。如果包括多于一种核酸序列,则可以将非天然(外源)核酸序列插入邻近天然植物病毒亚基因组启动子或天然和非天然植物病毒亚基因组启动子。非天然核酸序列在亚基因组启动子的控制下在宿主植物中转录或表现,以产生所需产物。
在第二实施例中,如第一个实施例中那样提供重组植物病毒核酸,不同之处在于将天然外壳蛋白编码序列设置于相邻的非天然外壳蛋白亚基因组启动子之一而不是设置于非天然外壳蛋白编码序列。
在第三实施例中,提供了重组植物病毒核酸,其中天然外壳蛋白基因与其亚基因组启动子相邻,并且一个或多个非天然亚基因组启动子已插入所述病毒核酸中。插入的非天然亚基因组启动子能够在植物宿主中转录或表现相邻基因,并且不能彼此重组以及不能与天然亚基因组启动子重组。非天然核酸序列可以插入非天然亚基因组植物病毒启动子附近,使得所述序列在亚基因组启动子的控制下在宿主植物中转录或表现,以产生所需产物。
在第四实施例中,如第三实施例中提供重组植物病毒核酸,不同之处在于天然外壳蛋白编码序列被非天然外壳蛋白编码序列取代。
病毒载体被编码于重组植物病毒核酸的外壳蛋白衣壳化,产生重组植物病毒。重组植物病毒核酸或所述重组植物病毒用于感染合适的宿主植物。重组植物病毒核酸能够在宿主中复制,在宿主中全身扩散,并且外源基因(分离的核酸)在宿主中转录或表现以产生所需蛋白质。
除上述之外,还可以将本发明一些实施例的核酸分子引入叶绿体基因组中,从而实现于叶绿体中表现。
用于将外源核酸序列引入叶绿体基因组的技术是已知的。所述技术涉及以下程序。首先,对植物细胞进行化学处理,以便将每个细胞的叶绿体数量减少到约1个。然后,通过粒子轰击将外源核酸引入细胞中,目的是将至少一种外源核酸分子引入叶绿体中。外源核酸经过选择,使其通过同源重组整合到叶绿体的基因组中,同源重组很容易受到叶绿体固有的酶的影响。为此,除了目标基因外,外源核酸还包括至少一个衍生自叶绿体基因组的核酸区段。此外,外源核酸包括选择标记,其通过顺序选择程序起作用以确定在这种选择之后叶绿体基因组的所有或基本上所有的复制将包括所述外源核酸。与上述技术有关的进一步细节可参见美国专号us4,945,050号以及us5,693,507,在此引用作为参考。因此,一多肽可以通过叶绿体的蛋白质表现系统产生并整合到叶绿体的内膜中。
根据本发明的一些实施例,通过基因组编辑实现上调本发明多肽在植物中的表现。
基因组编辑是通过修饰目标植物基因组序列来影响目标性状的有力手段。此类修饰可导致新的或修饰的等位基因或调控组件。因此,基因组编辑采用人工工程核酸酶的反向遗传学,在基因组中的所需位置切割并产生特定的双链断裂,然后通过细胞内源过程修复,如同源定向修复(hdr)以及非同源末端连接(nhej)。非同源末端连接在双链断裂处直接连接dna末端,而hdr利用同源序列作为一模板在断裂处再生缺失的dna序列。为了将特定的修饰核苷酸引入基因组dna,在hdr期间必须存在含有所需序列的dna修复模板。使用传统的限制性内切核酸酶不能进行基因组编辑,因为大多数限制酶识别dna上的一些碱基对作为它们的靶标,并且在基因组的许多位置发现识别的碱基对组合的概率非常高,导致多次切割而不是限于所需的位置。为了克服这一挑战并创建位点特异性的单炼或双链断裂,迄今已发现并生物工程化了几种不同类型的核酸酶。这些包括归巢核酸内切酶、锌指核酸酶(zfns)、转录激活因子如效应核酸酶(talen)以及crispr/cas系统。
由于与基因转殖植物相比,大多数基因组编辑技术可以留下少量核苷酸中明显的dna改变痕迹,通过基因编辑产生的作物可以避免通常与基因改造(gm)作物发育相关的严格调控程序。
通过基因组编辑上调多肽的植物表现可以通过以下方式实现:(i)替换编码所述目标多肽的内源序列或其对照组的调控序列,及/或(ii)在基因组的靶向区域中插入编码所述目标多肽,及/或(iii)引入点突变,其导致编码所述目标多肽的基因的上调(例如通过改变调节序列,例如启动子、增强子、5’-utr及/或3’-utr,或编码序列中的突变)。
根据一个实施例,同源定向修复(hdr)可用于产生特定核苷酸变化(也称为基因“编辑”),从单一核苷酸变化到大范围插入。hdr方法成功地用于靶向植物中基因编码序列的特定修饰[budhagatapallinagaveni等人,(2015)“基因功能的靶向修饰利用转录激活样效应因子核酸酶(transcriptionactivator-likeeffectornuclease,talen)介导的大麦双链断裂的同源性修复”,g3(贝塞斯达),2015年9月,5(9):1857-1863;赵永平等(2016)使用双sgrna/cas9设计的植物中靶向基因置换的替代策略。科学报告,文章编号:23890(2016)]。
根据一个实施例,crispr-cas系统可用于改变植物中的基因表现,如yang及yinong等人的美国专利申请公开号us20150067922中所述,其通过引用全部并入本文。
根据一个实施例,归巢核酸内切酶可用于改变植物中的基因表现。可以使用例如certomt等人描述的方法设计归巢核酸内切酶。自然方法(2012)9:073-975;美国专利号us8,304,222、us8,021,867、us8,119,381、us8,124,369、us8,129,134、us8133697、us8143015、us8143016、us8,148,098、或us8,163,514,各自的内容通过引用整体并入本文。
根据一个实施例,工程化核酸酶,包括锌指核酸酶(zfn)和转录激活样效应因子核酸酶(talen),可用于通过产生靶向双链断裂来改变植物中的基因表现(如christian等人所述),2010;kim等人,1996;li等人,2011;mahfouz等人,2011;miller等人,2010)。
也可以使用重组腺相关病毒(raav)平台或使用转座酶进行基因组编辑。
用于鉴定功效和检测序列改变的方法是本领域熟知的,包括但不限于dna测序、电泳、基于酶的错配检测测定和杂交测定,例如pcr、rt-pcr、核酸酶保护分析、原位杂合技术、引子延伸、南方墨点法、北方墨点法和墨点印迹分析。
特定基因的序列改变也可以从蛋白质含量来确定。例如色谱、电泳方法、免疫检测分析,如elisa和蛋白质印迹分析和免疫组织化学。
另外,本领域普通技术人员可以容易地设计包括阳性及/或阴性选择标记的表现/剔除建构体,用于有效地选择与建构体发生同源重组事件的转型细胞。阳性选择提供了丰富已吸收外源dna的复制体的手段。这种阳性标记的非限制性实例包括谷氨酰胺合成酶、二氢叶酸还原酶(dhfr),赋予抗生素抗性的标记,例如新霉素、潮霉素、嘌呤霉素和杀稻瘟素s抗性盒。需要使用阴性选择标记来针对标记序列(例如阳性标记)的随机整合及/或消除进行选择。此类阴性标记物的非限制性实例包括将更昔洛韦(gcv)转化为细胞毒性核苷类似物、次黄嘌呤磷酸核糖基转移酶(hprt)和腺嘌呤磷酸核糖转移酶(arpt)的单纯疱疹胸苷激酶(hsv-tk)。
根据本发明的一些实施例,提供了异源表达如上所述的本发明的分离的多核苷酸的宿主细胞。
如上所述,宿主细胞可以是任何合适的细胞,包括但不限于细菌、酵母和可以在发酵环境、植物和其他真核细胞中培养或生长的其他微生物。例如,宿主细胞可以是用异源核酸转化的细菌细胞(例如,大肠杆菌和枯草芽孢杆菌),例如噬菌体dna、质体粒dna或含有本文所述核酸分子的粘粒dna表现载体,用含有本文所述核酸分子的重组酵母表达载体转化的酵母(例如酿酒酵母或粟酒裂殖酵母)。
在一些实施例中,宿主细胞产生三叶苷。
如上所述,三叶苷生物合成通常需要共同受质根皮素和udp-葡萄糖。因此,根据一个实施例,宿主细胞包含根皮素和udp-葡萄糖。单独或组合的根皮素和udp-葡萄糖可以是细胞内源的或外源添加的。另外,为了上调三叶苷的产生,可以将受质(例如根皮素和/或udp-葡萄糖)外源添加到包含内源水平的这些受质的细胞中。这样的步骤通常导致受质含量(例如根皮素和/或udp-葡萄糖)增加至少约5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%或更多与未接受外源基质的宿主细胞相比。
另外或可替代地,为了上调三叶苷的产生,可以通过增加根皮素及/或udp-葡萄糖在生物合成途径中的组分含量来上调细胞中的受质(例如根皮素及/或udp-葡萄糖)含量。因此,对于上调的根皮素含量,柚皮苷二氢查耳酮、根皮苷、根皮素-4’-o-葡萄糖苷或二氢香胺酰辅酶a的含量可以被上调。或者,查耳酮合酶或柚皮素-查耳酮合成酶(chs)的含量可以与共同受质3x丙二酰辅酶a一起上调,用于上调根皮素的合成。同样,对于上调的udp-葡萄糖含量,葡萄糖-1-磷酸可以被上调。或者,udp-葡萄糖-焦磷酸化酶的含量可以与共同受质utp一起上调,以上调udp-葡萄糖的合成。
可以使用本领域已知的任何方法实现受质的外源添加(例如根皮素及/或udp-葡萄糖),例如通过使宿主细胞与受质(例如根皮素和udp-葡萄糖)接触,例如在细胞培养基中。
可以使用核酸建构体或使用如本文所述的基因组编辑来实现细胞中额外的酶的表现(例如用于表现包含与seqidno:8至少90%相同且具有4’-o-葡萄糖基转移酶活性的氨基酸序列的多肽)。应当理解,可以在单个核酸建构体中提供一种以上的外源多核苷酸(例如2、3、4、5等),或者可以将两种或更多种(例如3、4、5等)核酸建构体引入单个宿主细胞中。
根据一个实施例,提供了基因转殖植物或植物细胞,其包含编码一多肽的一外源核酸序列,所述多肽包含与seqidno:8至少90%相同并具有a’-o-葡萄糖基转移酶活性的氨基酸序列。
根据一个实施例,提供了产生基因转殖植物的方法,所述方法包括向植物细胞中引入核酸构建体,所述核酸构建体包含编码多肽的核酸序列,所述多肽包含与seqidno:8至少90%相同并具有a’-o-葡萄糖基转移酶活性的氨基酸序列。
根据一个实施例,细胞(例如宿主细胞)、植物细胞或植物包含一受质,所述受质选自下列所组成的群组:根皮素、三叶苷、根皮苷、槲皮素、柚皮素和叶黄素。
根据一个实施例,细胞(例如宿主细胞)、植物细胞或植物包含包含一尿苷二磷酸葡萄糖受质。
根据一个实施例,细胞(例如宿主细胞)、植物细胞或植物包含根皮素受质和udp-葡萄糖受质。
根据一个实施例,当所述细胞(例如宿主细胞)、植物细胞或植物包含所述根皮素与所述尿苷二磷酸葡萄糖时,所述基因转殖的植物或植物细胞产生三叶苷。
如上所述,可以使用本发明的一些实施例的酶产生另外的产物(即包含与seqidno:8至少90%相同并具有4’-o-葡萄糖基转移酶活性的氨基酸序列)。这些产物取决于受质。
本文描述的宿主细胞可用于产生三叶苷的方法中。例如,如果宿主细胞是微生物(例如大肠杆菌),则所述方法可以包括使所述微生物生长于一培养基中,其中酶-例如4’-o-葡萄糖基转移酶(例如mdph-4’-ogt)在催化本发明方法的步骤的条件下被表现。重组微生物可以以补料分批或连续过程生长。通常,重组微生物在发酵罐中在限定的温度下的生长需要一段时间。这种确定在本领域技术人员的技能范围内。
类似地,当宿主细胞是植物细胞(例如如下所述的叶细胞、花细胞、果实细胞、干细胞等)时,所述方法可以包括使所述微生物生长于一培养基中,其中酶-例如4’-o-葡萄糖基转移酶(例如mdph-4’-ogt)在催化本发明方法的步骤的条件下被表现。重组植物细胞可以以补料分批或连续过程生长。通常,重组植物细胞在细胞培养皿中在限定的温度下的生长需要一段时间。这种确定在本领域技术人员的技能范围内。
根据一个实施例,可以使用本发明的一些实施例的酶产生另外的产物(即包含与seqidno:8至少90%相同并且具有4’-o-葡萄糖基转移酶活性的氨基酸序列)。这些产物取决于所用的受质。本发明考虑的其他受质包括但不限于三叶苷、根皮苷、槲皮素、柚皮素、表儿茶素、花青素、4-香豆酸和咖啡酸。
多肽的含量(例如包含与seqidno:8至少90%相同且具有4’-o-葡萄糖基转移酶活性的氨基酸序列)、受质(例如根皮素或udp-葡萄糖)和产物(例如三叶苷)可以使用本领域已知的任何方法在宿主细胞中测定。例如,从培养基或宿主细胞的裂解物(如后讨论)获得样品可以用于根据众所周知的方法进行分析,例如但不限于elisa和西方墨点法(例如用于测量多肽含量),或使用纯化方法(如后讨论)。
根据一个实施例,细胞裂解物可以从表现本发明的酶的宿主细胞制备(即包含与seqidno:8至少90%相同并且具有4’-o-葡萄糖基转移酶活性的氨基酸序列)。并用于接触受质,例如根皮素和udp-葡萄糖,以产生三叶苷(例如体外)。
通常,细胞裂解物通过宿主细胞的物理破坏或基于洗涤剂的裂解获得。因此,例如细胞裂解物可以通过超声处理、均质化、使用溶菌酶的酶解、或通过冷冻和研磨宿主细胞来获得。
根据一个实施例,细胞裂解物包括编码包含4’-o-葡萄糖基转移酶活性的多肽(例如mdph-4’-ogt)的多核苷酸(外源的)。
根据一个实施例,细胞裂解物包含受质(例如根皮素及/或udp-葡萄糖)。
根据一个实施例,细胞裂解物包含三叶苷。
根据一个实施例,细胞裂解物可单独或与其他合适的受质或酶组合用于三叶苷的无细胞生成。
根据一个实施例,细胞裂解物可用于还原产物(例如三叶苷),用于还原重组表现的多肽(例如mdph-4’-ogt)或用于还原受质(例如根皮素及/或udp葡萄糖)。
用于提取活性酶多肽的方法是本领域熟知的[例如sasidharans.等人,辅助与替代疗法,(2011)8(1):1-10,通过引用并入本文]。
测定4’-o-葡萄糖基转移酶活性的方法是本领域熟知的,包括例如用于质谱联用-液相色谱法的标准葡萄糖基转移酶测定和用于酶udp-葡萄糖焦磷酸化酶的放射性测定。
纯化产物(例如三叶苷)或受质(例如根皮素及/或udp-葡萄糖)的方法是本领域熟知的,包括例如亲和纯化、过滤、离心、蒸发,液对液萃取、分馏和蒸馏。
纯化产物(例如三叶苷)或受质(例如根皮素及/或udp-葡萄糖)含量的方法是本领域熟知的,包括例如一维和二维核磁共振。
本文所用术语“植物”包括完整植物、嫁接植物、祖先和后代的植物,以及植物的部分,包括种子、枝条、茎、根(包括块茎)、初生主根、接穗、叶子(包括幼叶和成熟叶)、花、果实(包括果皮和果肉)、植物细胞、组织和器官。植物可以是任何形式,包括悬浮培养物、胚胎、分生组织部分、愈伤组织、叶子、配子体、孢子体、花粉和小孢子。
如本文所用术语“植物细胞”包括任何植物或植物部分的细胞,包括但不限于叶子的细胞(包括幼叶和成熟叶)、花的细胞、果实的细胞、(包括果皮细胞或果肉细胞)、根细胞、砧木细胞、茎细胞、枝条细胞、种子细胞和分生组织。
在本发明方法中特别有用的植物包括属于绿色植物的超级家族的所有植物,特别是单子叶植物和双子叶植物,包括饲料或饲料豆科植物、观赏植物、粮食作物、树木或灌木,如下列选自包括金合欢属物种(acaciaspp.)、槭树属物种(acerspp.)、称猴桃属物种(actinidiaspp.)、七叶树属物种(aesculusspp.)、新西兰贝壳杉(agathisaustralis)、albiziaamara、三色极稷(alsophilatricolor)、须芒草属物种(andropogonspp.)、落花生属物种(arachisspp)、模榔(arecacatechu)、asteliafragrans、黄苗(astragaluscicer)、baikiaeaplurijuga、样木属物种(betulaspp·)、芸苔属物种(brassicaspp.)、木揽(bruguieragymnorrhiza)、burkeaafricana、紫铆(buteafrondosa)、cadabafarinosa、朱缀花属物种(calliandraspp)、茶(camelliasinensis)、美人蕉(cannaindica)、辣椒属物种(capsicumspp.)、决明属物种(cassiaspp.)、距瓣豆(centroemapubescens)、木瓜属物种(chaenomelesspp.)、肉桂(cinnamomumcassia)、小果咖啡(coffeaarabica)、colophospermummopane、变异小冠花(coronilliavaria)、枸子(cotoneasterserotina)、山楂属物种(crataegusspp.)、香瓜属物种(cucumisspp·)、柏木属物种(cupressusspp.)、cyatheadealbata、木梨(cydoniaoblonga)、圆球柳杉(cryptomeriajaponica)、香茅属物种(cymbopogonspp.)、cyntheadealbata、木梨(cydoniaoblonga)、dalbergiamonetaria、大叶骨碎补(davalliadivaricata)、山马虫皇属物种(desmodiumspp·)、迪卡兰(dicksoniasquarosa)、diheteropogonamplectens、迪奥豆属、德扁豆属物种(dolichosspp.)、直矛豆、维穗稗(echinochloapyramidalis)、ehrartiaspp.、穆子(eleusinecoracana)、eragrestisspp.、剌桐属物种(erythrinaspp.)、按属物种(eucalyptusspp.)、希氏假乌木属、金茅(eulaliavillosa)、养麦属物种(fagopyrumspp.)、费约罗(feijasellowiana)、草雷属物种(fragariaspp.)、千斤拔属物种(flemingiaspp.)、藤露兜属、中日老鹳草、银杏(ginkgobiloba)、罗德葛藤、南洋樱属、陆地棉(gossypiumhirsutum)、银禅属物种(grevilleaspp.)、安哥拉小巴花、岩黄甚属物种(hedysarumspp.)、牛鞭草(hemarthiaaltissima)、扭黄茅(heteropogoncontortus)、大麦(hordeumvulare)、红苞茅、小连翅(hypericumerectum)、hypertheliadissoluta、白花庭蓝(indigoincarnata)、鸾尾属物种(irisspp.)、常绿虎耳草、胡枝子属物种(lespedizaspp·)、万苣属物种(lettucaspp.)、银合欢、单罗得草、罗顿豆、百脉根属物种(lotusspp·)、硬皮豆(macrotylomaaxillare)、苹果属物种(malusspp.)’manihotesculenta、紫苜猜(medicagosativa)、水杉(metasequoiaglyptostroboides)、大蕉(musasapientum)、烟草属物种(nicotianumspp·)、驴食草属物种(onobrychisspp·)、ornithopusspp.、稻属物种(oryzaspp.)、非洲双翼豆(peltophorumafricanum)、狼尾草属物种(pennisetumspp·)、鳄梨(perseagratissima)、碧冬煎属物种(petuniaspp·)、菜豆属物种(phaseolusspp·)、模榔竹(phoenixcanariensis)、三色山麻兰、石楠属物种(photiniaspp.)、白云杉(piceaglauca)、松属物种(pinusspp.)、豌豆(pisumsativum)、新西兰罗汉松(podocarpustotara)、pogonarthriafleckii、pogonarthriasquarrosa、杨属物种(populusspp.)、牧豆树(prosopiscineraria)、花方萁松(pseudotsugamenziesii)、pterolobiumstellatum、西洋梨(pyruscommunis)、栎属物种(quercusspp.)、rhaphiolepsisumbellata、美味棒花掠(rhopalostylissapida)、rhusnatalensis、欧洲醋粟(ribesgrossularia)、荼荐子属物种(ribesspp.)、洋槐(robiniapseudoacacia)、蔷薇属物种(rosaspp)、悬钩子属物种(rubusspp)、柳属物种(salixspp.)、红裂稃草、金松(sciadopitysverticillata)、北美红杉(sequoiasempervirens)、巨杉(sequoiadendrongiganteum)、两色蜀黍(sorghumbicolor)、菠菜属物种(spinaciaspp.)、鼠尾粟属、葫戸荼属、矮柱花草、葫芦荼属物种(tadehagispp)、落羽杉(taxodiumdistichum)、阿拉伯黄背草(themedatriandra)、车轴草属物种(trifoliumspp.)、小麦属物种(triticumspp.)、异叶铁杉(tsugaheterophylla)、越桔属物种(vacciniumspp.)、野豌豆属物种(viciaspp·)、葡萄(vitisyinifera)、锥穗沃森花(watsoniapyramidata)、马蹄莲(zantedeschiaaethiopica)、玉蜀泰(zeamays)、觅属植物(amaranth)、洋蓟(artichoke)、天门冬属(asparagus)、椰菜(broccoli)、抱子甘蓝(brusselssprouts)、甘蓝、芸苔(canola)、胡萝卜、花椰菜、序菜、羽衣甘蓝(collardgreens)、亚麻、无头甘蓝(kale)、兵豆属(lentil)、油菜籽油菜(oilseedrape)、秋葵(okra)、洋葱、马铃薯、稻、大豆、草莓、甜菜、甘蔗、向日葵、西红柿、南瓜(squash)、荼。可替换的和包括藻类和其他非绿色植物但可用于本发明的一些实施例的方法。在一个实施例中,植物是葫芦科(cucurbitaceae)的植物,例如罗汉果(s.grosvenorii)。
根据一个实施例,所述植物是蔷薇科植物,例如但不限于苹果树、梨树、木瓜树、杏树、李子树、樱桃树、桃树、覆盆子灌木、枇杷树、草莓植物、杏仁树、观赏树木和灌木(如玫瑰,旋果蚊子草、石楠、火棘属、花楸树以及山楂)。
根据一个实施例,植物是葡萄属植物。示例性的葡萄属物种包括但不限于变叶葡萄以及甘葛。
根据一个实施例,植物是苹果属植物。典型的苹果树种类包括但不限于:扁叶苹果、亚洲苹果、巴卡塔苹果、冠状苹果、家苹果、杜氏苹果、佛罗伦萨苹果、佛罗里伦达苹果、福斯加苹果、湖北海棠,草原海棠、陇东海棠、垂丝楸、西府海棠、红肉苹果、盐生苹果、檀香苹果、湖北苹果,美洲苹果、关岛苹果东方苹果、普拉提苹果、普拉提苹果、普拉提栽种苹果、苹果侧柏、西蜀海棠、楸子、苹果白榆、海棠琼花、三叶海棠、野苹果、欧洲野苹果、变叶海棠、花叶海棠、海棠、野木海棠、新疆野苹果、欧洲野苹果、栽种苹果、苹果种、西洋梨、小金海棠、滇池海棠、苹果属苹果、欧楂。
在一个具体实施例中,植物是苹果、野木海棠或三叶海棠。
在一个具体实施例中,植物是菝葜属(例如墨西哥菝葜)、石栎属(例如多穗石栎)或草莓属的植物。
如上所述,本发明的一些实施例的方法制备了产生三叶苷的植物。植物可以是自然下不生产三叶苷的植物,或者可以是包含内源的三叶苷含量的植物,其通过本发明的一些实施例的方法上调。
根据一个具体实施例,植物不包含可检测含量的内源性三叶苷(例如,通过质谱联用-液相色谱法和核磁共振测量)。
与植物相比,三叶苷含量的增加可以是至少约5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%或更多,相较于未经本发明的一些实施例的方法处理的含量。
制备产生三叶苷的植物的方法是通过在植物中表现包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列的多肽来实现的。
上调包含与seqidno:8至少90%相同且4’-o-糖基转移酶活性的氨基酸序列的多肽的植物表现可以是至少约5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、100%或更多,与未通过本发明一些实施例的方法处理的植物相比。
因此,根据一个实施例,增加植物中的三叶苷含量涉及用建构体转化至少一种植物细胞,所述建构体设计用于上调包含与seqidno:8至少90%相同的氨基酸序列并具有4’-o-糖基转移酶活性的多肽的表现(如上所述)。在三叶苷的受质(例如根皮素和udp-葡萄糖)存在下,在植物细胞中表达包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列的多肽,在这种植物细胞中上调三叶苷含量。可以通过测量三叶苷含量(例如,通过质谱联用-液相色谱法和核磁共振光谱)来验证植物中三叶苷含量的评估。
根据具体实施例,遗传修饰植物的发育和生长不受影响。评估植物的发育和生长可以通过例如确定果实成熟、器官生长、细胞分裂、细胞伸长、衰老、萌发、呼吸作用、光合作用、蒸腾作用、开花、授粉和受精来实现。
根据另一个实施例,增加植物中的三叶苷含量可涉及用表现所述多肽的植物进行育种,所述多肽包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列。这种植物可以是天然表现多肽的植物,所述多肽包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列。或者,植物可以是转化以表现多肽的基因转殖植物,所述多肽包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列(例如如上所述)。
根据本发明的一些实施例,进行育种使得受体的基因组至少为受体的基因组的95%-99%和供体的5%或低至1%(包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列)(例如如上所述))。这些后代通常涉及如本文所述的回交和选择的谱系程序。
如本文所用术语“基因转殖植物”是指一植物中一种或多种植物的细胞,其中用通过人为干预(例如通过植物的基因工程)引入的外源多核苷酸序列的稳定或暂时转型。基因转殖植物通常表达dna序列,其赋予植物不同于相同菌株的天然非转基因植物的特征。
因此,根据本发明的一个实施例,可以将一第一植物(即不表现包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列)与一第二植物(即表现包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列)进行杂交。
应当注意的是,尽管上述植物育种方法利用一种转型植物和一种未转型植物,但也可利用两种或更多种个别的转型植物的方法,每种植物包含一种或两种组分(例如多肽、受质等)。因此,经修饰以表现一种以上基因转殖的植物可以是表现基因转殖的第一基因转殖植物(a)与表现基因转殖的第二基因转殖植物(b)的杂交和选择表现基因转殖的植物后代(a+b)的结果。
根据另一个实施例,增加植物中的三叶苷含量可涉及杂交两种非基因转殖植物,例如一种苹果植物和一种梨植物,其中至少一种植物表现包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列的多肽。
杂交和育种可以通过本领域已知的用于育种植物的任何方法完成,例如,上述第一和第二植物的异花授粉以及选择表现包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列的多肽的后代并产生三叶苷的植物。本文使用的植物育种方法是本领域技术人员公知的。关于植物育种技术的讨论,参见poehlman(1987),育种田间作物,avi出版公司,康涅狄格州韦斯特波特。许多在这种方法中有用的作物是通过利用植物授粉方法的技术培育出来的。
通过不同品种、变异性、种或属的杂交育种可以进一步实现杂交和育种。例如,来自不同属(属间杂交种)的物种之间的杂交种可以包含栽培苹果(malus×domestica)和欧洲梨(pyruscommunis)的杂交种、苹果(malus)和花楸属杂交、木苹果的杂交种(malussylvestris)和野生楸树(sorbustorminalis),或梨(pyrus)和木瓜(cydoniaoblonga)的混种(其他例子在
www.agroforestry.co.uk/wp-content/uploads/agnews-sample/agn_sample.pdf,通过引用并入本文)。或者,来自相同属(种间杂交种)的物种之间的杂交种包括但不限于山荆子和栽培苹果之间的杂交种、野生苹果和栽培苹果之间的杂交种,或楸子和栽培苹果之间的杂交种(其他例子在www.inspection.gc.ca/plants/plants-with-novel-traits/applicants/directive-94-08/biology-documents/malus-domestica/eng/1404417088821/1404417158789?chap=5中提供,通过引用并入本文)。
应当理解,当提及遗传修饰的植物或植物细胞时,本发明人还提及涉及由其产生的后代。
通过验证4’-o-糖基转移酶活性的存在或通过测量植物产生的三叶苷的水平(如上所述),可以选择由育种或多重转型植物产生的子代。当改变的a’-o-糖基转移酶活性或三叶苷含量可能不一定容易测量时,这些方法可以在年轻或早期发育阶段应用。
一旦鉴定出产生三叶苷的后代,就在最大化三叶苷生产的条件下进一步培养这些植物。应当理解,这些条件可能在植物物种之间以及不同的环境生长区域和气候之间不同。
根据本发明的一个实施例,可以使用体外方法即无细胞产生三叶苷。因此,本发明的酶(即包含与seqidno:8至少90%相同并具有4’-o-糖基转移酶活性的氨基酸序列)可与受质接触,例如根皮素和udp-葡萄糖,在酶催化葡萄糖基团与4-羟基上的根皮素接触以产生三叶苷的条件下。本领域普通技术人员能够确定酶的量、受质的量和用于生产三叶苷的条件。
根据一个实施例,反应混合物中的三叶苷可以原样使用,即无需进一步纯化。根据另一个实施例,使用本领域熟知的方法从混合物中纯化三叶苷。例如,可以通过亲和纯化、过滤、离心、蒸发、液对液萃取、分馏和蒸馏来纯化三叶苷。
测量三叶苷含量的方法是本领域公知的,包括例如一维和二维核磁共振。
本发明还包括含有三叶苷的组合物。
包含三叶苷的组合物可以从细胞裂解物中获得(如上所述)。另外或可替代地,包含三叶苷的组合物可以从产生三叶苷的植物中获得。
可以通过本领域技术人员已知的不同方法从植物中提取三叶苷。例如,tanakat.等人,从葡萄(pitispiasezkiimaxim)叶中分离三叶苷,一种甜的二氢查耳酮-葡萄糖苷;以及v.sacchariferamakino,农业与生物化学,(1983)47:10,2403-2404(通过引用并入本文)提供了从葡萄叶中分离三叶苷的方法。此外,秦向东和ji-kailiuz.,naturforsch,(2003)58c,759-761(通过引用并入本文)提供了从石栎(lithocarpuspachyphyllus)叶中分离三叶苷的方法。
根据一个实施例,提供了包含根据本发明一些实施例的方法产生的三叶苷的组合物。
在一些实施例中,本发明的组合物是消耗品的组合物。
消耗品包括所有食品或饲料产品,包括但不限于谷物产品、大米产品、木薯产品、西米产品、烘焙产品、饼干产品、糕点产品、面包产品、糖果产品、甜点产品、口香糖、口嚼糖、巧克力、冰、蜂蜜制品、糖蜜制品、酵母制品、烤粉、盐和香料制品、咸味制品、芥末制品、醋制品、调味品(调味料)、烟草制品、雪茄、香烟、加工食品、熟果和蔬菜制品、肉类和肉制品、果冻、果酱、水果酱、蛋制品、牛奶和乳制品、酸奶、奶酪制品、黄油和黄油替代品、代乳品、豆制品、食用油和脂肪制品、药物、饮料、碳酸饮料、酒精饮料、啤酒、软性饮料、矿泉水和气泡水和其他非酒精饮料、果汁饮料、果汁、咖啡、速溶咖啡、茶、可可、包括需要重新定义形式的食物提取物、植物提取物、肉提取物、调味萃取物、甜味剂、营养制品、明胶,药剂和非药物胶、片剂、锭剂、滴剂、乳剂、酏剂、糖浆和其他制备饮料的制剂,以及其组合。
本发明的三叶苷组合物可用于各种消耗品,包括但不限于水性消耗品、固体干燥消耗品和乳制品、乳制品衍生产品和乳制品替代产品。在一些实施例中,所述组合物是食品。
因此,三叶苷组合物可以是选自颗粒形式、粉末形式、糊剂形式和液体形式的形式。
水性消耗品包括但不限于饮料、水、含水饮料、增强/微甜水饮料、矿泉水、碳酸饮料、非碳酸饮料、碳酸水、去离子水、软性饮料、非酒精饮料、酒精饮料饮料、啤酒、葡萄酒、白酒、水果饮料、果汁、水果汁、蔬菜汁、清汤饮料、咖啡、茶类、红茶、绿茶、乌龙茶、凉茶、可可(水性)、茶饮料、咖啡饮料、可可饮料、糖浆、冷冻水果、冷冻果汁、水基冰、水果冰、果汁冰糕、调味品、色拉酱、酱汁、汤以及植物材料饮料(整体或磨碎)、或复原用于即食的粉末(咖啡豆、咖啡粉、速溶咖啡、可可豆、可可粉、速溶可可、茶叶、速溶茶粉)。在一些实施例中,组合物可以是饮料,例如可口可乐、百事可乐等。
固体干燥消耗品包括但不限于谷物、烘焙食品、饼类、面包、早餐麦片、谷物棒、能量棒/营养棒、格兰诺拉麦片、蛋糕、饼干、薄脆饼干、甜甜圈、松饼、糕点、糖果、口香糖、巧克力、软糖、硬糖、棉花糖、糖片、休闲食品和植物材料(整体或磨碎),以及如上所述的用于复原的速溶粉末。
对于水基或固体干燥消耗品,有用的浓度可以是约5ppm至约100ppm、约5ppm至约500ppm、约5ppm至约1000ppm、约50ppm至约100ppm、约50ppm至约500ppm、约50ppm至约1000ppm、约100ppm至约500ppm、约100ppm至约1000ppm、约250ppm至约500ppm、约250ppm至约500ppm、750ppm、约250ppm至约1000ppm、约500ppm至约750ppm、约500ppm至约1000ppm或更高。
根据一个具体实施例,对于水基或固体干燥消耗品,有用的浓度可以为约5ppm至约500ppm。
对于人或动物的消耗,三叶苷组合物通常不含污染物(例如微生物污染物)。因此,三叶苷组合物适合人(或动物)消耗。
三叶苷以前被描述为天然甜味剂和苦味阻滞剂。因此,三叶苷组合物可用作食品、饲料、饮料和制药工业中的甜味剂组合物、苦味阻滞剂组合物和增味剂组合物。
在一些实施例中,可以将包含三叶苷的味道调节剂添加到包含一种或多种甜味剂组分(例如蔗糖)或苦味阻滞剂的另一种组合物中。确定添加到每种组合物中的三叶苷的量在本领域技术人员的技能范围内。例如,在某些产品中,通常需要较高的甜味剂浓度以达到类似的甜味强度,例如在乳制品中。
本发明的组合物还可包含一种或多种额外的调味成分。可用于本发明组合物的合适风味成分的非限制性群组包括蔗糖、果糖、葡萄糖、高果糖玉米糖浆、木糖、阿拉伯糖、鼠李糖、赤藓糖醇、木糖醇、甘露醇、山梨糖醇、肌醇、乙酰磺胺酸钾甜味剂、阿斯巴甜、纽甜、三氯蔗糖、糖精、柚皮苷二氢查耳酮(nardhc)、新橙皮苷二氢查耳酮(ndhc)、甜茶苷、甜菊糖双a、甜菊糖苷、甜叶菊及三叶草苷。
本发明的组合物还可包含一种或多种另外的添加剂,例如色素、防腐剂、营养添加剂如维生素和矿物质、调味品、氨基酸(即必需氨基酸)、乳化剂、ph控制剂如酸化剂、水胶体、消泡剂及脱模剂、面粉改良剂或增强剂、提升剂或膨松剂、粘合剂、气体和螯合剂,其效用和效果在本领域中是公知的。参见merriani-webster’s大学词典,第10版,1993。
包含本发明的提取物或化合物的组合物可以进一步配制成使用一种或多种消耗性载剂作为膳食补充剂给药。“消耗性载剂”在本文中定义为任何食品、食品成分或食品添加剂、或用于锭片、包封或用于口服给药的活性剂的其它制剂的任何赋形剂,无论是用于人还是动物。具体的添加剂是本领域技术人员所熟知的,并列于诸如美国药典中。对于膳食补充剂,可以根据本领域常规方法混合提取物。膳食补充剂可以多种形式制备,包括但不限于液体、粉末或固体药丸形式。
三叶苷组合物可以用于一般健康,但对于易受与氧化应激相关的病症的受试者尤其有利,例如动脉粥样硬化、糖尿病、癌症、心血管疾病、肝病和有患阿兹海默病等神经退化性疾病风险的个体,或暴露于致癌物中的受试者。
根据一个实施例,三叶苷组合物包含抗氧化活性(即中和自由基的作用,例如在生理环境中发现的那些)。
根据一个实施例,三叶苷组合物包含抗致癌活性(即抵消致癌物的作用,包括例如物质、放射性核元素或涉及引起癌症的辐射)。
因此,包含本发明一些实施例的三叶苷的组合物本身可以施用于生物体,或者在药物组合物中与合适的载剂或赋形剂混合。
如本文所用术语“药物组合物”是指本文所述的一种或多种活性成分与其他化学组分(例如生理学上合适的载剂和赋形剂)的制剂。药物组合物的目的是促进化合物向生物体的给药。
如本文所用术语“活性成分”是指对生物效应反应的三叶苷。
在下文中,可互换使用的载剂“生理学上可接受的载剂”和“药学上可接受的载剂”是指不会对生物体造成显着刺激并且不会消除所施用化合物的生物活性和性质的载剂或稀释剂。这些术语包括佐剂。
如本文所用术语“赋形剂”是指添加到药物组合物中以进一步促进活性成分给药的惰性物质。赋形剂的实例包括但不限于碳酸钙、磷酸钙、各种糖和各种类型的淀粉、纤维素衍生物、明胶、植物油和聚乙二醇。
用于配制和施用药物的技术可以在“雷明顿的制药科学“,mack出版公司,伊斯顿,最新版本中找到,其通过引用并入本文。
合适的给药途径可以包括例如口服、直肠、经粘膜、特别是经鼻、肠或肠胃外给药,包括肌肉内、皮下和髓内注射以及鞘内、直接心室内、心内、例如进入右心室或左心室腔、进入冠状动脉、静脉注射、腹腔内注射、鼻内注射或眼内注射。
用于向中枢神经系统(cns)递送药物的常规方法包括:神经外科手术策略(例如脑内注射或脑室内输注);所述试剂的分子操作(例如嵌合融合蛋白的产生,其包含对内皮细胞表面分子具有亲和力的运输肽类以及本身不能穿过血脑屏障的试剂),以试图利用其中一种血脑屏障的内源性运输途径;设计用于增加药剂脂质溶解度的药理学策略(例如水溶性药剂与脂质或胆固醇载体的结合);通过高渗性破坏(由甘露醇溶液注入颈动脉或使用生物活性剂如血管紧张素肽引起)对血脑屏障完整性的短暂破坏。
或者,可以以局部而非全身的方式施用所述药物组合物,例如,通过将药物组合物直接注射到一患者的一组织部分中。
本发明的一些实施例的药物组合物可以通过本领域熟知的方法制备,例如通过常规的混合、溶解、制粒、制糖衣、研磨、乳化、包封、包埋或冻干方法。
因此,根据本发明的一些实施例使用的药物组合物可以使用一种或多种生理学上可接受的载剂以常规方式配制,所述载剂包括赋形剂和助剂,其有助于将活性成分加工成可以药学上使用的制剂。适当的配方取决于所选择的给药途径。
适用于本发明一些实施例的药物组合物包括其中含有有效量的活性成分以实现预期目的的组合物。更具体地,治疗有效量是指有效预防、减轻或改善病症(例如心血管疾病、糖尿病、致癌疾病、神经病变性疾病)的症状或延长所治疗的受试者的存活的活性成分(三叶苷)的量。
治疗有效量的确定完全在本领域技术人员的能力范围内,特别是根据本文提供的详细公开内容。
对于本发明方法中使用的任何制剂,最初可以从体外和细胞培养测定中估计治疗有效量或剂量。例如可以在动物模型中配制剂量以达到所需的浓度或滴度。这些信息可用于更准确地确定人体中的有用剂量。
本文所述活性成分的毒性和治疗功效可通过体外标准药学方法、细胞培养物或实验动物测定。从这些体外和细胞培养测定和动物研究中获得的数据可用于配制用于人的一系列剂量。剂量可根据使用的剂型和所用的给药途径而变化。确切的配方,给药途径和剂量可以由个体医生根据患者的病情选择。(参见例如fingl等人,1975,“治疗的药理学基础”,第一章第1页)。
可以单独调整剂量和给药间隔以提供足以诱导或抑制生物效应的活性成分(最小有效浓度,mec)。每种制剂的最小有效浓度都不同,但可以从体外数据估算。实现最小有效浓度所需的剂量取决于个体特征和给药途径。检测分析可用于确定血浆的剂量浓度。
根据待治疗病症的严重程度和反应性,给药可以是单次或多次给药,治疗过程持续数天至数周或直至实现治愈或实现疾病减轻的状态。
当然,给药组合物的量取决于所治疗的受试者、痛苦的严重程度、给药方式、处方医师的判断等。
如果需要,本发明的一些实施例的组合物可以存在于包装或分配器装置中,例如fda批准的试剂盒,其可以含有一种或多种含有活性成分的单位剂型。所述包装可以例如包括金属或塑料薄片,例如吸塑包装。包装或分配器装置可附有给药说明。包装或分配器也可以由具有备注说明的相关容器来容纳,并由政府机构规定的形式来订定药品的制造、使用或销售,所述备注说明反映了上述机构对组合物形式或人或兽医管理部门的批准。例如,这种备注说明可以是美国食品药品管理局批准的用于处方药或批准的产品插页的卷标。还可以制备包含在兼容的药物载剂中配制的本发明制剂的组合物,将其置于合适的容器中,并标记用于治疗指定的病症,如上文进一步详述的。
如本文所用术语“治疗”或“治疗的”是指抑制、预防或阻止病理学上(疾病、病灶或病症)的发展及/或引起的病理的减轻、缓解或消退。本领域技术人员将理解,可以使用各种方法和测定来评估病理学的发展,并且类似地,可以使用各种方法和测定来评估病理学的减轻、缓解或消退。
如本文所用术语“预防”是指避免疾病、病灶或病症在可能有疾病风险但尚未被诊断为患有所术疾病的受试者中发生。
如本文所用术语“受试者”包括哺乳动物,优选患有病理学疾病的任何年龄或性别的人。根据一实施例,所述术语涵盖具有发展成病理学疾病的风险的个体。
根据一实施例,所述药物组合物用于治疗致癌疾病。因此,本发明一些实施例的三叶苷组合物抵消致癌物(例如物质、放射性核元素或参与引起癌症的辐射)及/或抑制癌症发展的作用。示例性癌症包括但不限于结肠腺癌、食道腺癌、肝细胞癌、鳞状细胞癌、胰腺癌、胰岛细胞瘤、直肠腺癌、胃肠道间质瘤、胃腺癌、肾上腺皮质癌、滤泡癌、乳头状癌、乳腺癌、导管癌、小叶癌、导管内癌、粘液癌、叶状肿瘤、尤文氏肉瘤、卵巢腺癌、子宫内膜腺癌、颗粒细胞瘤、粘液性囊腺癌、子宫颈腺癌、外阴鳞状细胞癌、基底细胞癌、前列腺癌、巨人骨细胞瘤、骨肉瘤、喉癌、肺腺癌、肾癌、膀胱癌、肾母细胞瘤或淋巴瘤。
根据一实施例,所述药物组合物用于治疗心血管疾病(例如心肌梗塞)。
根据一实施例,所述药物组合物用于治疗糖尿病(例如i型糖尿病、ii型糖尿病、代谢综合症、糖尿病性血管病)。
根据一个实施例,所述药物组合物用于治疗神经性退化性疾病(例如阿兹海默氏症、帕金森氏病、多发性硬化症、肌萎缩性脊髓侧索硬化症(als)、多系统萎缩、中风、癫痫、皮克病、脊柱-小脑性共济失调、亨廷顿舞蹈病、进行性核上性麻痹、进行性超核性麻痹、粒细胞性肺病、额颞叶痴呆、皮质基底节变性、癫痫症、自身免疫性脑脊髓炎、糖尿病神经病变、青光眼性神经病、路易体病、克雅氏病(cjd)、变异克雅氏疾病、新变种克雅氏病、或库鲁病)。
如本文所用的术语“约”是指±10%。
术语「包括(comprises)」、「包括(comprising)」、「包括(includes)」、「包含(including)」、「具有(having)」及其词形变化是指包括但不限于。
术语「由...组成(consistingof)」意指包括并且限于。
术语「本质上由......组成」指的是组成物、方法或可包括额外的成分和/或步骤,但仅当额外的成分和/或步骤不实质上改变所要求保护的组成或方法的基本和新颖特性。
本文所使用的单数形式「一」、「一个」及「至少一」包括复数引用,除非上下文另有明确规定。例如,术语「一化合物」或「至少一种化合物」可以包括多个化合物,包括其混合物。
在整个本申请中,本发明的各种实施例可以以一个范围的型式存在。应当理解,以一范围型式的描述仅仅是因为方便及简洁,不应理解为对本发明范围的硬性限制。因此,应当认为所述的范围描述已经具体公开所有可能的子范围以及该范围内的单一数值。例如,应当认为从1到6的范围描述已经具体公开子范围,例如从1到3,从1到4,从1到5,从2到4,从2到6,从3到6等,以及所数范围内的单一数字,例如1、2、3、4、5及6,此不管范围为何皆适用。
每当在本文中指出数值范围,是指包括所指范围内的任何引用的数字(分数或整数)。术语,第一指示数字及第二指示数字"之间的范围”及第一指示数字"到”第二指示数字"的范围"在本文中可互换,并指包括第一及第二指示数字,及其间的所有分数及整数。
如本文所用的术语「方法(method)」指的是用于完成一特定任务的方式(manner),手段(means),技术(technique)和程序(procedures),包括但不限于,那些方式,手段,技术和程序,其是已知的,或是从已知的方式,手段,技术或程序很容易地被化学,药理,生物,生化及医学领域从业者所开发。
可以理解,本发明中的特定特征,为清楚起见,在分开的实施例的内文中描述,也可以在单一实施例的组合中提供。相反地,本发明中,为简洁起见,在单一实施例的内文中所描述的各种特征,也可以分开地、或者以任何合适的子组合、或者在适用于本发明的任何其他描述的实施例中提供。在各种实施例的内文中所描述的特定特征,并不被认为是那些实施例的必要特征,除非该实施例没有那些元素就不起作用。
如上所述和如下面的权利要求书的部分所要求保护的本发明的各种实施例和目的在以下实验例中找到实验支持。
应当理解的是,本申请中公开的任何序列标识号(seqidno)可以指dna序列或rna序列,这取决于提及seqidno的上下文,即使表达seqidno也是如此。仅以dna序列形式或rna序列形式。例如,seqidno:7以dna序列形式表达(例如,描述t表示胸腺嘧啶),但它可以指dna序列或rna分子核酸序列的rna序列。类似地,尽管一些序列以rna序列形式表达(例如,描述u表示尿嘧啶),但是取决于所描述的分子的实际类型,它可以指包含dsrna的rna分子的序列,或者与所示rna序列对应的dna分子的序列。无论如何,dna分子和rna分子两者都具有任何公开的替代物序列。
实验例
现在参考以下实施例,它们与以上描述一起以非限制性方式说明本发明。
通常,本文使用的命名法和本发明中使用的实验室程序包括分子、生物化学、微生物学和重组dna技术。这些技术在文献中有详尽的解释。参见,例如“分子克隆:实验室手册”sambrook等人,(1989);“分子生物学中的现行方案”卷i-iii,奥苏贝尔,(1994);ausubel等人,“分子生物学中的现行方案”,johnwileyandsons,baltimore,maryland(1989);perbal,“分子克隆的实用指南”,johnwiley&sons,纽约(1988);watson等,“重组dna”,科学美国人书籍,纽约;birren等人(编辑)“基因组分析:实验室手册系列”,卷1-4,冷泉港实验室出版社,纽约(1998年);美国专利号us4,522,587、us4,666,828、us4,683,202、us4801531、us5,192,659及us5,272,057中所述的方法;“细胞生物学:实验室手册”,第i-iii卷,cellis(编辑),1994;“免疫学现行方案”第i-iii卷,coliganj.e.编辑(1994);stites等人(编辑),“基础和临床免疫学”(第8版),阿普尔顿和兰格,诺沃克,(1994);mishell和shiigi(编辑),“细胞免疫学中的选择方法”,w.h.freemanandco.,纽约(1980);在专利和科学文献中广泛描述了可用的免疫测定法,参见,例如美国专利号us3,791,932号;us3839153;us3,850,752;us3850578;us3853987;us3867517;us3879262;us3901654;us3935074;us3984533;us3,996,345;us4034074;us4098876;us4879219;us5,011,771及us5,281,521;“寡核苷酸合成”gaitm.j(编辑),(1984);“核酸杂交”hamesbd和higginssj(编辑),(1985);“转录和转译”hamesbd和higginssj(编辑),(1984);“动物细胞培养”freshney,ri(编辑);“固定化细胞和酶”irl出版社,(1986);“分子克隆实用指南”perbalb.,(1984)及“酶学方法”第1-317卷,学术出版社;“pcr流程:方法和应用指南”,学术出版社,圣地亚哥,ca(1990);marshak等人,“蛋白质纯化和表征策略-实验室课程手册”,cshl出版社(1996);所有这些都是由在本文件中提供了其他一般性参考文献。其中的程序被认为是本领域公知的并且是为了方便读者而提供的。其中包含的所有信息都通过引用结合在此。
一般材料和实验程序
化学制品
hplc级乙腈、异丙基-1-硫代-β-d-吡喃半乳糖苷(iptg)、甲醇、根皮素、紫铆花素、花青素、花青素-3-o-葡萄糖苷、花青素-5,3-o-葡萄糖苷等化学标准品购自sigma-aldrich公司。三叶苷、槲皮素-7-o-葡萄糖苷和柚皮素-o-葡萄糖苷购自extrasynthese公司(genaycedex,france,www.extrasynthese.com)。
植物材料
从neweyaar研究中心的苹果种质中采集花组织(完全开放)、幼叶和成熟叶,以及苹果品种金冠(goldendelicious)不同发育阶段的果实组织。发育阶段定义为costa等人先前报导的[costaf.等人,实验期刊,(2010)61:3029-3039]:“早绿”(第1阶段:开花后30天);“断路”(第3阶段);“成熟”(第4阶段)。用剃刀刀片将果实去皮,小心地将果皮与果肉分开。将所有植物材料快速冷冻并储存在-80℃直至使用。
数据挖掘和系统发育分析
www.rosaceae.org的数据库中的所有序列与来自地衣芽孢杆菌的yjic糖基转移酶相似[pandeyr.p.等人,环境应用微生物,使用生物信息学资源“expasy”服务器(www.expasy.org)翻译,(2013)79,3516-3521]并使用cap3序列组装程序重新组装。将得到的候选序列与来自地衣芽孢杆菌的udp-葡萄糖基转移酶进行比较,并使用blastp进行比较。使用系统发育分析mega6程序产生根皮素4’-o-葡萄糖基转移酶氨基酸序列和不同同源植物蛋白的无根邻接树。生成的演化树状图进行自举分析,重复1000次。
克隆和表现根皮素4’-o-葡萄糖基转移酶(mdph-4’-ogt)的cdna
基于序列信息,设计对应于5’末端(5’-atggtgcaacaccgctttctac-3’,seqidno:1)和3’末端(5’-gtgcct)的两种特异性引子。苹果根皮素4’-o-葡萄糖基转移酶核苷酸序列的agcatcttttaaaaccttgatctg-3’,seqidno:2)。使用qiagenrneasy试剂盒(hilden,germany)分离来自苹果果实和叶子的rna。为了复制用,用revertaid第一股cdna合成试剂盒(热科学公司)逆转录总rna中的5μg,并扩增相应的cdna,得到约1446个碱基对的片段。
将cdna连接到pexp5-nt/topota表现载体(invitrogen公司,卡尔斯巴德,加州,美国)中,以在n端产生开放可转译区域与his卷标编码延伸的融合,并转化为大肠杆菌top10细胞。使用t7启动子引子通过测序验证建构体。然后将表现建构体导入大肠杆菌菌株bl21(de3)(invitrogen公司)。将3毫升预培养物在37℃下在含有100μg·ml氨芐青霉素(amp)和34μg·ml-1氯霉素的lb培养基中培养过夜。
所述培养物用于接种500毫升新鲜培养基,当培养物达到od600密度为0.8时,加入1毫莫耳每升异丙基-1-硫代-β-d-吡喃半乳糖苷(iptg)以诱导蛋白质表现。然后将细胞在16℃下生长12小时。以11,000离心力离心10分钟后,将细胞重悬浮于含有10%甘油和1毫莫耳每升的2-巯基乙醇(ph7.5)的50毫莫耳每升的三羟甲基氨基甲烷盐酸盐缓冲液中。通过20分钟溶菌酶处理(每500毫升培养物比1毫克溶菌酶)和随后的超声处理的组合裂解细胞。
将含有可溶性重组根皮素4’-o-葡萄糖基转移酶蛋白的上清液进行金属(镍)亲和层析(凯杰公司,瓦伦西亚,加州,美国),并使用标准程序逐步增加咪唑浓度。汇集含有mdph-4’o-gt的组分,用含有10%甘油和1毫莫耳每升的2-巯基乙醇(ph7.5)的50毫莫耳每升的三羟甲基氨基甲烷盐酸盐缓冲液脱盐,使用vivaspin20(ge医疗集团,mwco[分子量截止-关闭为10kda)。
通过使用获自sigma-aldrich公司的bradford试剂测定蛋白质浓度。通过sds-page平行测定浓缩的蛋白质的葡萄糖基转移酶活性。
根皮素4’-o-葡萄糖基转移酶转录物分析
对于根皮素4’-o-葡萄糖基转移酶的定量rt-pcr(qrt-pcr)分析,提取来自不同苹果组织的总rna(5μg)(植物频谱总rna试剂盒,sigma-aldrich公司)并使用寡聚引子以及使用revertaid第一股cdna合成试剂盒(热科学公司,以色列)进行逆转录。
使用absolutetmblue
使用来自苹果的看家基因肌动蛋白作为对照基因进行基因表现的相对定量。用于肌动蛋白的引子是苹果-肌动蛋白-f-qpcr:5’-tcgtccgtggagaagagtta-3’,seqidno:5)和苹果-肌动蛋白-r-qpcr:(5’-aatcatgga)tggctggaagag-3’,seqidno:6)。在将根皮素4’-o-葡萄糖基转移酶数据标准化为肌动蛋白后,从2-δδct值计算根皮素4’-o-葡萄糖基转移酶的相对表现量的差异。使用至少三个生物学方法重复进行所有分析。
用于质谱联用-液相色谱法的标准葡萄糖基转移酶测定法
使用500奈克his标签纯化的(高纯度含量)重组根皮素4’-o-葡萄糖基转移酶蛋白,在100微升反应中一式三份进行根皮素4’-o-葡萄糖基转移酶活性测定。反应在葡萄糖基转移酶缓冲液(50毫莫耳每升的三羟甲基氨基甲烷盐酸盐ph7.5和2毫莫耳每升的2-巯基乙醇)中进行,并具有30μm根皮素和2mmudp-葡萄糖。反应在30℃下进行60分钟,并通过加入10微升的10%tca(体积/体积)终止反应。通过lc-uv-ms将2微升反应产物用于分析和鉴定。所有测定系列至少一式三份进行。
lc-tof-ms分析
uplc-ms分析在agilent1290infinity系列液相色谱仪上进行,所述液相色谱仪配有agilent1290infinitydad和agilent6224精确质量测定时间质谱仪(ms)(安捷伦科技公司,圣克拉拉,美国)。分析柱是zorbaxextend-c18rapidresolutionht柱(2.1×50.0mm,1.8μm,安捷伦科技公司,waldbronn,德国)。梯度洗脱流动相由含有0.1%(体积/体积)甲酸的h2o(洗脱液a)和含有0.1%(体积/体积)甲酸的乙腈(洗脱液b)组成。将柱用10%洗脱液b平衡1.5分钟。然后将洗脱液b增加至95%至12分钟,并在15分钟内恢复至10%。流动相的流速为0.3毫升/分钟,柱温箱温度为40℃。将洗脱的化合物进行双喷雾器正交esi源,其中一个喷雾器用于分析流动,一个用于参比化合物(安捷伦科技公司,圣克拉拉,美国)。esi源在负模式下操作,具有以下设置:气体温度为300℃,流量为8升/分钟,雾化器设置为35psig。将vcap设置为3000v,将片段器设置为-140v并将分离器设置为65v。应用质量检测器的扫描模式(100-1700质荷比),速率为1个光谱/秒。使用“通过配方找到化合物”功能检测目标化合物的[m-h]离子,并通过masshunter定性和定量分析软件b.07.00(安捷伦技术)进行分析。通过比较精确质量和保留时间与购买的标准物鉴定化合物。
表征异源表现的根皮素4’-o-葡萄糖基转移酶
包括的所有数据代表至少三次独立实验的平均值。通过混合0.5m柠檬酸和1m磷酸氢二钠溶液(ph4.0-7.0)和三羟甲基氨基甲烷盐酸盐(ph8.0-10.0)的储备缓冲液,确定ph最佳值在4.0-10.0范围内,最佳温度分别在20℃-45℃(5℃增量)范围内,所述测定使用根皮素和作为受质并在udp-葡萄糖存在下的进行标准葡萄糖基转移酶测定。
根皮素的表现km值通过将根皮素的浓度从0.5-500μm变化并将udp-葡萄糖浓度固定为2mm,以及500奈克his-标签纯化的重组根皮素4’-o-葡萄糖基转移酶蛋白来测定。udp-葡萄糖的km值通过改变udp-葡萄糖浓度来确定,其中0.01-50mm的udp-葡萄糖具有固定的根皮素浓度为30μm,和500奈克his-标签纯化的重组根皮素4’-o-葡萄糖基转移酶蛋白。
根皮素4’-o-葡萄糖基转移酶的受质特异性如对于使用不同受质的标准葡萄糖基转移酶测定所述,并且在udp-葡萄糖作为糖供体的存在下进行。将根皮素的活性任意设定为100%,并计算其他受质的相对转化率。
实验例1
来自苹果的4’-o-葡萄糖基转移酶基因的生物信息学筛选
先前在苹果和各种其他植物中描述了三叶苷的存在(图1和图4中的第6号说明)[jugdeh.等人,febs期刊,(2008)275:3804-3814;dugédebernonvillet.等人,植物化学,(2010)71:443-452;goschc.等人,植物科学,(2010)178:299-306]。然而,葡萄糖基转移酶(gt)酵素及其催化三叶苷的特异性反应的编码基因均未从苹果属或其他植物物种中分离和表征。
本发明人利用最近描述的来自b.licheniformic(yjic)的葡萄糖基转移酶(gt)的序列,其专门研究a’-o葡萄糖基化[pandeyrp等人,(2013),同上],以筛选苹果的可用est和基因组数据库以获得潜在的4’-o-葡萄糖基转移酶编码基因用于参与天然二氢查耳酮甜味剂三叶苷的生物合成。
因此在苹果基因组中鉴定了超过20个候选gt基因。大多数潜在的苹果葡萄糖基转移酶与地衣芽孢杆菌的yjic糖基转移酶蛋白具有不到40%的氨基酸序列同一性。然而,在苹果基因组中,至少有60个基因编码与udp-葡糖基转移酶相似的蛋白质。这些包括来自栽培种苹果和西洋梨的两种先前表征的根皮素2’-o-葡萄糖基转移酶,其将根皮素转化为根皮素2’-o-葡萄糖苷(phloridzin)。
几种的苹果葡萄糖基转移酶序列与yjic糖基转移酶的比对仅在udp-葡萄糖中显示出几个高度保留的区域:分别为黄酮类7-o-葡糖基转移酶(登录号aax16493)和栽培种苹果花青素5,3-ogt(图8)。然后,本发明人为了udp-葡萄糖:黄酮类7-o-葡糖基转移酶产生cdna,称为栽培种苹果udp-葡萄糖基转移酶:根皮素a’-o-葡萄糖基转移酶(mdph-4’-ogt)(如seqidnos:7和8分别为核酸和氨基酸序列所示),和来自苹果果实的rna的栽培种苹果花青素5,3-ogt(如seqidnos:11和12分别为核酸和氨基酸序列所示)。测试了用于两个全长苹果ugt序列的his-标记的重组蛋白在udp-葡萄糖存在下糖基化根皮素的能力。只有两种苹果ugt蛋白中的mdph-4’-ogt显示出具有根皮素糖基转移酶活性以形成三叶苷。
基于蛋白质序列和功能,植物葡萄糖基转移酶先前已根据其序列、动机、糖苷键的立体化学和已知的靶标特异性分类为从gt1至gt94编号的94个家族[hansens.f等人,植物科学前线,(2012)3:59]。gt1家族包括udp-gt,常见于植物、动物、真菌和细菌中,它们负责各种重要有机结构的糖基化,如、花青素、萜烯、辅助因子、类固醇和肽类抗生素,研究最深入的葡萄糖基转移酶家族之一。
使用根皮素4’-o-葡萄糖基转移酶和苹果根皮素2’-o-葡萄糖基转移酶的代表性成员以及家族1的许多其他植物udp-葡萄糖基转移酶构建系统演化树,包括一些细菌的udp-葡萄糖基转移酶蛋白(图2)。根皮素4’-o-葡萄糖基转移酶与来自红斑痤疮的其他几种葡萄糖基转移酶编码序列聚集在一起,包括草莓(fragariaananassa),白梨番红花酸葡萄糖基转移酶和西洋梨类黄酮7-o-葡萄糖基转移酶,并且葡萄糖基转移酶对于查耳酮中的2’或4’位置的特异性或分别在二氢查耳酮簇中的2’的特异性(图2)。
根皮素4’-o-葡萄糖基转移酶序列与来自栽培种苹果的预测的花青素5,3-ogt显示出99%的同一性,与来自西洋梨的黄酮类7-ogt具有95%的同一性,与来自白梨的番红花酸葡萄糖基转移酶具有89%的同一性。根皮素4’-o-葡萄糖基转移酶分别与金鱼草查耳酮4’-ogt具有显着较低的同一性(33%)[ono等人,(2006),同上],以及28%来自西洋苹果的根皮素2’-ogt[jugdeh.等人,(2008),同上]和栽培种苹果具有显着较低的同一性(28%)[goschc.等人,(2010),同上]。
实验例2
根皮素4’-o-葡萄糖基转移酶蛋白的表现和生物化学表征
取得表现根皮素4’-o-葡萄糖基转移酶的细菌细胞并裂解,用镍亲和柱纯化重组his标记的根皮素4’-o-葡萄糖基转移酶蛋白,并通过sds-page显现(图9)。预测的根皮素4’-o-葡萄糖基转移酶蛋白质序列由481个氨基酸组成,计算的分子量为53.4kda,与sds-page中观察到的迁移率一致(图9),理论等电点为4.9。
对于根皮素4’-o-葡萄糖基转移酶的菜单征,使用根皮素作为受质和udp-葡萄糖作为糖供体,测定his-标记和亲和层析以纯化大肠杆菌表现的蛋白质的等分试样的葡萄糖基转移酶活性。通过lc-ms分析由重组根皮素4’-o-葡萄糖基转移酶蛋白形成的产物,并与根皮素、三叶苷和根皮苷标准品进行比较(图3a-h)。在4.8分钟时观察到根皮素受质中根皮素4’-o-葡萄糖基转移酶催化的产物,这与三叶苷标准物的保留时间相同(图3a-h)。将三叶苷标准物掺入根皮素4’-o-葡萄糖基转移酶反应混合物中的lc-ms运行进一步证实反应产物具有相同的保留时间(数据未显示)。含有热灭活性的根皮素4’-o-葡萄糖基转移酶蛋白的测定或不含udp-葡萄糖作为共同受质的测定显示具有上述研究中测试的任何受质都没有可检测的葡萄糖基转移酶活性(图3a-h)。
本发明人在广泛的潜在受质上测试纯化的重组根皮素4’-o-葡萄糖基转移酶活性,例如是苹果果实的天然成分的三叶苷(图1和4中的第6号说明)、根皮苷(图4中的第7号说明)、槲皮素(图4中的第8号图示)、柚皮素(图4中的第9号图示)、表儿茶素(图4中的第10号图示)、花青素(图4中的第11号图示)、4-香豆素酸(图4中的第12号说明)和咖啡酸(图4中的第13号说明),以确定受质的偏好。此外,由于二氢查耳酮/查耳酮的4’位置对应于黄酮类化合物槲皮素、柚皮素、表儿茶素的7位置,因此可以认为7-o-葡萄糖基化类黄酮的糖苷配基也是天然受质。
4’-o-葡萄糖基转移酶对根皮素(图1和4中的第5号图示)受质具有最高的活性(图4)。用纯化的根皮素4’-o-葡萄糖基转移酶培养三叶苷和根皮苷导致产生相应的二-o-葡萄糖苷(图10a-f)。用纯化的根皮素4’-o-葡萄糖基转移酶培养柚皮素导致相应的柚皮素-7-o-葡萄糖苷的形成(图11a-e)。另一方面,槲皮素与纯化的根皮素4’-o-葡萄糖基转移酶的培养导致体外产生三种不同的产物,其中只有一种可以鉴定为槲皮素-7-o-葡糖苷(图12a-d)。此外,令人惊讶的是,形成了三种产物,因为通常葡萄糖基转移酶对于糖基化位点是相当区域选择性的。在作为糖供体的udp-葡萄糖的存在下,用查耳酮叶黄素(图4中的第14号图示)测试根皮素4’-o-葡萄糖基转移酶。这些酶反应导致产生相应的o-葡萄糖苷(数据未显示)。尽管尚未确定这些反应中糖基化的确切性质,但ms谱图清楚地表明糖分子分别与三叶苷、根皮苷、槲皮素和叶黄素相连;核磁共振可用于证实糖基化的区域特异性并阐明使用udp-葡萄糖作为糖供体获得的糖基化产物三叶苷、根皮苷、槲皮素和叶黄素的性质。
相反的,在标准测试条件下没有检测到表儿茶素、花青素、4-香豆酸和咖啡酸的产物(图4)。
为了表征一般动力学参数,本发明人使用his-标记的亲和层析纯化的4’-o-葡萄糖基转移酶蛋白(下表1和图5a-d)。测定根皮素4’-o-葡萄糖基转移酶相对于根皮素和udp-葡萄糖的动力学参数。具有根皮素的根皮素4’-o-葡萄糖基转移酶的km为26.11±6.97μm,vmax为1.86±0.30pkat.μg-1蛋白(图5a)。观察到的udp-葡萄糖的km为1.19±0.27μm,vmax为1.77±0.34pkatμg-1蛋白质(图5b)。在4.0-10.0的ph范围内测试根皮素4’-o-葡萄糖基转移酶的酵素活性。所述酶在ph7.0-9.0下显示出显着的活性,在ph9.0具有最大活性。活性在ph6.0下降至17%,在ph10.0下降至小于5%(图5c)。最大周转率达到50℃(图5d),计算的活化能为18.28千焦/莫耳。
表1:用his-标记和亲和层析纯化蛋白获得的苹果根皮素4’-o-葡萄糖基转移酶的动力学参数
二价阳离子mg2+、mn2+和一价阳离子ca+、k+不影响酶活性,表明它们不是辅因子。在另外的活化糖供体udp-半乳糖存在下,用根皮素测试根皮素4’-o-葡萄糖基转移酶。udp-半乳糖作为共同受质(数据未显示)情况下,所述反应显示没有可检测的葡萄糖基转移酶活性。相比之下,根皮素葡萄糖基转移酶1可以在下列三种糖供体存在下对根皮素进行糖基化:udp-葡萄糖、udp-半乳糖及udp-木糖[jugde等人,(2008),同上]。
受质、根皮素的这些特征动力学数值在其他植物的葡萄糖基转移酶所观察到的范围内[jugde等人,(2008),同上;goschc.等,树木期刊(2012)26:259-271]。然而,苹果ph-2’-ogt[goschc.等人,(2010),同上]显示根皮素的km比根皮素4’-o-葡萄糖基转移酶高3倍,而mdpgt1[jugde等人,(2008),同上]显示的km低41倍,因此,葡萄糖基转移酶对根皮素的亲和力高于根皮素4’-o-葡萄糖基转移酶。
通常,葡萄糖基转移酶被称为具有低序列相似性的仅有少数高度保留区域的超基因家族。它们被描述主要是关于糖附着位置点的区域选择性或区域特异性,但通常不是高度受质特异性。根皮素和udp-葡萄糖的葡萄糖基化产物与已知的三叶苷标准共迁移,表明根皮素4’-o-葡萄糖基转移酶可能是在植物中将根皮素糖基化为三叶苷的酶。此外,据上述,包括苹果在内的不同植物物种可产生几种根皮素衍生物,例如三叶苷、根皮苷及sieboldin(3-羟基卟啉-4’-o-葡萄糖苷)。
例3
mdph-4’-ogt的空间表现
通过qrt-pcr检测根皮素4’-o-葡萄糖基转移酶基因的表现量,使用肌动蛋白作为对照基因,对栽培种苹果金冠(goldendelicious)的叶、花和果组织进行检测。在花、叶和果实(果皮和果肉)样品中检测到根皮素4’-o-葡萄糖基转移酶基因的转录物,但组织之间的表现量在统计学上不同,特别是在果实发育期间(图6)。幼叶中根皮素4’-o-葡萄糖基转移酶转录本的表现量高于成熟叶片、花朵和果实(果皮和果肉)中的表现量,这与不同品种的苹果幼叶中高水平的三叶苷一致。
在果实第3阶段的花和果肉中观察到最低含量的根皮素4’-o-葡萄糖基转移酶基因转录物。表现数据表明苹果根皮素4’-o-葡萄糖基转移酶转录物在多种组织中表现并且能够在先前已描述过不同二氢查耳酮的所有组织中均可发现。
进行额外的葡萄糖基转移酶基因转录物分析,酶表现和随后的靶向基因沉默以更明白的理解三叶苷二氢查耳酮生物合成中的苹果葡萄糖基转移酶基因。
虽然本发明结合其具体实施例而被描述,显而易见的是,许多替代、修改及变化对于那些本领域的技术人员将是显而易见的。因此,其意在包括落入所附权利要求书的范围内的所有替代、修改及变化。
在本说明书中提及的所有出版物、专利及专利申请以其整体在此通过引用并入本说明书中。其程度如同各单独的出版物、专利或专利申请被具体及单独地指明而通过引用并入本文中。此外,所引用的或指出的任何参考文献不应被解释为承认这些参考文献可作为本发明的现有技术。本申请中标题部分在本文中用于使本说明书容易理解,而不应被解释为必要的限制。
序列表
<110>以色列国家农业部、农村发展农业研究组织•沃尔卡尼中心
艾柏达˙姆瓦哈格
<120>辨识与鉴别来自栽培种苹果的udp葡萄糖:根皮素的4'-o-葡萄糖基转移酶的方法
<130>69415
<150>us62/305,591
<151>2016-03-09
<160>12
<170>siposequencelisting1.0
<210>1
<211>22
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>gene
<222>(1)..(22)
<223>单股dna寡核苷酸
<400>1
atggtgcaacaccgctttctac22
<210>2
<211>30
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>gene
<222>(1)..(30)
<223>单股dna寡核苷酸
<400>2
gtgcctagcatcttttaaaaccttgatctg30
<210>3
<211>21
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>gene
<222>(1)..(21)
<223>单股dna寡核苷酸
<400>3
cgataacgaggcgaagaaaga21
<210>4
<211>22
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>gene
<222>(1)..(22)
<223>单股dna寡核苷酸
<400>4
gagaacctccacttgactacac22
<210>5
<211>20
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>gene
<222>(1)..(20)
<223>单股dna寡核苷酸
<400>5
tcgtccgtggagaagagtta20
<210>6
<211>21
<212>dna
<213>人工序列(artificialsequence)
<220>
<221>gene
<222>(1)..(21)
<223>单股dna寡核苷酸
<400>6
aatcatggatggctggaagag21
<210>7
<211>1446
<212>dna
<213>malusdomestica
<400>7
atggtgcaacaccgctttctactcgtcacatttccagctcaaggccacatcaacccttcc60
ctccaattcgccaagcgccttatcaacactacaggtgcgcatgtcacctacgttactagt120
ctgtcagcccatcgccgtataggcaatggctcaattccagatggattgacctatgcgccc180
ttctctgatgggtacgacgatgggtttaagcccggcgacaacgtcgacgactacatgtca240
gagctgcggcgccgcggagtacaagccattaccgaccttgtagtcgcaagtgcaaacgag300
ggtcacccttacacttgcctagtctactcattacttctcccttggtcggcagggatggca360
catgaacttcacctcccaagcgtgctgctttggattcagccagccacggttttcgacatc420
tactactattactttaacgggtacaaagatctcatccgggataatactagttctggtacg480
aacaatgtccttccatgttcaatagaattaccaggtttgccattatctttcacaagccga540
gaccttccctccttcatggtggatacaaatccgtacaatttcgccctcccgttgtttcaa600
gaacagatggagctgttggaaagagaaaccaatccgaccattctagtcaacacgttcgat660
gcactagagccggaagccttaaaagcaattgacaagtacaacttgattggagttgggcca720
ttgattccgtccgctttcttggacggcaaggatccatcggacaagtcatttggaggcgat780
cttttccaaaaatcaaaggactcttcatacctcgagtggctgaactcgaagccagaaggg840
tcggtgatttatgtgtccttcggaagcatttctgtgttgggaaaggcccaaatggaggaa900
atcgcaaaagggttgttggattgcggccttccgttcttgtgggttattagagataaggtc960
ggcaagaagggagacgataacgaggcgaagaaagaagaagagatgttgaggtgcagagag1020
gaattggaagagctcgggatgatagtgccgtggtgtagtcaagtggaggttctctctagt1080
ccttcgttgggttgctttgtgacacattgtgggtggaattcaagtttggagagcttggtt1140
tcaggggtgcccgtggtggcgtttcctcagtggacggaccaagggacgaatgccaagttg1200
atagaggactattggaagacaggagtgagggtgacaccaaatgaggaggggatagttacg1260
ggtgaggagctcaagaggtgcttggatttggtattgggaagtggggagattggtgaagac1320
gtgagaaggaatgctaagaaatggaaagatttggcaagagaggctgtgagtgaaggggac1380
tcttcggacaagaatctcagggctttcttggatcagatcaaggttttaaaagatgctagg1440
cactag1446
<210>8
<211>481
<212>prt
<213>malusdomestica
<400>8
metvalglnhisargpheleuleuvalthrpheproalaglnglyhis
151015
ileasnproserleuglnphealalysargleuileasnthrthrgly
202530
alahisvalthrtyrvalthrserleuseralahisargargilegly
354045
asnglyserileproaspglyleuthrtyralapropheseraspgly
505560
tyraspaspglyphelysproglyaspasnvalaspasptyrmetser
65707580
gluleuargargargglyvalglnalailethraspleuvalvalala
859095
seralaasngluglyhisprotyrthrcysleuvaltyrserleuleu
100105110
leuprotrpseralaglymetalahisgluleuhisleuproserval
115120125
leuleutrpileglnproalathrvalpheaspiletyrtyrtyrtyr
130135140
pheasnglytyrlysaspleuileargaspasnthrserserglythr
145150155160
asnasnvalleuprocysserilegluleuproglyleuproleuser
165170175
phethrserargaspleuproserphemetvalaspthrasnprotyr
180185190
asnphealaleuproleupheglngluglnmetgluleuleugluarg
195200205
gluthrasnprothrileleuvalasnthrpheaspalaleuglupro
210215220
glualaleulysalaileasplystyrasnleuileglyvalglypro
225230235240
leuileproseralapheleuaspglylysaspproserasplysser
245250255
pheglyglyaspleupheglnlysserlysaspsersertyrleuglu
260265270
trpleuasnserlysprogluglyservaliletyrvalserphegly
275280285
serileservalleuglylysalaglnmetglugluilealalysgly
290295300
leuleuaspcysglyleupropheleutrpvalileargasplysval
305310315320
glylyslysglyaspaspasnglualalyslysglugluglumetleu
325330335
argcysargglugluleuglugluleuglymetilevalprotrpcys
340345350
serglnvalgluvalleuserserproserleuglycysphevalthr
355360365
hiscysglytrpasnserserleugluserleuvalserglyvalpro
370375380
valvalalapheproglntrpthraspglnglythrasnalalysleu
385390395400
ilegluasptyrtrplysthrglyvalargvalthrproasngluglu
405410415
glyilevalthrglyglugluleulysargcysleuaspleuvalleu
420425430
glyserglygluileglygluaspvalargargasnalalyslystrp
435440445
lysaspleualaargglualavalsergluglyaspserserasplys
450455460
asnleuargalapheleuaspglnilelysvalleulysaspalaarg
465470475480
his
<210>9
<211>396
<212>prt
<213>bacilluslicheniformis
<400>9
metglyhislyshisilealailepheasnileproalahisglyhis
151015
ileasnprothrleualaleuthralaserleuvallysargglytyr
202530
argvalthrtyrprovalthraspgluphevallysalavalgluglu
354045
thrglyalagluproleuasntyrargserthrleuasnileasppro
505560
glnglnilearggluleumetlysasnlyslysaspmetserglnala
65707580
proleumetpheilelysglumetglugluvalleuproglnleuglu
859095
alaleutyrgluasnasplysproaspleuileleupheaspphemet
100105110
alametalaglylysleuleualaglulyspheglyileglualaval
115120125
argleucysserthrtyralaglnasngluhisphethrpheargser
130135140
ileserglugluphelysilegluleuthrprogluglngluaspala
145150155160
leulysasnserasnleuproserpheasnphegluaspmetpheglu
165170175
proalalysleuasnilevalphemetproargalapheglnprotyr
180185190
glygluthrpheaspgluargpheserphevalglyproserleuala
195200205
lysarglyspheglnglulysgluthrproileileseraspsergly
210215220
argprovalmetleuileserleuglythralapheasnalatrppro
225230235240
gluphetyrhismetcysileglualapheargaspthrlystrpgln
245250255
valilemetalavalglythrthrileaspprogluserpheaspasp
260265270
ileprogluasnpheserilehisglnargvalproglnleugluile
275280285
leulyslysalagluleupheilethrhisglyglymetasnserthr
290295300
metgluglyleuasnalaglyvalproleuvalalavalproglnmet
305310315320
progluglngluilethralaargargvalglugluleuglyleugly
325330335
lyshisleuglnprogluaspthrthralaalaserleuarggluala
340345350
valserglnthraspglyaspprohisvalleulysargileglnasp
355360365
metglnlyshisilelysglnalaglyglyalaglulysalaalaasp
370375380
gluileglualapheleualaproalaglyvallys
385390395
<210>10
<211>1763
<212>dna
<213>malusdomestica
<400>10
accttgaatgtatactcccacaagaatttcaactgcactcagcttataagcccacagtac60
caaatttttcaacaatcaactacatacctacttattctacttccaacaactccacactcc120
accgcgcacctccggcaatcgcatacgccgccatggtgcaacaccgctttctactcgtca180
catttccagctcaaggccacatcaacccttccctccaattcgccaagcgccttatcaaca240
ctacaggtgcgcatgtcacctacgttactagtctgtcagcccatcgccgtataggcaatg300
gctcaattccagatggattgacctatgcgcccttctctgatgggtacgacgatgggttta360
agcccggcgacaacatcgacgactacatgtcagagctgcggcgccgcggagtacaagcca420
ttaccgaccttgtagtcgcaagtgcaaacgagggtcacccttacacttgcctagtctact480
cattacttctcccttggtcggcagggatggcacatgaacttcacctcccaagcgtgctgc540
tttggattcagccagccacggttttcgacatctactactattactttaacgggtacaaag600
atctcatccgggataatactagttctggtacgaacaatgtccttccatgttcaatagaat660
taccaggtttgccattatctttcacaagccgagaccttccctccttcatggtggatacaa720
atccgtacaatttcgccctcccgttgtttcaagaacagatggagctgttggaaagagaaa780
ccaatccgaccattctagtcaacacgttcgatgcactagagccggaagccttaaaagcaa840
ttgacaagtacaacttgattggagttgggccattgattccgtccgctttcttggacggca900
aggatccatcggacaagtcatttggaggcgatcttttccaaaaatcaaaggactcttcat960
acctcgagtggctgaactcgaagccagaagggtcggtgatttatgtgtccttcggaagca1020
tttctgtgttgggaaaggcccaaatggaggaaatcgcaaaagggttgttggattgcggcc1080
ttccgttcttgtgggttattagagataaggtcgacaagaagggagacgataacgaggcga1140
agaaagaagaagagatgttgaggtgcagagaggaattggaagagctcgggatgatagtgc1200
cgtggtgtagtcaagtggaggttctctctagtccttcgttgggttgctttgtgacacatt1260
gtgggtggaattcaagtttggagagcttggtttcaggggtgcccgtggtggcgtttcctc1320
agtggacggaccaagggacgaatgccaagttgatagaggactattggaagacaggagtga1380
gggtgacaccaaatgaggaggggatagttacgggtgaggagctcaagaggtgcttggatt1440
tggtattgggaagtggggagattggtgaagacgtgagaaggaatgctaagaaatggaaag1500
atttggcaagagaggctgtgagtgaaggggactcttcggacaagaatctcaaggctttct1560
tggatcagatcaaggttttaaaagatgctaggcactagtcgggtggcggcctaggacctg1620
gggcctggcaactacgcggctaggtgtctaggcaggcgcctagacggattcgattaaatc1680
tattatatttcgtgtaagtaagtgtatgtttatgcttaaaatatatatgatgtcatcata1740
aacaacaaaatagaatgacatat1763
<210>11
<211>1452
<212>dna
<213>malusdomestica
<400>11
atggcagcgccgctgcccatcgaaatcgaaccatcatcaactaatggtcaaccccatctc60
gccgacgcctacaaccgtcacgtggctgtcgtagccttccctttcactagccatgcaagc120
gccttgcttgagaccgtgcgccgcctagccaccgcccttccaaacactctcttctcgttc180
ttcagcacttcaaaatccaacagctctctcttttccaacaacagcattgataacatgccg240
cgtaacataagggtgtacgatgtggctgacggggtgccggaggggtacgttttcgtgggc300
aagccgcaggaggacatagagctcttcatgaatgccgcaccggaaaacatccggaggagc360
ttagacgcttccgtggcggacatcgggaagcagatcagctgcttgatcaccgacgccttc420
ctttggtttggagtccacttggctgacgagttgggagtgccttgggtcactttctggatc480
tccggactcaaatccctctccgttcatgtgcatactgatctcatccgcgacactattgga540
actcaaggcattacaggtcgtgaaaacgacctcatcgtcgacaaaaatgttaacatccaa600
ggtctctccaatgtacgaatcaaagacttagcggaaggagtcattttcggaaacttggac660
tcggtaatttccggcatgctacttcagatgggacggctcctcccccgtgccaccgcagtt720
ttcatgaacggcttcgaagaattggaactccccataccaaacgacctaaagtccaaagtc780
aacaaactcctcaacgtaggaccttccaacgtagcatccccgctgccaccgctgccgcca840
tcagatgcttgcttgtcatggctagacaagcaacaggctccatcctccgtcgtgtacata900
agcttcgggacagtggcgagcccagcggagaaggagcagatggcaatagcggaggccctg960
gaagccaccggagcacccttcttgtggtctatcaaggacagctgcaagacaccgttgctg1020
aacgagttcttgacaaaaacattgtcaaagctgaacgggatggtggtgccgtgggctcca1080
cagccgcatgtactggcccacgattcggtcggagccttcgtgtcgcattgcggctggaac1140
tcgataatggagactatagcaggacgggtgcccatgatttgtaggccatattttgcagac1200
cagaggcttaatgcaaggatggtggaggaggtgtttgagatcggggtaaccgtggaggat1260
ggagtttttaccagggaggggctggtaaaaagcttggaagtggttttgtcgcctgaaagt1320
gggaggaaattcagagacaatataaagagggtcaaacaactggcagtagaggcggttgga1380
ccacaagggagctccactcggaacttcaaatcgctgttggacatcgtatcaggatccaat1440
tatcaagtatag1452
<210>12
<211>483
<212>prt
<213>malusdomestica
<400>12
metalaalaproleuproilegluilegluproserserthrasngly
151015
glnprohisleualaaspalatyrasnarghisvalalavalvalala
202530
pheprophethrserhisalaseralaleuleugluthrvalargarg
354045
leualathralaleuproasnthrleupheserphepheserthrser
505560
lysserasnserserleupheserasnasnserileaspasnmetpro
65707580
argasnileargvaltyraspvalalaaspglyvalprogluglytyr
859095
valphevalglylysproglngluaspilegluleuphemetasnala
100105110
alaprogluasnileargargserleuaspalaservalalaaspile
115120125
glylysglnilesercysleuilethraspalapheleutrpphegly
130135140
valhisleualaaspgluleuglyvalprotrpvalthrphetrpile
145150155160
serglyleulysserleuservalhisvalhisthraspleuilearg
165170175
aspthrileglythrglnglyilethrglyarggluasnaspleuile
180185190
valasplysasnvalasnileglnglyleuserasnvalargilelys
195200205
aspleualagluglyvalilepheglyasnleuaspservalileser
210215220
glymetleuleuglnmetglyargleuleuproargalathralaval
225230235240
phemetasnglypheglugluleugluleuproileproasnaspleu
245250255
lysserlysvalasnlysleuleuasnvalglyproserasnvalala
260265270
serproleuproproleuproproseraspalacysleusertrpleu
275280285
asplysglnglnalaproserservalvaltyrileserpheglythr
290295300
valalaserproalaglulysgluglnmetalailealaglualaleu
305310315320
glualathrglyalapropheleutrpserilelysaspsercyslys
325330335
thrproleuleuasnglupheleuthrlysthrleuserlysleuasn
340345350
glymetvalvalprotrpalaproglnprohisvalleualahisasp
355360365
servalglyalaphevalserhiscysglytrpasnserilemetglu
370375380
thrilealaglyargvalprometilecysargprotyrphealaasp
385390395400
glnargleuasnalaargmetvalglugluvalphegluileglyval
405410415
thrvalgluaspglyvalphethrarggluglyleuvallysserleu
420425430
gluvalvalleuserprogluserglyarglyspheargaspasnile
435440445
lysargvallysglnleualavalglualavalglyproglnglyser
450455460
serthrargasnphelysserleuleuaspilevalserglyserasn
465470475480
tyrglnval
- 还没有人留言评论。精彩留言会获得点赞!