灵芝萃取物协同两性霉素B的抗癌医药组合物的制作方法
本发明关于一种抗癌医药组合物,尤指一种灵芝萃取物协同两性霉素B的抗癌医药组合物。
背景技术:
根据近年来的统计,恶性肿瘤一直都位居国人十大死因之首,其中又以肺癌、肝癌、结肠直肠癌为癌症死亡的前三大癌症。因此,如何有效治疗癌症及降低癌症死亡率一直是医药界所致力努力的目标。
由于文明快速发展,生活环境中含有许多无形的有害物质,长时间暴露在此种环境中将对身体有所伤害,而经过流行病学及统计学研究,显示大约有八成的癌症是由外在因素所引起,其中包括生活方式的改变、传染病造成的感染因素、职业及其环境造成的因素等,而当中又以化学致癌物为最危险因子,化学致癌物一旦经人体吸收进入体内经过代谢活化,将可能导致细胞内基因发生一连串的突变,使细胞失去控制而持续不断分裂生长,最终导致肿瘤细胞形成。
也因此,各种针对癌症的治疗方法不断被研发,包含化疗、放射性治疗、免疫疗法、单株抗体疗法、及基因疗法等,然而其中亦突显出许多问题,例如化疗所产生一连串的副作用,或者病患对药物产生抗药性等。
另一方面,癌症治疗也开始往天然食物研究,筛选出具有抗癌潜力的功能性食物或营养食物也变成一个重要的方向,在过去研究中,亦有许多中草药被推测具有抗癌效果。因此,本发明即在萃取灵芝中的有效成分,并研究其与两性霉素B的协同作用,以开发更具疗效的抗癌医药组合物。
技术实现要素:
本发明的目的在于研究灵芝萃取物与两性霉素B的协同作用,以开发更具疗效的抗癌医药组合物。
为达上述目的,本发明的一较佳实施方式为提供一种抗癌医药组合物, 其包含:一灵芝萃取物,其浓度为1-5mg/ml;以及一两性霉素B,其浓度为3-10μM,其中,该灵芝萃取物及该两性霉素B以分段方式给药,先以该灵芝萃取物投药一预定时间后再以该两性霉素B投药,以增进该两性霉素B的抑癌效力。
在一实施例中,该灵芝为赤芝(Ganoderma lucidum)。
在一实施例中,该灵芝萃取物为以酒精萃取法萃取而得,且萃取自灵芝的子实体。
在一实施例中,该灵芝萃取物包含固醇及三萜类。
在一实施例中,该两性霉素B的浓度为3-5μM。
在一实施例中,该预定时间为12-48小时,且较佳为24小时。
在一实施例中,该抗癌医药组合物为用于治疗肝癌。
在一实施例中,该抗癌医药组合物为用于治疗肺癌。
附图说明
图1A及1B显示实施例1的Hep G2细胞实验结果。
图1C及1D显示实施例1的Hep 3B细胞实验结果。
图1E及1F显示实施例1的Hep 5J细胞实验结果。
图2A及2B显示实施例2的Hep G2细胞实验结果。
图2C及2D显示实施例2的Hep 3B细胞实验结果。
图2E及2F显示实施例2的Hep 5J细胞实验结果。
图3A显示实施例3的A549细胞实验结果。
图3B显示实施例3的H460细胞实验结果。
具体实施方式
体现本发明特征与优点的一些典型实施例将在后段的说明中详细叙述。应理解的是本发明能够在不同的态样上具有各种的变化,然其皆不脱离本发明的范围,且其中的说明及附图在本质上当作说明之用,而非用以限制本发明。
根据文献得知,有些药用真菌含有丰富的三萜类(triterpenoids)、多醣体(polysaccharides)及固醇(sterols),其对于保护肝脏、促进肝细胞再生、对抗肝癌有相当程度的疗效。此外,两性霉素B(Amphotericin B,简称AmB)为一 种多烯类抗霉菌药,藉由与真菌细胞膜上所嵌的麦角固醇(Ergosterol)结合产生孔洞,而造成细胞膜通透性的改变,使得真菌细胞产生裂解而死亡。因此,本发明进一步研究灵芝萃取物及两性霉素B的协同作用,以致力开发更具疗效的抗癌医药组合。
本发明主要检测灵芝萃取物是否能促进两性霉素B抑制人类肝癌细胞的效力。本发明选用赤芝(Ganoderma lucidum)进行酒精萃取,以取得灵芝酒精萃取物(简称灵芝酒萃物),其将赤芝子实体切片打成粉末,取10克加入500ml的99%酒精,再置于回转式振荡器(200rpm)持续振荡24小时,再过滤收取滤液,并减压浓缩至干燥,秤重后计算回收率,于4℃避光保存。
当然,本发明的灵芝萃取物不限于以酒精萃取所得的萃取物,其他能萃取出灵芝的固醇及三萜类的萃取方法及萃取物皆适用于本发明,例如亦可利用具有不同极性的有机溶剂(如正己烷)来进行萃取,但不以此为限。
以下以实验进一步说明本发明所开发的医药组合物实施例。
实施例1:
本实施例以Hep G2、Hep 3B及Hep 5J等人类肝癌细胞的细胞株来进行实验,并以96格(well)细胞培养盘进行培养。试验方法主要分成两组,一组是先以灵芝酒萃物预处理24小时再以两性霉素B处理48小时,另一组则是以灵芝酒萃物及两性霉素B共同处理48小时。
在预处理实验组中,细胞先以0、1、2.5及5mg/ml的灵芝酒萃物处理24小时之后,再以0~80μM递增浓度的两性霉素B处理48小时,之后进行细胞存活率分析(MTT assay)。在共同处理实验组中,细胞则以0、1、2.5及5mg/ml的灵芝酒萃物及0~80μM递增浓度的两性霉素B共同处理48小时,之后进行细胞存活率分析(MTT assay)。细胞存活率分析是将MTT染剂(3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide)加入每一培养格并继续培养45-60分钟,之后移除培养液并置换成DMSO(dimethyl sulfoxide),再检测溶液在550nm的吸光度(optical density,OD)。
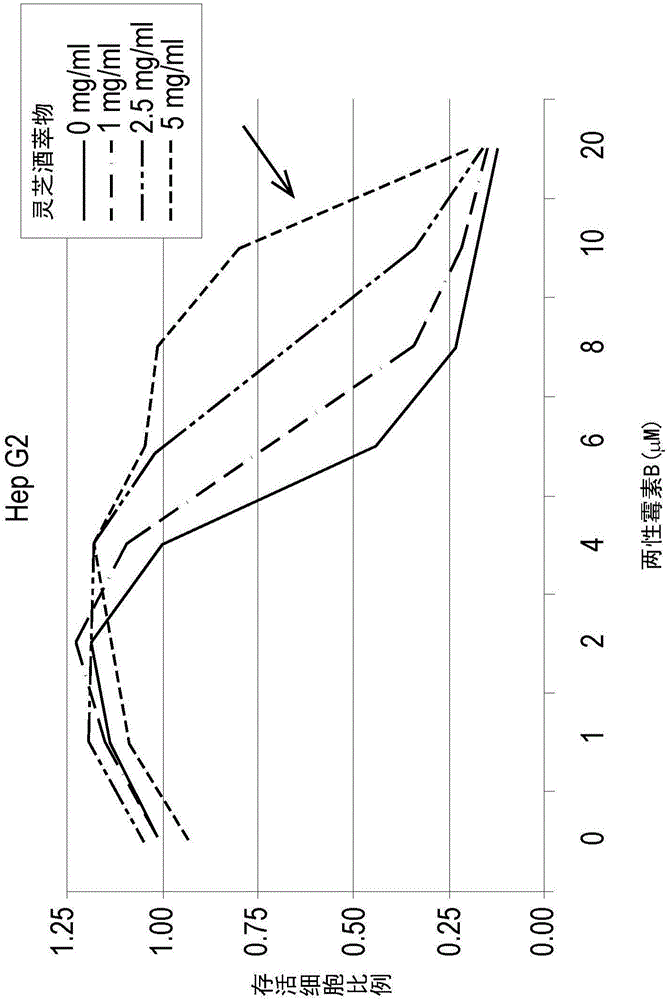
图1A及1B显示实施例1的Hep G2细胞实验结果。图1A为预处理实验组,图1B为共同处理实验组,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,四条曲线则分别为灵芝酒萃物浓度为0、1、2.5及5mg/ml的曲线。由图1A的图示结果可知,相较于灵芝酒萃物浓度为0的曲线(亦即仅以 两性霉素B处理),预先处理灵芝酒萃物1、2.5及5mg/ml皆能明显促进两性霉素B抑制Hep G2生长的能力,使得两性霉素B在用药浓度为5μM时即可抑制约75%的癌细胞生长,显现相当好的抑癌效果。然而由图1B的图示结果可知,共同处理灵芝酒萃物1、2.5及5mg/ml及两性霉素B皆明显拮抗两性霉素B抑制Hep G2生长的能力,且此一拮抗能力与灵芝酒萃物剂量成正比。
图1C及1D显示实施例1的Hep 3B细胞实验结果。图1C为预处理实验组,图1D为共同处理实验组,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,四条曲线则分别为灵芝酒萃物浓度为0、1、2.5及5mg/ml的曲线。由图1C的图示结果可知,相较于灵芝酒萃物浓度为0的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物2.5及5mg/ml皆能明显促进两性霉素B抑制Hep 3B生长的能力,且抑制能力与灵芝酒萃物剂量成正比,其中当灵芝酒萃物浓度为5mg/ml且两性霉素B浓度为10μM时可抑制约75%的癌细胞生长,显现相当好的抑癌效果。然而由图1D的图示结果可知,共同处理灵芝酒萃物及两性霉素B则无明显效果。
图1E及1F显示实施例1的Hep 5J细胞实验结果。图1E为预处理实验组,图1F为共同处理实验组,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,四条曲线则分别为灵芝酒萃物浓度为0、1、2.5及5mg/ml的曲线。由图1E的图示结果可知,相较于灵芝酒萃物浓度为0的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物5mg/ml能明显促进两性霉素B抑制Hep5J生长的能力,其中当灵芝酒萃物浓度为5mg/ml且两性霉素B浓度为10μM时可抑制超过85%的癌细胞生长,显现相当好的抑癌效果,但灵芝酒萃物1及2.5mg/ml预处理则与两性霉素B略呈拮抗效果。而由图1F的图示结果可知,共同处理灵芝酒萃物1、2.5及5mg/ml及两性霉素B皆明显拮抗两性霉素B抑制Hep 5J生长的能力,且此一拮抗能力与灵芝酒萃物剂量成正比。
由上述实施例1的结果可知,预处理灵芝酒萃物24小时后可明显促进两性霉素B对Hep G2、Hep 3B及Hep 5J等三株人类肝癌细胞的抑癌效力,然而此促进作用在共同处理时并不存在,甚至拮抗两性霉素B的抑癌效力。因此可推论,是当使用灵芝酒萃物,例如以足够剂量进行预处理,可有效促进两性霉素B抑制人类肝癌细胞的能力,故可发展为更具疗效的抗癌医药组 合物。
实施例2:
实施例2的实验方法与实施例1相同,仅为不同批次的细胞实验。
图2A及2B显示实施例2的Hep G2细胞实验结果。图2A为预处理实验组,图2B为共同处理实验组,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,四条曲线则分别为灵芝酒萃物浓度为0、1、2.5及5mg/ml的曲线。由图2A的图示结果可知,相较于灵芝酒萃物浓度为0的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物1、2.5及5mg/ml皆能明显促进两性霉素B抑制Hep G2生长的能力,且抑制能力与灵芝酒萃物剂量成正比,其中当灵芝酒萃物浓度为5mg/ml且两性霉素B浓度为4μM时可抑制约80%的癌细胞生长,显现相当好的抑癌效果。然而由图2B的图示结果可知,共同处理灵芝酒萃物1、2.5及5mg/ml及两性霉素B反而拮抗两性霉素B抑制Hep G2生长的能力。
图2C及2D显示实施例2的Hep 3B细胞实验结果。图2C为预处理实验组,图2D为共同处理实验组,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,四条曲线则分别为灵芝酒萃物浓度为0、1、2.5及5mg/ml的曲线。由图2C的图示结果可知,相较于灵芝酒萃物浓度为0的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物1、2.5及5mg/ml皆能明显促进两性霉素B抑制Hep 3B生长的能力,且抑制能力与灵芝酒萃物剂量成正比,其中当灵芝酒萃物浓度为5mg/ml且两性霉素B浓度为5μM时可抑制约75%的癌细胞生长,显现相当好的抑癌效果。而由图2D的图示结果可知,共同处理灵芝酒萃物及两性霉素B同样能明显促进两性霉素B抑制Hep 3B生长的能力。
图2E及2F显示实施例2的Hep 5J细胞实验结果。图2E为预处理实验组,图2F为共同处理实验组,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,四条曲线则分别为灵芝酒萃物浓度为0、1、2.5及5mg/ml的曲线。由图2E的图示结果可知,相较于灵芝酒萃物浓度为0的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物2.5及5mg/ml能明显促进两性霉素B抑制Hep 5J生长的能力,其中当灵芝酒萃物浓度为5mg/ml且两性霉素B浓度为5μM时可抑制约75%的癌细胞生长,显现相当好的抑癌效果,但灵芝酒 萃物1mg/ml预处理则与两性霉素B略呈拮抗效果。而由图2F的图示结果可知,共同处理灵芝酒萃物及两性霉素B反而拮抗两性霉素B抑制Hep 5J生长的能力。
由上述实施例2的结果可知,预处理灵芝酒萃物24小时后可明显促进两性霉素B对Hep G2、Hep 3B及Hep 5J等三株人类肝癌细胞的抑癌效力,与实施例1的结果近似。
根据本发明的实施例,预处理灵芝酒萃物可明显促进两性霉素B的抑癌效力,其中,灵芝酒萃物的有效浓度为1-5mg/ml,两性霉素B的有效浓度为3μM以上,但两性霉素B若剂量过高将产生较严重的副作用,因此在临床上用药剂量须小心控制,因此,根据实施例1及实施例2实验结果,安全且有效浓度约为3-10μM,且较佳为3-5μM。另外,灵芝酒萃物预处理的时间不限于24小时,亦可为12-48小时。
推论预处理灵芝酒萃物可明显促进两性霉素B的抑癌效力的原理在于,癌细胞细胞膜中的固醇组成与正常细胞有所不同,其中癌细胞的固醇具有较多的不饱和双键,因此细胞较柔软易移动与转移,正常细胞则无此现象。由于本发明的灵芝酒萃物含有真菌固醇与三萜类,且其相较于正常细胞的固醇具有更多的双键,在癌细胞快速复制分裂的过程中,容易取代癌细胞上的固醇,且由于双键更多,与两性霉素B的亲和力更大,使得两性霉素B容易与癌细胞膜上的真菌固醇结合,进而产生孔洞造成细胞膜通透性的改变,因而使癌细胞产生裂解而死亡,故达成标靶治疗的功效。由上述机制可知,本发明的抗癌医药组合物不限于用来治疗肝癌,亦可用来治疗其他癌症,例如肺癌及结肠直肠癌等。
以下实施例更进一步验证本发明是抗癌医药组合物亦可用来治疗其他癌症。
实施例3:
本实施例以A549及H460等人类肺癌细胞的细胞株来进行实验,并以96格(well)细胞培养盘进行培养。试验方法先以2.5mg/ml的灵芝酒萃物预处理24小时再以两性霉素B处理48小时。
图3A显示实施例3的A549细胞实验结果,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,线条Con为未以灵芝酒萃物预处理的曲线,线条 GT则为以2.5mg/ml的灵芝酒萃物预处理的曲线。由图3A的图示结果可知,相较于未以灵芝酒萃物预处理的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物2.5mg/ml可明显促进两性霉素B抑制A549细胞生长的能力,使得两性霉素B在用药浓度为5μM时即可抑制90%以上的癌细胞生长,显现相当好的抑癌效果。
图3B显示实施例3的H460细胞实验结果,其中横轴为两性霉素B浓度,纵轴为存活细胞比例,线条Con为未以灵芝酒萃物预处理的曲线,线条GT则为以2.5mg/ml的灵芝酒萃物预处理的曲线。由图3B的图示结果可知,相较于未以灵芝酒萃物预处理的曲线(亦即仅以两性霉素B处理),预先处理灵芝酒萃物2.5mg/ml可明显促进两性霉素B抑制H460细胞生长的能力,使得两性霉素B在用药浓度为5μM时即可抑制约85%的癌细胞生长,显现相当好的抑癌效果。
综上所述,本发明提供一种新的抗癌医药组合物,其包含灵芝萃取物及两性霉素B,其中,以灵芝萃取物对癌细胞预处理一段时间后,再加入两性霉素B,可明显增进两性霉素B的抑癌效力。换言之,灵芝萃取物及两性霉素B以分段方式给药,先以灵芝萃取物投药一预定时间后再以两性霉素B投药,以增进两性霉素B的抑癌效力。由于本发明的抗癌医药组合物较佳可抑制75%以上的癌细胞生长,且可降低两性霉素B的用药剂量,故本发明极具产业价值,爰依法提出申请。
本发明得由本领域技术人员任施匠思而为诸般修饰,然皆不脱如附权利要求书所欲保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!