一种可控制备载紫杉醇PLGA多孔微球的方法与流程
本发明涉及新型多孔微球缓释给药的制备技术领域,具体涉及载紫杉醇PLGA多孔微球的可控制备。
背景技术:
多孔微球作为一种药物新剂型,在药物新制剂的研发以及新剂型的改造方面应用广泛。目前,现有制备多孔微球的方法主要有乳化剂分散溶剂挥发法、喷雾干燥法、相分离法和熔融法等,其中最常用的是致孔剂联合乳化分散溶剂挥发法,且致孔剂多采用NH4HCO3、蔗糖、NaHCO3等。此种方法在制备多孔微球时往往微球的尺寸不可控,且孔径的直径也较大,平均孔径能达到20微米以上,从而影响了多孔微球的比表面积,降低药物吸附在多孔微球的表面或孔道内部的含量,最终影响微球制成速释或缓释制剂的药效。
技术实现要素:
为了解决现有技术存在的问题,本发明提供一种可控制备载紫杉醇PLGA多孔微球的方法。本发明以蛋白分子为致孔剂,通过控制蛋白分子的含量、成球材料的性质可控制多孔微球的直径与孔径,达到优化载药微球的性能的目的。本发明以抗肿瘤药物紫杉醇为模型药物,聚乳酸羟基乙酸(poly(lactic-co-glycolic acid),PLGA)为载体,以牛血清白蛋白(BSA)为致孔剂,采用复乳溶剂挥发法,制备PLGA多孔微球,同时可将药物吸附于多孔微球的表面或孔道内部,对孔结构的控制可实现药物释放速度的可控。另外PLGA微球中孔道结构的存在可降低微球密度,调节微球粒径和孔径可获得较为理想空气动力学性质,便于吸入给药,提高药物在肺部的沉积从而延长药物作用浓度与时间,有望用于肿瘤的吸入式给药治疗。
本发明所述一种可控制备载紫杉醇PLGA多孔微球的方法,是采用复乳溶剂挥发法,以BSA为致孔剂,PLGA为载体,将紫杉醇包裹于微球内部;将水洗沉淀物离心冷冻干燥后,最后得到载紫杉醇PLGA多孔微球。
具体包括以下步骤:
1)PLGA固体和紫杉醇固体按照一定比例溶于少量二氯甲烷溶液中,再按照一定的比例称取BSA固体溶于少量去离子水,混合后探针型超声冰浴(20s),再倒入4%PVA溶液中;
2)用均质机将混合溶液在室温条件下搅拌5min。再将上述溶液倒入0.4%PVA溶液中,在室温下机械搅拌并过夜。
3)第二天早上将混合溶液离心,水洗沉淀物,取其上清液备用最后将沉淀物冷冻干燥,获得载紫杉醇PLGA多孔微球固体粉末。
本发明所述步骤1)中,先将PLGA固体充分溶于二氯甲烷中,再加入紫杉醇充分溶于上述溶液。目的是先使PLGA在二氯甲烷中分散均匀,再将紫杉醇加入到二氯甲烷溶液中,可提高混物的均匀性。
所述步骤1)中,PLGA与紫杉醇的质量比为10:3。在此比例下,紫杉醇的载药率较10:1高,且药物释放速率和MTT实验结果显示都具有良好的药效。
所述步骤1)中,BSA与PLGA的质量比为0.6。此质量比例制备的PLGA多孔微球性能最优。
所述步骤1)中,BSA/PLGA的比值可调节为0.2,0.4,0.6。不同比例条件下,控制PLGA的分子量,LA/GA的比值不变,通过BSA/PLGA的比值改变微球粒径和孔径的大小,并考察对非小细胞型肺癌(A549)细胞的MTT实验结果。当BSA/PLGA为0.2时,如实施例一;当BSA/PLGA为0.4时,如实施例二;当BSA/PLGA为0.6时,如实施例三。
所述步骤1)中,当BSA/PLGA为0.6时。在此条件下,载紫杉醇PLGA多孔微球能够明显抑制非小细胞型肺癌(A549)细胞的生长。
本发明方法简单、环保;与现有载紫杉醇PLGA微球缓释给药系统相比,载紫杉醇PLGA多孔微球,因其比表面积的增大,可实现药物的高效负载。除此此外,本发明的关键点在于通过控制致孔剂的浓度,PLGA的分子量、LA/GA的比例,可有效控制微球的尺寸及孔径大小,以解决现有技术与手段制备的多孔微球尺寸及孔径偏大的现状,为紫杉醇的可控负载与有效缓释提供了物质与结构基础。本发明优化条件后得到的PLGA微球粒径在5-6μm左右,微球孔径为0.12-0.24μm左右,载药率为13.74%,包封率为51.10%。采用本发明制备载紫杉醇PLGA多孔微球,不仅粒径较均匀,而且多孔结构可以控制释放速度,便于吸入给药,可以有效延长药物作用时间。
附图说明
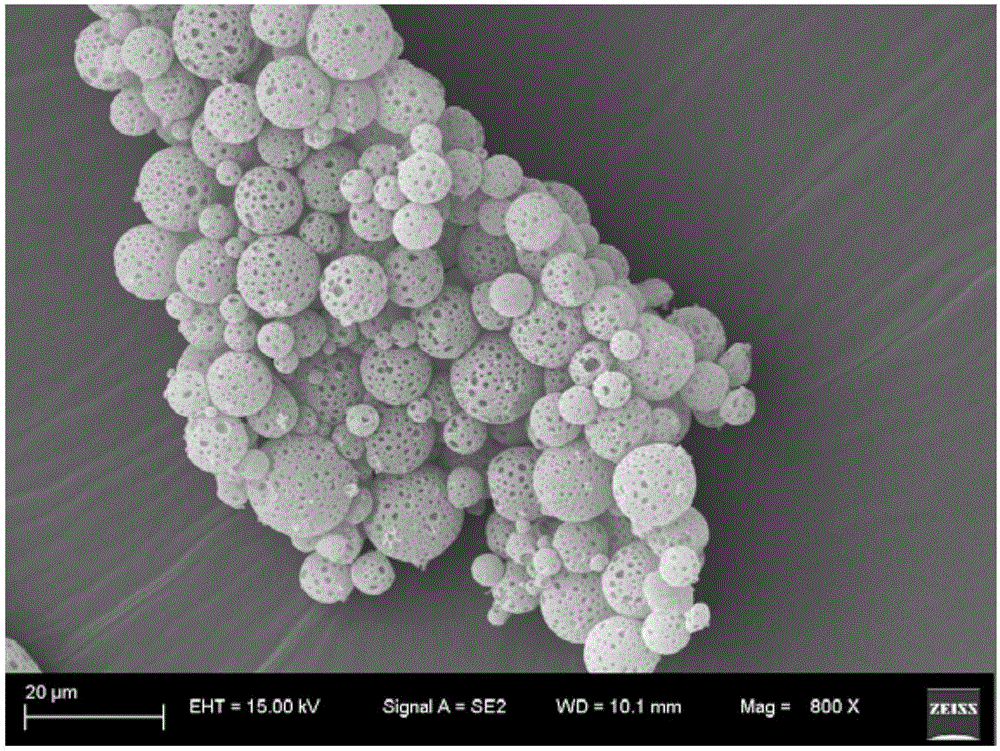
图1为采用本发明方法制备的载紫杉醇PLGA多孔微球的SEM图。
图2为采用本发明方法制备的载紫杉醇PLGA多孔微球的X-射线衍射图。
图3为采用本发明方法制备的载紫杉醇PLGA多孔微球的释放曲线图。
图4为采用本发明方法制备的载紫杉醇PLGA多孔微球MTT实验结果图,与实际载紫杉醇的量乘以第一天释放速率所得的紫杉醇的量作对照比较。
具体实施方式
一、制备工艺:
1、实施例1:
1)先将50mgPLGA固体溶于1ml二氯甲烷溶液中,再将15mg紫杉醇溶于其中,称取10mg BSA溶于0.2mL去离子水,混合后探针型超声冰浴(20s),再倒入5mL的4%PVA溶液中。
2)用均质机(转速为8000)将混合溶液在室温条件下搅拌5min。再将上述溶液倒入100mL的0.4%PVA溶液中,在室温下机械搅拌,转速为800,并过夜。
3)第二天早上将混合溶液离心,转速为6000,水洗沉淀物5次,取其上清液备用。最后将沉淀物冷冻干燥,条件为-60摄氏度,获得载紫杉醇PLGA多孔微球固体粉末。
2、实施例2:
1)先将50mg PLGA固体溶于1ml二氯甲烷溶液中,再将15mg紫杉醇溶于其中,称取20mg BSA溶于0.2mL去离子水,混合后探针型超声冰浴(20s),再倒入5mL的4%PVA溶液中。
2)用均质机,转速为8000将混合溶液在室温条件下搅拌5min。再将上述溶液倒入100mL的0.4%PVA溶液中,在室温下机械搅拌,转速为800,并过夜。
3)第二天早上将混合溶液离心,转速为6000,水洗沉淀物5次,取其上清液备用。最后将沉淀物冷冻干燥,条件为零下60摄氏度,获得载紫杉醇PLGA多孔微球固体粉末。
3、实施例3:
1)先将50mg PLGA固体溶于1mL二氯甲烷溶液中,再将15mg紫杉醇溶于其中,称取30mg BSA溶于0.2mL去离子水,混合后探针型超声冰浴(20s),再倒入5mL的4%PVA溶液中。
2)用均质机,转速为8000将混合溶液在室温条件下搅拌5min。再将上述溶液倒入100mL的0.4%PVA溶液中,在室温下机械搅拌,转速为800,并过夜。
3)第二天早上将混合溶液离心,转速为6000,水洗沉淀物5次,取其上清液备用。最后将沉淀物冷冻干燥,条件为-60摄氏度,获得载紫杉醇PLGA多孔微球固体粉末。
二、产物特性:
图1为采用本发明方法制备的载紫杉醇PLGA多孔微球的SEM图,从图中看出,载药微球大小分布,粒径孔径较为均一。
图2为采用本发明方法制备的载紫杉醇PLGA多孔微球的X-射线衍射图,根据X-射线衍射结果可知,紫杉醇以分子形式包裹于PLGA多孔微球内部。
图3为采用本发明方法制备的载紫杉醇PLGA多孔微球的释放曲线图,从图中可以看出不同投药比的载紫杉醇PLGA多孔微球释放完全约9-10天,说明载药微球具有缓释功能。
图4为采用本发明方法制备的载紫杉醇PLGA多孔微球MTT实验结果图,与实际载紫杉醇的量乘以第一天释放速率所得的紫杉醇的量作对照比较。从结果可以看出,较BSA/PLGA的比值为0.2,0.4条件下,BSA/PLGA的比值为0.6的载紫杉醇PLGA多孔微球对A549细胞有明显的抑制作用,并且与实际载药量乘以释放速率的紫杉醇对照组作比较,更加说明本设计的缓释载药微球具有一定的药效。
- 还没有人留言评论。精彩留言会获得点赞!