一种奥曲肽修饰金球壳纳米脂质体及其制备方法与流程
本发明属于医药技术领域,特别涉及一种纳米脂质体及其制备方法。
背景技术:
目前,全球范围内恶性肿瘤发病率越来越高,新药及新型疗法层出不穷,但是这些治疗手段对机体具有非常大的副作用,且大部分恶性肿瘤难以治愈,所以寻求一种特异性、安全、无副作用的癌症治疗手段仍然是全球癌症治疗的一大难题。
研究发现天然植物抗肿瘤药物的抗癌疗效显著,且毒副作用小。齐墩果酸是一种天然抗肿瘤药物,广泛分布于多种植物,如酿酒葡萄、山楂、大枣等。齐墩果酸具有多种的生物学以及药理学活性,如抗肿瘤、抗病毒、抗氧化和抗炎等。然而由于其亲水性低,生物利用度差以及血液半衰期短,至今未广泛应用。纳米脂质体是目前公认的、可提高包载药物生物利用度的新型载体系统,由于其良好的生物相容性受到社会广泛关注。然而常规脂质体载药系统又具有一系列缺陷,如不能控制释放化疗药物、靶向性不强等。癌症治疗中增加肿瘤细胞对药物的高效摄取是癌症治疗成功与否的关键步骤,药物的可控释放可以提高包载药物的生物利用度,降低毒副作用。因此,发明一种多功能脂质体,使其可控释放抗肿瘤药物,提高肿瘤细胞药物摄取率,是目前亟待解决的问题。
技术实现要素:
本发明的目的是提供一种制备方法简单、重复性高、能高效进行光热转换,且对肿瘤组织或细胞具有靶向性,提高细胞对药物的摄取率的奥曲肽修饰金球壳纳米脂质体及其制备方法。
本发明的方法主要是以齐墩果酸纳米脂质体为基础,在其表面结合一层谷胱甘肽,谷胱甘肽携带的巯基修饰到脂质体表面,使制备的金纳米粒子易与其结合,在温和条件下避光孵育,得到光热转化性能良好且可控释放药物的纳米金球壳包覆的齐墩果酸脂质体。由于奥曲肽上具有氨基、羟基等基团,在一定条件下,将纳米金球壳包覆的脂质体与奥曲肽水溶液共孵育,使奥曲肽包覆在金球壳表面,得到具有靶向性能、可控释放、光热转换、化学治疗的多功能脂质体。
本发明的奥曲肽修饰金球壳纳米脂质体是一种在齐墩果酸纳米脂质体表面形成一层致密的纳米金球壳,然后在金球壳表面包覆奥曲肽配体的脂质体,其粒径为50-200nm,表面等离子共振吸收波长为650-950nm。
本发明的制备方法如下:
(1)制备金球壳纳米脂质体
①原料:胆固醇、大豆卵磷脂、齐墩果酸、谷胱甘肽,氯化金,奥曲肽;
②按胆固醇:大豆卵磷脂:齐墩果酸按质量比1~3:7~14:1的比例,将它们磁力搅拌溶解于无水乙醇中,每毫升无水乙醇加入上述3种混合物18~54mg,形成脂质乙醇溶液;按每毫升磷酸缓冲液加入0.3~0.6mg谷胱甘肽的比例,将谷胱甘肽溶解到pH为6.0~7.0的磷酸缓冲液,作为水化介质;按脂质乙醇溶液与水化介质的体积比为1:4~10,将脂质乙醇溶液逐滴滴入35~55℃的水化介质中,滴加过程中磁力搅拌器缓慢搅拌,得到脂质体悬液;搅拌1~2小时除去无水乙醇,得到齐墩果酸纳米脂质体;
③在-20℃低温条件下,将30~80μL浓度为230~270mM的硼氢化钠(NaBH4)溶液迅速滴加到浓度为0.1~1.5mM的氯化金溶液中,每毫升氯化金溶液中含5~10μL硼氢化钠溶液,剧烈摇晃,反应1~8min后,得到粒径在5-10nm的金纳米粒子溶液;
④采用晶种生长法,将步骤③得到的金纳米粒子溶液与步骤②制得的齐墩果酸纳米脂质体以1:1~5的体积比混合,置于摇床,25~30℃,90~140rpm,避光孵育10~25h,即得到金纳米粒子包覆的齐墩果酸脂质体。
⑤向步骤④制得的金纳米粒子包覆的齐墩果酸脂质体中按体积比1:1~6的比例加入浓度为1~6mM AuCl3溶液,混合均匀,在室温条件下,再加入浓度为35~90mM硼氢化钠溶液,硼氢化钠溶液与上述混合液的体积比为3~8:100,摇晃均匀,将其置于摇床,25~30℃,90~140rpm,孵育5~15h,即制得纳米金球壳包覆的齐墩果酸脂质体。
(2)制备奥曲肽修饰的纳米金球壳脂质体
①将奥曲肽用去离子水溶解,水浴超声0.5~2min,配制成浓度为1~5mg/mL的奥曲肽溶液;
②用共孵育法,将步骤(1)得到的纳米金球壳包覆的齐墩果酸脂质体与步骤①配制的奥曲肽溶液,按体积比1:0.3~1混合均匀,制得脂质体/奥曲肽混悬液;
③将步骤②制备的脂质体/奥曲肽混悬液置于摇床25~30℃,90~140rpm,孵育2~20小时,得到奥曲肽修饰的金球壳纳米脂质体。
本发明与现有技术相比具有以下优点:
1、制备方法在常温、常压及温和条件下完成,所需实验条件温和,操作简便,易于控制,重复性高。
2、制备的金球壳纳米脂质体具有理想的形貌,粒径分布在50-200nm之间,不仅通过渗透和滞留增强效应更易于在肿瘤部位积累,达到更好的治疗效果,还具有极佳的光热转换性能,使包载的齐墩果酸实现可控释放。
3、在金球壳纳米脂质体基础上,对其进一步修饰肿瘤特异性配体奥曲肽,采用“受体-配体”相互作用基本原理,使其具有靶向性,提高肿瘤细胞对药物的摄取率。
4、制备的奥曲肽修饰的金球壳纳米脂质体在奥曲肽特异性配体作用下,可以靶向到达肿瘤细胞,近红外激光照射下能很好的将化学治疗和光热治疗、控制释放结合在一起,不仅可以高效进行癌症治疗,且无毒副作用,减小了对正常组织和细胞的损伤。
附图说明
图1是本发明实施例1制得的齐墩果酸纳米脂质体透射电子显微镜图。
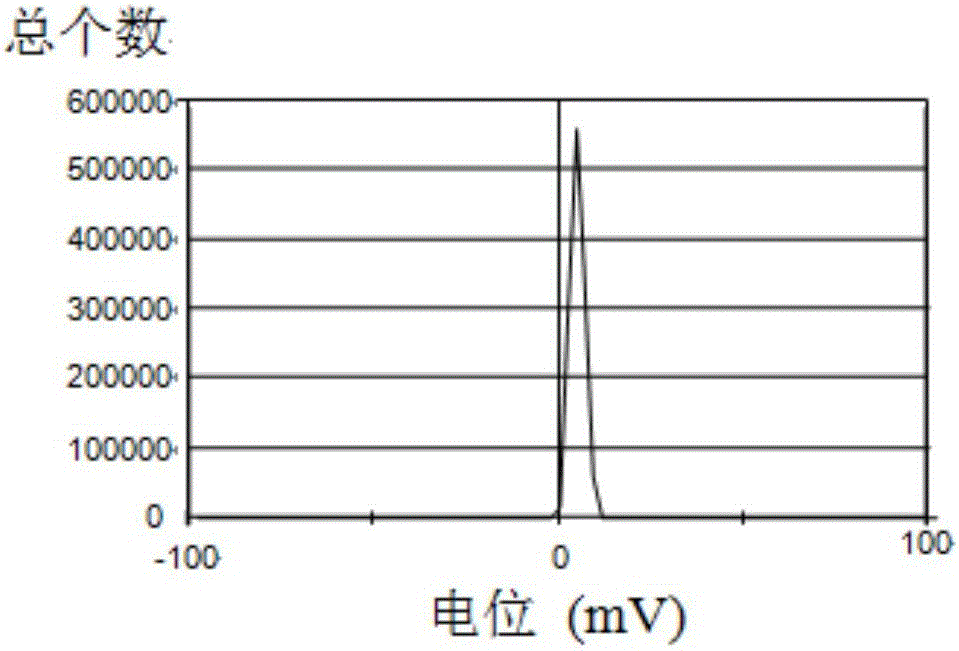
图2是本发明实施例1制得的金球壳纳米脂质体透射电子zeta电位图。
图3是本发明实施例1制得的奥曲肽修饰金球壳纳米脂质体粒径分布图。
图4是本发明实施例2对比的普通脂质体光热转换结果图。
图5是本发明实施例2制得的奥曲肽修饰金球壳纳米脂质体光热转换结果图。
图6是本发明实施例3制得的奥曲肽修饰的金球壳纳米脂质体竞争抑制性实验结果图。
具体实施方式
实施例1
将14mg大豆卵磷脂(购自沈阳天峰生物制药有限公司)、2.0mg胆固醇(购自天津市大茂化学仪器供应站)和2.0mg齐墩果酸(购自四川什邡市华康药物原料厂),溶解于1mL无水乙醇中,通过磁力搅拌得到脂质乙醇溶液;将1.2mg谷胱甘肽溶于4mL pH=6.0磷酸缓冲液中作为水化介质,在磁力搅拌下,将1mL脂质乙醇溶液匀速逐滴滴入到4mL 35℃的水化介质中,得到脂质体悬液;然后搅拌1小时除去脂质体悬液中的无水乙醇,得到谷胱甘肽修饰的齐墩果酸纳米脂质体;
在-20℃低温条件下,将30μL浓度为240mM的硼氢化钠(NaBH4)溶液,迅速滴加到1mL 0.1mM的氯化金溶液中,剧烈摇晃,反应1min后,即得到粒径在5-10nm的金纳米粒子溶液,4℃贮存备用;
将得到的金纳米粒子溶液与齐墩果酸纳米脂质体以1:1的体积比混合,置于摇床,25℃,90rpm,避光孵育10h,即得到金纳米粒子包覆的齐墩果酸脂质体;
向金纳米粒子包覆的齐墩果酸脂质体中按体积比1:1的比例加入浓度为1mM的AuCl3溶液,混合均匀,在室温条件下,再加入浓度为35mM的硼氢化钠溶液,硼氢化钠溶液与上述混合液的体积比为3:100,摇晃均匀,将其置于摇床,25℃,90rpm,孵育5h,即制得纳米金球壳包覆的齐墩果酸脂质体。
将奥曲肽用去离子水溶解,水浴超声0.5min,配制成浓度为1mg/mL的奥曲肽溶液;采用共孵育法,将得到的纳米金球壳包覆的齐墩果酸脂质体按体积比1:0.3的比例与奥曲肽溶液混合,制得脂质体/奥曲肽混悬液;将脂质体/奥曲肽混悬液置于摇床,25℃,90rpm,孵育2h得到奥曲肽修饰的金球壳纳米脂质体。
应用透射电子显微镜对奥曲肽修饰的金球壳纳米脂质体进行形貌表征,如图1所示,奥曲肽修饰的金球壳纳米脂质体呈球形,形貌规则,在其表面有可观察到一层致密的纳米金球壳。利用激光粒度仪检测奥曲肽修饰的金球壳纳米脂质体带电荷状态和粒径分布情况,如图2和图3所示,由于纳米金球壳带负电荷,奥曲肽带正电荷,从图2中可以看出脂质体带正电荷,证明奥曲肽成功修饰到金球壳纳米脂质体上;从图3中可以看出奥曲肽修饰的金球壳纳米脂质体粒径分布在50-200nm左右,证明奥曲肽修饰的金球壳纳米脂质体粒径均匀,分散性良好。
实施例2
将25mg大豆卵磷脂(购自沈阳天峰生物制药有限公司)、5mg胆固醇(购自天津市大茂化学仪器供应站)和2.5mg齐墩果酸(购自四川什邡市华康药物原料厂),溶解于1mL无水乙醇中,通过磁力搅拌得到脂质乙醇溶液;将3.5mg谷胱甘肽溶于7mL pH=6.5磷酸缓冲液中作为水化介质,在磁力搅拌下,将1mL脂质乙醇溶液匀速逐滴滴入到7mL 45℃的水化介质中,得到脂质体悬液;然后搅拌1.5小时除去脂质体悬液中的无水乙醇,得到谷胱甘肽修饰的齐墩果酸纳米脂质体;
在-20℃低温条件下,将50μL浓度为250mM的硼氢化钠(NaBH4)溶液,迅速滴加到1mL 0.7mM的氯化金溶液中,剧烈摇晃,反应4min后,即得到粒径在5-10nm的金纳米粒子溶液,4℃贮存备用;
将得到的金纳米粒子溶液与齐墩果酸纳米脂质体以1:3的体积比混合,置于摇床,28℃,110rpm,避光孵育15h,即得到金纳米粒子包覆的齐墩果酸脂质体。
向金纳米粒子包覆的齐墩果酸脂质体中按体积比1:3的比例加入浓度为3mM的AuCl3溶液,混合均匀,在室温条件下,再加入浓度为55mM硼氢化钠溶液,硼氢化钠溶液与上述混合液的体积比为5:100,摇晃均匀,将其置于摇床,28℃,110rpm,孵育10h,即制得纳米金球壳包覆的齐墩果酸脂质体;
将奥曲肽用去离子水溶解,水浴超声1.0min,配制成浓度为3mg/mL的奥曲肽溶液;采用共孵育法,将得到的纳米金球壳包覆的齐墩果酸脂质体按体积比1:0.5的比例与奥曲肽溶液混合,制得脂质体/奥曲肽混悬液;将脂质体/奥曲肽混悬液置于摇床,28℃,110rpm,孵育10h得到奥曲肽修饰的金球壳纳米脂质体。
利用近红外激光器(808nm,1.5W)检测奥曲肽修饰的金球壳纳米脂质体光热效果,如图4和图5所示,从图4中可以看出普通脂质体在激光照射10分钟后,温度变化不大,升高3℃左右,图5为奥曲肽修饰的金球壳纳米脂质体,在照射10分钟后,温度升高到69.9℃,在此温度下可以杀死癌细胞,证明金球壳包覆脂质体后具有光热效果,且光热转换性能良好。
实施例3
将42mg大豆卵磷脂(购自沈阳天峰生物制药有限公司)、9.0mg胆固醇(购自天津市大茂化学仪器供应站)和3.0mg齐墩果酸(购自四川什邡市华康药物原料厂),溶解于1mL无水乙醇中,通过磁力搅拌得到脂质乙醇溶液;将6.0mg谷胱甘肽溶于10mL pH=7.0磷酸缓冲液中作为水化介质,在磁力搅拌下,将1mL脂质乙醇溶液匀速逐滴滴入到10mL 55℃的水化介质中,得到脂质体悬液;然后搅拌2小时除去脂质体悬液中的无水乙醇,得到谷胱甘肽修饰的齐墩果酸纳米脂质体;
在-20℃低温条件下,将80μL浓度为270mM的硼氢化钠(NaBH4)溶液,迅速滴加到1mL 1.5mM的氯化金溶液中,剧烈摇晃,反应8min后,即得到粒径在5-10nm的金纳米粒子溶液,4℃贮存备用;
将得到的金纳米粒子溶液与齐墩果酸纳米脂质体以1:5的体积比混合,置于摇床,30℃,140rpm,避光孵育25h,即得到金纳米粒子包覆的齐墩果酸脂质体。
向金纳米粒子包覆的齐墩果酸脂质体中按体积比1:6的比例加入浓度为6mM的AuCl3溶液,混合均匀,在室温条件下,再加入浓度为90mM的硼氢化钠溶液,硼氢化钠溶液与上述混合液的体积比为8:100,摇晃均匀,将其置于摇床,30℃,140rpm,孵育15h,即制得纳米金球壳包覆的齐墩果酸脂质体。
将奥曲肽用去离子水溶解,水浴超声2min,配制成浓度为5mg/mL的奥曲肽溶液;采用共孵育法,将得到的纳米金球壳包覆的齐墩果酸脂质体按体积比1:1的比例与奥曲肽溶液混合,制得脂质体/奥曲肽混悬液;将脂质体/奥曲肽混悬液置于摇床,30℃,140rpm,孵育20h得到奥曲肽修饰的金球壳纳米脂质体。
利用MTT法通过竞争抑制实验检测奥曲肽修饰的金球壳纳米脂质体靶向细胞能力,如图6所示,可以看出奥曲肽修饰脂质体后可以显著提高细胞毒性,加入竞争抑制剂奥曲肽后,奥曲肽修饰脂质体与普通脂质体对细胞毒性没有差异,证明奥曲肽修饰的金球壳纳米脂质体具有靶向性,可以抗肿瘤药物的治疗效果。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种磁性纳米粒子与超滤膜结合处理废弃乳化液的方法与流程
- 一种多肽修饰纳米粒子在制备治疗急性肺损伤的药物中的应用的制作方法与工艺
- 一种金纳米花修饰的离子液体功能化石墨烯纸电极、其制备方法和应用与流程
- 一种新型的透明质酸修饰的多级纳米颗粒及其制备与应用的制作方法与工艺
- 一种核壳结构的磁性纳米粒子及其制备与应用的制作方法与工艺
- 一种室温固相反应制备的纳米铁修饰的铁基氨合成催化剂及其制备方法和应用与流程
- 一种丁氧基修饰的TiO2单晶空心四方纳米锥材料、制备方法及其应用与流程
- 一种改性粒子修饰的有机无机杂化聚合物涂料的制作方法与工艺
- 一种表面修饰片状纳米铜及含有该纳米铜的复合润滑油的制备方法与流程
- 一种用于简便修饰磁性纳米粒子的手性拆分添加剂的制备和应用的制作方法与工艺