一种修复型球囊导管及其制备方法与流程
本发明属于医疗技术领域,尤其涉及一种修复型球囊导管及其制备方法。
背景技术:
在阶段,人们较常出现在血管内的某处形成狭窄或者闭塞部,会造成血液、流动变差,造成血栓或者血管狭窄的问题。现在广泛实行如下治疗方法:将导丝插入狭窄或者闭塞的部位,然后通过跟随导丝的修复型球囊导管对狭窄或者闭塞的部位进行扩张。
一般情况下,球囊扩张导管扩充时,因为血管所承受的内应力比较小,当球囊扩充到一定程度时,血管内膜易产生撕裂,进而导致血栓及血管内再狭窄等问题。现有技术中,主要采用药物球囊来解决该问题,比如雷帕霉素和紫杉醇,但使用药物球囊的患者,需长时间服用抗双重抗血小板药预防血管内血栓,长时间的药物服用易对肝、肾造成损害,对人体健康极为不利。
技术实现要素:
本发明提供一种结构简单、使用方便且可以有效防止血管内膜撕裂的修复型球囊导管及其制备方法。
本发明通过以下技术方案实现:
一种修复型球囊导管,其包括依次相连的针座、海波管、导管组、球囊以及尖端管,所述球囊上套设有壳聚糖生物胶管,所述针座与所述海波管的交接处套设有应力释放胶套,所述壳聚糖生物胶管外部设置有凝胶层,所述聚糖生物胶管的内壁设置有抗凝血涂层。
进一步的,所述导管组包括内管和套设于所述内管上的外管,所述内管与所述外管通过热焊接的方式焊接连接。
进一步的,所述球囊采用尼龙原料制成,在标准大气压下,所述球囊的长度为8至18毫米,所述球囊的外径为2至5毫米。
进一步的,所述球囊靠近所述针座一端为球囊近端,所述球囊远离所述针座的一端为球囊远端,所述球囊近端和所述球囊远端分别与所述外管和所述内管通过激光焊接的方式连接。
进一步的,所述海波管的一端与所述导管组通过热焊接的方式连接,所述海波管的另一端与所述针座通过紫外线焊接的方式连接。
进一步的,所述修复型球囊导管还包括设置于所述尖端导管及所述壳聚糖生物胶管的外侧且与所述尖端导管相连的导向丝。
进一步的,所述壳聚糖生物胶管采用热固定的方式固定于折叠后的球囊上。
进一步的,所述壳聚糖生物胶管由脱乙酰度为25%-95%、分子量为(110-150)×104Da的壳聚糖原料制成。
进一步的,所述凝胶层为壳聚糖或者甲壳素或者两者组合所形成的凝胶层;所述抗凝血涂层为雷帕霉素抗凝血涂层或者紫杉醇抗凝血涂层。
一种修复性修复型球囊导管的制备方法,包括上述的任意一项所述的修复型球囊导管,所述方法包括以下步骤:
步骤(1):将海波管的一端伸入针座,并通过紫外线焊接的方式将海波管和针座焊接连接,使两者紧密连接不透气;
步骤(2):将应力释放胶套套设在针座和海波管的连接处,防止海波管打折;
步骤(3):通过热焊接的方式将海波管的另一端与导管组一端焊接连接;
步骤(4):将球囊两端的管脚切除保留2至5毫米,将导管组插入球囊一端的管脚内,并通过激光焊接的方式将导管组和球囊焊接连接;
步骤(5):将尖端导管的一端插入球囊另一端的管脚内,并通过激光焊接的方式将尖端导管和球囊焊接连接;
步骤(6):将球囊在折叠机上折叠,形成折叠状态的球囊;
步骤(7):采用直接插入法或者卷曲法或者湿法纺丝制备壳聚糖胶套;
步骤(8):在壳聚糖胶套内部使用喷涂或者浸泡的方法涂敷雷帕霉素或者紫杉醇形成抗凝血涂层;
步骤(9):将壳聚糖生物胶套设在折叠后的球囊上,热定型控制壳聚糖生物胶管和球囊之间的粘着力;
步骤(10):在固定好的壳聚糖胶管上,喷涂壳聚糖或者甲壳素或者两者结合形成凝胶层,得到修复型球囊导管。
与现有技术相比,通过本发明的修复型球囊导管的制备方法制得的修复型球囊导管,在医生或者别的操作人员的操作下进入人体的血管内,球囊扩张时,壳聚糖生物胶管因自身的粘附力和内应力的作用下贴附在血管内壁上,由于壳聚糖具有促进伤口愈合性、可降解吸收性和良好的生物相容性,故当其作用在撕裂的血管内膜上时,可慢慢修复该撕裂创口,且在三十天之内可以完成血管内膜的修复,并且在血管内降解吸收完全,在防止血栓和血管再狭窄的同时对血管起到保护及修复的作用。
附图说明
此处所说明的附图用来提供对本发明的进一步理解,构成本发明的一部分,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
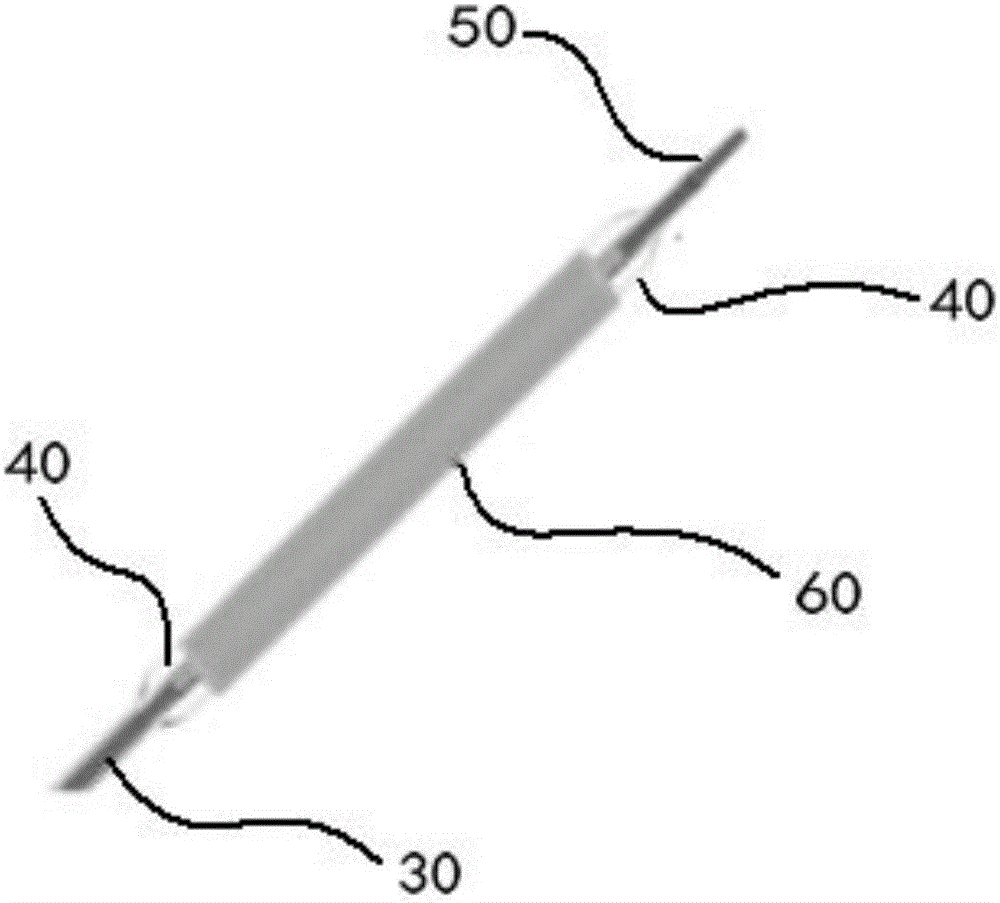
图1是本发明提供的修复型球囊导管的示意图;
图2是图1中A处的放大图;
图3是本发明提供的修复型球囊导管的针座的示意图;
图4是本发明提供的修复型球囊导管的应力释放胶套的示意图;
图5是本发明提供的修复型球囊导管的尖端导管与球囊交接处的结构图;
图6是本发明提供的修复型球囊导管带有导向丝的示意图;
图中标记为:修复型球囊导管100,针座10,应力释放胶套11,海波管20,导管组30,球囊40,尖端管50,壳聚糖生物胶管60,导向丝70。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
如图1至图5所示,一种修复型球囊导管100,其包括依次相连的针座10、海波管20、导管组30、球囊40及尖端导管50,针座10与海波管20的交接处套设有应力释放胶套11,球囊40上套设有壳聚糖生物胶管60;壳聚糖生物胶管60外部设置有凝胶层(未图示),聚糖生物胶管60的内壁设置有抗凝血涂层(未图示)。
当修复型球囊导管100在医生或者别的操作人员的操作下进入人体的血管内,球囊40扩张时,壳聚糖生物胶管60在其外部的凝胶层的粘附力和内应力的作用下贴附在血管内壁上,由于壳聚糖具有促进伤口愈合性、可降解吸收性和良好的生物相容性,故当其作用在撕裂的血管内膜上时,可慢慢修复该撕裂创口,且在30天之内可以完成血管内膜的修复,并且在血管内降解吸收完全,壳聚糖生物胶管60内壁上的抗凝血涂层为雷帕霉素或者紫杉醇的抗凝血涂层,在防止血栓和血管再狭窄的同时对血管起到保护及修复的作用。
以下对本发明的修复型球囊导管100进行详细说明。
如图1至图5所示,针座10可以是内圆锥鲁尔接头,是用于与外部充压装置连接的零件,可保证修复型球囊导管100与外部充压装置在高压的情况下还能紧密连接。其主要材料是医用级热塑聚碳酸酯,长度约为45mm。
海波管20可以由不锈钢材料制成,长度为800至1300毫米。作为本发明的优选实施方式,海波管20的长度约为1100毫米,满足使用需求。不锈钢材料的海波管20具有抗酸、抗碱、抗各种有机溶剂的优点,使得修复型球囊导管100在血管中的阻力较小,且稳定性好。海波管20的一端通过紫外线焊接的方式与针座10焊接连接。
导管组30包括内管及套设于内管上的外管,内管包括三层,由内向外依次为尼龙、高密度聚乙烯和塑胶。外管为尼龙材料,长度为300至350毫米,作为本发明的优选实施方式,外管的长度为325毫米。内管与外管采用热焊接的方式焊接连接。
应力释放胶套11为磷酸三苯脂制成,长度约为30至40毫米,作为本发明的优选实施例,应力释放胶套11的长度为36毫米。应力释放胶套11一端固定在针座10上,另一端紧紧套住海波管20。其作用主要是让导管组30更方便的进入血管内,加强其可控性。
尖端管50包括三层,由内而外依次为高密度聚乙烯、尼龙弹性体以及塑胶。导管组30的内管与尖端管50通过激光焊接的方式焊接连接。
如图1及图2所示,球囊40采用尼龙原料制成,在标准大气压下,球囊40的长度为8至18毫米,球囊40的外径为2至5毫米。更进一步的,球囊40的长度可以为8毫米或者10毫米或者12毫米或者15毫米或者18毫米;其分别通过激光焊接和热焊接的方式与外管和尖端管进行连接。球囊40主要起扩充病变处血管并将壳聚糖生物胶管60固定在血管内壁上的作用。
壳聚糖生物胶管60的主要材料是壳聚糖,其为固定内、外径的生物管材,且内、外表面分别设置有坑凝血涂层和凝胶层,通过热处理壳聚糖胶管使其固定在折叠后的球囊40上面。壳聚糖生物胶管60在球囊40扩充时,因自身力学性质和外壁凝胶层的粘附性粘贴在血管内壁上。由于壳聚糖具有促进伤口愈合性、可降解吸收性和良好的生物相容性,故当其作用在撕裂的血管内膜上时,可慢慢修复该撕裂创口,且在三十天之内可以完成血管内膜的修复,并且在血管内降解吸收完全;抗凝血涂层在防止血栓和血管再狭窄的同时对血管起到保护及修复的作用。壳聚糖生物胶管60可以采用直接插入法制备、卷曲法制备或者湿法纺丝制备而成。
结合图6所示,为了增强修复型球囊导管100的强度,防止其发生变形,还可以在修复型球囊导管100的尖端导管50及导管组30处设置导向丝70对其进行导向。具体的,导向丝70可以包括一个或者多个,导向丝70的截面可以为圆形、三角形、四边形或者四边形以上,导向丝70可以先贯穿导管组30的内部后,再绕经球囊40的外部,最后穿过尖端导管50的内部并与尖端导管15的顶端相连。
本发明的修复型球囊导管100的制备方法包括以下步骤:
步骤(1):将海波管20的一端伸入针座10,并通过紫外线焊接的方式将海波管20和针座10焊接连接,使两者紧密连接且不透气;
步骤(2):将应力释放胶套11套装在针座10和海波管20的连接处,防止海波管20打折;
步骤(3):通过热焊接的方式将海波管20的另一端与导管组30一端焊接连接;
步骤(4):将球囊40两端的管脚切除保留2至5毫米,将导管组30插入球囊40一端的管脚内,并通过激光焊接的方式将导管组30和球囊40焊接连接;
步骤(5):将尖端导管50的一端插入球囊40另一端的管脚内,并通过激光焊接的方式将尖端导管50和球囊40焊接连接;
步骤(6):将球囊40在折叠机上折叠,形成折叠状态的球囊;
步骤(7):采用直接插入法或者卷曲法制备或者湿法纺丝制备壳聚糖胶套60;
步骤(8):在壳聚糖胶套60内部使用喷涂或者浸泡的方法涂敷雷帕霉素或者紫杉醇等抗凝血药物形成抗凝血涂层;
步骤(9):将壳聚糖生物胶60套设在折叠后的球囊40上,热定型控制壳聚糖生物胶管60和球囊40之间的粘着力。
步骤(10):在固定好的壳聚糖胶管60上,喷涂壳聚糖或者甲壳素形成凝胶层,得到修复型球囊导管100。凝胶层增加了壳聚糖胶管60的粘性,便于手术过程中壳聚糖胶管60和血管内部贴合的更好。
通过本发明的修复型球囊导管的制备方法制得的修复型球囊导管100,当修复型球囊导管100在医生或者别的操作人员的操作下进入人体的血管内,球囊40扩张时,壳聚糖生物胶管60在其外部的凝胶层的粘附力和内应力的作用下贴附在血管内壁上,由于壳聚糖具有促进伤口愈合性、可降解吸收性和良好的生物相容性,故当其作用在撕裂的血管内膜上时,可慢慢修复该撕裂创口,且在30天之内可以完成血管内膜的修复,并且在血管内降解吸收完全,壳聚糖生物胶管60内壁上的抗凝血涂层为雷帕霉素或者紫杉醇的抗凝血涂层,在防止血栓和血管再狭窄的同时对血管起到保护及修复的作用。
与现有技术相比,本发明修复型球囊导管100具有以下优点:(1)本发明的壳聚糖生物胶管60主要成分是壳聚糖,有促进伤口愈合的效果;(2)本发明的壳聚糖生物胶管60和球囊40可以分离,喷涂在球囊40的药物药量可以调节,即施加在病变部位的药量可以调节,从而疗效更加稳定;(3)本发明的修复性球囊内壁可以涂敷抗凝血涂层,在外层加速了伤口愈合的同时,内壁可以持续抑制血栓的形成,具有药物球囊的效果。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!