溶液‑颗粒相转变型抗肿瘤药物传递系统及其制备方法与流程
本发明属于药品、生物制品及保健品技术领域,具体地说,本发明涉及一种“溶液-颗粒”相转变型抗肿瘤药物传递系统及其制备方法。
背景技术:
目前癌症仍是尚未解决的全球性医疗难题。纳米药递送系统作为抗肿瘤药物载体被寄予厚望,以期通过纳米载体靶向递送药物,提高疗效,降低对正常组织的毒副作用。抗肿瘤药物治疗目标是抑制或杀伤肿瘤细胞,不具备靶向性的抗肿瘤药物对正常组织有严重不良反应,临床报告表现为骨髓抑制、肝脏毒性、神经系统毒性、胃肠道反应等。不良反应的发生导致药物疗效降低甚至治疗被迫终止。目前肿瘤靶向药物递送系统的研究主要基于以下两种理论:(1)增强渗透和滞留(epr)效应;由于肿瘤组织血管的高通透性,可致纳米制剂被动滞留于肿瘤部位,也称为被动靶向。(2)抗体或配体导向。纳米药物递送系统表面修饰抗体或配体如rgd、egf、叶酸、转铁蛋白等配体,可通过结合肿瘤细胞高表达的抗原或受体而靶向递送抗肿瘤药物至肿瘤组织,称为主动靶向。然而多量研究显示无论是基于epr效应的被动靶向还是抗体或配体修饰的主动靶向纳米制剂,由于其颗粒结构,肝脏蓄积量均高达60-90%。由此可见,纳米制剂肝脏蓄积是阻碍制剂发挥靶向作用的关键因素之一,限制了其临床疗效。需要从纳米制剂的源头设计上来突破这个局限性。
技术实现要素:
基于此,为了克服上述现有纳米靶向制剂颗粒结构导致蓄积于非靶组织的缺陷,提供了一种新的“溶液-颗粒”相转变型抗肿瘤药物传递系统及其制备方法。
为了实现上述发明目的,本发明采取了以下技术方案:
一种“溶液-颗粒”相转变型抗肿瘤药物传递系统,所述传递系统由质量比为1~20:1~10:1~20的大分子骨架、两性分子链段和连接臂组成,所述连接臂为缩水甘油醚类分子。
在其中一些实施例中,所述大分子骨架、两性分子链段和连接臂的质量比为1~5:1~3:1~5。
在其中一些实施例中,所述大分子骨架、两性分子链段和连接臂的质量比为1~4:1~2:1~4。
在其中一些实施例中,所述含有氨基的大分子骨架为聚乙烯亚胺、聚氨基酸、壳聚糖、聚α羟基酸、聚丙烯酸、聚丙烯酰胺中的一种或多种。
在其中一些实施例中,所述大分子骨架为聚乙烯亚胺,分子量为400-100000da。
在其中一些实施例中,所述大分子骨架为聚氨基酸,分子量为1000-200000da。
在其中一些实施例中,所述缩水甘油醚类分子为乙二醇二缩水甘油醚类、烯丙基缩水甘油基醚、丙三醇缩水甘油醚、烷基缩水甘油醚中的一种或多种。
在其中一些实施例中,所述两性分子链段为带有氨基和羧基的分子,为氨基酸、两性磷酸胆碱衍生物、含磺酸盐基两性分子中的一种或多种。
在其中一些实施例中,所述氨基酸为半胱氨酸、谷氨酰胺、谷氨酸、组氨酸、天冬氨酸、精氨酸、蛋氨酸、赖氨酸、脯氨酸、甘氨酸、缬氨酸中的一种或多种。
本发明还提供了上述“溶液-颗粒”相转变型抗肿瘤药物传递系统的制备方法,包括以下步骤:
(1)、制备大分子骨架-连接臂:
将连接臂缩水甘油醚类分子溶于甲醇中得到质量体积浓度为0.01-0.5g/ml的缩水甘油醚类分子溶液,将含有氨基的大分子骨架溶于去离子水中得到质量体积浓度为0.01-1g/ml的大分子骨架溶液,按体积比1:10~5:1将大分子骨架溶液在机械搅拌下缓慢滴入缩水甘油醚类分子溶液中,20-80℃反应2-12小时,随后透析纯化,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将两性分子链段溶解于甲醇/tris-hcl水溶液中得到质量体积浓度为0.01-0.5g/ml的两性分子链段溶液,加入质量体积浓度为0.1-5%的偶氮二异丁腈溶解;在搅拌下将其缓慢加入到质量体积浓度为0.01-0.5g/ml的大分子骨架-连接臂水溶液中,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为1:1:1-10:1:1,在氮气保护下于20-80℃反应4-24小时,反应结束后透析纯化,冻干得大分子骨架-连接臂接枝两性分子,即为“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述药物传递系统中,大分子骨架、两性分子链段和连接臂的质量比为1~20:1~10:1~20,所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为1:1~10。
本发明还提供了上述制备方法制备得到的“溶液-颗粒”相转变型抗肿瘤药物传递系统,制备得到的大分子骨架-连接臂接枝两性分子(即“溶液-颗粒”相转变型抗肿瘤药物传递系统)在中性介质中(ph~7.4)如体外或血液循环,体系中两性链段分子的氨基和羧基均质子化,体系呈溶液,而非现有纳米制剂的颗粒状,溶液体系与细胞相互作用弱,避免非靶部位的摄取和蓄积,且具有抗非特异性吸附特性;在弱酸性条件下(ph6.0~6.8)如肿瘤微环境,两性链段分子羧基质子化程度降低,疏水性增加,触发体系相转变,形成粒径大小范围在10-500nm的正电荷纳米粒,粘附肿瘤相关细胞,被靶细胞快速摄取,富集于肿瘤组织,有利于抗肿瘤药物靶向递送。
与现有纳米制剂相比,本发明具有以下有益效果:
1、本发明的“溶液-颗粒”相转变型抗肿瘤药物传递系统,使单一载体组成既能在血循环中以亲水溶液态逃避调理素作用和肝脏蓄积,又能在肿瘤靶组织以颗粒态高效粘附肿瘤细胞,增强靶细胞摄取,达到结构简单智能递药的目的;
2、本发明的“溶液-颗粒”相转变型抗肿瘤药物传递系统在体外和到达肿瘤靶部位之前为溶液态,制备、灭菌和贮存无需考虑粒径控制问题,体内转运避免异体颗粒易被调理清除,可以克服现有纳米粒制剂不足,有利于开发和临床应用前景;
3、本发明的“溶液-颗粒”相转变型抗肿瘤药物传递系统的制备过程中不需要大量表面活性剂,有利于降低系统毒性提高安全性;也不需要高剪切机械力耗能,制备简单,便于工业化生产。
附图说明
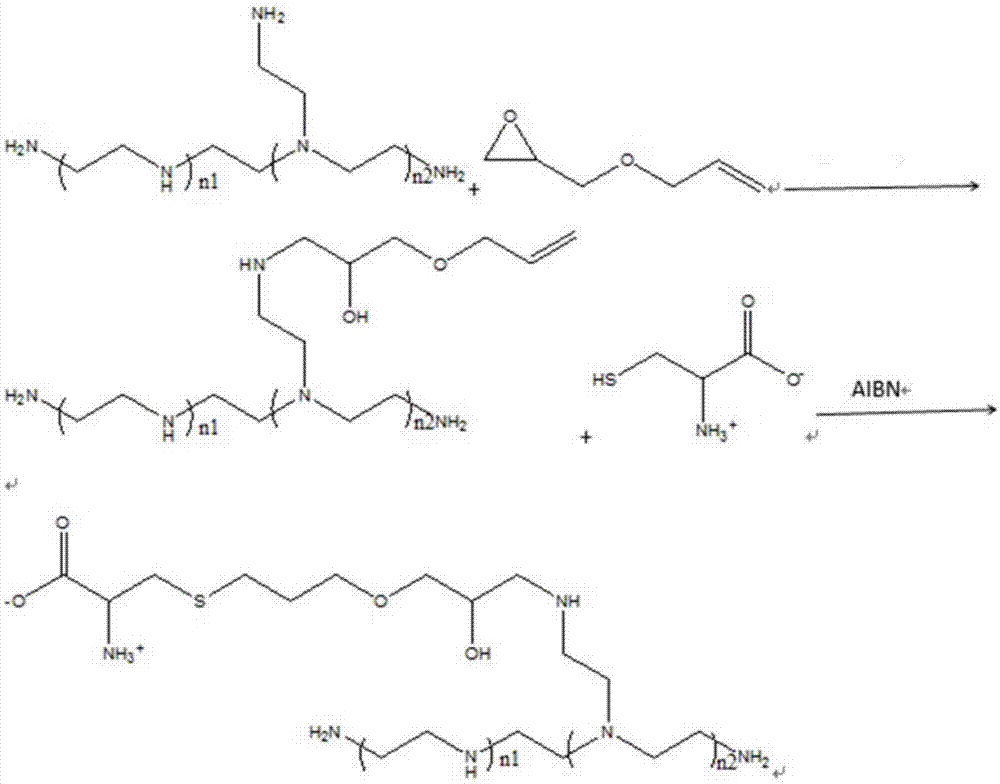
图1为本发明实施例1所述“溶液-颗粒”相转变型抗肿瘤药物传递系统聚乙烯亚胺-半胱氨酸的制备图;
图2为本发明试验例1所述“溶液-颗粒”相转变型抗肿瘤药物传递系统在中性介质和微酸性介质中由溶液转变为纳米粒图;
图3为本发明试验例2所述“溶液-颗粒”相转变型抗肿瘤药物传递系统在微酸性介质中的粒子尺寸和分布图;
图4为本发明试验例3所述“溶液-颗粒”相转变型抗肿瘤药物传递系统聚乙烯亚胺-半胱氨酸诱导肿瘤细胞凋亡图。
具体实施方式
下面结合附图和具体实施例进一步叙述本发明,本发明未述及之处适用于现有技术。下面给出本发明的具体实施例,但实施例仅是为了进一步详细叙述本发明,并不限制本发明的权利要求。
实施例1
请参阅图1,为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统的制备方法图,本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统中,大分子骨架(聚乙烯亚胺800)、两性分子链段(半胱氨酸)和连接臂(乙二醇二缩水甘油醚)三者的质量比为2:5:20,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将10g乙二醇二缩水甘油醚(连接臂)溶于100ml甲醇中,磁力搅拌得到质量体积浓度为0.1g/ml的缩水甘油醚类分子溶液,将1g聚乙烯亚胺800(含有氨基的大分子骨架)溶于10ml去离子水中得到质量体积浓度为0.1g/ml的大分子骨架溶液,按体积比1:10将聚乙烯亚胺800溶液在磁力搅拌下缓慢滴入乙二醇二缩水甘油醚溶液中,40℃反应4小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将2.5g半胱氨酸(两性分子链段)溶解于25ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.1g/ml的半胱氨酸溶液,加入质量体积浓度为1%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.05g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于70℃反应12小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得聚乙烯亚胺800-半胱氨酸(大分子骨架-连接臂接枝两性分子),即为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为1:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为4:1:1。
实施例2
本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统中,大分子骨架(聚乙烯亚胺25kda)、两性分子链段(半胱氨酸)和连接臂(烯丙基缩水甘油基醚)三者的质量比为2:5:15,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将15g烯丙基缩水甘油基醚(连接臂)溶于120ml甲醇中,磁力搅拌得到质量体积浓度为0.125g/ml的烯丙基缩水甘油醚溶液,将2g聚乙烯亚胺25kda(含有氨基的大分子骨架)溶于20ml去离子水中得到质量体积浓度为0.1g/ml的大分子骨架溶液,按体积比1:6将聚乙烯亚胺25kda溶液在磁力搅拌下缓慢滴入烯丙基缩水甘油基醚溶液中,30℃反应6小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将5g半胱氨酸(两性分子链段)溶解于100ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.05g/ml的半胱氨酸溶液,加入质量体积浓度为5%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.15g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于45℃反应24小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得聚乙烯亚胺25kda-半胱氨酸(大分子骨架-连接臂接枝两性分子),即为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为1:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为5:1:1。
实施例3
本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统中,大分子骨架(聚谷氨酰胺50kda)、两性分子链段(组氨酸)和连接臂(烯丙基缩水甘油醚)三者的质量比为2:3:5,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将5g烯丙基缩水甘油基醚(连接臂)溶于80ml甲醇中,磁力搅拌得到质量体积浓度为0.0625g/ml的烯丙基缩水甘油醚类分子溶液,将2g聚谷氨酰胺50kda(含有氨基的大分子骨架)溶于20ml去离子水中得到质量体积浓度为0.1g/ml的大分子骨架溶液,按体积比1:4将聚谷氨酰胺50kda溶液在磁力搅拌下缓慢滴入烯丙基缩水甘油基醚溶液中,45℃反应2小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将3g组氨酸(两性分子链段)溶解于50ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.06g/ml的半胱氨酸溶液,加入质量体积浓度为3%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.2g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于60℃反应14小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得聚谷氨酰胺-组氨酸(大分子骨架-连接臂接枝两性分子),即为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为1:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为6:1:1。
实施例4
本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统中,大分子骨架(聚天冬酰胺70kda)、两性分子链段(半胱氨酸)和连接臂(乙二醇二缩水甘油醚)三者的质量比为1:5:12,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将12g乙二醇二缩水甘油醚(连接臂)溶于80ml甲醇中,磁力搅拌得到质量体积浓度为0.15g/ml的乙二醇二缩水甘油醚溶液,将1g聚天冬酰胺70kda(含有氨基的大分子骨架)溶于30ml去离子水中得到质量体积浓度为0.033g/ml的大分子骨架溶液,按体积比3:8将聚天冬酰胺70kda溶液在磁力搅拌下缓慢滴入乙二醇二缩水甘油醚溶液中,25℃反应6小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将5g半胱氨酸(两性分子链段)溶解于25ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.2g/ml的半胱氨酸溶液,加入质量体积浓度为2%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.08g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于60℃反应24小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得聚天冬酰胺-半胱氨酸(大分子骨架-连接臂接枝两性分子),即为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为2:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为5:1:1。
实施例5
本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统中,大分子骨架(壳聚糖45kda)、两性分子链段(半胱氨酸)和连接臂(乙二醇二缩水甘油醚)三者的质量比为1:3:10,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将20g乙二醇二缩水甘油醚(连接臂)溶于100ml甲醇中,磁力搅拌得到质量体积浓度为0.2g/ml的乙二醇二缩水甘油醚溶液,将2g壳聚糖45kda(含有氨基的大分子骨架)溶于10ml5%(v/v)冰醋酸水溶液得到质量体积浓度为0.2g/ml的大分子骨架溶液,按体积比1:10将壳聚糖45kda溶液在磁力搅拌下缓慢滴入乙二醇二缩水甘油醚溶液中,45℃反应4小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将6g半胱氨酸(两性分子链段)溶解于30ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.2g/ml的半胱氨酸溶液,加入质量体积浓度为0.8%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.0125g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于65℃反应16小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得壳聚糖-半胱氨酸(大分子骨架-连接臂接枝两性分子),即为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为1:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为4:1:1。
实施例6
本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统中,大分子骨架(聚赖氨酸65kda)、两性分子链段(半胱氨酸)和连接臂(烯丙基缩水甘油醚)三者的质量比为1:2:3,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将3g烯丙基缩水甘油基醚(连接臂)溶于100ml甲醇中,磁力搅拌得到质量体积浓度为0.03g/ml的烯丙基缩水甘油基醚溶液,将1g聚赖氨酸65kda(含有氨基的大分子骨架)溶于10ml去离子水得到质量体积浓度为0.1g/ml的大分子骨架溶液,按体积比1:10将壳聚糖45kda溶液在磁力搅拌下缓慢滴入烯丙基缩水甘油基醚溶液中,65℃反应2小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将2g半胱氨酸(两性分子链段)溶解于20ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.1g/ml的半胱氨酸溶液,加入质量体积浓度为1%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.1g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于45℃反应24小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得聚赖氨酸-半胱氨酸(大分子骨架-连接臂接枝两性分子),即为本实施例的“溶液-颗粒”相转变型抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为3:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为4:1:1。
对比例
本对比例的抗肿瘤药物传递系统中,大分子骨架(聚天冬酰胺70kda)、两性分子链段(半胱氨酸)和连接臂(乙二醇二缩水甘油醚)三者的质量比为23:1:21,其制备方法包括以下步骤:
(1)、制备大分子骨架-连接臂:
将21g乙二醇二缩水甘油醚(连接臂)溶于150ml甲醇中,磁力搅拌得到质量体积浓度为0.14g/ml的乙二醇二缩水甘油醚溶液,将23g聚天冬酰胺70kda(含有氨基的大分子骨架)溶于150ml5%(v/v)冰醋酸水溶液得到质量体积浓度为0.15g/ml的大分子骨架溶液,按体积比1:1将聚天冬酰胺70kda溶液在磁力搅拌下缓慢滴入乙二醇二缩水甘油醚溶液中,45℃反应4小时,随后于3l去离子水中用截留分子量为3500的透析袋透析2天,冻干得大分子骨架-连接臂;
(2)、制备大分子骨架-连接臂接枝两性分子:
将1g半胱氨酸(两性分子链段)溶解于5ml甲醇/tris-hcl水溶液中得到质量体积浓度为0.2g/ml的半胱氨酸溶液,加入质量体积浓度为0.8%的偶氮二异丁腈溶解;在磁力搅拌下把半胱氨酸溶液缓慢加入到质量体积浓度为0.0125g/ml的大分子骨架-连接臂水溶液中,在氮气保护下于65℃反应16小时,反应结束后在3l去离子水中透析3天(透析袋截留分子量为3500),冻干得聚天冬酰胺-半胱氨酸(大分子骨架-连接臂接枝两性分子),即为本对比例的抗肿瘤药物传递系统;所述甲醇/tris-hcl水溶液中甲醇与tris-hcl的体积比为1:5,所述两性分子链段溶液、偶氮二异丁腈溶液和大分子骨架-连接臂水溶液的体积比为4:1:1。试验例1
采用nanosightlm10纳米示踪技术仪对实施例1所得的“溶液-颗粒”相转变型抗肿瘤药物传递系统聚乙烯亚胺-半胱氨酸在中性介质和微酸性介质中的相转变进行测试,结果见图2。在近中性介质中(ph7.4)体系为溶液,纳米示踪技术仪检测不到颗粒;而在微酸性介质中(ph6.5)体系为纳米颗粒分散体。
采用该技术仪对对比例所得的药物传递系统聚天冬酰胺70kda-半胱氨酸在中性介质和微酸性介质中的相转变进行测试,在近中性介质中(ph7.4)体系为颗粒,在微酸性介质中(ph6.5)体系也为颗粒,不能进行相转变。
试验例2
采用zetasizernanozs90纳米粒度仪对实施例1~6所得的“溶液-颗粒”相转变型抗肿瘤药物传递系统以及对比例所得的抗肿瘤药物传递系统在不同ph介质中所形成的纳米粒进行测试,结果见表1和图3。
表1抗肿瘤药物传递系统在不同ph介质中的粒径分布及电位
注:--:无可靠的粒径结果
从表1结果可知,实施例中的“溶液-颗粒”相转变型抗肿瘤药物传递系统在近中性介质中(ph7.4)无可靠的粒径结果,在微酸性介质中(ph6.5)为粒径50~400nm的纳米颗粒;对比例中药物传递系统在近中性介质中(ph7.4)为50~400nm的纳米颗粒,在微酸性介质中(ph6.5)也为粒径50~400nm的纳米颗粒。
试验例3
接种结肠癌细胞lovo和肺癌细胞a549到6孔板中,接种密度为1.8×105个/孔。于37℃、5%co2条件下继续培养24h。待细胞密度达到50%时,吸弃培养基,用pbs冲洗细胞,每孔分别加入1800μl含10%胎牛血清的rpmi1640完全培养基。弃去旧培养基,加入由实施例2所得含有10-80μg/ml聚乙烯亚胺-半胱氨酸的rpmi1640培养基,37℃、5%co2条件下继续培养24h。收集培养基,用pbs清洗细胞两次,用显微镜观察细胞状态。每孔加入不含edta的胰酶1ml,37℃消化3min至细胞开始脱落,加入2ml培养基终止消化,收集细胞悬液。1500r离心3min,弃去上清,收集细胞沉淀,用冷pbs清洗2次。用400ul1×bindingbuffer悬浮细胞,浓度大约为1×106/ml。在细胞悬浮液中加入5ulannexinv-fitc,轻轻混匀后于2-8℃避光条件下孵育15min。加入10ulpi后轻轻混匀于2-8℃避光条件下孵育5min。在1h内用流式细胞仪检测凋亡率,结果见图4。
由图4可知,本发明的“溶液-颗粒”相转变型抗肿瘤药物传递系统正常生理条件下诱导结肠癌细胞的凋亡率为4.98%,而在肿瘤微环境条件下显著增加凋亡率到49.54%。在肺癌细胞a549上也得到相同的趋势。该体系可应用于响应肿瘤微环境的靶向抗肿瘤药物递送的研发中。
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!