一种化合物的医药用途的制作方法
本发明属于制药领域。具体地,本发明涉及2-甲基-1-[3-(4-吗啉基)丙]-5-苯基-N-[3-(三氟甲基)苯]-1H-吡咯-3-甲酰胺的医药用途。
背景技术:
原发性肝癌是世界卫生组织公布的十大恶性肿瘤之一,其男性发病率和女性发病率在全球范围内分列第五位和第七位,在癌致死疾患中位居第三位。全世界每年新发及死亡病例约占所有恶性肿瘤的5.4%。在美国,由丙型肝炎感染导致的原发性肝癌的发病率逐年上升。慢性乙肝病毒感染,丙肝病毒感染,酒精性肝病,非酒精性脂肪肝以及代谢相关疾病(血色素沉着症)等均可导致肝癌的发生。约85%的肝癌患者由进展性肝纤维化和/或肝硬化发展而致。在全球范围内乙型肝炎依然为主要的致癌病因。我国是一个肝病大国,据统计现有肝病人群一亿以上,即每十个人中就有一位肝病患者,其中尤以乙型肝炎病毒感染导致的肝硬化、进而演变为肝癌最为突出。据世界卫生组织2005年全球肿瘤统计分析,目前每年新患肝癌人数为626000,死亡数598000。据估计,全球范围内20亿人患有乙型肝炎,2亿人患有丙型肝炎。同时还预计,至2030年原发性肝癌将成为第二位癌症致死疾病。新患肝癌病人55%发生在我国。
目前,随着医学的发展与进步,原发性肝癌的治疗效果得到一定程度的改善,5年生存率达到40-70%。综合治疗已成为肝癌治疗的基本原则,包括外科的肝切除术和肝移植手术,介入治疗包括射频消融、微波治疗及经动脉化学栓塞治疗等。部分靶向药物已应用于临床,如索拉菲尼(Sorafenib)、舒尼替尼等。但因为原发性肝癌的高侵袭性和高复发率,其依然严重影响该类患者的治疗效果。新肝癌治疗药物的发现有望为肝癌的治疗提供新的途径和手段。
技术实现要素:
2-甲基-1-[3-(4-吗啉基)丙]-5-苯基-N-[3-(三氟甲基)苯]-1H-吡咯-3-甲酰胺又名HC 067047,其分子式为C26H28F3N3O2,具有下式I所示结构:
本发明的目的在于提供具有式I结构的2-甲基-1-[3-(4-吗啉基)丙]-5-苯基-N-[3-(三氟甲基)苯]-1H-吡咯-3-甲酰胺(又名HC 067047)或者其药学可接受的盐或溶剂合物在制备用于治疗肝癌的药物中的用途。
在一些实施方案中,上述肝癌是高分化肝癌。
本发明所称的药学可接受的盐,指式I化合物与酸或碱形成的对生物体无毒性或低毒性的盐。所述酸可以是无机酸或有机酸,诸如盐酸、氢溴酸、硝酸、硫酸、磷酸、抗化学酸、柠檬酸、乳酸、甲酸、马来酸、乙酸、富马酸、琥珀酸、酒石酸、甲磺酸、对甲苯磺酸等。所述碱可以是无机碱或有机碱,所成盐例如是碱金属盐,如Li盐、Na盐或K盐;碱土金属盐,如Ca盐和Mg盐;或铵盐或取代的铵盐,诸如,三甲铵盐。
本发明所称的溶剂合物,指式I化合物或其盐与一种或多种药学上可接受的溶剂分子所形成的复合物。所述溶剂分子可以是水或醇,如乙醇等。
优选地,所述药物中还包括一种或多种可药用辅料。
本发明所称的药用辅料,指本领域所常规使用的药学可接受的固态、液态或其他形态的载体、赋形剂、稀释剂、着色剂、增塑剂等添加剂。例如碳酸镁、硬脂酸镁、磷酸钙、硅藻土、微晶纤维素、羟甲基纤维素及盐、滑石、乳糖、葡萄糖、甘露糖醇、蔗糖、果胶、糊精、淀粉、明胶、纤维素材料、低熔点蜡、可可脂等。
优选地,所述药物与用于治疗肝癌的至少一种另外的药物联用。进一步地,所述另外的药物选自索拉菲尼、舒尼替尼或其组合。进一步地,所述另外的药物为索拉菲尼。
优选地,所述药物是能够抑制肝癌肿瘤细胞生长和/或增殖的药物。
优选地,所述药物是能够抑制肝癌肿瘤细胞迁移和/或侵袭转移的药物。
本发明的由上述式I化合物制备的药物或药物组合物可以采用口服给药、注射给药(如肌肉注射、静脉注射、腹腔注射)、皮下给药、吸入给药、直肠给药等常用给药方式;并可以制备成本领域常见的剂型,如片剂、胶囊剂、栓剂、粉针、注射剂、气雾剂等。
在本发明的优选实施方案中,本发明的上述式I所示结构的化合物采用注射给药方式,按照人的体重(kg)来计算,优选给药剂量为50μg/kg,给药方式为腹腔内注射,给药频率1次/天。动物的给药剂量为50μg/kg,给药方式为腹腔内注射,给药频率1次/天。
使用本发明式I化合物治疗肝癌时,所述药物可明显抑制肝癌细胞的增殖和生长,为肝癌治疗提供了一条新途径。
附图说明
图1示出了实施例1中对照组和治疗干预组的Scid-Huh7-皮下瘤相对体积。
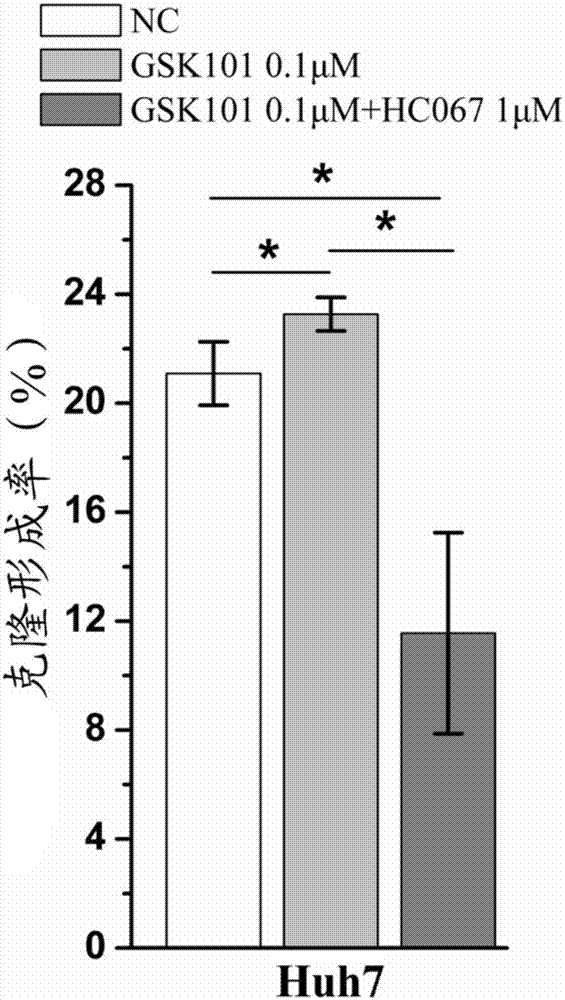
图2示出了实施例2中对照组、激动剂组和抑制剂组的克隆形成率。
图3示出了实施例3中对照组、激动剂组和抑制剂组的细胞迁移率。
具体实施方式
以下结合具体实施例对本发明的技术方案做进一步详细说明。应当理解,这些实施例是用于示例性地说明本发明的基本原理、主要特征和优点,实施例中采用的具体实施条件可以在本领域范围内做适当调整,而本发明的保护范围不受实施例的限制。
在本发明的实施例中,使用如下原料:
雌性四周龄裸鼠NOD/SCID(非肥胖型糖尿病/重症联合免疫缺陷小鼠),购自北京维通利华公司,所有小鼠均喂养于湘雅二医院实验动物中心SPF级别小鼠饲养间内,环境温度稳定在18~22℃,湿度控制在50~60%。NOD/SCID小鼠喂养在无毒无特定病原体的塑料鼠盒内,以标准颗粒饲料和纯净水饲养并保持其昼夜12小时节律,所需环境均满足国家实验动物管理及使用指南要求,所有操作均得到中南大学湘雅二医院动物伦理委员会批准及监督;
肝癌细胞株Huh7,购自中国科学院上海生命科学院细胞库;
抑制剂HC 067047,2-甲基-1-[3-(4-吗啉基)丙]-5-苯基-N-[3-(三氟甲基)苯]-1H-吡咯-3-甲酰胺,购自Abcam公司,规格:25mg,货号:ab145868;
DMSO,购自Sigma-Aldrich公司;V900090-500ML;纯度99%;
DMEM高葡萄糖完全培养基,购自美国洛根Hyclone公司;
胎牛血清FBS,10099-141,购自美国格兰德岛Gibco公司;
胰蛋白酶,SH30042.01,购自美国洛根Hyclone公司;
磷酸盐缓冲盐水(PBS),SH20256.01B,购自美国洛根Hyclone;
激动剂GSK1016790A,N-((1S)-1-{[4-((2S)-2-{[(2,4-二氯苯基)磺酰基]氨基}-3-羟基丙酰基)-1-哌嗪基]羰基}-3-甲基丁基)-1-苯并噻吩-2-甲酰胺,购自Sigma-Aldrich;
游标卡尺,广陆量具厂生产,0-150mm电子数显;
Varioskan Flash多功能酶标仪,Thermo。
实施例1裸鼠模型试验
将5×106个肝癌细胞株Huh7细胞分别注射至裸鼠NOD/SCID(共12只)的右侧腹,然后按照上文所述标准进行饲养。使用游标卡尺分别测量皮下肿瘤的长短径(长短径需垂直),以1/2×长度×宽度2确定肿瘤大小,当肿瘤形成至体积约80mm3时将小鼠随机分为对照组和治疗干预组,每组各6只。
将HC 067047注射给药至小鼠,观察肿瘤的变化,具体给药方式为:
治疗干预组:
将25mg HC 067047溶解于2.5ml DMSO中,制成浓度为21.2mM的母液。试验时用DMSO稀释母液,以形成注射药物,对该组小鼠进行腹腔内定容注射,剂量为100μL,即50μgHC 067047/(kg体重),1次/天。
对照组:
于腹腔内注射DMSO空白溶剂,定容注射,剂量为100μL,1次/天。
肿瘤大小以体积=1/2×长度×宽度2检测。在第6周将小鼠处死,比较生存率和肿瘤体积大小。本实施例的实验结果如下:
表1对照组和治疗干预组的Scid-Huh7-皮下瘤(裸鼠NOD/SCID-Huh7细胞株-皮下瘤)相对体积
aN.S无显著性差异,b由于绝大多数小鼠于药物干预32天后死亡,故未测量第5、6周数据
在表1中,P值代表对照组和治疗干预组的Scid-HepG2-皮下瘤相对体积之间的差异。给药第一天的肿瘤大小为100%。
由表1及图1的结果可以看出,注射了2-甲基-1-[3-(4-吗啉基)丙]-5-苯基-N-[3-(三氟甲基)苯]-1H-吡咯-3-甲酰胺的小鼠皮下的肿瘤体积变化明显较慢,表明2-甲基-1-[3-(4-吗啉基)丙]-5-苯基-N-[3-(三氟甲基)苯]-1H-吡咯-3-甲酰胺对于Huh7肿瘤具有治疗作用。
实施例2:平板细胞克隆形成实验
I.克隆形成率试验
1、前日下午分别取对数生长期的Huh7肝癌细胞,用0.25%胰蛋白酶消化并吹打成单个细胞,完成细胞计数;
2、将细胞悬液于10%胎牛血清的DMEM完全培养基中混匀,调整细胞密度,将每组细胞分别以每孔2ml培养基、1500个细胞/孔密度分别接种于6孔板中,并轻轻转动,使细胞分散均匀,置于含5%CO2的37℃培养箱中培养过夜;
3、次日上午根据实验设计用含10%胎牛血清的DMEM完全培养基配制所需不同浓度梯度的药物,每组浓度3个复孔,激动剂GSK1016790A及抑制剂HC067047组浓度分别为0.1μmol/L和1μmol/L。轻柔地将6孔板上层培养基吸出,加入相应浓度药物,置于37℃,5%CO2及饱和湿度的细胞培养箱中培养1~2周;
4、经常观察,当培养皿中出现肉眼可见的克隆时,终止培养。弃去上清液,用PBS小心浸洗2次,加4%多聚甲醛2mL固定细胞15分钟。然后去固定液,加适量0.5%结晶紫染色液染10~15分钟,然后用清水缓慢洗去染色液,空气干燥,计数拍照。
5、将6孔板底部叠加一张带网格的透明胶片,用肉眼直接计数克隆,计数大于50个细胞的克隆数。最后计算克隆形成率。将上述实验平行进行三组,记为组1-3,结果由表2-3及图2所示。
克隆形成率=(克隆数/接种细胞数)×100%
表2实施例1中各组的克隆数
表3实施例1中各组的克隆形成率
小结:由上表和图2可知,HC 067047可有效抑制肝癌细胞株的克隆形成。
II.细胞侵袭能力试验
本试验中采用的是Corning公司的3422#8.0μm孔径的24孔板。
1、将Huh7肝癌细胞血清饥饿12-24h,进一步去除血清的影响;
2、使用0.25%胰蛋白酶消化细胞,终止消化后离心弃去培养液,用PBS洗1-2遍,使用无血清培养基重悬,完成细胞计数,调整细胞密度至2.5×105个/mL;
3、实验中激动剂GSK1016790A及抑制剂HC067047组浓度分别为0.1μmol/L和1μmol/L,加上空白对照组,共7组,每组3个复孔,共21个孔;
4、取7个EP管,第一管为空白对照组,加入200μl细胞悬液,即5000个细胞;其余6管内各加入600μl(200μl×3个复孔)细胞悬液,即5000×3个细胞,于800rpm/min转速下离心5分钟,去除各EP管内上层无血清培养基,重新加入各种含有相应浓度药物的无血清培养基,充分混匀后,以每孔200μl种入Transwell上层小室;
5、向24孔Transwell板下室加入500μl含10%胎牛血清的DMEM完全培养基;于37℃,5%CO2及饱和湿度的细胞培养箱常规培养48h;
6、用棉签擦去各室基质胶和上室内的细胞,用PBS小心浸洗小室2次,加4%多聚甲醛2mL固定细胞15分钟。然后去固定液,加适量0.5%结晶紫染色液染10~15分钟,然后用清水缓慢洗去染色液,空气干燥,显微镜下计数拍照,将上述实验平行进行三组,记为组4-6,具体的细胞迁移数结果结果由表4及图3所示。
表4实施例2中各组的迁移细胞数
小结:HC 067047可有效抑制肝癌细胞的迁移侵袭。
- 还没有人留言评论。精彩留言会获得点赞!