一种ZrO2纳米粉体的制备方法及催化应用与流程
本发明属于纳米催化材料制备及应用的技术领域,具体涉及一种氧空缺可控的zro2纳米粉体制备方法及催化应用。
背景技术:
煤、石油和天然气等石化资源是当今社会发展的主要能源支撑和现代工业发展的命脉,然而它们是不可再生的、有限的,随着人口增长和经济发展正以越来越快的速度消减。同时,石化资源的开采和利用也造成环境污染和极端气候等问题。而生物质资源因其可再生、环境友好、分布广泛、储量丰富等特点受到世界各国人民的广泛关注。生物质大都以植物体形式存在,主要成分是木质素、纤维素和半纤维素。在木质生物质中,木质素含量在20%左右,纤维素约占40%,半纤维素约为25%左右。zro2材料因其具有弱的酸碱性和氧化-还原特性,被广泛应用于氢化、酯化和氧化等可再生的化工行业。2012年,美国林鸿飞课题组发现zro2水热氧化纤维素转化羧酸平台化合物具有较好的选择性,尤其乙酰丙酸产率可达50%,且5次循环使用后,其产率仍达到40%(hongfeilin,etal.energy&environmentalscience,5(2012)9773)。该绿色催化工艺为生物质纤维素转化羧酸平台化合物的研究提供了新的思路,但需要进一步开发催化剂以提高选择性和产率。
环境污染是当今世界各国面临的另一大难题。许多有毒有害的有机污染物具有致癌、致畸、致突变性,这些有机污染物采用传统的生物处理工艺难以去除,而光催化氧化降解对许多有毒有害的有机污染物的处理显示出其独特的优势。光催化能将难降解的有机污染物氧化、分解成h2o、co2和无机盐等,使有机物部分或完全矿物质化,从而达到污染物无害化处理的要求。四环素抗菌素由于其生物活性能产生抗药性细菌和诱导许多类生物体的不理想的生物反应,被认为是潜在的微污染物。这些抗菌素广泛用于人类和牲畜的疾病控制,排泄物或处理的过期药物最终沉入水和土壤中,然而通过传统的生物降解难以去除。因而需要开发一种光催化剂进行净化处理。zro2材料通常具有宽的带隙,引入氧空位能窄化带隙,促进其在可见光催化净化处理中的应用。目前,zro2纳米材料被广泛应用于光催化降解甲基蓝、甲基橙、罗丹明b等染料,但未见光催化降解抗菌素的报道。
技术实现要素:
本发明针对宽带隙zro2材料的可见光催化效率低的技术问题,以及改善生物质催化氧化选择性、产率,提出了一种氧空位可控zro2纳米粉体的制备方法及其在催化领域中的应用,具有很好的市场应用前景。
一种zro2纳米粉体制备方法,其制备过程如下:
(1)将15~30ml乙酰丙酮和15~30ml乙二醇乙醚混合,搅拌10~30min,配成均一透明的a溶液;
(2)在a溶液中加入0.01~0.1mol乳酸稳定剂,搅拌10~30min,配制透明的b溶液;
(3)在b溶液中加入0.01~0.1mol有机锆源,搅拌10~30min,制得透明状溶胶前驱体;
(4)将溶胶前驱体移至内衬为石英玻璃的100ml可通气的反应釜中,通入0~2.4mpa氮气和氧气的混合气,180-240℃溶剂热反应4-24h;反应完成后,经洗涤、干燥,得到zro2纳米粉体。
进一步的,所述有机锆源为正丙醇锆和正丁醇锆。
此外,本发明还要求保护上述zro2纳米粉体在光催化降解抗菌素方面的应用,其特征在于:所述zro2纳米粉体在150min氙灯照射下对盐酸四环素的降解率最大达到95%,而150min可见光催化降解率最大达到70%。
本发明具有以下有益效果:
本发明制备方法简单、重复性好,可有效调控zro2纳米粉体的晶相、晶粒尺度以及氧空位浓度;同时,可见光能有效催化降解抗菌素,解决抗菌素难以生物降解的问题,避免因抗菌素的生物活性而对环境造成污染。
附图说明
图1为不同温度溶剂热反应条件下合成zro2粉体的xrd图。
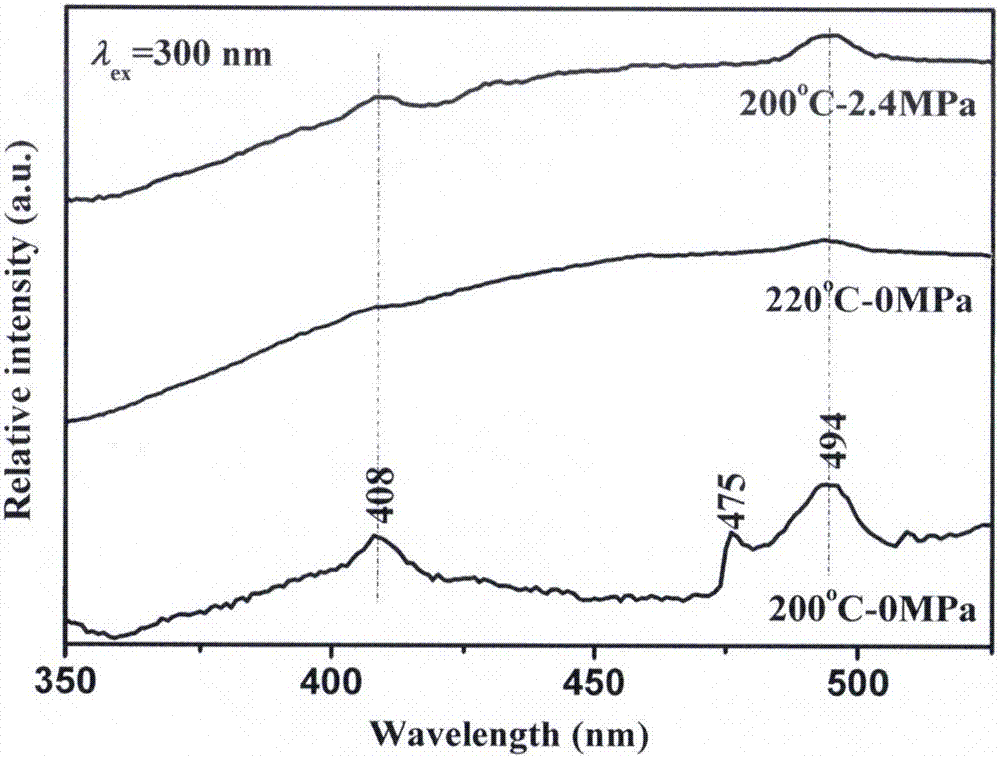
图2为通入0mpa(80%氮气+20%氧气)混合气后在不同温度下以及通入2.4mpa(80%氮气+20%氧气)混合气后在200℃下合成zro2粉体的荧光光谱。
图3为通入(a)0mpa和(b)2.4mpa(80%氮气+20%氧气)混合气后在200℃下合成zro2粉体的tem照片。
图4为以通入2.4mpa(80%氮气+20%氧气)混合气后在200℃下合成zro2粉体为催化剂,不同(a)氙灯和(b)可见光照射时间催化降解盐酸四环素的紫外-可见吸收光谱。
具体实施方式
下面结合实例对本发明作进一步描述。
原料来源:正丙醇锆(70wt%,上海阿拉丁生化科技股份有限公司)、正丁醇锆(80wt%,上海阿拉丁生化科技股份有限公司)、乳酸(85.0%,国药集团上海化学试剂有限公司)、乙酰丙酮(99.8%,国药集团上海化学试剂有限公司)和乙二醇乙醚(99.0%,国药集团上海化学试剂有限公司)。
实施例1
将25ml乙酰丙酮和25ml乙二醇乙醚混合,搅拌10~30min,然后加入0.01mol乳酸稳定剂,搅拌10~30min,配制混合溶液;在上述混合溶液中加入0.01mol正丙醇锆,搅拌10~30min,制得透明状溶胶前驱体;最后将溶胶前驱体移至内衬为石英玻璃的100ml可通气的反应釜中,180-240℃溶剂热反应8h;反应完成后,经洗涤、干燥,得到zro2纳米粉体。
不同温度溶剂热反应条件下合成zro2粉体的xrd图如图1所示,结果显示180℃条件下反应得到的zro2粉体为非晶相,而200℃以上温度反应得到zro2粉体为单斜相。对比200℃和220℃反应得到zro2粉体在300nm激发下的荧光光谱如图2所示,发现高温度合成zro2粉体的发射光谱在408和494nm处宽化,说明zro2粉体存在较多的氧空位。
实施例2
将25ml乙酰丙酮和25ml乙二醇乙醚混合,搅拌10~30min,然后加入0.01mol乳酸稳定剂,搅拌10~30min,配制混合溶液;在上述混合溶液中加入0.01mol正丙醇锆,搅拌10~30min,制得透明状溶胶前驱体;最后将溶胶前驱体移至内衬为石英玻璃的100ml可通气的反应釜中,通入0~2.4mpa(80%氮气+20%氧气)混合气后,200℃溶剂热反应8h;反应完成后,经洗涤、干燥,得到zro2纳米粉体。
通入0mpa和2.4mpa(80%氮气+20%氧气)混合气后在200℃条件下合成zro2粉体的tem照片如图3所示,结果发现通入0mpa混合气在200℃条件下合成的zro2粉体具有小的晶粒尺寸(~4nm),但存在明显的团聚现象(100nm团聚颗粒与邻近颗粒也铰链在一起);而通入2.4mpa(80%氮气+20%氧气)混合气后同样反应温度下合成的zro2粉体晶粒尺寸并未发生明显变化,但其分散性得到显著改善。对比其在300nm激发下的荧光光谱(图2),发现通入2.4mpa混合气合成zro2粉体的发射光谱在408和494nm处宽化,说明zro2粉体存在较多的氧空位。
实施例3
将25ml乙酰丙酮和25ml乙二醇乙醚混合,搅拌10~30min,然后加入0.01mol乳酸稳定剂,搅拌10~30min,配制混合溶液;在上述混合溶液中加入0.01mol正丙醇锆,搅拌10~30min,制得透明状溶胶前驱体;最后将溶胶前驱体移至内衬为石英玻璃的100ml可通气的反应釜中,通入2.4mpa不同氧气含量的混合气后,200℃溶剂热反应8h;反应完成后,经洗涤、干燥,得到zro2纳米粉体。结果发现,通入氧含量少的混合气合成zro2纳米粉体具有较多的氧空位。
将0.1gzro2纳米粉体放入浓度为5mg/l的100ml盐酸四环素溶液中,在搅拌下先暗反应60min,然后放在氙灯和可见光(λ>420nm)下照射,每隔30min取一次盐酸四环素测其紫外-可见吸收光谱。以通入2.4mpa(80%氮气+20%氧气)混合气后在200℃合成zro2粉体为催化剂,不同氙灯和可见光照射时间催化降解盐酸四环素的紫外-可见吸收光谱如图4所示,结果发现60min暗反应后,盐酸四环素的吸收峰迅速降低;同时发现氙灯照射比可见光照射更有效催化降解盐酸四环素,这是由于氙灯照射的能量超过zro2粉体的带隙产生更多自由基的缘故,而可见光照射时主要是通过氧空位作用而产生自由基。以吸收光谱所围面积比计算盐酸四环素的浓度比c/c0,结果发现氧含量少的混合气合成zro2纳米粉体具有更高的催化降解率;通入2.4mpa纯氮气合成zro2纳米粉体在氙灯照射下,150min内对抗菌素的降解率达到95%,而150min可见光催化降解率达到70%。
实施例4
将25ml乙酰丙酮和25ml乙二醇乙醚混合,搅拌10~30min,然后加入0.01mol乳酸稳定剂,搅拌10~30min,配制混合溶液;在上述混合溶液中加入0.01mol正丁醇锆,搅拌10~30min,制得透明状溶胶前驱体;最后将溶胶前驱体移至内衬为石英玻璃的100ml可通气的反应釜中,通入0~2.4mpa不同氧气含量的混合气后,180~240℃溶剂热反应8h;反应完成后,经洗涤、干燥,得到zro2纳米粉体。将0.1gzro2纳米粉体放入浓度为5mg/l的100ml盐酸四环素溶液中,在搅拌下先暗反应60min,然后放在氙灯和可见光(λ>420nm)下照射,每隔30min取一次盐酸四环素测其紫外-可见吸收光谱。所得结果与用正丙醇锆源所得结果相似。
- 还没有人留言评论。精彩留言会获得点赞!