一种产生抗HIV活性物质的链霉菌及其应用的制作方法
本发明属于微生物制药领域,具体地说,涉及一株产生的抗HIV-1活性物质的链霉菌(Streptomycessp.)CPCC201585及其用。
背景技术:
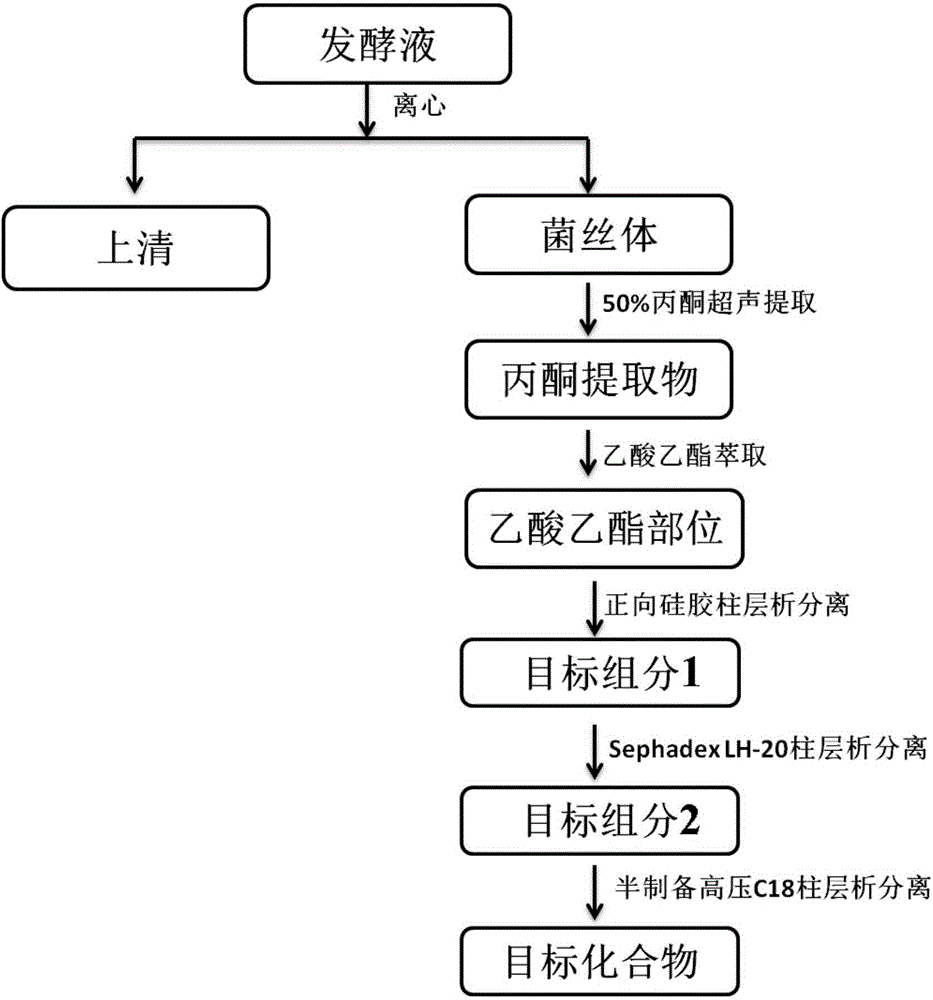
:HIV(HumanImmunodeficiencyVirus)病毒,中文全称人类免疫缺陷病毒,属于逆转录病毒的一种。HIV病毒侵入宿主细胞后,会严重破坏宿主机体免疫功能,从而引起严重的机会性感染以致引起以恶性疾病为特征的继发性免疫缺陷综,即为获得性免疫缺陷综合征(acquiredimmunodeficiencysyndrome,AIDS)。首例艾滋病于1981年发现于美国,随后开始在全球蔓延,严重威胁着人类的健康。HIV病毒可分为HIV-1型和HIV-2型,两者基因组具有很大的差异,其中HIV-1是引起全球性艾滋病蔓延的主要病原体。化学治疗仍然是目前最重要的HIV-1治疗手段。从1987年齐多夫定应用与抗HIV-1治疗,至今已有25种药物进入临床应用。按药物的作用机制分类,这些已上市药物中主要是逆转录酶抑制剂和蛋白酶抑制剂。另外,还有1种整合酶抑制剂和2种病毒进入抑制剂。随着抗HIV药物的不断研发应用,特别是依靠联合药物治疗方式即高效联合抗逆转录病毒疗法(HAART)对艾滋病患者进行治疗,已可以有效降低病毒载量,显著延长患者生存时间,但是药物的耐药性、不良反应及患者的依从性等方面存在的问题常会引起临床治疗的失败。因此,仍需要坚持开发不同结构类型,特别是不同作用机制的新型抗HIV-1药物供临床应用。微生物种类庞大,具有丰富类型的代谢产物,是寻找高效低毒的新抗HIV活性化合物和先导化合物的重要来源。通过建立相应筛选模型快速筛选出抗HIV活性微生物菌株,继而从其代谢产物中寻找活性化合物或具有一定活性的化合物为先导,进行结构简化和修饰,揭示作用机理和构效关系,是发现新抗HIV药物的有效途径。病毒的耐药性是目前艾滋病药物治疗中最亟需解决的问题。HIV-1之所以能够迅速产生针对现有临床应用的抗病毒药物的耐药性,其主要根源在于这些药物所针对的靶点都是病毒本身。而病原病毒天然就具有高变异的特点,在药物的选择压力下,很容易引起病毒的迅速变异从而产生耐药。因此,解决HIV-1的耐药性问题的关键之一在于必须突破传统的“以病原病毒本身为靶”的药物发展模式。在众多的潜在新靶点当中,HIV-1宿主限制因子(restrictionfactors)APOBEC3G(humanproteinapoliproteinBmRNA-editingenzyme-catalyticpolypeptide-like-3G,简称hA3G)以其高效抑制HIV-1复制的能力、独特的抗病毒机制及广谱的抗病毒活性,而成为极具发展潜力的抗HIV-1药物的新靶点。hA3G是在人的淋巴细胞中表达的一种RNA/DNA编辑酶,归属于APOBEC蛋白超家族。该家族至少有11个成员,其中包括AID、APOBEC1、APOBEC2、APOBEC3A-H,以及APOBEC4。这些同源蛋白都含有高度保守的胞嘧啶脱氨基功能域(cytodinedeaminatingdomain,简称CD),而且具有比较高的序列及结构相似性。该家族的多数成员都具有编辑核酸的功能,可以使mRNA上的胞嘧啶残基脱氨形成尿嘧啶,或单链DNA上的脱氧胞嘧啶残基脱氨形成脱氧尿嘧啶。hA3G不仅可以抑制包括HIV-1在内的各种逆转录病毒的复制,而且对非逆转录病毒象乙肝病毒也有很好的抑制效果,具有广谱的抗病毒活性。随后的研究进一步发现,该家族的其他成员以及其他物种所编码同源蛋白对不同的逆转录病毒都具有不同程度的抑制能力,其中包括HIV-1、鼠白血病病毒(MuLV)、内源性逆转录病毒等。因此,hA3G和其他APOBEC3蛋白不仅仅是一类HIV-1限制因子,更是代表了一种全新的宿主天然免疫系统。作为病毒的拮抗手段,HIV-1的Vif蛋白可以特异性地结合hA3G,并与细胞蛋白Cu15,elonginsBandC,Rbx1相互作用,形成Skp1-cullin-F-box(SCF)复合物,通过泛素介导的降解途径,导致hA3G的降解,从而阻断了宿主细胞hA3G抗病毒系统对HIV-1病毒复制的抑制作用。鉴于HIV-1主要的靶细胞(外周血单核细胞、T-淋巴细胞、单核巨噬细胞)均为非允许性细胞,如果能特异而有效地阻断VIF介导的降解途径,宿主细胞就可以利用自身编码的hA3G抑制HIV-1的复制。因此,阻断Vif降解hA3G成为极具发展潜力的抗HIV-1药物的新靶点。技术实现要素:本发明的目的是提供一株链霉菌(Streptomycessp.)CPCC201585,其发酵液的提取物可明显抑制HIV-1的复制;从其菌丝体的提取物中分离得到的Surfactin类化合物具有抑制HIV-1复制的活性。为了实现上述目的,本发明采用如下技术方案:一株链霉菌(Streptomycessp.)CPCC201585,其分离自云南省景洪勐海县的土壤样品中,已经于2014年12月30日保藏在中国微生物菌种保藏管理委员会普通微生物中心(CGMCC),地址为北京市朝阳区北辰西路1号院3号,邮政编码为100101,保藏号为CGMCCNo.10265。所述链霉菌(Streptomycessp.)CPCC201585在ISP2培养基上生长良好,培养7天时,菌落多数呈白色至棕色,无可溶性色素生成。该菌株在培养基上形成高度分支的基内菌丝和气生菌丝,并产生松散的螺旋形孢子链,孢子表面多刺状突起。本发明还提供了所述链霉菌(Streptomycessp.)CPCC201585在制备抗HIV-1病毒药物中的应用。本发明还提供了所述链霉菌(Streptomycessp.)CPCC201585在制备Surfactin类化合物中的应用。本发明所述的链霉菌(Streptomycessp.)CPCC201585,其发酵液的提取物可明显抑制HIV-1的复制;从其菌丝体的提取物中分离得到的Surfactin类化合物具有抑制HIV-1复制的活性。本发明还提供含有权利要求1所述的链霉菌(Streptomycessp.)CPCC201585的菌剂。本发明还提供了一株链霉菌(Streptomycessp.)CPCC201585发酵液的提取方法,包括如下步骤:1)将上述链霉菌(Streptomycessp.)CPCC201585活化,接种到发酵培养基中进行发酵培养;其中,所述发酵培养采用本领域技术人员所掌握的常规培养基和培养条件;2)向步骤1)所得的发酵液中加入等体积的丙酮,超声提取,离心,回收丙酮,冷冻干燥后即得。本发明所述链霉菌(Streptomycessp.)CPCC201585发酵液的提取方法中,在步骤1)中,所述发酵培养条件为:温度26~32℃,摇床震荡培养4~8天。本发明所述链霉菌(Streptomycessp.)CPCC201585发酵液的提取方法中,在步骤2)中,所述超声提取条件为:室温,超声提取20~30min。本发明还提供了一种利用链霉菌(Streptomycessp.)CPCC201585产生Surfactin类化合物的方法。所述Surfactin类化合物的结构通式(I)如下:其中,R选自链烷基,优选-(CH2)6CH(CH3)CH2CH3、-(CH2)8CH(CH3)2、-(CH2)10CH3、-(CH2)8CH(CH3)CH2CH3。所述优选的Surfactin类化合物的分子式分别为C51H89N7O13,C52H91N7O13,C52H91N7O13,C53H93N7O13,结构如式(II)所示:所述化合物1-4均为白色固体粉末,易溶于甲醇、乙醇等溶剂中。本发明所述利用链霉菌(Streptomycessp.)CPCC201585产生Surfactin类化合物的方法包括如下步骤:1)将链霉菌(Streptomycessp.)CPCC201585活化,接种到发酵培养基中进行发酵培养;其中,所述发酵培养采用本领域技术人员所掌握的常规培养基和培养条件;2)将步骤1)所得的发酵液离心处理,得上清液和菌丝两部分;3)所得菌丝用丙酮超声提取,减压回收丙酮后再用乙酸乙酯萃取,减压回收乙酸乙酯,得棕褐色浸膏;4)将所得浸膏洗脱分离,冷冻干燥即得目标化合物。所述化合物的制备方法中,步骤1)中,所述培养条件为:温度26~32℃,摇床震荡培养4~8天。所述化合物的制备方法中,步骤2)中,所述离心处理为本领域常规离心方法。所述化合物的制备方法中,步骤3)中,所述超声提取条件为:室温,超声提取20~30min。所述化合物的制备方法中,步骤3)中,所述丙酮质量百分比浓度为45-55%,优选50%;所述萃取为采用等体积的乙酸乙酯萃取3~6h,再于40~50℃减压浓缩回收乙酸乙酯。所述化合物的制备方法中,步骤4)中,所述洗脱分离过程为:先进行正相硅胶柱层析分离,再进行SephadexLH-20柱层析分离,最后利用半制备型反相C18柱分离。其中,所述正相硅胶柱层析分离过程中,洗脱液由石油醚与乙酸乙酯按体积比3:1~2:1混合而得,所得粗组分中富集较多目标化合物,优选体积比为2:1时,富集的目标化合物最多。其中,所述SephadexLH-20柱层析分离过程中,洗脱液为甲醇、乙醇等。其中,所述半制备型反相C18柱分离过程中,洗脱液为水相含0.01%TFA(三氟乙酸)的90%甲醇-水,按色谱峰收集,冷冻干燥即得目标化合物。上述各分离过程的洗脱条件可采用本领域技术人员所熟知的各分离方法的常规洗脱条件,本发明在此不再赘述。采用上述方法得到的化合物经荧光显色和硫酸显色,显色不明显,碘熏显淡黄色,用氯仿-甲醇-水(体积比70:15:2)溶剂体系展开Rf值为0.3~0.4左右。本发明还提供上述Surfactin类化合物在制备抗HIV-1药物中的应用。本发明首次发现从链霉菌(Streptomycessp.)CPCC201585发酵液中可获得具有抗HIV-1活性的Surfactin类化合物,在20μM浓度下,该类化合物对VSVG/HIV假病毒的抑制达到84%以上,能够有效抑制Vif对APOBEC3G(hA3G)的降解,其抗HIV作用机制不同于目前上市药物,具有靶点新颖的特点,为抗HIV新药的研发奠定了基础,具有一定的市场前景。附图说明图1为链霉菌(Streptomycessp.)CPCC201585发酵产生的活性化合物的制备流程图。图2为活性化合物1的1H-NMR(600MHz,DMSO-d6)谱图。图3为活性化合物1的1C-NMR(150MHz,DMSO-d6)谱图。图4为活性化合物2的1H-NMR(600MHz,DMSO-d6)谱图。图5为活性化合物2的1C-NMR(150MHz,DMSO-d6)谱图。图6为活性化合物3的1H-NMR(600MHz,DMSO-d6)谱图。图7为活性化合物3的1C-NMR(150MHz,DMSO-d6)谱图。图8为活性化合物4的1H-NMR(600MHz,CD3OD)谱图。图9为活性化合物4的1C-NMR(150MHz,CD3OD)谱图。图10为实施例3中阳性对照药MG132和Surfactin类化合物1-4抑制hA3G蛋白的降解的WesternBlot检测图。图11为实施例3中Surfactin类化合物1-4对于vif与hA3G相互作用的影响的WesternBlot检测图。具体实施方式以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段,所用原料均为市售商品。实施例1链霉菌(Streptomycessp.)CPCC201585制备Surfactin类化合物的方法本发明的链霉菌(Streptomycessp.)CPCC201585,其分离自云南省景洪勐海县的土壤样品中,已经于2014年12月30日保藏在中国微生物菌种保藏管理委员会普通微生物中心(CGMCC),地址为北京市朝阳区北辰西路1号院3号,邮政编码为100101,保藏号为CGMCCNo.10265。如图1所示,利用链霉菌(Streptomycessp.)CPCC201585制备Surfactin类化合物的方法,步骤如下:1)、所述链霉菌(Streptomycessp.)CPCC201585的发酵菌种活化:配制斜面培养基,分装试管,121℃灭菌30min后,制斜面;将保存的链霉菌(Streptomycessp.)CPCC201585菌种转接至斜面培养基上,28℃下培养4天;所述斜面培养基配方如下:葡萄糖4g,麦芽膏10g,酵母膏4g,琼脂14g,加水至终体积1L。发酵培养:挑取菌丝块接种于液体发酵培养基中,28℃下摇床震荡培养2天,即为种子培养物;将100ml种子培养物接种到装有1000ml的发酵培养基中,28℃摇床振荡培养5天。所述发酵培养基配方如下:葡萄糖5g,酵母膏5g,蛋白胨5g,牛肉膏5g,玉米浆4g,黄豆饼粉10g,碳酸钙4g,二氯化钴(0.002%溶液)1mL,可溶性淀粉20g,加水至终体积1L,调pH至7.0-8.0。2)发酵结束后,将发酵液离心,固液分离,得上清液和菌丝(即图1中菌丝体)两部分;3)、抗HIV活性化合物的提取:所得菌丝用质量百分数50%丙酮在室温下超声(功率90%)提取两次,每次30min,得图1中丙酮提取物,减压回收丙酮,再用等体积的乙酸乙酯萃取三次,得图1中乙酸乙酯部位,于45℃减压回收乙酸乙酯,得棕褐色浸膏;4)、抗HIV活性化合物的分离:将所得浸膏用正相硅胶柱层析分离,得图1中目标组分1,其中洗脱液为石油醚与乙酸乙酯体积比2:1的混合液,按此体积比配制的洗脱液分离得到的组分中可富集到较多的目标化合物;接着进行SephadexLH-20柱层析分离,以甲醇为溶剂洗脱,得图1中目标组分2;再进行半制备型反相C18柱分离,以水相含0.01%TFA的90%甲醇-水为流动相恒定洗脱,按色谱峰收集,冷冻干燥,即得Surfactin类目标化合物。上述各分离过程的洗脱条件采用本领域技术人员所熟知的各分离方法的常规洗脱条件。所得的Surfactin类化合物1-4均为白色固体粉末,易溶于甲醇、乙醇等溶剂中,其分子式分别为C51H89N7O13,C52H91N7O13,C52H91N7O13,C53H93N7O13,结构如式(II)所示。其1H-NMR和1C-NMR谱图如图2-图9所示。经检测,所得化合物荧光显色和硫酸显色不明显,碘熏显淡黄色,用氯仿-甲醇-水(体积比70:15:2)溶剂体系展开Rf值为0.3~0.4左右。对所得化合物进行HPLC检测,检测条件:Agilent1100series高效液相色谱仪,Alltech2000ES(Evap:110/Gas:2.4ml/min)检测器,甲醇-水(0.01%TFA)(88:12)流动相,PhecdaC18(4.6mm*250mm,5μm)色谱柱,化合物的保留时间分别为:20.5min,26.8min,28.9min,34.5min。实施例2Surfactin类化合物1-4的抗HIV活性测试应用假病毒细胞水平药理筛选模型测定活性化合物的抗HIV-1活性。1.药理筛选模型的原理该高通量筛选模型应用重组技术,将表达HIV-1核心和VSV-G的质粒共转染293T细胞后生成以VSV-G外壳包裹HIV-1核心的VSVG/HIV假病毒颗粒,是以HIV-1复制为靶标的细胞水平筛选模型。HIV-1基因组去除了HIV-1的env,因此其单独转染后形成的病毒颗粒不能再次感染宿主细胞,可在常规实验室进行操作;同时在nef基因的位置引入了荧光素酶报告基因,报告基因的活性可以反映假病毒在细胞中的复制水平。水泡性口膜炎病毒(vesicularstomatitisvirus,VSV)的受体在多种细胞内广泛存在,可以进入多种细胞系。将表达水泡性口膜炎病毒外壳蛋白的质粒pCMV-VSV-G与质粒pNL4-3Luc.R-E-共转染至293T细胞后,可组装成为VSVG/HIV假病毒。假病毒感染人T淋巴细胞SupT1细胞后,通过测定报告基因的表达可以间接反映对HIV复制水平。2.样品制备化合物样品:将实施例1中所得的Surfactin类化合物1-4分别溶解在DMSO中,制备成浓度为2mM的样品溶液。3.样品活性检测将浓度为5×105/ml的SupT1细胞直接铺96孔板(空白对照孔除外),每孔200μL;按20μL/mL细胞比例加入病毒颗粒,分别向反应体系中添加各组分:A.空白对照组:在96孔板中加200μL空白培养基。B.阴性对照组(化合物):向活性测定体系中加入2μlDMSO溶剂,反应体系的总体积为200μl。C.阳性对照组:向活性测定体系中加入2μlEFV(1μM)溶剂,反应体系的总体积为200μl。D.样品实验组(化合物):取2μl用DMSO溶解的待测样品加入到该活测定体系中,反应体系的总体积为200μl。将96板置于37℃孵育48h。取50μL细胞悬液,加入2X裂解液50μL,37℃孵育半个小时后,取其中5μL细胞裂解液加入40μL荧光素酶底物,在荧光检测器上测定荧光素酶的活性(RLUs)。依照下述公式计算HIV抑制率:4.测试结果样品浓度(μM)抑制率(%)Efavirenz(EFV)0.0199.9化合物12084.4化合物22089.6化合物32088.3化合物42094.6实施例3Surfactin类化合物1-4抑制Vif降解APOBEC3G(hA3G)1.所得的Surfactin类化合物1-4抑制Vif降解hA3G293T铺板于6孔板,细胞浓度2.0×105个/ml。24h后,共转hA3G(600ng)与vif(200ng),转染试剂采用Lipofectamine2000(Invitrogen)。转染12h后,加入阳性对照药MG132((5μM))与所得的Surfactin类化合物1-4(各20μM),作用36h后,收集细胞样品,加入上样缓冲液金属浴加热,保存于-20℃。测试样品经聚丙烯酰胺电泳和转膜后,依次加入抗体。一抗HA抗体(hA3G)1:3000,vif抗体1:5000,二抗山羊抗兔1:3000。结果发现,发现阳性对照药即MG132和筛选到的Surfactin类化合物1-4均能不同程度的抑制hA3G蛋白的降解(见图10)。2.化合物对vif与hA3G相互作用的影响。293T铺板于10cm培养皿,细胞浓度2.0×105个/ml。24h后,共转hA3G(1800ng)与vif(600ng),转染试剂采用Lipofectamine2000(Invitrogen)。转染12h后,加入阳性对照药MG132((5μM))与Surfactin类化合物1-4(各20μM),作用36h后,5ml预冷PBS收集细胞样品。。加入0.5mlNP-40裂解液裂解,冰上处理1h,每10min涡旋振荡一次。4℃,12000g离心10min。取上清,即得到细胞总蛋白。取出40μl,加入10μl5×蛋白上样缓冲液。金属浴加热得到Pre-IP蛋白样品,储存于-20℃或者-80℃。剩余蛋白样品用上述NP-40裂解液补充体积到0.5ml,加入抗体anti-HA兔(1:200),4℃混合孵育4h。加入20μlProteinA琼脂糖珠,4℃混合孵育过夜。4℃,1000g离心5min,弃上清,1ml冰上预冷的PBS清洗4次。加入上样缓冲液,金属浴加热,离心取上清,得到IP样品,WesternBlot检测。Westernblots抗体:一抗HA抗体兔(hA3G)1:3000,vif抗体1:5000,二抗山羊抗兔1:3000。结果发现,Surfactin类化合物1-4对于vif与hA3G相互作用无明显影响(见图11)实施例4链霉菌(Streptomycessp.)CPCC201585发酵液的提取方法及提取物的抗HIV-1活性测试1、链霉菌(Streptomycessp.)CPCC201585发酵液的提取方法1)、将上述链霉菌(Streptomycessp.)CPCC201585接种于斜面培养基,28℃下培养4天;活化后挑取菌丝块接种到液体发酵培养基中,28-30℃下摇床震荡培养5d。所述液体发酵培养基配方如下:葡萄糖5g,酵母膏5g,蛋白胨5g,牛肉膏5g,玉米浆4g,黄豆饼粉10g,碳酸钙4g,二氯化钴(0.002%溶液)1mL,可溶性淀粉20g,加水至终体积1L,调pH至7.0~8.0。2)向所得发酵液中加入等体积的质量百分数50%丙酮,室温下超声提取两次,每次20~30min,离心,上清液回收丙酮后再经真空冷冻离心干燥12小时即得发酵液提取物。2、丙酮提取物的抗HIV-1活性测试将所得丙酮提取物溶解在DMSO中,制备成浓度为3mM的样品溶液,按实施例2中的方法进行抗HIV活性测定,结果显示丙酮提取物在4mg/mL浓度下的HIV-1抑制率为94.2%。虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1