包含支化聚合物的颗粒的制作方法
本发明涉及包含有机聚合物的颗粒。这些颗粒可用于例如药物递送应用。
背景技术:
我们之前公开了多种聚合物材料和技术来产生可用于包括生物学和纳米技术的多种领域的分子结构。
例如,WO 2009/12220公开了聚合物-树枝状聚合物杂化物(hybrid),也称为聚树枝状分子(polydendron),其包含携带树枝状分子的支化乙烯基聚合物支架:这些聚树枝状分子由于它们的多重支化性质具有部分的有利的树枝状聚合物类性能,而没有复杂的常规树枝状聚合物加工的缺点。
能够控制这种材料的性能,包括例如它们的尺寸、尺寸分布、官能度、疏水性/亲水性、和在用于例如生物应用情况下的含水体系的体系中的行为,是有用的。
我们现在研发了新种类的有用的材料。
技术实现要素:
本发明的第一方面提供了包含支化聚合物以及嵌段共聚物或线性树枝状杂化物中的任一种的颗粒。
支化聚合物可以是多种类型。两种实例类型是支化乙烯基聚合物和支化聚酯。
可以通过已知的方法由单官能的乙烯基单体和二官能的乙烯基单体(支化剂)制备支化乙烯基聚合物。
可以通过例如单官能的内酯单体和二官能的内酯单体(支化剂)的开环聚合制备支化聚酯。
嵌段共聚物包含嵌段或片段,其各自具有各嵌段内的相同类型的重复单元并且在嵌段片段之间是不同的。发现本发明使用二嵌段共聚物(即具有两种不同嵌段的共聚物)是特别有效的。可以使用其他嵌段共聚物,例如三嵌段共聚物。
线性树枝状杂化物,也称为线性树枝状聚合物,同样包含不同的片段,其中的一种是线性聚合物链且另一种是树枝状分子。我们发现使用包含以树枝状分子封端或起始的均聚物的线性树枝状杂化物是特别有效的。然而,在本发明可以使用其他类型的线性树枝状杂化物(例如其中线性聚合物本身是共聚物,例如统计共聚物、嵌段共聚物或二嵌段共聚物)。因此,例如,线性树枝状杂化物可以包含连接至另一个嵌段,其然后连接至树枝状分子的一个嵌段。
颗粒可以是纳米颗粒,例如其中至少一个尺寸、或其中z平均直径(也称为平均流体力学直径)不大于约1000nm的颗粒。颗粒可以具有小于800nm、或小于500nm、或小于300nm、例如约50至300nm、或50至250nm、或100至200nm的z平均直径。
重要的是注意本发明的颗粒含有两种类型的聚合物材料,即支化聚合物以及嵌段共聚物或线性树枝状杂化物中的任一种(和可选地如以下所讨论的另外的材料),但是这些没有彼此共价键连。相反,如在例如WO2009/12220中公开的,聚树枝状分子含有共价附接至支化乙烯基聚合物支架的树枝状分子单元。在本发明中,不同的聚合物材料在颗粒结构内彼此结合但不是彼此共价键合。优选地,大部分、或基本上所有、或所有的颗粒具有相同的一般结构。其中各部分结合、混合或组合的普通方式带来了可靠的和可再现的性能。
本发明中的聚合物结构的组合带来特定的优点。
第一主要组分支化聚合物组分通常可以是疏水性的并因此可用于提供结合、携带或包封疏水性化合物、部分或负载(例如药物)的环境。可替换地,其可以具有亲水性质。其可以响应于pH或其他条件或刺激使得其性质、例如其疏水/亲水性质、其结构、和/或其在液相中的行为可以根据环境改变。
第二主要组分具有至少两种片段(在嵌段共聚物的情况下不同的均聚物或共聚物嵌段,或在线性树枝状杂化物的情况下线性聚合物嵌段加树枝状分子)。这使得到的颗粒能够适合或适应用于各种介质和环境以及用于各种应用。这还使片段中的一种能够充当稳定剂来稳定液体介质,例如含水介质内的颗粒,以及可选地提供盐稳定性以稳定在生命系统中可能遇到的各自盐条件和/或各种生理条件中的颗粒。
嵌段共聚物或线性树枝状杂化物可以包含疏水性片段。这使其能够与疏水性支化聚合物(和可选地具有疏水性传送材料)结合。疏水片段可以包含乙烯基聚合物。
嵌段共聚物或线性树枝状杂化物可以包含亲水性片段。这在例如含水环境中是有用的并能够稳定纳米颗粒。亲水性片段可以包含例如聚醚结构如聚乙二醇(PEG)或PEO。
当然,嵌段共聚物或线性树枝状杂化物可以包含疏水性片段和亲水性片段两者,并从而表现出两亲行为。
因此,我们研发了特别有利的组合,其中支化聚合物是疏水性的并形成疏水核,并且其中嵌段共聚物或线性树枝状杂化物是两亲的,使得其一种片段可以与疏水核结合且其另一种片段可以在含水介质中稳定颗粒。这些在尺寸以及在含水介质和改变的盐条件下的稳定性方面表现出相当大的均一性。
然而,聚合物的其他类型的组合和因此的性质在其他情形下也是有用的,并在本发明的范围内。
支化聚合物、嵌段共聚物或线性树枝状杂化物可以包含响应于pH或其他条件或刺激的化学性质使得其性质、例如其疏水/亲水性质可以根据环境改变。
线性树枝状杂化物包含线性聚合物链和树枝状分子。所述线性聚合物链可以本身是共聚物,例如统计共聚物或嵌段共聚物。
颗粒可以包含进一步的材料,例如化合物、有机化合物、疏水性化合物、亲水性化合物、药物、前体药物或治疗上、诊断上或生物上有用材料。实际上,本发明的一种主要用途是药物递送。
进一步的材料、例如药物或生物活性材料可以作为颗粒内的单独的化合物包含或包含在颗粒内的单独化合物内,或可以共价键合至聚合物结构中的一种,例如共价键合至支化聚合物、嵌段共聚物或线性树枝状杂化物。
从进一步的方面,通过共沉淀制备颗粒。
制备方法可以包括:
‐将支化聚合物和嵌段共聚物或线性树枝状杂化物中的任一种以及可选地其他组分溶解在溶剂中以形成溶液;
‐将所述溶液添加到不同的液体中,
‐除去溶剂以形成共沉淀的颗粒在液体内的分散体。
可以通过例如使得所述溶剂蒸发或通过透析除去溶剂。
分散体可以原样用于例如治疗应用的应用,或可替换地,可以浓缩或凝胶化该分散体,或可以除去液体以产生固体颗粒。
材料溶解在其中的溶剂可以是有机溶剂,合适地是与其中沉淀出现的液体可互溶的溶剂,例如水溶性的溶剂。例如,材料溶解在其中的溶剂可以是例如丙酮、乙腈、二甲基甲酰胺、二甲亚砜、二噁烷、乙醇、异丙醇、甲醇、四氢呋喃和它们的任意组合和混合物或包含水的组合。
材料溶解在其中的溶剂可以是因为其相对容易蒸发而选择的一种,例如具有80摄氏度或更低、或70摄氏度或更低、或60摄氏度或更低的沸点的一种。
其中发生沉淀的液体可以是例如水或其他含水体系、或其中材料不能溶解或相比第一溶剂溶解较不良好的其他液体。
可以使用多种水溶液。一些实例包括:
-碱金属/卤素盐(例如NaCl、LiBr、KCl)的所有浓度(最高达饱和)的水溶液
-0至12pH范围内的水溶液,包括酸和碱(布朗斯特-劳里(-Lowry)无机和有机酸以及碱)溶液(例如,例如HCl、H2SO4、乙酸、NaOH或KOH的水溶液)
-表面活性剂(例如十二烷基硫酸钠、两亲性二嵌段共聚物、)在水中的所有浓度(临界胶束浓度以上和以下)的溶液
-所有合适浓度的含水体系中的生物培养基[例如输送缓冲剂(transport buffer)、牛血清蛋白(BSA)、培养基杜尔伯科改良伊格尔培养基(dulbecco’s modified eagle’s medium)(DMEM)、洛斯维帕克纪念研究所(Roswell park memorial institute)1640(RPMI 1640)、胎牛血清(FBS)]及它们的混合物。
以上所列的含水体系提供了其中本发明作用、符合包括治疗应用的各种条件下的应用的各种各样的体系的一些指示,其中存在承受变化的以及有时极端的生理环境的需要。
其中沉淀发生的液体可以是水和有机溶剂的混合物,例如丙酮/水混合物、THF/水、MeOH/水、EtOH/水或IPA/水。这种混合物中的水的量可以可选地是按体积计2份水比按体积计1份有机溶剂、或大于按体积计2份水(例如大于3份水,例如大于4份水)比按体积计1份有机溶剂。
本发明相比现有技术的区别的发明点之一在于本发明涉及两种特定类型的聚合物同时从有机溶剂共沉淀到水中。尽管有机聚合物的沉淀(包括纳米沉淀)之前在多个文献中公开并且已经以不同的成功程度实施(参见例如Slater et al,Soft Matter 2012,8,9816-9827),但是这还没有涉及本发明中限定的聚合物类型的组合。我们首先认识到并证明了这种共沉淀的益处。
可选地,可以进行共沉淀多次。因此,在液体中形成共沉淀的颗粒的分散体(以及随后除去有机溶剂)之后,可以另外进行以下方法步骤一次或多次:
‐将另外的溶液(支化聚合物以及嵌段共聚物或线性树枝状杂化物中的任一种以及可选地其他组分在溶剂中的溶液)添加到液体中,
‐除去溶剂。
我们发现通过多次进行共沉淀,可以增加液体内的颗粒的浓度,同时基本上保持颗粒尺寸、PdI和稳定性。换句话说,可以使用多次纳米沉淀来提供每单位体积更多的相同类型的纳米颗粒,而可以预期多次纳米沉淀将导致显著较大的颗粒、不同的分散性特征或不稳定性。这在促进药物递送中是特别有利的,其中增强的有效载荷可以导致实际的治疗优势和成本效益。
支化聚合物组分
支化聚合物是本发明的颗粒中的主要组分。
支化聚合物是非凝胶化的和可加工的并可选地具有低粘度。如以上关于通过从这种溶剂沉淀到不同的介质中形成颗粒的合适方法所描述的,其可溶于有机溶剂。其可以与不可溶和/或表现出高粘度的聚合物结构如大规模交联的不可溶聚合物网络、高分子量线性聚合物或微凝胶形成对比。
支化乙烯基聚合物
支化聚合物可以是支化乙烯基聚合物。其可以通过以下制备但不限于此:活性聚合、受控聚合或常规的链增长聚合技术如自由基聚合。几种类型的活性和受控聚合是本领域已知的并适合用于本发明。优选类型的活性聚合是原子转移自由基聚合(ATRP);然而通过有意添加链转移剂控制的其他技术如可逆加成-裂解链转移(RAFT)和氮氧调控聚合(NMP)或常规的自由基聚合也是合适的合成。
技术人员知道提供支化但非凝胶化的乙烯基聚合物的技术。例如,以下中描述了合适的流程:N.O’Brien,A.McKee,D.C.Sherrington,A.T.Slark and A.Titterton,Polymer 2000,41,6027-6031;T.He,D.J.Adams,M.F.Butler,C.T.Yeoh,A.I.Cooper and S.P.Rannard,Angew.Chem.Int.Ed.2007,46,9243-9247;V.Bütün,I.Bannister,N.C.Billingham,D.C.Sherrington and S.P.Armes,Macromolecules 2005,38,4977-4982;I.Bannister,N.C.Billingham,S.P.Armes,S.P.Rannard and P.Findlay,Macromolecules 2006,39,7483-7492;和R.A.Slater,T.O McDonald,D.J.Adams,E.R.Draper,J.V.M.Weaver and S.P.Rannard,Soft Matter 2012,8,9816-9827。本发明的非凝胶化的和可溶的产物不同于L.A.Connal,R.Vestberg,CJ.Hawker and G.G.Qiao,Macromolecules 2007,40,7855-7863中公开的材料,已知其在凝胶化网络中包含多重交联。
每个乙烯基聚合物链的聚合起始于引发剂。单官能乙烯基单体的聚合导致线性聚合物链。与二官能乙烯基单体的共聚导致链之间的支化。为了控制支化和防止凝胶化,每条链应存在少于一个有效的支化物(二官能乙烯基单体)。在某些条件下,其可以通过使用小于一的支化物与引发剂的摩尔比实现:这假设单体(即单官能乙烯基单体)和支化物(即二官能乙烯基单体)具有相同的反应性而不存在分子内反应,支化物的两个官能团具有相同或类似的反应性,以及反应性即使在部分反应之后保持相同。当然,体系和条件可以不同,但是技术人员理解如何控制反应和在没有过度实验的情况下确定如何实现非凝胶化的结构。例如,在稀释条件下,一些支化物形成限制链之间的支化的支化物的数目的分子内环,即使反应中的支化物与引发剂(即聚合物链)的摩尔比高于1:1。
用于聚合过程的引发剂和其他试剂如本领域已知的。例如,在ATRP中,方便的和有效的引发剂包括烷基卤化物(例如烷基溴化物),以及在常规的自由基聚合中,有效的引发剂包括偶氮化合物。
其他支化聚合物
其他合适类型的支化聚合物包括支化聚酯。可以通过例如单官能的内酯单体和二官能的内酯单体(支化剂)的开环聚合制备这些。开环聚合方法和材料是本领域例如由Nguyen et al.,Polym Chem 2014,5,2997-3008已知的。
支化聚合物相对于线性聚合物和其他可选组分的量
支化聚合物(例如支化乙烯基聚合物)的量可以可选地不大于95wt%、或不大于75wt%、或不大于50wt%、或不大于10wt%、或不大于1wt%。在这方面,wt%表示作为颗粒中的固体材料的总质量的百分比的支化乙烯基聚合物的量。支化聚合物的量可以可选地是至少0.1wt%、或至少0.5wt%。例如,支化聚合物的量可以在约0.1wt%和95wt%之间、例如1wt%和10wt%之间。
出乎意料地,我们发现相对少量的支化聚合物(可选地在一些情况下约1-10wt%)对于能够引导纳米沉淀并使得形成窄分散度的规则颗粒是有效的。因此,在一些应用中,这可以带来使得他组分(即嵌段共聚物组分或线性树枝状杂化物加任何其他组分例如携带的材料)的量最大化的益处。
嵌段共聚物组分
嵌段共聚物组分可以包含多种类型的聚合物,包括例如乙烯基聚合物、聚醚(例如PEO或PPO)、聚酯(例如聚己内酯或聚乳酸)、聚氨酯、聚酰胺或聚碳酸酯。存在(至少)两种不同的嵌段。形成每个嵌段的聚合物的类型可以相同或不同,尽管当然如果聚合物的类型相同,那么对于区分单体的嵌段或单体的混合物必须不同。
例如,嵌段共聚物可以包含两个嵌段,其各自是乙烯基聚合物链,其中,组成一个嵌段的乙烯基单体不同于组成另一个嵌段的乙烯基单体。
可替换地,形成每个嵌段的聚合物的类型可以不同。例如,嵌段共聚物可以包含是乙烯基聚合物链的一个嵌段和是聚醚链或聚酯链的第二嵌段。
制备其中一个嵌段是乙烯基链的嵌段共聚物的一种方便的已知方式是在乙烯基聚合过程中使用大分子引发剂,其中,大分子引发剂包含其他的或另一个嵌段。例如,大分子引发剂可以是包含PEO或其他聚合物链的溴化物引发剂。在进一步的变体中,所述引发剂可以是二官能的并因此可以允许制备三嵌段共聚物(例如A-B-A嵌段共聚物,其中A是经常为疏水性嵌段的乙烯基,以及B是亲水性嵌段PEO)。
PEO的分子质量可以是例如大于1,000g/mol,例如在1,000和10,000g/mol之间;例如是PEG 2K或PEG 5K。
另一个实例是使用带有羟基基团的聚合物(例如亲水性聚合物)作为大分子引发剂用于开环聚合(例如环酯,例如己内酯或其他环状结构)。可以使用已知的开环聚合技术。
合成二嵌段共聚物的其他方式包括例如一锅法(one-pot method),其中首先聚合一种单体(例如乙烯基单体)(通常首先是亲水性嵌段,但不是必须的),然后当第一反应达到期望的单体转化率时以及在没有第一嵌段的任何纯化的情况下,可以原位添加第二单体(如果第一单体导致亲水性嵌段,则其可以例如导致疏水性嵌段)。在每种情况下,添加的单体可以是导致每个嵌段内的统计共聚的单体的混合物。
可以使用其他已知的制备嵌段共聚物的方法。
线性树枝状杂化物
线性树枝状杂化物包含线性聚合物链和树枝状分子。树枝状分子共价附接至聚合物链。聚合物链可以包含多种类型的聚合物,包括乙烯基聚合物、聚酯、聚酰胺、聚碳酸酯、聚胺脂或聚醚(例如PEO或PPO)。
线性树枝状杂化物是由例如F.Wurm,H.Frey,Prog.Polym.Sci.2011,36,1-52的多个文献已知的。
可以以多种方式并入树枝状分子。一种可能的方法将树枝状分子用作例如乙烯基聚合中的大分子引发剂。这使得形成例如具有乙烯基聚合物链与链末端的树枝状分子的线性树枝状杂化物。也可以将树枝状分子用作链转移剂来调节和引发链增长聚合。
为了能够引发聚合,树枝状分子必须带有合适的反应性官能团。例如,在ATRP中,在它们的焦点处携带卤化物(例如溴化物)的树枝状分子可以充当引发剂。在这种情形下,扩增在树枝状分子“楔”的顶点或焦点处开始。技术人员熟知用于包括ATRP和其他活性或受控聚合以及常规的自由基聚合的聚合的组分和试剂的类型,并因此用于它们的必须存在于或被引入至树枝状分子的类型的官能团充当引发剂或链转移剂。
例如,将溴基团引入至树枝状分子的一种可能的方式是用α-溴代异丁酰溴官能化树枝状分子醇。然而存在许多官能化树枝状分子使得它们可以充当引发剂和链转移剂的其他方式以及将引发聚合的其他类型的官能团。树枝状分子引发剂的概念适用于所有合适类型的聚合,并且官能团可以根据需要改变。
并入树枝状分子的另一种方法包括使用具有合适的官能团(例如-OH基团)的树枝状分子的例如环状酯的开环聚合。
进一步的方法将树枝状分子用作链转移剂用于使用可逆加成裂解链转移(RAFT)的聚合或常规的自由基聚合。
其他可能的方法包括经由链端/树枝状分子连接,例如通过使用焦点处的硫醇基团的聚合物的后官能化。
可以使用本领域已知的用于将树枝状分子并入线性树枝状杂化物中的其他方法。
关于可以使用的树枝状分子的类型或用于制备树枝状分子的化学过程没有特别的限制。在一些情形下,期望在表面(即树枝状分子的“树枝”的尖端)具有特定的基团,并且可以在树枝状分子的合成期间并入这些。树枝状分子优选地是非乙烯基的。
可以使用任何合适的连接化学过程来构建树枝状分子。在一个实施例中,可以例如使用羰基二咪唑将胺和醇连接在一起。然而,这仅是一个实例,且多种其他连接方法如迈克尔加成化学过程或熟知的酯化技术是可能的。
树枝状分子可以包含多个部分,包括例如胺(例如在叔胺中心分支的树枝状分子,或以NMe2基团封端的树枝状分子)、羟基基团、酸、羧基基团或PEG基团。
支化聚合物可以可选地包含醇基团。
支化聚合物可以可选地包含胺基团。
支化聚合物可以可选地包含羧基基团。
嵌段共聚物可以可选地包含醇基团。
嵌段共聚物可以可选地包含胺基团。
嵌段共聚物可以可选地包含羧基基团。
线性树枝状杂化物的聚合物链可以可选地包含醇基团。
线性树枝状杂化物的聚合物链可以可选地包含胺基团。
线性树枝状杂化物的聚合物链可以可选地包含羧基基团。
附图说明
实施例、附图和实验详述
现将参考以下附图,通过示例的方式对本发明进行进一步非限制性详细地描述,其中:
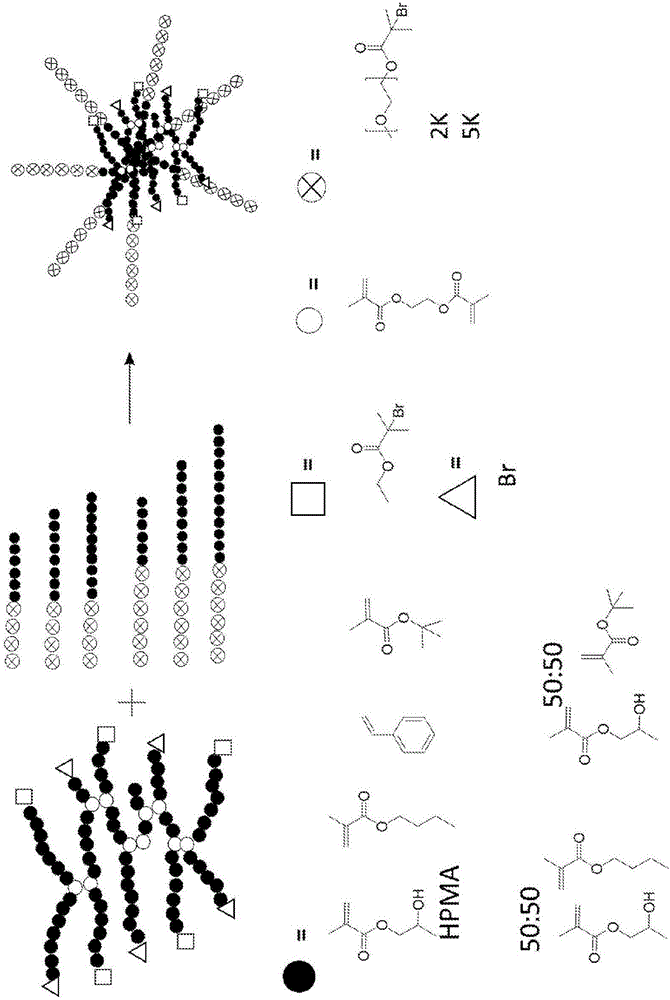
图1示出了支化乙烯基聚合物、二嵌段共聚物、和含有支化乙烯基聚合物和二嵌段共聚物的本发明的颗粒、以及可用于制备聚合物的一些单体的图示;
图2示出了根据本发明的一种可能的共沉淀流程的图示;
图3示出了根据本发明的一些纳米颗粒的SEM图像;
图4和5示出了本发明的颗粒对盐溶液和随时间的稳定性;
图6示出了根据本发明的纳米颗粒的SEM图像;
图7至12示出了负载药物的颗粒的粒径分布;
图13示出了支化聚合物、线性树枝状杂化物、和包含该两者的两种不同结构的本发明的纳米颗粒;
图14至18示出了支化聚合物和线性树枝状杂化物的一些组合以及它们的性质;
图19示出了一些纳米颗粒的SEM图像;以及
图20示出了本发明的一些纳米颗粒对细胞存活率的影响。
具体实施方式
包含支化聚合物和嵌段共聚物的颗粒
根据本发明的一组颗粒是包含支化聚合物和嵌段共聚物的那些。
图1示出了使用的一些组分的总览。支化乙烯基聚合物(左上)含有由乙烯基单体形成的直链,其通过支化物支化。可以使用各种各样的乙烯基单体,示出了其中的一些实例(左下)。
如本文所使用的图1的左下方所示的乙烯基单体和它们的缩写如下:
‐HPMA:甲基丙烯酸羟基丙基酯。示出了甲基丙烯酸2-羟基丙基酯,尽管本发明不仅可以单独利用该异构体而且可选地可以利用可商购的该异构体和甲基丙烯酸2-羟基异丙基酯的混合物或单独的后者。
‐nBuMA:甲基丙烯酸正丁酯
‐苯乙烯
‐tBuMA:甲基丙烯酸叔丁酯
‐DEAEMA:N,N-二乙基氨基乙基甲基丙烯酸酯,与上述单体相比是亲水性的单体和pH响应的。
如图1所指出的,可以使用单体的组合,例如HPMA和nBuMA或HPMA和tBuMA。
使用的其他材料包括以下,也在图1中示出:
‐EBIB:α-溴代异丁酸乙酯,通常用于引发聚合的引发剂。
‐EGDMA:二甲基丙烯酸乙二醇酯,合适的支化物
‐PEG 2K或PEG 5K:大小2K或5K的聚氧化乙烯(尽管当然其他大小也是可能的),其是溴官能化的使得其可以充当用于乙烯基聚合的大分子引发剂。由于存在于聚氧化乙烯(PEO)中的氧化乙烯基团的数目,PEG 2K还称为PEO45以及PEG 5K还称为PEO114。
也可以使用其他单体、支化物、引发剂和其他材料,包括:
‐BDME,1,4-丁二醇二(甲基丙烯酰氧基)-乙基醚,pH响应支化物
示出了长度变化的二嵌段共聚物(中上):这些可以例如具有由选自示出的那些的乙烯基单体(例如HPMA)形成的一个嵌段和不同化学过程(例如聚氧化乙烯)的第二嵌段。一种可能的制备流程将溴官能化的聚氧化乙烯(例如PEG 2K或5K)(图1,右下)用作用于乙烯基聚合的大分子引发剂。得到的两亲性二嵌段共聚物可以与支化乙烯基聚合物共沉淀以形成右上示意性示出的颗粒。在该实例中,示出嵌段共聚物的亲水性聚氧化乙烯链在颗粒的外侧,如在含水体系中的情况。
如图2所示,可以例如通过将合适的有机溶剂中的两种聚合物添加到水中,然后使有机溶剂蒸发来进行共沉淀。
支化乙烯基聚合物(聚-HPMA-EGDMA)与两亲性二嵌段共聚物(一个嵌段是PEG 5K或PEG 2K,以及另一个是HPMA40、HPMA80或HPMA120)以多种比率的共沉淀的粒径(动态光散射尺寸)和多分散系数(PDI)值在下表中示出。
可以看出在这些实例中,共纳米沉淀颗粒的尺寸(z均直径)在90至230nm的范围,且自始至终存在较窄的PDI值,示出它们的一致性和均一性。
SEM示出了纳米颗粒的尺寸和球形性质。图3示出了一些实例:支化乙烯基聚合物(聚-HPMA-EGDMA)与PEG 5K-HPMA120以比率80:20(上)和90:10(中)以及与PEG 2K-HPMA120以比率50:50(下)的共沉淀。
图4示出了多种颗粒对盐溶液(0.5M NaCl)的稳定性。“空白”表示在添加盐之前,“瞬时”为添加盐之后马上、且1、7和21为添加盐之后的天数。颗粒表现出相当大的盐稳定性,这对于用于生理环境是重要的。之前仅由单独的支化乙烯基聚合物形成的颗粒的实例示出在盐存在下是不稳定的(Slater et al,Soft Matter 2012,8,9816-9827)。
以下实施例提供了含有疏水性核和两亲性二嵌段稳定剂的一些纳米颗粒的更多细节。
实施例1:包含支化的疏水性核聚合物和直链两亲性二嵌段共聚物的纳米颗粒
聚合物的制备
将ATRP用于合成直链PEO45-p(HPMA120)以及EGDMA和HPMA p(HPMA50-EGDMA0.9)的支化统计共聚物。通过三重探测(triple detection)凝胶渗透色谱法(GPC)和1H NMR分析聚合物。将苯甲醚用作内标通过1H NMR监测单体至聚合物的转化率。
在30℃下甲醇中的一步ATRP反应期间合成直链两亲性嵌段共聚物。为了引入亲水性嵌段,以以下比率[大分子引发剂]:[单体]:[Cu(I)Cl]:[Bpy]=1:120:1:2将PEO45-Br大分子引发剂(2kDa)与催化体系Cu(I)Cl/2,2’-双吡啶(Bpy)添加到HPMA中。目标的数均聚合度(DPHPMA)是120HPMA单体单元且GPC确认了数均DPHPMA=127单体单元(Mn=20300Da),具有较窄的分散性
使用之前描述的催化体系以以下比率[大分子引发剂]:[EGDMA]:[单体]:[Cu(I)Cl]:[Bpy]=1:0.9:50:1:2用2-溴代异丁酸乙酯(EBIB)引发HPMA和EGDMA的支化统计共聚。[EGDMA]/[EBIB]<1的摩尔比是重要的参数以对支化反应具有控制和避免凝胶化。如预期的,与显示出单峰窄分子量分布的直链两亲性聚合物形成对比,存在的EGDMA显著增加聚合物分子量(例如Mw=295,000Da)和分散性另外,直链PEO45-p(HPMA120)和支化p(HPMA50-EGDMA0.9)两者的1H NMR分析示出高的单体转化率(>98%)。
纳米沉淀和共纳米沉淀
通过纳米沉淀制备聚合物纳米颗粒,纳米沉淀对应于通过快速的沉淀反应将溶剂转换为水(环境温度)。假设在p(HPMA50-EGDMA0.9)疏水支化核的结合期间,来自二嵌段共聚物的直链HPMA链也变得并入疏水核,使得PEO45(2kDa)链存在于得到的颗粒的表面上并通过立体稳定化防止聚合。将重量分数变化的p(HPMA50-EGDMA0.9)x:PEO45-p(HPMA120)y(x:y)以5mg mL-1的总浓度溶解在丙酮中六个小时以确保完全溶解。1mL聚合物溶液至5mL水的快速沉淀给出丙酮完全蒸发之后1mg mL-1的最终的纳米颗粒浓度。通过动态光散射(DLS)和扫描电子显微(SEM)分析纳米颗粒分散体。将得到的z均直径(nm)、多分散系数(PDI)、ζ电位(mV)和数均直径(nm)收集在下表中。
表.通过共纳米沉淀p(HPMA50-EGDMA0.9)、PEO45-p(HPMA120)和p(HPMA50-EGDMA0.9)x:PEO45-p(HPMA120)y(x:y)丙酮溶液到水中得到的纳米颗粒的DLS和SEM表征
支化p(HPMA50-EGDMA0.9)和两亲性PEO45-p(HPMA120)聚合物在从丙酮至H2O的共纳米沉淀期间的自组装产生界限分明的颗粒,这通过分别由DLS测量和SEM观察得到的低PDI值(0.046-0.107)和尺寸均匀性指出。
共纳米沉淀的颗粒表现出-19mV和-25mV范围的ζ电位值(表1,项目3-7)。
盐稳定性
通过添加等份(20μL)的含水0.5M NaCl盐溶液到1mL的纳米沉淀的分散体中表明共沉淀的颗粒的盐稳定性。在0-21天期间测量z均直径和PDI。
共纳米沉淀的颗粒表明优异的在添加20μL之后的21天内的盐稳定性和窄多分散性的保持。仅包含支化乙烯基聚合物的纳米颗粒在添加NaCl时立即从溶液中析出,而包含支化乙烯基聚合物和二嵌段两亲性共聚物两者的纳米颗粒保持为稳定的纳米颗粒分散体。纳米颗粒(0.1mg mL-1)的SEM分析示出颗粒和由颗粒的组组成的共纳米沉淀的球形性质。
图5示出了在添加NaCl(20μL 0.5M NaCl)至p(HPMA50-EGDMA0.9):PEO45-p(HPMA120)60:40的1mg mL-1含水分散体时z均直径和PDI是如何变化的。纵轴表示强度(百分比)且横轴示出了z均直径(d,nm)。实线:添加之前。短划线:紧接添加NaCl之后。点线:添加NaCl之后21天。
图6示出了p(HPMA50-EGDMA0.9):PEO45-p(HPMA120)60:40;1mg mL-1的扫描电子显微图像。
实施例1的结论
实施例1示出以低浓度添加两亲性二嵌段“稳定剂”(PEO 2000Da)至支化疏水性聚合物,随后共纳米沉淀可以形成具有期望的z均直径和非常窄的PDI值的颗粒。可以制备各种各样的共纳米沉淀的颗粒。共纳米沉淀的颗粒由于引入了立体稳定剂而提供增强的稳定性。这依赖于防止颗粒变得极为贴近的材料的外层的形成。
HIV抗病毒剂的负载
研究了纳米颗粒负载包含以下HIV抗逆转录病毒的多种药物的用途:
依法韦仑(Efavirenz):
洛匹那韦(Lopinavir):
利托那韦(Ritonavir):
可以以可靠的和可再现的方式将药物包封在聚合物颗粒内,使得产生具有非常窄的粒径分布的颗粒。
发现在疏水核中使用支化乙烯基聚合物与两种单体[HPMA加甲基丙烯酸叔丁酯(tBMA)或甲基丙烯酸正丁酯(nBMA)中的任一种]的共混物在允许要实现的高药物负载中是特别有效的。当将nBMA用作支化乙烯基聚合物中的唯一单官能单体时也得到了良好的结果。
在图7至12中示出了结果如下:
图7-12中所示的利用为形成颗粒的嵌段共聚物是PEG 5K-HPMA120并且支化聚合物与直链聚合物的比率是50:50。
可以通过进一步使聚合物化学过程适于使得对依法韦仑实现25wt%的药物负载来增加药物负载。负载药物的颗粒稳定延长的时间。研究了不同药物类型的负载的进一步的实验以及这些的细节(以及在这方面的聚合物合成和共纳米沉淀)如下。
包含10wt%依法韦仑、利托那韦和洛匹那韦负载的一般的纳米颗粒制备
在一般的纳米颗粒制备期间,将5.5mL的依法韦仑、利托那韦或洛匹那韦的1mg/mL丙酮溶液添加到小瓶中并静置蒸发整夜。将25mg的支化聚合物和25mg的二嵌段聚合物添加到该小瓶中并在6-8小时期间将其溶解在10mL丙酮中以确保完全溶解。将1mL的聚合物和溶解药物的5mg/mL溶液添加到5mL的搅拌蒸馏水(500rpm)中并静置24小时用于完全蒸发丙酮(聚合物的最终浓度是1mg/mL)。
抗癌药物
可以合并的药物的其他实例是抗癌药物。
伊立替康(Irinotecan)是疏水性抗癌药物以及SN-38是伊立替康的疏水性抗癌活性代谢物。
特别地,将伊立替康以10wt%或15wt%有效包封在具有低PdI值的共纳米沉淀的颗粒中,例如其中,支化聚合物包含nBMA或tBMA-HPMA且两亲聚合物包含PEG5K-HPMA120。
伊立替康(一般10wt%负载)
在一般的纳米颗粒制备期间,将5.5mL的伊立替康的1mg/mL丙酮溶液添加到小瓶中并静置蒸发整夜。将25mg的支化聚合物和25mg的聚合物二嵌段添加到该小瓶中并在6-8小时期间将其溶解在10mL丙酮中以确保完全溶解。将1mL的聚合物和溶解药物的5mg/mL溶液添加到5mL的搅拌中的(500rpm)水中并静置24小时用于完全蒸发丙酮。
SN-38(一般2wt%负载)
在一般的纳米颗粒制备期间,将1.03mL的SN-38的1mg/mL的THF/乙腈(50:50)溶液添加到小瓶中并静置蒸发整夜。将25mg的支化聚合物核和25mg的聚合物二嵌段添加到该小瓶中并在6-8小时期间将其溶解在10mL丙酮中以确保完全溶解。将1mL的聚合物和溶解的药物的5mg/mL溶液添加到5mL的搅拌中的(500rpm)水中并静置24小时用于完全蒸发丙酮。
通过DMSO透析制备SN-38纳米颗粒
在通过透析的一般的纳米颗粒制备期间,添加2.65mL的SN-38的1mg/mL DMSO溶液、25mg的支化聚合物核和25mg的聚合物二嵌段,并在6-8小时期间将其溶解在7.35mL的DMSO中以确保完全溶解。将1mL的聚合物的5mg/mL溶液添加到具有2000g/mol截留分子量(MWCO)的透析袋中,并置于蒸馏水中透析4天(每4小时换水)。
ATRP聚合-支化聚合物核p(HPMA50-EGDMA0.9)的形成
目标的数均聚合度(DPn)是50重复单元。在一般的ATRP合成期间,将EBIB引发剂(0.14g,0.69mmol 1eq.)和HPMA(5g,34.68mmol 50eq.)添加到配备有氮气入口/出口和搅拌棒的圆底烧瓶中。添加甲醇(基于HPMA,50wt/wt%),并在氮气下强力搅拌溶液10-15分钟。将支化剂EGDMA(0.12g,0.62mmol,0.9eq.至EBIB引发剂)、铜催化剂Cu(I)Cl(0.069g,0.69mmol 1eq.)和bpy(0.22g,1.39mmol 2eq.)添加到烧瓶中并将温度固定在30℃。通过1H NMR质谱监测反应,并当HPMA单体达到>99%转化率时用甲醇终止反应。使用Dowex Marathon交换珠(~12g)纯化聚合物以除去过量的铜催化剂,随后使样品通过碱性氧化铝柱。在沉淀到冷的己烷中之前,在真空下除去过量的THF以浓缩样品。通过在MeOD中的1H NMR、使用THF洗脱液的三重探测GPC确认得到的聚合物。
对所有其他单体:nBMA p(nBMA50-EGDMA0.9)、tBMA p(tBMA50-EGDMA0.9)、HPMA-nBMA p(HPMA25-nBMA25-EGDMA0.9)和HPMA-tBMA p(HPMA25-tBMA25-EGDMA0.9)进行聚合
聚(乙二醇)单官能ATRP大分子引发剂(PEOx-Br)(当x=45时,大分子引发剂在本文中称为PEG 2K)的实例合成
在一般的合成中,在装有添加漏斗、氮气入口/出口和搅拌棒的两颈圆底烧瓶中在三乙胺(2.275g,22.5mmol,1.5eq.)和4-二甲基氨基吡啶(0.092g,0.75mmol 0.05eq.)的存在下将PEO45-OH(30g,15mmol,1eq.)溶解在100mL的甲苯中。将用25mL甲苯稀释的2-溴-2-甲基丙酰溴(5.175g,22.5mmol,1.5eq.)置于添加漏斗中。将反应器置于搅拌下,在约0℃下的冰浴中冷却,并在20-30min期间缓慢添加2-溴-2-甲基丙酰溴溶液。完成添加之后,使反应器达到室温并置于搅拌下24小时。白色沉淀(三乙胺盐)的形成表示反应进程。然后,在约50℃的水浴中使反应介质变热,过滤并在旋转蒸发器上浓缩。将得到的产物稀释在丙酮中并通过在石油醚中的沉淀来纯化。重复一次上一步骤,并最终在40℃下在真空下干燥产物24小时。以70%产率回收的得到的大分子引发剂,并通过在D2O中的1H NMR、使用DMF的洗脱液的三重探测GPC和MALDI-TOF质谱分析确认其结构。
PEG 5K
PEO-5K引发剂的相同合成-使用PEO114-OH而不是PEO45-OH。
ATRP聚合-直链PEO45-p(HPMA120)的合成
目标的数均聚合度(DPn)是120重复单元。在一般的ATRP合成中,将PEO45-Br大分子引发剂(0.62g,0.29mmol 1eq.)和HPMA(5g,34.68mmol 120eq.)添加到配备有氮气入口/出口和搅拌棒的圆底烧瓶中。添加甲醇(基于HPMA,33.5w/v%),并在氮气下强力搅拌溶液10-15分钟。将铜催化剂Cu(I)Cl(0.029g,0.29mmol 1eq.)和bpy(0.09g,0.58mmol2eq.)添加到烧瓶中并将温度固定在30℃。通过1H NMR质谱监测反应,并当HPMA单体达到>99%转化率时用甲醇终止反应。使用Dowex Marathon交换珠(~12g)纯化聚合物以除去过量的铜催化剂,随后使样品通过碱性氧化铝柱。在沉淀至石油醚30/40之前,在真空下除去过量的THF以浓缩样品。通过在d6-DMSO中的1H NMR、使用DMF洗脱液的三重探测GPC确认得到的聚合物。
上述流程适用于所有其他的对于HPMA以及PEO5K-nBMA120的ATRP的数均聚合度。
其他药物和其他药物并入方法
本发明还与许多其他药物以及并入药物的其他方法相容,并入药物的其他方法不仅包括如之前所述的包封而且包括化学键合(有时称为配合)至支化聚合物或直链聚合物中的任一种或颗粒的两种组分。
在这方面,将布洛芬用作模型药物。包封游离的布洛芬,且其还经由其酸官能团键合以产生前体药物模型。
布洛芬作用-前体药物模型
布洛芬(IBU)改性的HPMA(IbuPMA)的合成
在一般的合成期间,将HPMA(1.5g,10.40mmol 1eq.)、布洛芬(2.79g,13.53mmol 1.3eq)、DMAP(0.64g,5.5mmol,0.5eq)和DCC(2.79g,13.53mmol,1.3eq)溶解在圆底烧瓶中的40mL THF中并在环境温度下搅拌24小时。过滤DCU盐并用THF洗涤,随后旋转蒸发。添加DCM(100mL)并用1M硫酸氢钠溶液洗涤以除去过量的DCU,然后在MgSO4上干燥,在真空中浓缩并在0℃下存储。
ATRP聚合-并入的IBU单体:目标总计DP80
组合物PEO114-p(HPMA60-IbuPMA20)
目标的数均聚合度(DPn)是HPMA60-IbuPMA20。将PEO114-Br大分子引发剂(0.59g,0.12mmol 1eq.)和HPMA(1g,6.94mmol 60eq.)和IbuPMA(0.77g 2.3mmol,20eq.)添加到配备有氮气入口/出口和搅拌棒的圆底烧瓶中。添加甲醇(基于HPMA+IbuPMA,37w/w%),并在氮气下强力搅拌溶液10-15分钟。将铜催化剂Cu(I)Cl(0.0114g,0.12mmol1eq.)和bpy(0.036g,0.23mmol 2eq.)添加到烧瓶中并将温度固定在30℃。通过1H NMR质谱监测反应,并当单体达到99%转化率时用甲醇终止反应。使用中性氧化铝柱纯化聚合物,用THF冲洗以除去过量的铜催化剂。在沉淀至冷石油醚30/40之前,在真空下除去过量的THF以浓缩样品。通过在MeOD中的1H NMR、使用THF洗脱液的三重探测GPC确认得到的聚合物。
改性后的PEO114-HPMA120-目标40HPMA单体单元
将PEO114-HPMA120(1g,0.033mmol,1eq.)、布洛芬(0.27g,1.33mmol,40eq.)、DCC(0.274g,1.33mmol,40eq.)和DMAP(1x10-3g)溶解在THF(12mL)中并静置24小时。滤出DCU并用THF洗涤,和在真空中浓缩。将过量的DMAP和DCU溶解在DCM中,以及用1M硫酸氢钠洗涤和用MgSO4干燥并在真空下干燥。
ATRP聚合-支化IBU改性的共聚物p(HPMA60-IBU20-EGDMA0.9)
目标的聚合度(DPn)是50重复单元。在一般的ATRP合成中,将EBIB引发剂(0.024g,0.12mmol 1eq.)和HPMA(1.04g,7.23mmol 60eq.)和IbuPMA(0.8g,2.41mmol,20eq.)添加到配备有氮气入口/出口和搅拌棒的圆底烧瓶中。添加甲醇(基于HPMA,50wt/wt%),并在氮气下强力搅拌溶液10-15分钟。将支化剂EGDMA(0.021g,0.11mmol 0.9eq.至EBIB引发剂)、铜催化剂Cu(I)Cl(0.012g,0.12mmol 1eq.)和bpy(0.038g,0.24mmol 2eq.)添加到烧瓶中并将温度固定在30℃。通过1H NMR质谱监测反应,并当HPMA单体达到>99%转化率时用甲醇终止反应。使用中性的氧化铝柱纯化聚合物,用THF冲洗。在沉淀之前,在真空下除去过量的THF以浓缩样品。将聚合物从MeOH沉淀到冷的石油醚30/40中。通过在MeOD中的1H NMR、用THF洗脱液的三重探测GPC确认得到的聚合物。
纳米颗粒制备
IBU改性的二嵌段–p(EO)114-p(HPMA60-HPMA:IBU20):p(HPMA50-EGDMA0.9)
在一般的纳米颗粒制备中,在6-8小时期间将25mg的PEO114-p(HPMA60-HPMA:IBU20)和25mg的p(HPMA50-EGDMA0.9)添加到10mL的甲醇中以确保在6-8小时内完全溶解。将1mL的聚合物的5mg/mL溶液添加到5mL的搅拌中的(500rpm)蒸馏水中并静置24小时用于完全蒸发。
IBU改性的支化聚合物核p(HPMA60-IBU20-EGDMA0.9)
在一般的纳米颗粒制备过程中,在6-8小时期间将25mg的PEO114-p(HPMA120)和25mg的p(HPMA60-IbuPMA20-EGDMA0.9)添加到10mL的甲醇中以确保在6-8小时内完全溶解。将1mL的聚合物的5mg/mL溶液添加到5mL的搅拌中的(500rpm)蒸馏水中并静置24小时用于完全蒸发。
可以使用以上实验对纳米颗粒的其他变体重复相同流程。对于游离的IBU添加,可以在溶解之前以期望的比率将其简单地添加到甲醇中以得到颗粒内包封的IBU和IBU-前体药物的混合物。
示出可以制备不同类型的嵌段共聚物-三嵌段A-B-A(疏水-亲水-疏水)聚合物并将其与支化聚合物和药物包封组合使用的进一步的实施例
为了示出在本发明的范围内可以使用的化学过程的变体,制备双官能引发剂并将其用作“A-B-A”三嵌段共聚物的制备中的“B”嵌段。然后将三嵌段共聚物与支化乙烯基聚合物和药物分子组合使用以形成合适的共纳米沉淀的颗粒。
PEG双官能大分子引发剂的合成
在一般的合成期间,将OH-PEG104-OH(Mn~4600g,1当量,20g,4.3mmol)、TEA(3当量,0.013mol,1.83mL)和DMAP(0.1当量,4.0mmol,0.053g)添加到配备有氮气入口/出口和搅拌棒的两径圆底烧瓶中的甲苯(80mL)中。将α-溴代异丁酰溴(3当量,13mmol,1.61mL)稀释在甲苯(20mL)中,并在15分钟内经由滴液漏斗逐滴添加,并置于搅拌下24小时。然后过滤反应混合物并在真空中除去过量的溶剂。将产物溶解在最少量的丙酮中,沉淀至40-60℃的冷石油醚(1:10产物:溶剂)并使其在40℃下在真空中干燥48小时。
p(HPMAx-嵌段-PEG104-嵌段-HPMAx)嵌段聚合物的合成
在一般的合成期间,将Br-PEG104-Br(1当量,2.17g,0.43mmol,HPMA(80当量,5.0g,34.6mmol)、苯甲醚(0.1ml)和无水甲醇(50wt%)添加到配备有氮气入口/出口和搅拌棒的圆底烧瓶中。将无水甲醇(基于HPMA,50wt%)、CuCl(1当量,0.042g,0.43mmol)和bpy(2当量,0.135g,0.867mmol)添加到该溶液中,并在氮气下脱气反应混合物15-20分钟。将反应置于搅拌下24小时并通过1H NMR谱确认高转化率。通过添加甲醇(~50ml))终止反应,然后使剩余溶液通过中性的氧化铝柱以除去催化体系。通过在真空中浓缩溶液来纯化产物并将聚合物沉淀到冷的己烷(1:10产物:溶剂)中。通过1H NMR和GPC分析得到的嵌段共聚物。
如之前所描述的合成支化p(DEAEMA50)聚合物。
药物分子至由A-B-A三嵌段和支化聚合物核组成的共纳米沉淀的颗粒中的包封
将溶解的药物分子(利托那韦和洛匹那韦)的储备溶液添加到样品小瓶(每个最高达5wt%),并使丙酮蒸发蒸发。将支化聚合物、A-B-A三嵌段聚合物(每种的比率变化)和丙酮添加到该小瓶中以组成5mg/mL的溶液。为了确保完全溶解,是该溶液翻转24小时。在一般的共纳米沉淀过程中,将1mL的聚合物/药物溶液添加到5mL的搅拌中的水中。使溶液搅拌整夜以确保完全除去溶剂,以及随后通过动态光散射测量纳米颗粒分散体。
得到稳定的纳米颗粒,无论是包封单独的利托那韦、单独的洛匹那韦还是两者的按重量计1:1的混合物。
包含支化聚合物和直链树枝状杂化物的颗粒
根据本发明的第二组颗粒是包含支化聚合物和直链树枝状杂化物的那些。
通过ATRP制备的聚合物和这种聚合物在颗粒中的组合的实例
以上已经描述和限定了用于支化乙烯基聚合物和嵌段共聚物的组分的一些非限制性实例。
直链树枝状杂化物可以包含如以上提及的单体,以及另外地当然包含树枝状分子。在此背景下,用于本发明的聚合物的组分的一些非限制性实例包括以下。
‐G2-M:具有以下结构的2代树枝状分子引发剂:
‐G2-Bz:具有以下结构的具有苄基官能化的末端的2代树枝状分子引发剂:
‐G1-M:具有以下结构的1代树枝状分子引发剂:
‐G0-M:具有以下结构的0代引发剂:
图13示出了支化聚合物和直链树枝状杂化物的共纳米沉淀的图示。树枝状分子示出为楔。在一些实施例中(右上),假设树枝状分子至少部分在颗粒内,而在其他实施例中(右下),假设树枝状分子主要暴露在表面上。当使用pH响应材料如DEAEMA时,这可以通过改变pH控制。
图14至18中示出了聚合物的组合和在不同pH条件下得到的颗粒的性质的一些实例。图14至18使用缩写CNP,其表示共纳米沉淀。图19示出了包含EBIB tBuMA-EGDMA和G2-M DEAEMA(图14)的pH 7.8颗粒的SEM图像。
a作为如由动态光散射测量的z均值给出所有直径。
b作为如由动态光散射测量的表面电荷值给出所有ζ电位。
支化乙烯基聚合物和直链树枝状杂化物的组合的进一步实例
通过ATRP制备的支化乙烯基聚合物和直链树枝状杂化物的组合的进一步实例包括下表中所列的那些。这举例说明了一些化学性质(包括亲水、疏水和pH响应)和不同的共聚物方式(包括嵌段共聚物和统计共聚物)。还将看出将嵌段共聚物方式可以与直链树枝状杂化物方式组合,即直链树枝状杂化物可以包含连接到一个嵌段,然后连接到另一个嵌段的树枝状分子。此外,代替G2-M或G2-Bz,可以使用G1-M、G0-M或EBIB,即可以通过较小的树枝状分子或通过非树枝状分子(在这样情况下,与支化乙烯基聚合物共沉淀的材料不是直链树枝状杂化物而仅是直链聚合物,本发明涉及其的子集,即嵌段共聚物)的引发剂引发直链。
上表中的材料可以是例如以90:10支化:直链来共纳米沉淀的。一个合适的方法包括:将0.2ml(在丙酮、THF或IPA中5mg ml-1)直链聚合物和1.8ml(在丙酮、THF或IPA中5mg ml-1)支化聚合物滴入10mL水中;以及使有机溶剂蒸发整夜以形成1mg ml-1的纳米颗粒在水中的分散体。
可以使用一定范围的pH,以及可选地可以选择条件和单体来提供特定的结构。仅通过非限制性示例的方式,在低pH下胺部分(例如在DEAEMA或在树枝状分子中)的质子化是指胺部分更可能向颗粒外暴露。
通过开环聚合制备的聚合物和颗粒中的这种聚合物的实例
本发明中可以使用的另一种聚合方法是开环聚合(ROP)。例如,可以在本领域已知的合适条件下通过与醇反应使内酯单体开环。
例如,通过苄醇可以引发己内酯单体的聚合来产生苄基-聚己内酯(本文中缩写为Bz-PCL)。
单种内酯环如聚己内酯的开环导致直链聚合物。
通过使用支化物,例如具有连接在一起的两个内酯环的单体,例如BOD(4,4’-二环氧己烷基-7,7’-二酮)可以得到支化聚合物。以下方案示出了制备BOD的方法:
可以通过使用引发剂(例如Bz-OH))共聚单官能的内酯(例如己内酯)和二官能的内酯(例如BOD)制备支化聚酯。
可以将这种支化聚已酸内酯代替支化乙烯基聚合物与直链聚合物(即嵌段共聚物或直链树枝状杂化物)组合使用。
支化聚己内酯(通过ROP制备)和我们已经共纳米沉淀的直链树枝状杂化物(通过ATRP制备)的组合的实例包括下表中所列的那些。如之前的,代替G2,可以替代使用G1、G0或EBIB。
还可以将ROP用于制备直链树枝状杂化物(或其他直链聚合物组分),并可以组合ROP和ATRP。
可以在直链树枝状杂化物中使用聚酯,并且在此背景下用于ROP的合适引发剂的非限制性实例包括以下。
‐G2-pOH:以下结构的带有羟基基团以引发ROP的2代树枝状分子:
‐G1-pOH:以下结构的带有羟基基团以引发ROP的1代树枝状分子:
‐G0-pOH:以下结构的0代引发剂:
可以与例如Bz-PCL50-BOD0.6的支化聚合物组合的直链树枝状杂化物的实例包括:
‐G1-p-PCL50-DEAEMA20
‐G2-p-PCL50
‐G2-p-PCL30
‐G2-p-PCL20
用于ATRP和ROP聚合和用于制备在这些聚合中使用的材料的示例实验流程
1.通过ATRP的聚合
1.1 ATRP树枝状分子引发剂合成
1.1.1 G1-M-OH的合成
将2-(二甲基氨基)乙基丙烯酸酯(6.0g,42mmol,6eq.)添加到包含异丙醇(IPA)(12mL)的50mL圆形2颈圆底烧瓶中。在正向N2吹扫下将烧瓶脱氧10分钟。逐滴添加溶解在IPA(12mL)中的1-氨基-2-丙醇(0.5246g,7.0mmol,1eq.),同时在正向N2流下在冰浴中搅拌溶液。在0℃下搅拌最终的混合物另外的10分钟,之后使其温暖至室温并搅拌48小时。除去溶剂并使产物在真空中干燥整夜。测量的C,57.45;H,9.77;N,11.12%。C17H35N3O5要求,C,56.43;H,9.68;N,11.62%。1H NMR(400MHz,CDCl3)δ1.08(d,3H),2.18-2.62(m,22H),2.69(m,2H),2.89(m,2H),3.77(m,1H),4.16(m,4H)。13C NMR(100MHz,CDCl3)δ19.8,32.6,45.6,49.7,57.8,62.0,63.7,76.9,128.4,130.9,172.5。m/z(ES MS)362.3[M+H]+,384.3[M+Na]+。
1.1.2 G2-M-OH的合成
将2-(二甲基氨基)乙基丙烯酸酯(6.0g,42mmol,6eq.)添加到包含IPA(12mL)的50mL圆形2颈圆底烧瓶中。在正向N2吹扫将烧瓶脱氧10分钟。逐滴添加溶解在IPA(12mL)中的双(3-氨基丙基)氨基)丙-2-醇(1.3221g,6.984mmol,1eq.),同时在正向的N2流下在冰浴中搅拌溶液。在0℃下搅拌最终的混合物另外的10分钟,使其温暖至室温并搅拌48小时。除去溶剂并在使产物在真空中干燥整夜。测量的C,58.32;H,9.92;N,12.87%。C37H75N7O9要求,C,58.27;H,9.84;N,12.86%。1H NMR(400MHz,CDCl3)δ1.13(d,3H),1.67(m,4H),2.26-2.65(m,50H),2.77(m,8H),3.87(m,1H),4.17(m,8H)。m/z(ES MS)762.6[M+H]+,784.6[M+Na]+。
1.1.3 G0-M的合成
将1-二甲基氨基-2-丙醇(1.1207g,10.86mmol,1eq.)、三乙醇胺(TEA)(1.5390g,15.2mmol,1.4eq.)和二甲基氨基吡啶(DMAP)(132.7mg,1.086mmol,0.1eq.)添加到包含二氯甲烷(DCM)(160mL)的250mL的2颈圆底烧瓶中。在正向的N2吹扫下使烧瓶脱氧10分钟。逐滴添加α-溴代异丁酰溴(2.622g,1.4mL,11.4mmol,1.05eq.),同时在正向的N2流下在冰浴中搅拌溶液。使得反应混合物温暖至室温并置于搅拌下整夜。用饱和的碳酸氢钠(NaHCO3)溶液(3x30mL)洗涤有机相。用无水Na2SO4干燥溶液。测量的C,42.87;H,7.20;N,5.55%。C9H18NO2Br要求,C,42.86;H,7.14;N,5.55%。1H NMR(400MHz,CDCl3)δ1.27(d,3H),1.89(s,6H),2.17-2.55(m,8H),5.07(m,1H)。13C NMR(100MHz,CDCl3)δ17.6,30.9,46.1,56.1,63.5,70.6,76.9,170.8。m/z(ES MS)252[M+H]+。
1.1.4 G1-M的合成
将G1-OH(1.1207g,10.86mmol,1eq.)、TEA(1.5390g,15.2mmol,1.4eq.)和DMAP(132.7mg,1.086mmol,0.1eq.)添加到包含DCM(160mL)的250mL的2颈圆底烧瓶中。在正向的N2吹扫下使烧瓶脱氧10分钟。逐滴添加α-溴代异丁酰溴(2.622g,1.4mL,11.4mmol,1.05eq.),同时在正向的N2流下在冰浴中搅拌溶液。使得反应混合物温暖至室温并置于搅拌下整夜。用饱和的碳酸氢钠(NaHCO3)溶液(3x160mL)洗涤有机相。用无水Na2SO4干燥溶液并使产物在真空中干燥整夜。测量的C,49.41;H,7.90;N,8.23%。C21H40N3O6Br要求,C,49.41;H,7.84;N,8.24%。1H NMR(400MHz,CDCl3)δ1.22(d,3H),1.89(s,6H),2.24-2.69(m,22H),2.83(m,4H),4.20(m,4H),5.0(m,1H)。13C NMR(100MHz,CDCl3)δ18.6,30.9,32.8,50.0,56.4,58.8,60.3,69.6,77.2,125.7,144.3,172.3。m/z(ES MS)510.2[M+H]+,534.2[M+Na]+。
1.1.5 G2-M的合成
将G2-OH(5.1431g,6.749mmol,1eq.)、TEA(0.9561g,9.449mmol,1.4eq.)和DMAP(82.5mg,0.6749mmol,0.1eq.)添加到包含DCM(160mL)的250mL的2颈圆底烧瓶中。在10分钟正向的N2吹扫下使烧瓶脱氧。逐滴添加α-溴异丁酰溴(1.629g,0.88mL,7.087mmol,1.05eq.),同时在正向的N2流下在冰浴中搅拌溶液。允许反应混合物温暖至室温并置于搅拌下整夜。用饱和的碳酸氢钠(NaHCO3)溶液(3x160mL)洗涤有机相。用无水Na2SO4干燥溶液并使产物在真空中干燥整夜。测量的C,54.05;H,8.85;N,10.76%。C41H80N7O10Br要求,C,54.01;H,8.78;N,10.76%。1H NMR(400MHz,CDCl3)δ1.26(d,3H),1.56(m,4H),1.91(s,6H),2.22-2.67(m,50H),2.76(m,8H),4.19(m,8H),5.04(m,1H)。13C NMR(100MHz,CDCl3)δ24.5,25.5,28.4,45.6,62.2,64.2,77.2,173.5。m/z(ES MS)912.5[M+H]+,934.5[M+Na]+,950.5[M+K]+。
1.1.6 G2-Bz-OH的合成
将丙烯酸苄酯(6.7966g,42mmol,6eq.)添加到包含IPA(12mL)的50mL圆形2颈圆底烧瓶中。在正向的N2吹扫下使烧瓶脱氧10分钟。逐滴添加溶解在IPA(12mL)中的双(3-氨基丙基)氨基)丙-2-醇(1.3221g,6.984mmol,1eq.),同时在正向的N2流下在冰浴中搅拌溶液。在0℃下搅拌最终的混合物另外的10分钟,使其温暖至室温并搅拌48小时。除去溶剂并使产物在真空中干燥整夜。
1.1.7 G2-Bz的合成
将G2-Bz(1.664g,1.86mmol,1eq.)、TEA(0.2639g,2.6mmol,1.4eq.)和DMAP(22.8mg,0.1866mmol,0.1eq.)添加到包含DCM(110mL)的250mL的2颈圆底烧瓶中。在正向的N2吹扫下使烧瓶脱氧10分钟。逐滴添加α-溴代异丁酰溴(0.5354g,0.29mL,2.329mmol,1.25eq.),同时在正向的N2流下在冰浴中搅拌溶液。使得反应混合物温暖至室温并置于搅拌下整夜。用饱和的碳酸氢钠(NaHCO3)溶液(3x110mL)洗涤有机相。用无水Na2SO4干燥溶液并使产物在真空中干燥整夜。测量的C,63.40;H,6.96;N,4.18%。C53H68N3O10Br要求,C,64.44;H,6.89;N,4.26%。1H NMR(400MHz,CDCl3)δ1.22(d,3H),1.54(m,4H),1.90(s,6H),2.24-2.65(m,18H),2.77(m,8H),5.00(m,1H),5.09(s,8H),7.33(m,20H)。13C NMR(100MHz,CDCl3)δ18.1,30.6,32.3,44.1,48.8,51.7,52.7,66.7,76.7,128.6,135.8,144.1,172.3。m/z(ES MS)988.4[M+H]+。
1.2 pH响应支化物合成
1.2.1 1,4-丁二醇二(甲基丙烯酰氧基)-乙基醚(BDME)的合成
将1,4-丁二醇二乙烯基醚(BDVE)(5.6ml,35.21mmol)添加到配备有冷凝器、磁搅拌器和正向的氮气流的两颈250mL圆底烧瓶中。添加少量的自由基抑制剂4-叔丁基儿茶酚(刮刀末端)并使用氮气吹扫使混合物脱氧15分钟。一旦溶解,将温度升高至70℃。在10分钟内通过隔片逐滴添加甲基丙烯酸(MAA)(14.9ml,175.8mmol)。用搅拌使反应在70℃下进行另外的6小时。该时间之后,通过冷却和暴露于空气停止反应。将粗产物溶解在氯仿(100mL)中并用碱性H2O(~pH12,3x 100ml)洗涤。收集组合的洗涤物并在NaSO4上干燥,并通过旋转蒸发除去溶剂。
(测量:的C 61.45;H 8.28%。C16H26O6要求C 61.15;H 8.28%);1H NMR(400MHz;CDCl3;Me4Si)δ1.44(6H,d,CH3CH),1.65(4H,m,CH2CH2CH2),1.95(6H,s,CH3C=CH2),3.50-3.69(4H,m,OCH2CH2),5.60和6.15(4H,2s,CH2=CCH3)和5.95-5.99(2H,q,CHCH3)。13C NMR(400MHz;CDCl3;Me4Si)δ18.27(s),20.83(s),26.29(s)68.85(s),96.93(s),125.90(s),136.37(s)和167.01(s)。m/z(EI)314.2(M+-C16H26O6要求314)。
1.3 HPMA的聚合
1.3.1 HPMA50的聚合
在一般的合成中,目标数均聚合度(DPn)=50单体单元P(HPMA)50;nHPMA/N引发剂:50),将bpy(173.3mg,1.1096mmol,2eq.)、HPMA(4g,27.7mmol,50eq.)和甲醇(MeOH))(基于HPM,56%v/v)置于25mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(54.9mg,0.5548mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将G2-M(0.5054g,0.5548mmol,1eq.)添加到烧瓶中,并在30℃下使溶液聚合。当如由1H NMR(参见图8)判断的达到>99%转化率时,通过暴露于氧和添加THF终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去THF以浓缩样品,之后沉淀至己烷中并在真空烘箱中干燥整夜。
1.3.2 HPMA50-EGDMAx的聚合
在一般的合成中,目标数均聚合度(DPn)=50单体单元P(HPMA)50;nHPMA/n引发剂:50),将bpy(173.3mg,1.1096mmol,2eq.)、HPMA(4g,27.7mmol,50eq.)、EGDMA(99.0mg,0.4993mmol,0.9eq)和甲醇(MeOH))(基于HPMA,38.9%v/v)置于25mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(54.9mg,0.5548mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将EBIB(0.1082g,0.5548mmol,1eq.)添加到烧瓶中,并使溶液在30℃下聚合。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加THF终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在沉淀到己烷中之前,在真空下除去THF以浓缩样品。
1.4 DEAEMA的聚合
1.4.1 DEAEMA50的聚合
在一般的合成中,目标DPn=50单体单元PDEAEMA50;nDEAEMA/n引发剂:50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(4g,21.59mmol,50eq.)和IPA(基于DEAEMA,56%v/v)置于25mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将G2-M(0.3934g,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。
1.4.2 DEAEMA50-EGDMAx的聚合
在一般的合成中,目标DPn)=50单体单元PDEAEMA50;nDEAEMA/n引发剂:50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(4g,21.59mmol,50eq.)、EGDMA(77.0mg,0.3886mmol,0.9eq)和IPA(基于DEAEMA,38.9%v/v)置于25mL的圆底烧瓶中。搅拌溶液并使用N2吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将EBIB(84.2mg,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。聚合条件和流程与对以上直链聚合物所描述的那些相同。
1.4.3 DEAEMA50-BDME2.0的聚合
在一般的合成中,目标DPn)=50单体单元PDEAEMA50;nDEAEMA/n引发剂:50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(4g,21.59mmol,50eq.)、BDME(291.2mg,0.8637mmol,0.9eq)和IPA(基于DEAEMA,38.9%)置于25mL的圆底烧瓶中。搅拌溶液并使用N2吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将EBIB(84.2mg,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。聚合条件和流程与对以上直链聚合物所描述的那些相同。
1.5 tBuMA的聚合
1.5.1 tBuMA50的聚合
在一般的合成中,目标数均聚合度(DPn)=50单体单元(tBuMA50);ntBuMA/n引发剂:50),将bpy(175.7mg,1.125mmol,2eq.)、tBuMA(4g,28.129mmol,50eq.)和含水异丙醇(IPA/H2O)(92.5/7.5%)(基于tBuMA,50.4%v/v)置于50mL圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(55.7mg,0.5626mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将G2-M(0.3934g,0.5626mmol,1eq.)添加到烧瓶中,并在20℃下使溶液聚合,且从反应混合物中定期取出样品用于1H NMR分析。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加THF终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去THF以浓缩样品,之后沉淀至己烷中并在真空烘箱中干燥整夜。
1.5.2 tBuMA50-EGDMA0.95的聚合
在一般的合成中,目标数均聚合度(DPn)=50单体单元(tBuMA50);ntBuMA/n引发剂:50),将bpy(175.7mg,1.125mmol,2eq.)、tBuMA(4g,28.13mmol,50eq.)、EGDMA(105.9mg,0.5345mmol)和含水异丙醇(IPA/H2O)(92.5/7.5%)(基于tBuMA,38.4%v/v)放置到50mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(55.7mg,0.5626mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将EBIB(0.1097g,0.5626mmol,1eq.)添加到烧瓶中,并在20℃下使溶液聚合,并从反应混合物中定期取出样品用于1H NMR分析。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加THF终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去THF以浓缩样品,之后沉淀至己烷中并在真空烘箱中干燥整夜。
1.6 DEAEMA-tBuMA的聚合
1.6.1 G2-DEAEMAx-stat-tBuMAy的聚合
在一般的合成中,目标DPn=50单体单元PDEAEMA25-tBuMA25;nDEAEMA/n引发剂:50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(2g,10.80mmol,25eq.)、tBuMA(1.5352,10.80mmol,25eq.)和IPA/H2O(92.5/7.5%)(基于DEAEMA/tBuMA,30.6%v/v)置于50mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将G2-M(0.3934g,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。
1.6.2 EBIB-DEAEMAx-stat-tBuMAy-EGDMA0.9的聚合
在一般的合成中,目标DPn=50单体单元PDEAEMA25-tBuMA25;nDEAEMA/n引发剂::50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(2g,10.80mmol,25eq.)、tBuMA(1.5352,10.80mmol,25eq.)、EGDMA(77mg,0.9mmol,0.9eq.)和IPA/H2O(92.5/7.5%)(基于DEAEMA/tBuMA,30.6%v/v)置于50mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将EBIB(84.2mg,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。
1.6.3 G2-DEAEMAx-嵌段-tBuMAy的聚合
在一般的合成中,目标DPn=50单体单元PDEAEMA25-tBuMA25;nDEAEMA/n引发剂:50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(4g,21.59mmol,50eq.)和IPA(基于DEAEMA,38.9%v/v)置于50mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将G2-M(0.3934mg,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。使反应达到80-90%转化率,之后将溶解在H2O/IPA(92.5/7.5%)(基于tBuMA,27.3%v/v)中的tBuMA(1.5352,10.80mmol,25eq.)、bpy(134.9mg,0.8637mmol,2eq.)和Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到反应混合物中并使其聚合整夜。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。
1.6.4 EBIB-DEAEMAx-嵌段-tBuMAy-EGDMA0.9的聚合
在一般的合成中,目标DPn=50单体单元PDEAEMA25-tBuMA25;nDEAEMA/n引发剂:50),将bpy(134.9mg,0.8637mmol,2eq.)、DEAEMA(4g,21.59mmol,50eq.)和IPA(基于DEAEMA,38.9%v/v)置于50mL的圆底烧瓶中。搅拌溶液并使用氮气(N2)吹扫脱氧15分钟。将Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到烧瓶中并置于吹扫另外的5分钟。在正向的N2流下将EBIB(84.2mg,0.4318mmol,1eq.)添加到烧瓶中,并在40℃下使溶液聚合。使反应达到80-90%转化率,之后将溶解在H2O/IPA(92.5/7.5%)(基于tBuMA,27.3%v/v)中的tBuMA(1.5352,10.80mmol,25eq.)、bpy(134.9mg,0.8637mmol,2eq.)、EGDMA(77mg,0.9mmol,0.9eq.)和Cu(I)Cl(42.8mg,0.4318mmol,1eq.)添加到反应混合物中并使其聚合整夜。当如由1H NMR判断达到>99%的转化率时,通过暴露于氧气和添加丙酮终止反应。通过使混合物通过碱性氧化铝柱除去催化剂残留。在真空下除去丙酮以浓缩样品,之后沉淀至冷的石油醚(40℃-60℃)并在真空烘箱中干燥整夜。
2.通过ROP的聚合
2.1 ROP树枝状分子引发剂合成
2.1.1 G1-pOH的合成
将2-(二甲基氨基)乙基丙烯酸酯(6.0g,42mmol,6eq.)添加到包含IPA(12mL)的50mL圆形2颈圆底烧瓶中。在正向的N2吹扫下使烧瓶脱氧10分钟。逐滴添加溶解在IPA(12mL)中的乙醇胺(0.4266g,6.9843mmol,1eq.),同时在正向的N2流下在冰浴中搅拌溶液。在0℃下搅拌最终的混合物另外的10分钟,之后使其温暖至室温并搅拌48小时。除去溶剂并使产物真空中干燥整夜。
2.1.2 G2-pOH的合成
将CDI(39.137g,0.241mol)添加到配备有回流冷凝器、磁搅拌器和干燥N2入口的500mL的2颈RBF中。添加干燥甲苯(350mL)并用N2吹扫烧瓶10分钟。在60℃下搅拌溶液,并通过温热的注射器添加叔丁醇(35.7g,46mL,0.483mol)(注意:叔丁醇是低熔点固体,因此在35℃的水浴中加热它以使其熔融为液体以容易地通过注射器从瓶中将其取出)。在正向的氮气流下在60℃下将混合物置于搅拌6小时。之后,逐滴添加BAPA(16.077g,17.14mL,0.121mol),同时搅拌并保持在60℃的温度。添加时,白色固体沉淀开始在烧瓶中形成(咪唑)。在正向的氮气流下在60℃下将反应置于搅拌另外的18小时,然后使其冷却至室温。过滤浅黄色的溶液以除去任何固体咪唑,并在真空中浓缩。将剩余的油溶解在二氯甲烷(250mL)中,用蒸馏水(3x250mL)且最终用饱和盐水溶液(150mL)洗涤。用无水Na2SO4干燥有机层,过滤并在真空中浓缩以给出作为白色固体粉末的G1-BAPA。物除去任何残余的剩余溶剂,将化合物置于高真空下整夜。(38g,95%)测量的C,57.84;H,10.45;N,12.91%。C16H33N3O4要求,C,57.98;H,10.04;N,12.68%。1H NMR(400MHz,CDCl3)5.19(s,br,NH–添加D2O时消失),3.21(t,4H),2.65(t,4H),1.65(q,4H),1.44(s,18H)13C NMR(100MHz,CDCl3)156.48,79.34,47.77,39.29,30.11,28.79。m/z(ES MS)332.3[M+H]+
将1,4-二噁烷(200mL)中的G1-BAPA(20g,0.06mol)16mmol)、溴乙醇(7.54g,0.6mol)、30mg的碘化钠和碳酸钾(25.0g,1.8mol)的混合物回流整夜。在浓缩反应混合物之后,将其用乙酸乙酯(200mL)萃取,用水(100mL)洗涤,在硫酸钠上干燥,并且过滤,并在降低的压力下除去溶剂。通过快速层析(2:1,乙酸乙酯-己烷)纯化粗产物产生G1-OH。
在1L RBF中,将G1-OH(33.70g)溶解在乙酸乙酯(330mL)中并非常缓慢地添加浓HCl(35.03g,30mL,d=1.1836%活性)。CO2开始释出。保持反应容器打开并搅拌6小时。然后在真空中除去乙酸乙酯,并进行剩余油的粗1H NMR(D2O)。粗1H NMR示出不完全的脱羧的标志(参见第7页的质谱),所以将油再溶解在250mL乙酸乙酯中并加热至55℃持续5小时。除去乙酸乙酯之后,将粗油溶解在4M NaOH(300mL)中,然后在旋转蒸发器(60℃)上浓缩至一半(约)。随后,用CHCl3(300mL)萃取油混合物两次。然后组合有机层,用无水Na2SO4干燥,过滤并在真空中浓缩以给出作为浅黄色油的双(3-氨基丙基)氨基)丙醇。
将2-(二甲基胺基)乙基丙烯酸酯(6.0g,42mmol,6eq.)添加到包含IPA(12mL)的50mL圆形2颈圆底烧瓶中。在正向的N2吹扫下使烧瓶脱氧10分钟。逐滴添加溶解在IPA(12mL)中的双(3-氨基丙基)氨基)丙醇(1.2271g,6.984mmol,1eq.),同时在正向的N2流下在冰浴中搅拌溶液。在0℃下搅拌最终的混合物另外的10分钟,使其温暖至室温并搅拌48小时。除去溶剂并使产物在真空中干燥整夜。
2.2二官能己内酯的合成
2.2.24,4’-二环氧己烷基-7,7’-二酮(BOD)的合成
将过氧化脲(CO(NH2).H2O2)(20g,0.21mol)添加到包含甲酸(100mL)的500mL圆底烧瓶中。在室温下搅拌溶液2h。然后将烧瓶浸入冰浴中以控制由该流程的以下阶段导致的放热。在5-10min期间将双环己酮(10g,0.05mol)缓慢添加到溶液中。搅拌反应混合物4h,同时定期更换冰浴。然后将200mL水添加到混合物中,随后用氯仿萃取(200mL x 4)。收集有机馏份,并用饱和的碳酸氢钠水溶液洗涤,然后用Na2SO4干燥整夜。在降低的压力下除去溶剂之后,分离白色粉末并通过NMR分析,并与文献报告的值比较。
2.3通过ROP的聚合
2.3.1 ε-己内酯的开环聚合
对于目标数均聚合程DP=50的CL的均聚的一般流程如下。用氮气吹扫50mL单颈圆底烧瓶15分钟。通过注射器和针头添加SnOct2催化剂(0.0018g,0.0044mmol)并进一步吹扫烧瓶。将蒸馏的CL(3.773g,3.5mL,33.06mmol)引入到50mL烧瓶中,并吹扫烧瓶另外的10分钟。经由注射器添加无水G1pOH(0.2316g,0.6666mmol)。然后将烧瓶浸入预热的110℃下的油浴中,并强力搅拌~20小时的要求反应时间。通过将反应浸入冰浴终止反应,并通过溶解在THF中纯化聚合物并将其沉淀到己烷中。
2.3.2 ε-己内酯和4,4’-bioxepanyl-7,7’-二酮(PCL-BOD)的开环聚合
对于目标数均聚合度DP=50的CL的均聚的一般流程如下。用氮气吹扫包含BOD(0.9183g,4.059mmol)的50mL单颈圆底烧瓶15分钟。通过注射器和针头添加SnOct2催化剂(0.0079g,0.0195mmol)并进一步吹扫烧瓶。将蒸馏的CL(23.28g,21.6mL,204mmol)引入到50mL烧瓶中,并吹扫烧瓶另外的10分钟。经由注射器添加无水BzOH(0.7315g,0.7mL,6.764mmol)。然后将烧瓶浸入预热的110℃下的油浴中,并强力搅拌~20小时的要求反应时间。通过将反应浸入冰浴终止反应,并通过溶解在THF中纯化聚合物并将其沉淀到己烷中。
体外细胞存活率实验
研究了根据本发明的携带SN38的纳米颗粒对小鼠CT-26细胞的存活率的影响。发现虽然SN38是降低细胞存活率的原因,纳米颗粒载体本身对细胞存活率没有影响。
使用了以下聚合物组合物(支化聚合物和嵌段共聚物的混合物):
JF1:p(HPMA50-共-EGDMA0.9):p(PEG114-嵌段-HPMA120)50:50wt%
JF2:p(nBuMA50-共-EGDMA0.8):p(PEG114-嵌段-HPMA120)50:50wt%
JF3:p(tBuMA25-共-HPMA25-共-EGDMA0.9):p(PEG114-嵌段-HPMA120)50:50wt%
遵循以下流程。
纳米颗粒样品-SN-38的5wt%包封
1.将30uL样品(JF1-3)添加到970uL培养基中(最终浓度是4uM)
2.将15uL样品(JF1-3)添加到970uL培养基和15uL水中(最终浓度是2uM)
3.将7.5uL样品(JF1-3)添加到970uL培养基和22.5uL水中(最终浓度是1uM)
对于DMSO中的SN38
1.制备2.5mM的储备SN38溶液(在2000uL DMSO中2mg)
2.将1.6uL的储液添加到968.4uL培养基中,然后添加30uL无菌水(最终浓度是4uM)
3.将2uL储液添加到2ul的DMSO中(1:2连续稀释),将其1.6uL添加到968.4uL培养基和30uL无菌水中(最终浓度是2uM)
4.将2uL先前的中间储液添加至2ul的DMSO中(1:2系列稀释),将其1.6uL添加到968.4uL培养基和30uL无菌水中(最终浓度是1uM)
对于对照
1.添加1.6uL的DMSO到968.4uL培养基,然后添加30uL无菌水
2.将30uL无菌水添加到970uL培养基中
对于空白
1.将30uL样品(B1-3)添加到970uL培养基中(最终浓度是4uM)
2.将15uL样品(B1-3)添加到970uL培养基和15uL水中(最终浓度是2uM)
3.将7.5uL样品(B1-3)添加到970uL培养基和22.5uL水中(最终浓度是1uM)
将培养基抽吸到96孔板上并用100uL的每种溶液(一式三份)给药,随后用96孔板读数器检测,吸光度490nm。
如图20所示,在48小时温育周期之后,5wt%SN38包封的纳米颗粒样品和SN38在DMSO/水中的样品导致细胞存活率降低(相比对照的100%,约25%至45%)。相反,空白样品(即包含纳米颗粒的聚合物成分而不包含SN38的那些)导致在允许误差内的100%细胞存活率。
- 还没有人留言评论。精彩留言会获得点赞!