一种含吡嗪环链接的苯丙酸类化合物、其药物组合物、制备方法和用途与流程
本发明涉及一种新型gpr40激动剂。具体地说,涉及一种含吡嗪环的苯丙酸类化合物、其药物学上可接受的盐、立体异构体或其前药分子;其药物组合物;制备方法;以及在制备治疗糖尿病及糖脂代谢紊乱的药物中的用途,尤其是在制备治疗ⅱ型糖尿病的药物的用途。
背景技术:
众所周知,糖尿病是继肿瘤、心脑血管疾病后第三位严重威胁人类健康的慢性病,糖尿病死亡率大于艾滋病、结核病和疟疾死亡率的总和,大约每6秒就有1个糖尿病患者死亡。2015年全球有4.15亿糖尿病成年患者,3.18亿人存在患糖尿病的风险,预计至2040年每十个人中将有一人患糖尿病,中国糖尿病患者的人数居于全球首位,高达1.14亿,并且每年还以350万至400万人的幅度递增。鉴于目前严峻的形势,开发新型治疗糖尿病的药物是非常有必要的。
糖尿病按照病因、临床表现和并发症的不同分为ⅰ型和ⅱ型糖尿病。ⅰ型糖尿病的特征是缺乏胰岛素分泌能力,称为胰岛素依赖型糖尿病(iddm),ⅱ型糖尿病则是由于自身无法有效利用胰岛素造成,称为非胰岛素依赖型糖尿病(niddm)。ⅱ型糖尿病患者占全球糖尿病总数的90%以上。ⅱ型糖尿病的糖尿病的发病机制复杂,其基本特征是骨骼肌、肝脏、脂肪等组织对胰岛素产生抵抗。病程早期患者胰岛β细胞可代偿性分泌胰岛素以抵消胰岛素作用的缺陷,从而维持机体正常的血糖水平。然而,随着病程的发展,胰岛β细胞胰岛素分泌功能不足,患者的代偿机制崩溃,导致机体血糖水平异常升高,进而产生体内糖脂代谢紊乱发生ⅱ型糖尿病。胰岛素分泌不足和胰岛素抵抗是ii型糖尿病发病的两大重要因素,其中,葡萄糖刺激的胰岛素分泌功能(glucosestimulatedinsulinsecretion,gsis)失常是ii型糖尿病发生发展中至关重要的环节。研究表明,多个g蛋白耦联受体(gpcr)由于在gsis调节中发挥着重要作用而成为糖尿病新药研发的新靶标,其中,gpr40是最受关注的靶标之一。gpr40表达较广泛,在胰腺组织中尤为丰富,人、小鼠和大鼠等多个种属的胰岛β细胞中均检测到gpr40高表达,最新研究发现,gpr40在两种重要的肠道内分泌细胞k细胞和l细胞中也有表达。gpr40的天然配体为中长链脂肪酸,包括10-23个碳的饱和脂肪酸、部分中长链单不饱和脂肪酸、多不饱和脂肪酸如棕榈油酸、亚油酸、二十碳三烯酸等。激活胰岛β细胞中gpr40可促进葡萄糖依赖的胰岛素分泌,而激活肠道l细胞中gpr40则可促进胰高血糖素样肽1(glucagon-likepeptide-1,glp-1)的分泌,进而发挥促胰岛素分泌、抑制胰高血糖素分泌、保护胰岛β细胞、抑制β细胞凋亡、抑制食欲、减缓胃排空和降低体重等多种糖尿病相关治疗作用。因此,gpr40激动剂具有促进胰岛素分泌和glp-1分泌的双重功效,这种不同于现有药物的全新作用机制使其成为全球抗糖尿病新药研发的新兴靶点。
gpr40激动剂作为新型的糖尿病靶点治疗药物还处于开发初期,目前公开的gpr40激动剂的现有技术包括例如cn104109115a等。
技术实现要素:
本发明在已申请专利cn104109115a基础上,提供具有下面通式i所示结构的化合物,其与已报道化合物的结构明显不同。本发明的化合物具有显著的降血糖及调节糖脂代谢活性的功能,是一类新型gpr40激动剂。
本发明一方面提供如下通式i所示的含吡嗪环的苯丙酸类化合物、其药学上可接受的盐、立体异构体或其混合物(包括对映异构体、外消旋体或其混合物),或其前药,
其中:
ar选自芳基或杂芳基;
r1为ar上的单取代基或多取代基,其独立地选自:h;羟基、卤素;羧基;硝基;任选被取代的c1-c20烷基;任选被取代的c1-c20烷氧基;任选被取代的c3-c10环烷基;任选被取代的c3-c10环烷基氧基;任选被取代的c6-c20芳基;任选被取代的c3-c10芳氧基;含有选自s、o和n中的1至3个杂原子的任选被取代的3至10元杂环基;含有选自s、o和n中的1至3个杂原子的任选被取代的3至10元杂环基氧基;含有选自s、o和n中的1至3个杂原子的任选被取代的3至20元杂芳基;-n(ra)so2rb;-nrarb;-n(ra)c(o)rb;-c(o)nrarb;-so2ra;-srb;
r2a、r2b、r2c、r2d、r3a和r3b各自独立选自:h、羟基、卤素、任选被取代的c1-c20烷基、任选被取代的c1-c20烷氧基;
r4、r5、r6各自独立选自:h、羟基、卤素、任选被取代的c1-c20烷基、任选被取代的c1-c20烷氧基、任选被取代的c3-c10环烷基、任选被取代的c3-c10环烷氧基;
ra和rb各自独立选自:h、任选被取代的c1-c6烷基、任选被取代的c3-c8环烷基;任选被取代的含有选自o、s和n中1~3个杂原子的3-8元杂环基。
在本发明中,若无另外说明,相关术语含义如下。
术语“卤素”包括氟、氯、溴和碘。术语“卤代”指的是用单个或多个卤素原子取代。
术语“芳基”是指稠合或非稠合的含c6-c20的芳香不饱和碳环,例如,c6-c10芳基,更具体地可以列举例如苯基、萘基等;
术语“芳氧基”中的芳基含义同上。
术语“杂芳基”是指不饱和碳环含n、o和s中的1至3个杂原子,具有芳香性的3至20元杂环,例如5至10元杂芳基,具体可以列举吡啶基、噻吩基、噁唑基、咪唑基等。
术语“c1-c20烷基”是指具有1至20个碳原子的直链或支链烷基,术语“c1-c10烷基”、“c1-c6烷基”和“c1-c4烷基”具有类似的含义。非限制性地包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、戊基、已基、辛基、癸基、十一烷基、十二烷基、十四烷基、十六烷基、十七烷基、十八烷基、二十烷基等。
术语“c1-c20烷氧基”中的c1-c20烷基含义同上。
术语“c3-c10环烷基”是指在环上具有3至10个碳原子的环状烷基,术语“c3-c8环烷基”和“c3-c6环烷基”具有类似的含义。非限制性地包括环丙基、环丁基、环戊基、环己基和环庚基等。
术语“c3-c10环烷基氧基”中的“c3-c10环烷基”含义同上。
术语“3-10元杂环基”是指环上具有3-10个原子的含有选自n、o和s原子中至少一个原子的非芳香族环基,术语“3-8元杂环基”、“5-8元杂环基”和“3-6元杂环基”具有类似的含义。如环氧基、吡咯烷基、吗啉基等。
术语“任选被取代的”是指未被取代的,或者被取代基所取代;所述取代基可以为例如选自羟基、卤素、羧基、硝基、c1-c10烷基、c3-c10环烷基、氧代基团等。
其中,当r1为c1-c20烷基时,该c1-c20烷基还可以被-src、-so2rc或-nrcrd取代;
当r1为c1-c20烷氧基时,该c1-c20烷氧基还可以被选自-src、-so2rc、-nrcrd、未取代或被c1-c6烷基、羟基或氧代基团取代的含有选自o、s和n中1~3个杂原子的3-8元杂环基中的取代基取代;
其中,rc和rd各自独立地选自:h、c1-c6烷基、未取代或者被c1-c3烷基取代的含有选自o、s和n中1~3个杂原子的3-8元杂环基。
本发明中的术语“药学上可接受的盐”是指本发明的通式i所示的化合物与选自磷酸、硫酸、盐酸等无机酸,醋酸、酒石酸、柠檬酸、苹果酸、富马酸等有机酸,或天冬氨酸、谷氨酸等酸性氨基酸中的酸所形成的盐,或与上述酸成酯或酰胺后再与无机碱形成的盐,如钠、钾、钙、铝盐和铵盐。
上述通式i所示的化合物中:
可选地,ar选自苯基、吡啶基、噻吩基、噁唑基、咪唑基;
可选地,r1选自:h;羟基;卤素;羧基;硝基;c1-c6烷基;卤代c1-c6烷基;c1-c6烷氧基;卤代c1-c6烷氧基;c3-c8环烷基;c3-c8环烷基氧基;含有至少一个氮原子的3至10元杂环基;未取代或者被c1-c6烷基或氧代基团取代的含有选自o、s和n中1~3个杂原子的3-8元杂环基氧;-n(ra)so2rb;-nrarb;-n(ra)c(o)rb;-c(o)nrarb;-so2ra;-srb;被选自c1-c4烷氧基、c3-c8环烷基、-src、-so2rc、-nrcrd、未取代或者被c1-c4烷基、羟基或氧代基团取代的含有选自o、s和n中1~3个杂原子的3-6元杂环基中的取代基取代的c1-c6烷氧基;或者被c1-c4烷氧基、c3-c8环烷基、-src、-so2rc或-nrcrd取代的c1-c6烷基;其中,ra、rb、rc和rd如上所述定义。
可选地,r1选自:h;羟基;卤素;羧基;硝基;c1-c4烷基;卤代c1-c4烷基;c1-c4烷氧基;卤代c1-c4烷氧基;c3-c8环烷基;c3-c8环烷基氧基;氮杂环丙烷-1-基;未取代或者被c1-c3烷基或氧代基团取代的含有选自o、s和n中1~3个杂原子的3-6元杂环基;-n(ra)so2rb;-nrarb;-n(ra)c(o)rb;-c(o)nrarb;-so2ra;-srb;被选自c1-c4烷氧基、c3-c6环烷基、-src、-so2rc、-nrcrd、未取代或被c1-c4烷基、羟基或氧代基团取代的含有选自o、s和n中1~3个杂原子的3-6元杂环基中的取代基取代的c1-c4烷氧基;和被c1-c4烷氧基、c3-c6环烷基、-src、so2rc或nrcrd取代的c1-c4烷基;
可选地,r2a、r2b、r2c和r2d选自h、卤素;可选地,r2a为氢或卤素,r2b、r2c和r2d为h;
可选地,r3a、r3b选自h、c1-c4烷基;可选地,r3a为氢或甲基,r3b为氢;
可选地,r4、r5和r6为h;
可选地,ra和rb各自独立选自h、c1-c4烷基、c3-c6环烷基、未取代或者被c1-c3烷基或氧代基团取代的含有选自o、s和n中的1~3个杂原子的3-6元杂环基;
rc和rd各自独立地选自h、c1-c3烷基、未取代或者被c1-c3烷基取代的含有选自o、s和n中1~3个杂原子的3-6元杂环基。
可选地,所述通式(i)所示的化合物,是如下式(ii)所示结构的化合物,
其中:
ar和r1如上文所述定义。
r2选自h、羟基、卤素、c1-c20烷基和卤代c1-c20烷基;可选地为h或卤素。
r3选自h、c1-c20烷基和卤代c1-c20烷基;可选地为h或甲基。
可选地,所述通式(i)所示的化合物,选自如下式所示的化合物yhhu-001~yhhu-019:
本发明另一方面提供通式i所示的含吡嗪环的苯丙酸类化合物的制备方法,其特征在于包括由化合物7与下式化合物经过suzuki反应偶联得到化合物8的步骤,
其中,ar、r1、r2a、r2b、r2c、r2d、r3a、r3b、r4、r5和r6如上所述定义,x为卤素,r7为羟基保护基团,r7选自烷基、取代烷基、烷基硅基、烷基硫基等,例如为c1-c6烷基。
可选地,上述的制备方法中,还包括由化合物8经过水解反应除去羟基保护基团得到式(i)化合物的步骤。
可选地,上述的制备方法中,还包括由化合物5和化合物6经亲核取代反应得到化合物7的步骤,
其中,r2a、r2b、r2c、r2d、r3a、r3b、r4、r5、r6和r7如上所述定义,x、y各自独立选自卤素。
本发明另一方面还提供用于制备上述通式(i)所示的含吡嗪环的苯丙酸类化合物的中间体,其为下式的化合物:
其中,ar、r1、r2a、r2b、r2c、r2d、r3a、r3b、r4、r5、r6和r7如上所述定义,x为卤素。
作为通式i所示的苯丙酸类化合物的制备方法的一个具体实施方式,如下反应式1所示:
其中,ar、r1、r2、r3如上所述定义。
可选地,反应式1所示的方法,包含如下步骤中一个或多个步骤:
步骤1:将r2取代的对溴苄醇1和丙烯酸乙酯2经过heck反应得到中间体3,将双键还原得到中间体4,再经过溴化反应把苄醇变成苄溴得到中间体5;所述heck反应可以在例如醋酸钯、四(三苯基膦)钯或二(三苯基膦)二氯化钯等钯金属催化剂存在下,在例如n,n-二甲基甲酰胺或三乙胺等溶剂中进行;所述双键还原反应可以在例如钯碳复合物催化剂存在下,在例如乙酸乙酯、乙酸丁酯、甲醇、乙醇或正丙醇等溶剂中,使用例如氢气作为还原剂进行;所述溴化反应可以使用例如三溴化磷,五溴化磷,三溴氧磷或二溴亚砜等溴化剂,在例如乙腈、二氯甲烷或乙醚等溶剂中进行;
步骤2:将中间体5和底物6经过亲核取代反应得到中间体7;所述亲核取代反应可以在例如碳酸钾、碳酸铯、氢化钠、氢化钾、叔丁醇钾、叔丁醇钠或氢氧化钠等碱存在下,在例如乙腈、n,n-二甲基甲酰胺或四氢呋喃的溶剂中进行;
步骤3:中间体7和
所述suzuki反应可以在例如四(三苯基膦)钯、二(三苯基膦)二氯化钯、醋酸钯或钯碳复合物等催化剂存在下,在例如甲苯/乙腈/水的混合溶剂、甲苯/乙醇/水的混合溶剂、乙腈/水的混合溶剂或乙醇/水的混合溶剂中进行;以及所述中间8的水解反应可以在例如氢氧化钾、氢氧化钠或氢氧化锂等碱的存在下,在例如乙腈/水混合溶剂、甲醇/水混合溶剂或乙醇/水混合溶剂的溶剂中进行;
在上述步骤1~步骤3中,各个步骤的反应均在本领域普通技术人员公知的反应条件下进行。
本发明的又一方面提供一种药物组合物,该药物组合物包含治疗有效量的选自上述通式i所示的含吡嗪环的苯丙酸类化合物、其立体异构体或其混合物(包括其对映异构体、外消旋体及其混合物)、其药学上可接受的盐及其前药中一种或多种,以及任选的药学上可接受的辅料。所述药物组合物可以用于治疗糖尿病或糖脂代谢紊乱。
本发明的又一方面提供选自上述通式i所示的含吡嗪环的苯丙酸类化合物、其立体异构体或其混合物(包括其对映异构体、外消旋体及其混合物)、其药学上可接受的盐及其前药中一种或多种在制备用作gpr40激动剂的药物中的应用;可选地,所述的药物用于降血糖或调节糖脂代谢;可选地,所述的药物用于治疗糖尿病或糖脂代谢紊乱;特别是,所述药物用于治疗ⅱ型糖尿病。
本发明的又一个方面,提供一种治疗糖尿病或糖脂代谢紊乱的方法,其包括向具有该需要的患者施用治疗有效量的选自上述通式(i)所示的含吡嗪环的苯丙酸类化合物、其立体异构体或其混合物(包括其对映异构体、外消旋体及其混合物)、其药学上可接受的盐及其前药中一种或多种,或者上述药物组合物。
上述通式(i)所示的化合物,是一类新型gpr40激动剂,具有显著的降血糖及调节糖脂代谢活性的功能。
附图说明
图1:化合物yhhu-007及溶剂对照的血糖浓度-时间曲线
图2:化合物yhhu-007及溶剂对照的血糖曲线下面积
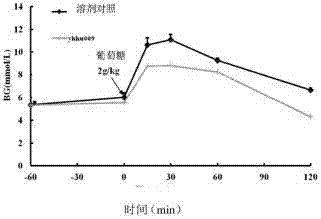
图3:化合物yhhu-009及溶剂对照的血糖浓度-时间曲线
图4:化合物yhhu-009及溶剂对照的血糖曲线下面积。
图5:化合物yhhu-010及溶剂对照的血糖浓度-时间曲线
图6:化合物yhhu-010及溶剂对照的血糖曲线下面积
图7:化合物yhhu-007大鼠血药浓度-时间曲线
图8:化合物yhhu-009大鼠血药浓度-时间曲线
图9:化合物yhhu-010大鼠血药浓度-时间曲线
具体实施方式
以下通过实施例进一步说明本发明,但所述实施例并不限制本发明的范围。
核磁共振氢谱用brukeramx-400型核磁共振仪记录,化学位移δ的单位为ppm。所用微波为cem-discovery微波反应器。所有反应溶剂均按照常规方法进行纯化。柱层析用硅胶(200-300目)为青岛海洋化工分厂生产。薄层层析使用gf254高效板,为烟台化工研究所生产。制备型薄层层析板由自己制备,固定相采用gf254(hg/t2354-92)硅胶和羧甲基纤维素钠(800-1200)制备,分别为青岛海洋化工有限公司和中国医药(集团)上海化学试剂公司生产。所有溶剂均为分析纯试剂,所用试剂均购自国药集团化学试剂有限公司。采用碘、紫外荧光等方法显色。减压蒸除有机溶剂在旋转蒸发仪中进行。
实施例1:3-(4-溴甲基-2-氟苯基)丙酸乙酯的制备
称取2-氟-4-溴苯甲醇1(购自韶远化学科技(上海)有限公司,11.48g,56.0mmol,)溶于100ml三乙胺中,加入20.0ml丙烯酸乙酯2,醋酸钯(0.50g,2.2mmol),三苯基膦(0.50g,1.9mmol)。反应体系用氮气置换三次,然后置于油浴中95℃反应72小时,反应液冷却至室温,过滤,滤液浓缩后,硅胶柱层析(石油醚/乙酸乙酯=4/1(v/v))分离得到白色固体311.3g,产率93%。1hnmr(400mhz,cdcl3)δ7.76(d,j=16.2hz,1h),7.50(t,j=7.7hz,1h),7.13(d,j=10.5hz,2h),6.50(d,j=16.2hz,1h),4.71(s,2h),4.26(q,j=7.1hz,2h),1.33(t,j=7.1hz,3h)。
将11.3g中间体3溶解于100ml乙酸乙酯中,加入10%钯碳200mg,氢气置换三次后,室温下反应4小时,反应液垫硅藻土过滤,滤液浓缩后硅胶柱层析分离(乙酸乙酯/石油醚=1/8),得白色固体410.7g,产率93%。1hnmr(400mhz,cdcl3)δ7.19(t,j=7.8hz,1h),7.07–7.02(m,2h),4.65(d,j=5.9hz,2h),4.12(q,j=7.1hz,2h),2.96(t,j=7.7hz,2h),2.61(dd,j=9.1,6.3hz,2h),1.23(t,j=7.1hz,3h).将10.7g中间体4溶解于200ml无水乙醚中,冰水浴下滴加入20.0g三溴化磷,然后保温反应1小时,加入水洗涤,有机层用无水硫酸钠干燥,浓缩后硅胶柱层析分离(乙酸乙酯/石油醚=1/15),得白色固体512.9g,产率92%。1hnmr(300mhz,cdcl3)δ7.19(t,j=7.8hz,1h),7.11–7.03(m,2h),4.43(s,2h),4.12(q,j=7.1hz,2h),2.96(t,j=7.6hz,2h),2.61(t,j=7.7hz,2h),1.23(t,j=7.1hz,3h)。
实施例2:3-(4-(((6-氯吡嗪-2-基)氧)甲基-2-氟苯基)丙酸乙酯的制备
称取2.38g化合物6,3.90g化合物5,4.0g碳酸钾加入到100ml圆底烧瓶中,加入无水乙腈50ml,50℃反应5小时。将反应液降至室温,过滤,滤液浓缩硅胶柱层析分离(乙酸乙酯/石油醚=1/10),得3.44g白色固体化合物7,产率69%。1hnmr(400mhz,cdcl3)δ8.18(s,2h),7.23(d,j=7.5hz,1h),7.17–7.11(m,2h),5.34(s,2h),4.12(q,j=7.1hz,2h),2.98(t,j=7.7hz,2h),2.63(t,j=7.7hz,2h),1.23(t,j=7.1hz,3h)。
实施例3:3-(4-(((6-(2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-001)的制备
称取100.0mg化合物7,45.0mg2,6-二甲基苯硼酸,15.0mg四(三苯基膦)钯和75.0mg碳酸钾加入到10ml微波反应器专用管中,加入2.0ml甲苯,0.4ml乙醇和0.4ml水,用氮气置换3次,然后置于cem微波反应器中120℃反应30分钟,反应液浓缩后硅胶柱层析分离,得到3-(4-(((6-(2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸乙酯97.0mg,为无色油状物。1hnmr(400mhz,cdcl3)δ8.29(s,1h),8.14(d,j=4.8hz,1h),7.29-7.22(m,2h),7.16(dd,j=8.4,5.9hz,4h),5.37(s,2h),4.16(q,j=7.1hz,2h),3.00(t,j=7.7hz,2h),2.65(dd,j=9.1,6.3hz,2h),2.09(s,6h),1.26(t,j=7.1hz,3h)。将上述得到的油状物溶于5.0ml乙腈中,加入1.0ml水,加入氢氧化锂10.0mg,置于40℃油浴中反应12小时,tlc检测反应结束。用2m盐酸溶液调ph=2-3,加入水,用乙酸乙酯萃取3次,合并有机层用饱和食盐水洗涤,有机层用无水硫酸钠干燥,过滤浓缩得3-(4-(((6-(2,6-二甲基苯基)吡嗪-2-基)氧)甲基)-2-氟苯基)丙酸90mg,为白色固体。1hnmr(400mhz,cdcl3)δ8.26(s,1h),8.10(s,1h),7.25–7.18(m,2h),7.13(dd,j=8.3,4.1hz,4h),5.34(s,2h),2.98(t,j=7.6hz,2h),2.68(t,j=7.6hz,2h),2.05(s,6h)。
实施例4:3-(4-(((6-(2-甲基-4-氟苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-002)的制备
除了使用2-甲基-4-氟苯硼酸代替2,6-二甲基苯硼酸之外,以按照与实施例3类似的方法制得化合物3-(4-(((6-(2-甲基-4-氟苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.25(d,j=5.2hz,2h),7.43–7.35(m,1h),7.23(d,j=7.5hz,1h),7.16–7.09(m,2h),7.00(t,j=8.5hz,2h),5.37(s,2h),2.99(t,j=7.6hz,2h),2.69(t,j=7.6hz,2h),2.36(s,3h)。
实施例5:3-(4-(((6-(2,4,6-三甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-003)的制备
除了使用2,4,6-三甲基苯硼酸苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(4-(((6-(2,4,6-三甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.24(s,1h),8.08(s,1h),7.21(t,j=7.6hz,1h),7.12(d,j=9.2hz,2h),6.96(s,2h),5.34(s,2h),2.98(t,j=7.6hz,2h),2.68(t,j=7.6hz,2h),2.34(s,3h),2.02(s,6h)。
实施例6:3-(4-(((6-(4-乙氧基-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-004)的制备
除了使用4-乙氧基-2,6-二甲基苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(4-(((6-(4-乙氧基-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.23(s,1h),8.08(s,1h),7.21(t,j=7.7hz,1h),7.12(d,j=9.0hz,2h),6.67(s,2h),5.33(s,2h),4.12(q,j=7.2hz,2h),2.97(t,j=7.5hz,2h),2.61(t,j=7.7hz,2h),2.04(s,6h),1.43(t,j=7.0hz,3h)。
实施例7:3-(2-氟-4-(((6-(4-(甲氧基甲氧基)-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)丙酸(化合物yhhu-005)的制备
除了使用4-甲氧基甲氧基-2,6-二甲基苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(2氟-4-(((6-(4-(甲氧基甲氧基)-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)丙酸。1hnmr(400mhz,cdcl3)δ8.24(s,1h),8.07(s,1h),7.22(t,j=7.6hz,1h),7.12(d,j=9.4hz,2h),6.82(s,2h),5.34(s,2h),5.20(s,2h),3.50(s,3h),2.98(t,j=7.6hz,2h),2.68(t,j=7.7hz,2h),2.03(s,6h)。
实施例8:3-(2-氟-4-(((6-(4-(2-甲氧基乙氧基)-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)苯基)丙酸(化合物yhhu-006)的制备
除了使用4-(2-甲氧基乙氧基)-2,6-二甲基苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(4-(2-甲氧基乙氧基)-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.23(s,1h),8.07(s,1h),7.20(t,j=7.5hz,1h),7.11(d,j=9.3hz,2h),6.71(s,2h),5.33(s,2h),4.14–4.09(m,2h),3.77(dd,j=5.5,4.0hz,2h),3.47(s,3h),2.97(t,j=7.7hz,2h),2.61(t,j=7.7hz,2h),2.03(s,6h)。
实施例9:3-(4-(((6-(2,6-二甲基-4-吗啉基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-007)的制备
除了使用4-吗啉基-2,6-二甲基苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3所示类似的方法制得化合物3-(4-(((6-(2,6-二甲基-4-吗啉基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.22(s,1h),8.08(s,1h),7.21(t,j=7.4hz,1h),7.12(d,j=9.4hz,2h),6.68(s,2h),5.34(s,2h),3.93–3.79(m,4h),3.27–3.15(m,4h),2.98(t,j=7.5hz,2h),2.68(t,j=7.6hz,2h),2.04(s,6h)。
实施例10:3-(4-(((6-(2,6-二甲基-4-((四氢-2h-吡喃-4-基)氧)苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-008)的制备
除了使用2,6-二甲基-4-(四氢-2h-吡喃-4-基)氧苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(4-(((6-(2,6-二甲基-4-((四氢-2h-吡喃-4-基)氧)苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.23(s,1h),8.08(s,1h),7.22(t,j=7.5hz,1h),7.12(d,j=9.3hz,2h),6.69(s,2h),5.34(s,2h),4.59–4.48(m,1h),4.06–3.94(m,2h),3.66–3.55(m,2h),2.98(t,j=7.8hz,2h),2.68(t,j=7.7hz,2h),2.03(s,8h),1.83(dt,j=8.6,6.2hz,2h)。
实施例11:3-(4-(((6-(4-(环己氧基)-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-009)的制备
除了使用2,6-二甲基-4-环己氧基苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(4-(((6-(4-(环己氧基)-2,6-二甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.23(s,1h),8.08(s,1h),7.22(t,j=7.6hz,1h),7.12(d,j=9.2hz,2h),6.67(s,2h),5.34(s,2h),4.33–4.22(m,1h),2.98(t,j=7.7hz,2h),2.68(t,j=7.7hz,2h),2.01(d,j=12.8hz,8h),1.87–1.77(m,2h),1.63–1.49(m,3h),1.46–1.29(m,3h)。
实施例12:3-(4-(((6-(2,6-二甲氧基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-010)的制备
除了使用2,6-二甲氧基苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例4类似的方法制得化合物3-(4-(((6-(2,6-二甲氧基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.16(d,j=10.3hz,2h),7.36(t,j=8.3hz,1h),7.19(dt,j=16.3,7.3hz,3h),6.67(d,j=8.4hz,2h),5.36(s,2h),3.74(s,6h),2.98(t,j=7.7hz,2h),2.69(t,j=7.7hz,2h)。
实施例13:3-(2-氟-4-(((6-(3,4,5-三氟苯基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸(化合物yhhu-011)的制备
除了使用3,4,5-三氟苯硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(3,4,5-三氟苯基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.46(s,1h),8.17(s,1h),7.68–7.52(m,2h),7.18(t,j=7.6hz,1h),7.13–7.02(m,2h),5.36(s,2h),2.88(t,j=7.9hz,2h),2.54(t,j=7.6hz,2h)。
实施例14:3-(2-氟-4-(((6-(2-甲氧基吡啶-3-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸(化合物yhhu-012)的制备
除了使用2-甲氧基吡啶-3-硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(2-甲氧基吡啶-3-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.97(s,1h),8.30(d,j=7.8hz,1h),8.27–8.19(m,2h),7.24(d,j=7.3hz,1h),7.17(d,j=13.1hz,2h),7.10–7.02(m,1h),5.43(s,2h),4.08(s,3h),2.99(t,j=7.7hz,2h),2.69(t,j=7.7hz,2h)。
实施例15:3-(2-氟-4-(((6-(噻吩-3-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸(化合物yhhu-013)的制备
除了使用噻吩-3-硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(噻吩-3-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.37(s,1h),8.00(s,1h),7.89(s,1h),7.55(d,j=5.0hz,1h),7.35(s,1h),7.15(t,j=7.6hz,1h),7.12–7.03(m,2h),5.34(s,2h),2.87(t,j=7.7hz,2h),2.52(t,j=7.7hz,2h)。
实施例16:3-(2-氟-4-(((6-(1-丙基-1-氢-吡唑-4-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸(化合物yhhu-014)的制备
除了使用1-丙基吡唑-4-硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(1-丙基-1-氢-吡唑-4-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.33(s,1h),8.06(s,1h),7.99(s,1h),7.91(s,1h),7.28–7.22(m,1h),7.20–7.14(m,2h),5.40(s,2h),4.15(t,j=7.1hz,2h),2.99(t,j=7.7hz,2h),2.69(t,j=7.7hz,2h),2.00–1.87(m,2h),0.96(t,j=7.4hz,3h)。
实施例17:3-(4-(((6-(3,5-二甲基异噁唑-4-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸(化合物hyh-015)的制备
除了使用3,5-二甲基异噁唑-4-硼酸代替2,6-二甲基苯硼酸之外,按照与实施例3类似的方法制得化合物3-(4-(((6-(3,5-二甲基异噁唑-4-基)吡嗪-2-基)氧)亚甲基)-苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.28(s,1h),8.25(s,1h),7.29–7.26(m,1h),7.18–7.10(m,2h),5.40(s,2h),3.02(t,j=7.7hz,2h),2.72(t,j=7.6hz,2h),2.61(s,3h),2.45(s,3h)。
实施例18:3-(4-(((6-(2-氟-5-甲氧基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-016)的制备
除了使用2-氟-5-甲氧基苯硼酸代替2,6-二甲基苯硼酸之外,以按照与实施例3类似的方法制得化合物3-(4-(((6-(2-氟-5-甲氧基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.62(s,1h),8.15(s,1h),7.42(dd,j=5.7,3.3hz,1h),7.18(t,j=7.7hz,1h),7.14–7.02(m,3h),6.92–6.85(m,1h),5.38(s,2h),3.79(s,3h),2.90(t,j=7.8hz,2h),2.56(t,j=7.7hz,2h)。
实施例19:3-(2-氟-4-(((6-(6-氟-2-甲基吡啶基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-017)的制备
除了使用2-甲基-6-氟-3-吡啶硼酸代替2,6-二甲基苯硼酸之外,以按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(4-氟-2-甲基苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.29(d,j=3.0hz,2h),7.84(t,j=8.1hz,1h),7.24(d,j=7.8hz,1h),7.17–7.08(m,2h),6.89(dd,j=8.1,3.1hz,1h),5.38(s,2h),2.99(t,j=7.5hz,2h),2.69(t,j=7.6hz,2h),2.53(s,3h)。
实施例20:3-(2-氟-4-(((6-(2-氟苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-018)的制备
除了使用2-氟苯硼酸代替2,6-二甲基苯硼酸之外,以按照与实施例3类似的方法制得化合物3-(2-氟-4-(((6-(2-氟苯基)吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.71(s,1h),8.25(s,1h),7.99(t,j=7.3hz,1h),7.43(dd,j=12.9,6.7hz,1h),7.33–7.12(m,5h),5.44(s,2h),2.99(t,j=7.1hz,2h),2.69(t,j=7.6hz,2h)。
实施例21:3-(2-氟-4-(((6-(2-氟-5-甲氧基苯基)-5-甲基吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸(化合物yhhu-019)的制备
用2-羟基-5-甲基-6-氯吡嗪代替2-羟基-6-氯吡嗪6,2-氟-5-甲氧基苯硼酸代替2,6-二甲基苯硼酸之外,以按照与实施例2,3类似的方法制得化合物3-(2-氟-4-(((6-(2-氟-5-甲氧基苯基)-5-甲基吡嗪-2-基)氧)亚甲基)-2-氟苯基)丙酸。1hnmr(400mhz,cdcl3)δ8.60(s,1h),8.13(s,1h),7.39(dd,j=5.7,3.3hz,1h),7.20(t,j=7.7hz,1h),7.13–7.05(m,3h),6.95–6.85(m,1h),5.38(s,2h),3.79(s,3h),2.95(s,3h),2.90(t,j=7.8hz,2h),2.56(t,j=7.7hz,2h)。
实施例22:化合物对稳定转染人源gpr40的hek293细胞株激动活性
hek293细胞,转染真核表达载体人源gpr40-pcdna3.1,经筛选获得稳定表达人源gpr40的单克隆细胞株。稳定转染人源gpr40的hek293细胞株,培养于含10%fbs的高糖dmem培养液。实验前一天将细胞接种于96孔细胞培养板,每孔25000个细胞。实验当天,配制fluo-8工作液(hank's平衡盐溶液含钙离子指示剂(fluo-8)2μm,丙磺舒2mm,酒石黄1.5mm,酸性红14mm)。弃细胞培养液后加入fluo-8工作液,100μl每孔,37℃5%co2孵育1小时。待测化合物的dmso储备液以hank's平衡盐溶液稀释40倍置于96孔样品板。阳性对照化合物为终浓度为5μm的tak-875,空白对照为含0.5%dmso的hank's平衡盐溶液。将孵育完成的细胞板、样品板放于flexstation多功能酶标仪工作站,设置加药25μl每孔,检测加药后细胞内钙离子信号。钙离子信号取max-min转化为原始数据,根据如下公式计算效率%。应用graphpadprism软件计算化合物的ec50。
效率%=[值(compound)-值(bc)]/[值(pc)-值(bc)]×100%
compound,受试化合物;bc,空白对照;pc,阳性对照tak-875。
结果如表1所示。
表1、本申请化合物对人源gpr40的hek293细胞株的激动活性
实施例23:化合物对sd大鼠的急性降血糖作用
选择化合物yhhu-007、yhhu-009、yhhu-010进行sd大鼠体内急性降血糖作用实验。雄性sd大鼠,禁食不禁水过夜(15h),随机分组。分别灌胃给予1%hpmc+0.1%tween-80(control,溶剂对照组)、化合物(yhhu-007、yhhu-009、yhhu-010)10mg/kg,给药容积均为2ml/kg。给药60min后灌胃给予葡萄糖2g/kg,分别于给葡萄糖前(计为0min)和给葡萄糖后15、30、60、120min剪尾取血,血糖仪测定葡萄糖含量。
数据用均数±标准误表示,差异显著性分析采用组间t检验,大鼠口服葡萄糖耐量曲线下面积(auc)采用梯形法计算。结果如图1-6所示,表明化合物yhhu-007、yhhu-009、yhhu-010跟对照组相比体内急性降血糖降糖效果显著,单次给药可显著改善sd大鼠的口服耐糖量。
实施例24:化合物的口服药代研究
化合物经大鼠口服给药,进行药代研究,结果如图7-9所示。yhhu-007、yhhu-009、yhhu-010的平均(取三组1-1、1-2、1-3)auc0-24值依次是48.3356μg/ml.h、6.8505μg/ml.h和19.921μg/ml.h,平均cmax依次是13.521μg/ml、2.1783μg/ml和6.759μg/ml。
实施例25:化合物体外对代谢酶的诱导和抑制实验
化合物对cyp1a2,2b6和3a4酶诱导试验
人原代肝细胞复苏后,以7×104/孔的密度分别接种于96孔胶原包被板,在37℃培养箱(潮湿,含5%co2)中静置培养4h后,换液加入含有matrigel的培养基,在37℃培养箱(潮湿,含5%co2)中静置培养24h后,浓度为0.100、1.00和10.0μm的yhhu-007、yhhu-009、yhhu-010分别与人原代肝细胞共同孵育。cyp1a2、cyp2b6和cyp3a4的阳性对照分别为奥美拉唑、苯巴比妥和利福平,探针底物分别为非那西丁、安非他酮和睾酮。含0.10%dmso的培养液作为空白对照。
试验结果显示,不同浓度下的yhhu-007、yhhu-009、yhhu-010处理人原代肝细胞后,cyp1a2(阳性对照:奥美拉唑,100μm)和cyp2b6酶(阳性对照:苯巴比妥750μm)的活性均小于阳性对照组的40%;在10.0μm的yhhu009和yhhu010作用下cyp3a4酶(利福平,20μm)的活性分别为阳性对照组的44.0%和48.0%,在其他测定浓度的yhhu009和yhhu010以及各测定浓度的yhhu-007的作用下,cyp3a4酶(利福平,20μm)的活性均小于阳性对照组的40%。
化合物对人肝微粒体中主要cyp酶亚型的抑制试验
受试化合物与人肝微粒体及探针底物共孵育,各亚型均设置阳性对照;每孔100μl孵育体积的96-孔板。每孔含20μl人肝微粒体(最终浓度为0.3mg/ml)、50μl受试化合物或阳性抑制剂及20μl探针底物的0.1mtris(ph7.4)液。37℃下预孵育10min,加入10μlnadph使得最终浓度达1mm,孵育15min,加入100μl乙腈及内标混合物(普萘洛尔,纳多洛尔)(50nm)淬灭。反应结束,离心机分离,上层清液lc/ms/ms检测。
考察受试化合物yhhu-007三个非零孵育浓度(0.100、1.00和10.0μm),测定cyp1a2,2c19,2c9,2d6,3a4-m和3a4-t的酶活性变化,阳性对照分别为等浓度的呋拉茶碱、磺胺苯吡唑、反苯环丙胺、奎宁丁、酮康唑、酮康唑,探针底物分别为非那西汀、甲糖宁、美芬妥因、右美沙芬、咪达唑仑、睾丸素,评价yhhu-007对cyp酶的抑制潜能。试验结果显示不同浓度下,yhhu-007处理人肝微粒体后,cyp1a2,2c19,2c9,2d6,3a4-m和3a4-t酶的活性均小于等浓度梯度阳性对照组。
以上通过实施例对本发明进行了示例性说明,但这些实施例并非用以限制本专利的保护范围,凡未脱离本发明精神的等效实施或变更,均应包含于本专利的保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!