一类含四个相同取代基的六元双氮杂环衍生物的制备方法及其应用与流程
本发明涉及一类含四个相同取代基的六元双氮杂环衍生物的制备方法及其应用,属于发光材料在制备有机电致发光器件的应用
技术领域:
。
背景技术:
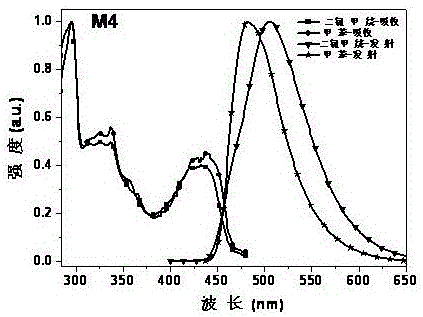
:进入信息化的21世纪后,随着计算机技术及网络的空前繁荣,移动通信及电子商务的蓬勃发展,人们需要性能更好、更能符合未来生活需求的新一代平板显示器。未来的趋势是要在轻巧的载体上传输大量的信息和图像,现今的平板显示器显然已不能满足需求。有机电致发光二极管(OLEDs,OrganicLight-EmittingDiodes)是近几年得到快速发展并有巨大应用前景的新型平板显示技术。这是因为有机电致发光是自发光型的,并有丰富颜色的发光材料以供选择,在显示和发光特性上具有高效率,高亮度(>10000cd/m2),高对比度(>1000:1),色域宽(>100%NTSC),视角广(0-180°),响应快(微秒级)等优点,并且可实现轻薄化(小于1mm),柔性化的显示,这些性能超越了现在所有的显示技术。正是由于有机电致发光器件的诸多优点以及广阔的应用前景,这使得有机发光技术得到了突飞猛进的发展,成为当今国际显示领域的一个研究热点。在有机电致发光材料中,与传统的荧光材料和磷光材料相比,热致延迟荧光材料兼具二者的优点,它既能够充分利用单重态和三重态激子发光而使得器件内量子效率理论上达到100%;同时,热致延迟荧光材料为有机小分子,化学性质稳定且不需要和贵重金属配位使得器件成本大幅降低。因而,研究、开发新型的热致延迟荧光材料具有十分重要的现实意义。技术实现要素:本发明的目的是以六元含氮杂环作为电子受体,咔唑、吩噁嗪、9,9-二甲基-9,10-二氢吖啶等作为电子供体,直接或者通过桥的形式将它们连接起来,适当调控分子的立体构型,以合成一类新型的有机电致发光材料,即一类六元双氮杂环衍生物。本发明所采用的技术方案是:一类含四个相同取代基的六元双氮杂环衍生物,该类衍生物的结构通式如下:其中:X=N时,Y=C-D;Y=N时,X=C-D;D的结构为D1、D2、D3、D4、D5中的一种,D1、D2、D3、D4、D5的结构式如下:一类含四个相同取代基的六元双氮杂环衍生物的制备方法,当D=D1或D2时,反应方程为:该方法包括如下步骤:a)将D-H加入到250ml的三口烧瓶里,然后加入N,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min;冰浴条件下,将NaH分批加入到反应瓶中,继续搅拌1h;b)底物A1或A2溶解在N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,25-60℃下反应15h;c)反应结束后,将反应液倒入浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品进行柱层析提纯,得目标产物;一类含四个相同取代基的六元双氮杂环衍生物的制备方法,当D=D1或D2时,反应方程为:该方法包括如下步骤:a)将D-H加入到250ml的三口烧瓶里,然后加入N,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min;冰浴条件下,将NaH分批加入到反应瓶中,继续搅拌1h;b)底物A3溶解在N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,25-60℃下反应15h;c)反应结束后,将反应液倒入浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品进行柱层析提纯,得目标产物;一类含四个相同取代基的六元双氮杂环衍生物的制备方法,当D=D3、D4或D5时,反应方程为:该方法包括如下步骤:a)称取底物A1或A2、D-B(OH)2、磷酸三钾、四(三苯基膦)钯于干燥的两口烧瓶里,加入甲苯:乙醇体积比为5:1混合溶剂作为反应溶剂,氮气保护下,加热至60-100℃反应20小时;所述底物A1或A2:D-B(OH)2:磷酸三钾的摩尔比为1:6:60,所述四(三苯基膦)钯的用量为底物A1或A2的2mol%;b)反应结束后,减压抽出溶剂后二氯甲烷萃取三次反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干;粗产品进行柱层析提纯,得目标产物。所述六元双氮杂环衍生物用于制备有机电致发光器件中。一类六元双氮杂环衍生物M1、M2、M3、M4、M5、M6、M7,M8、M9、M10的化学分子结构式分别为:所述的一类六元双氮杂环衍生物作为发光材料应用在制备有机电致发光器件中。本发明的有益效果是:这些衍生物是以吡嗪、哒嗪作为发光材料的电子受体,在其外围连接咔唑、吩噁嗪、9,9-二甲基-9,10-二氢吖啶等电子供体,进而获得一些具有电致发光性质的材料。室温下,这些衍生物在紫外-可见光区有强吸收,并且其稀溶液发射强荧光,发光峰位于450-615纳米之间,属于蓝光-橙光范围,可作为发光材料应用于有机电致发光器件。例如:基于化合物M2的器件,启亮电压为3.9V,当电压达到12V时达到最大亮度3846cdm-2。在电流密度为0.06mAcm-2(4.5V)时,器件达到最大发光效率17.4cdA-1和最大功率效率12.2lmW-1。附图说明图1是M2在二氯甲烷和甲苯稀溶液中的紫外-可见吸收光谱和荧光发射光谱。图2是M4在二氯甲烷和甲苯稀溶液中的紫外-可见吸收光谱和荧光发射光谱。图3是M1-M10十种化合物在甲苯溶液中的紫外发射光谱。图4是M2电流密度-电压-亮度曲线。图5是M2的电流效率-亮度-功率效率曲线。图6是M2在不同电压下的电致发光光谱。具体实施方式下面通过实施例对本发明作进一步说明,目的在于更好理解本发明的内容。因此所举实例并不限制本发明的保护范围。实施例1:衍生物M1的合成将1.69g(10.10mmol)咔唑加入到250ml的三口烧瓶里,然后加入100mLN,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min。冰浴条件下,将0.49g(20.19mmol)NaH分批加入到反应瓶中,继续搅拌1h。0.50g(2.30mmol)的3,4,5,6-四氯哒嗪溶解在20ml的N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,60℃下反应15h。反应结束后,将反应液倒入150ml浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品用石油醚和乙酸乙酯(PE:EA=10:1)为流动相进行柱层析冲下杂质,再用纯的二氯甲烷(DCM)冲柱,得到浅黄色固体1.16g,产率68.0%。MS(EI):m/z:740.2688([M]+)。实施例2:衍生物M2的合成方法(1)将1.35g(8.08mmol)咔唑加入到250ml的三口烧瓶里,然后加入100mLN,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min。冰浴条件下,将0.39g(16.16mmol)NaH分批加入到反应瓶中,继续搅拌1h。0.40g(1.84mmol)2,3,5,6-四氯吡嗪溶解在20ml的N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,60℃下反应15h。反应结束后,将反应液倒入150ml浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品用石油醚和乙酸乙酯(PE:EA=10:1)为流动相进行柱层析冲下杂质,再用纯的二氯甲烷(DCM)冲柱,得到黄色固体0.96g,产率70.6%。MS(EI):m/z:740.2653([M]+)。方法(2)将1.86g(11.11mmol)咔唑加入到250ml的三口烧瓶里,然后加入100mLN,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min。冰浴条件下,将0.53g(22.23mmol)NaH分批加入到反应瓶中,继续搅拌1h。0.5g(2.53mmol)2,3-二氯-5,6-二氰基吡嗪溶解在20ml的N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,60℃下反应15h。反应结束后,将反应液倒入150ml浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品用石油醚和乙酸乙酯(PE:EA=10:1)为流动相进行柱层析冲下杂质,再用纯的二氯甲烷冲柱,得到黄色固体0.83g,产率44.3%。MS(EI):m/z:740.2655([M]+)。实施例三中的方法(1),方法(2)都可以得到目标产物M2。实施例3:衍生物M3的合成将2.82g(10.10mmol)3,6-二叔丁基咔唑加入到250ml的三口烧瓶里,然后加入150mLN,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min。冰浴条件下,将0.49g(20.19mmol)NaH分批加入到反应瓶中,继续搅拌1h。0.50g(2.30mmol)3,4,5,6-四氯哒嗪溶解在20ml的N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,60℃下反应15h。反应结束后,将反应液倒入150ml浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品用石油醚和二氯甲烷(PE:DCM=30:1)为流动相进行柱层析提纯,得到浅黄色固体2.10g,产率77.2%。MS(MALDI-TOF):m/z:1188.7679([M]+)。实施例4:衍生物M4的合成方法(1)将2.82g(10.10mmol)3,6-二叔丁基咔唑加入到250ml的三口烧瓶里,然后加入150mLN,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min。冰浴条件下,将0.49g(20.19mmol)NaH分批加入到反应瓶中,继续搅拌1h。0.50g(2.30mmol)2,3,5,6-四氯吡嗪溶解在20ml的N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,60℃下反应15h。反应结束后,将反应液倒入150ml浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品用石油醚和二氯甲烷(PE:DCM=35:1)为流动相进行柱层析提纯,得到黄色固体2.15g,产率79.3%。MS(MALDI-TOF):m/z:1188.7687([M]+)。方法(2)将1.86g(6.67mmol)3,6-二叔丁基咔唑加入到250ml的三口烧瓶里,然后加入150mLN,N-二甲基甲酰胺作为反应溶剂,在磁力搅拌器上搅拌10min。冰浴条件下,将0.32g(13.34mmol)NaH分批加入到反应瓶中,继续搅拌1h。0.30g(1.52mmol)的2,3-二氯-5,6-二氰基吡嗪溶解在10ml的N,N-二甲基甲酰胺里,逐滴加入到反应体系中,添加完毕后,氮气保护下,60℃下反应15h。反应结束后,将反应液倒入150ml浓度为10%的稀盐酸里淬灭,减压抽滤后,水洗,烘干,粗产品用石油醚和二氯甲烷(PE:DCM=30:1)为流动相进行柱层析提纯,得到黄色固体0.85g,产率47.3%。MS(MALDI-TOF):m/z:1188.7649([M]+)。实施例六中的方法(1),方法(2)都可以得到目标产物M6。实施例5:衍生物M5的合成称取1.78g(10.64mmol)咔唑,3.0g(10.64mmol)对溴碘苯,2.93g(21.28mmol)无水碳酸钾,0.38g(2.13mmol)1,10-邻菲啰啉,0.41g(2.13mmol)碘化亚铜于100mL三口瓶中,然后加入50mLN,N-二甲基甲酰胺作为反应溶剂。氮气保护下,加热至165℃反应24小时。反应结束后,将反应液倒入150mL饱和食盐水中淬灭,减压抽滤后用二氯甲烷(100mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋出溶剂、烘干。粗产品用石油醚和二氯甲烷(PE:DCM=25:1)为流动相进行柱层析提纯,得到白色固体1.72g,产率50.3%。MS(EI):m/z:321.0166([M]+)。称取1.72g(5.36mmol)中间体1于100mL干燥的两口瓶内,加入50mL干燥的四氢呋喃作为反应溶剂。氮气保护下,将其用液氮丙酮冷却到-78℃,在此温度下搅拌5min,氮气保护下向反应体系中逐滴加入5.0mL(1.6mol/L,8.04mmol)的正丁基锂。-78℃下反应1小时后,向反应体系中滴加1.2mL(10.72mmol)的硼酸三甲酯,并使之自然升温搅拌过夜。反应结束后加入稀盐酸溶液并调节溶液为酸性。用二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋出溶剂、烘干。粗产品用二氯甲烷和乙酸乙酯为洗脱剂梯度进行柱层析提纯,得到白色结晶状固体1.02g,产率66.5%。MS(EI):m/z:287.1124([M]+)。称取1.02g(3.55mmol)的中间体2,0.13g(0.59mmol)的3,4,5,6-四氯哒嗪,7.6g(35.5mmol)的磷酸三钾,0.023g(0.012mmol)的四(三苯基膦)钯于100ml干燥的两口烧瓶里,加入50mL(甲苯:乙醇=5:1)作为反应溶剂,氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到淡黄色结晶粉末0.53g,产率85.6%。MS(MALDI-TOF):m/z:1044.3902([M]+)。实施例6:衍生物M6的合成称取1.0g(3.48mmol)的中间体2,0.13g(0.58mmol)的2,3,5,6-四氯吡嗪,7.4g(34.8mmol)的磷酸三钾,0.014g(0.012mmol)的四(三苯基膦)钯于100ml干燥的两口烧瓶里,加入50mL(甲苯:乙醇=5:1)作为反应溶剂,氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到白色结晶粉末0.54g,产率89.7%。MS(MALDI-TOF):m/z:1044.3938([M]+)。实施例7:衍生物M7的合成称取2.0g(10.92mmol)吩噁嗪,3.08g(10.92mmol)对溴碘苯,7.12g(21.85mmol)无水碳酸铯,0.82ml(0.33mmol)的三叔丁基膦,0.049g(0.22mmol)的醋酸钯于250mL三口瓶中,然后加入80mL干燥的四氢呋喃作为反应溶剂。氮气保护下,加热至100℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到白色结晶粉末2.42g,产率65.7%。MS(EI):m/z:337.0125([M]+)。称取2.42g中间体3(7.18mmol)于100mL干燥的两口瓶内,加入50mL干燥的四氢呋喃作为反应溶剂。氮气保护下,将其用液氮丙酮冷却到-78℃,在此温度下搅拌5min,氮气保护下向反应体系中逐滴加入6.73mL(1.6mol/L,10.77mmol)的正丁基锂。-78℃下反应1小时后,向反应体系中滴加1.63ml(8.8mol/L,14.36mmol)的硼酸三甲酯,并使之自然升温搅拌过夜。反应结束后加入稀盐酸溶液并调节溶液为酸性。用二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋出溶剂、烘干。粗产品用二氯甲烷和乙酸乙酯为洗脱剂梯度进行柱层析提纯,得到白色结晶状固体1.50g,产率68.9%。MS(EI):m/z:303.1066([M]+)。称取0.5g(1.60mmol)的中间体4,0.06g(0.28mmol)的3,4,5,6-四氯哒嗪,3.4g(16.0mmol)的磷酸三钾,0.01g(0.008mmol)的四(三苯基膦)钯于50ml干燥的两口烧瓶里,加入25mL(甲苯:乙醇=5:1)作为反应溶剂,氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(25mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到淡黄色结晶粉末0.26g,产率85.2%。MS(MALDI-TOF):m/z:1108.3730([M]+)。实施例8:衍生物M8的合成称取0.5g(1.60mmol)的中间体4,0.06g(0.28mmol)的2,3,5,6-四氯吡嗪,3.4g(16.0mmol)的磷酸三钾,0.01g(0.008mmol)的四(三苯基膦)钯于50ml干燥的两口烧瓶里,加入25mL(甲苯:乙醇=5:1)作为反应溶剂,氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(25mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到黄色结晶粉末0.28g,产率90.5%。MS(MALDI-TOF):m/z:1108.3755([M]+)。实施例9:衍生物M9的合成称取2.0g(9.56mmol)的9,9-二甲基-9,10-二氢吖啶,2.70g(9.56mmol)对溴碘苯,18.4g(191.2mmol)无水叔丁醇钠,0.73ml(0.29mmol)的三叔丁基膦,0.043g(0.19mmol)的醋酸钯于250mL三口瓶中,然后加入100mL干燥的四氢呋喃作为反应溶剂。氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到白色结晶粉末2.28g,产率65.7%。MS(EI):m/z:363.0633([M]+)。称取2.28g中间体5(6.28mmol)于100mL干燥的两口瓶内,加入50mL干燥的四氢呋喃作为反应溶剂。氮气保护下,将其用液氮丙酮冷却到-78℃,在此温度下搅拌5min,氮气保护下向反应体系中逐滴加入5.89mL(1.6mol/L,9.42mmol)的正丁基锂。-78℃下反应1小时后,向反应体系中滴加1.43ml(8.8mol/L,12.56mmol)的硼酸三甲酯,并使之自然升温搅拌过夜。反应结束后加入稀盐酸溶液并调节溶液为酸性。用二氯甲烷(50mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋出溶剂、烘干。粗产品用二氯甲烷和乙酸乙酯为洗脱剂梯度进行柱层析提纯,得到白色固体1.45g,产率69.9%。MS(EI):m/z:329.1590([M]+)。称取0.4g(1.22mmol)的中间体6,0.044g(0.20mmol)的3,4,5,6-四氯哒嗪,2.6g(12.2mmol)的磷酸三钾,0.007g(0.006mmol)的四(三苯基膦)钯于100ml干燥的两口烧瓶里,加入50mL(甲苯:乙醇=5:1)作为反应溶剂,氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(25mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到淡黄色结晶粉末0.21g,产率84.2%。MS(MALDI-TOF):m/z:1212.5820([M]+)。实施例10:衍生物M10的合成称取0.4g(1.22mmol)的中间体6,0.044g(0.20mmol)的2,4,5,6-四氯嘧啶,2.6g(12.2mmol)的磷酸三钾,0.007g(0.006mmol)的四(三苯基膦)钯于100ml干燥的两口烧瓶里,加入50mL(甲苯:乙醇=5:1)作为反应溶剂,氮气保护下,加热至80℃反应20小时。反应结束后,减压抽出溶剂后二氯甲烷(25mL×3)萃取反应液,合并萃取液并用无水硫酸镁干燥,旋干溶剂,烘干。粗产品用石油醚和二氯甲烷(PE:DCM=15:1)为洗脱剂进行柱层析提纯,得到黄色结晶粉末0.23g,产率92.1%。MS(MALDI-TOF):m/z:1212.5827([M]+)。实施例11:选取其中M2和M4化合物,测得了它们的最大吸收波长分别为423nm和435nm,M2的最大发射波长为477nm(甲苯溶液中)和490nm(二氯甲烷溶液中),M4的最大发射波长为481nm(甲苯溶液中)和506nm(二氯甲烷溶液中),M2和M4在二氯甲烷溶液的波长比在甲苯溶液中都发生了明显的红移现象(如图1和图2)。M1~M10化合物在甲苯溶液中荧光发射光谱如图3,发光峰位于450-615纳米之间,属于蓝光-橙光范围,如表1。表1.十种化合物在甲苯溶液中的最大吸收波长和最大发射波长化合物M1M2M3M4M5M6M7M8M9M10最大吸收波长(nm)441423422435415401476465458449最大发射波长(nm)495477503481469450615580565540实施例12:将M2作为发光材料应用于有机电致发光器件中。器件结构为:ITO/PEDOT/TAPC(20nm)/8%M2:mCP(20nm)/TmPyPB(40nm)/LiF(0.5nm)/Al(200nm)得到了M2化合物电流密度-电压-亮度曲线(图4),电流效率-亮度-功率效率曲线(图5),以及在不同电压下的电致发光光谱(图6),基于化合物M2的器件,启亮电压为3.9V,当电压达到12V时达到最大亮度3846cdm-2。在电流密度为0.06mAcm-2(4.5V)时,器件达到最大发光效率17.4cdA-1和最大功率效率12.2lmW-1。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 一种含硫的取代基取代的二噻吩衍生物及其共轭聚合物的制备方法及应用
- N2-糖基取代的1,2,3-三唑化合物及其合成方法与应用
- 4-(3-取代苯胺基)-6-取代基喹唑啉类化合物及制备和应用
- 被具有包含炔基取代基的苯基取代的除草活性环二酮化合物或其衍生物的制作方法
- 1-N-取代苄基-6-N’-取代基-2,3,6,9-四氢-1H-[1,4]噁嗪并[3,2-g]喹啉-9-酮-8-甲酸 ...的制作方法
- 具有取代苯基硫属原子代低级烷基和导入酯结构的苯基作为取代基的新型1,2-二氢喹啉 ...的制作方法
- 2
- 制备区域规则的聚-(3-取代的)噻吩、硒吩、噻唑和硒唑的方法
- 一种取代五并苯类红色有机电致发光材料及其制备方法
- 光子型间苯取代基全氟环戊烯类二芳烯光致变色材料的制备及其在双光子光存储中的应用的制作方法
- 一种含硫的取代基取代的二噻吩衍生物及其共轭聚合物的制备方法及应用
- N2-糖基取代的1,2,3-三唑化合物及其合成方法与应用
- 4-(3-取代苯胺基)-6-取代基喹唑啉类化合物及制备和应用
- 被具有包含炔基取代基的苯基取代的除草活性环二酮化合物或其衍生物的制作方法
- 1-N-取代苄基-6-N’-取代基-2,3,6,9-四氢-1H-[1,4]噁嗪并[3,2-g]喹啉-9-酮-8-甲酸 ...的制作方法
- 具有取代苯基硫属原子代低级烷基和导入酯结构的苯基作为取代基的新型1,2-二氢喹啉 ...的制作方法
- 2
- 一种降低偏苯三酸酐中杂质含量的方法
- 一种取代五并苯类红色有机电致发光材料及其制备方法
- 光子型间苯取代基全氟环戊烯类二芳烯光致变色材料的制备及其在双光子光存储中的应用的制作方法