化合物及使用其制成的电子组件的制作方法
本发明提出一种化合物及电子组件,特别是一种用于电子组件中发光材料或有机材料的化合物。
背景技术:
最早的有机发光二极管(OLED)是由伊斯特曼柯达(Eastman Kodak)公司经由真空蒸镀程序制作,柯达公司的唐(Tang)和凡斯赖克(VanSlyke)于带有芳二胺基的有机层之透明铟锡氧化物(ITO)玻璃上沉积电子传输材料,例如Alq3,随后将金属电极以蒸镀方式沉积于所述Alq3层上,制造成有机电激发光(EL)组件。所述有机EL组件由于具有高亮度、快反应速度、轻量、紧密度、全彩色、无视角差异、无需使用液晶显示器(LCD)背光板以及低能耗,目前已成为新一代的发光组件或显示器。
近年来、一些像是电子传输层及电洞传输层等中间层被设置于阴极及阳极之间,以提高OLED的电流效率及功率效率。例如,如图1中所例示的OLED 100被设计成由阴极11、电子注入层12、发光层15、电洞传输层17及阳极18所构成。
从组件功能概念来看,从OLED 100发出的光线起因于所述发光层15中的电子及电洞重组所产生的激子。然而,根据理论推测,单重态的激子与三重态的激子之比例为3:1,因此,当小分子荧光材料用于所述OLED 1’的所述发光层时,约有25%激子被用于发光,以及其余75%三重态激子经由非发光机制而损失。所以,一般的荧光材料可已达成的量子效率,相对于原件中外部量子效率5%之量,上限为25%。
再者,研究人员还发现特定的电洞传输型材料可以同时达成电子限制能力,像是由以下化学式1’及2’所表示的材料。所述化学式1’表示了被缩写称为TCTA的三(4-肼甲酰基-9-基-苯基)胺。所述化学式2’表示了被缩写称为NPB的N,N’-二(1-萘基)-N,N’-二苯基-(1,1’-联苯基)-4,4’-二胺。
此外,在OLED应用中为了有效的蓝色发光效能,研究人员开发出基于三芳基胺基二聚物形态的电洞传输型蓝色发光体,像是发明人于实验室中开发得到由以下化学式3’、4’及5’所代表的IDE-102、N-STIF-N,以及螺二芴为基底的系统。
化学式3’
目前,为了有效提升OLED的发光性能,OLED制造商及研究人员已付出很多努力而开发得到具有电洞阻挡功能的电子传输材料,像是由以下化学式6’到10’所分别代表的TmPyPb、TPBi、3TPYMB、BmPyPb以及DPyPA。TmPyPb是3,3'-[5'-[3-(3-吡啶基)苯基][1,1':3',1”-三苯]-3,3”-二基]双吡啶的缩写,TPBi是1,3,5-Tris(1-苯基-1H-苯并咪唑-2-基)苯的缩写,3TPYMB是参(2,4,6-三甲基-3-(吡啶-3-基l)苯基)硼烷的缩写,BmPyPb是1,3-双(3,5-双吡啶-3-基-苯基)苯的缩写,以及DPyPA是9,10-双(3-(吡啶-3-基)苯基)蒽的缩写。
化学式10’
虽然各种的蓝色发光掺杂材料以及具有电子阻挡功能发光体已开发,使用所述蓝色发光掺杂材料还无法完成优良的发光效率以及装置的生命期。因此,对于习知例如所述商业化的蓝色发光掺杂材料及具有电子阻挡和三重态-三重态消灭功能,本案发明人已尽最大努力进行发明性研究,且终于提供一系列的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,作为用于OLED的蓝色发光掺杂材料及发光体材料。
技术实现要素:
本发明之一面向系提供一种化合物,所述化合物包括:顺式二苯乙烯段;由四键原子构成的桥接原子段,所述四键原子以两个键连接于所述顺式二苯乙烯段,形成七员环结构段;以及咪唑段,连接于所述顺式二苯乙烯段。
本发明之另一面向系提供一种电子组件,所述电子组件由化合物制成,其中所述化合物包括:顺式二苯乙烯段;由四键原子构成的桥接原子段,所述四键原子以两个键连接于所述顺式二苯乙烯段,形成七员环结构段;以及咪唑段,连接于所述顺式二苯乙烯段。
本领域技术人员在阅读以下详细实施方式的叙述及所附的图式之后,将对本发明的目的及优点有更清楚明白的了解。
附图说明
图1显示现有的OLED的结构;
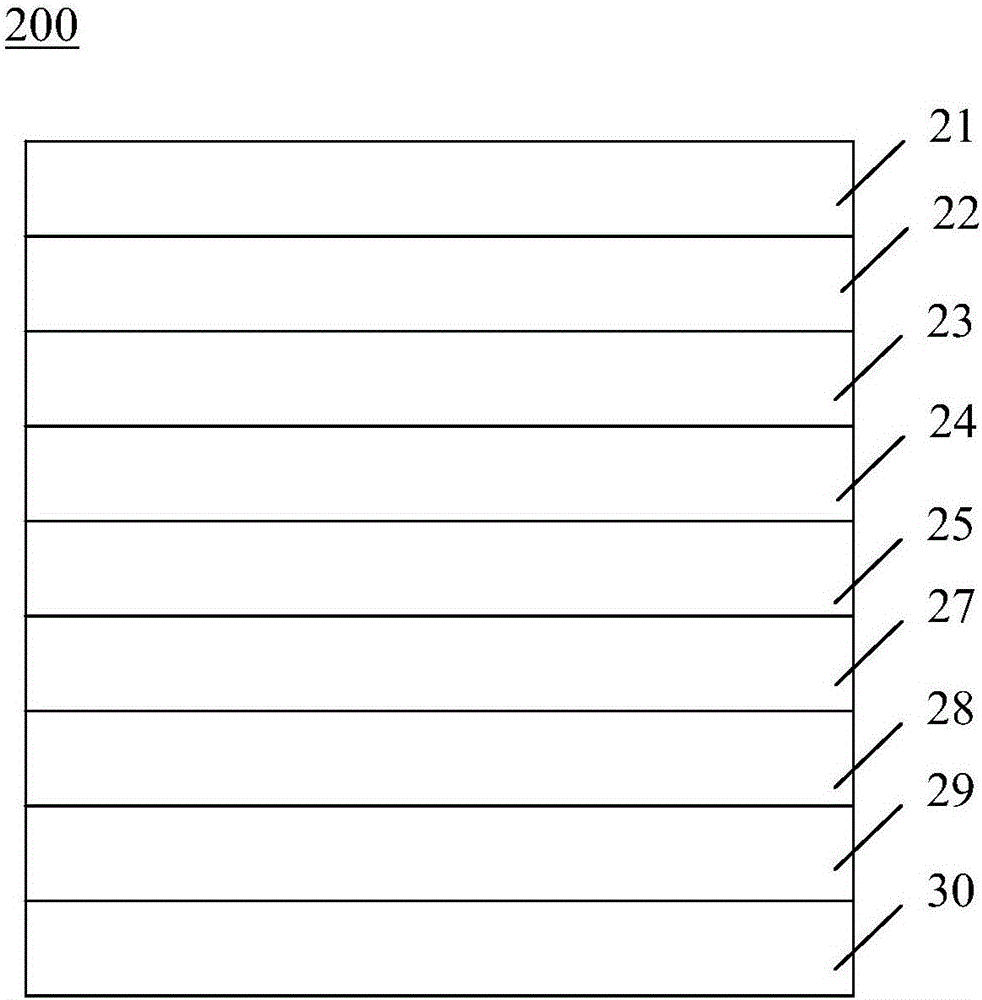
图2显示本发明制成OLED的一实施例的结构。
图3显示本发明制成OLED的另一实施例的结构。
主要组件符号说明
11、21:阴极
12、22:电子注入层
15、25:发光层
17、27:电洞传输层
19、29:阳极
23:电子传输层
24:电洞阻挡层
28:电洞注入层
30:基板
35:电洞传输型的发光层
100、200、300:有机发光二极管
具体实施方式
本发明将藉由下述实施例并配合图示,作进一步的详细说明。值得一提的是,本发明下列实施例的叙述仅用于说明和描述,并非用来限制本发明至任何所揭露的精确形式或数据。
本发明提供一系列的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,所述化合物包括顺式二苯乙烯段;由四键原子构成的桥接原子段,所述四键原子以两个键连接于所述顺式二苯乙烯段,形成七员环结构段;以及咪唑段,连接于所述顺式二苯乙烯段。所述化合物或其衍生物除了具有发光特性,也具有传输电洞的功能,因此,当所述化合物或其衍生物应用于荧光OLED时,除了作为电洞传输层之材料外,还能作为具有电洞传输功能的发光层之材料,其中具有电洞传输功能的发光层即可称为电洞传输型的发光层。依据本发明一种实施例的OLED 200如图2所示,OLED 200依序包括阴极21、电子注入层22、电子传输层23、电洞阻挡层24、发光层25、电洞传输层27、电洞注入层28、阳极29以及基板30。当所述电洞传输层27及所述发光层25以单层形成,所述单层为由所述化合物或其衍生物所制成的电洞传输型的的发光层35,如图3的OLED 300中所示。
前述之各种电子组件可应用于各种具有显示器的组件或装置,例如有机发光装置、太阳能电池装置、有机晶体管、侦测装置、平面显示器、计算机显示屏幕、电视、告示牌、室内或室外照明、室内或室外讯号灯、可挠式显示器、激光打印机、桌上型电话、可携式电话、遥控装置、平板计算机、笔记本电脑、数字相机、摄录像机、探视器、微型显示设备、车用装置、外墙显示设备、视听屏幕、或讯号装置。
本发明提供一系列的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,其中所述化合物中的咪唑段具有连接于一号氮位置的H或连接于二号碳位置的H的至少其中之一被芳香基取代;其中所述芳香基为苯基,当所述连接于一号氮位置的H与所述连接于二号碳位置的H分别被苯基取代时,所述咪唑段为1,2-二苯基咪唑段,所述1,2-二苯基咪唑段由化学式1a来表示:
化学式1a
当所述连接于二号碳位置的H被苯基取代时,所述咪唑段为2-苯基咪唑段,所述2-苯基咪唑段由化学式1b来表示:
化学式1b
当所述连接于一号氮位置的H被苯基取代时,所述咪唑段为1-苯基咪唑段,所述1-苯基咪唑段由化学式1c来表示:
化学式1c
本发明提供一系列的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,其中所述顺式二苯乙烯段由化学式2来表示:
化学式2
其中R3为H、叔丁基或萘基,R1或R11为H、卤素、-Ar、-CN、-CF3、-Ar-F、芳胺基、或由化学式3a或3b来表示:
其中卤素为F、Cl、Br或I,m为1-3的整数,Ar及G为苯基,以及所述芳胺基为-NR4R5,其中R4或R5为H、苯基或萘基。更特定地,所述-NR4R5由化学式3m、3n或3p来表示:
其中X为H或未取代或被取代的具有1-20个碳原子的烷基。
本发明提供一系列的咪唑螺顺式二苯乙烯/芴化合物及其衍生物,其中所述四键原子为碳或硅;更特定地,所述由四键原子构成的桥接原子段为由化学式A1、A2、A3或A4所表示:
其中R3为H、叔丁基或萘基。
第一实施例
根据本发明第一实施例的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,当所述咪唑段中连接于一号氮位置的H与所述连接于二号碳位置的H分别被苯基取代而形成1,2-二苯基咪唑段(由化学式1a来表示)、以及所述由四键原子构成的桥接原子段为由化学式A1所表示时,所述化合物为1,2-二苯基咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物之衍生物其中之一,且为由化学式4A来表示:
化学式4A
其中R1、R3及R11同前述。
第二实施例
根据本发明第二实施例的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,当所述咪唑段中连接于二号碳位置的H被苯基取代而形成2-苯基咪唑段(由化学式1b来表示)时,所述化合物为2-苯基咪唑融合螺顺式二苯乙烯/芴化合物之衍生物其中之一,且为由化学式4B来表示:
化学式4B
其中R1、R3及R11同前述。
第三实施例
根据本发明第三实施例的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,当所述咪唑段中连接于一号氮位置的H被苯基取代而形成1-苯基咪唑段(由化学式1c来表示)时,所述化合物为1-苯基咪唑融合螺顺式二苯乙烯/芴化合物之衍生物其中之一,且为由化学式4C来表示:
化学式4C
其中R1、R3及R11同前述。
第四实施例
根据本发明又一实施例的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,当所述咪唑段由化学式1a来表示且R1与R11相同(由R表示)时,所述化合物为1,2-二苯基咪唑融合螺顺式二苯乙烯/芴化合物之衍生物其中之一,且为由化学式4D来表示:
化学式4D
所述有机化合物的制造方法
由化学式5表示的所述有机化合物,其合成方法包括以下步骤:
化学式5
步骤1
取5505.9毫克(10.7毫莫耳)由化学式11表示的化合物11放入反应瓶中,并加入15ml醋酸,再加入浓盐酸1.5mL形成溶液,此时反应瓶内的溶液的颜色变为红色。在反应瓶上方安装回流装置,将反应瓶置入约120℃的油浴中,使其反应30分钟后,溶液的红色会褪去,并有大量沈淀出现,升起反应瓶待其回温,将回流管卸下且以正己烷冲洗除去瓶底中残留物中所残余的硅油。将瓶底中残留物以二氯甲烷(三次,每次50毫升)与水萃取,所得到的有机萃取液加入硫酸镁干燥后过滤、回旋浓缩抽干溶剂,粗产物以管柱层析(使用1:3之比例之二氯甲烷及正己烷)纯化,所得产物再利用二氯甲烷与正己烷以再结晶方式进行纯化,可得到4985.3毫克以化学式12表示的固体化合物12,即3,7-二溴-5,5-螺芴基-5H-二苯并[a,d]环庚烯(3,7-dibromo-5,5-spirofluorenyl-5H-dibenzo[a,d]cycloheptene),产率为91%。
步骤2
取由化学式12表示的化合物2489.8毫克(5毫莫耳)与苯亚硒酸酐(BSA)2340.8毫克(6.5毫莫耳)放入反应瓶中,并加入20ml氯苯,在反应瓶上方安装回流装置,将反应瓶置入约130℃油浴中,使其反应18小时后,以薄层层析法(TLC)确定无反应起始物存在,升高反应瓶待其回温,将回流管卸下且以正己烷冲洗除去瓶底残留物所残余的硅油,利用回旋浓缩仪将氯苯从残留物抽干,加入20毫升正己烷至抽滤漏斗(内置2公分厚硅胶与滤纸)以溶解残留物中的副产物二苯基二硒醚(Diphenylselenide),并过滤以得到固体沈淀物,并以正己烷清洗固体多次,将固体刮下可直接得到粗产物,再利用二氯甲烷与正己烷以再结晶方式进行纯化,可得到2164.5毫克的以化学式13表示的固体化合物13,即螺-芴-3,7-二溴-二苯并环庚烷-10,11-二酮(spiro-fluorene-3,7-dibromo-dibenzosuberan-10,11-dione),产率为82%,同时可回所述副产物二苯基二硒醚。
步骤3
取一100毫升双颈圆底瓶,内放搅拌子,上接回流管并开启回流装置,真空干燥后,在氮气环境下,分别加入以化学式13表示的化合物1594毫克(3毫莫耳)、以化学式14表示的化合物815.1毫克(4.5毫莫耳)与乙酸铵(NH4OAc)3004.9毫克(39毫莫耳)于反应瓶中,并打入15毫升的醋酸,以磁石搅拌混合均匀,将反应瓶置入约70℃油浴中,使其反应30小时后,以TLC确定无起始物存在,升高反应瓶待其回温,将回流管卸下且以正己烷冲洗去除残余的硅油。使用二氯甲烷(三次,每次20毫升)与水萃取,所得到的萃取液加入硫酸镁干燥之,过滤,回旋浓缩将溶剂抽干,粗产物以管柱层析(使用1:8之比例之乙酸乙酯及正己烷)纯化,所得产物再利用二氯甲烷与正己烷以再结晶方式进行纯化,可得到1655毫克的以化学式10表示的固体化合物10,即螺-芴-3,7-二溴-二苯并环庚烯[d]咪唑(spiro-fluorene-e,7-dibromo-dibenzosuberene[d]imidazole),产率为80%。
其余的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物,例如由化学式15-17所表示的化合物15-17,能够使用前述相似的偶合反应来得到。本领域技术人士可以了解,相似的衍生物及其制造方法仍不脱离本发明的范畴。
化学式17
其中R3为H、叔丁基或萘基,R1为-NR4R5,其中R4或R5为H,苯基或萘基,以及X为H或未取代或被取代的具有1-20个碳原子的烷基。
化学式5是表示化合物15-17的通式,其中具有的取代基-NArR为化学式3m、3n及3p其中之一。当所述取代基-NArR为由化学式3m表示,所述有机化合物即为化合物15。化合物15的合成方法包括以下步骤。
首先,将4870.8mg(7mmol)的化合物10(99%)、192mg(1.5mmol)的Pd2(dba)3、4035mg(60mmol)的三级丁氧化钙(sodium tert-butoxide)、1ml的三-三级丁基膦(tri-tert-butylphosphine)、以及2960mg,(17.5mmol)的二苯胺,在氮气环境下溶于70ml的甲苯,并回流4至8小时以得到混合物。然后该混合物以100ml水淬息,并将水溶液层分离,再以二氯甲烷萃取三次,每次200ml。所得到的混合有机层使用硫酸镁干燥、加以过滤且被蒸发,得到的粗固态产物使用1:1比例的二氯甲烷及正己烷再结晶,来得到5030mg(83%)的化合物15。化合物16及17也可以使用与化合物15相似的合成方法来得到。
所得到的化合物15的核磁共振(NMR)分析资料如下:Tm 311℃(DSC);M.W.:869.06;1H NMR(500MHz,CDCl3)δ7.59(d,J=7.5,2H),7.51(s,2H),7.36-7.29(m,6H),7.16-7.13(m,14H),6.9-6.8(m,15H),6.70(s,3H),6.55(s,2H);13C NMR(100MHz,CDCl3)δ149.47,147.76,147.50,146.99,146.70,143.21,142.26,140.03,139.47,137.61,131.09,130.84,129.47,129.40,129.08,128.98,128.75,128.44,128.30,128.15,128.01,127.44,126.98,124.94,124.50,124.38,123.20,123.10,122.59,122.37,121.66,119.71,119.11,66.35,53.38;MS(20eV)869.4(M+,100),870.4(66),871.4(21),1736.7(11),1737.7(15),1738.7(9);IR(KBr)3057(m),1588(s),1488(s),1445(s),1399(s),1373(s),1278(s),1155(s),1074(s),1027(s);HR-MS calcd for C64H44N4:869.0610,found:869.0618;Anal.Calcd for C64H44N4:C,88.45,H,5.10,N,6.45.found:C,88.57,H,5.12,N,6.42;TLC Rf0.28(CH2Cl2/hexane,1/1)。
所得到的化合物16的NMR分析资料如下:m.p.317.6℃(DSC);M.W.:696.18;1H NMR(400MHz,CDCl3)δ8.24(d,J=8.2,1H),7.89(d,J=8.2,2H),7.72(d,J=7.1,4H),7.80(d,J=7.9,2H),7.57(d,J=8.4,1H),7.48(m,4H),7.4(d,J=7.6,2H),7.3(m,4H),7.28(s,2H),7.24(m,2H),7.20(s,1H),7.18(s,1H)7.09(m,5H),7.03(d,J=8.3,2H),6.98(t,J=7.5,3H),6.91(d,J=7.9,3H),6.86(d,J=8.0,2H),6.80(d,J=7.8,2H),6.53(s,2H),6.31(m,5H);13C NMR(100MHz,CDCl3)δ139.24,129.42,129.40,128.90,128.86,128.44,128.19,128.11,127.98,127.34,127.05,126.18,126.11,126.05,125.95,125.86,119.36,66.22;HR-MS calcd for C72H48N4:969.1783,found:969.1787;Anal.Calcd for C72H48N4:C,89.23,H,4.99,N,5.78.found:C,89.01,H,5.02,N,5.97;TLC Rf0.23(CH2Cl2/hexane,2/1)。
所得到的化合物17的NMR分析资料如下:m.p.266.17℃(DSC);M.W.:744.33;1H NMR(400MHz,CDCl3)δ8.30(d,J=8.3,1H),7.68(d,J=7.5,2H),7.50(s,2H),7.29(m,7H),7.20(m,7H),7.09(m,3H),6.99(m,3H),6.92(d,J=8.3,4H),6.87(d,J=8.1,2H),6.67(s,1H),6.59(d,J=8.6,1H),6.37(d,J=8.5,1H),3.11(s,3H),2.97(d,J=6.8,3H);13C NMR(100MHz,CDCl3)δ148.72,148.14,147.62,142.33,139.79,129.82,129.59,129.47,129.21,128.96,128.48,128.26,128.07,128.00,127.70,126.90,123.17,122.83,121.07,120.58,120.03,118.64,114.91,66.88,39.93,39.69;HR-MS calcd for C54H40N4:744.3253,found:744.3259;Anal.Calcd for C54H40N4:C,87.07,H,5.41,N,7.52found:C,86.80,H,5.36,N,7.84;TLC Rf 0.42(CH2Cl2/hexane,2/1)。
前述化合物15-化合物17的玻璃转移温度(Tg)、热裂解温度(Td)、吸收光谱的最高波峰波长值(λmax)、以及光致发光(photoluminescence)光谱的最高波峰波长值(PL_λmax)被量测并记录于表1中。由表1可知,本发明所提出的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物的玻璃转移温度范围介于143至185℃之间、以及其热裂解温度范围介于429至474℃之间,此意谓这些咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物具有优秀的热稳定性,且在高电压及高电流密度操作条件下不易裂解。在表1中,Φ代表苯基、N代表氮、BS代表咪唑融合螺顺式二苯乙烯/芴结构、Np代表萘基、以及Me代表甲基。
表1
此外,前述化学式15-17的1,2-咪唑融合螺顺式二苯乙烯/芴衍生物的氧化电位及还原电位可由循环伏安法(CV)来量测并记录于表2中。本领域技术人士由表2可以了解,本发明所提出的1,2咪唑融合螺顺式二苯乙烯/芴衍生物,化合物15-17具有第一氧化电位介于0.13V至0.30V之间、化合物15-17具有第二氧化电位介于0.39V至0.57V之间。
表2
依据本发明所制作OLED的过程说明如下。将鋁基板經清洗後,放入蒸镀机中,于真空度达约7×10-6torr以下,将下列表3中之各种有机材料及金属依序蒸镀至鋁基板上,以氮气破真空后取出蒸镀好之基板以进行评估。可选择地,也可以取ITO玻璃来制作所述OLED装置。所述ITO玻璃于清洗后,放入蒸镀机中,以前述相反的顺序于所述ITO玻璃上沉积各种有机材料及金属,来得到所述OLED装置。
为了证明本发明提出的咪唑融合螺顺式二苯乙烯/芴混成材料的确能够应用作为有机发光二极管之电洞传输层及或发光层,多个实验组及控制组之OLED组件被设计及制作,其中OLED的各层组成材料显示于表3。
表3
其中Alq3为三(8-烃基喹啉)铝的缩写;BCP为2,9-双甲基-4,7-双苯基-1,10-啡啉;BANE为10,10-双(二苯-4基)-9,9’-二蒽的缩写;NPB为N,N’-二(1-萘基)-N,N’-二苯基-(1,1’-联苯基)-4,4’-二胺的缩写;螺芴为由化学式18所表示的化合物;TAPC为4,4’-亚环己基双[N,N-双(4-甲基苯)苯胺](4,4’-cyclohexylidenebis[N,N-bis(4-methylphenyl)benzenamine])的缩写并由化学式19所表示;HATCN为1,4,5,8,9,11-六氮杂三伸苯基六腈(1,4,5,8,9,11-hexaazatriphenylene hexacarbonitrile)的缩写并由化学式20所表示。
以上各组OLED组件的开启电压(Von)、外部量子效率(ηext)、电流效率(ηc)、功率效率(ηp)、以及最大亮度(Lmax)被量测并记录于表4。
表4
参照表4中的各蓝色荧光OLE组件的量测数据,可以得知,相较于控制组1的单一发光层的OLED,使用单一电洞传输层的实验组1~3的OLED组件具有更优秀的ηext、ηc、ηp及Lmax,且优于具有单一掺杂物发光层的控制组1的OLED组件,且使用NpΦNBSNΦNp的实验组2的OLED组件最为优异,其ηext为2.8%、ηc为2.5cd/A、ηp为1.3lm/w及Lmax为6530cd/m2。
此外,从量测到的数据能看出,使用单一掺杂物发光层的实验组4的OLED组件的ηext、ηc及ηp也优于使用单一掺杂物发光层的控制组1的OLED组件;而且,也优于使用单一掺杂物发光层的控制组2的OLED。
还有,所制成的蓝色荧光OLED组件也经过基于起始亮度为1,000cd/cm2的寿命评估测试,寿命评估测试的结果显示,实验组4的OLED组件的半衰寿命(LT50)为930小时,而控制组2的蓝色荧光OLED组件之半衰寿命则仅有902小时。
经由以上的说明可知,本发明的咪唑融合螺顺式二苯乙烯/芴化合物及其衍生物已可完全地被引进用于OLED材料,且本发明的材料具有以下优点:
(1)本发明的咪唑融合螺顺式二苯乙烯/芴化合物具有介于143至185℃之间的玻璃转移温度、以及介于429至474℃之间热裂解温度。
(2)多项实验数据证明,本发明的咪唑融合螺顺式二苯乙烯/芴化合物的确能被使用作为OLED的发光层主体材料、发光层的掺杂物、或是电洞传输型的发光层的材料,且由实验数据可知,所制成的OLED,其外部量子效率(ηext)、电流效率(ηc)、功率效率(ηp)、最大亮度(Lmax)及组件寿命,皆优于习知或已商业化的OLED。
虽然本发明已将较佳实施例揭露如上,但其并非用以限定本发明,任何熟知本领域的技术人员,在不脱离本发明的精神和范围内,可作更动与润饰。因此本发明的保护范围以后附的权利要求保护的范围为准。本案由熟悉本领域的技术人员所作的各种修饰,皆不脱离所附的权利要求的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!