一种芳基腈化合物的合成方法与流程
本发明属于医药化工中间体合成技术领域,涉及一种芳基腈类化合物的合成方法。
背景技术:
芳基腈类化合物不但是医药、农药、染料、功能材料、香料和天然产物等重要结构组成部分,而且也是有机合成重要的中间体。在一定的反应条件下芳基腈化合物可以很容易的转化为其它化合物,如醛、酮、羧酸、胺、酰胺和杂环衍生物等。制备芳基腈化合物的方法有很多种,其中sandmeyerreaction和rosemund-vonbraunreaction是合成芳腈的经典方法,然而,上述两种方法都需要化学计量的氰化亚铜(cucn)以及苛刻的反应条件(150–250℃)。工业中制备芳腈类化合物是利用氨氧化法。其反应条件苛刻,需要高温、高压、过量的氨,对设备要求比较高,这些弊端也大大限制其在工业上的应用。
过渡金属催化的n-氰基-n-苯基-p-苯磺酰胺(ncts)制备芳基腈由于具有非常高的反应活性,并且ncts作为一种低毒,易制备且容易保存的氰基试剂,引起了科学家们的广泛关注。其中主要是贵金属催化反应。
(1)rh催化氰基化
2013年,anbarasan课题组报道了以金属铑为催化剂的直接氰基化反应,其使用的定位基团有吡啶,喹啉,吡嗪,嘧啶等[参见:chaitanyam,anbarasanp.organicletters.2013,15:4960-4963.]。
(2)ru催化氰基化
2014年,ackermann小组首次报道了以一种廉价的金属钌为催化剂的直接氰基化反应[参见:liuw.;ackermannl.chemicalcommunications.2014,50:1878-1881.]。
技术实现要素:
本发明的目的是提供一种廉价金属锰催化、步骤简单、原料易得、反应条件温的合成芳基腈类化合物的新方法。
一种芳基腈化合物的合成方法,步骤如下:以2-苯基吡啶衍生物和n-氰基-n-对甲氧基苯基-p-苯磺酰胺为原料,以锰盐为催化剂,在溶剂中加热反应,合成一系列芳基腈化合物,反应式如下:
式中:r1为烷基、三氟甲基或芳基;
r2为烷基、烷氧基、卤素或芳基;
所述的锰盐选自氯化锰、醋酸锰、溴化锰、乙酰丙酮锰、十羰基二锰、五羰基溴化锰,锰盐加入量为2-苯基吡啶衍生物的1-5mol%;
所述的n-氰基-n-对甲氧基苯基-p-苯磺酰胺加入量为2-苯基吡啶衍生物的100-200mol%;
所述的溶剂为甲苯、1,4-二氧六环、n,n-二甲基甲酰胺、乙醇、二氯甲烷、乙醚、四氢呋喃、丙酮中的一种或两种以上混合,溶剂的加入量为2-苯基吡啶重量的10~100倍;
反应温度为25~100℃。
本发明的有益效果是:芳基腈类化合物是许多药物和生物活性分子的重要组成部分,在有机合成及药物化学等领域有着重要的应用,具有广阔的市场前景。本项目涉及一种芳基腈类化合物的合成方法,该方法以2-苯基吡啶衍生物和n-氰基-n-对甲氧基苯基-p-苯磺酰胺为原料,以锰盐为催化剂,合成一系列芳基腈化合物。该发明专利方法步骤简单、原料易得、反应条件温和等优点。本发明具有较大的使用价值和社会经济效益。
附图说明
图1为化合物1a的1h-nmr谱图。
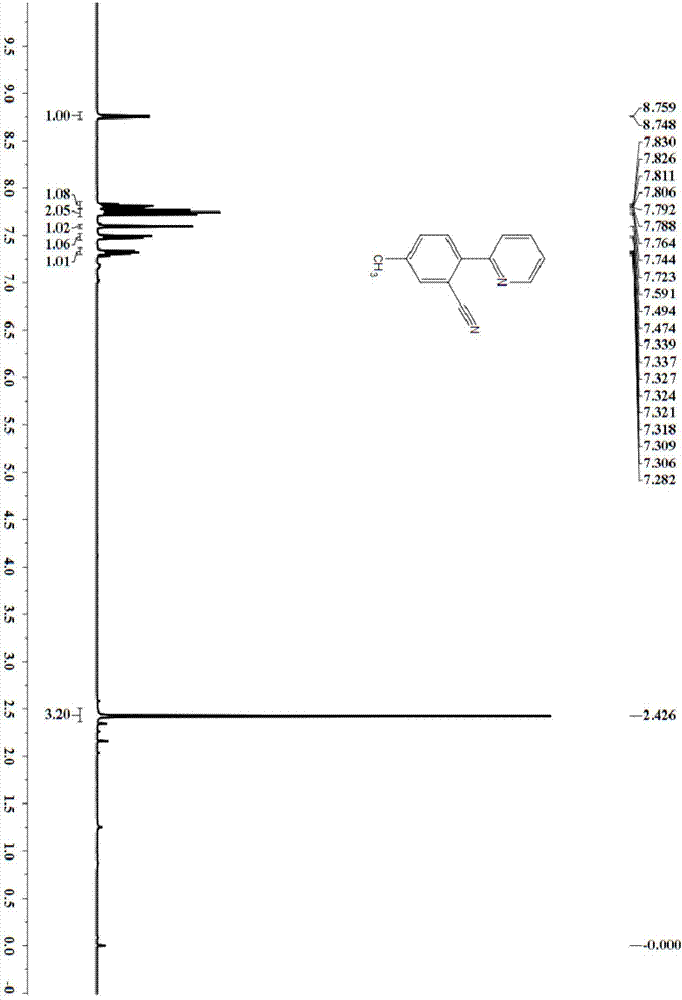
图2为化合物1b的1h-nmr谱图。
图3为化合物1c的1h-nmr谱图。
图4为化合物1d的1h-nmr谱图。
图5为化合物1e的1h-nmr谱图。
图6为化合物1f的1h-nmr谱图。
图7为化合物1g的1h-nmr谱图。
图8为化合物1h的1h-nmr谱图。
具体实施方式
以下结合附图和技术方案,进一步说明本发明的具体实施方式。
实施例1:2-(2-吡啶基)苯甲腈(1a)的合成
称取2-苯基吡啶(53.7mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(181.2mg,0.6mmol)和乙酰丙酮锰(3.6mg,0.01mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入甲苯(2.7ml),并置于25℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为89%。1hnmr(cdcl3,400mhz):δ8.78(d,j=4.8,1h),7.87-7.78(m,4h),7.70(dd,j=7.6,1h),7.53-7.49(m,1h),7.38-7.35(m,1h).
实施例2:5-甲基-(2-吡啶基)苯甲腈(1b)的合成
称取2-(4-甲基苯基)吡啶(58.2mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(151.1mg,0.5mmol)和氯化锰(1.9mg,0.015mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入乙醚(1.1ml),并置于50℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为93%。1hnmr(400mhz,cdcl3):δ8.76(d,j=4.4,1h),7.83-7.79(m,1h),7.74(dd,j=8.0,2h),7.59(s,1h),7.48(d,j=8.0,1h).
实施例3:5-甲氧基-(2-吡啶基)苯甲腈(1c)的合成
称取2-(4-甲氧基苯基)吡啶(63.1mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(135.9mg,0.45mmol)和溴化锰(3.2mg,0.015mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入n,n-二甲基甲酰胺(2.5ml),并置于70℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为95%。1hnmr(400mhz,cdcl3):δ8.75(d,j=4.8hz,1h),7.83-7.74(m,3h),7.32(dd,j=6.4,5.6hz,1h),7.27(s,1h),7.22(d,j=8.0hz,1h),3.89(s,3h).
实施例4:5-氟-(2-吡啶基)苯甲腈(1d)的合成
称取2-(对氟苯基)吡啶(59.4mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(90.6mg,0.3mmol)和五羰基溴化锰(0.9mg,0.003mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入二氯甲烷(5.9ml),并置于80℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为89%。1hnmr(cdcl3,400mhz):δ8.77(d,j=4.8hz,1h),7.85(dt,j=7.6,5.5hz,2h),7.77(d,j=8.0hz,1h),7.50(dd,j=8.0,2.8hz,1h),7.42-7.35(m,2h).
实施例5:5-氯-(2-吡啶基)苯甲腈(1e)的合成
称取2-(对氯苯基)吡啶(64.2mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(135.9mg,0.45mmol)和溴化锰(3.2mg,0.015mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入乙醇(4.5ml),并置于100℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为87%。1hnmr(cdcl3,400mhz):δ8.78(d,j=4.8hz,1h),7.87-7.77(m,4h),7.66(dd,j=8.4,2.0hz,1h),7.39-7.36(m,1h).
实施例6:2-(3-甲基-2-吡啶基)苯甲腈(1f)的合成
称取3-甲基-2-苯基吡啶(58.2mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(120.8mg,0.4mmol)和十羰基二锰(2.4mg,0.006mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入四氢呋喃(1.7ml),并置于40℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为92%。白色固体,yield;1hnmr(cdcl3,400mhz):δ8.56(dd,j=4.8hz,1h),7.77(d,j=7.6hz,1h),7.69–7.64(m,2h),7.50(dd,j=6.8hz,2h),7.28(dd,j=8.0,4.8hz,1h),2.26(s,3h)
实施例7:2-(5-甲基-2-吡啶基)苯甲腈(1g)的合成
称取5-三氟甲基-2-苯基吡啶(74.4mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(90.6mg,0.3mmol)和五羰基溴化锰(0.9mg,0.003mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入丙酮(15ml),并置于60℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为85%。1hnmr(cdcl3,400mhz):δ9.04(s,1h),8.09(dd,j=8.0,2.0hz,1h),7.93(d,j=8.4hz,1h),7.95(dd,j=14.8,8.0hz,2h),7.76-7.72(m,1h),7.60-7.56(m,1h).
实施例8:2-(1-异喹啉)苯甲腈(1h)的合成
称取1-苯基异喹啉(69.1mg,0.3mmol)、n-氰基-n-对甲氧基苯基-p-苯磺酰胺(151.1mg,0.5mmol)、醋酸锰(1.6mg,0.009mmol)和吗啉(0.5mg,0.006mmol),并依次加入到25ml的schlenk反应瓶中,然后,加入1,4-二氧六环(4.1ml),并置于90℃油浴中反应12h。反应结束后,减压除去溶剂,使用石油醚/乙酸乙酯作为洗脱剂,硅胶柱分离,收率为83%。1hnmr(cdcl3,400mhz):δ8.66(d,j=5.6hz,1h),7.91(d,j=8.4hz,1h),7.86(d,j=7.6hz,1h),7.75-7.71(m,4h),7.65(d,j=7.6hz,1h),7.60-7.55(m,2h)。
- 还没有人留言评论。精彩留言会获得点赞!