羧酸盐为有机配体合成金属有机骨架材料MIL‑101‑Cr的方法及其纯化方法与流程
本发明属于金属有机骨架材料合成技术领域,具体涉及一种羧酸盐为有机配体合成金属有机骨架材料mil-101-cr的方法及其纯化方法。
背景技术:
金属有机骨架材料(mofs)是由金属或金属簇与有机配体杂化形成一维、二维或者三维的多孔材料。mofs材料具有有序可调而且尺寸范围较广的孔结构,这些特殊的结构性质使它具有较高的比表面积和较大的孔体积。但是大多数mofs材料的水热稳定性较低,限制了其应用,而mil-101-cr在350℃高温下依然保持良好的热稳定性,而且mil-101-cr还具有其它mofs材料所无法比拟的特征,比如拥有非常大的比表面积(slangmuir=4500-5500m2·g-1)和晶胞体积(702nm3),含有三种类型的孔,微孔(0.96nm)和两种中孔(2.9nm和3.4nm),还具有大量的不饱和金属铬位(理论上能够达到大约3mmol·g-1),这些优异的性能使得mil-101-cr成为当下的热点材料。
mil-101-cr优异的独特性能,引起了研究者广泛的关注,研究者们致力于寻求一种结晶度高,收率高,比表面积大,纯化处理简单、绿色环保的mil-101-cr合成新方法。目前mil-101-cr的合成方法有很多,以水热法为主,水热法成本低,操作简单,易于合成。
两步水热合成mil-101-cr及其纯化方法如下:
水热合成过程:第一步,取2.0g九水合硝酸铬、0.82g的对苯二甲酸和35μl乙酸于50ml的去离子水中充分均匀搅拌,移入聚四氟乙烯材质的反应釜内;并于180℃下晶化12h后,冷却至室温。第二步,向上述反应液中添加0.3g无水乙酸钠和10ml无水乙醇,搅拌后密封,再次于180℃下晶化12h后冷却至室温。过滤、水洗、烘干后得到绿色晶体mil1。
纯化过程:(1)热醇法,将mil1(1g)搅拌分散于70ml无水乙醇溶液中,将混合溶液移入高压反应釜中,置于100℃下恒温12h后冷却至室温,抽滤洗涤干燥后得到mil2。(2)氟化铵溶液法,将mil2(1g)均匀分散在150ml的30mmol·l-1的nh4f溶液中,60℃搅拌10h,并用60℃热水进行洗涤、过滤、烘干后得到样品mil3。
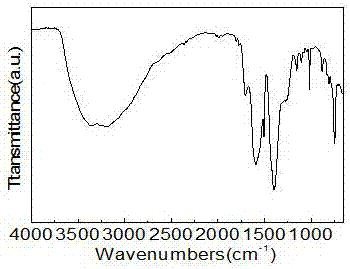
图1所示为两步水热合成mil-101-cr纯化前mil1的xrd图,图2所示为两步水热合成mil-101-cr纯化前mil1的ft-ir图。从图1的xrd图可以看出,主要特征峰(2θ)在2.9°、3.4°、5.2°、8.5°和9.1°处为mil-101-cr晶体的特征峰。图2红外谱图在1510cm-1和1406cm-1处为骨架中-(o-c-o)-的伸缩振动吸收峰,图1和图2证明两步水热法合成了mil-101-cr。但是在图1的17.5°和图2的1700cm-1处出峰说明样品中存在对苯二甲酸。
图3所示为mil1的吸脱附等温线图,图4所示为mil1的孔径分析图。图3的吸脱附等温线图可以看出相对压力p/p0=0.1~0.3之间出现两个台阶,这是mil-101-cr氮气吸附等温线的典型特征,但是在图4的孔径分析图中看出,mil1只出现两个介孔,而mil-101-cr特有的微孔并未出现。这是由于对苯二甲酸难溶于水,在水中去质子化过程较为缓慢,未反应的对苯二甲酸分子在mil-101-cr形成过程中被包裹在微孔中,堵塞其孔道。缺少微孔的mil-101-cr产品将大大降低其在吸附分离领域的作用。针对堵塞在微孔中的对苯二甲酸,采用热乙醇和氟化铵溶液对mil1样品进行纯化处理,制得mil3。
图5为mil-101-cr纯化前后氮吸附对比图,图6为mil-101-cr纯化前后氮吸附对数坐标对比图,图7为mil-101-cr纯化前后孔径分析对比图。由图5可以看出mil3比mil1在相同压力下吸附量增加了,bet比表面积也从纯化前的3150m2·g-1提高到纯化后的3862m2·g-1。图6可以清晰看出mil3在低压区的吸附量急剧上升,说明mil3的微孔非常发达。图7孔径分析图上清晰显示,mil3的微孔已经显露出来,说明热乙醇和氟化铵溶液能够将微孔中的对苯二甲酸去除干净,制得结构性能优异的mil-101-cr产品。
但是未反应的对苯二甲酸堵塞在狭窄的微孔中,使得mil-101-cr纯化过程较为复杂。热乙醇和氟化铵溶液可以有效去除堵塞物对苯二甲酸,但是条件非常苛刻,处理起来相当困难,而且纯化工艺流程较长,样品损失非常严重,非常不利于mil-101-cr的批量化生产。
技术实现要素:
本发明要解决的技术问题是提供一种羧酸盐为有机配体合成金属有机骨架材料mil-101-cr的方法及其纯化方法,缩减反应流程,得到比较纯净、结晶度高、比表面积大、收率高的mil-101-cr。
为解决上述技术问题,本发明的实施例提供一种羧酸盐为有机配体合成金属有机骨架材料mil-101-cr的方法,包括如下步骤:
(1)对苯二甲酸盐的制备:将碱溶液缓慢滴加至溶有对苯二甲酸的二甲基甲酰胺溶液中,得到白色粉末,二甲基甲酰胺和水等体积的混合溶液对白色粉末进行重结晶,制得对苯二甲酸盐晶体;
(2)样品的合成:取摩尔比为0.8~1.2:1的九水合硝酸铬和对苯二甲酸氢钾,用乙酸调节至体系ph值为3~4后,溶解于与九水合硝酸铬的摩尔比为400~800的去离子水中充分搅拌均匀,移入聚四氟乙烯材质的反应釜内,置于150~180℃下晶化18~30h,自然冷却至室温,水洗、抽滤、烘干后得到绿色晶体样品mil-101-cr-1。
其中,步骤(1)中的对苯二甲酸盐为对苯二甲酸钾、对苯二甲酸钠、对苯二甲酸氢钾、对苯二甲酸氢钠、对苯二甲酸氢胺,对苯二甲酸胺中的一种或多种混合。
优选地,步骤(1)中的对苯二甲酸盐为对苯二甲酸氢钾,其制备方法为:将氢氧化钾溶液缓慢滴加至溶有对苯二甲酸的二甲基甲酰胺(dmf)溶液中,得到白色粉末,二甲基甲酰胺(dmf)和水等体积的混合溶液对白色粉末进行重结晶,制得对苯二甲酸氢钾晶体。
进一步,步骤(1)中,氢氧化钾和对苯二甲酸的摩尔比为0.9~1.1:1。
本发明中,mil-101-cr晶体的生成过程包括晶核形成和晶体成长两个阶段,成核的关键是次级结构单元(sbus)的形成,sbus是由六水合三价铬离子[cr(h2o)6]3+和部分去质子化的对苯二甲酸根配位形成。六水合三价铬离子由可溶性的铬盐提供,对苯二甲酸氢钾可直接提供部分去质子化的对苯二甲酸根。对苯二甲酸氢钾在水中的溶解度要比对苯二甲酸大,可解决合成过程中原料溶解度低堵塞微孔的问题,因此采用对苯二甲酸氢钾和九水硝酸铬为原料水热合成mil-101-cr。
其中,样品相对结晶度rc由下式计算:
其中,s为基准样品;j为基准样品之外的样品;i为xrd图谱中特征峰的绝对强度。
本发明实施例还提供一种羧酸盐为有机配体合成金属有机骨架材料mil-101-cr的纯化方法,首先利用热醇法,将1g绿色晶体样品mil-101-cr-1搅拌分散于50~70ml无水乙醇溶液中,将混合溶液移入高压反应釜中,置于100℃下恒温6~12h后冷却至室温,抽滤、洗涤、干燥后得到样品,然后将1g样品搅拌分散于30~50ml的二甲基甲酰胺溶液中,混合溶液放入250ml的平底烧瓶中,150℃油域中搅拌8~12h,并用热水洗涤、抽滤、烘干后得到样品mil-101-cr-2。
本发明的上述技术方案的有益效果如下:本发明采用对苯二甲酸氢钾为有机配体原料水热合成mil-101-cr,得到的样品结晶度较高、晶形完美、收率高、后处理步骤较少。对苯二甲酸氢钾在水中去质子化速度较快,对苯二甲酸根在水中的溶度变高,而使得样品在结晶过程中,形成尺寸在60nm左右且较为均匀的晶体颗粒。这些小尺寸的mil-101-cr晶体在膜、催化和分离方面的应用广泛。对苯二甲酸氢钾为有机配体水热合成的mil-101-cr解决了常规水热合成法中对苯二甲酸堵塞微孔的问题,经过简单纯化就可得到比较纯净的样品,而且反应温度低为160℃,收率接近70%,非常利于mil-101-cr的批量化生产。
附图说明
图1为本发明背景技术中两步水热合成mil-101-cr纯化前mil1的xrd图;
图2为本发明背景技术中两步水热合成mil-101-cr纯化前mil1的ft-ir图;
图3为本发明背景技术中mil1的吸脱附等温线图;
图4为本发明背景技术中mil1的孔径分析图;
图5为本发明背景技术中mil-101-cr纯化前后氮吸附对比图;
图6为本发明背景技术中mil-101-cr纯化前后氮吸附对数坐标对比图;
图7为本发明背景技术中mil-101-cr纯化前后孔径分析对比图;
图8为本发明实施例中样品mil-101-cr-1的xrd谱图;
图9为本发明实施例中样品mil-101-cr-1的ft-ir谱图;
图10为本发明实施例中样品mil-101-cr-1与背景技术中的mil3晶体的sem比较图;
图11为本发明实施例中样品mil-101-cr-1的tem图;
图12为本发明实施例中样品mil-101-cr-1的吸脱附等温线图;
图13为本发明实施例中样品mil-101-cr-1的孔径分析图;
图14为本发明实施例中样品mil-101-cr-2的吸脱附等温线图;
图15为本发明实施例中样品mil-101-cr-2的孔径分析图。
具体实施方式
为使本发明要解决的技术问题、技术方案和优点更加清楚,下面将结合附图及具体实施例进行详细描述。
一种羧酸盐为有机配体合成金属有机骨架材料mil-101-cr的方法及其纯化方法,包括如下步骤:
(1)对苯二甲酸盐的制备:将碱溶液缓慢滴加至溶有对苯二甲酸的二甲基甲酰胺(dmf)溶液中,得到白色粉末,二甲基甲酰胺(dmf)和水等体积的混合溶液对白色粉末进行重结晶,制得对苯二甲酸盐晶体;
其中,对苯二甲酸盐优选对苯二甲酸氢钾,其制备方法为:将氢氧化钾溶液缓慢滴加至溶有对苯二甲酸的二甲基甲酰胺(dmf)溶液中,得到白色粉末,二甲基甲酰胺(dmf)和水等体积的混合溶液对白色粉末进行重结晶,制得对苯二甲酸氢钾晶体。
氢氧化钾和对苯二甲酸的摩尔比为1:1。
(2)样品的合成:取摩尔比为0.8~1.2:1的九水合硝酸铬和对苯二甲酸氢钾,用乙酸调节至体系ph值为3~4后,溶解于与九水合硝酸铬的摩尔比为400~800的去离子水中充分搅拌均匀,移入聚四氟乙烯材质的反应釜内,置于150~180℃下晶化18~30h,自然冷却至室温,水洗、抽滤、烘干后得到绿色晶体样品mil-101-cr-1。
(3)样品的纯化:首先利用热醇法,将1g绿色晶体样品mil-101-cr-1搅拌分散于50~70ml无水乙醇溶液中,将混合溶液移入高压反应釜中,置于100℃下恒温6~12h后冷却至室温,抽滤、洗涤、干燥后得到样品,然后将1g样品搅拌分散于30~50ml的二甲基甲酰胺溶液中,混合溶液放入250ml的平底烧瓶中,150℃油域中搅拌8~12h,并用热水洗涤、抽滤、烘干后得到样品mil-101-cr-2。
样品相对结晶度rc由下式计算:
其中,s为基准样品;j为基准样品之外的样品;i为xrd图谱中特征峰的绝对强度。
本发明中,mil-101-cr晶体的生成过程包括晶核形成和晶体成长两个阶段,成核的关键是次级结构单元(sbus)的形成,sbus是由六水合三价铬离子[cr(h2o)6]3+和部分去质子化的对苯二甲酸根配位形成。六水合三价铬离子由可溶性的铬盐提供,对苯二甲酸氢钾可直接提供部分去质子化的对苯二甲酸根。对苯二甲酸氢钾在水中的溶解度要比对苯二甲酸大,可解决合成过程中原料溶解度低堵塞微孔的问题,因此采用对苯二甲酸氢钾和九水硝酸铬为原料水热合成mil-101-cr。
具体实施例:实验原料配比对苯二甲酸氢钾:九水硝酸铬=1:1(摩尔比),这是合成mil-101-cr中有机配体与金属离子最佳配比。选取醋酸作为矿化剂,拥有单齿配体的醋酸可以诱导双齿配体的对苯二甲酸根与金属离子进行配位,利于晶体的成核。醋酸还可调节溶液的ph值,ph为3~4时利于mil-101-cr的形成。
温度是水热反应非常关键的因素,选择温度为140℃、160℃和180℃反应12h,如下表1所示。发现140℃温度过低,除了对苯二甲酸重结晶体未产生任何固体;180℃温度过高,产生的固体经检测为不定型物质。
表1不同温度下反应12h的样品
水热合成mil-101-cr过程中反应物的浓度影响晶体的成核,水作为溶剂介质,可溶解反应物也可参与到mil-101-cr的次级结构单元sbus的形成过程中。因此,水与金属铬离子的摩尔比(h2o/cr3+)和反应时间作为影响晶体结晶度的变量,如下表2。
表2160℃温度下不同反应时间、水与铬离子不同摩尔比的样品结晶度rc
注:结晶度rc值是以样品mil3为基准样计算。
由表2可知,反应温度为160℃条件下,反应时间为24h,h2o/cr3+为600时样品的结晶度最高。对苯二甲酸氢钾为有机配体原料水热合成mil-101-cr的最佳条件是160℃反应温度和24h反应时间,水与金属离子的摩尔比为600,经计算样品的收率高达70%。
对苯二甲酸氢钾为有机配体原料水热合成mil-101-cr的表征结果如图8-图15所示,其中,图8为样品mil-101-cr-1的xrd谱图,图9为样品mil-101-cr-1的ft-ir谱图,图10为样品mil-101-cr-1与mil3晶体的sem比较图,图11为样品mil-101-cr-1的tem图,图12为样品mil-101-cr-1的吸脱附等温线图,图13为样品mil-101-cr-1的孔径分析图,图14为样品mil-101-cr-2的吸脱附等温线图,图15为样品mil-101-cr-2的孔径分析图。
从图8所示的样品mil-101-cr-1的xrd图可以看出,样品mil-101-cr-1在mil-101-cr的主要特征峰(2θ)位置2.9º、3.4º、5.2º、8.5º和9.1º均有出峰,说明所合成的样品是目标产物,并以mil3为基准样,计算出样品mil-101-cr-1的相对结晶度rc为84%。图9的样品mil-101-cr-1的ft-ir谱图在1510cm-1和1406cm-1处为骨架中-(o-c-o)-的伸缩振动吸收峰,3443cm-1和1625cm-1处的吸收峰对应骨架中残留的自由水分子。但是样品mil-101-cr-1在图8的17.5°处和图9的1700cm-1处出峰说明有对苯二甲酸存在,这是因为水在反应过程中会电离出h+和oh-离子,oh-参与到mil-101-cr的次级结构单元sbus的形成过程中,使得溶液中含有h+,而对苯二甲酸氢钾溶解在水中主要以对苯二甲酸根形式存在,在反应完降温过程中,h+和对苯二甲酸根离子会结合重结晶为对苯二甲酸晶体,使得样品mil-101-cr-1中存在对苯二甲酸晶体。
从图10和图11可以看出,样品的颗粒较小,尺寸仅有60nm左右,这是由于对苯二甲酸氢钾的溶解度较大,使得对苯二甲酸根在水中的溶度变高,晶体在生长过程中,成核速率大于生长速率,导致晶体小而多。常规水热法合成的mil-101-cr晶体尺寸均大于100nm,有些能够达到500nm,颗粒尺寸为50nm左右的晶体需要微波辅助或者加入模板剂。本实验以对苯二甲酸氢钾为有机配体,采用较低温度的常规水热法即合成尺寸为60nm的mil-101-cr小晶体,开创了小颗粒样品合成的新方法。常规水热法和微波辅助法合成mil-101-cr的颗粒尺寸的对比如下表3。
表3常规水热法和微波辅助法合成mil-101-cr的颗粒尺寸的对比
从图12所示的样品mil-101-cr-1的吸附等温线图看出,该型等温线在低压区为ⅰ型等温线,吸附量急剧上升,在p/p0=0.1~0.3之间有两个台阶,这是mil-101-cr的典型特征。在高压区出现脱附滞后环,这是因为样品颗粒较小出现团聚,颗粒与颗粒之间出现大的缝隙孔,而导致脱附滞后出现。由吸附等温线计算出样品mil-101-cr-1的bet比表面积sbet=2630m2·g-1。图13的nldft全孔分析图可以看出样品mil-101-cr-1的微孔非常发达,说明样品mil-101-cr-1的微孔并未被堵塞,也验证了该方法彻底解决了对苯二甲酸堵塞微孔的问题。但是图12的样品mil-101-cr-1吸脱附等温线在p/p0=0.2处的台阶上升趋势并不明显,图13孔径分析图在3.4nm处出峰不明显,说明3.4nm的中孔中可能存在对苯二甲酸重结晶体。
针对mil-101-cr中孔中可能存在的对苯二甲酸重结晶体,采用热乙醇和dmf溶液进行简单的处理,比较处理前后孔结构的变化。纯化后的样品mil-101-cr-2的微结构表征如图14和图15。
图14的样品mil-101-cr-2的吸脱附等温线图显示,经过乙醇和dmf简单处理的样品mil-101-cr-2的两个台阶已经显现出来,纯化后的样品mil-101-cr-2吸附量得到提升,根据吸附等温线计算样品mil-101-cr-2的bet比表面积sbet=2837m2·g-1。从图15的微结构表征可以看出,经过热乙醇和dmf简单处理,样品mil-101-cr-2三种类型的孔均显现出来。与常规水热法的纯化条件较为苛刻相比,对苯二甲酸氢钾为有机配体的新合成方法的纯化方法较为简单,这主要是因为对苯二甲酸重结晶体残留在较大的中孔中易于除去。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!