一种H7N9禽流感病毒奥司他韦敏感或耐药基因型的检测试剂盒及检测方法与流程
(一)技术领域
本发明涉及一组检测h7n9禽流感病毒奥司他韦耐药性突变基因型的方法及其应用。
(二)
背景技术:
流感(流行性感冒)是由流感病毒引起的一种人、禽、畜共患的急性传染病,其发病率、死亡率和造成的经济损失位居各传染病之首。以往感染人的禽流感病毒亚型主要为h5n1、h9n2、h7n7,其中感染h5n1的患者病情重,病死率高。以前已经报道的人感染h7亚型的禽流感病毒的有h7n2、h7n3和h7n7,引起人的呼吸道感染和结膜炎等症状,在荷兰、美国、英国等国家共造成100多例感染,其中1例死亡。2013年3月,我国上海、江苏、安徽、浙江等地出现人感染h7n9禽流感病例,这是全球首次发现人感染h7n9禽流感,是由来自于h9n2内部蛋白基因、h7血凝素基因和n9神经氨酸酶基因等禽源流感病毒基因片段重配形成的一个新病毒所致。自此,由h7n9禽流感病毒感染造成的疫情持续在我国发生。
目前临床上使用两类抗流感病毒的药物,一类是干扰病毒m2蛋白功能的药物,即金刚烷胺类药物。金刚烷胺类药物用于预防和治疗a型流感病毒感染,但随着多年使用已经产生大量耐药,a型流感病毒中m蛋白普遍存在的s31n耐药突变已使金刚烷胺类失去临床价值。另一类是神经氨酸酶抑制剂(neuraminidaseinhibitor,nai)。与m2通道阻滞剂不同,神经氨酸酶抑制剂可以同时控制a型和b型流感病毒感染。目前批准使用的神经氨酸酶抑制剂主要有扎那米韦(zanamivir)和奥司他韦(oseltamivir)。扎那米韦的口服生物利用度太低,必需经吸入途径给药而直接到达呼吸道感染部位,因此在应用上受到很大限制。另一种唾液酸类似物奥司他韦可以通过口服发挥作用。奥司他韦(商品名:达菲,tamiflu)是一种强效的高选择性的流感病毒na抑制剂。奥司他韦能够竞争性地与流感病毒神经氨酸酶的活动位点结合,抑制病毒的神经氨酸酶而阻止流感病毒侵犯呼吸道细胞,干扰病毒从被感染的宿主细胞中释放。奥司他韦的使用应注意要尽早足量使用,对有发热、明显流感样症状及有接触患者或禽类史者等疑似患者,即使尚未确诊,也应及时使用奥司他韦进行治疗。除了应用于流感的治疗以外,在流行季节还可用于有可疑暴露人员和易感人群的流感预防。迄今也有少数发达国家批准了其它针对神经氨酸酶的药物,但应用非常少。然而,n9亚型流感病毒中第294位由精氨酸突变为赖氨酸(r294k)能使病毒株对奥司他韦表现出了强烈的耐药性。
目前建立了多种利用分子生物学方法检测具有奥司他韦耐药性基因型流感病毒的方法,如单核苷酸多态性分析、滚环扩增技术、sanger测序、二代测序、数字pcr等,但这些方法不仅费时、费力、比较昂贵,而且还会由于实验室、工作人员、操作方法和标本的不同而影响其敏感性和特异性。耐药表型的检测需要在生物安全3级实验室(bsl-3)进行病毒分离和神经氨酸酶活性实验,其实验周期至少一周以上,费时费力,费用昂贵,而且检测难度很高,生物安全风险大。
大多数患者感染来源是农贸市场,因此需要对农贸市场等外环境进行持续监测。此外,对已经确诊的人感染h7n9禽流感患者进行持续的耐药基因型监测也缺乏相应的快速便捷的方法。目前,区分h7n9禽流感病毒奥司他韦敏感或耐药基因型尚没有商品化的试剂盒,然而监测病毒耐药突变情况、监测禽类来源和外环境h7n9禽流感病毒耐药突变情况均有重要意义。
(三)
技术实现要素:
本发明建立h7n9禽流感病毒奥司他韦敏感或耐药基因型鉴别方法,检测成本低廉,可大幅度节省检测费用。所建立的h7n9亚型禽流感病毒双重荧光rt-pcr方法具有特异、敏感、重复性好、快速、费用低廉,一次试验即可完成h7n9亚型禽流感病毒敏感和/或耐药基因型的分型等优点。是n9亚型禽流感病毒奥司他韦敏感或耐药基因型快速筛选与及确认的良好方法。
本发明采用的技术方案是:
本发明提供一种h7n9禽流感病毒奥司他韦敏感或耐药基因型(即r294k突变基因型)的检测试剂盒,所述试剂盒包括rt-pcr或pcr扩增反应液和阳性对照,所述rt-pcr或pcr扩增反应液包括特异性扩增引物和荧光探针,所述特异性扩增引物和荧光探针序列如下;
所述特异性扩增引物序列如下:
r294k-f:5’tgactggaactgctaagcatattga3’;
r294k-r:5’tgtcattgctactggrtctatctga3’;
所述荧光探针序列如下:
k294-pb1:5’fam-cacatgcaaggaca-mgb-nfq3’;
r294-pb2:5’vic-ctgcacatgcaggg-mgb-nfq3’;
其中,fam和vic均为标记的荧光基团,mgb-nfq为荧光淬灭基团;
阳性对照:h7n9禽流感病毒的奥司他韦敏感型基因和/或耐药基因型dna或rna为模板。
进一步,所述试剂盒由pcr缓冲液、dna聚合酶、脱氧三磷酸核苷混合物、特异性扩增引物、荧光探针、roxtm均一化参比染料、模板和水组成,更优选所述试剂盒组成:2×premixextaq(probeqpcr)12.5μl、引物r294k-f0.4μl、引物r294k-r0.4μl、探针k294k-pb10.2μl、探针r294k-pb20.2μl、roxtm均一化参比染料0.5μl、模板cdna5μl、水补足至25μl。
进一步,所述试剂盒由rt-pcr缓冲液、dna聚合酶、逆转录酶、特异性扩增引物、荧光探针、roxtm均一化参比染料、模板和水组成,更优选所述试剂盒由2×buffer12.5μl、引物r294k-f0.4μl、引物r294k-r0.4μl、探针k294k-pb10.2μl、探针r294k-pb20.2μl、roxtm均一化参比染料0.5μl、taq酶0.5μl、逆转录酶0.5μl、模板病毒rna5μl、水补足至25μl。
本发明还提供一种所述h7n9禽流感病毒奥司他韦敏感或耐药基因型的检测试剂盒的检测方法,所述检测方法为:以待测样品rna或cdna为模板,利用所述的试剂盒进行rt-pcr或pcr扩增,若扩增产物fam荧光扩增曲线的ct<38,则待测病毒为奥司他韦耐药基因型;若扩增产物vic荧光扩增曲线的ct<38,则待测病毒为奥司他韦敏感基因型;若两种荧光扩增曲线同为ct<38,则待测病毒为奥司他韦耐药基因型与敏感基因型混合。
进一步,所述pcr反应程序如下:60℃1min;94℃1min;94℃15s,55℃~60℃(优选58.5℃)1min,读取荧光,循环40次;60℃1min。
本发明试剂盒同样适用其它n9亚型流感病毒。
与现有技术相比,本发明有益效果主要体现在:本发明所述h7n9禽流感病毒的奥司他韦敏感或耐药基因型的检测试剂盒具有特异、敏感、重复性好、快速、费用低廉,一次试验即可完成h7n9亚型禽流感病毒敏感和/或耐药基因型的检测等优点。克服了现有测序方法耗时长,成本高,敏感性低等缺点。表型检测实验周期至少一周以上,费时费力,费用昂贵,而且检测难度很高,生物安全风险大。
(四)附图说明
图1为na基因pcr产物琼脂糖凝胶电泳分析结果;1:pcr产物;m:dl2000dnamarker。
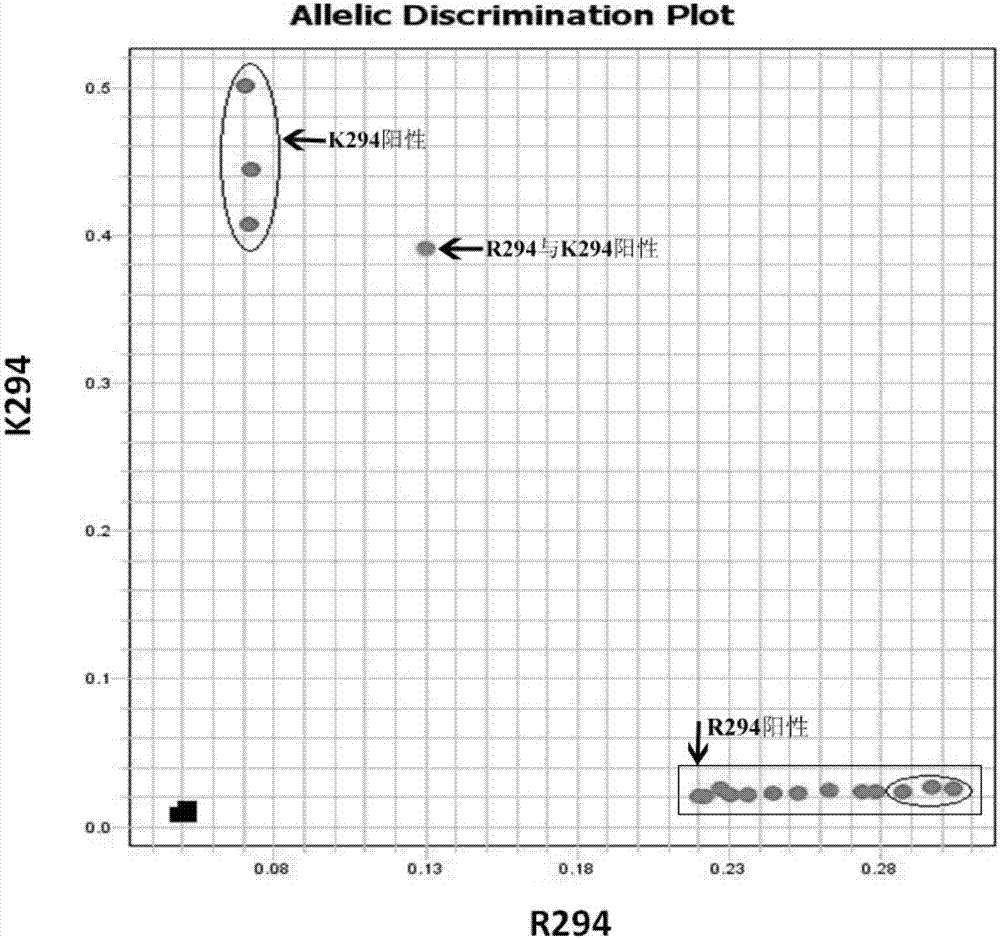
图2为h7n9禽流感病毒奥司他韦敏感基因型或耐药基因型快速鉴定图。r294阳性(vic荧光)包括患者临床样本cdna和3份含r294基因的质粒dna对照(椭圆圈中);k294阳性(fam荧光)包括3份含k294基因的质粒dna对照(椭圆圈中);r294和k294均阳性的为临床样本a/zhejiang/s30/2013(h7n9);3份阴性对照。
图3为奥司他韦敏感基因型与耐药基因型的敏感性检测结果;a为pgem-teasy-r294质粒dna,b为pgem-teasy-k294质粒dna。
图4为奥司他韦敏感基因型与耐药基因型扩增标准曲线,a为pgem-teasy-r294质粒dna扩增的标准曲线;b为pgem-teasy-k294质粒dna扩增的标准曲线。
图5为奥司他韦敏感基因型与耐药基因型相对敏感性检测,a为r294k基因型检测,b为甲型流感的相对敏感性检测。
图6为双重荧光定量pcr区分奥司他韦敏感基因型与耐药基因型的混合基因型的能力,a到p分别代表r294k模板中k294分子数的含量分别为0%、1%、2%、3%、5%、10%、20%、50%、80%、90%、95%、97%、98%、99%、100%,其中r为pgem-teasy-r294质粒dna,k为pgem-teasy-k294质粒dna。
图7:临床样本中奥司他韦敏感基因型与耐药基因型检测散点图结果,包含2013年51份和2014年早期的23份样本。■:阴性对照;×:未检出;黑色圆圈标记的分别为r294、k294和r294/k294混合的质粒dna标准品的检测结果。
(五)具体实施方式
下面结合具体实施例对本发明进行进一步描述,但本发明的保护范围并不仅限于此:
本发明实施例所用分子生物学操作参照《现代分子生物学(第二版)》。
实施例1:奥司他韦敏感型和r294k变异耐药型的na基因质粒构建
rt-pcr扩增h7n9禽流感病毒na基因片段:以-70℃保存的a/zhejiang/22/2013(h7n9)标本的rna为模板,以n9na-f:atgaatccaaatcagaagattc
和n9na-r:ttagaggaagtactctattttag为引物,反应体系见表1。
表1、na基因扩增rt-pcr反应体系
rt-pcr程序如下:42℃30min;94℃2min;94℃15s,55℃30s,68℃2min,循环40次;68℃10min。配制1.5%的琼脂糖凝胶,取扩增产物进行凝胶电泳,根据dna分子量标准判断扩增条带大小是否正确。选取约1.4kb的特异性扩增条带,用琼脂糖凝胶回收试剂盒(invitrogen)纯化目的条带。割胶纯化后利用pgem-teasy载体克隆试剂盒(promega)与载体连接并转化大肠杆菌dh5α感受态细胞,测序正确后,再按照定点突变试剂盒(takara)的说明设计引物,进行定点突变(将294位r突变为k)并测序验证,分别构建含pgem-teasy-r294基因(敏感型)的dna质粒和含pgem-teasy-k294基因(耐药型)的dna质粒。
实施例2:快速鉴定h7n9禽流感病毒r294k突变基因型的方法
1、设计双重荧光定量方法检测敏感基因型与耐药基因型的引物和探针
下载有代表性的h7n9禽流感病毒na序列,用primerexpress3.0设计2条特异性扩增引物以及2条分别标记不同荧光染料的探针。
所述特异性扩增引物序列如下:
r294k-f:5’tgactggaactgctaagcatattga3’;
r294k-r:5’tgtcattgctactggrtctatctga3’;
该引物与h7n9禽流感病毒神经氨酸酶294位点编码序列两端互补;
标记不同荧光染料的探针:
k294-pb1:5’fam-cacatgcaaggaca-mgb-nfq3’;
r294-pb2:5’vic-ctgcacatgcaggg-mgb-nfq3’。
探针的5’端分别标记荧光基团fam和vic,3’端标记荧光淬灭基团mgb-nfq,突变位点位于探针的近3’端。
2、快速鉴定h7n9禽流感病毒r294k突变基因型的方法
以实施例1构建的含pgem-teasy-r294基因的dna质粒(标准质粒)和含pgem-teasy-k294基因的dna质粒(标准质粒)作为各自基因型的阳性参照,以2013年疫情早期的11份h7n9禽流感患者标本的病毒rna的逆转录cdna为模板进行r294k基因型的pcr鉴定(试剂盒组成:2×premixextaq(probeqpcr)(pcr缓冲液、dna聚合酶、脱氧三磷酸核苷混合物(dntp))、特异性扩增引物、荧光探针、roxtm均一化参比染料、cdna或阳性参照、水)。
pcr反应液(以takara荧光定量pcr试剂盒为例)每25μl组成如下:
以appliedbiosystem7500荧光定量pcr仪为例,设置反应程序如下:60℃1min(pre-read);94℃1min;94℃15s,55℃~60℃之间以0.5℃为梯度,分别进行1min退火与扩增并读取收集荧光,循环40次;60℃1min(post-read)。反应结束后,根据扩增曲线判别样本为r294、k294或杂合子,并生成散点图。
实验结果显示,根据ct值范围、扩增曲线、检测敏感性综合判断,最终将退火与扩增温度优化为58.5℃。r294、k294标准质粒和h7n9禽流感标本的扩增生成的散点图见图2。结果表明11份早期的样本中10份为奥司他韦敏感基因型,1份样本为奥司他韦敏感与耐药基因型混合。
实施例3、双重荧光定量rt-pcr快速鉴定h7n9禽流感病毒r294k突变基因型方法的特异性
以h1n1pdm09流感病毒、h3n2流感病毒、h5n1禽流感病毒、h9n2禽流感病毒、乙型流感病毒flub和人感染h7n9禽流感毒株,记为a/zhejiang/s30/2013(h7n9)(同时包含奥司他韦敏感与耐药基因型)的病毒rna为模板,采用takara一步法荧光定量rt-pcr试剂盒进行扩增。
上述病毒样品rna提取可按常规方法进行,如采用qiagenrneasyminikit或其它试剂盒所提取。
本发明中,所述样品rna的提取步骤可为:
1)离心管中加入500μlrlt和6μlβ-巯基乙醇;
2)向上述溶液中加入200μl样本(包括含漱液、咽拭子、呼吸道吸出物等),振荡混匀1min;
3)加入等体积的70%乙醇混匀;
4)取700μl混合液加入收集管内的离心柱中,12000rpm离心15s;
5)重复步骤4一次;
6)加入700μlrw1缓冲液于离心柱中,12000rpm离心15s;
7)加入500μlrpe缓冲液于离心柱中,12000rpm离心15s;
8)重复步骤7一次;
9)倒尽收集管中液体,空离一次;
10)加入适量无rna酶的水溶解rna并离心收集,置于-70℃保存。
所述双重实时荧光定量rt-pcr反应试剂组成(以takara一步法荧光定量rt-pcr试剂盒为例,试剂盒由rt-pcr缓冲液(2×buffer)、dna聚合酶(taq)、逆转录酶、特异性扩增引物、荧光探针、roxtm均一化参比染料、模板(病毒rna)和水组成)和反应程序(以abi7500荧光定量pcr仪为例)为:
rt-pcr反应体系如下:
表2、rt-pcr反应体系
设置反应程序如下:42℃15min;94℃1min;94℃15s,58.5℃1min并读取收集荧光,循环40次。根据反应的曲线分别判别样本的阴阳性,结果见下表:
表3、奥司他韦敏感与耐药基因型检测的特异性
注:“-”表示无,“+”表示有。h7n9std为毒株a/zhejiang/s30/2013(h7n9),ntc为不含r294和k294的灭菌水的阴性对照。
将a/zhejiang/s30/2013(h7n9)的rna为模板的扩增产物利用purelinkquickpcrpurification试剂盒(invitrogen)进行纯化,连接t载体后加入50ul感受态细胞e.colidh5α,轻弹混匀后置于冰上30min。42℃水浴中热击90s后立即置于冰上2min,加入1mlsoc培养基,恒温摇床225rpm,37℃培养1h后8000rpm离心2min,弃上清,加氨苄青霉素抗生素、iptg和x-gal混匀涂lb平板,倒置于恒温培养箱37℃培养过夜。挑取白色细菌单菌落接种至含抗生素的液体lb培养基进行振荡培养。将菌液进行测序,序列分别进行blastn检索,以进一步确认双重荧光定量rt-pcr快速鉴定r294k突变基因型h7n9禽流感病毒奥司他韦敏感或耐药基因型(即r294k突变基因型)的方法的特异性。blastn检索见表4-1和表4-2。根据测序结果,本试剂盒扩增的片段均为n9亚型的目的区域,特异性好。
表4-1、奥司他韦敏感型病毒扩增产物核酸序列blastn检索结果
表4-2、奥司他韦敏感型病毒扩增产物核酸序列blastn检索结果
实施例4、双重荧光定量pcr快速鉴定h7n9禽流感病毒r294k突变基因型方法的敏感性
将实施例1构建的pgem-teasy-r294基因质粒dna和pgem-teasy-k294基因质粒dna,采用nanovue微型光度计(gehealthcare)进行dna定量。每个质粒dna分别检测3次重复,记录质粒dna浓度和a260/a280纯度并计算其平均值,其浓度结果见表5。
表5奥司他韦敏感与耐药基因型质粒dna浓度
根据pgem-teasy-r294基因质粒dna和pgem-teasy-k294基因质粒dna浓度,以及pgem-teasy3015bp和na基因1398bp的分子量,计算每ul质粒dna中的r294和k294的分子数。用tebuffer将pgem-teasy-r294质粒dna和pgem-teasy-k294质粒dna分别稀释至108copies/ul的浓度,并以10倍梯度依次稀释至100copy/ul。以梯度稀释的含有已知分子数的质粒dna为模板,按照实施例2建立的方法进行扩增,根据ct值和扩增曲线判断h7n9禽流感病毒r294k突变基因型检测方法的敏感性。每个浓度重复3次。
通过对每个反应中的r294或k294分子数进行赋值,选取所有浓度点的ct值进行标准曲线制作,横坐标为模板数量,纵坐标ct值。
r294和k294的检测敏感性扩增曲线分别见图3中a(108~102copies均扩增良好,且ct值较好,101copies虽然3条扩增曲线均为阳性,但ct值均在38左右且荧光值低。100copy和阴性对照均为阴性。)和b(108~102copies均扩增良好,且ct值较好,101copies虽然3条扩增曲线均为阳性,但ct值均在38左右且荧光值低。100copy和阴性对照均为阴性。)。r294和k294的扩增标准曲线分别见图4中a(通过对每个反应中的r294分子数进行赋值,选取108copies~100copy各浓度点的ct值进行标准曲线制作)和b(通过对每个反应中的k294分子数进行赋值,选取108copies~100copy各浓度点的ct值进行标准曲线制作)。
r294和k294的检测敏感性分别为102copies/反应。
除了上述的绝对定量评价反应敏感性之外,还利用监测甲型流感(flua)的引物探针对flua和建立的h7n9禽流感病毒r294k突变基因型检测方法进行了不同方法之间的相对敏感性比较。flua的引物探针为who推荐的检测方法,扩增区域位于基质蛋白(m)基因。引物探针序列见表6:
表6甲型流感通用检测引物与探针
将人感染h7n9禽流感毒株a/zhejiang/s30/2013(h7n9)的病毒rna的逆转录产物以10倍梯度进行稀释,此毒株为同时含有奥司他韦敏感与耐药基因型的病毒。以101~108不同稀释度cdna模板,采用takara荧光定量pcr试剂盒进行扩增,同时进行r294k基因型和flua(甲型流感)扩增检测,每个浓度重复3次。
r294k的敏感性扩增曲线和flua的敏感性扩增曲线分别见图5中a(101~105稀释的反应中r294和k294均扩增良好,106稀释后的反应中r294和k294共k294有3条扩增曲线而r294有2条扩增曲线。108倍稀释和阴性对照均为阴性。)和b(101~105稀释的反应中均扩增良好,106和107稀释后的反应中均只有2条扩增曲线。108倍稀释和阴性对照均为阴性)。虽然相同浓度的模板flua扩增的ct值小于r294k扩增的ct值,但在106×稀释的反应中,r294k的r和k均有3条ct<38的扩增曲线,而flua仅有两条。因此但r294k相对敏感性高于flua。
实施例5、双重荧光定量pcr鉴定奥司他韦敏感与耐药混合基因型的能力
根据实施例4不同分子数pgem-teasy-r294基因质粒dna和pgem-teasy-k294基因质粒dna的扩增曲线,均选取104copies/ul浓度的质粒dna,以不同体积的r294和k294质粒dna进行混合,使其中的k294与r294的分子数比值分别为0%、1%、2%、3%、5%、10%、20%、50%、80%、90%、95%、97%、98%、99%、100%,同时以不含r294和k294的灭菌水为ntc对照。按照前述实施例2建立的方法进行扩增,根据ct值和扩增曲线判断h7n9禽流感病毒r294k突变基因型检测方法的敏感性。每个浓度重复4次。
扩增曲线中,以r=0%k=100%曲线中的高于r检测曲线的荧光值为r294检测阈值,以r=100%k=0%曲线中的高于k检测曲线的荧光值为k294检测阈值,判断不同比例混合基因型的检测能力。
双重荧光定量pcr区分奥司他韦敏感与耐药混合基因型的能力的结果分别见图6。当病毒株中含有奥司他韦敏感与耐药混合基因型时,耐药基因型含量>2%时可以检测出两种基因型混合并加以区分,敏感基因型含量>10%时可以检测出两种基因型混合并加以区分。
实施例6、双重荧光定量rt-pcr快速鉴定h7n9禽流感病毒r294k突变基因型的方法在临床标本中的应用
以实施例1构建的分别包含r294、k294基因的质粒dna和同时包含等量r294、k294基因的质粒dna作为阳性参照,以h7n9禽流感患者标本的病毒rna进行逆转录的cdna为模板进行r294k基因型的鉴定。样本为2013年51份和2014年早期的23份人感染h7n9禽流感患者的咽拭子,按照前述实施例2建立的方法进行奥司他韦敏感与耐药基因型检测,扩增结果生成散点图,根据扩增结果判别各临床样本中h7n9禽流感病毒中奥司他韦耐药基因型的突变情况。若扩增曲线fam荧光扩增曲线的ct<38,则待测病毒为奥司他韦耐药基因型;若扩增曲线vic荧光扩增曲线的ct<38,则待测病毒为奥司他韦敏感基因型;若两种荧光扩增曲线同为ct<38,则待测病毒为奥司他韦耐药基因型与敏感基因型混合。双重荧光定量rt-pcr快速鉴定h7n9禽流感病毒r294k突变基因型的方法在临床标本中的应用检测结果见图7。在临床样本的检测中,2份为同时含有奥司他韦敏感与耐药基因型的混合型病毒,2份检测为阴性,其余均为奥司他韦敏感基因型的病毒。
sequencelisting
<110>浙江省疾病预防控制中心
<120>一种h7n9禽流感病毒奥司他韦敏感或耐药基因型的检测试剂盒及检测方法
<130>
<160>4
<170>patentinversion3.5
<210>1
<211>25
<212>dna
<213>unknown
<220>
<223>人工序列
<400>1
tgactggaactgctaagcatattga25
<210>2
<211>25
<212>dna
<213>unknown
<220>
<223>人工序列
<400>2
tgtcattgctactggrtctatctga25
<210>3
<211>14
<212>dna
<213>unknown
<220>
<223>人工序列
<400>3
cacatgcaaggaca14
<210>4
<211>14
<212>dna
<213>unknown
<220>
<223>人工序列
<400>4
ctgcacatgcaggg14
- 还没有人留言评论。精彩留言会获得点赞!
- 一种用于检测牛源大肠杆菌喹诺酮耐药基因的分子标记及其应用的制造方法与工艺
- 一种用于检测肉鸡沙门氏菌环丙沙星耐药基因的分子标记及其应用的制造方法与工艺
- 一种用于检测大肠埃希菌氧氟沙星耐药基因的分子标记及其应用的制造方法与工艺
- 检测巨细胞病毒UL54和UL97基因耐药突变的巢式PCR引物及方法与制造工艺
- 幽门螺旋杆菌及其耐药基因突变检测试剂盒和检测方法与制造工艺
- 一种糖肽类抗生素耐药基因检测试剂盒的制造方法与工艺
- 用于检测产AmpC酶的三种细菌耐药基因的LAMP引物组合及其应用的制造方法与工艺
- 环介导等温扩增多重耐药基因oqxAB的检测引物、检测试剂盒及检测方法与制造工艺
- 一种同时检测多种病原体的三重PCR检测方法与制造工艺
- 四环素耐药基因检测并联探针、基因芯片、试剂盒与检测法的制造方法与工艺
- 逆转肿瘤多药耐药的基因组合物h‑R3/PAMAM G5/MDR1 siRNA及其应用的制作方法与工艺
- 盐生草耐盐基因HgS2及其应用的制造方法与工艺
- 一种快速核酸检测肺炎支原体及耐药突变的方法和试剂盒与流程
- 一种用于检测巴氏杆菌氯霉素类药物耐药基因的分子标记及其应用的制造方法与工艺
- 一种用于检测B族链球菌四环素耐药基因的分子标记及其应用的制造方法与工艺
- 一种用于检测粪肠球菌庆大霉素耐药基因的分子标记及其应用的制造方法与工艺
- 一种用于检测葡萄球菌磺胺类药物耐药基因的分子标记及其应用的制造方法与工艺
- 一种用于检测肉鸡沙门氏菌环丙沙星耐药基因的分子标记及其应用的制造方法与工艺
- 检测巨细胞病毒UL54和UL97基因耐药突变的巢式PCR引物及方法与制造工艺
- 一种检测幽门螺杆菌耐药突变位点的试剂盒和方法与制造工艺
- 一种封闭式病原体检测卡盒的制作方法与工艺
- 检测16种呼吸道病原体的基因芯片检测用试剂盒及方法与流程
- 一种同时检测多种病原体的五重PCR检测方法与流程
- 逆转肿瘤多药耐药的基因组合物h‑R3/PAMAM G5/MDR1 siRNA及其应用的制作方法与工艺
- 用于对肉类、植物或植物部分进行病原体检测和病害治理的方法与流程
- 一种用于检测治疗恶性肿瘤的一线药物耐药基因表达量的试剂盒的制造方法与工艺
- 用于检测植物病原体的装置和方法与流程
- 用于检测多种病原体的荧光实时检测方法及应用与流程
- 一种用于检测手足口病相关病原体的LAMP引物组合物及其相关应用的制造方法与工艺
- 一种用于检测巴氏杆菌氯霉素类药物耐药基因的分子标记及其应用的制造方法与工艺